Cadmium
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kadmium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Aussprache | /ˈkædmiəm/ (KAD-mee-əm) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Erscheinungsbild | silbrig bläulich-grau metallisch | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Standard-Atomgewicht Ar°(Cd) |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cadmium im Periodensystem | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordnungszahl (Z) | 48 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe | Gruppe 12 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periode | Periode 5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Block | d-Block | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronen-Konfiguration | [[[Krypton|Kr]]] 4d10 5s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronen pro Schale | 2, 8, 18, 18, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physikalische Eigenschaften | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase bei STP | fest | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzpunkt | 594,22 K (321,07 °C, 609,93 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Siedepunkt | 1040 K (767 °C, 1413 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dichte (nahe r.t.) | 8,65 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| in flüssigem Zustand (bei mittlerem Druck) | 7,996 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzwärme | 6,21 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verdampfungswärme | 99,87 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molare Wärmekapazität | 26.020 J/(mol-K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Verdampfungsdruck
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomare Eigenschaften | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidationsstufen | -2, +1, +2 (ein schwach basisches Oxid) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativität | Pauling-Skala: 1.69 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionisierungsenergien |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomradius | empirisch: 151 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalenter Radius | 144±9 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van-der-Waals-Radius | 158 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spektrallinien von Cadmium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Andere Eigenschaften | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Natürliches Vorkommen | primordial | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallstruktur | hexagonal dicht gepackt (hcp) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schallgeschwindigkeit dünner Stab | 2310 m/s (bei 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermische Ausdehnung | 30,8 µm/(m⋅K) (bei 25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 96,6 W/(m⋅K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrischer Widerstand | 72,7 nΩ⋅m (bei 22 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetische Ordnung | diamagnetisch | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molare magnetische Suszeptibilität | -19,8×10-6 cm3/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elastizitätsmodul | 50 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schermodul | 19 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elastizitätsmodul | 42 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poissonzahl | 0.30 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs-Härte | 2.0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell-Härte | 203-220 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-Nummer | 7440-43-9 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Geschichte | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entdeckung und erste Isolierung | Karl Samuel Leberecht Hermann und Friedrich Stromeyer (1817) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benannt durch | Friedrich Stromeyer (1817) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hauptisotope von Cadmium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Kadmium ist ein chemisches Element mit dem Symbol Cd und der Ordnungszahl 48. Dieses weiche, silbrig-weiße Metall ist den beiden anderen stabilen Metallen der Gruppe 12, Zink und Quecksilber, chemisch ähnlich. Wie Zink weist es in den meisten seiner Verbindungen die Oxidationsstufe +2 auf, und wie Quecksilber hat es einen niedrigeren Schmelzpunkt als die Übergangsmetalle der Gruppen 3 bis 11. Cadmium und seine Verwandten der Gruppe 12 werden häufig nicht als Übergangsmetalle angesehen, da sie keine teilweise gefüllten d- oder f-Elektronenschalen in den elementaren oder üblichen Oxidationsstufen aufweisen. Die durchschnittliche Konzentration von Cadmium in der Erdkruste liegt zwischen 0,1 und 0,5 Teilen pro Million (ppm). Es wurde 1817 gleichzeitig von Stromeyer und Hermann, beide in Deutschland, als Verunreinigung in Zinkkarbonat entdeckt. ⓘ
Kadmium kommt als geringer Bestandteil in den meisten Zinkerzen vor und ist ein Nebenprodukt der Zinkherstellung. Kadmium wurde lange Zeit als korrosionsbeständiger Überzug auf Stahl verwendet, und Kadmiumverbindungen werden als rote, orangefarbene und gelbe Pigmente, zum Färben von Glas und zur Stabilisierung von Kunststoffen eingesetzt. Die Verwendung von Cadmium ist im Allgemeinen rückläufig, da es giftig ist (es ist in der europäischen Richtlinie zur Beschränkung der Verwendung gefährlicher Stoffe ausdrücklich aufgeführt) und Nickel-Cadmium-Batterien durch Nickel-Metallhydrid- und Lithium-Ionen-Batterien ersetzt wurden. Eine der wenigen neuen Verwendungen ist die Verwendung in Cadmiumtellurid-Solarzellen. ⓘ
Obwohl keine biologische Funktion von Cadmium in höheren Organismen bekannt ist, wurde in marinen Kieselalgen eine cadmiumabhängige Karbonatanhydrase gefunden. ⓘ
Cadmium (selten auch Kadmium; von altgriechisch καδμία kadmía, lateinisch cadmia und cadmea „Galmei“) ist ein chemisches Element mit dem Elementsymbol Cd und der Ordnungszahl 48. Es wird meist zu den Übergangsmetallen gezählt, obwohl es eine abgeschlossene d-Schale besitzt und damit eher den Hauptgruppenelementen, vor allem den Erdalkalimetallen ähnelt. Im Periodensystem steht es in der 5. Periode sowie der 2. Nebengruppe (Gruppe 12) oder Zinkgruppe. ⓘ
Geschichte

Cadmium (lateinisch cadmia, griechisch καδμεία für "Kalamin", ein cadmiumhaltiges Mineraliengemisch, das nach der griechischen Sagengestalt Κάδμος, Cadmus, dem Gründer von Theben, benannt wurde) wurde 1817 von Friedrich Stromeyer in verunreinigten Zinkverbindungen entdeckt, die in deutschen Apotheken verkauft wurden. Karl Samuel Leberecht Hermann untersuchte gleichzeitig die Verfärbung in Zinkoxid und fand aufgrund des gelben Niederschlags mit Schwefelwasserstoff eine Verunreinigung, die zunächst als Arsen vermutet wurde. Außerdem entdeckte Stromeyer, dass ein Lieferant Zinkkarbonat anstelle von Zinkoxid verkaufte. Stromeyer fand das neue Element als Verunreinigung in Zinkkarbonat (Galmei), und Deutschland blieb 100 Jahre lang der einzige wichtige Produzent des Metalls. Das Metall wurde nach dem lateinischen Wort für Calamin benannt, weil es in diesem Zinkerz gefunden wurde. Stromeyer stellte fest, dass einige unreine Kalaminproben beim Erhitzen ihre Farbe änderten, reines Kalamin jedoch nicht. Er blieb hartnäckig bei der Untersuchung dieser Ergebnisse und isolierte schließlich Cadmiummetall durch Rösten und Reduzieren des Sulfids. Das Potenzial von Cadmiumgelb als Pigment wurde in den 1840er Jahren erkannt, aber der Mangel an Cadmium schränkte diese Anwendung ein. ⓘ
Obwohl Cadmium und seine Verbindungen in bestimmten Formen und Konzentrationen giftig sind, wurde Cadmiumjodid laut dem British Pharmaceutical Codex von 1907 als Medikament zur Behandlung von "vergrößerten Gelenken, skrofulösen Drüsen und Frostbeulen" verwendet. ⓘ
Im Jahr 1907 definierte die Internationale Astronomische Union den internationalen ångström anhand einer roten Cadmium-Spektrallinie (1 Wellenlänge = 6438,46963 Å). Diese Definition wurde 1927 von der 7. Generalkonferenz für Maße und Gewichte angenommen. Im Jahr 1960 wurden die Definitionen sowohl des Meters als auch des ångström auf Krypton umgestellt. ⓘ
Nachdem die industrielle Produktion von Cadmium in den 1930er und 1940er Jahren begonnen hatte, bestand die Hauptanwendung von Cadmium in der Beschichtung von Eisen und Stahl zum Schutz vor Korrosion. 1944 wurden 62 % und 1956 59 % des Cadmiums in den Vereinigten Staaten für Beschichtungen verwendet. Im Jahr 1956 wurden 24 % des Cadmiums in den Vereinigten Staaten für eine zweite Anwendung in Form von roten, orangefarbenen und gelben Pigmenten aus Sulfiden und Seleniden des Cadmiums verwendet. ⓘ
Die stabilisierende Wirkung von Cadmiumchemikalien wie den Carboxylaten Cadmiumlaurat und Cadmiumstearat auf PVC führte in den 1970er und 1980er Jahren zu einer verstärkten Verwendung dieser Verbindungen. Die Nachfrage nach Cadmium in Pigmenten, Beschichtungen, Stabilisatoren und Legierungen ging aufgrund von Umwelt- und Gesundheitsvorschriften in den 1980er und 1990er Jahren zurück; 2006 wurden nur noch 7 % des gesamten Cadmiumverbrauchs für Beschichtungen und nur noch 10 % für Pigmente verwendet. Gleichzeitig wurde dieser Verbrauchsrückgang durch eine steigende Nachfrage nach Cadmium für Nickel-Cadmium-Batterien kompensiert, auf die 2006 81 % des Cadmiumverbrauchs in den Vereinigten Staaten entfielen. ⓘ
Plinius der Ältere berichtet in seiner um das Jahr 77 entstandenen Naturkunde Naturalis historia von Galmeifunden in Germanien: “cadmea […] ferunt nuper etiam in Germania provincia repertum” (deutsch: „kürzlich wurde in der Provinz Germanien Galmei gefunden“). Die Bezeichnung Cadmium wurde schon im Mittelalter verwendet, vermutlich für Zink oder sein Karbonaterz. Wie aus einer von Kaiser Friedrich II. im April 1226 in Ravenna ausgestellten Urkunde hervorgeht, räumt dieser dem Benediktiner-Kloster St. Paul im Lavanttal das Recht ein “ut Cadmiae tam argentj quam plumbi et ferri, que in territorio ipsius monasteri de cetero inveniri contigerint, ad opus suum” (deutsch: „dass das Zink, sowie Silber, als auch Blei und Eisen, welches auf dem Gebiet des Klosters gefunden wird, für dessen Zwecke verwendet wird“). ⓘ
1942 benutzte Enrico Fermi Cadmiumbleche im weltweit ersten Kernreaktor. Die Bleche konnten in den Reaktor hinein- und hinausgeschoben werden, um die Kettenreaktion steuern zu können. Cadmium kann moderierte Spaltneutronen einfangen und so die Kritikalität des Reaktors beeinflussen. ⓘ
Vorkommen
Cadmium ist ein sehr seltenes Element. Sein Anteil an der Erdkruste beträgt nur etwa 3 · 10−5 %. Gediegen, das heißt in elementarer Form, kommt Cadmium äußerst selten vor. Bisher sind nur fünf Fundorte in drei Ländern bekannt: Der Fluss Khann'ya im Wiljui-Becken, das Jana-Flussbecken nahe Werchojansk und die Billeekh Intrusion in der russischen Republik Sacha (Jakutien, Ostsibirien); die Goldstrike-Gruben bei Lynn im Eureka County des US-Bundesstaates Nevada sowie das Burabaiskii-Massiv im Gebiet Aqmola von Kasachstan. ⓘ
Als cadmiumhaltige Erze sind vor allem die Cadmiumblende Greenockit (CdS) mit bis zu 77,81 % Cd und der Cadmiumspat Otavit (CdCO3) mit bis zu 65,20 % Cd bekannt, die allerdings zu selten für den kommerziellen Abbau sind. Beide sind fast immer mit verschiedenen Zinkerzen wie Sphalerit (ZnS) und Smithsonit (ZnCO3) vergesellschaftet. ⓘ
Insgesamt sind bisher (Stand 2018) etwas mehr als 20 Cadmiumminerale bekannt. Das sehr seltene Cadmiumoxid Monteponit hat den höchsten Cd-Gehalt mit bis zu 87,54 %. Weitere Minerale sind unter anderem Hawleyit (77,81 % Cd), Cadmoselit (58,74 % Cd) und Drobecit (IMA 2002-034, 40,07 % Cd). ⓘ
Cadmium als Mineral
Natürlich vorkommendes Cadmium in seiner elementaren Form wurde erstmals 1979 durch B. V. Oleinikov, A. V. Okrugin und N. V. Leskova beschrieben und von der International Mineralogical Association (IMA) als eigenständige Mineralart anerkannt (Interne Eingangs-Nr. der IMA: 1980-086a). ⓘ
Gemäß der Systematik der Minerale nach Strunz (9. Auflage) wird Cadmium unter der System-Nr. 1.AB.05 (Elemente – Metalle und intermetallische Verbindungen – Zink-Messing-Familie – Zink-Gruppe) eingeordnet. In der veralteten 8. Auflage der Strunz’schen Mineralsystematik ist Cadmium dagegen noch nicht aufgeführt. Nur im zuletzt 2018 aktualisierten „Lapis-Mineralienverzeichnis“, das sich aus Rücksicht auf private Sammler und institutionelle Sammlungen noch an dieser Form der System-Nummerierung orientiert, erhielt das Mineral die System- und Mineral-Nr. I/A.04-40. Die vorwiegend im englischsprachigen Raum verwendete Systematik der Minerale nach Dana führt das Element-Mineral unter der System-Nr. 01.01.05.02. ⓘ
Gewinnung und Darstellung

Cadmium wird ausschließlich als Nebenprodukt bei der Zinkverhüttung, in kleinem Umfang auch bei der Blei- und Kupferverhüttung gewonnen. Kleinere Mengen fallen auch beim Recycling von Eisen und Stahl an. ⓘ
Die Gewinnung von Cadmium hängt vom Verfahren ab, wie das Zink gewonnen wird. Bei der trockenen Zinkgewinnung wird zunächst das Cadmium mit dem Zink reduziert. Da Cadmium einen niedrigeren Siedepunkt als Zink besitzt, verdampft es leichter. Dadurch verdampft ein Cadmium-Zink-Gemisch aus dem Reduktionsgefäß und reagiert an anderer Stelle mit Sauerstoff zu Cadmium- und Zinkoxid. Anschließend wird dieses Gemisch in einem Destillationsgefäß mit Koks vermischt und das Cadmium vom Zink abdestilliert. Durch fraktionierende Destillation lassen sich höhere Reinheiten an Cadmium erreichen. ⓘ
Bei der nassen Zinkgewinnung werden die gelösten Cadmiumionen mit Zinkstaub reduziert und ausgefällt. Das dabei entstehende Cadmium wird mit Sauerstoff zu Cadmiumoxid oxidiert und in Schwefelsäure gelöst. Aus der so entstandenen Cadmiumsulfat-Lösung wird durch Elektrolyse mit Aluminiumanoden und Bleikathoden besonders reines Elektrolyt-Cadmium gewonnen. ⓘ
Die weltweite Gewinnung von Cadmium betrug im Jahr 2020 ca. 24.000 Tonnen. Der größte Produzent ist China, gefolgt von Südkorea. Eine zunehmende Rolle bei der Cadmiumgewinnung spielt auch das Recycling von NiCd Batterien ⓘ
| Land | 2006 | 2019 | 2020 ⓘ |
|---|---|---|---|
| Raffinerieerzeugung (in Tonnen) | |||
| 700 | nicht veröffentlicht | nicht veröffentlicht | |
| 400 | 348 | ||
| 1.710 | 1.803 | 1.800 | |
| 3.000 | 8.200 | 10.000 | |
| 640 | 450 | ||
| 450 | |||
| 2.290 | 2.000 | 1.880 | |
| 2.000 | 1.500 | 1.500 | |
| 3.250 | 4.400 | 3.000 | |
| 1.400 | 1.395 | 978 | |
| 570 | 1.100 | 880 | |
| 400 | |||
| 420 | 772 | 700 | |
| 1.100 | 900 | 1.000 | |
| 400 | |||
| Andere Länder | 1.370 | 2.320 | 520 |
| Gesamt (gerundet) | 19.300 | 24.400 | 24.000 |
Cadmiumproduktion im Jahr 2005 ⓘ
Eigenschaften

Physikalische Eigenschaften
Cadmium ist ein silbrig glänzendes Metall mit einer Dichte von 8,65 g/cm³. Es ist weich (Mohshärte 2), plastisch verformbar und lässt sich ebenso mit dem Messer anschneiden wie zu Drähten ziehen und zu Blättchen aushämmern. ⓘ
Cadmium erstarrt ausschließlich im hexagonalen Kristallsystem in der Raumgruppe P63/mmc (Raumgruppen-Nr. 194). Die Gitterparameter von reinem Cadmium betragen a = 0,2979 nm (entspricht 2,98 Å) und c = 0,5617 nm (entspricht 5,62 Å) bei 2 Formeleinheiten pro Elementarzelle. Ähnlich wie bei Zinn treten beim Verbiegen von Cadmium mittlerer Reinheit typische Geräusche auf (bei Zinn Zinngeschrei genannt). Poliertes Cadmium verliert an Luft nach einigen Tagen seinen Glanz, auch wenn es korrosionsbeständiger ist als Zink. In kohlensäurehaltiger Luft bildet es einen grauweißen, kohlendioxidhaltigen Überzug. Stark erhitzt verbrennt es mit rötlicher bis gelber Flamme zu bräunlich dampfendem Cadmiumoxid CdO. ⓘ
CdO wurde wegen seiner hohen Toxizität im Zweiten Weltkrieg von den USA auf seine Verwendbarkeit als chemischer Kampfstoff untersucht. ⓘ
Cadmium ist ein weiches, verformbares, dehnbares, silbrig-weißes, zweiwertiges Metall. Es ähnelt in vielerlei Hinsicht dem Zink, bildet jedoch komplexe Verbindungen. Im Gegensatz zu den meisten anderen Metallen ist Kadmium korrosionsbeständig und wird als Schutzschicht auf anderen Metallen verwendet. Als Massenmetall ist Kadmium unlöslich in Wasser und nicht brennbar; in seiner pulverförmigen Form kann es jedoch brennen und giftige Dämpfe freisetzen. ⓘ
Chemische Eigenschaften
In chemischen Verbindungen liegt es meist zweiwertig vor. Chemisch gleicht es dem Zink, es neigt aber eher zur Bildung von Komplex-Verbindungen mit der Koordinationszahl 4. An der Luft bildet Cadmium durch die Oxidation eine Verdunklung der Oberfläche. In alkalischem Milieu ist die Oberfläche unlöslich, in Schwefelsäure und Salzsäure schwer und in Salpetersäure gut löslich. ⓘ
Isotope
Das natürlich vorkommende Cadmium besteht aus acht Isotopen. Zwei davon sind radioaktiv, und von drei Isotopen wird erwartet, dass sie zerfallen, was aber unter Laborbedingungen nicht geschehen ist. Die beiden natürlichen radioaktiven Isotope sind 113Cd (Betazerfall, Halbwertszeit 7,7×1015 Jahre) und 116Cd (Zwei-Neutrino-Doppelbetazerfall, Halbwertszeit 2,9×1019 Jahre). Die anderen drei Isotope sind 106Cd, 108Cd (beide doppelter Elektroneneinfang) und 114Cd (doppelter Betazerfall); für diese Halbwertszeiten wurden nur untere Grenzwerte ermittelt. Mindestens drei Isotope - 110Cd, 111Cd und 112Cd - sind stabil. Von den Isotopen, die in der Natur nicht vorkommen, sind die langlebigsten 109Cd mit einer Halbwertszeit von 462,6 Tagen und 115Cd mit einer Halbwertszeit von 53,46 Stunden. Alle übrigen radioaktiven Isotope haben eine Halbwertszeit von weniger als 2,5 Stunden, und die meisten haben eine Halbwertszeit von weniger als 5 Minuten. Cadmium hat 8 bekannte Metazustände, wobei die stabilsten 113mCd (t1⁄2 = 14,1 Jahre), 115mCd (t1⁄2 = 44,6 Tage) und 117mCd (t1⁄2 = 3,36 Stunden) sind. ⓘ
Die bekannten Isotope von Cadmium haben eine Atommasse zwischen 94,950 u (95Cd) und 131,946 u (132Cd). Bei Isotopen, die leichter als 112 u sind, ist der primäre Zerfallsmodus der Elektroneneinfang, und das vorherrschende Zerfallsprodukt ist Element 47 (Silber). Schwerere Isotope zerfallen hauptsächlich durch Betastrahlung und erzeugen das Element 49 (Indium). ⓘ
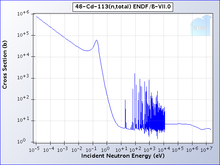
Ein Isotop von Cadmium, 113Cd, absorbiert Neutronen mit hoher Selektivität: Mit sehr hoher Wahrscheinlichkeit werden Neutronen mit einer Energie unterhalb des Cadmium-Cut-off absorbiert; Neutronen mit einer Energie oberhalb des Cut-off werden durchgelassen. Der Cadmium-Cut-Off liegt bei etwa 0,5 eV, und Neutronen unterhalb dieses Niveaus werden als langsame Neutronen bezeichnet, die sich von den mittleren und schnellen Neutronen unterscheiden. ⓘ
Cadmium wird in Sternen mit geringer bis mittlerer Masse (0,6 bis 10 Sonnenmassen) im Laufe von Jahrtausenden durch den s-Prozess erzeugt. Bei diesem Prozess fängt ein Silberatom ein Neutron ein und unterliegt dann einem Betazerfall. ⓘ
Anwendungen
Wegen der hohen Toxizität von Cadmium nimmt dessen Bedeutung ab. Seit Dezember 2011 ist es in Schmuck, Legierungen zum Löten und in PVC in der Europäischen Union verboten. Cadmium wird bzw. wurde eingesetzt:
- als Korrosionsschutz für Eisenwerkstoffe (Kadmierung und massive Verlustanoden im Schiffbau)
- als Oberflächenüberzug für Aluminiumwerkstoffe in der Wehrtechnik (z. B. bei Raketenwerfern)
- für Nickel-Cadmium-Akkumulatoren
- für gelbe bis tiefrote Farbpigmente aus Cadmiumsulfid und Cadmiumselenid für Lacke und Kunststoffe (mittlerweile geringe Praxisbedeutung wegen möglicher Gesundheitsgefährdung, vor allem bei der Verbrennung entsprechender Artikel)
- als Legierungsmetall in niedrigschmelzenden Legierungen, zum Beispiel Lagerwerkstoffe oder Woodsches Metall
- früher als Schmiermittel in Scheibenbremsen
- als Bestandteil von Lötwerkstoffen (Lötzinn), auch für Hartlote
- zur Herstellung von Halbleitern
- Cadmiumoxid als Leuchtstoff in Schwarz-Weiß-Fernsehröhren sowie Zusatz in Blau- und Grünphosphor von Farbröhren
- Cadmiumoxid als Beimischung zu Silber in Schaltkontakten
- als Abschirmmaterial gegen thermische Neutronen und für Regelstäbe in der Nukleartechnik aufgrund des besonders hohen Wirkungsquerschnitts des Isotops 113 für den Neutroneneinfang
- als Quelle von energiereicher Gammastrahlung (rund 7 MeV) aus thermischen Neutronen zur späteren Erzeugung von Positronen durch Paarerzeugung
- Cadmiumsulfid in Belichtungsmessern, deren spektrale Empfindlichkeit der des menschlichen Auges gleicht
- Cadmiumtellurid als infrarotempfindlicher Sensor für Kameras (focal plane arrays)
- in Dünnschicht-Solarzellen als Cadmiumtellurid oder Cadmiumsulfid zur Stromerzeugung
- Cd-Stearat als Stabilisator in Kunststoffen beispielsweise in PVC (unempfindlich gegen Licht, allerdings mittlerweile von geringer Praxisbedeutung wegen möglicher Gesundheitsgefährdungen)
- früher in den Weston-Normalelementen zur Festlegung der Maßeinheit der elektrischen Spannung, 1 Volt
- Cadmium-Bismut-Legierungen für Schmelzsicherungen
- Silber-Cadmium-Legierungen als Desoxidationsmittel in der Herstellung von Sterling-Silber
- bei Schmuckwaren: goldgrüne Gold-Cadmium-Legierungen
- Cadmium-Lampe
- Helium-Cadmium-Laser
- Cadmium-Ionen zur Blockade spannungsaktivierter Calciumkanäle in der Elektrophysiologie
- zum Färben von Glas in Gelb, Orange und Rot durch Zusatz von Cadmiumsulfid, -selenid und -tellurid oder Mischungen davon. ⓘ
Die Cadmium-Chalkogenide Cadmiumsulfid (gelb), Cadmiumselenid (rot) und Cadmiumtellurid (schwarz) sind wichtige II-VI-Halbleiter. Sie werden beispielsweise nanopartikulär als Quantenpunkte (engl. Quantum Dots) hergestellt und u. a. in der Biochemie in-vitro eingesetzt. ⓘ
Cadmium ist ein häufiger Bestandteil von elektrischen Batterien, Pigmenten, Beschichtungen und Galvanik. ⓘ
Batterien

Im Jahr 2009 wurden 86 % des Cadmiums in Batterien verwendet, vor allem in wiederaufladbaren Nickel-Cadmium-Batterien. Nickel-Cadmium-Zellen haben ein Nennpotential von 1,2 V. Die Zelle besteht aus einer positiven Nickelhydroxid-Elektrode und einer negativen Cadmium-Elektrodenplatte, die durch einen alkalischen Elektrolyten (Kaliumhydroxid) getrennt sind. Die Europäische Union hat 2004 einen Grenzwert für den Cadmiumgehalt in elektronischen Geräten von 0,01 % festgelegt, mit einigen Ausnahmen, und 2006 den Grenzwert für den Cadmiumgehalt auf 0,002 % gesenkt. Ein weiterer Batterietyp, der auf Cadmium basiert, ist die Silber-Cadmium-Batterie. ⓘ
Galvanisierung

Die Galvanisierung von Cadmium, die 6 % der Weltproduktion ausmacht, wird in der Luftfahrtindustrie eingesetzt, um die Korrosion von Stahlteilen zu verringern. Diese Beschichtung wird durch Chromatsalze passiviert. Eine Einschränkung der Kadmiumbeschichtung ist die Wasserstoffversprödung von hochfesten Stählen durch den Galvanisierungsprozess. Daher sollten Stahlteile, die auf eine Zugfestigkeit von mehr als 1300 MPa (200 ksi) wärmebehandelt werden, mit einer alternativen Methode beschichtet werden (z. B. mit speziellen Cadmium-Galvanisierungsverfahren mit geringer Versprödung oder physikalischer Gasphasenabscheidung). ⓘ
Die Versprödung von Titan durch Rückstände von kadmierten Werkzeugen führte zur Verbannung dieser Werkzeuge (und zur Einführung routinemäßiger Werkzeugprüfungen zur Feststellung von Kadmiumverunreinigungen) in den A-12/SR-71-, U-2- und nachfolgenden Flugzeugprogrammen, die Titan verwenden. ⓘ
Kernspaltung
Cadmium wird in den Steuerstäben von Kernreaktoren verwendet und wirkt als sehr wirksames Neutronengift zur Kontrolle des Neutronenflusses bei der Kernspaltung. Wenn Cadmiumstäbe in den Kern eines Kernreaktors eingesetzt werden, absorbiert Cadmium die Neutronen und verhindert so, dass sie weitere Spaltungsereignisse auslösen, wodurch die Reaktivität kontrolliert wird. Der von der Westinghouse Electric Company entwickelte Druckwasserreaktor verwendet eine Legierung, die zu 80 % aus Silber, zu 15 % aus Indium und zu 5 % aus Cadmium besteht. ⓘ
Fernsehapparate
QLED-Fernseher enthalten seit einiger Zeit Cadmium in der Konstruktion. Einige Unternehmen sind bestrebt, die Umweltauswirkungen der Exposition des Menschen und der Verschmutzung durch das Material bei der Herstellung von Fernsehern zu verringern. ⓘ
Medikamente gegen Krebs
Komplexe auf der Basis von Schwermetallen haben ein großes Potenzial für die Behandlung einer Vielzahl von Krebsarten, aber ihr Einsatz ist aufgrund der toxischen Nebenwirkungen oft begrenzt. Die Wissenschaftler machen jedoch Fortschritte auf diesem Gebiet, und es wurden neue vielversprechende Cadmiumkomplexverbindungen mit geringerer Toxizität entdeckt. ⓘ
Verbindungen

Cadmiumoxid wurde in Schwarz-Weiß-Fernsehleuchtstoffen und in den blauen und grünen Leuchtstoffen von Farbfernseh-Kathodenstrahlröhren verwendet. Kadmiumsulfid (CdS) wird als fotoleitende Oberflächenbeschichtung für Trommeln von Fotokopierern verwendet. ⓘ

Verschiedene Cadmiumsalze werden in Farbpigmenten verwendet, wobei CdS als gelbes Pigment am häufigsten eingesetzt wird. Cadmiumselenid ist ein rotes Pigment, das gemeinhin als Cadmiumrot bezeichnet wird. Für Maler, die mit diesem Pigment arbeiten, liefert Kadmium die leuchtendsten und haltbarsten Gelb-, Orange- und Rottöne - so sehr, dass diese Farben bei der Herstellung deutlich abgeschwächt werden, bevor sie mit Ölen und Bindemitteln gemahlen oder in Aquarelle, Gouachen, Acrylfarben und andere Farben und Pigmentformulierungen gemischt werden. Da diese Pigmente potenziell giftig sind, sollten die Anwender eine Schutzcreme auf den Händen verwenden, um eine Aufnahme über die Haut zu verhindern, auch wenn die über die Haut in den Körper aufgenommene Cadmiummenge Berichten zufolge weniger als 1 % beträgt. ⓘ
In PVC wurde Cadmium als Wärme-, Licht- und Witterungsstabilisator verwendet. Heute sind die Cadmium-Stabilisatoren vollständig durch Barium-Zink-, Calcium-Zink- und zinnorganische Stabilisatoren ersetzt worden. Kadmium wird in vielen Arten von Lötmitteln und Lagerlegierungen verwendet, da es einen niedrigen Reibungskoeffizienten und eine hohe Ermüdungsbeständigkeit aufweist. Es ist auch in einigen der am niedrigsten schmelzenden Legierungen, wie Woods Metall, enthalten. ⓘ
Halbleiter
Cadmium ist ein Element in einigen Halbleitermaterialien. Cadmiumsulfid, Cadmiumselenid und Cadmiumtellurid werden in einigen Fotodetektoren und Solarzellen verwendet. HgCdTe-Detektoren sind empfindlich für Licht im mittleren Infrarotbereich und werden in einigen Bewegungsmeldern verwendet. ⓘ
Verwendung im Labor
Helium-Cadmium-Laser sind eine gängige Quelle für blaues oder ultraviolettes Laserlicht. Laser mit Wellenlängen von 325, 354 und 442 nm werden mit diesem Verstärkungsmedium hergestellt; einige Modelle können zwischen diesen Wellenlängen umschalten. Sie werden vor allem in der Fluoreszenzmikroskopie sowie bei verschiedenen Laboranwendungen eingesetzt, die Laserlicht bei diesen Wellenlängen erfordern. ⓘ
Kadmiumselenid-Quantenpunkte emittieren unter UV-Anregung (z. B. He-Cd-Laser) eine helle Lumineszenz. Die Farbe dieser Lumineszenz kann je nach Größe der Partikel grün, gelb oder rot sein. Kolloidale Lösungen dieser Partikel werden für die Darstellung von biologischem Gewebe und Lösungen mit einem Fluoreszenzmikroskop verwendet. ⓘ
In der Molekularbiologie wird Cadmium verwendet, um spannungsabhängige Kalziumkanäle am Fluss von Kalziumionen zu hindern, und in der Hypoxieforschung, um den proteasomabhängigen Abbau von Hif-1α zu stimulieren. ⓘ
Cadmiumselektive Sensoren auf der Grundlage des Fluorophors BODIPY wurden für die Bildgebung und die Erfassung von Cadmium in Zellen entwickelt. Eine leistungsfähige Methode zur Überwachung von Cadmium in wässrigen Umgebungen ist die Elektrochemie. Durch den Einsatz einer selbstorganisierten Monoschicht kann eine cadmiumselektive Elektrode mit einer Empfindlichkeit im ppt-Bereich hergestellt werden. ⓘ
Nachweis
Als Vorprobe für Cadmium kann die sogenannte Glühröhrchenprobe dienen. Hierzu wird etwas Ursubstanz in einem hochschmelzenden Glühröhrchen erhitzt und das entstehende Sulfid-Oxid-Gemisch mit Natriumoxalat zu den Metallen reduziert. Als leichtflüchtiger Bestandteil verdampft Cadmium und scheidet sich als Metallspiegel am oberen Teil des Röhrchens ab. ⓘ
Durch anschließende Zugabe von Schwefel und erneutem Glühen bildet sich aus dem Metallspiegel und Schwefeldampf Cadmiumsulfid, welches in der Hitze rot und bei Raumtemperatur gelb ist. Dieser Farbwechsel lässt sich einige Male wiederholen. ⓘ
Als Nachweisreaktion für Cadmium-Kationen gilt die Ausfällung mit Sulfid-Lösung oder Schwefelwasserstoff-Wasser als gelbes Cadmiumsulfid. Andere Schwermetallionen stören diesen Nachweis, so dass zuvor ein Kationentrenngang durchzuführen ist. ⓘ
Zur quantitativen Bestimmung von Cadmiumspuren bietet sich die Polarographie an. Cadmium(II)-Ionen geben in 1 M KCl eine Stufe bei −0,64 V (gegen SCE). Im Ultraspurenbereich kann die Inversvoltammetrie an Quecksilberelektroden eingesetzt werden. Sehr empfindlich ist auch die Graphitrohr-AAS von Cadmium. Hierbei können noch 0,003 µg/l nachgewiesen werden. Das relativ leicht flüchtige Element verträgt dabei keine hohe Pyrolysetemperatur. Ein Matrixmodifizierer wie Palladium-Magnesiumnitrat kann Abhilfe schaffen. ⓘ
Sicherheitshinweise
Cadmium ist als sehr giftig und seine Verbindungen von gesundheitsschädlich (wie Cadmiumtellurid) über giftig (z. B. Cadmiumsulfid) bis sehr giftig (so bei Cadmiumoxid) eingestuft; außerdem besteht begründeter Verdacht auf krebsauslösende Wirkung beim Menschen. Eingeatmeter cadmiumhaltiger Staub führt zu Schäden an Lunge, Leber und Niere. ⓘ
In Arbeitsbereichen, in denen mit erhitzten Cadmiumverbindungen gearbeitet wird (Lötplätze und Cadmierbäder), ist für eine gute Durchlüftung oder Absaugung zu sorgen. ⓘ
In der Europäischen Union gilt seit 10. Dezember 2011 für Cadmium ein Verbot der Verwendung und des Inverkehrbringens in vielen Kunststoffen, Farben, Stabilisierungsmitteln, Loten sowie bestimmten Metallerzeugnissen, insbesondere Bedarfsgegenständen wie etwa Schmuck Vorher war in Silberhartlot typischerweise 10 % bis 25 %, in Schmuck für Kinder bis zu 30 %, in PVC 0,2 % Cadmium enthalten. Oft wird für das Inverkehrbringen ein Grenzwert von 0,01 Gewichtsprozent (100 mg/kg) gesetzt, da man davon ausgeht, dass es sich bei einem Gehalt darunter um eine unbeabsichtigte, also unvermeidbare Verunreinigung handelt. Mit der Verordnung (EU) 2016/217 vom 16. Februar 2016 wurde das Verbot auf das Inverkehrbringen von Cadmium in bestimmten Anstrichfarben und Lacken – auch mit höherem Zinkgehalt – und in mit solchen Mitteln gestrichenen Erzeugnissen erweitert. Es gibt noch Ausnahmen etwa für bestimmte Baustoffe wie Zäune aus hartem PVC-Recyclat, sofern der Cadmiumgehalt im Kunststoff 0,1 Masseprozent nicht übersteigt und das Erzeugnis als Recycling-PVC gekennzeichnet ist, für besondere Anwendungen wie Luftfahrt oder Militär oder wegen der hohen Leistungsdichte für Ni-Cd-Akkus in Schnurloselektrogeräten. ⓘ
Toxikologie
Cadmium ist in der chemischen Industrie ein unvermeidbares Nebenprodukt der Zink-, Blei- und Kupfergewinnung. Auch in Düngern und Pestiziden ist Cadmium zu finden. ⓘ
Aufnahme und Gefahren
| Gefahren | |
|---|---|
| GHS-Kennzeichnung: | |
Piktogramme
|
  
|
Signalwort
|
Gefahr |
Gefahrenhinweise
|
H301, H330, H341, H350, H361fd, H372, H410 |
Sicherheitshinweise
|
P201, P202, P260, P264, P273, P304+P340+P310 |
| NFPA 704 (Feuerdiamant) | |
Einzelpersonen und Organisationen haben die bioanorganischen Aspekte von Cadmium auf seine Toxizität hin untersucht. Die gefährlichste Form der berufsbedingten Exposition gegenüber Cadmium ist das Einatmen von Feinstaub und Rauch oder das Verschlucken von hochlöslichen Cadmiumverbindungen. Das Einatmen von Cadmiumdämpfen kann zunächst zu Metalldampffieber führen, kann aber auch zu chemischer Pneumonitis, Lungenödem und Tod führen. ⓘ
Cadmium stellt auch eine Gefahr für die Umwelt dar. Der Mensch ist in erster Linie durch die Verbrennung fossiler Brennstoffe, Phosphatdünger, natürliche Quellen, die Eisen- und Stahlproduktion, die Zementproduktion und damit verbundene Tätigkeiten, die Produktion von Nichteisenmetallen und die Verbrennung fester Siedlungsabfälle exponiert. Weitere Quellen für Cadmium sind Brot, Hackfrüchte und Gemüse. ⓘ

Es gab einige wenige Fälle von Vergiftungen in der Allgemeinbevölkerung, die auf eine langfristige Exposition gegenüber Cadmium in kontaminierten Lebensmitteln und Wasser zurückzuführen sind. Die Forschung über eine Östrogenimitation, die Brustkrebs auslösen kann, ist noch nicht abgeschlossen. In den Jahrzehnten vor dem Zweiten Weltkrieg wurde der Jinzū-Fluss in Japan durch Bergbauarbeiten mit Cadmium und Spuren anderer giftiger Metalle verseucht. Infolgedessen reicherte sich Cadmium in den Reispflanzen entlang der Flussufer stromabwärts der Minen an. Einige Mitglieder der örtlichen landwirtschaftlichen Gemeinschaften verzehrten den kontaminierten Reis und entwickelten die Itai-Itai-Krankheit und Nierenanomalien, einschließlich Proteinurie und Glucosurie. Bei den Opfern dieser Vergiftung handelte es sich fast ausschließlich um Frauen nach der Menopause mit niedrigem Eisengehalt und geringen Vorräten an anderen Mineralien im Körper. Ähnliche Cadmiumexpositionen der Allgemeinbevölkerung in anderen Teilen der Welt haben nicht zu denselben Gesundheitsproblemen geführt, da die Bevölkerung über ausreichende Eisen- und andere Mineralienspiegel verfügte. Obwohl Cadmium also ein wichtiger Faktor für die Itai-itai-Krankheit in Japan ist, sind die meisten Forscher zu dem Schluss gekommen, dass es nur einer von mehreren Faktoren war. ⓘ
Kadmium ist einer von sechs Stoffen, die durch die RoHS-Richtlinie (Restriction of Hazardous Substances) der Europäischen Union verboten sind, die gefährliche Stoffe in Elektro- und Elektronikgeräten regelt, aber bestimmte Ausnahmen und Befreiungen vom Geltungsbereich des Gesetzes zulässt. ⓘ
Die Internationale Agentur für Krebsforschung hat Cadmium und Cadmiumverbindungen als krebserregend für den Menschen eingestuft. Obwohl die berufliche Exposition gegenüber Cadmium mit Lungen- und Prostatakrebs in Verbindung gebracht wird, besteht nach wie vor Unsicherheit über die Karzinogenität von Cadmium bei geringer Umweltexposition. Jüngste Daten aus epidemiologischen Studien deuten darauf hin, dass die Aufnahme von Cadmium über die Nahrung mit einem höheren Risiko für Endometrium-, Brust- und Prostatakrebs sowie für Osteoporose beim Menschen verbunden ist. Eine kürzlich durchgeführte Studie hat gezeigt, dass das Endometriumgewebe von Frauen, die derzeit oder früher geraucht haben, durch höhere Cadmiumwerte gekennzeichnet ist. ⓘ
Die Cadmiumexposition wird mit einer Vielzahl von Krankheiten in Verbindung gebracht, darunter Nierenerkrankungen, frühe Atherosklerose, Bluthochdruck und Herz-Kreislauf-Erkrankungen. Obwohl Studien einen signifikanten Zusammenhang zwischen der Cadmiumexposition und dem Auftreten von Krankheiten in menschlichen Populationen zeigen, ist ein molekularer Mechanismus noch nicht identifiziert worden. Eine Hypothese besagt, dass Cadmium ein endokriner Disruptor ist, und einige experimentelle Studien haben gezeigt, dass es mit verschiedenen hormonellen Signalwegen interagieren kann. So kann Cadmium beispielsweise an den Östrogenrezeptor alpha binden und die Signalübertragung entlang der Östrogen- und MAPK-Signalwege bei niedrigen Dosen beeinflussen. ⓘ
Die Tabakpflanze absorbiert und akkumuliert Schwermetalle wie Cadmium aus dem umgebenden Boden in ihren Blättern. Nach dem Einatmen des Tabakrauchs werden diese leicht in den Körper der Konsumenten aufgenommen. Tabakrauchen ist die wichtigste Einzelquelle für die Cadmiumexposition der Allgemeinbevölkerung. Schätzungsweise 10 % des Cadmiumgehalts einer Zigarette werden durch das Rauchen inhaliert. Die Absorption von Cadmium über die Lunge ist effektiver als über den Darm. Bis zu 50 % des mit dem Zigarettenrauch eingeatmeten Cadmiums können absorbiert werden. Im Durchschnitt ist die Cadmiumkonzentration im Blut von Rauchern 4 bis 5 Mal höher als die von Nichtrauchern und in den Nieren 2 bis 3 Mal höher als bei Nichtrauchern. Trotz des hohen Cadmiumgehalts im Zigarettenrauch scheint die Cadmiumexposition durch Passivrauchen gering zu sein. ⓘ
Bei einer nicht rauchenden Bevölkerung ist die Nahrung die größte Expositionsquelle. Hohe Cadmiummengen finden sich in Krebstieren, Weichtieren, Innereien, Froschschenkeln, Kakaofeststoffen, Bitter- und Halbbitterschokolade, Meeresalgen, Pilzen und Algenprodukten. Getreide, Gemüse, stärkehaltige Wurzeln und Knollen werden jedoch in den USA in weitaus größeren Mengen verzehrt und sind dort die Quelle der größten ernährungsbedingten Belastung. Die meisten Pflanzen akkumulieren Metalltoxine wie Cadmium, und wenn sie zu organischem Dünger kompostiert werden, entsteht ein Produkt, das oft hohe Mengen (z. B. über 0,5 mg) an Metalltoxinen pro Kilogramm Dünger enthalten kann. Düngemittel aus Tiermist (z. B. Kuhmist) oder Siedlungsabfällen können ähnliche Mengen an Cadmium enthalten. Das dem Boden durch Düngemittel (Rohphosphate oder organische Düngemittel) zugeführte Cadmium wird nur dann bioverfügbar und giftig, wenn der pH-Wert des Bodens niedrig ist (d. h. bei sauren Böden). ⓘ
Zink-, Kupfer-, Kalzium- und Eisenionen sowie Selen in Verbindung mit Vitamin C werden zur Behandlung von Cadmiumvergiftungen eingesetzt, die jedoch nicht ohne weiteres rückgängig gemacht werden können. ⓘ
Die Weltgesundheitsorganisation hat ihre Aussage zur tolerierbaren Aufnahmemenge für Cadmium in den letzten Jahren mehrfach nach unten angepasst, zuletzt 2013 auf eine tolerierbare monatliche Aufnahmemenge (TMI) von 25 µg je Kilogramm Körpergewicht. Die Europäische Behörde für Lebensmittelsicherheit hat 2009 einen wiederum deutlich niedrigeren Wert von 2,5 µg je Kilogramm Körpergewicht tolerierbare wöchentlich Aufnahmemenge (TWI) ausgegeben. ⓘ
Cadmium wird vom Menschen hauptsächlich durch die Nahrung aufgenommen. Zu den cadmiumreichen Nahrungsmitteln zählen: Leber, Pilze, Muscheln und andere Schalentiere, Kakaopulver und getrockneter Seetang. Darüber hinaus enthalten Leinsamen viel Cadmium, weshalb empfohlen wird, täglich nicht mehr als 20 g Leinsamen zu sich zu nehmen. Zudem kommt es seit der Einführung von Kunstdüngern zu einer Anreicherung von Cadmium auf landwirtschaftlichen Flächen und somit in nahezu allen Lebensmitteln. Die Ressourcen von Phosphaten sind begrenzt, und die meisten Vorkommen sind belastet mit Cadmium oder radioaktiven Schwermetallen. Der Cadmiumgehalt der Phosphatlagerstätten ist sehr unterschiedlich. Viele Industrieländer haben bereits einen Grenzwert für Cadmium in Düngemitteln eingeführt. So gilt für das Inverkehrbringen von Düngemittel in Deutschland ein Grenzwert von 1,5 mg/kg und bei Düngemittel mit mehr als 5 % Phosphat bei 50 mg/kg, während diese Grenzwerte in Österreich bei 3 mg/kg und 75 mg/kg P2O5 liegen. Auch Tabakrauch transportiert relativ große Cadmiummengen in die Lungen, von wo aus es sich mit dem Blut im Körper verteilt. ⓘ
Besonders Personen, die in Fabriken mit hohem Cadmiumausstoß arbeiten, sind erhöhten Gefahren ausgesetzt. Auch von wilden Müllplätzen, Metallwerken oder Bränden gehen Gefahren aus. Das Einatmen von Cadmium kann die Lungen ernsthaft schädigen und sogar zum Tod führen. Dokumentierte Folgen nach Unfällen in der Industrie – wie in der chinesischen Provinz Guangdong – oder nach jahrzehntelanger Emissionen – wie im Falle der Itai-Itai-Krankheit (bei Menschen) und der Gressenicher Krankheit (bei Weidevieh) – machen die realen Gefahren deutlich. ⓘ
Schädigungen im Menschen
Cadmium kann sich industrie- oder umweltbedingt allmählich im Körper anreichern und eine schwer erkennbare chronische Vergiftung hervorrufen. ⓘ
Cadmium wird aus der Nahrung zu ungefähr 5 % im Darm resorbiert. Bei Eisen- und Calciummangel steigt die Resorptionsrate, was annehmen lässt, dass alle drei Metalle denselben Transportweg nutzen. Cadmium stimuliert zunächst in der Leber die Synthese von Metallothioneinen, mit denen es einen Komplex bildet und über den Blutkreislauf zu den Nierenglomeruli transportiert, dort filtriert und aus den Nierentubuli wieder aufgenommen wird. In den Tubuluszellen wird der Metallothionein-Cadmium-Komplex metabolisiert und Cd freigesetzt. Cd aktiviert hier wiederum eine vermehrte Metallthionsynthese, wodurch noch mehr Cadmium gebunden wird. Durch die Akkumulation in den Nieren kommt es zu Schädigungen dieses Organs mit der Folge einer Proteinurie. Durch diese Proteinbindung wird Cadmium nur extrem langsam ausgeschieden, die Halbwertszeit für den Verbleib im Körper beträgt bis zu 30 Jahren. Daher steigt der Cadmiumgehalt von Geburt an und fällt erst wieder bei einem Alter von 50–60 Jahren. ⓘ
Cadmium schädigt auch die Knochen, da es letztendlich zur Mobilisierung des Calciums führt. Cd konkurriert im Darm mit dem Calcium um die Bindungsstellen am Ca-bindenden Protein in der Darmmukosa. Zusätzlich blockiert Cd die Neusynthese des 1,25-Dihydroxycholecalciferol (Calcitriol) in den Nierentubuluszellen. 1,25-Dihydroxycholecalciferol ist notwendig, um die Synthese des Calciumbindenden Proteins in der Darmmukosazelle zu aktivieren. In summa bewirkt Cadmium eine verminderte Rückresorption des Calciums in Darm und Niere sowie die erhöhte Ausscheidung mit dem Harn mit der Folge einer Calciumfreisetzung aus den Knochen und damit dem Abbau derselbigen. ⓘ
Bei einer akuten Cadmiumvergiftung kann die biliäre Ausscheidung durch Gabe von Penicillamin oder Dimercaprol unterstützt werden. Eine effektive, darüber hinausgehende Therapie einer akuten Cadmiumvergiftung ist nicht bekannt. ⓘ
Symptome
- Durchfall, Magenschmerzen und heftiges Erbrechen
- Nierenschädigung
- Knochenbrüche
- Schäden am Zentralnervensystem
- Schäden am Immunsystem
- Störungen in der Fortpflanzung und eventuell sogar Unfruchtbarkeit
- Psychische Störungen
- Mögliche DNA-Schäden und Krebsentstehung
- Verlust des Geruchssinns ⓘ
Verbindungen
→ :Kategorie:Cadmiumverbindung ⓘ
Oxide und Hydroxide
- Cadmiumoxid CdO
- Cadmiumhydroxid Cd(OH)2 ⓘ
Halogenide
- Cadmiumfluorid CdF2
- Cadmiumchlorid CdCl2
- Cadmiumbromid CdBr2
- Cadmiumiodid CdI2 ⓘ
Chalkogenide
- Cadmiumsulfid CdS
- Cadmiumselenid CdSe
- Cadmiumtellurid CdTe ⓘ
Sonstige Verbindungen
- Cadmiumsulfat CdSO4
- Cadmiumnitrat Cd(NO3)2
- Cadmiumcyanid Cd(CN)2
- Cadmiumstearat Cd(C17H35COO)2 ⓘ
Biologische Rolle und Forschung
Cadmium hat in höheren Organismen keine bekannte Funktion und gilt als giftig. Cadmium gilt als Umweltschadstoff, der für lebende Organismen gesundheitsschädlich ist. Die Verabreichung von Cadmium an Zellen führt zu oxidativem Stress und erhöht den Gehalt an Antioxidantien, die von den Zellen zum Schutz vor makromolekularen Schäden produziert werden. ⓘ
In einigen marinen Kieselalgen wurde jedoch eine cadmiumabhängige Kohlensäureanhydrase gefunden. Die Diatomeen leben in Umgebungen mit sehr niedrigen Zinkkonzentrationen, und Cadmium übernimmt die Funktion, die normalerweise von Zink in anderen Anhydrasen übernommen wird. Dies wurde mit Hilfe der Röntgenabsorptions-Nahkantenstruktur-Spektroskopie (XANES) entdeckt. ⓘ
Cadmium wird vorzugsweise in den Nieren des Menschen absorbiert. Bis zu 30 mg Cadmium werden im Kindes- und Jugendalter üblicherweise eingeatmet. Die Toxizität von Cadmium für den Menschen wird derzeit erforscht, da es möglicherweise das Risiko von Krebs, Herz-Kreislauf-Erkrankungen und Osteoporose erhöht. ⓘ
Umwelt
Die Biogeochemie von Cadmium und seine Freisetzung in die Umwelt sind Gegenstand von Untersuchungen, ebenso wie die Speziation von Cadmium in der Umwelt. ⓘ
Vorschriften
Aufgrund der nachteiligen Auswirkungen von Cadmium auf die Umwelt und die menschliche Gesundheit ist die Lieferung und Verwendung von Cadmium in Europa durch die REACH-Verordnung eingeschränkt. ⓘ
Das EFSA-Gremium für Kontaminanten in der Lebensmittelkette gibt 2,5 μg/kg Körpergewicht als zulässige wöchentliche Aufnahmemenge für Menschen an. Der Gemeinsame FAO/WHO-Sachverständigenausschuss für Lebensmittelzusatzstoffe hat 7 μg/kg Körpergewicht als vorläufige zulässige wöchentliche Aufnahmemenge festgelegt. Der US-Bundesstaat Kalifornien schreibt vor, dass Produkte wie Kakaopulver auf dem Etikett einen Warnhinweis über eine mögliche Cadmiumexposition tragen müssen. ⓘ
Die U.S. Occupational Safety and Health Administration (OSHA) hat den zulässigen Expositionsgrenzwert (PEL) für Cadmium auf einen zeitlich gewichteten Durchschnitt (TWA) von 0,005 ppm festgelegt. Das National Institute for Occupational Safety and Health (NIOSH) hat keinen empfohlenen Expositionsgrenzwert (REL) festgelegt und Cadmium als bekanntes Karzinogen für den Menschen eingestuft. Der IDLH-Wert (unmittelbar lebens- und gesundheitsgefährdend) für Cadmium beträgt 9 mg/m3. ⓘ
| Tödliche Dosis | Organismus | Weg | Zeit ⓘ |
|---|---|---|---|
| LD50: 225 mg/kg | Ratte | oral | k.A. |
| LD50: 890 mg/kg | Maus | oral | k.A. |
| LC50: 25 mg/m3 | Ratte | k.A. | 30 Minuten |
Zusätzlich zu Quecksilber hat das Vorhandensein von Cadmium in einigen Batterien dazu geführt, dass eine ordnungsgemäße Entsorgung (oder Recycling) von Batterien vorgeschrieben ist. ⓘ
Produktrückrufe
Im Mai 2006 wurde der Verkauf der Sitze des alten Stadions von Arsenal F.C., Highbury in London, England, annulliert, als festgestellt wurde, dass die Sitze Spuren von Cadmium enthielten. Berichte über hohe Cadmiumwerte in Kinderschmuck führten 2010 zu einer Untersuchung der US-amerikanischen Kommission für die Sicherheit von Verbraucherprodukten. Die US-amerikanische CPSC erließ spezielle Rückrufaufrufe wegen des Cadmiumgehalts in Schmuck, der von Claire's und Wal-Mart verkauft wurde. ⓘ
Im Juni 2010 rief McDonald's freiwillig mehr als 12 Millionen Shrek Forever After 3D Collectible Drinking Glasses wegen des Cadmiumgehalts in den Farbpigmenten der Gläser zurück. Die Gläser wurden von Arc International in Millville, NJ, USA, hergestellt. ⓘ






