Palladium
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Palladium | |||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Aussprache | /pəˈleɪdiəm/ (pə-LAY-dee-əm) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Erscheinungsbild | silbrig-weiß | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Standard-Atomgewicht Ar°(Pd) |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Palladium im Periodensystem | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordnungszahl (Z) | 46 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe | Gruppe 10 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periode | Periode 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Block | d-Block | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronen-Konfiguration | [[[Krypton|Kr]]] 4d10 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronen pro Schale | 2, 8, 18, 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physikalische Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase bei STP | fest | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzpunkt | 1828,05 K (1554,9 °C, 2830,82 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Siedepunkt | 3236 K (2963 °C, 5365 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dichte (nahe r.t.) | 12,023 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| in flüssigem Zustand (bei mittlerem Druck) | 10,38 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzwärme | 16,74 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verdampfungswärme | 358 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molare Wärmekapazität | 25,98 J/(mol-K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
Verdampfungsdruck
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomare Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidationsstufen | 0, +1, +2, +3, +4 (ein schwach basisches Oxid) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativität | Pauling-Skala: 2,20 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionisierungsenergien |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomradius | empirisch: 137 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalenter Radius | 139±6 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van-der-Waals-Radius | 163 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spektrallinien von Palladium | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Andere Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Natürliches Vorkommen | primordial | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallstruktur | kubisch-flächenzentriert (fcc) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schallgeschwindigkeit dünner Stab | 3070 m/s (bei 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermische Ausdehnung | 11,8 µm/(m⋅K) (bei 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 71,8 W/(m⋅K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrischer Widerstand | 105,4 nΩ⋅m (bei 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetische Ordnung | paramagnetisch | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molare magnetische Suszeptibilität | +567,4×10-6 cm3/mol (288 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elastizitätsmodul | 121 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schermodul | 44 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elastizitätsmodul | 180 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poissonzahl | 0.39 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs-Härte | 4.75 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vickers-Härte | 400-600 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell-Härte | 320-610 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-Nummer | 7440-05-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Geschichte | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Namensgebung | nach dem Asteroiden Pallas, der seinerseits nach Pallas Athena benannt wurde | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entdeckung und erste Isolierung | William Hyde Wollaston (1802) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hauptisotope von Palladium | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
Palladium ist ein chemisches Element mit dem Symbol Pd und der Ordnungszahl 46. Es ist ein seltenes, silbrig-weiß glänzendes Metall, das 1803 von dem englischen Chemiker William Hyde Wollaston entdeckt wurde. Er benannte es nach dem Asteroiden Pallas, der seinerseits nach dem Beinamen der griechischen Göttin Athene benannt wurde, den diese erhielt, als sie Pallas erschlug. Palladium, Platin, Rhodium, Ruthenium, Iridium und Osmium bilden eine Gruppe von Elementen, die als Platingruppenmetalle (PGMs) bezeichnet werden. Sie haben ähnliche chemische Eigenschaften, aber Palladium hat den niedrigsten Schmelzpunkt und die geringste Dichte. ⓘ
Mehr als die Hälfte des Angebots an Palladium und seinem Verwandten Platin wird in Katalysatoren verwendet, die bis zu 90 % der schädlichen Gase in Autoabgasen (Kohlenwasserstoffe, Kohlenmonoxid und Stickstoffdioxid) in harmlose Stoffe (Stickstoff, Kohlendioxid und Wasserdampf) umwandeln. Palladium wird auch in der Elektronik, der Zahnmedizin, der Medizin, der Wasserstoffreinigung, in chemischen Anwendungen, der Grundwasseraufbereitung und in der Schmuckherstellung verwendet. Palladium ist ein wichtiger Bestandteil von Brennstoffzellen, in denen Wasserstoff und Sauerstoff reagieren, um Strom, Wärme und Wasser zu erzeugen. ⓘ
Erzvorkommen von Palladium und anderen Platinmetallen sind selten. Die umfangreichsten Vorkommen befinden sich im Noritgürtel des Bushveld Igneous Complex, der das Transvaal-Becken in Südafrika bedeckt, im Stillwater Complex in Montana (USA), im Sudbury-Becken und im Thunder Bay District in Ontario (Kanada) sowie im Norilsk-Komplex in Russland. Eine weitere Quelle ist das Recycling, vor allem von verschrotteten Katalysatoren. Die zahlreichen Anwendungen und die begrenzten Bezugsquellen führen zu einem erheblichen Investitionsinteresse. ⓘ
Merkmale
Palladium gehört zur Gruppe 10 des Periodensystems, aber die Konfiguration der äußersten Elektronen entspricht der Hundschen Regel. Die Elektronen im 5s-Orbital wandern in die 4d-Orbitale, da es energetisch günstiger ist, eine vollständig gefüllte 4d10-Schale statt der 5s2 4d8-Konfiguration zu haben. ⓘ
| Z | Element | Anzahl der Elektronen/Schale ⓘ |
|---|---|---|
| 28 | Nickel | 2, 8, 16, 2 (oder 2, 8, 17, 1) |
| 46 | Palladium | 2, 8, 18, 18, 0 |
| 78 | Platin | 2, 8, 18, 32, 17, 1 |
| 110 | Darmstadtium | 2, 8, 18, 32, 32, 16, 2 (vorhergesagt) |
Diese in der Periode 5 einzigartige 5s0-Konfiguration macht Palladium zum schwersten Element mit nur einer unvollständigen Elektronenschale, während alle darüber liegenden Schalen leer sind. ⓘ
Palladium sieht aus wie ein weiches, silberweißes Metall, das dem Platin ähnelt. Es hat die geringste Dichte und den niedrigsten Schmelzpunkt der Platingruppenmetalle. Es ist weich und dehnbar, wenn es geglüht wird, und gewinnt durch Kaltverformung stark an Festigkeit und Härte. Palladium löst sich langsam in konzentrierter Salpetersäure, in heißer, konzentrierter Schwefelsäure und, wenn es fein gemahlen ist, in Salzsäure. Es löst sich bei Raumtemperatur leicht in Königswasser. ⓘ
Palladium reagiert bei Normaltemperatur nicht mit Sauerstoff (und läuft daher an der Luft nicht an). Auf 800 °C erhitztes Palladium bildet eine Schicht aus Palladium(II)-oxid (PdO). Diese kann im Laufe der Zeit eine leichte bräunliche Färbung annehmen, was wahrscheinlich auf die Bildung einer Oberflächenschicht aus seinem Monoxid zurückzuführen ist. ⓘ
Palladiumfilme mit Defekten, die durch Alphateilchenbeschuss bei niedriger Temperatur erzeugt wurden, weisen Supraleitfähigkeit mit Tc=3,2 K auf. ⓘ
Isotope
Das natürlich vorkommende Palladium besteht aus sieben Isotopen, von denen sechs stabil sind. Die stabilsten Radioisotope sind 107Pd mit einer Halbwertszeit von 6,5 Millionen Jahren (in der Natur gefunden), 103Pd mit 17 Tagen und 100Pd mit 3,63 Tagen. Achtzehn weitere Radioisotope mit Atomgewichten zwischen 90,94948(64) u (91Pd) und 122,93426(64) u (123Pd) wurden charakterisiert. Diese Isotope haben Halbwertszeiten von weniger als dreißig Minuten, mit Ausnahme von 101Pd (Halbwertszeit: 8,47 Stunden), 109Pd (Halbwertszeit: 13,7 Stunden) und 112Pd (Halbwertszeit: 21 Stunden). ⓘ
Bei Isotopen mit einer Atommasseneinheit, die kleiner ist als die des häufigsten stabilen Isotops, 106Pd, ist der primäre Zerfallsmodus der Elektroneneinfang, wobei das primäre Zerfallsprodukt Rhodium ist. Der primäre Zerfallsmodus für die Pd-Isotope mit einer Atommasse von mehr als 106 ist der Betazerfall, wobei das Hauptprodukt dieses Zerfalls Silber ist. ⓘ
Radiogenes 107Ag ist ein Zerfallsprodukt von 107Pd und wurde erstmals 1978 im Santa-Clara-Meteoriten von 1976 entdeckt. Die Entdecker vermuten, dass die Koaleszenz und Differenzierung der eisenhaltigen Kleinplaneten 10 Millionen Jahre nach einem nukleosynthetischen Ereignis stattgefunden haben könnte. Die Korrelationen zwischen 107Pd und Ag, die in Körpern beobachtet wurden, die seit der Akkretion des Sonnensystems geschmolzen sind, müssen das Vorhandensein von kurzlebigen Nukliden im frühen Sonnensystem widerspiegeln. 107
Pd entsteht auch als Spaltprodukt bei der spontanen oder induzierten Spaltung von 235
U. Da es in der Umwelt nicht sehr mobil ist und eine relativ niedrige Zerfallsenergie hat, wird 107
Pd in der Regel als eines der weniger problematischen langlebigen Spaltprodukte angesehen. ⓘ
Verbindungen
Palladiumverbindungen kommen hauptsächlich in den Oxidationsstufen 0 und +2 vor. Andere, weniger häufige Zustände sind ebenfalls bekannt. Im Allgemeinen sind die Verbindungen von Palladium denen von Platin ähnlicher als denen jedes anderen Elements. ⓘ
Struktur von β-PdCl2 ⓘ
Palladium(II)
Palladium(II)-chlorid wird als Katalysator im Wacker-Hoechst-Verfahren verwendet. Dabei entsteht aus Palladium(II)-chlorid, Ethen und einem Chloridion ein zum Zeise-Salz äquivalenter anionischer Palladium(II)-Ethen-Komplex, das Trichloridoethylenpalladinat(II)-Anion. Der Ethenligand übt einen starken trans-Effekt aus, wodurch die Bindung des trans-ständigen Chloridoliganden geschwächt und die Anlagerung von Wasser unter Verdrängungen eines Chlorid-Ions ermöglicht. Durch diesen Austausch entsteht letztendlich wieder ein anionischer Ethen-Hydroxo-Komplex. Durch Insertion des Ethen-Liganden in die Pd-OH-Bindung und Addition von Wasser entsteht ein 2-Hydroxyethyl-Komplex. Letztendlich entsteht durch Eliminierung von Acetaldehyd und zwei Wasserstoffionen metallisches Palladium, welches durch Kupfer(II)-Salze reoxidiert wird. Die entstehenden Kupfer(I)-Salze lassen sich in Gegenwart von Säure durch Luft reoxidieren. ⓘ
Die Teilreaktionen lassen sich als gekoppelte Teilreaktionen darstellen:


Palladium(0)
Palladium bildet eine Reihe von nullwertigen Komplexen mit der Formel PdL4, PdL3 und PdL2. Beispielsweise ergibt die Reduktion einer Mischung aus PdCl2(PPh3)2 und PPh3 Tetrakis(triphenylphosphin)palladium(0):
Ein weiterer wichtiger Palladium(0)-Komplex, Tris(dibenzylidenaceton)dipalladium(0) (Pd2(dba)3), wird durch Reduktion von Natriumtetrachlorpalladat in Gegenwart von Dibenzylidenaceton hergestellt. ⓘ
Sowohl Palladium(0) als auch Palladium(II) sind Katalysatoren in Kupplungsreaktionen, wie der Nobelpreis für Chemie 2010 an Richard F. Heck, Ei-ichi Negishi und Akira Suzuki belegt. Solche Reaktionen werden häufig für die Synthese von Feinchemikalien eingesetzt. Zu den bekanntesten Kupplungsreaktionen gehören die Heck-, Suzuki-, Sonogashira-, Stille- und Kumada-Kupplung. Palladium(II)-acetat, Tetrakis(triphenylphosphin)-palladium(0) (Pd(PPh3)4) und Tris(dibenzylidenaceton)-dipalladium(0) (Pd2(dba)3) dienen entweder als Katalysatoren oder Präkatalysatoren. ⓘ
Andere Oxidationsstufen
Obwohl Pd(IV)-Verbindungen vergleichsweise selten sind, ist ein Beispiel Natriumhexachlorpalladat(IV), Na2[PdCl6]. Es sind auch einige Palladium(III)-Verbindungen bekannt. Palladium(VI) wurde im Jahr 2002 behauptet, aber später widerlegt. ⓘ
Es gibt Palladiumkomplexe mit gemischter Wertigkeit, z. B. Pd4(CO)4(OAc)4Pd(acac)2, die eine unendliche Pd-Kettenstruktur mit abwechselnd miteinander verbundenen Pd4(CO)4(OAc)4- und Pd(acac)2-Einheiten bilden. ⓘ
Wenn es mit einem elektropositiven Element legiert wird, kann Palladium eine negative Ladung erhalten. Solche Verbindungen sind als Palladide bekannt, wie z. B. Galliumpalladid. Es gibt Palladide mit der Stöchiometrie RPd3, wobei R für Scandium, Yttrium oder eines der Lanthanide steht. ⓘ
Vorkommen
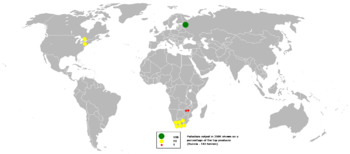
Die gesamte Minenproduktion von Palladium erreichte im Jahr 2016 208.000 Kilogramm, wobei Russland mit 82.000 Kilogramm der größte Produzent war, gefolgt von Südafrika, Kanada und den USA. Das russische Unternehmen Norilsk Nickel steht mit einem Anteil von 39 % an der weltweiten Produktion an erster Stelle der größten Palladiumproduzenten. ⓘ
Palladium kommt als freies Metall, das mit Gold und anderen Platingruppenmetallen legiert ist, in Seifenlagerstätten im Ural, in Australien, Äthiopien, Nord- und Südamerika vor. Für die Produktion von Palladium spielen diese Lagerstätten nur eine untergeordnete Rolle. Die wichtigsten kommerziellen Quellen sind die Nickel-Kupfer-Lagerstätten im Sudbury-Becken, Ontario, und die Norilsk-Talnakh-Lagerstätten in Sibirien. Die andere große Lagerstätte ist das Merensky-Riff, ein Platingruppenmetallvorkommen im Bushveld-Egneo-Komplex in Südafrika. Der Stillwater-Erzkomplex in Montana und der Roby-Zonen-Erzkörper im Lac des Îles-Erzkomplex in Ontario sind die beiden anderen Palladiumvorkommen in Kanada und den Vereinigten Staaten. Palladium kommt in den seltenen Mineralien Cooperit und Polarit vor. Es sind noch viele weitere Pd-Minerale bekannt, die jedoch alle sehr selten sind. ⓘ
Palladium wird auch in Kernspaltungsreaktoren gewonnen und kann aus abgebrannten Kernbrennstoffen extrahiert werden (siehe Synthese von Edelmetallen), allerdings wird diese Palladiumquelle nicht genutzt. Keine der bestehenden nuklearen Wiederaufbereitungsanlagen ist für die Gewinnung von Palladium aus hochradioaktiven Abfällen ausgerüstet. Eine Komplikation bei der Rückgewinnung von Palladium in abgebrannten Brennelementen ist das Vorhandensein von 107
Pd, einem schwach radioaktiven, langlebigen Spaltprodukt. Je nach Endverwendung kann die Radioaktivität des 107
Pd beigetragene Radioaktivität das zurückgewonnene Palladium ohne einen kostspieligen Schritt der Isotopentrennung unbrauchbar machen. ⓘ
Anwendungen


Am häufigsten wird Palladium heute in Katalysatoren verwendet. Palladium wird auch in der Schmuckherstellung, in der Zahnmedizin, bei der Herstellung von Uhren, Blutzuckerteststreifen, Flugzeugzündkerzen, chirurgischen Instrumenten und elektrischen Kontakten verwendet. Palladium wird auch für die Herstellung professioneller Querflöten (Konzert- oder klassische Flöten) verwendet. Palladiumbarren haben als Rohstoff die ISO-Währungscodes XPD und 964. Palladium ist eines von nur vier Metallen mit einem solchen Code, die anderen sind Gold, Silber und Platin. Da es Wasserstoff adsorbiert, war Palladium eine Schlüsselkomponente bei den umstrittenen Experimenten zur kalten Fusion in den späten 1980er Jahren. ⓘ
Katalyse
In fein verteilter Form, wie bei Palladium auf Kohlenstoff, ist Palladium ein vielseitiger Katalysator, der heterogene katalytische Prozesse wie Hydrierung, Dehydrierung und Cracken von Erdöl beschleunigt. Palladium ist auch für den Lindlar-Katalysator, auch Lindlar's Palladium genannt, wesentlich. Zahlreiche Kohlenstoff-Kohlenstoff-Bindungsreaktionen in der organischen Chemie werden durch Katalysatoren aus Palladiumverbindungen erleichtert. Zum Beispiel:
- Heck-Reaktion
- Suzuki-Kupplung
- Tsuji-Trost-Reaktionen
- Wacker-Verfahren
- Negishi-Reaktion
- Stille-Kupplung
- Sonogashira-Kupplung ⓘ
(Siehe Palladiumverbindungen und Palladium-katalysierte Kupplungsreaktionen). ⓘ
Auf leitfähigen Materialien dispergiert, ist Palladium ein ausgezeichneter Elektrokatalysator für die Oxidation primärer Alkohole in alkalischen Medien. Palladium ist auch ein vielseitiges Metall für die homogene Katalyse, das in Kombination mit einer breiten Palette von Liganden für hochselektive chemische Umwandlungen verwendet wird. ⓘ
Im Jahr 2010 wurde der Nobelpreis für Chemie "für palladiumkatalysierte Kreuzkupplungen in der organischen Synthese" an Richard F. Heck, Ei-ichi Negishi und Akira Suzuki verliehen. Eine Studie aus dem Jahr 2008 zeigte, dass Palladium ein effektiver Katalysator für Kohlenstoff-Fluor-Bindungen ist. ⓘ
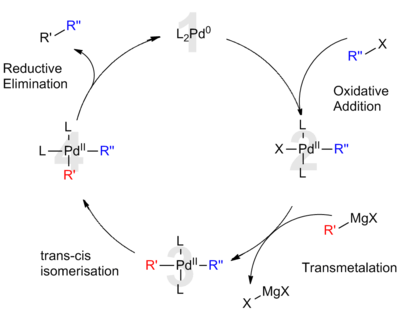
Die Palladiumkatalyse wird in erster Linie in der organischen Chemie und in industriellen Anwendungen eingesetzt, obwohl ihre Verwendung als Werkzeug für die synthetische Biologie zunimmt; 2017 wurde eine wirksame katalytische In-vivo-Aktivität von Palladium-Nanopartikeln in Säugetieren zur Behandlung von Krankheiten nachgewiesen. ⓘ
Ein Lindlar-Katalysator ist ein heterogener Kontakt, der aus auf Calciumcarbonat abgeschiedenem Palladium besteht. Der Palladiumgehalt des Trägerkatalysators beträgt etwa 5 %. Zur Verringerung der katalytischen Aktivität wird das Palladium zum Beispiel mit Blei, Schwefel oder Chinolin vergiftet. Es wird zur Hydrierung von Alkinen zu Alkenen verwendet, etwa zur Reduktion von Phenylacetylen zu Styrol ohne eine weitere Reduktion zu Alkanen und ist nach seinem Erfinder Herbert Lindlar benannt. ⓘ
Elektronik
Die erste große Anwendung von Palladium in der Elektronik sind keramische Mehrschichtkondensatoren, bei denen Palladium (und Palladium-Silber-Legierungen) für Elektroden verwendet werden. Palladium (manchmal mit Nickel legiert) wird oder kann für die Beschichtung von Bauteilen und Steckern in der Unterhaltungselektronik und in Lötmaterialien verwendet werden. Einem Bericht von Johnson Matthey zufolge verbrauchte der Elektroniksektor im Jahr 2006 1,07 Millionen Feinunzen (33 Tonnen) Palladium. ⓘ
Verwendung in der chemischen Industrie
- Platintiegel (80 % Pt, 20 % Pd)
- Durch heißes Palladiumblech diffundiert Wasserstoff fast ohne Widerstand, wodurch es sich zum Reinigen von Wasserstoff oder Abtrennung von Wasserstoff aus Gasgemischen eignet. In heißem Palladium besitzt Wasserstoff ein hohes Diffusionsvermögen.
- Speichermedium für Wasserstoff, da es sehr große Mengen Wasserstoff absorbieren kann. Aus diesem Grund wurde es auch als Kathodenmaterial in den notorischen Experimenten von Fleischmann und Pons zur Kalten Fusion (und zahlreichen Nachfolgeexperimenten) verwendet. ⓘ
Speicherung von Wasserstoff
Palladium adsorbiert bei Raumtemperaturen leicht Wasserstoff und bildet dabei Palladiumhydrid PdHx mit x kleiner als 1. Diese Eigenschaft ist zwar vielen Übergangsmetallen gemeinsam, doch Palladium hat eine einzigartig hohe Absorptionskapazität und verliert seine Duktilität erst, wenn x sich 1 nähert. Diese Eigenschaft wurde bei der Entwicklung eines effizienten, kostengünstigen und sicheren Wasserstoffspeichermediums untersucht, obwohl Palladium selbst für diesen Zweck derzeit unerschwinglich ist. Der Wasserstoffgehalt in Palladium kann mit der magnetischen Suszeptibilität in Verbindung gebracht werden, die mit zunehmendem Wasserstoffgehalt abnimmt und für PdH0,62 gleich Null wird. Bei jedem höheren Verhältnis wird der Mischkristall diamagnetisch. ⓘ
Palladium wird auch für die Reinigung von Wasserstoff über Wasserstoffreinigungsmembranen verwendet. ⓘ
Zahnmedizin
Palladium wird in geringen Mengen (etwa 0,5 %) in einigen Legierungen für Zahnamalgam verwendet, um die Korrosion zu verringern und den Metallglanz der endgültigen Restauration zu erhöhen. ⓘ
Schmuck
Palladium wird seit 1939 als Edelmetall in der Schmuckherstellung verwendet, und zwar als Alternative zu Platin in den als "Weißgold" bezeichneten Legierungen, bei denen die von Natur aus weiße Farbe des Palladiums keine Rhodiumbeschichtung erfordert. Palladium hat eine wesentlich geringere Dichte als Platin. Ähnlich wie Gold kann Palladium zu Blättern mit einer Dicke von bis zu 100 nm (1⁄250.000 in) geschlagen werden. Im Gegensatz zu Platin kann sich Palladium bei Temperaturen über 400 °C (752 °F) aufgrund von Oxidation verfärben, wodurch es spröder wird und sich daher weniger für die Verwendung in Schmuckstücken eignet; um dies zu verhindern, wird Palladium, das für Schmuckstücke bestimmt ist, unter kontrollierten Bedingungen erhitzt. ⓘ
Vor 2004 wurde Palladium in der Schmuckherstellung hauptsächlich zur Herstellung von Weißgold verwendet. Palladium ist eines der drei beliebtesten Legierungsmetalle für Weißgold (Nickel und Silber können ebenfalls verwendet werden). Palladium-Gold ist teurer als Nickel-Gold, verursacht aber nur selten allergische Reaktionen (obwohl bestimmte Kreuzallergien mit Nickel auftreten können). ⓘ
Als Platin während des Zweiten Weltkriegs zu einer strategischen Ressource wurde, wurden viele Schmuckbänder aus Palladium hergestellt. Palladium wurde wegen der technischen Schwierigkeiten beim Gießen nur wenig für Schmuck verwendet. Als das Gussproblem gelöst war, nahm die Verwendung von Palladium in Schmuckstücken zu, was ursprünglich darauf zurückzuführen war, dass der Preis von Platin stieg, während der Preis von Palladium sank. Anfang 2004, als die Gold- und Platinpreise steil anstiegen, begann China mit der Herstellung von Palladiumschmuck in großen Mengen und verbrauchte im Jahr 2005 37 Tonnen. Spätere Veränderungen des relativen Platinpreises ließen die Nachfrage nach Palladium auf 17,4 Tonnen im Jahr 2009 sinken. Die Nachfrage nach Palladium als Katalysator hat dazu geführt, dass der Palladiumpreis im Januar 2019 etwa 50 % über dem Platinpreis lag. ⓘ
Im Januar 2010 führten die Prüfstellen im Vereinigten Königreich Punzierungen für Palladium ein, und die Punzierung wurde für alle Schmuckstücke, die mit reinem oder legiertem Palladium werben, obligatorisch. Die Artikel können mit 500, 950 oder 999 Teilen Palladium pro Tausend der Legierung gekennzeichnet werden. ⓘ
Füllfederhalterfedern aus Gold werden manchmal mit Palladium beschichtet, wenn ein silbernes (statt goldenes) Aussehen gewünscht wird. Sheaffer verwendet die Palladiumbeschichtung seit Jahrzehnten, entweder als Akzent auf ansonsten goldenen Federn oder zur vollständigen Abdeckung des Goldes. ⓘ
Palladium wird auch von der Luxusmarke Hermes als eines der Metalle verwendet, mit denen die Beschläge ihrer Handtaschen beschichtet sind, von denen die Birkin die berühmteste ist. ⓘ
Fotografie
Im Platinotypie-Verfahren stellen Fotografen mit Hilfe von Platin- oder Palladiumsalzen hochwertige Schwarz-Weiß-Drucke her. Palladium wird häufig zusammen mit Platin verwendet und stellt eine Alternative zu Silber dar. ⓘ
Auswirkungen auf die Gesundheit
Toxizität
| Gefahren | |
|---|---|
| GHS-Kennzeichnung: | |
Piktogramme
|

|
Signalwort
|
Warnhinweis |
Gefahrenhinweise
|
H317 |
Sicherheitshinweise
|
P261, P273, P280, P302+P352, P321, P333+P313, P363, P501 |
| NFPA 704 (Feuerdiamant) | |
Palladium ist ein Metall mit geringer Toxizität, wie sie konventionell gemessen wird (z. B. LD50). Neuere Forschungen über den Mechanismus der Palladiumtoxizität deuten auf eine hohe Toxizität hin, wenn sie über einen längeren Zeitraum und auf zellulärer Ebene in Leber und Niere gemessen wird. Die Mitochondrien scheinen eine Schlüsselrolle bei der Palladiumtoxizität zu spielen, da das mitochondriale Membranpotenzial zusammenbricht und der zelluläre Glutathionspiegel (GSH) sinkt. Bis zu dieser jüngsten Arbeit war man davon ausgegangen, dass Palladium bei der Aufnahme durch den menschlichen Körper nur schlecht absorbiert wird. Pflanzen wie die Wasserhyazinthe werden durch geringe Mengen von Palladiumsalzen abgetötet, aber die meisten anderen Pflanzen tolerieren es, obwohl Tests zeigen, dass bei Mengen über 0,0003 % das Wachstum beeinträchtigt wird. Hohe Palladiumdosen könnten giftig sein; Tests an Nagetieren deuten darauf hin, dass es krebserregend sein könnte, obwohl es bis zu den oben zitierten jüngsten Forschungsergebnissen keine eindeutigen Hinweise darauf gab, dass das Element für den Menschen schädlich ist. ⓘ
Vorsichtsmaßnahmen
Wie andere Metalle der Platingruppe ist auch Pd in der Masse recht inert. Es wurde zwar über Kontaktdermatitis berichtet, doch liegen nur wenige Daten über die Auswirkungen vor. Es hat sich gezeigt, dass Menschen, die allergisch auf Palladium reagieren, auch auf Nickel reagieren, so dass es ratsam ist, die Verwendung von palladiumhaltigen Dentallegierungen bei solchen Allergikern zu vermeiden. ⓘ
Ein Teil des Palladiums wird mit den Abgasen von Autos mit Katalysator ausgestoßen. Zwischen 4 und 108 ng/km an Palladiumpartikeln werden von solchen Autos freigesetzt, während die Gesamtaufnahme über die Nahrung auf weniger als 2 µg pro Person und Tag geschätzt wird. Die zweite mögliche Palladiumquelle ist die Zahnrestauration, bei der die Aufnahme von Palladium auf weniger als 15 µg pro Person und Tag geschätzt wird. Personen, die mit Palladium oder Palladiumverbindungen arbeiten, könnten eine wesentlich höhere Aufnahme aufweisen. Bei löslichen Verbindungen wie Palladiumchlorid werden 99 % innerhalb von 3 Tagen aus dem Körper ausgeschieden. ⓘ
Die mittlere tödliche Dosis (LD50) von löslichen Palladiumverbindungen bei Mäusen beträgt 200 mg/kg bei oraler und 5 mg/kg bei intravenöser Verabreichung. ⓘ
Geschichte

William Hyde Wollaston vermerkte die Entdeckung eines neuen Edelmetalls im Juli 1802 in seinem Laborbuch und nannte es im August desselben Jahres Palladium. Wollaston reinigte eine Menge des Materials und bot es im April 1803 in einem kleinen Geschäft in Soho an, ohne den Entdecker zu nennen. Nach harscher Kritik von Richard Chenevix, der behauptete, Palladium sei eine Legierung aus Platin und Quecksilber, setzte Wollaston anonym eine Belohnung von 20 Pfund für 20 Körner der synthetischen Palladiumlegierung aus. Chenevix erhielt 1803 die Copley-Medaille, nachdem er seine Experimente mit Palladium veröffentlicht hatte. Wollaston veröffentlichte 1804 die Entdeckung von Rhodium und erwähnte einige seiner Arbeiten über Palladium. In einer Veröffentlichung im Jahr 1805 gab er bekannt, dass er der Entdecker des Palladiums war. ⓘ
Es wurde von Wollaston 1802 nach dem Asteroiden 2 Pallas benannt, der zwei Monate zuvor entdeckt worden war. Wollaston fand Palladium in rohem Platinerz aus Südamerika, indem er das Erz in Königswasser auflöste, die Lösung mit Natriumhydroxid neutralisierte und das Platin mit Ammoniumchlorid als Ammoniumchloroplatinat ausfiel. Er fügte Quecksilbercyanid hinzu, um die Verbindung Palladium(II)-cyanid zu bilden, die zur Gewinnung von Palladiummetall erhitzt wurde. ⓘ
Palladiumchlorid wurde einst zur Behandlung von Tuberkulose in einer Dosierung von 0,065 g pro Tag (etwa ein Milligramm pro Kilogramm Körpergewicht) verschrieben. Diese Behandlung hatte viele negative Nebenwirkungen und wurde später durch wirksamere Medikamente ersetzt. ⓘ
Das meiste Palladium wird für Katalysatoren in der Autoindustrie verwendet. Katalysatoren sind ein Ziel für Diebe, weil sie Palladium und andere seltene Metalle enthalten. Im Vorfeld des Jahres 2000 kam es wiederholt zu Verzögerungen und Unterbrechungen bei der russischen Versorgung des Weltmarktes mit Palladium; aus politischen Gründen wurde die Exportquote nicht rechtzeitig gewährt. Die darauf folgende Marktpanik trieb den Preis im Januar 2001 auf ein Allzeithoch von 1.340 $ pro Feinunze (43 $/g). Zu dieser Zeit legte die Ford Motor Company, die eine Störung der Automobilproduktion durch einen Palladiummangel befürchtete, Lagerbestände des Metalls an. Als die Preise Anfang 2001 fielen, verlor Ford fast 1 Milliarde US-Dollar. ⓘ
Die weltweite Nachfrage nach Palladium stieg von 100 Tonnen im Jahr 1990 auf fast 300 Tonnen im Jahr 2000. Nach Angaben des United States Geological Survey belief sich die weltweite Produktion von Palladium aus Minen im Jahr 2006 auf 222 Tonnen. Nach der Annexion der Krim durch Russland sorgten sich viele um ein stabiles Palladiumangebot, auch weil die Sanktionen die russischen Palladiumexporte behindern könnten; etwaige Beschränkungen der russischen Palladiumexporte hätten das für 2014 ohnehin erwartete große Palladiumdefizit noch verschärfen können. Diese Bedenken ließen die Palladiumpreise auf den höchsten Stand seit 2001 steigen. Im September 2014 kletterten sie über die Marke von 900 $ pro Unze. Im Jahr 2016 kostete Palladium jedoch rund 614 $ pro Unze, da es Russland gelang, das Angebot stabil zu halten. Im Januar 2019 kletterten die Palladium-Futures zum ersten Mal in der Geschichte über die Marke von $ 1.344 pro Unze, was vor allem auf die starke Nachfrage aus der Automobilindustrie zurückzuführen war. Am 6. Januar 2020 erreichte Palladium 2.024,64 $ pro Feinunze (65,094 $/g) und überschritt damit zum ersten Mal die Marke von 2.000 $ pro Feinunze. Im Mai 2021 und März 2022 stieg der Preis auf über 3.000 $ je Feinunze. ⓘ
Palladium als Investition
Die weltweiten Palladiumverkäufe beliefen sich 2017 auf 8,84 Millionen Unzen (250,6 Tonnen), wovon 86 % für die Herstellung von Autokatalysatoren verwendet wurden, gefolgt von Industrie-, Schmuck- und Investitionszwecken. Mehr als 75 % des weltweiten Platins und 40 % des Palladiums werden in Südafrika abgebaut. Die russische Bergbaugesellschaft Norilsk Nickel fördert weitere 44 % des Palladiums, der Rest stammt aus Minen in den USA und Kanada. ⓘ
Der Preis für Palladium erreichte am 3. Mai 2021 ein Allzeithoch von $ 2.981,40 pro Unze, was vor allem auf Spekulationen über die Nachfrage der Automobilindustrie nach Katalysatoren zurückzuführen war. Palladium wird auf dem Kassamarkt unter dem Code "XPD" gehandelt. Wird es in USD abgerechnet, lautet der Code "XPDUSD". Ein späterer Überschuss des Metalls wurde durch den Verkauf von Lagerbeständen aus der Sowjetzeit durch die russische Regierung verursacht, und zwar in einer Größenordnung von etwa 1,6 bis 2 Millionen Unzen (45,4 bis 56,7 metrische Tonnen) pro Jahr. Die Menge und der Status dieser Bestände sind ein Staatsgeheimnis. ⓘ
Während des russisch-ukrainischen Krieges im März 2022 stiegen die Preise für Palladium seit dem ersten März um 13 %. Russland ist der Hauptlieferant für Europa, und das Land liefert 37 % der weltweiten Produktion. ⓘ
Palladiumproduzenten
- Norilsk Nickel (MCX: GMKN, LSE: MNOD), Palladiumpulver und -barren.
- North American Palladium (NYSE: PAL), Kanadas größter Palladiumproduzent, betreibt die Palladiummine Lac des Iles in der Nähe von Thunder Bay, Ontario.
- Stillwater Mining (NYSE: SWC), ein großer nordamerikanischer Palladiumförderer in Montana. ⓘ
Börsengehandelte Produkte
WisdomTree Physical Palladium (LSE: PHPD) ist durch zugewiesene Palladiumbarren unterlegt und war der erste börsengehandelte Palladiumfonds der Welt. Er ist an der Londoner Börse als PHPD, im Xetra Trading System, an der Euronext und in Mailand notiert. ETFS Physical Palladium Shares (NYSE: PALL) ist ein an der New Yorker Börse gehandelter ETF. ⓘ
Bullionmünzen und -barren
Eine traditionelle Möglichkeit, in Palladium zu investieren, ist der Kauf von Anlagemünzen und -barren aus Palladium. Zu den verfügbaren Palladiummünzen gehören der kanadische Palladium Maple Leaf, der chinesische Panda und der amerikanische Palladium Eagle. Die Liquidität einer direkten Anlage in Palladiumbarren ist geringer als die von Gold und Silber, da Palladiummünzen nur in geringem Umfang in Umlauf sind. ⓘ
Eigenschaften
Chemische Eigenschaften
Palladium ist ein Edelmetall, auch wenn es deutlich reaktiver ist als das verwandte Element Platin: Es löst sich in Salpetersäure, wobei Palladium(II)-nitrat Pd(NO3)2 gebildet wird. Es löst sich ebenfalls in Königswasser und in heißer konzentrierter Schwefelsäure. In Salzsäure löst es sich bei Luftzutritt langsam unter Bildung eines Palladiumchloridanions (PdCl42−) auf. Der Edelmetallcharakter von Palladium ist dem des benachbarten Silbers vergleichbar. In Salzsäure verhält es sich aufgrund der Bildung leichtlöslicher Palladiumchloridverbindungen unedel. In feuchter Atmosphäre bei Anwesenheit von Schwefel wird die Oberfläche von Palladium getrübt. ⓘ
Palladium besitzt die höchste Absorptionsfähigkeit aller Elemente für Wasserstoff. Diese grundlegende Entdeckung geht auf Thomas Graham im Jahre 1869 zurück. Bei Raumtemperatur kann es das 900fache, Palladiummohr (feinverteiltes schwarzes Palladiumpulver) das 1200fache und kolloidale Palladiumlösungen können das 3000fache des eigenen Volumens binden. Die Wasserstoffaufnahme kann als Lösen von Wasserstoff im Metallgitter und als Bildung eines Palladiumhydrids mit der ungefähren Zusammensetzung Pd2H beschrieben werden. ⓘ
Gewöhnlich nimmt es die Oxidationsstufen +2 und +4 an. Bei Verbindungen der scheinbaren Oxidationsstufe +3 handelt es sich meist um Pd(II)/Pd(IV)-Mischverbindungen. Die dreiwertige Oxidationsstufe von Palladium wurde etwa in Form von NaPdF4 stabilisiert. Dieser Komplex wird unter hohem Druck synthetisiert. Verbindungen vom Elpasolithtyp A2BPdF6, wobei A und B verschiedene Alkalimetalle sind, werden über Festkörperreaktionen erhalten. Diese Verbindungen weisen eine starke Tendenz zur Disproportionierung in Pd(II)/Pd(IV)-Verbindungen auf. Weiterhin wurde dreiwertiges Palladium als relativ stabiles Lanthan-Palladiumoxid der Zusammensetzung LaPdO3 dargestellt. ⓘ
In neueren Untersuchungen konnte auch sechswertiges Palladium dargestellt werden. Es sind aber auch die Oxidationsstufen 0 [Pd(PR3)4], +1 oder +5 möglich. ⓘ
Verwendung
Feinverteilt ist Palladium ein exzellenter Katalysator zur Beschleunigung von chemischen Reaktionen, insbesondere Hydrierungen und Dehydrierungen (Addition und Eliminierung von Wasserstoff) sowie zum Cracken von Kohlenwasserstoffen. ⓘ
Verwendung als Katalysator
- als Hydrierkatalysator in der Fetthärtung ⓘ
Drei-Wege-Katalysator
Drei-Wege-Katalysatoren eliminieren gleichzeitig Stickoxide, Kohlenstoffmonoxid und Kohlenwasserstoffe aus den Autoabgasen. Die Katalysatoren enthalten oft Platin, Palladium und Rhodium, wobei Palladium die Oxidation von Kohlenstoffmonoxid zu Kohlenstoffdioxid und die Oxidation von Kohlenwasserstoffen zu Kohlenstoffdioxid und Wasser katalysiert. Auch Katalysatoren, die nur Palladium und Rhodium enthalten, sind gebräuchlich. ⓘ
Rosenmund-Kontakt
Beim Rosenmund-Kontakt handelt es sich um einen durch Reduktion von Palladium(II)-chlorid in Gegenwart von BaSO4 hergestellten Katalysator. Er wird in der Rosenmund-Reduktion eingesetzt, einem Hydrierprozess, bei dem ein Acylchlorid zum Aldehyd reduziert wird. Die Reaktion wurde nach Karl Wilhelm Rosenmund benannt, der sie erstmals 1918 berichtete. Bariumsulfat dient als Metallträger und limitiert die Aktivität des Palladiums und verhindert so eine Reduktion über die Stufe des Aldehyds heraus. Durch Zugabe von Katalysatorgiften wie Thioharnstoff kann die Aktivität des Palladiums weiter vermindert werden. ⓘ
Verwendung in der Schmuckindustrie
- Schmuckwaren (vor allem in Ostasien)
- Armbanduhren
- Weißgold (Palladium „entfärbt“ Gold)
- Anlagemünzen, z. B. Palladium Maple Leaf
- Federn für Füllfederhalter
- Feinstfolien. Analog zum Blattgold kann Palladium zu 0,5 µm dünnen Folien ausgewalzt werden (Toleranz ±25 % in der Dicke). ⓘ
Medizinische Verwendung
- Zahnersatz
- Medizinische Instrumente
- Implantatbeschichtungen ⓘ
In vitro konnte die biologische Wirksamkeit des Palladiumkomplexes Bis(diphenylphosphino)-2-ethylpyridylpalladium(II)-chlorid gegen Mycobacterium tuberculosis bei gleichzeitiger Hemmung der HIV-1-Protease nachgewiesen werden. Dies würde die Behandlung der HIV, die oft durch eine Koinfektion mit Mycobacterium tuberculosis erschwert wird, erleichtern. ⓘ
Sonstige Verwendung
- Kontaktwerkstoffe für Relais in Kommunikationsanlagen
- Elektrodenwerkstoffe für Brennstoffzellen und Zündkerzen (Luftfahrt)
- Pd/Ni-Legierungen als Ersatz für Gold in der Elektroindustrie (z. B. bei der galvanischen Beschichtung von Kontakten)
- Nanotechnologie (dient als Katalysator, um z. B. molekulare Verbindungen herzustellen)
- p-Kontakt für galliumnitridbasierte Halbleiterbauelemente
- zum Legieren des Werkstoffes Titan, als Grade 7- und Grade 11-Legierung
- in GASFET-Sensoren als Gate
- In der Leiterplattenbeschichtung: Der Kunststoff, teils auch nur Bohrungen (Bekeimung), wird mit Palladium beschichtet, um darauf eine Nickel- oder Kupferschicht aufzubringen.
- 2011 wurde ein extrem widerstandsfähiges, amorphes Material – sogenanntes Metallisches Glas – mit dem Hauptbestandteil (etwa 40 %) Palladium hergestellt, das die für diese Materialklasse typische Sprödigkeit nicht aufweist.
- Hydrodechlorierung von chlororganischen Verbindungen im Grundwasser ⓘ
Palladiumpreis

Die Bezeichnung für Palladium, das an der Börse gehandelt wird, ist XPD. Die Internationale Wertpapierkennnummer ist ISIN XC0009665529. ⓘ
Sicherheitshinweise
Palladium ist in kompakter Form nicht brennbar, jedoch als Pulver oder Staub leicht entzündlich. Als Löschmittel kann Wasser, Kohlenstoffdioxid oder Schaum verwendet werden. Palladium ist ein Schwermetall, Erkenntnisse über eine akute Toxizität sind jedoch nicht verfügbar. ⓘ
Nachweis
Palladium(II) wird quantitativ durch Dimethylglyoxim aus Lösungen von verdünnten Mineralsäuren bei einem pH-Wert von etwa 2 als Bis(dimethylglyoximato)palladium(II) ausgefällt und löst sich in basischen Lösungen bei einem pH-Wert größer 9. Der Dimethylglyoxim-Nickel-Komplex hat die gleiche Zusammensetzung wie der Palladium-Komplex, jedoch löst sich dieser in Säuren und erlaubt so die die analytische Trennung von Palladium und Nickel. ⓘ
Philatelistisches
Mit dem Erstausgabetag 6. Juni 2019 gab die Deutsche Post AG in der Serie Mikrowelten ein Postwertzeichen im Nennwert von 85 Eurocent heraus. Das Markenbild zeigt eine Mikrofotografie mit 230facher Vergrößerung des kristallinen Palladiums. Der Entwurf stammt von der Grafikerin Andrea Voß-Acker aus Wuppertal. ⓘ





