Destillation

Die Destillation, auch klassische Destillation genannt, ist ein Verfahren zur Abtrennung von Bestandteilen oder Stoffen aus einem Flüssigkeitsgemisch durch selektives Sieden und Kondensation. Die trockene Destillation ist die Erhitzung fester Stoffe zur Erzeugung gasförmiger Produkte (die zu Flüssigkeiten oder Feststoffen kondensieren können). Die trockene Destillation kann mit chemischen Veränderungen wie destruktiver Destillation oder Cracken einhergehen und wird in diesem Artikel nicht behandelt. Die Destillation kann zu einer im Wesentlichen vollständigen Trennung führen (nahezu reine Bestandteile), oder es kann sich um eine partielle Trennung handeln, die die Konzentration ausgewählter Bestandteile im Gemisch erhöht. In beiden Fällen nutzt das Verfahren die Unterschiede in der relativen Flüchtigkeit der Bestandteile des Gemischs aus. In der Industrie ist die Destillation ein praktisch universell einsetzbares Verfahren, bei dem es sich jedoch um ein physikalisches Trennverfahren und nicht um eine chemische Reaktion handelt. ⓘ
Die Destillation findet in vielen Bereichen Anwendung. Ein Beispiel:
- Durch die Destillation von fermentierten Produkten werden destillierte Getränke mit hohem Alkoholgehalt hergestellt oder andere Fermentationsprodukte von kommerziellem Wert abgetrennt.
- Die Destillation ist eine wirksame und traditionelle Methode der Entsalzung.
- In der Erdölindustrie ist die Ölstabilisierung eine Form der partiellen Destillation, bei der der Dampfdruck des Rohöls gesenkt wird, um es für die Lagerung und den Transport sicher zu machen und die Emissionen flüchtiger Kohlenwasserstoffe in die Atmosphäre zu verringern. Im Midstream-Bereich von Erdölraffinerien ist die fraktionierte Destillation eine der wichtigsten Verfahren zur Umwandlung von Rohöl in Kraftstoffe und chemische Grundstoffe.
- Die kryogene Destillation führt zur Trennung von Luft in ihre Bestandteile - insbesondere Sauerstoff, Stickstoff und Argon - für die industrielle Nutzung.
- In der chemischen Industrie werden große Mengen von flüssigen Rohprodukten der chemischen Synthese destilliert, um sie entweder von anderen Produkten, von Verunreinigungen oder von nicht umgesetzten Ausgangsstoffen zu trennen. ⓘ
Eine Anlage für die Destillation, insbesondere von destillierten Getränken, ist eine Brennerei. Die Destillationsanlage selbst ist ein Destillierapparat. ⓘ

1: Heizplatte
2: Rundkolben
3: Kolbenaufsatz/Destillationskolonne
4: Thermometer
5: Kondensator (Gegenstromkühler)
6: Kühlwasserzufuhr
7: Kühlwasserauslass
8: Rundkolben für das Destillat
9: Vakuum-/Gaseinlass
10: Verbindungsstück zur Destillatüberleitung
11: Wärmeregler
12: Regler der Rührgeschwindigkeit
13: Magnetrührer
14: Ölbad, Sandbad, oder Wasserbad
15: Rührmagnet/Siedesteinchen
16: Kühlendes Wasser-/Eisbad ⓘ
Destillation (lateinisch destillatio, von destillare „herabtröpfeln, herabtropfen“, von stilla „Tropfen“) ist ein thermisches Trennverfahren, um verdampfbare Flüssigkeiten zu gewinnen oder Lösungsmittel von schwer verdampfbaren Stoffen abzutrennen und anschließend durch Kondensation aufzufangen. Die Destillation hat gegenüber anderen Trennverfahren den Vorteil, dass in der Regel keine weiteren Stoffe wie Adsorbentien oder Lösungsmittel hinzugefügt werden müssen. ⓘ
Bei der Destillation wird zunächst das Ausgangsgemisch zum Sieden gebracht. Der entstehende Dampf, der sich aus den verschiedenen flüchtigen Komponenten der zu trennenden Lösung zusammensetzt, wird in einem Kondensator durch Abkühlen wieder verflüssigt. Im Labormaßstab wird oft der Liebigkühler verwendet. Im Anschluss wird das flüssige Kondensat aufgefangen. Typische Anwendungen der Destillation sind das Brennen von Alkohol und das Destillieren (die Rektifikation) von Erdöl in der Raffinerie oder auch die Herstellung von destilliertem Wasser. ⓘ
Geschichte

Frühe Belege für die Destillation wurden auf akkadischen Tafeln gefunden, die auf ca. 1200 v. Chr. datiert sind und Parfümiervorgänge beschreiben. Die Tafeln belegen, dass den Babyloniern im alten Mesopotamien eine frühe primitive Form der Destillation bekannt war. Frühe Belege für die Destillation wurden auch im Zusammenhang mit Alchemisten gefunden, die im 1. Jahrhundert n. Chr. in Alexandria im römischen Ägypten arbeiteten. ⓘ
Jahrhundert n. Chr. Destillation wurde auf dem alten indischen Subkontinent praktiziert, was aus gebrannten Tongefäßen und Retorten in Taxila, Shaikhan Dheri, Charsadda in Pakistan und Rang Mahal in Indien aus den ersten Jahrhunderten der gemeinsamen Zeitrechnung hervorgeht. Allchin stellt fest, dass diese Terrakotta-Destilliergefäße "zur Imitation von Bambus hergestellt wurden". Diese "Gandhara-Destillierapparate" waren nur in der Lage, sehr schwachen Schnaps zu produzieren, da es keine effiziente Möglichkeit gab, die Dämpfe bei niedriger Hitze aufzufangen. Destilliertes Wasser wird mindestens seit ca. 200 n. Chr. verwendet, als Alexander von Aphrodisias das Verfahren beschrieb. Die Arbeit an der Destillation anderer Flüssigkeiten wurde im frühen byzantinischen Ägypten unter Zosimus von Panopolis im 3. ⓘ
In China könnte die Destillation während der östlichen Han-Dynastie (1.-2. Jahrhundert n. Chr.) begonnen haben, aber die Destillation von Getränken begann nach archäologischen Erkenntnissen in der Jin- (12.-13. Jahrhundert) und südlichen Song-Dynastie (10.-13. Jahrhundert). ⓘ
Mittelalterliche muslimische Chemiker wie Jābir ibn Ḥayyān (lateinisch: Geber, neuntes Jahrhundert) und Abū Bakr al-Rāzī (lateinisch: Rhazes, ca. 865-925) experimentierten ausgiebig mit der Destillation verschiedener Substanzen. ⓘ
Die Destillation von Wein ist in arabischen Werken belegt, die al-Kindī (ca. 801-873 n. Chr.) und al-Fārābī (ca. 872-950) zugeschrieben werden, sowie im 28. Buch des Kitāb al-Taṣrīf von al-Zahrāwī (lateinisch: Abulcasis, 936-1013) (später ins Lateinische als Liber servatoris übersetzt). Im zwölften Jahrhundert tauchten in einigen lateinischen Werken Rezepte für die Herstellung von aqua ardens ("brennendes Wasser", d. h. Ethanol) durch Destillation von Wein mit Salz auf, und gegen Ende des dreizehnten Jahrhunderts war diese Substanz unter westeuropäischen Chemikern weithin bekannt. In den Werken von Taddeo Alderotti (1223-1296) wird eine Methode zur Konzentrierung von Alkohol beschrieben, die eine wiederholte Destillation in einer wassergekühlten Brennblase vorsah und mit der eine Alkoholreinheit von 90 % erreicht werden konnte. ⓘ
Die fraktionierte Destillation organischer Substanzen spielt in den Werken, die Jābir ibn Ḥayyān zugeschrieben werden, eine wichtige Rolle, so z. B. im Kitāb al-Sabʿīn ("Das Buch der Siebzig"), das von Gerard von Cremona (um 1114-1187) unter dem Titel Liber de septuaginta ins Lateinische übersetzt wurde. Die jabirischen Experimente mit der fraktionierten Destillation von tierischen und pflanzlichen Stoffen und in geringerem Maße auch von mineralischen Stoffen sind das Hauptthema von De anima in arte alkimiae, einem ursprünglich arabischen Werk, das fälschlicherweise Avicenna zugeschrieben wird, ins Lateinische übersetzt wurde und später die wichtigste alchemistische Quelle für Roger Bacon (ca. 1220-1292) sein sollte. ⓘ
Ein Destillierapparat wurde in einer archäologischen Stätte in Qinglong, Provinz Hebei, in China gefunden, der aus dem 12. Destillierte Getränke waren während der Yuan-Dynastie (13. bis 14. Jahrhundert) weit verbreitet. ⓘ
Im Jahr 1500 veröffentlichte der deutsche Alchemist Hieronymus Braunschweig Liber de arte destillandi (Das Buch von der Kunst der Destillation), das erste Buch, das ausschließlich dem Thema Destillation gewidmet war, gefolgt von einer stark erweiterten Version im Jahr 1512. Im Jahr 1651 veröffentlichte John French The Art of Distillation, das erste große englische Kompendium über die Destillationspraxis, von dem jedoch behauptet wird, dass es in weiten Teilen auf Braunschweigs Werk zurückgeht. Dazu gehören auch Diagramme mit Menschen, die eher den industriellen als den handwerklichen Maßstab des Vorgangs zeigen. ⓘ


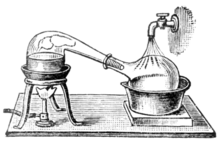


Als sich die Alchemie zu einer chemischen Wissenschaft entwickelte, wurden für die Destillation Gefäße verwendet, die Retorten genannt wurden. Sowohl bei Alembics als auch bei Retorten handelt es sich um Glasgefäße mit langen Hälsen, die schräg nach unten zeigen und als luftgekühlte Kondensatoren dienen, um das Destillat zu kondensieren und zum Auffangen nach unten abtropfen zu lassen. Später wurden Kupfer-Ambrillen erfunden. Die Nietverbindungen wurden oft durch verschiedene Mischungen, z. B. einen Teig aus Roggenmehl, dicht gehalten. Diese Destillierapparate verfügten oft über ein Kühlsystem um den Schnabel herum, beispielsweise mit kaltem Wasser, wodurch die Kondensation des Alkohols effizienter wurde. Diese Destillierapparate wurden Pot Stills genannt. Heute sind die Retorten und Pot Stills in den meisten industriellen Prozessen durch effizientere Destillationsmethoden weitgehend verdrängt worden. Für die Herstellung einiger feiner Alkohole wie Cognac, schottischer Whisky, irischer Whiskey, Tequila, Rum, Cachaça und einige Wodkas wird der Pot Still jedoch nach wie vor häufig verwendet. Pot Stills aus verschiedenen Materialien (Holz, Ton, rostfreier Stahl) werden auch von Schmugglern in verschiedenen Ländern verwendet. Kleine Brennblasen werden auch für die Herstellung von Blütenwasser oder ätherischen Ölen im Haushalt verkauft. ⓘ
Bei den frühen Formen der Destillation handelte es sich um Batch-Verfahren mit einer Verdampfung und einer Kondensation. Die Reinheit wurde durch weitere Destillation des Kondensats verbessert. Größere Mengen wurden durch einfache Wiederholung der Destillation verarbeitet. Es wird berichtet, dass Chemiker bis zu 500 bis 600 Destillationen durchführten, um eine reine Verbindung zu erhalten. ⓘ
Im frühen 19. Jahrhundert wurden die Grundlagen der modernen Techniken, einschließlich Vorwärmung und Rückfluss, entwickelt. 1822 entwickelte Anthony Perrier einen der ersten kontinuierlichen Destillierapparate, und 1826 verbesserte Robert Stein diesen Entwurf, um seinen Patent-Destillierapparat herzustellen. Im Jahr 1830 erhielt Aeneas Coffey ein Patent für eine weitere Verbesserung der Konstruktion. Coffeys kontinuierlicher Destillierapparat kann als Urform der modernen petrochemischen Anlagen betrachtet werden. Der französische Ingenieur Armand Savalle entwickelte seinen Dampfregler um 1846. Im Jahr 1877 erhielt Ernest Solvay ein US-Patent für eine Bodenkolonne zur Ammoniakdestillation, und im selben Jahr und in den Folgejahren gab es weitere Entwicklungen in diesem Bereich für Öle und Spirituosen. ⓘ
Mit dem Aufkommen des Chemieingenieurwesens als Disziplin Ende des 19. Jahrhunderts konnten eher wissenschaftliche als empirische Methoden angewandt werden. Die sich zu Beginn des 20. Jahrhunderts entwickelnde Erdölindustrie gab den Anstoß zur Entwicklung genauer Auslegungsmethoden, wie der McCabe-Thiele-Methode von Ernest Thiele und der Fenske-Gleichung. Die erste industrielle Anlage in den Vereinigten Staaten, die Destillation als Mittel zur Meerwasserentsalzung einsetzte, wurde 1961 in Freeport, Texas, eröffnet, in der Hoffnung, die Wasserversorgung der Region zu sichern. Die Verfügbarkeit leistungsfähiger Computer ermöglichte direkte Computersimulationen von Destillationskolonnen. ⓘ

Die Destillation von Pech und Teer zur Abdichtung von Schiffen, als Klebemittel und auch als Heilmittel ist seit der Jungsteinzeit bekannt; sie wurde mit einfachsten Mitteln bewerkstelligt. In der Antike wurden vor allem ätherische Öle, als Riech- und Duftstoffe, destilliert. Die ältesten bei archäologischen Ausgrabungen aufgefundenen Darstellungen von Destilliergeräten stammen aus Mesopotamien, dem heutigen Irak, und werden auf ein Alter von über 5500 Jahren geschätzt. Diese ersten Destillationsvorrichtungen bestanden aus einem Gefäß mit einem Deckel, an dem sich beim Erhitzen das Destillat niederschlug. Damit diese Flüssigkeit nicht wieder in das Gefäß zurück tropfte, verwendete man im Deckel Schwämme oder Wollbüschel, um die Flüssigkeit aufzusaugen. Diese wurden dann einfach regelmäßig ausgepresst, um das Destillat zu erhalten. ⓘ
Die Destillation wurde von dem Chemiker Abu Musa Dschābir ibn Hayyān um 800 n. Chr. weiter verbessert. Auch der persische Wissenschaftler und Arzt ar-Razi („Rhases“, 865–925) schrieb seine Kenntnisse in einer Reihe umfangreicher Schriften nieder. Sein wichtigstes Werk ist das Kitab sirr al-asrar, das „Buch des Geheimnisses der Geheimnisse“. Hier beschreibt er die Destillation des naft, des rohen Erdöls, und erläutert hierbei eine einfache Art des „Crack-Verfahrens“ zum Zwecke der Gewinnung niedrig siedender Produkte wie Bitumen und des sogenannten Ziegelöles (oleum laterinum). Mit der Erfindung des Destillierhelms (genannt auch Alembik) wurde auch die Destillation von Alkohol möglich. ⓘ
Anwendungen
Die Anwendungen der Destillation lassen sich grob in vier Gruppen einteilen: Labormaßstab, industrielle Destillation, Destillation von Kräutern für die Parfümerie und Medizin (Kräuterdestillat) und Lebensmittelverarbeitung. Die beiden letztgenannten Gruppen unterscheiden sich deutlich von den beiden erstgenannten, da die Destillation nicht als echte Reinigungsmethode eingesetzt wird, sondern eher dazu dient, bei der Verarbeitung von Getränken und Kräutern alle flüchtigen Bestandteile aus den Ausgangsstoffen in das Destillat zu übertragen. ⓘ
Der Hauptunterschied zwischen der Destillation im Labormaßstab und der industriellen Destillation besteht darin, dass die Destillation im Labormaßstab häufig in Chargen durchgeführt wird, während die industrielle Destillation häufig kontinuierlich erfolgt. Bei der Chargendestillation ändert sich die Zusammensetzung des Ausgangsmaterials, der Dämpfe der destillierenden Verbindungen und des Destillats während der Destillation. Bei der Batch-Destillation wird eine Brennblase mit einer Charge des Ausgangsmaterials beschickt, die dann in die einzelnen Fraktionen aufgeteilt wird, die nacheinander von der flüchtigsten zur weniger flüchtigen Fraktion gesammelt werden, wobei der Bodensatz - die verbleibende am wenigsten oder nicht flüchtige Fraktion - am Ende entfernt wird. Der Destillierapparat kann dann wieder befüllt und der Prozess wiederholt werden. ⓘ
Bei der kontinuierlichen Destillation werden die Ausgangsstoffe, die Dämpfe und das Destillat auf einer konstanten Zusammensetzung gehalten, indem die Ausgangsstoffe sorgfältig nachgefüllt und Fraktionen sowohl aus den Dämpfen als auch aus der Flüssigkeit im System entfernt werden. Dies führt zu einer genaueren Kontrolle des Trennungsprozesses. ⓘ
Idealisiertes Modell
Der Siedepunkt einer Flüssigkeit ist die Temperatur, bei der der Dampfdruck der Flüssigkeit gleich dem Druck um die Flüssigkeit herum ist, so dass sich Blasen bilden können, ohne zerdrückt zu werden. Ein Sonderfall ist der normale Siedepunkt, bei dem der Dampfdruck der Flüssigkeit gleich dem atmosphärischen Umgebungsdruck ist. ⓘ
Es ist ein Irrglaube, dass in einem Flüssigkeitsgemisch bei einem gegebenen Druck jeder Bestandteil an dem dem gegebenen Druck entsprechenden Siedepunkt siedet, so dass sich die Dämpfe der einzelnen Bestandteile getrennt und rein sammeln können. Dies ist jedoch nicht der Fall, auch nicht in einem idealisierten System. Idealisierte Destillationsmodelle beruhen im Wesentlichen auf dem Raoult'schen Gesetz und dem Dalton'schen Gesetz und gehen davon aus, dass Dampf-Flüssigkeits-Gleichgewichte erreicht werden. ⓘ
Das Raoultsche Gesetz besagt, dass der Dampfdruck einer Lösung abhängig ist von 1) dem Dampfdruck jeder chemischen Komponente in der Lösung und 2) dem Anteil jeder Komponente an der Lösung, auch bekannt als Molanteil. Dieses Gesetz gilt für ideale Lösungen oder für Lösungen, die aus verschiedenen Bestandteilen bestehen, deren molekulare Wechselwirkungen jedoch gleich oder sehr ähnlich sind wie bei reinen Lösungen. ⓘ
Das Daltonsche Gesetz besagt, dass der Gesamtdruck die Summe der Partialdrücke der einzelnen Komponenten im Gemisch ist. Wenn eine Mehrkomponentenflüssigkeit erhitzt wird, steigt der Dampfdruck der einzelnen Komponenten, wodurch der Gesamtdampfdruck ansteigt. Wenn der Gesamtdampfdruck den die Flüssigkeit umgebenden Druck erreicht, kommt es zum Sieden und die Flüssigkeit wird in der gesamten Masse der Flüssigkeit zu Gas. Ein Gemisch mit einer bestimmten Zusammensetzung hat einen Siedepunkt bei einem bestimmten Druck, wenn die Komponenten ineinander löslich sind. Ein Gemisch mit konstanter Zusammensetzung hat nicht mehrere Siedepunkte. ⓘ
Ein Siedepunkt hat zur Folge, dass leichtere Bestandteile nie eindeutig "zuerst sieden". Am Siedepunkt sieden alle flüchtigen Bestandteile, aber der prozentuale Anteil eines Bestandteils am Dampf entspricht seinem prozentualen Anteil am Gesamtdampfdruck. Leichtere Bestandteile haben einen höheren Partialdruck und sind daher im Dampf konzentriert, aber schwerere flüchtige Bestandteile haben ebenfalls einen (geringeren) Partialdruck und verdampfen zwangsläufig auch, wenn auch in geringerer Konzentration im Dampf. Bei der Chargendestillation und der Fraktionierung wird die Zusammensetzung des Gemischs variiert. Bei der Chargendestillation verdampft die Charge, wodurch sich ihre Zusammensetzung ändert; bei der Fraktionierung enthält die Flüssigkeit in der Fraktionierungskolonne mehr Licht und siedet bei niedrigeren Temperaturen. Ausgehend von einem gegebenen Gemisch scheint es daher einen Siedebereich und keinen Siedepunkt zu haben, obwohl sich seine Zusammensetzung ändert: Jedes Zwischengemisch hat seinen eigenen, einzigartigen Siedepunkt. ⓘ
Das idealisierte Modell ist genau, wenn es sich um chemisch ähnliche Flüssigkeiten wie Benzol und Toluol handelt. In anderen Fällen werden starke Abweichungen vom Raoult'schen Gesetz und vom Dalton'schen Gesetz beobachtet, am bekanntesten bei der Mischung von Ethanol und Wasser. Wenn diese Verbindungen zusammen erhitzt werden, bilden sie ein Azeotrop, d. h. die Dampfphase und die flüssige Phase haben die gleiche Zusammensetzung. Obwohl es Berechnungsmethoden gibt, mit denen das Verhalten eines Gemischs aus beliebigen Komponenten abgeschätzt werden kann, ist die einzige Möglichkeit, genaue Daten zum Dampf-Flüssigkeits-Gleichgewicht zu erhalten, die Messung. ⓘ
Es ist nicht möglich, ein Gemisch von Bestandteilen durch Destillation vollständig zu reinigen, da dies voraussetzen würde, dass jeder Bestandteil des Gemischs einen Partialdruck von Null aufweist. Wenn hochreine Produkte das Ziel sind, muss eine weitere chemische Trennung vorgenommen werden. Wenn ein binäres Gemisch verdampft wird und die andere Komponente, z. B. ein Salz, für praktische Zwecke einen Partialdruck von Null aufweist, ist das Verfahren einfacher. ⓘ
Batch- oder Differenzialdestillation

Erhitzt man ein ideales Gemisch aus zwei flüchtigen Stoffen, A und B, wobei A die höhere Flüchtigkeit bzw. den niedrigeren Siedepunkt hat, in einem Batch-Destillationsapparat (z. B. in dem in der Abbildung dargestellten Apparat), bis das Gemisch siedet, so entsteht über der Flüssigkeit ein Dampf, der ein Gemisch aus A und B enthält. Das Verhältnis in der Flüssigkeit wird dadurch bestimmt, wie die ursprüngliche Mischung hergestellt wurde, während das Verhältnis im Dampf mit der flüchtigeren Verbindung A angereichert ist (aufgrund des Raoultschen Gesetzes, siehe oben). Der Dampf durchläuft den Kondensator und wird aus dem System entfernt. Dies wiederum bedeutet, dass das Verhältnis der Verbindungen in der verbleibenden Flüssigkeit nun anders ist als das ursprüngliche Verhältnis (d. h., dass B stärker angereichert ist als in der Ausgangsflüssigkeit). ⓘ
Die Folge ist, dass sich das Verhältnis im flüssigen Gemisch ändert und reicher an der Komponente B wird. Dadurch steigt der Siedepunkt des Gemischs, was zu einem Anstieg der Temperatur im Dampf führt, was wiederum ein sich änderndes Verhältnis von A : B in der Gasphase zur Folge hat (mit fortschreitender Destillation steigt der Anteil von B in der Gasphase). Dies führt zu einem sich langsam ändernden Verhältnis von A : B im Destillat. ⓘ
Ist der Dampfdruckunterschied zwischen den beiden Komponenten A und B groß - im Allgemeinen ausgedrückt durch den Unterschied der Siedepunkte -, so ist das Gemisch zu Beginn der Destillation stark mit der Komponente A angereichert, und wenn die Komponente A abdestilliert ist, ist die siedende Flüssigkeit mit der Komponente B angereichert. ⓘ
Kontinuierliche Destillation
Die kontinuierliche Destillation ist eine fortlaufende Destillation, bei der ein Flüssigkeitsgemisch kontinuierlich (ohne Unterbrechung) in den Prozess eingespeist wird und die abgetrennten Fraktionen kontinuierlich mit den im Laufe des Prozesses auftretenden Ausgangsströmen entfernt werden. Bei der kontinuierlichen Destillation werden mindestens zwei Ausgangsfraktionen erzeugt, darunter mindestens eine flüchtige Destillatfraktion, die gesiedet und separat als Dampf aufgefangen und dann zu einer Flüssigkeit kondensiert wurde. Es gibt immer eine Bodenfraktion (oder Rückstandsfraktion), bei der es sich um den am wenigsten flüchtigen Rückstand handelt, der nicht separat als kondensierter Dampf aufgefangen wurde. ⓘ
Die kontinuierliche Destillation unterscheidet sich von der Chargendestillation insofern, als sich die Konzentrationen im Laufe der Zeit nicht ändern sollten. Die kontinuierliche Destillation kann für eine beliebige Zeitspanne in einem stationären Zustand betrieben werden. Die wichtigsten Variablen, die sich bei der kontinuierlichen Destillation auf die Reinheit der Produkte auswirken, sind für jedes Ausgangsmaterial mit einer bestimmten Zusammensetzung das Rückflussverhältnis und die Anzahl der theoretischen Gleichgewichtsstufen, die in der Praxis durch die Anzahl der Böden oder die Höhe der Packung bestimmt wird. Der Rückfluss ist ein Strom vom Kondensator zurück in die Kolonne, der einen Kreislauf erzeugt, der eine bessere Trennung bei einer bestimmten Anzahl von Böden ermöglicht. Gleichgewichtsstufen sind ideale Schritte, bei denen die Zusammensetzungen ein Dampf-Flüssigkeits-Gleichgewicht erreichen, wodurch der Trennprozess wiederholt wird und eine bessere Trennung bei einem bestimmten Rückflussverhältnis möglich ist. Eine Säule mit einem hohen Rückflussverhältnis kann weniger Stufen haben, aber sie refluxiert eine große Menge an Flüssigkeit, was zu einer breiten Säule mit einem großen Holdup führt. Umgekehrt muss eine Säule mit einem niedrigen Rückflussverhältnis eine große Anzahl von Stufen aufweisen, was eine höhere Säule erfordert. ⓘ
Allgemeine Verbesserungen
Sowohl Batch- als auch kontinuierliche Destillationen können durch den Einsatz einer Fraktionierkolonne auf dem Destillationskolben verbessert werden. Die Kolonne verbessert die Trennung, indem sie eine größere Oberfläche für den Kontakt zwischen Dampf und Kondensat bietet. Dies trägt dazu bei, dass sie so lange wie möglich im Gleichgewicht bleiben. Die Säule kann sogar aus kleinen Teilsystemen ("Böden" oder "Schalen") bestehen, die alle ein angereichertes, siedendes Flüssigkeitsgemisch enthalten, wobei jedes sein eigenes Dampf-Flüssigkeits-Gleichgewicht hat. ⓘ
Es gibt Unterschiede zwischen Fraktionierkolonnen im Labormaßstab und im industriellen Maßstab, aber die Prinzipien sind die gleichen. Beispiele für Fraktionierkolonnen im Labormaßstab (mit steigender Effizienz) sind
- Luftkondensator
- Vigreux-Säule (normalerweise nur im Labormaßstab)
- Gepackte Kolonne (gepackt mit Glasperlen, Metallstücken oder anderem chemisch inerten Material)
- Spinning-Band-Destillationssystem. ⓘ
Laborverfahren
Destillationen im Labormaßstab werden fast ausschließlich als Batch-Destillationen durchgeführt. Das für die Destillation verwendete Gerät, das manchmal auch als Destillierapparat bezeichnet wird, besteht mindestens aus einem Reboiler oder Topf, in dem das Ausgangsmaterial erhitzt wird, einem Kondensator, in dem der erhitzte Dampf wieder in den flüssigen Zustand abgekühlt wird, und einem Sammelbehälter, in dem die konzentrierte oder gereinigte Flüssigkeit, das so genannte Destillat, aufgefangen wird. Für die Destillation gibt es mehrere Techniken im Labormaßstab (siehe auch Destillationsarten). ⓘ
Ein vollständig abgedichteter Destillationsapparat könnte extremen und schnell schwankenden Innendrücken ausgesetzt sein, die ihn an den Verbindungsstellen zum Bersten bringen könnten. Daher wird in der Regel ein Weg offen gelassen (z. B. am Aufnahmekolben), damit sich der Innendruck an den Atmosphärendruck angleichen kann. Alternativ kann eine Vakuumpumpe verwendet werden, um die Apparatur auf einem niedrigeren Druck als dem Atmosphärendruck zu halten. Handelt es sich um luft- oder feuchtigkeitsempfindliche Stoffe, kann die Verbindung zur Atmosphäre durch ein oder mehrere Trockenrohre hergestellt werden, die mit Materialien gefüllt sind, welche die unerwünschten Luftbestandteile abfangen, oder durch Bubbler, die eine bewegliche Flüssigkeitsbarriere bilden. Schließlich kann das Eindringen unerwünschter Luftbestandteile verhindert werden, indem ein geringer, aber gleichmäßiger Strom eines geeigneten Inertgases, z. B. Stickstoff, in die Apparatur gepumpt wird. ⓘ
Einfache Destillation

Bei der einfachen Destillation wird der Dampf sofort in einen Kondensator geleitet. Folglich ist das Destillat nicht rein, sondern seine Zusammensetzung ist identisch mit der Zusammensetzung der Dämpfe bei der gegebenen Temperatur und dem gegebenen Druck. Diese Konzentration folgt dem Raoultschen Gesetz. ⓘ
Folglich ist die einfache Destillation nur dann effektiv, wenn die Siedepunkte der Flüssigkeiten stark voneinander abweichen (Faustregel: 25 °C) oder wenn Flüssigkeiten von nicht flüchtigen Feststoffen oder Ölen getrennt werden sollen. In diesen Fällen sind die Dampfdrücke der Komponenten in der Regel so unterschiedlich, dass das Destillat für den vorgesehenen Zweck ausreichend rein sein kann. ⓘ
Rechts ist die schematische Darstellung eines einfachen Destillationsvorgangs zu sehen. Die Ausgangsflüssigkeit 15 im Siedekolben 2 wird durch eine Kombination aus Heizplatte und Magnetrührer 13 über ein Silikonölbad (orange, 14) erhitzt. Der Dampf fließt durch eine kurze Vigreux-Kolonne 3, dann durch einen Liebig-Kondensator 5 und wird durch Wasser (blau) gekühlt, das durch die Anschlüsse 6 und 7 zirkuliert. Die kondensierte Flüssigkeit tropft in den Auffangkolben 8, der sich in einem Kühlbad (blau, 16) befindet. Der Adapter 10 hat einen Anschluss 9, an den eine Vakuumpumpe angeschlossen werden kann. Die Komponenten sind durch Schliffverbindungen miteinander verbunden. ⓘ
Fraktionierte Destillation
In vielen Fällen werden die Siedepunkte der Komponenten im Gemisch so nahe beieinander liegen, dass das Raoultsche Gesetz berücksichtigt werden muss. Daher muss die fraktionierte Destillation eingesetzt werden, um die Komponenten durch wiederholte Verdampfungs-Kondensations-Zyklen in einer gepackten Fraktionierkolonne zu trennen. Diese Trennung durch aufeinanderfolgende Destillationen wird auch als Rektifikation bezeichnet. ⓘ
Wenn die zu reinigende Lösung erhitzt wird, steigen ihre Dämpfe in die Fraktionierkolonne auf. Beim Aufsteigen kühlen sie ab und kondensieren an den Wänden des Kondensators und an den Oberflächen des Füllkörpers. Hier wird das Kondensat durch die aufsteigenden heißen Dämpfe weiter erwärmt und verdampft erneut. Die Zusammensetzung der neuen Dämpfe wird jedoch wieder durch das Raoultsche Gesetz bestimmt. Jeder Verdampfungs-Kondensations-Zyklus (theoretische Platte genannt) ergibt eine reinere Lösung der flüchtigeren Komponente. In der Realität findet jeder Zyklus bei einer bestimmten Temperatur nicht an genau derselben Stelle in der Fraktionierkolonne statt; die theoretische Platte ist also eher ein Konzept als eine genaue Beschreibung. ⓘ
Mehr theoretische Böden führen zu besseren Trennungen. Bei einem Spinnband-Destillationssystem wird ein Spinnband aus Teflon oder Metall verwendet, um die aufsteigenden Dämpfe in engen Kontakt mit dem absteigenden Kondensat zu bringen, wodurch die Anzahl der theoretischen Böden erhöht wird. ⓘ
Dampfdestillation
Wie die Vakuumdestillation ist auch die Wasserdampfdestillation ein Verfahren zur Destillation hitzeempfindlicher Verbindungen. Die Temperatur des Dampfes ist leichter zu kontrollieren als die Oberfläche eines Heizelements und ermöglicht eine hohe Wärmeübertragungsrate ohne Erhitzung auf eine sehr hohe Temperatur. Bei diesem Verfahren wird Dampf durch eine erhitzte Rohstoffmischung geblasen. Nach dem Raoultschen Gesetz verdampft ein Teil der Zielverbindung (entsprechend ihrem Partialdruck). Das Dampfgemisch wird abgekühlt und kondensiert, wobei in der Regel eine Ölschicht und eine Wasserschicht entstehen. ⓘ
Bei der Wasserdampfdestillation von verschiedenen aromatischen Kräutern und Blumen können zwei Produkte entstehen: ein ätherisches Öl und ein wässriges Kräuterdestillat. Die ätherischen Öle werden häufig in der Parfümerie und Aromatherapie verwendet, während die wässrigen Destillate zahlreiche Anwendungen in der Aromatherapie, Lebensmittelverarbeitung und Hautpflege finden. ⓘ


- Rührstab/Anti-Bumping-Granulat
- Destillationstopf
- Fraktionierkolonne
- Thermometer/Siedepunkttemperatur
- Teflon-Hahn 1
- Kalter Finger
- Kühlwasser raus
- Kühlwasser ein
- Teflonhahn 2
- Vakuum-/Gaseinlass
- Teflon-Hahn 3
- Destillationsbehälter ⓘ
Vakuum-Destillation
Einige Verbindungen haben sehr hohe Siedepunkte. Um solche Verbindungen zu sieden, ist es oft besser, den Druck zu senken, bei dem solche Verbindungen gesiedet werden, anstatt die Temperatur zu erhöhen. Sobald der Druck auf den Dampfdruck der Verbindung (bei der gegebenen Temperatur) gesenkt ist, können das Sieden und der Rest des Destillationsprozesses beginnen. Diese Technik wird als Vakuumdestillation bezeichnet und ist im Labor häufig in Form des Rotationsverdampfers anzutreffen. ⓘ
Diese Technik ist auch sehr nützlich für Verbindungen, die bei Atmosphärendruck über ihre Zersetzungstemperatur hinaus sieden und daher bei jedem Versuch, sie unter Atmosphärendruck zu sieden, zersetzt würden. ⓘ
Kurzweg- und Molekulardestillation
Die Molekulardestillation ist eine Vakuumdestillation unterhalb eines Drucks von 0,01 Torr. 0,01 Torr liegt eine Größenordnung über dem Hochvakuum, in dem sich die Flüssigkeiten im Bereich des freien Molekularflusses befinden, d. h. die mittlere freie Weglänge der Moleküle ist vergleichbar mit der Größe der Anlage. Die Gasphase übt keinen nennenswerten Druck mehr auf die zu verdampfende Substanz aus, und folglich hängt die Verdampfungsrate nicht mehr vom Druck ab. Da die Kontinuumsannahmen der Fluiddynamik nicht mehr gelten, wird der Massentransport durch die Molekulardynamik und nicht durch die Fluiddynamik bestimmt. Daher ist ein kurzer Weg zwischen der heißen Oberfläche und der kalten Oberfläche erforderlich, in der Regel durch Aufhängen einer mit einem Futterfilm bedeckten heißen Platte neben einer kalten Platte mit einer Sichtlinie dazwischen. Die Molekulardestillation wird industriell zur Reinigung von Ölen eingesetzt. ⓘ

- Destillationstopf mit Rührstab/Anti-Bumping-Granulat
- Kalter Finger - gebogen, um das Kondensat
- Kühlwasser raus
- Kühlwasser einzuleiten
- Vakuum-/Gaseinlass
- Destillatkolben/Destillat. ⓘ
Die Kurzwegdestillation ist eine Destillationstechnik, bei der das Destillat eine kurze Strecke zurücklegt, oft nur wenige Zentimeter, und die normalerweise bei reduziertem Druck durchgeführt wird. Ein klassisches Beispiel wäre eine Destillation, bei der das Destillat von einem Glaskolben zum anderen geleitet wird, ohne dass ein Kondensator die beiden Kammern trennt. Diese Technik wird häufig für Verbindungen verwendet, die bei hohen Temperaturen instabil sind, oder um kleine Mengen einer Verbindung zu reinigen. Der Vorteil besteht darin, dass die Heiztemperatur (bei vermindertem Druck) wesentlich niedriger sein kann als der Siedepunkt der Flüssigkeit bei Normaldruck, und dass das Destillat nur einen kurzen Weg zurücklegen muss, bevor es kondensiert. Ein kurzer Weg sorgt dafür, dass wenig Substanz an den Seiten der Apparatur verloren geht. Die Kugelrohrapparatur ist eine Art Kurzweg-Destillationsverfahren, das häufig mehrere Kammern zum Auffangen der Destillatfraktionen enthält. ⓘ
Luftempfindliche Vakuumdestillation
Einige Verbindungen haben einen hohen Siedepunkt und sind zudem luftempfindlich. Ein einfaches Vakuumdestillationssystem wie oben beschrieben kann verwendet werden, wobei das Vakuum nach Abschluss der Destillation durch ein Inertgas ersetzt wird. Dieses System ist jedoch weniger zufriedenstellend, wenn man Fraktionen unter vermindertem Druck sammeln möchte. Zu diesem Zweck kann ein "Kuh"- oder "Schwein"-Adapter am Ende des Kondensators angebracht werden, oder für bessere Ergebnisse oder für sehr luftempfindliche Verbindungen kann eine Perkin-Dreieck-Apparatur verwendet werden. ⓘ
Die Perkin-Dreiecksapparatur verfügt über eine Reihe von Glas- oder Teflonhähnen, die es ermöglichen, die Fraktionen vom Rest der Destillationsanlage zu isolieren, ohne dass der Hauptteil der Destillation vom Vakuum oder der Wärmequelle abgetrennt wird, und kann daher im Rückflusszustand verbleiben. Das Vakuum über der Probe wird dann durch ein inertes Gas (z. B. Stickstoff oder Argon) ersetzt und kann dann verschlossen und entfernt werden. Anschließend kann ein neues Sammelgefäß in das System eingebracht, evakuiert und über die Hähne wieder mit dem Destillationssystem verbunden werden, um eine zweite Fraktion zu sammeln, usw., bis alle Fraktionen gesammelt sind. ⓘ
Zonendestillation
Die Zonendestillation ist ein Destillationsprozess in einem Container gestreckter Form mit partieller Verschmelzung des raffinierten Stoffes in einer sich bewegenden flüssigen Zone und mit einer Kondensation des Dampfes in die feste Phase im Zuge des Ausgangs des Kondensats zum kalten Gebiet. Der Prozess ist theoretisch bearbeitet. ⓘ
Bei der Bewegung des Zonenerhitzers den Container entlang von oben nach unten lässt sich ein festes Kondensat im Container mit der gleichmäßigen Verteilung der Beimischungen formen und der reinste Teil des Kondensats kann als Produkt ausgegrenzt werden. Der Prozess kann mehrmals wiederholt werden, wofür das früher erhaltene Kondensat (ohne Umwälzung) in den unteren Teil des Containers an den Ort des raffinierten Stoffes versetzt werden soll. Die ungleichmäßige Verteilung der Beimischungen im Kondensat (d. h. die Reinigungswirkung) steigt mit der Anzahl der Wiederholungen des Prozesses. ⓘ
Die Zonendestillation ist ein destillatives Analogon der Zonenumkristallisation. Die Verteilung der Beimischungen im Kondensat wird durch bekannte Gleichungen der Zonenumkristallisation mit verschiedener Anzahl der Durchläufe der Zone beschrieben – bei der Ersetzung des Verteilungskoeffizienten k für die Kristallisation durch den Separationskoeffizienten α für die Destillation. ⓘ
Vakuumdestillation im geschlossenen System (Kryodestillation)
Nicht kondensierbares Gas kann durch den Dampf eines relativ flüchtigen Co-Lösungsmittels, das beim ersten Abpumpen spontan verdampft, aus der Apparatur verdrängt werden; dies kann mit einer normalen Öl- oder Membranpumpe erreicht werden. ⓘ
Andere Arten
- Bei der reaktiven Destillation wird das Reaktionsgefäß als Destillationsapparat verwendet. Bei diesem Verfahren ist das Produkt in der Regel deutlich niedriger siedend als die Reaktanden. Während sich das Produkt aus den Reaktanten bildet, wird es verdampft und aus dem Reaktionsgemisch entfernt. Diese Technik ist ein Beispiel für einen kontinuierlichen Prozess im Gegensatz zu einem Batch-Prozess; zu den Vorteilen gehören weniger Stillstandszeiten, um das Reaktionsgefäß mit Ausgangsmaterial zu füllen, und weniger Aufarbeitung. Die Destillation "über einen Reaktanten" könnte als reaktive Destillation eingestuft werden. Sie wird in der Regel eingesetzt, um flüchtige Verunreinigungen aus dem Destillationsansatz zu entfernen. So kann beispielsweise etwas Kalk zugesetzt werden, um Kohlendioxid aus dem Wasser zu entfernen, gefolgt von einer zweiten Destillation mit etwas Schwefelsäure, um Spuren von Ammoniak zu entfernen.
- Bei der katalytischen Destillation werden die Reaktanten während der Destillation katalysiert, um die Produkte kontinuierlich von den Reaktanten zu trennen. Diese Methode wird angewandt, um Gleichgewichtsreaktionen zum Abschluss zu bringen.
- Pervaporation ist ein Verfahren zur Trennung von Flüssigkeitsgemischen durch partielle Verdampfung durch eine nicht poröse Membran.
- Unter Extraktivdestillation versteht man die Destillation in Gegenwart eines mischbaren, hochsiedenden, relativ nicht flüchtigen Bestandteils, des Lösungsmittels, das mit den anderen Bestandteilen der Mischung kein Azeotrop bildet.
- Die Entspannungsverdampfung (oder partielle Verdampfung) ist die partielle Verdampfung, die auftritt, wenn ein gesättigter Flüssigkeitsstrom durch ein Drosselventil oder eine andere Drosselvorrichtung eine Druckreduzierung erfährt. Dieses Verfahren ist eines der einfachsten Verfahren, da es einer Destillation mit nur einer Gleichgewichtsstufe entspricht.
- Die Kodestillation ist eine Destillation, die mit Gemischen durchgeführt wird, bei denen die beiden Verbindungen nicht mischbar sind. Im Labor wird zu diesem Zweck der Dean-Stark-Apparat verwendet, um Wasser aus Syntheseprodukten zu entfernen. Ein weiteres Beispiel ist der Bleidner-Apparat mit zwei rückfließenden Lösungsmitteln.
- Die Membrandestillation ist eine Art der Destillation, bei der die Dämpfe eines zu trennenden Gemisches durch eine Membran geleitet werden, die selektiv eine Komponente des Gemisches durchlässt. Der Dampfdruckunterschied ist die treibende Kraft. Sie kann bei der Meerwasserentsalzung und bei der Entfernung von organischen und anorganischen Bestandteilen eingesetzt werden. ⓘ
Der Einheitsprozess der Verdampfung kann auch als "Destillation" bezeichnet werden:
- Bei der Rotationsverdampfung wird ein Vakuumdestillationsapparat verwendet, um Lösungsmittel aus einer Probe zu entfernen. In der Regel wird das Vakuum durch einen Wasserabsauger oder eine Membranpumpe erzeugt.
- In einer Kugelrohrapparatur wird typischerweise eine Kurzweg-Destillationsapparatur verwendet (im Allgemeinen in Kombination mit einem (Hoch-)Vakuum), um hochsiedende (> 300 °C) Verbindungen zu destillieren. Die Apparatur besteht aus einem Ofen, in den die zu destillierende Verbindung eingebracht wird, einem außerhalb des Ofens befindlichen Aufnahmeteil und einer Vorrichtung zum Drehen der Probe. Das Vakuum wird normalerweise mit einer Hochvakuumpumpe erzeugt. ⓘ
Andere Verwendungen:
- Bei der trockenen oder destruktiven Destillation handelt es sich trotz des Namens nicht um eine echte Destillation, sondern um eine als Pyrolyse bekannte chemische Reaktion, bei der feste Stoffe in einer inerten oder reduzierenden Atmosphäre erhitzt werden und flüchtige Fraktionen, die hochsiedende Flüssigkeiten und Pyrolyseprodukte enthalten, aufgefangen werden. Die destruktive Destillation von Holz zur Gewinnung von Methanol ist der Grund für seinen allgemeinen Namen - Holzalkohol.
- Die Gefrierdestillation ist eine analoge Reinigungsmethode, bei der das Gefrieren anstelle der Verdampfung verwendet wird. Es handelt sich dabei nicht um eine echte Destillation, sondern um eine Umkristallisation, bei der das Produkt die Mutterlauge ist und keine der Destillation gleichwertigen Produkte erzeugt werden. Dieses Verfahren wird bei der Herstellung von Eisbier und Eiswein eingesetzt, um den Ethanol- bzw. Zuckergehalt zu erhöhen. Es wird auch zur Herstellung von Apfelschnaps verwendet. Anders als bei der Destillation werden bei der Gefrierdestillation die giftigen Kongenere nicht entfernt, sondern konzentriert. Auch bei der Destillation durch Verdampfung können diese getrennt werden, da sie unterschiedliche Siedepunkte haben.
- Destillation durch Filtration: In der frühen Alchemie und Chemie, auch bekannt als Naturphilosophie, war eine Form der "Destillation" durch Kapillarfiltration damals als eine Form der Destillation bekannt. Dabei wurde eine Reihe von Bechern oder Schalen auf eine gestufte Halterung mit einem "Docht" aus Baumwolle oder filzähnlichem Material gesetzt, der mit Wasser oder einer klaren Flüssigkeit benetzt wurde, wobei jede Stufe durch das benetzte Tuch durch Kapillarwirkung in den nachfolgenden Stufen heruntertropfte und eine "Reinigung" der Flüssigkeit bewirkte, wobei feste Stoffe in den oberen Schalen zurückblieben und das nachfolgende Produkt durch Kapillarwirkung durch das befeuchtete Tuch gereinigt wurde. Dies wurde von den Anwendern der Methode "Destillation" durch Filtration genannt. ⓘ
Azeotropes Verfahren
Die Wechselwirkungen zwischen den Bestandteilen der Lösung führen zu einzigartigen Eigenschaften der Lösung, da die meisten Prozesse nicht-ideale Mischungen beinhalten, für die das Raoultsche Gesetz nicht gilt. Solche Wechselwirkungen können zu einem konstant siedenden Azeotrop führen, das sich so verhält, als wäre es eine reine Verbindung (d. h. es siedet bei einer einzigen Temperatur statt bei einem Bereich). Bei einem Azeotrop enthält die Lösung die jeweilige Komponente im gleichen Verhältnis wie der Dampf, so dass die Verdampfung die Reinheit nicht verändert und die Destillation keine Trennung bewirkt. Zum Beispiel bilden Ethylalkohol und Wasser bei 78,1 °C ein Azeotrop von 95,6 %. ⓘ
Wird das Azeotrop für die Verwendung als nicht ausreichend rein angesehen, gibt es einige Techniken, um das Azeotrop aufzubrechen und ein reines Destillat zu erhalten. Diese Techniken sind als azeotrope Destillation bekannt. Einige Verfahren erreichen dies durch "Springen" über die azeotrope Zusammensetzung (durch Zugabe einer anderen Komponente, um ein neues Azeotrop zu erzeugen, oder durch Veränderung des Drucks). Bei anderen Verfahren wird die Verunreinigung auf chemischem oder physikalischem Wege entfernt oder sequestriert. Um beispielsweise Ethanol auf über 95 % zu reinigen, kann ein Trocknungsmittel (oder Trockenmittel wie Kaliumcarbonat) hinzugefügt werden, um das lösliche Wasser in unlösliches Kristallwasser umzuwandeln. Auch Molekularsiebe werden häufig zu diesem Zweck eingesetzt. ⓘ
Unmischbare Flüssigkeiten, wie Wasser und Toluol, bilden leicht Azeotrope. Im Allgemeinen werden diese Azeotrope als niedrig siedende Azeotrope bezeichnet, weil der Siedepunkt des Azeotrops niedriger ist als der Siedepunkt der beiden reinen Komponenten. Die Temperatur und Zusammensetzung des Azeotrops lässt sich leicht aus dem Dampfdruck der reinen Komponenten vorhersagen, ohne dass das Raoultsche Gesetz angewendet werden muss. Das Azeotrop lässt sich in einer Destillationsanlage leicht aufbrechen, indem man einen Flüssigkeitsabscheider (einen Dekanter) verwendet, um die beiden Flüssigkeitsschichten, die über dem Kopf kondensieren, zu trennen. Nur eine der beiden Flüssigkeitsschichten wird in den Destillationsapparat zurückgeführt. ⓘ
Es gibt auch hochsiedende Azeotrope, wie z. B. eine 20-prozentige Mischung von Salzsäure in Wasser. Wie der Name schon sagt, ist der Siedepunkt des Azeotrops höher als der Siedepunkt der beiden reinen Komponenten. ⓘ
Um azeotrope Destillationen aufzubrechen und Destillationsgrenzen zu überschreiten, wie beim DeRosier-Problem, ist es notwendig, die Zusammensetzung des leichten Schlüssels im Destillat zu erhöhen. ⓘ
Hierbei wird eine Komponente zugegeben, die mit dem abzutrennenden Stoff ein Azeotrop bildet. Beispielsweise kann bei einer sauer katalysierten Veresterung das entstehende Wasser als Azeotrop mit Toluol, Hexan, Chloroform oder anderen geeigneten Lösemitteln fast quantitativ entfernt werden, wodurch die Reaktion fast vollständig abläuft. Bei den genannten Lösemitteln bildet sich ein Heteroazeotrop, das beim Kondensieren wiederum in zwei Phasen zerfällt, was mit einem Wasserabscheider eine Rückführung des Lösungsmittels erlaubt. ⓘ
Aufbrechen eines Azeotrops mit unidirektionaler Druckmanipulation
Die Siedepunkte der Komponenten eines Azeotrops überschneiden sich und bilden ein Band. Setzt man ein Azeotrop einem Vakuum oder Überdruck aus, kann man den Siedepunkt einer Komponente von dem der anderen ablenken, indem man die unterschiedlichen Dampfdruckkurven der beiden Komponenten ausnutzt; die Kurven können sich am azeotropen Punkt überlappen, sind aber weiter entlang der Druckachse zu beiden Seiten des azeotropen Punktes wahrscheinlich nicht identisch. Wenn die Verzerrung groß genug ist, überschneiden sich die beiden Siedepunkte nicht mehr und die azeotrope Zone verschwindet. ⓘ
Diese Methode kann die Zugabe anderer Chemikalien zu einer Destillation überflüssig machen, hat aber zwei potenzielle Nachteile. ⓘ
Bei Unterdruck wird Energie für eine Vakuumquelle benötigt, und die niedrigeren Siedepunkte der Destillate erfordern, dass der Kondensator kühler betrieben wird, um zu verhindern, dass Destillatdämpfe an die Vakuumquelle verloren gehen. Ein erhöhter Kühlbedarf erfordert oft zusätzliche Energie und möglicherweise neue Geräte oder einen Wechsel des Kühlmittels. ⓘ
Wenn ein Überdruck erforderlich ist, können keine Standard-Glasgeräte verwendet werden, es muss Energie für die Druckbeaufschlagung aufgewendet werden, und es besteht ein höheres Risiko von Nebenreaktionen bei der Destillation, wie z. B. Zersetzung, aufgrund der höheren Temperaturen, die für den Siedevorgang erforderlich sind. ⓘ
Eine unidirektionale Destillation beruht auf einer Druckänderung in einer Richtung, entweder positiv oder negativ. ⓘ
Druckschwingungsdestillation
Die Druckschwingungsdestillation entspricht im Wesentlichen der unidirektionalen Destillation, die zur Spaltung azeotroper Gemische verwendet wird, doch können hier sowohl Über- als auch Unterdruck eingesetzt werden. ⓘ
Dies verbessert die Selektivität der Destillation und ermöglicht es dem Chemiker, die Destillation zu optimieren, indem er extreme Druck- und Temperaturwerte vermeidet, die Energie verschwenden. Dies ist besonders wichtig für kommerzielle Anwendungen. ⓘ
Ein Beispiel für die Anwendung der Druckschwingungsdestillation ist die industrielle Reinigung von Ethylacetat nach dessen katalytischer Synthese aus Ethanol. ⓘ
Industrieller Prozess

Zu den großtechnischen Anwendungen der industriellen Destillation gehören sowohl diskontinuierliche als auch kontinuierliche fraktionierte, Vakuum-, azeotrope, extraktive und Dampfdestillation. Die am weitesten verbreiteten industriellen Anwendungen der kontinuierlichen, stationären fraktionierten Destillation finden sich in Erdölraffinerien, petrochemischen und chemischen Anlagen sowie in Erdgasverarbeitungsanlagen. ⓘ
Zur Kontrolle und Optimierung dieser industriellen Destillation wurde eine standardisierte Labormethode, ASTM D86, eingeführt. Diese Prüfmethode erstreckt sich auf die atmosphärische Destillation von Erdölprodukten unter Verwendung einer Labor-Batch-Destillationseinheit zur quantitativen Bestimmung der Siedebereichseigenschaften von Erdölprodukten. ⓘ
Die industrielle Destillation wird in der Regel in großen, vertikalen zylindrischen Kolonnen durchgeführt, die als Destillationstürme oder Destillationskolonnen mit Durchmessern von etwa 0,65 bis 16 Metern und Höhen von etwa 6 bis 90 Metern oder mehr bezeichnet werden. Wenn die Prozesszufuhr eine unterschiedliche Zusammensetzung hat, wie bei der Destillation von Rohöl, ermöglichen Flüssigkeitsauslässe in Abständen in der Kolonne die Entnahme verschiedener Fraktionen oder Produkte mit unterschiedlichen Siedepunkten oder Siedebereichen. Die "leichtesten" Produkte (mit dem niedrigsten Siedepunkt) treten am Kopf der Kolonne aus und die "schwersten" Produkte (mit dem höchsten Siedepunkt) treten am Boden der Kolonne aus und werden oft als Sumpfprodukt bezeichnet. ⓘ
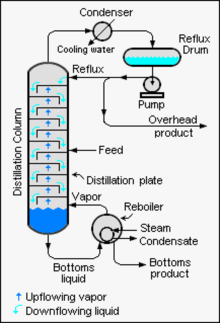
Industrielle Destillationstürme verwenden Rückfluss, um eine vollständigere Trennung der Produkte zu erreichen. Als Rückfluss wird der Teil des kondensierten flüssigen Kopfprodukts eines Destillations- oder Fraktionierungsturms bezeichnet, der in den oberen Teil des Turms zurückgeführt wird, wie in der schematischen Darstellung eines typischen, großtechnischen Destillationsturms gezeigt. Im Turm sorgt die nach unten fließende Rücklaufflüssigkeit für die Kühlung und Kondensation der nach oben fließenden Dämpfe und erhöht so die Effizienz des Destillationsturms. Je mehr Rückfluss für eine bestimmte Anzahl theoretischer Platten zur Verfügung steht, desto besser trennt der Turm die niedriger siedenden Stoffe von den höher siedenden Stoffen. Umgekehrt gilt: Je mehr Rückfluss für eine bestimmte gewünschte Trennung bereitgestellt wird, desto weniger theoretische Platten sind erforderlich. Chemieingenieure müssen die Kombination aus Rückflussrate und Anzahl der Böden wählen, die für die in der Destillationskolonne gereinigten Produkte sowohl wirtschaftlich als auch physikalisch machbar ist. ⓘ
Solche industriellen Fraktioniertürme werden auch bei der kryogenen Luftzerlegung zur Herstellung von flüssigem Sauerstoff, flüssigem Stickstoff und hochreinem Argon eingesetzt. Die Destillation von Chlorsilanen ermöglicht auch die Herstellung von hochreinem Silizium für die Verwendung als Halbleiter. ⓘ
Aufbau und Betrieb eines Destillationsturms hängen von der Beschickung und den gewünschten Produkten ab. Bei einer einfachen, aus zwei Komponenten bestehenden Beschickung können analytische Methoden wie die McCabe-Thiele-Methode oder die Fenske-Gleichung verwendet werden. Bei einer Mehrkomponentenbeschickung werden Simulationsmodelle sowohl für die Auslegung als auch für den Betrieb verwendet. Darüber hinaus sind die Wirkungsgrade der in Destillationstürmen verwendeten Dampf-Flüssigkeits-Kontaktvorrichtungen (als "Platten" oder "Böden" bezeichnet) in der Regel niedriger als die einer theoretischen Gleichgewichtsstufe mit 100 % Wirkungsgrad. Daher benötigt ein Destillationsturm mehr Böden als die Anzahl der theoretischen Dampf-Flüssigkeits-Gleichgewichtsstufen. Zur Schätzung des Wirkungsgrads der Böden wurde eine Reihe von Modellen aufgestellt. ⓘ
Bei modernen industriellen Anwendungen wird anstelle von Böden ein Füllmaterial in der Kolonne verwendet, wenn ein geringer Druckabfall in der Kolonne erforderlich ist. Andere Faktoren, die eine Packung begünstigen, sind: Vakuumsysteme, Kolonnen mit kleinerem Durchmesser, korrosive Systeme, Systeme, die zum Schäumen neigen, Systeme, die eine geringe Flüssigkeitsaufnahme erfordern, und Batch-Destillation. Umgekehrt sprechen folgende Faktoren für Plattenkolonnen: Vorhandensein von Feststoffen in der Beschickung, hohe Flüssigkeitsraten, große Kolonnendurchmesser, komplexe Kolonnen, Kolonnen mit großen Schwankungen in der Zusammensetzung der Beschickung, Kolonnen mit einer chemischen Reaktion, Absorptionskolonnen, Kolonnen, die durch die Toleranz des Fundamentgewichts begrenzt sind, niedrige Flüssigkeitsraten, ein großes Turn-Down-Verhältnis und Prozesse, die Prozessschwankungen unterliegen. ⓘ

Bei dem Packungsmaterial kann es sich entweder um willkürlich abgelegte Packungen (25-76 Millimeter breit) wie Raschig-Ringe oder strukturierte Bleche handeln. Flüssigkeiten neigen dazu, die Oberfläche der Packung zu benetzen, und die Dämpfe strömen über diese benetzte Oberfläche, wo der Stoffaustausch stattfindet. Im Gegensatz zur herkömmlichen Destillation mit Böden, bei der jeder Boden einen separaten Punkt des Dampf-Flüssigkeits-Gleichgewichts darstellt, ist die Dampf-Flüssigkeits-Gleichgewichtskurve in einer Füllkörperkolonne kontinuierlich. Bei der Modellierung von Füllkörperkolonnen ist es jedoch sinnvoll, eine Anzahl von "theoretischen Stufen" zu berechnen, um die Trennleistung der Füllkörperkolonne im Vergleich zu herkömmlichen Böden anzugeben. Unterschiedlich geformte Packungen haben unterschiedliche Oberflächen und Leerräume zwischen den Packungen. Beide Faktoren wirken sich auf die Packungsleistung aus. ⓘ
Ein weiterer Faktor, der neben der Packungsform und der Oberfläche die Leistung einer ungeordneten oder strukturierten Packung beeinflusst, ist die Flüssigkeits- und Dampfverteilung beim Eintritt in das Füllkörperbett. Die Anzahl der theoretischen Stufen, die für eine bestimmte Abscheidung erforderlich sind, wird anhand eines bestimmten Dampf-Flüssigkeits-Verhältnisses berechnet. Wenn die Flüssigkeit und der Dampf beim Eintritt in das Schüttbett nicht gleichmäßig über die Oberfläche des Turms verteilt sind, stimmt das Flüssigkeits-Dampf-Verhältnis im Schüttbett nicht und die erforderliche Trennung wird nicht erreicht. Die Schüttung scheint nicht richtig zu funktionieren. Die Höhe, die einer theoretischen Platte entspricht (HETP), wird größer sein als erwartet. Das Problem liegt nicht an der Schüttung selbst, sondern an der Fehlverteilung der in die Schüttung eintretenden Fluide. Flüssigkeitsfehlverteilungen sind häufiger das Problem als Dampf. Die Konstruktion der Flüssigkeitsverteiler, die für die Zufuhr und den Rückfluss in ein Füllkörperbett verwendet werden, ist entscheidend für die maximale Effizienz der Packung. Methoden zur Bewertung der Wirksamkeit eines Flüssigkeitsverteilers für die gleichmäßige Verteilung der in ein Schüttbett eintretenden Flüssigkeit sind in der Literatur zu finden. Die Fractionation Research, Inc. (allgemein bekannt als FRI) hat zu diesem Thema umfangreiche Arbeiten durchgeführt. ⓘ
Multi-Effekt-Destillation
Ziel der Multi-Effekt-Destillation ist es, die Energieeffizienz des Prozesses für die Entsalzung oder in einigen Fällen für eine Stufe der Reinstwasserproduktion zu erhöhen. Die Anzahl der Effekte ist umgekehrt proportional zur Zahl kW-h/m3 des gewonnenen Wassers und bezieht sich auf das Volumen des pro Energieeinheit gewonnenen Wassers im Vergleich zur Destillation mit einem Effekt. Ein Effekt entspricht etwa 636 kW-h/m3.
- Bei der mehrstufigen Flash-Destillation können, wie in dem Artikel erwähnt, mehr als 20 Effekte mit thermischem Energieeinsatz erzielt werden.
- Brüdenkompressionsverdampfung - Kommerzielle Großanlagen können nach Angaben der Hersteller mit elektrischer Energiezufuhr etwa 72 Effekte erzielen. ⓘ
Es gibt noch viele andere Arten von Multieffekt-Destillationsverfahren, darunter auch die so genannte einfache Multieffekt-Destillation (MED), bei der mehrere Kammern mit dazwischen liegenden Wärmetauschern eingesetzt werden. ⓘ
In der Lebensmittelverarbeitung
Getränke
Man lässt kohlenhydrathaltige Pflanzenmaterialien gären, wobei eine verdünnte Ethanollösung entsteht. Spirituosen wie Whiskey und Rum werden durch Destillation dieser verdünnten Ethanollösungen hergestellt. Im Kondensat sammeln sich neben Ethanol auch andere Bestandteile wie Wasser, Ester und andere Alkohole, die für den Geschmack des Getränks verantwortlich sind. Einige dieser Getränke werden anschließend in Fässern oder anderen Behältern gelagert, um weitere Aromastoffe und charakteristische Geschmacksrichtungen zu erhalten. ⓘ
Galerie
 |
In den Anfängen der Chemie wurden Retorten als Laborgeräte ausschließlich für Destillationsverfahren verwendet. ⓘ |
 |
Ein einfacher Aufbau zur Destillation von trockenem und sauerstofffreiem Toluol. |
 |
Schema einer Vakuumdestillationskolonne im Industriemaßstab, wie sie in Erdölraffinerien üblich ist |
 |
Ein Rotationsverdampfer ist in der Lage, Lösungsmittel durch die Nutzung des Vakuums bei niedrigeren Temperaturen schneller zu destillieren. |
 |
Destillation mit einer halbmikroskopischen Apparatur. Die fugenlose Konstruktion macht das Zusammenstecken von Teilen überflüssig. Der birnenförmige Kolben ermöglicht es, den letzten Tropfen Rückstand zu entfernen, verglichen mit einem Rundkolben ähnlicher Größe. Das geringe Auffangvolumen verhindert Verluste. Mit einem "Molch" werden die verschiedenen Destillate in drei Auffangkolben geleitet. Bei Bedarf kann die Destillation mit Hilfe des Vakuumadapters am Molch unter Vakuum durchgeführt werden. |
Prinzipien
Einfache Destillation
Bei der einfachen Destillation wird der Sumpf mithilfe einer geeigneten Wärmequelle (z. B. Heizhaube oder Heizbad) auf die gewünschte Temperatur erhitzt, bei der die Zielkomponente zu sieden beginnt. Ist diese erreicht, steigt der Stoff gasförmig auf und kondensiert wieder im Kühler. Im Labor wird meist ein Liebigkühler verwendet. Auf dem Thermometer kann man die Kopftemperatur des verdampften Stoffes ablesen und anhand dieses Wertes sicherstellen, dass man die gewünschte Komponente aus dem Gemisch entfernt bzw. gewinnt. Am Ende der Apparatur befindet sich der Auffangkolben. ⓘ
Ein Beispiel für die Anwendung der einfachen Destillation ist die Abtrennung gelöster Verunreinigungen (Salze oder anderer Feststoffe) aus einer Flüssigkeit. Durch Filtration lassen diese sich nicht entfernen. ⓘ
Fraktionierte Destillation
Ein aus mehreren Komponenten bestehendes Gemisch kann durch fraktionierte Destillation getrennt werden. Dabei wird der zum Auffangen des Destillates genutzte Behälter nach dem Abtrennen der am niedrigsten siedenden Fraktion ausgewechselt. Der Zeitpunkt zum Wechseln wird dabei durch eine Änderung der Temperatur im Destillationskopf angezeigt. Meist wird noch bis zum Erreichen des Siedepunkts der nächsten Komponente eine Zwischenfraktion abgetrennt, da im Übergangsbereich häufig ein Gemisch entsteht, und um Reste der vorherigen Fraktion aus dem Kühler zu entfernen. Liegen die Siedepunkte nahe beieinander, kann durch Zwischenschalten einer Kolonne das Volumen der unsauberen Zwischenfraktion klein gehalten werden. ⓘ
- Hinweis
Die Begriffe „fraktionierte Destillation“ und „Rektifikation“ als Gegenstromdestillation, Rückflussdestillation, Kolonnendestillation werden häufig synonym verwendet. Im strengen Sinne bedeutet es, dass ein aus mehreren Komponenten bestehendes Gemisch durch Destillation und Fraktionierung getrennt werden kann. Dabei wird der zum Auffangen des Destillates genutzte Behälter nach dem Auffangen der am niedrigsten siedenden Fraktion ausgewechselt. Fraktionieren bedeutet dabei lediglich das Auffangen mehrerer Fraktionen. ⓘ
Vakuumdestillation
Die Vakuumdestillation ist eine Destillation bei verringertem Gesamtdruck in der Destillationsanlage. Dadurch werden die Siedetemperaturen der einzelnen Komponenten gesenkt, was die Destillation von Stoffgemischen ermöglicht, deren im Sumpf verbleibenden Komponenten nicht ausreichend temperaturstabil sind. Bei höheren Temperaturen können im Sumpf oder im übrigen Edukt Katalysatorrückstände oder Nebenprodukte enthalten sein, die durch unerwünschte Reaktionen die Ausbeute senken. ⓘ
Großtechnisch wird das „Sumpfprodukt“ der atmosphärischen Destillation bei der Erdölraffination anschließend noch einer Vakuumdestillation unterworfen. So sollen hauptsächlich die Grundöle zur Schmierölproduktion und sogenanntes Vakuumgasöl hergestellt werden. Dies dient weiterhin als wertvolles Edukt für einen Cat Cracker oder einen Hydrocracker. ⓘ
Überdruckdestillation
Bei der Überdruckdestillation wird die Anlage mit Überdruck gefahren, um die Siedepunktdifferenzen der Komponenten zu vergrößern. Der Anwendungsbereich liegt üblicherweise bei Stoffen mit sehr niedrigen Siedepunkten, die eng beieinander liegen, wie bei der Luftverflüssigung. ⓘ
Auch bei Pflanzenmaterial mit schwer destillierbaren Ölen wird zuweilen die Überdruckdestillation mit überhitztem Wasserdampf angewandt. Hierbei ist das Öl-Wasser-Verhältnis im Destillat günstiger als bei Normaldruck. ⓘ
Kugelrohrdestillation
Destillationen im Kugelrohr werden im Labor mit kleinen Substanzmengen durchgeführt. Näheres wird in diesem Artikel beschrieben. ⓘ
Schleppdestillation
Hierbei wird mit einem Stoffzusatz destilliert, der das Produkt „mitschleppt“. Bekannteste Variante dieser Destillationsart ist die Wasserdampfdestillation. Wenn eine Vakuumdestillation nicht optimal durchzuführen ist, wird diese angewandt, um wärmeempfindliche Substanzen mit geringem Dampfdruck zu destillieren. Beispiele sind die Extraktion von ätherischen Ölen aus Pflanzen oder die Anwendung bei der Reinigung substituierter Aromaten. ⓘ
Kurzwegdestillation

Als Kurzwegdestillation (KWD) bezeichnet man eine Destillation, die im Feinvakuumbereich, also im Druckbereich zwischen 1 und 0,001 mbar durchgeführt wird und bei der die Gasphase nur einen sehr kurzen Weg zwischen der Vorlage und dem Kondensator zurückzulegen hat. Sie wird auch als Molekulardestillation bezeichnet und gehört zu den schonendsten thermischen Trennverfahren. Aufgrund des geringen Arbeitsdrucks erfolgt die Destillation schon bei relativ niedrigen Temperaturen. Im Vergleich zu anderen Destillationsverfahren können somit thermisch empfindliche Produkte wie Tocopherole, Fettsäureester, Monoglyceride, Prepolymere, Epoxidharze und Pharmawirkstoffe sehr schonend getrennt werden. Geeignet ist die Methode auch für schwer verdampfbare Moleküle, wie langkettige Kohlenwasserstoffe aus den Rückständen der Mineralölindustrie, die unter Feinvakuum abdestilliert werden. Eine modifizierte Variante ist die Kugelrohrdestillation. In der Industrie sind plattenwärmetauscherähnliche Apparate im Einsatz, bei denen der Abstand zwischen Verdampfer und Kondensator nur wenige Millimeter beträgt. ⓘ
Reaktivdestillation

Bei der Reaktivdestillation wird die (mehrstufige) Destillation mit einer chemischen Reaktion kombiniert. Durch die Kombination beider Mechanismen können Vorteile im Vergleich zu einfachen, seriellen Reaktions-Destillations-Verfahren erzielt werden. Reaktivdestillation eignet sich vor allem für „gleichgewichtslimitierte“ Reaktionen. Durch das ständige Entfernen eines Reaktionspartners wird das Gleichgewicht immer wieder neu eingestellt und auf diese Weise ein vollständiger Umsatz ermöglicht. Andererseits können durch die Reaktion auftretende Azeotrope gebrochen werden. Bei exothermen Reaktion wird dabei die auftretende Wärme zur Stofftrennung ausgenutzt. Die optimalen Betriebsbedingungen und hierbei vor allem der optimale Temperaturbereich für Reaktion und Stofftrennung können diese Methode verhindern. ⓘ
Die auftretende chemische Reaktion kann sowohl homogen als auch heterogen katalysiert werden. Bei der Verwendung eines homogenen Katalysators ist eine weitere Trennstufe zur Abtrennung des Katalysators notwendig. Bei der heterogen katalysierten Reaktivdestillation wird der Katalysator häufig in Form von reaktiven Packungen in der Destillationskolonne eingebaut. Dabei handelt es sich oftmals um Trennpackungen, in die der meist kugelförmige Katalysator in Metallsäckchen integriert ist. Trotz intensiver Forschungen in den letzten Jahrzehnten findet die Reaktivdestillation in der Industrie nur relativ selten Verwendung. Wichtig ist sie allerdings bei der Kaliumproduktion. ⓘ

Unbeabsichtigte Destillationsvorgänge
In technischen Anlagen, beispielsweise in Absauganlagen für Dämpfe, treten oft unbeabsichtigt Abscheidungen nach vorheriger Verdampfung auf, indem abgesaugte Dämpfe in den Absaugrohren kondensieren und diese Kondensate langfristig zu Verstopfungen oder zu weiteren Anbackungen führen. Beispielsweise Fettablagerungen bei Dunstabzugshauben oder Wasserkondensat in Druckluftschläuchen (das bei tiefen Temperaturen gefriert). ⓘ