Bor
 Bor (β-rhomboedrisch) | ||||||||||||||||
| Bor | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Aussprache . | /ˈbɔːrɒn/ (BOR-on) | |||||||||||||||
| Allotrope | α-, β-rhomboedrisch, β-tetragonal (und mehr) | |||||||||||||||
| Erscheinungsbild | schwarz-braun | |||||||||||||||
| Standard-Atomgewicht Ar°(B) |
| |||||||||||||||
| Bor im Periodensystem | ||||||||||||||||
| ||||||||||||||||
| Ordnungszahl (Z) | 5 | |||||||||||||||
| Gruppe | Gruppe 13 (Bor-Gruppe) | |||||||||||||||
| Periode | Periode 2 | |||||||||||||||
| Block | p-Block | |||||||||||||||
| Elektronen-Konfiguration | [[[Helium|He]]] 2s2 2p1 | |||||||||||||||
| Elektronen pro Schale | 2, 3 | |||||||||||||||
| Physikalische Eigenschaften | ||||||||||||||||
| Phase bei STP | fest | |||||||||||||||
| Schmelzpunkt | 2349 K (2076 °C, 3769 °F) | |||||||||||||||
| Siedepunkt | 4200 K (3927 °C, 7101 °F) | |||||||||||||||
| Dichte in flüssigem Zustand (bei m.p.) | 2,08 g/cm3 | |||||||||||||||
| Schmelzwärme | 50,2 kJ/mol | |||||||||||||||
| Verdampfungswärme | 508 kJ/mol | |||||||||||||||
| Molare Wärmekapazität | 11,087 J/(mol-K) | |||||||||||||||
Verdampfungsdruck
| ||||||||||||||||
| Atomare Eigenschaften | ||||||||||||||||
| Oxidationsstufen | -5, -1, 0, +1, +2, +3 (ein leicht saures Oxid) | |||||||||||||||
| Elektronegativität | Pauling-Skala: 2,04 | |||||||||||||||
| Ionisierungsenergien |
| |||||||||||||||
| Atomradius | empirisch: 90 pm | |||||||||||||||
| Kovalenter Radius | 84±3 pm | |||||||||||||||
| Van-der-Waals-Radius | 192 pm | |||||||||||||||
| Spektrallinien des Bors | ||||||||||||||||
| Andere Eigenschaften | ||||||||||||||||
| Natürliches Vorkommen | primordial | |||||||||||||||
| Kristallstruktur | rhomboedrisch | |||||||||||||||
| Schallgeschwindigkeit dünner Stab | 16.200 m/s (bei 20 °C) | |||||||||||||||
| Thermische Ausdehnung | β-Form: 5-7 µm/(m⋅K) (bei 25 °C) | |||||||||||||||
| Thermische Leitfähigkeit | 27,4 W/(m⋅K) | |||||||||||||||
| Elektrischer Widerstand | ~106 Ω⋅m (bei 20 °C) | |||||||||||||||
| Magnetische Ordnung | diamagnetisch | |||||||||||||||
| Molare magnetische Suszeptibilität | -6,7×10-6 cm3/mol | |||||||||||||||
| Mohs-Härte | ~9.5 | |||||||||||||||
| CAS-Nummer | 7440-42-8 | |||||||||||||||
| Geschichte | ||||||||||||||||
| Entdeckung | Joseph Louis Gay-Lussac und Louis Jacques Thénard (30. Juni 1808) | |||||||||||||||
| Erste Isolierung | Humphry Davy (9. Juli 1808) | |||||||||||||||
| Hauptisotope des Bors | ||||||||||||||||
| ||||||||||||||||
| Der 10B-Gehalt beträgt in natürlichen Proben 19,1-20,3%, der Rest ist 11B. | ||||||||||||||||
Bor ist ein chemisches Element mit dem Symbol B und der Ordnungszahl 5. In seiner kristallinen Form ist es ein sprödes, dunkles, glänzendes Metalloid; in seiner amorphen Form ist es ein braunes Pulver. Als leichtestes Element der Bor-Gruppe verfügt es über drei Valenzelektronen, mit denen es kovalente Bindungen eingehen kann. Daraus ergeben sich zahlreiche Verbindungen wie Borsäure, das Mineral Natriumborat und die ultraharten Kristalle von Borkarbid und Bornitrid. ⓘ
Bor wird ausschließlich durch Spallation kosmischer Strahlung und Supernovae synthetisiert und nicht durch stellare Nukleosynthese, weshalb es im Sonnensystem und in der Erdkruste nur in geringen Mengen vorkommt. Es macht etwa 0,001 Gewichtsprozent der Erdkruste aus. Auf der Erde ist es aufgrund der Wasserlöslichkeit seiner häufigsten natürlich vorkommenden Verbindungen, der Boratminerale, konzentriert. Diese werden industriell als Evaporite, wie Borax und Kernit, abgebaut. Die größten bekannten Vorkommen befinden sich in der Türkei, dem größten Produzenten von Bormineralien. ⓘ
Elementares Bor ist ein Metalloid, das in geringen Mengen in Meteoroiden vorkommt, aber chemisch ungebundenes Bor kommt auf der Erde sonst nicht vor. In der Industrie ist die Herstellung des sehr reinen Elements aufgrund der Verunreinigung durch Kohlenstoff oder andere Elemente, die sich nicht entfernen lassen, schwierig. Es gibt mehrere Allotrope: amorphes Bor ist ein braunes Pulver; kristallines Bor ist silbrig bis schwarz, extrem hart (etwa 9,5 auf der Mohs-Skala) und bei Raumtemperatur ein schlechter elektrischer Leiter. Das Element selbst wird in erster Linie in Form von Bor-Filamenten verwendet, die ähnlich wie Kohlenstofffasern in einigen hochfesten Materialien eingesetzt werden. ⓘ
Bor wird hauptsächlich in chemischen Verbindungen verwendet. Etwa die Hälfte der weltweit verbrauchten Produktion ist ein Zusatzstoff in Glasfasern für Isolier- und Strukturmaterialien. Die zweitwichtigste Verwendung ist die in Polymeren und Keramiken für hochfeste, leichte Struktur- und hitzebeständige Materialien. Borosilikatglas ist wegen seiner höheren Festigkeit und Temperaturwechselbeständigkeit als gewöhnliches Kalknatronglas gefragt. Als Natriumperborat wird es als Bleichmittel verwendet. Eine geringe Menge wird als Dotierstoff in Halbleitern und als Zwischenprodukt bei der Synthese von organischen Feinchemikalien verwendet. Einige borhaltige organische Pharmazeutika werden verwendet oder sind in der Forschung. Natürliches Bor besteht aus zwei stabilen Isotopen, von denen eines (Bor-10) als Neutronenfänger verwendet wird. ⓘ
Die Berührungspunkte von Bor mit der Biologie sind sehr gering. Es besteht kein Konsens darüber, dass es für das Leben von Säugetieren wesentlich ist. Borate haben eine geringe Toxizität für Säugetiere (ähnlich wie Kochsalz), sind aber giftiger für Gliederfüßer und werden gelegentlich als Insektizide eingesetzt. Borhaltige organische Antibiotika sind bekannt. Obwohl es nur in Spuren benötigt wird, ist es ein essentieller Pflanzennährstoff. ⓘ
Geschichte
Das Wort Bor wurde von Borax, dem Mineral, aus dem es isoliert wurde, in Analogie zu Kohlenstoff geprägt, dem Bor chemisch ähnelt. ⓘ

Borax in seiner mineralischen Form (damals als Tinkal bekannt) wurde erstmals um 300 n. Chr. in China als Glasur verwendet. Rohes Borax gelangte nach Westen und wurde offenbar um 700 n. Chr. von dem Alchemisten Jabir ibn Hayyan erwähnt. Marco Polo brachte im 13. Jahrhundert einige Glasuren mit nach Italien. Georgius Agricola berichtete um 1600 n. Chr. über die Verwendung von Borax als Flussmittel in der Metallurgie. Im Jahr 1777 wurde Borsäure in den heißen Quellen (soffioni) in der Nähe von Florenz, Italien, entdeckt, wo sie als sal sedativum bekannt wurde, mit angeblichen medizinischen Vorteilen. Das Mineral wurde Sassolith genannt, nach Sasso Pisano in Italien. Sasso war von 1827 bis 1872 die Hauptquelle für europäisches Borax, bis es durch amerikanische Quellen ersetzt wurde. Borverbindungen wurden bis zum Ende des 19. Jahrhunderts relativ selten verwendet, als die Pacific Coast Borax Company von Francis Marion Smith sie zum ersten Mal populär machte und in großen Mengen zu niedrigen Kosten herstellte. ⓘ
Bor wurde erst als Element erkannt, als es von Sir Humphry Davy sowie von Joseph Louis Gay-Lussac und Louis Jacques Thénard isoliert wurde. Im Jahr 1808 beobachtete Davy, dass sich beim Durchleiten von elektrischem Strom durch eine Boratlösung ein brauner Niederschlag auf einer der Elektroden bildete. In seinen nachfolgenden Experimenten verwendete er Kalium zur Reduktion von Borsäure anstelle der Elektrolyse. Er stellte genügend Bor her, um ein neues Element zu bestätigen und nannte es Boracium. Gay-Lussac und Thénard verwendeten Eisen, um Borsäure bei hohen Temperaturen zu reduzieren. Durch die Oxidation von Bor mit Luft wiesen sie nach, dass Borsäure sein Oxidationsprodukt ist. Jöns Jacob Berzelius identifizierte es 1824 als Element. Reines Bor wurde wohl erstmals 1909 von dem amerikanischen Chemiker Ezekiel Weintraub hergestellt. ⓘ
Borverbindungen (von persisch بوره burah über arabisch بورق buraq und griech. βοραχου bzw. lat. borax „borsaures Natron“, „Borax“) sind seit Jahrtausenden bekannt. Im alten Ägypten nutzte man zur Mumifikation das Mineral Natron, das neben anderen Verbindungen auch Borate enthält. Seit dem 4. Jahrhundert wird Boraxglas im Kaiserreich China verwendet. Borverbindungen wurden im antiken Rom zur Glasherstellung verwendet. ⓘ
Herstellung von elementarem Bor im Labor
Die frühesten Wege zu elementarem Bor führten über die Reduktion von Boroxid mit Metallen wie Magnesium oder Aluminium. Das Produkt ist jedoch fast immer mit Boriden dieser Metalle verunreinigt. Reines Bor kann durch Reduktion flüchtiger Borhalogenide mit Wasserstoff bei hohen Temperaturen hergestellt werden. Hochreines Bor zur Verwendung in der Halbleiterindustrie wird durch Zersetzung von Diboran bei hohen Temperaturen hergestellt und anschließend durch das Zonenschmelz- oder Czochralski-Verfahren weiter gereinigt. ⓘ
Bei der Herstellung von Borverbindungen wird kein elementares Bor gebildet, sondern die günstige Verfügbarkeit von Boraten ausgenutzt. ⓘ
Merkmale
Allotrope

Bor ist ähnlich wie Kohlenstoff in der Lage, stabile kovalent gebundene molekulare Netzwerke zu bilden. Selbst nominell ungeordnetes (amorphes) Bor enthält regelmäßige Bor-Ikosaeder, die ohne weitreichende Ordnung zufällig aneinander gebunden sind. Kristallines Bor ist ein sehr hartes, schwarzes Material mit einem Schmelzpunkt von über 2000 °C. Es bildet vier Hauptallotrope: α-rhomboedrisch und β-rhomboedrisch (α-R und β-R), γ-orthorhombisch (γ) und β-tetragonal (β-T). Alle vier Phasen sind bei Umgebungsbedingungen stabil, wobei die β-rhomboedrische Phase die häufigste und stabilste ist. Es gibt auch eine α-tetragonale Phase (α-T), die jedoch ohne erhebliche Verunreinigung nur sehr schwer herzustellen ist. Die meisten Phasen basieren auf B12-Ikosaedern, aber die γ-Phase kann als eine steinsalzartige Anordnung der Ikosaeder und B2-Atompaare beschrieben werden. Sie kann durch Komprimieren anderer Borphasen auf 12-20 GPa und Erhitzen auf 1500-1800 °C hergestellt werden; sie bleibt nach Ablassen von Temperatur und Druck stabil. Die β-T-Phase wird bei ähnlichen Drücken, aber höheren Temperaturen von 1800-2200 °C hergestellt. Die α-T- und die β-T-Phase können bei Umgebungsbedingungen koexistieren, wobei die β-T-Phase die stabilere ist. Bei einer Komprimierung von Bor über 160 GPa entsteht eine Borphase mit einer noch unbekannten Struktur, die bei Temperaturen unter 6-12 K supraleitend ist. 2014 wurden Borospheren (Fulleren-ähnliche B40-Moleküle) und Borophen (vorgeschlagene Graphen-ähnliche Struktur) beschrieben. ⓘ
| Bor-Phase | α-R | β-R | γ | β-T ⓘ |
|---|---|---|---|---|
| Symmetrie | Rhomboedrisch | Rhomboedrisch | Orthorhombisch | Tetragonal |
| Atome/Einheitszelle | 12 | ~105 | 28 | |
| Dichte (g/cm3) | 2.46 | 2.35 | 2.52 | 2.36 |
| Vickers-Härte (GPa) | 42 | 45 | 50–58 | |
| Elastizitätsmodul (GPa) | 185 | 224 | 227 | |
| Bandlücke (eV) | 2 | 1.6 | 2.1 |
Chemie des Elements
Elementares Bor ist selten und wenig erforscht, da das reine Material extrem schwierig herzustellen ist. Die meisten Studien über "Bor" beziehen sich auf Proben, die geringe Mengen an Kohlenstoff enthalten. Das chemische Verhalten von Bor ähnelt dem von Silizium mehr als dem von Aluminium. Kristallines Bor ist chemisch inert und widersteht dem Angriff von kochender Flusssäure oder Salzsäure. In feiner Verteilung wird es von heißem konzentriertem Wasserstoffperoxid, heißer konzentrierter Salpetersäure, heißer Schwefelsäure oder heißen Schwefel-Chromsäure-Gemischen langsam angegriffen. ⓘ
Die Oxidationsgeschwindigkeit von Bor hängt von der Kristallinität, der Korngröße, der Reinheit und der Temperatur ab. Bei Raumtemperatur reagiert Bor nicht mit Luft, aber bei höheren Temperaturen verbrennt es unter Bildung von Bortrioxid:
- 4 B + 3 O2 → 2 B2O3 ⓘ

Bor lässt sich durch Halogenierung in Trihalogenide umwandeln, z. B,
- 2 B + 3 Br2 → 2 BBr3
Das Trichlorid wird in der Praxis meist aus dem Oxid hergestellt. ⓘ
Atomare Struktur
Bor ist das leichteste Element, das in seinem Grundzustand ein Elektron in einem p-Orbital besitzt. Im Gegensatz zu den meisten anderen p-Elementen hält es sich jedoch selten an die Oktettregel und belegt seine Valenzschale in der Regel mit nur sechs Elektronen (in drei Molekülorbitalen). Bor ist der Prototyp der Borgruppe (IUPAC-Gruppe 13), obwohl die anderen Mitglieder dieser Gruppe Metalle und typischere p-Elemente sind (nur Aluminium teilt bis zu einem gewissen Grad die Abneigung des Bors gegen die Oktettregel). ⓘ
Chemische Verbindungen

In den meisten bekannten Verbindungen hat Bor die formale Oxidationsstufe III. Dazu gehören Oxide, Sulfide, Nitride und Halogenide. ⓘ
Die Trihalogenide weisen eine planare trigonale Struktur auf. Diese Verbindungen sind Lewis-Säuren, da sie leicht Addukte mit Elektronenpaardonatoren bilden, die als Lewis-Basen bezeichnet werden. So bilden beispielsweise Fluorid (F-) und Bortrifluorid (BF3) zusammen das Tetrafluoroborat-Anion BF4-. Bortrifluorid wird in der petrochemischen Industrie als Katalysator verwendet. Die Halogenide reagieren mit Wasser und bilden Borsäure. ⓘ
In der Natur kommt es auf der Erde fast ausschließlich in Form von verschiedenen B(III)-Oxiden vor, oft in Verbindung mit anderen Elementen. Mehr als einhundert Boratminerale enthalten Bor in der Oxidationsstufe +3. Diese Minerale ähneln in mancher Hinsicht den Silikaten, obwohl es häufig nicht nur in tetraedrischer Koordination mit Sauerstoff, sondern auch in trigonal-planarer Konfiguration vorkommt. Im Gegensatz zu den Silikaten kommt Bor in den Mineralen nie mit einer Koordinationszahl von mehr als vier vor. Ein typisches Motiv sind die Tetraborat-Anionen des häufigen Minerals Borax, das links abgebildet ist. Die formale negative Ladung des tetraedrischen Borat-Zentrums wird durch Metallkationen in den Mineralien, wie z. B. das Natrium (Na+) in Borax, ausgeglichen. Die Turmalingruppe der Borat-Silikate ist ebenfalls eine sehr wichtige borhaltige Mineralgruppe, und es sind auch einige Borsilikate bekannt, die in der Natur vorkommen. ⓘ
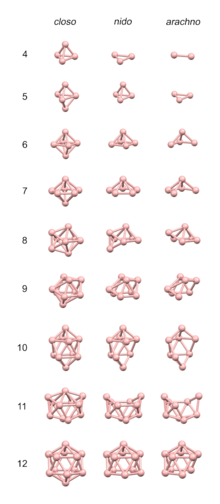
Borane sind chemische Verbindungen aus Bor und Wasserstoff, mit der allgemeinen Formel BxHy. Diese Verbindungen kommen in der Natur nicht vor. Viele der Borane oxidieren leicht bei Kontakt mit Luft, einige sogar heftig. Das Stammglied BH3 wird als Boran bezeichnet, ist aber nur im gasförmigen Zustand bekannt und dimerisiert zu Diboran, B2H6. Die größeren Borane bestehen alle aus polyedrischen Borclustern, von denen einige als Isomere vorliegen. Die Isomere von B20H26 beispielsweise beruhen auf der Verschmelzung von zwei 10-Atom-Clustern. ⓘ
Die wichtigsten Borane sind Diboran B2H6 und zwei seiner Pyrolyseprodukte, Pentaboran B5H9 und Decaboran B10H14. Es ist eine große Anzahl anionischer Borhydride bekannt, z. B. [B12H12]2-. ⓘ
Die formale Oxidationszahl in Boranen ist positiv und beruht auf der Annahme, dass Wasserstoff wie in aktiven Metallhydriden als -1 gezählt wird. Die mittlere Oxidationszahl für die Borverbindungen ist dann einfach das Verhältnis von Wasserstoff zu Bor im Molekül. In Diboran B2H6 beispielsweise ist die Oxidationsstufe des Bors +3, in Decaboran B10H14 jedoch 7/5 oder +1,4. In diesen Verbindungen ist die Oxidationsstufe des Bors oft nicht ganzzahlig. ⓘ
Die Bornitride zeichnen sich durch eine Vielzahl von Strukturen aus, die sie annehmen. Sie weisen Strukturen auf, die verschiedenen Allotropen des Kohlenstoffs entsprechen, darunter Graphit, Diamant und Nanoröhren. In der diamantähnlichen Struktur, die als kubisches Bornitrid (Handelsname Borazon) bezeichnet wird, liegen die Boratome in der tetraedrischen Struktur der Kohlenstoffatome in Diamant vor, aber eine von vier B-N-Bindungen kann als koordinative kovalente Bindung betrachtet werden, bei der zwei Elektronen vom Stickstoffatom abgegeben werden, das als Lewis-Base für eine Bindung an das Lewis-saure Bor(III)-Zentrum dient. Kubisches Bornitrid wird unter anderem als Schleifmittel verwendet, da es eine mit Diamant vergleichbare Härte aufweist (die beiden Stoffe können sich gegenseitig verkratzen). In der BN-Verbindung, die dem Graphit entspricht, dem hexagonalen Bornitrid (h-BN), liegen die positiv geladenen Bor- und negativ geladenen Stickstoffatome in jeder Ebene neben dem entgegengesetzt geladenen Atom in der nächsten Ebene. Folglich haben Graphit und h-BN sehr unterschiedliche Eigenschaften, obwohl beide Schmiermittel sind, da diese Ebenen leicht aneinander vorbeigleiten. Allerdings ist h-BN ein relativ schlechter elektrischer und thermischer Leiter in den planaren Richtungen. ⓘ
Chemie der Organoborone
Es ist eine große Anzahl von Organoborverbindungen bekannt, von denen viele in der organischen Synthese nützlich sind. Viele werden durch Hydroborierung hergestellt, bei der Diboran, B2H6, eine einfache Boranchemikalie, verwendet wird. Organobor(III)-Verbindungen sind in der Regel tetraedrisch oder trigonal planar, z. B. Tetraphenylborat, [B(C6H5)4]- gegenüber Triphenylboran, B(C6H5)3. Mehrere Boratome, die miteinander reagieren, neigen jedoch dazu, neuartige dodekaedrische (12-seitige) und ikosaedrische (20-seitige) Strukturen zu bilden, die vollständig aus Boratomen oder einer unterschiedlichen Anzahl von Kohlenstoff-Heteroatomen bestehen. ⓘ
Bororganische Chemikalien werden für so unterschiedliche Zwecke eingesetzt wie Borcarbid (siehe unten), eine komplexe, sehr harte Keramik, die aus Bor-Kohlenstoff-Cluster-Anionen und -Kationen besteht, und Carborane, Verbindungen aus der Kohlenstoff-Bor-Cluster-Chemie, die halogeniert werden können, um reaktive Strukturen zu bilden, darunter auch Carboran-Säure, eine Supersäure. Carborane bilden beispielsweise nützliche Molekülteile, die anderen biochemischen Stoffen beträchtliche Mengen an Bor hinzufügen, um borhaltige Verbindungen für die Bor-Neutroneneinfangtherapie bei Krebs zu synthetisieren. ⓘ
Verbindungen von B(I) und B(II)
Wie seine Hydridcluster vermuten lassen, bildet Bor eine Vielzahl stabiler Verbindungen mit einer formalen Oxidationsstufe von weniger als drei. B2F4 und B4Cl4 sind gut charakterisiert. ⓘ

Binäre Metall-Bor-Verbindungen, die Metallboride, enthalten Bor in negativen Oxidationsstufen. Ein Beispiel hierfür ist Magnesiumdiborid (MgB2). Jedes Bor-Atom hat eine formale Ladung von -1 und Magnesium eine formale Ladung von +2. In diesem Material sind die Bor-Zentren trigonal planar mit einer zusätzlichen Doppelbindung für jedes Bor und bilden Schichten, ähnlich wie der Kohlenstoff in Graphit. Im Gegensatz zu hexagonalem Bornitrid, dem Elektronen in der Ebene der kovalenten Atome fehlen, ermöglichen es die delokalisierten Elektronen in Magnesiumdiborid jedoch, Elektrizität ähnlich wie isoelektronischer Graphit zu leiten. Im Jahr 2001 wurde festgestellt, dass dieses Material ein Hochtemperatursupraleiter ist. Es ist ein Supraleiter, der aktiv entwickelt wird. Ein Projekt am CERN zur Herstellung von MgB2-Kabeln hat zu supraleitenden Testkabeln geführt, die 20.000 Ampere für Anwendungen mit extrem hoher Stromstärke leiten können, wie z. B. die geplante Version des großen Hadronenbeschleunigers mit hoher Luminosität. ⓘ
Bestimmte andere Metallboride finden spezielle Anwendungen als harte Materialien für Schneidwerkzeuge. Das Bor in den Boriden weist häufig fraktionierte Oxidationsstufen auf, wie z. B. -1/3 in Calciumhexaborid (CaB6). ⓘ
Strukturell gesehen sind die markantesten chemischen Verbindungen des Bors die Hydride. Zu dieser Reihe gehören die Clusterverbindungen Dodecaborat (B
12H2-
12), Decaboran (B10H14) und die Carborane wie C2B10H12. Charakteristisch für diese Verbindungen ist, dass sie Bor mit Koordinationszahlen größer als vier enthalten. ⓘ
Isotope
Bor hat zwei natürlich vorkommende und stabile Isotope, 11B (80,1%) und 10B (19,9%). Der Massenunterschied führt zu einem breiten Spektrum von δ11B-Werten, die als Bruchteil des Unterschieds zwischen 11B und 10B definiert und traditionell in Teilen pro Tausend ausgedrückt werden und in natürlichen Gewässern von -16 bis +59 reichen. Es gibt 13 bekannte Bor-Isotope, das kurzlebigste ist 7B, das durch Protonenemission und Alphazerfall zerfällt. Es hat eine Halbwertszeit von 3,5×10-22 s. Die Isotopenfraktionierung von Bor wird durch die Austauschreaktionen der Borspezies B(OH)3 und [B(OH)4]- gesteuert. Borisotope werden auch während der Mineralkristallisation, während H2O-Phasenänderungen in hydrothermalen Systemen und während der hydrothermalen Umwandlung von Gestein fraktioniert. Der letztgenannte Effekt führt zu einer bevorzugten Entfernung des [10B(OH)4]-Ions auf Tonen. Er führt zu Lösungen, die mit 11B(OH)3 angereichert sind, und könnte daher für die starke Anreicherung von 11B im Meerwasser im Vergleich zu ozeanischer und kontinentaler Kruste verantwortlich sein; dieser Unterschied könnte als Isotopensignatur dienen. ⓘ
Das exotische 17B weist einen nuklearen Halo auf, d. h. sein Radius ist deutlich größer als derjenige, der durch das Flüssigtropfenmodell vorhergesagt wird. ⓘ
Das Isotop 10B ist nützlich für den Einfang thermischer Neutronen (siehe Neutronenquerschnitt#Typische Querschnitte). Die Atomindustrie reichert natürliches Bor zu fast reinem 10B an. Das weniger wertvolle Nebenprodukt, abgereichertes Bor, ist nahezu reines 11B. ⓘ
Kommerzielle Isotopenanreicherung
Wegen seines hohen Neutronenquerschnitts wird Bor-10 häufig als Neutronenfänger zur Spaltungskontrolle in Kernreaktoren eingesetzt. Es wurden mehrere Verfahren zur Anreicherung im industriellen Maßstab entwickelt; derzeit werden jedoch nur die fraktionierte Vakuumdestillation des Dimethylether-Addukts von Bortrifluorid (DME-BF3) und die Säulenchromatographie von Boraten eingesetzt. ⓘ
Angereichertes Bor (Bor-10)

Angereichertes Bor oder 10B wird sowohl für den Strahlenschutz als auch als Hauptnuklid in der Neutroneneinfangtherapie von Krebs eingesetzt. Bei letzterer ("Bor-Neutroneneinfangtherapie" oder BNCT) wird eine 10B-haltige Verbindung in ein Arzneimittel eingebracht, das selektiv von einem bösartigen Tumor und Geweben in dessen Nähe aufgenommen wird. Der Patient wird dann mit einem Strahl niederenergetischer Neutronen mit einer relativ geringen Neutronenstrahlendosis behandelt. Die Neutronen lösen jedoch energiereiche und kurzreichweitige sekundäre Alphateilchen- und Lithium-7-Schwerionenstrahlung aus, die Produkte der Kernreaktion Bor + Neutron sind, und diese Ionenstrahlung bombardiert den Tumor zusätzlich, insbesondere aus dem Inneren der Tumorzellen. ⓘ
In Kernreaktoren wird 10B zur Reaktivitätskontrolle und in Notabschaltsystemen eingesetzt. Es kann entweder in Form von Borsilikat-Steuerstäben oder als Borsäure verwendet werden. In Druckwasserreaktoren wird 10B-Borsäure dem Reaktorkühlmittel zugesetzt, wenn die Anlage zum Brennelementwechsel abgeschaltet wird. Sie wird dann über viele Monate hinweg langsam herausgefiltert, wenn das spaltbare Material verbraucht ist und der Brennstoff weniger reaktiv wird. ⓘ
In zukünftigen interplanetaren Raumfahrzeugen mit Besatzung könnte 10B theoretisch als Strukturmaterial (als Bor-Fasern oder BN-Nanoröhren) eingesetzt werden, das auch eine besondere Rolle im Strahlungsschutz spielen würde. Eine der Schwierigkeiten beim Umgang mit der kosmischen Strahlung, bei der es sich hauptsächlich um hochenergetische Protonen handelt, besteht darin, dass eine sekundäre Strahlung aus der Wechselwirkung zwischen der kosmischen Strahlung und den Materialien des Raumfahrzeugs hochenergetische Spallationsneutronen sind. Solche Neutronen können durch Materialien mit einem hohen Anteil an leichten Elementen, wie z. B. Polyethylen, abgeschwächt werden, aber die abgeschwächten Neutronen stellen weiterhin eine Strahlungsgefahr dar, sofern sie nicht aktiv von der Abschirmung absorbiert werden. Unter den leichten Elementen, die thermische Neutronen absorbieren, erscheinen 6Li und 10B als potenzielle Strukturmaterialien für Raumfahrzeuge, die sowohl zur mechanischen Verstärkung als auch zum Strahlenschutz dienen. ⓘ
Abgereichertes Bor (Bor-11)
Strahlungsgehärtete Halbleiter
Kosmische Strahlung erzeugt sekundäre Neutronen, wenn sie auf Raumfahrzeugstrukturen trifft. Diese Neutronen werden in 10B eingefangen, wenn es in den Halbleitern des Raumfahrzeugs vorhanden ist, und erzeugen eine Gammastrahlung, ein Alphateilchen und ein Lithiumion. Diese Zerfallsprodukte können dann nahegelegene Halbleiter-"Chip"-Strukturen bestrahlen und Datenverluste verursachen (Bit-Flipping oder Single Event Upset). Eine Gegenmaßnahme bei strahlengeschützten Halbleiterkonstruktionen ist die Verwendung von abgereichertem Bor, das stark mit 11B angereichert ist und fast kein 10B enthält. Dies ist nützlich, weil 11B weitgehend immun gegen Strahlungsschäden ist. Abgereichertes Bor ist ein Nebenprodukt der Atomindustrie (siehe oben). ⓘ
Protonen-Bor-Fusion
11B ist auch ein Kandidat als Brennstoff für die aneutronische Fusion. Wenn es von einem Proton mit einer Energie von etwa 500 keV getroffen wird, erzeugt es drei Alphateilchen und eine Energie von 8,7 MeV. Die meisten anderen Fusionsreaktionen, an denen Wasserstoff und Helium beteiligt sind, erzeugen eine durchdringende Neutronenstrahlung, die die Reaktorstrukturen schwächt und eine lang anhaltende Radioaktivität verursacht, wodurch das Betriebspersonal gefährdet wird. Die Alphateilchen der 11B-Fusion können jedoch direkt in elektrische Energie umgewandelt werden, und die Strahlung endet, sobald der Reaktor abgeschaltet wird. ⓘ
NMR-Spektroskopie
Sowohl 10B als auch 11B verfügen über einen Kernspin. Der Kernspin von 10B ist 3 und der von 11B ist 3/2. Diese Isotope eignen sich daher für die kernmagnetische Resonanzspektroskopie, und im Handel sind Spektrometer erhältlich, die speziell für den Nachweis der Bor-11-Kerne geeignet sind. Die 10B- und 11B-Kerne verursachen auch eine Aufspaltung der Resonanzen der gebundenen Kerne. ⓘ
Vorkommen


Bor ist im Universum und im Sonnensystem aufgrund der Spurenbildung beim Urknall und in Sternen selten. Es wird in geringen Mengen bei der Spallationsnukleosynthese durch kosmische Strahlung gebildet und kann ungebunden in kosmischem Staub und Meteoritenmaterial vorkommen. ⓘ
In der sauerstoffreichen Umgebung der Erde liegt Bor immer vollständig zu Borat oxidiert vor. Bor kommt auf der Erde nicht in elementarer Form vor. Äußerst geringe Spuren von elementarem Bor wurden im Regolith des Mondes nachgewiesen. ⓘ
Obwohl Bor ein relativ seltenes Element in der Erdkruste ist und nur 0,001 % der Masse der Erdkruste ausmacht, kann es durch die Einwirkung von Wasser, in dem viele Borate löslich sind, stark konzentriert werden. In der Natur kommt es in Verbindungen wie Borax und Borsäure (manchmal in vulkanischen Quellen) vor. Es sind etwa hundert Boratminerale bekannt. ⓘ
Am 5. September 2017 meldeten Wissenschaftler, dass der Rover Curiosity auf dem Planeten Mars Bor entdeckt hat, einen wesentlichen Bestandteil des Lebens auf der Erde. Zusammen mit früheren Entdeckungen, dass es auf dem alten Mars Wasser gegeben haben könnte, ist dies ein weiterer Beleg für die mögliche frühe Bewohnbarkeit des Gale-Kraters auf dem Mars. ⓘ
Produktion
Wirtschaftlich wichtige Borquellen sind die Mineralien Colemanit, Rasorit (Kernit), Ulexit und Tinkal. Zusammen machen sie 90 % der geförderten borhaltigen Erze aus. Die weltweit größten bekannten Boraxvorkommen, von denen viele noch unerschlossen sind, liegen in der Zentral- und Westtürkei, einschließlich der Provinzen Eskişehir, Kütahya und Balıkesir. Die weltweit nachgewiesenen Borreserven belaufen sich auf mehr als eine Milliarde Tonnen, denen eine jährliche Produktion von etwa vier Millionen Tonnen gegenübersteht. ⓘ
Die Türkei und die Vereinigten Staaten sind die größten Produzenten von Borprodukten. Die Türkei produziert etwa die Hälfte des weltweiten Jahresbedarfs über Eti Mine Works (türkisch: Eti Maden İşletmeleri), ein staatliches türkisches Bergbau- und Chemieunternehmen, das sich auf Borprodukte spezialisiert hat. Es besitzt ein staatliches Monopol auf den Abbau von Boratmineralien in der Türkei, die über 72 % der weltweit bekannten Vorkommen verfügt. Im Jahr 2012 hatte das Unternehmen einen Anteil von 47 % an der weltweiten Produktion von Boratmineralien und lag damit vor seinem Hauptkonkurrenten, der Rio Tinto Group. ⓘ
Fast ein Viertel (23 %) der weltweiten Borproduktion stammt aus der einzigen Borax-Mine von Rio Tinto (auch bekannt als U.S. Borax Boron Mine) 35°2′34.447″N 117°40′45.412″W / 35.04290194°N 117.67928111°W in der Nähe von Boron, Kalifornien. ⓘ
Marktentwicklung
Die durchschnittlichen Kosten für kristallines Bor liegen bei 5 $/g. Freies Bor wird hauptsächlich zur Herstellung von Bor-Fasern verwendet, wo es durch chemische Abscheidung aus der Gasphase auf einen Wolframkern aufgebracht wird (siehe unten). Bor-Fasern werden in leichten Verbundwerkstoffen, wie z. B. hochfesten Bändern, verwendet. Diese Verwendung macht nur einen sehr kleinen Teil der Gesamtverwendung von Bor aus. Bor wird in Form von Borverbindungen durch Ionenimplantation in Halbleiter eingebracht. ⓘ
Der geschätzte weltweite Borverbrauch (fast ausschließlich in Form von Borverbindungen) lag 2012 bei etwa 4 Millionen Tonnen B2O3. Es wird davon ausgegangen, dass die Borabbau- und -raffineriekapazitäten ausreichen, um das erwartete Wachstum im nächsten Jahrzehnt zu decken. ⓘ
Die Form, in der Bor verbraucht wird, hat sich in den letzten Jahren geändert. Die Verwendung von Erzen wie Colemanit ist aufgrund von Bedenken wegen des Arsengehalts zurückgegangen. Die Verbraucher sind dazu übergegangen, raffinierte Borate und Borsäure zu verwenden, die einen geringeren Schadstoffgehalt aufweisen. ⓘ
Die steigende Nachfrage nach Borsäure hat eine Reihe von Herstellern veranlasst, in zusätzliche Kapazitäten zu investieren. Das türkische Staatsunternehmen Eti Mine Works eröffnete 2003 in Emet eine neue Borsäureanlage mit einer Produktionskapazität von 100.000 Tonnen pro Jahr. Die Rio Tinto Group erhöhte die Kapazität ihrer Boranlage von 260.000 Tonnen pro Jahr im Jahr 2003 auf 310.000 Tonnen pro Jahr im Mai 2005 und plant, diese auf 366.000 Tonnen pro Jahr im Jahr 2006 zu erhöhen. Die chinesischen Borhersteller waren nicht in der Lage, die rasch wachsende Nachfrage nach hochwertigen Boraten zu befriedigen. Dies hat dazu geführt, dass die Einfuhren von Natriumtetraborat (Borax) zwischen 2000 und 2005 um das Hundertfache gestiegen sind und die Borsäureeinfuhren im gleichen Zeitraum um 28 % pro Jahr zugenommen haben. ⓘ
Der Anstieg der weltweiten Nachfrage wurde durch die hohen Wachstumsraten bei der Herstellung von Glasfasern, Glasfasern und Borosilikatglasprodukten angetrieben. Die rasche Zunahme der Herstellung von borhaltigem Glasfaserverstärkungsmaterial in Asien hat die Entwicklung von borfreiem Glasfaserverstärkungsmaterial in Europa und den USA ausgeglichen. Der jüngste Anstieg der Energiepreise könnte zu einer stärkeren Verwendung von Isolierglasfasern führen, was einen Anstieg des Borverbrauchs zur Folge hätte. Die Roskill Consulting Group prognostiziert, dass die weltweite Nachfrage nach Bor bis 2010 um 3,4 % pro Jahr auf 21 Millionen Tonnen ansteigen wird. Das stärkste Nachfragewachstum wird in Asien erwartet, wo die Nachfrage um durchschnittlich 5,7 % pro Jahr steigen könnte. ⓘ
Anwendungen
Nahezu das gesamte aus der Erde gewonnene Borerz ist für die Veredelung zu Borsäure und Natriumtetraborat-Pentahydrat bestimmt. In den Vereinigten Staaten werden 70 % des Bors für die Herstellung von Glas und Keramik verwendet. Die weltweit größte industrielle Verwendung von Borverbindungen (etwa 46 % des Endverbrauchs) ist die Herstellung von Glasfasern für borhaltige Isolier- und Strukturglasfasern, insbesondere in Asien. Bor wird dem Glas in Form von Boraxpentahydrat oder Boroxid zugesetzt, um die Festigkeit oder die Flusseigenschaften der Glasfasern zu beeinflussen. Weitere 10 % der weltweiten Borproduktion entfallen auf Borosilikatglas, das in hochfesten Glaswaren verwendet wird. Etwa 15 % des weltweit produzierten Bors werden in Bor-Keramik verwendet, einschließlich der weiter unten beschriebenen superharten Materialien. Die Landwirtschaft verbraucht 11 % der weltweiten Borproduktion, Bleichmittel und Reinigungsmittel etwa 6 %. ⓘ
Elementare Borfasern
Bor-Fasern (Bor-Filamente) sind hochfeste, leichte Werkstoffe, die vor allem für fortschrittliche Strukturen in der Luft- und Raumfahrt als Bestandteil von Verbundwerkstoffen sowie für eine begrenzte Anzahl von Konsum- und Sportartikeln wie Golfschläger und Angelruten verwendet werden. Die Fasern können durch chemische Gasphasenabscheidung von Bor auf einem Wolframfaden hergestellt werden. ⓘ
Bor-Fasern und submillimetergroße kristalline Bor-Federn werden durch laserunterstützte chemische Gasphasenabscheidung hergestellt. Durch Translation des fokussierten Laserstrahls lassen sich auch komplexe schraubenförmige Strukturen herstellen. Solche Strukturen weisen gute mechanische Eigenschaften auf (Elastizitätsmodul 450 GPa, Bruchdehnung 3,7%, Bruchspannung 17 GPa) und können zur Verstärkung von Keramiken oder in mikromechanischen Systemen eingesetzt werden. ⓘ
Boriertes Glasfasergewebe
Glasfaser ist ein faserverstärktes Polymer, das aus mit Glasfasern verstärktem Kunststoff besteht und in der Regel zu einer Matte gewebt wird. Die im Material verwendeten Glasfasern bestehen je nach Glasfaserverwendung aus verschiedenen Glasarten. Diese Gläser enthalten alle Kieselsäure oder Silikat mit unterschiedlichen Mengen an Kalzium- und Magnesiumoxiden und manchmal auch Bor. Das Bor liegt in Form von Borsilikat, Borax oder Boroxid vor und wird zugesetzt, um die Festigkeit des Glases zu erhöhen, oder als Flussmittel, um die Schmelztemperatur der Kieselsäure zu senken, die zu hoch ist, um in reiner Form leicht zu Glasfasern verarbeitet werden zu können. ⓘ
Die hochborierten Gläser, die in Glasfasern verwendet werden, sind E-Glas (benannt nach der Verwendung in der Elektrotechnik, aber heute das gebräuchlichste Glasfaser für den allgemeinen Gebrauch). E-Glas ist ein Alumino-Borosilicatglas mit weniger als 1 % Alkalioxiden (w/w), das hauptsächlich für glasfaserverstärkte Kunststoffe verwendet wird. Andere gebräuchliche Gläser mit hohem Borgehalt sind C-Glas, ein Alkali-Kalk-Glas mit hohem Boroxid-Gehalt, das für Glasstapelfasern und Isolierungen verwendet wird, und D-Glas, ein Borosilikatglas, das seinen Namen von seiner niedrigen Dielektrizitätskonstante hat). ⓘ
Nicht alle Glasfasern enthalten Bor, aber auf globaler Ebene enthalten die meisten der verwendeten Glasfasern Bor. Aufgrund der allgegenwärtigen Verwendung von Glasfasern im Bauwesen und bei der Isolierung verbrauchen borhaltige Glasfasern die Hälfte der weltweiten Borproduktion und stellen den größten Einzelmarkt für Bor dar. ⓘ
Borosilikatglas

Borosilikatglas, das in der Regel aus 12-15 % B2O3, 80 % SiO2 und 2 % Al2O3 besteht, hat einen niedrigen Wärmeausdehnungskoeffizienten und ist daher gut gegen Temperaturschocks geschützt. Duran" von der Schott AG und Pyrex von Owens-Corning sind zwei wichtige Markennamen für dieses Glas, das vor allem wegen seiner Widerstandsfähigkeit sowohl für Laborglas als auch für Koch- und Backgeschirr verwendet wird. ⓘ
Borkarbid-Keramik
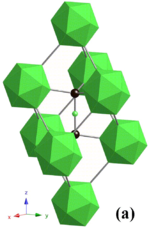
Mehrere Borverbindungen sind für ihre extreme Härte und Zähigkeit bekannt. Borkarbid ist ein keramisches Material, das durch Zersetzung von B2O3 mit Kohlenstoff in einem Elektroofen gewonnen wird:
- 2 B2O3 + 7 C → B4C + 6 CO ⓘ
Die Struktur von Borkarbid ist nur annähernd B4C, und es zeigt eine deutliche Verarmung des Kohlenstoffs gegenüber diesem vorgeschlagenen stöchiometrischen Verhältnis. Dies ist auf seine sehr komplexe Struktur zurückzuführen. Die Substanz kann mit der empirischen Formel B12C3 gesehen werden (d. h. mit B12-Dodekaedern als Motiv), aber mit weniger Kohlenstoff, da die vorgeschlagenen C3-Einheiten durch C-B-C-Ketten ersetzt werden und auch einige kleinere (B6) Oktaeder vorhanden sind (siehe den Artikel über Borkarbid zur Strukturanalyse). Das sich wiederholende Polymer und die teilkristalline Struktur von Borkarbid verleihen ihm eine hohe strukturelle Festigkeit pro Gewicht. Es wird in Panzerungen, kugelsicheren Westen und zahlreichen anderen strukturellen Anwendungen eingesetzt. ⓘ
Die Fähigkeit von Borkarbid, Neutronen zu absorbieren, ohne langlebige Radionuklide zu bilden (vor allem, wenn es mit zusätzlichem Bor-10 dotiert ist), macht das Material als Absorptionsmittel für Neutronenstrahlung, die in Kernkraftwerken entsteht, attraktiv. Zu den nuklearen Anwendungen von Borkarbid gehören Abschirmungen, Steuerstäbe und Abschaltpellets. In Steuerstäben wird Borkarbid häufig pulverisiert, um seine Oberfläche zu vergrößern. ⓘ
Hohe Härte und abrasive Verbindungen
| Werkstoff | Diamant | kubisch-BC2N | kubisch-BC5 | kubisch-BN | B4C | ReB2 ⓘ |
|---|---|---|---|---|---|---|
| Vickers-Härte (GPa) | 115 | 76 | 71 | 62 | 38 | 22 |
| Bruchzähigkeit (MPa m1⁄2) | 5.3 | 4.5 | 9.5 | 6.8 | 3.5 |
Borkarbid- und kubisches Bornitridpulver werden häufig als Schleifmittel verwendet. Bornitrid ist ein Material, das isoelektronisch zu Kohlenstoff ist. Ähnlich wie Kohlenstoff hat es sowohl hexagonale (weiches, graphitähnliches h-BN) als auch kubische (hartes, diamantähnliches c-BN) Formen. h-BN wird als Hochtemperaturkomponente und Schmiermittel verwendet. c-BN, auch unter dem Handelsnamen Borazon bekannt, ist ein hervorragendes Schleifmittel. Seine Härte ist nur geringfügig kleiner als die von Diamant, aber seine chemische Stabilität ist besser als die von Diamant. Heterodiamant (auch BCN genannt) ist eine weitere diamantähnliche Borverbindung. ⓘ
Metallurgie
Bor wird Borstählen in einer Menge von einigen Teilen pro Million zugesetzt, um die Härtbarkeit zu erhöhen. Höhere Prozentsätze werden Stählen zugesetzt, die in der Nuklearindustrie verwendet werden, da Bor Neutronen absorbieren kann. ⓘ
Bor kann auch die Oberflächenhärte von Stählen und Legierungen durch Borieren erhöhen. Außerdem werden Metallboride zur Beschichtung von Werkzeugen durch chemische oder physikalische Gasphasenabscheidung verwendet. Die Implantation von Bor-Ionen in Metalle und Legierungen durch Ionenimplantation oder Ionenstrahlabscheidung führt zu einer spektakulären Erhöhung der Oberflächenbeständigkeit und Mikrohärte. Auch das Laserlegieren wurde für den gleichen Zweck erfolgreich eingesetzt. Diese Boride sind eine Alternative zu diamantbeschichteten Werkzeugen, und ihre (behandelten) Oberflächen haben ähnliche Eigenschaften wie die des Massenborids. ⓘ
Rheniumdiborid zum Beispiel kann bei Umgebungsdruck hergestellt werden, ist aber wegen des Rheniums recht teuer. Die Härte von ReB2 weist aufgrund seiner hexagonalen Schichtstruktur eine erhebliche Anisotropie auf. Sie ist vergleichbar mit der von Wolframcarbid, Siliciumcarbid, Titandiborid oder Zirkoniumdiborid. Auch AlMgB14 + TiB2-Verbundwerkstoffe weisen eine hohe Härte und Verschleißfestigkeit auf und werden entweder in loser Form oder als Beschichtung für Bauteile verwendet, die hohen Temperaturen und Verschleißbelastungen ausgesetzt sind. ⓘ
Waschmittelformulierungen und Bleichmittel
Borax wird in verschiedenen Haushaltswasch- und -reinigungsmitteln verwendet, z. B. im "20 Mule Team Borax"-Waschmittelverstärker und in der pulverförmigen Handseife "Boraxo". Es ist auch in einigen Zahnbleichmitteln enthalten. ⓘ
Natriumperborat dient als Aktivsauerstoffquelle in vielen Waschmitteln, Reinigungsmitteln und Bleichmitteln. Trotz seines Namens enthält das Waschmittel "Borateem" jedoch keine Borverbindungen mehr und verwendet stattdessen Natriumpercarbonat als Bleichmittel. ⓘ
Insektizide
Borsäure wird als Insektizid eingesetzt, vor allem gegen Ameisen, Flöhe und Schaben. ⓘ
Halbleiter
Bor ist ein nützlicher Dotierstoff für Halbleiter wie Silizium, Germanium und Siliziumkarbid. Da es ein Valenzelektron weniger hat als das Wirtsatom, spendet es ein Loch, was zu einer p-Leitfähigkeit führt. Die traditionelle Methode, Bor in Halbleiter einzubringen, ist die atomare Diffusion bei hohen Temperaturen. Bei diesem Verfahren werden entweder feste (B2O3), flüssige (BBr3) oder gasförmige Borquellen (B2H6 oder BF3) verwendet. Nach den 1970er Jahren wurde es jedoch größtenteils durch die Ionenimplantation ersetzt, bei der hauptsächlich BF3 als Borquelle verwendet wird. Bortrichloridgas ist ebenfalls eine wichtige Chemikalie in der Halbleiterindustrie, allerdings nicht zur Dotierung, sondern zum Plasmaätzen von Metallen und deren Oxiden. Triethylboran wird auch in Aufdampfungsreaktoren als Borquelle eingesetzt. Beispiele sind die Plasmabeschichtung von borhaltigen Hartkohlenstoffschichten, Siliziumnitrid-Bornitrid-Schichten und die Dotierung von Diamantschichten mit Bor. ⓘ
Magnete
Bor ist ein Bestandteil von Neodym-Magneten (Nd2Fe14B), die zu den stärksten Dauermagneten gehören. Diese Magnete finden sich in einer Vielzahl von elektromechanischen und elektronischen Geräten, wie z. B. in medizinischen Bildgebungssystemen mit Magnetresonanztomographie (MRT), in kompakten und relativ kleinen Motoren und Aktuatoren. In Computer-Festplattenlaufwerken (HDD), CD- (Compact Disk) und DVD-Playern (Digital Versatile Disk) beispielsweise werden Neodym-Magnetmotoren eingesetzt, um eine starke Drehkraft in einem bemerkenswert kompakten Gehäuse zu erzeugen. In Mobiltelefonen sorgen "Neo"-Magnete für das Magnetfeld, das es winzigen Lautsprechern ermöglicht, eine beachtliche Audioleistung zu liefern. ⓘ
Abschirmung und Neutronenabsorber in Kernreaktoren
Die Borabschirmung wird zur Kontrolle von Kernreaktoren eingesetzt, wobei der hohe Wirkungsquerschnitt für den Neutroneneinfang genutzt wird. ⓘ
In Druckwasserreaktoren wird eine variable Konzentration von Borsäure im Kühlwasser als Neutronengift verwendet, um die variable Reaktivität des Brennstoffs zu kompensieren. Beim Einsetzen neuer Brennstäbe ist die Borsäurekonzentration maximal und wird im Laufe der Lebensdauer reduziert. ⓘ
Andere nicht-medizinische Verwendungen
- Wegen seiner charakteristischen grünen Flamme wird amorphes Bor in pyrotechnischen Fackeln verwendet.
- Klebstoffe auf Stärke- und Kaseinbasis enthalten Natriumtetraboratdecahydrat (Na2B4O7-10 H2O)
- Einige Korrosionsschutzsysteme enthalten Borax.
- Natriumborate werden als Flussmittel zum Löten von Silber und Gold und zusammen mit Ammoniumchlorid zum Schweißen von Eisenmetallen verwendet. Sie sind auch feuerhemmende Zusatzstoffe für Kunststoffe und Gummiartikel.
- Borsäure (auch bekannt als Orthoborsäure) H3BO3 wird bei der Herstellung von Textilglas und Flachbildschirmen sowie in vielen PVAc- und PVOH-basierten Klebstoffen verwendet.
- Triethylboran ist eine Substanz, die den JP-7-Treibstoff der Pratt & Whitney J58-Turbostrahltriebwerke zündet, die den Lockheed SR-71 Blackbird antreiben. Es wurde auch zur Zündung der F-1-Triebwerke der Saturn-V-Rakete verwendet, die von 1967 bis 1973 im Rahmen der Apollo- und Skylab-Programme der NASA eingesetzt wurde. Heute verwendet SpaceX es für die Zündung der Triebwerke seiner Falcon 9-Rakete. Triethylboran eignet sich hierfür aufgrund seiner pyrophoren Eigenschaften, insbesondere der Tatsache, dass es mit einer sehr hohen Temperatur verbrennt. Triethylboran wird in der Industrie als Initiator für Radikalreaktionen verwendet, wo es auch bei niedrigen Temperaturen wirksam ist.
- Borate werden als umweltverträgliche Holzschutzmittel verwendet. ⓘ
Pharmazeutische und biologische Anwendungen
Borsäure hat antiseptische, antimykotische und antivirale Eigenschaften und wird aus diesen Gründen als Wasserklärer in der Schwimmbadwasseraufbereitung eingesetzt. Milde Lösungen von Borsäure wurden als Augenantiseptika verwendet. ⓘ
Bortezomib (vermarktet als Velcade und Cytomib). Bor ist ein aktiver Bestandteil des organischen Arzneimittels Bortezomib, einer neuen Klasse von Medikamenten, die als Proteasom-Inhibitoren bezeichnet werden und zur Behandlung von Myelomen und einer Form von Lymphomen eingesetzt werden (derzeit laufen Versuche zur Behandlung anderer Lymphomarten). Das Boratom in Bortezomib bindet mit hoher Affinität und Spezifität an die katalytische Stelle des 26S-Proteasoms.
- Eine Reihe potenzieller borhaltiger Arzneimittel, die Bor-10 enthalten, wurden für den Einsatz in der Borneutroneneinfangtherapie (BNCT) hergestellt.
- Einige Borverbindungen sind bei der Behandlung von Arthritis vielversprechend, obwohl bisher noch keine für diesen Zweck allgemein zugelassen wurde. ⓘ
Tavaborol (vermarktet als Kerydin) ist ein Aminoacyl-tRNA-Synthetase-Hemmer, der zur Behandlung von Zehennagelpilz eingesetzt wird. Es wurde im Juli 2014 von der FDA zugelassen. ⓘ
Die Dioxaborolan-Chemie ermöglicht die Markierung von Antikörpern oder roten Blutkörperchen mit radioaktivem Fluorid (18F), was die Positronen-Emissions-Tomographie (PET) zur Darstellung von Krebs bzw. Blutungen ermöglicht. Ein vom Menschen abgeleitetes, genetisches, Positronen emittierendes und fluoreszierendes (HD-GPF) Reportersystem verwendet ein menschliches, nicht immunogenes Protein, PSMA, und ein kleines Molekül, das Positronen emittiert (borgebundenes 18F) und fluoresziert, für die duale Modalität PET und fluoreszierende Bildgebung von genomveränderten Zellen, z. B. Krebs, CRISPR/Cas9 oder CAR-T-Zellen, in einer ganzen Maus. Das dualmodale kleine Molekül, das auf PSMA abzielt, wurde am Menschen getestet und ermöglichte die Lokalisierung von primärem und metastasierendem Prostatakrebs, die fluoreszenzgesteuerte Entfernung von Krebs und den Nachweis einzelner Krebszellen in Geweberändern. ⓘ
Da die Borversorgung über die Nahrung und das Trinkwasser in der Regel ausreichend ist und ein zusätzlicher Nutzen von borhaltigen Nahrungsergänzungsmitteln unbelegt ist, wird angesichts der möglichen Risiken von deren Verwendung abgeraten. ⓘ
Forschungsgebiete
Magnesiumdiborid ist ein wichtiges supraleitendes Material mit einer Übergangstemperatur von 39 K. MgB2-Drähte werden mit dem Pulver-in-Rohr-Verfahren hergestellt und in supraleitenden Magneten eingesetzt. ⓘ
Amorphes Bor wird als Schmelzpunkterniedriger in Nickel-Chrom-Lötlegierungen verwendet. ⓘ
Hexagonales Bornitrid bildet atomar dünne Schichten, die zur Verbesserung der Elektronenbeweglichkeit in Graphen-Bauelementen verwendet wurden. Außerdem bildet es nanoröhrenförmige Strukturen (BNNTs), die unter anderem eine hohe Festigkeit, eine hohe chemische Stabilität und eine hohe Wärmeleitfähigkeit aufweisen. ⓘ
Biologische Rolle
Bor ist ein essentieller Pflanzennährstoff, der vor allem für die Aufrechterhaltung der Integrität der Zellwände benötigt wird. Hohe Bodenkonzentrationen von mehr als 1,0 ppm führen jedoch zu Rand- und Spitzennekrosen in den Blättern sowie zu einer schlechten allgemeinen Wachstumsleistung. Bei Pflanzen, die besonders empfindlich auf Bor im Boden reagieren, führen bereits Werte von 0,8 ppm zu den gleichen Symptomen. Nahezu alle Pflanzen, auch solche, die gegenüber Bor im Boden einigermaßen tolerant sind, zeigen zumindest einige Symptome der Bortoxizität, wenn der Borgehalt im Boden mehr als 1,8 ppm beträgt. Bei einem Borgehalt von mehr als 2,0 ppm sind nur noch wenige Pflanzen leistungsfähig, und einige überleben möglicherweise nicht. ⓘ
Man geht davon aus, dass Bor bei Tieren, einschließlich des Menschen, mehrere wichtige Funktionen erfüllt, aber die genaue physiologische Rolle ist kaum bekannt. In einer kleinen, 1987 veröffentlichten Studie am Menschen wurde über postmenopausale Frauen berichtet, die zunächst einen Bormangel erlitten und dann mit 3 mg/Tag aufgefüllt wurden. Die Borsupplementierung verringerte die Kalziumausscheidung im Urin deutlich und erhöhte die Serumkonzentrationen von 17 Beta-Estradiol und Testosteron. ⓘ
Das U.S. Institute of Medicine hat nicht bestätigt, dass Bor ein essentieller Nährstoff für den Menschen ist, so dass weder eine empfohlene Tagesdosis (Recommended Dietary Allowance, RDA) noch eine angemessene Zufuhr festgelegt wurden. Die Nahrungsaufnahme von Erwachsenen wird auf 0,9 bis 1,4 mg/Tag geschätzt, wobei etwa 90 % absorbiert werden. Was absorbiert wird, wird größtenteils mit dem Urin ausgeschieden. Die zulässige obere Aufnahmemenge für Erwachsene beträgt 20 mg/Tag. ⓘ
Im Jahr 2013 wurde eine Hypothese aufgestellt, die besagt, dass Bor und Molybdän die Produktion von RNA auf dem Mars katalysiert haben könnten, als das Leben vor etwa 3 Milliarden Jahren über einen Meteoriten auf die Erde gelangte. ⓘ
Es gibt mehrere bekannte borhaltige natürliche Antibiotika. Das erste, das gefunden wurde, war Boromycin, das aus Streptomyces isoliert wurde. ⓘ
Die kongenitale endotheliale Dystrophie Typ 2, eine seltene Form der Hornhautdystrophie, ist mit Mutationen im SLC4A11-Gen verbunden, das für einen Transporter kodiert, der angeblich die intrazelluläre Konzentration von Bor reguliert. ⓘ
Bor ist möglicherweise ein essentielles Spurenelement, das unter anderem positiven Einfluss auf Knochenstoffwechsel und Gehirnfunktion hat. ⓘ
Menschen nehmen Bor über Trinkwasser und Nahrung auf. Im Körper liegt ein Gehalt von etwa 0,7 ppm vor. Die World Health Organization (WHO) stellte 1998 in einer Studie fest, dass weltweit von einer durchschnittlichen Aufnahme von 1–2 mg Bor pro Tag ausgegangen werden kann, und empfiehlt einen Richtwert (Guideline value) von 2,4 mg/l Trinkwasser. ⓘ
Analytische Quantifizierung
Bor lässt sich in der analytischen Chemie mit der Curcumin-Methode quantitativ in Form des rot gefärbten Komplexes Rosocyanin, bzw. unter zusätzlicher Verwendung von Oxalsäure durch die Farbreaktion zu Rubrocurcumin nachweisen. Hierzu wird eine Probe des Bor-haltigen Materials oxidativ aufgeschlossen. Die durch den Aufschluss gebildete Borsäure kann anschließend kolorimetrisch bestimmt werden. ⓘ
Gesundheitliche Probleme und Toxizität
| Gefahren | |
|---|---|
| GHS-Kennzeichnung: | |
Piktogramme
|

|
Signalwort
|
Warnhinweis |
Gefahrenhinweise
|
H302, H412 |
Sicherheitshinweise
|
P264, P270, P273, P301+P312, P501 |
| NFPA 704 (Feuerdiamant) | |
Elementares Bor, Boroxid, Borsäure, Borate und viele Organoborverbindungen sind für Menschen und Tiere relativ ungiftig (mit einer Toxizität ähnlich der von Kochsalz). Die LD50 (Dosis, bei der 50 % der Tiere sterben) liegt bei etwa 6 g pro kg Körpergewicht. Stoffe mit einer LD50 über 2 g/kg gelten als ungiftig. Eine Aufnahme von 4 g Borsäure pro Tag wurde ohne Zwischenfälle berichtet, aber mehr als diese Menge wird in mehr als nur einigen Dosen als toxisch angesehen. Eine Aufnahme von mehr als 0,5 g pro Tag über 50 Tage verursacht leichte Verdauungsprobleme und andere Probleme, die auf eine Toxizität hindeuten. Eine Nahrungsergänzung mit Bor kann für das Knochenwachstum, die Wundheilung und die antioxidative Wirkung hilfreich sein, und eine unzureichende Bormenge in der Nahrung kann zu einem Bormangel führen. ⓘ
Medizinische Einzeldosen von 20 g Borsäure für die Neutroneneinfangtherapie wurden ohne übermäßige Toxizität verwendet. ⓘ
Borsäure ist für Insekten giftiger als für Säugetiere und wird daher routinemäßig als Insektizid eingesetzt. ⓘ
Die Borane (Borwasserstoffverbindungen) und ähnliche gasförmige Verbindungen sind ziemlich giftig. Wie üblich ist Bor kein Element, das an sich giftig ist, aber die Toxizität dieser Verbindungen hängt von der Struktur ab (ein weiteres Beispiel für dieses Phänomen ist Phosphin). Die Borane sind außerdem leicht entzündlich und erfordern besondere Vorsicht bei der Handhabung; einige Kombinationen aus Boranen und anderen Verbindungen sind hochexplosiv. Natriumborhydrid ist aufgrund seines reduzierenden Charakters und der Freisetzung von Wasserstoff bei Kontakt mit Säure brandgefährlich. Borhalogenide sind ätzend. ⓘ

Bor ist für das Pflanzenwachstum notwendig, aber ein Überschuss an Bor ist für Pflanzen giftig und tritt besonders in sauren Böden auf. Er äußert sich in einer Vergilbung der ältesten Blätter von der Spitze nach innen und in schwarzen Flecken auf Gerstenblättern, kann aber auch mit anderen Stressfaktoren wie Magnesiummangel bei anderen Pflanzen verwechselt werden. ⓘ
Vorkommen
Wie die beiden im Periodensystem vorangehenden Elemente Lithium und Beryllium ist auch Bor ein im Sonnensystem auffallend seltenes Element. Die Seltenheit dieser drei Elemente erklärt sich daraus, dass sie keine Produkte der stellaren Kernfusionen sind, die zur Elemententstehung (Nukleosynthese) führen. Das Wasserstoffbrennen führt zu Heliumatomen, das darauffolgende Heliumbrennen (der Drei-Alpha-Prozess) schon zu Kohlenstoffatomen. Bor entsteht ausschließlich bei der Spallation schwerer Atomkerne durch kosmische Strahlung. ⓘ
Bor kommt auf der Erde nur in sauerstoffhaltigen Verbindungen vor. Große Lagerstätten befinden sich in Bigadiç, einem Landkreis der Provinz Balıkesir im Westen der Türkei. Die größten Boratminen befinden sich bei Boron (Kalifornien) (die Kramer-Lagerstätte) und in Kırka (Türkei). Abgebaut werden die Mineralien Borax, Kernit und Colemanit. In der Türkei sind 70 % der abgebauten Erze Colemanit und werden für die Herstellung von hitzeresistentem Glas verwendet. Weitere Vorkommen gibt es in der Mojave-Wüste in den USA, sowie in den Anden und alpinen Regionen im südlichen Eurasien. Staßfurter Kalisalze enthalten geringe Mengen vergesellschafteten Boracit. ⓘ
Die weltweiten Abbaumengen betrugen im Jahr 2005 geschätzt 4.910.000 t Bortrioxid Seit dem Jahr 2007 veröffentlichen die USA ihre Abbaumengen nicht mehr, da sie ein Geschäftsgeheimnis darstellen. Die globalen Abbaumengen verteilen sich, wie folgt:
| Land | 2005 als B2O3 | 2019 | 2020 | Reserven ⓘ |
|---|---|---|---|---|
| Abbau (in Tonnen) | ||||
| 1.150.000 | nicht veröffentlicht | nicht veröffentlicht | 40.000.000 | |
| 820.000 | 71.000 (Roherz) | 71.000 (Roherz) | n. bek. | |
| 68.000 | 200.000 (Ulexit) | 200.000 (Ulexit) | n. bek. | |
| 590.000 | 400.000 (Ulexit) | 350.000 (Ulexit) | 35.000.000 | |
| 140.000 | 250.000 (B2O3-Equivalent) | 380.000 (B2O3-Equivalent) | 24.000.000 | |
| 120.000 (Borverbindungen) | 120.000 (Borverbindungen) | n. bek. | ||
| 3.000 | n.bek. | |||
| 30.000 | n.bek. | |||
| 9.000 | 111.000 (Rohborate) | 110.000 (Rohborate) | 4.000.000 | |
| 400.000 | 80.000 (Datolitherz) | 80.000 (Datolitherz) | 40.000.000 | |
| 1.700.000 | 2.400.000 (raffinierte Borate) | 2.000.000 (raffinierte Borate) | 1.200.000.000 | |
| Gesamt (gerundet) | 4.910.000 | n.bek. | n.bek. | n.bek. |
In Wasser kommt Bor überwiegend als undissoziierte Borsäure vor. ⓘ
Bor kommt im Meerwasser in einer Konzentration von 4–5 mg/l vor. In Meeresluft wurden 0,17 μg/m3 gemessen (WHO, 1996). ⓘ
In Mineralwässern wurden durchschnittlich 500 μg/l Bor gemessen, mit einem Wertespektrum zwischen weniger als 20 μg/l und 3,23 mg/l. ⓘ
Der Gehalt im Grundwasser sowie in Binnengewässern liegt in Deutschland im Bereich von 10 bis 50 μg/l, wobei in Baden-Württemberg von einem Hintergrundwert (ohne anthropogene Beeinflussung) im Grundwasser von 50 μg/l ausgegangen wird. ⓘ
In der Außenluft sind in Deutschland im Durchschnitt 16 ng/m³ und im Trinkwasser Werte von 10 bis 210 μg/l gemessen worden. Im Boden liegt die Konzentration an Borax zwischen 88 und 177 mg/kg bezogen auf das Trockengewicht. ⓘ
In der Schweiz wird von natürlichen Borgehalten im Flusswasser von rund 10 μg/l und im Grundwasser von bis zu 40 μg/l ausgegangen, während die tatsächlichen Werte in Flüssen und Seen bis über 200 μg/l betragen können und das Trinkwasser durchschnittlich rund 20 μg/l und höchstens 60 μg/l Bor enthält. ⓘ
Pflanzen benötigen Bor und der Gehalt in der Trockenmasse beträgt 30–75 ppm. Menschen nehmen Bor über Trinkwasser und Nahrung auf. Im Körper liegt ein Gehalt von etwa 0,7 ppm vor. ⓘ
Gewinnung und Darstellung
Amorphes Bor wird durch die Reduktion von Bortrioxid, B2O3, mit Magnesiumpulver hergestellt:
Derartig gewonnenes Bor besitzt nach Abtrennen der Beimengungen eine Reinheit von 98 %. Die Reinheit des Stoffes kann erhöht werden, indem das Bor als Reinstoff aus einer Platinschmelze bei 800–1200 °C auskristallisiert wird. ⓘ
Kristallines Bor lässt sich auch durch andere Verfahren darstellen: Das Element lässt sich meist aus seinen Halogeniden als Reinstoff gewinnen. Mittels eines 1000–1400 °C heißen Wolfram- oder Tantaldrahts kann durch Reduktion von Bortrichlorid oder Bortribromid mit Wasserstoff das Element in sehr hoher Reinheit dargestellt werden. Um Bortrifluorid mit Wasserstoff zu reduzieren, wären Reaktionstemperaturen von 2000 °C erforderlich, sodass diese Verbindung nicht als Ausgangsstoff zur Darstellung genutzt wird.
Eine weitere Möglichkeit stellt die thermische Zersetzung von Diboran bei 600–800 °C bzw. von Bortriiodid bei 800–1000 °C an einer Tantal-, Wolfram- oder Bornitrid-Oberfläche dar.
- Fehler beim Parsen (Syntaxfehler): {\displaystyle \ce{2BI3 -> 2B + 3I2 <span title="Aus: Deutsche Wikipedia, Abschnitt "Gewinnung und Darstellung"" class="plainlinks">[https://de.wikipedia.org/wiki/Bor#Gewinnung_und_Darstellung <span style="color:#dddddd">ⓘ</span>]</span>}}
Eigenschaften

Physikalische Eigenschaften
Wegen der hohen Ionisierungsenergie sind von Bor keine B3+-Kationen bekannt. Die komplizierten Strukturen in vielen Borverbindungen und deren Eigenschaften zeigen, dass die Beschreibung der Bindungsverhältnisse als kovalent, metallisch oder ionisch stark vereinfachend sind und durch einen Molekülorbital(MO)-Ansatz ersetzt werden müssen. ⓘ
Die Elektronenkonfiguration 1s22s22p1 des Bors zeigt, dass nur die drei Elektronen der zweiten Schale für die Ausbildung von kovalenten Bindungen mit s-, px-, py- und pz-Orbitalen zur Verfügung stehen. Dieser Elektronenmangel wird durch Ausbildung von Mehrzentrenbindungen, insbesondere einer Dreizentrenbindung, und Elektronenakzeptorverhalten (Lewis-Acidität) kompensiert. Es ist gelungen, eine Borverbindung mit einer Bor-Bor-Dreifachbindung herzustellen. ⓘ
Bor ist durchlässig für Infrarotlicht. Bei Raumtemperatur zeigt es eine geringe elektrische Leitfähigkeit, die bei höheren Temperaturen stark ansteigt. ⓘ
Bor besitzt die höchste Zugfestigkeit aller bekannten Elemente sowie die zweithöchste Härte, nur übertroffen von der Kohlenstoffmodifikation Diamant. Bormodifikationen haben physikalische und chemische Ähnlichkeit mit Hartkeramiken wie Siliciumcarbid oder Wolframcarbid. ⓘ
Chemische Eigenschaften
Bis 400 °C ist Bor reaktionsträge, bei höheren Temperaturen wird es zu einem starken Reduktionsmittel. Bei Temperaturen über 700 °C verbrennt es in Luft zu Bortrioxid B2O3. Von siedender Salz- und Fluorwasserstoffsäure wird Bor nicht angegriffen. Oxidierend wirkende, konzentrierte Schwefelsäure greift Bor erst bei Temperaturen über 200 °C an, konzentrierte Phosphorsäure hingegen erst bei Temperaturen über 600 °C. ⓘ
Löst man B2O3 in Wasser, so entsteht die sehr schwache Borsäure. Deren flüchtige Ester, am deutlichsten Borsäuretrimethylester, färben Flammen kräftig grün. ⓘ
Die Fähigkeit des Bors, über kovalente Bindungen stabile räumliche Netzwerke auszubilden, sind ein weiterer Hinweis auf die chemische Ähnlichkeit des Bors mit seinen Periodennachbarn Kohlenstoff und Silicium. ⓘ
Eine wichtige Forschungsdisziplin der heutigen anorganischen Chemie ist die der Verbindungen des Bors mit Wasserstoff (Borane) sowie mit Wasserstoff und Stickstoff, die den Kohlenwasserstoffen ähneln (isoelektronisch), z. B. Borazol B3N3H6 („anorganisches Benzol“). Eine Reihe organischer Borverbindungen sind bekannt, beispielsweise Boronsäuren. ⓘ
Verwendung
Die wirtschaftlich wichtigste Verbindung ist Borax (Natriumtetraborat-Decahydrat, Na2B4O7 · 10 H2O) zur Herstellung von Isolier- und Dämmstoffen sowie Bleichstoffen (Perborate). Weitere Anwendungen: ⓘ
Elementares Bor
- Additiv für Raketentreibstoffe
- Ferrobor und Bor als Legierungszusatz für Feinkornbaustähle und Nickelbasislegierungen
- Reduktionsmittel bei der Herstellung von reinem Kupfer, um Sauerstoff zu entfernen
- Bor als Kornfeinungsmittel für Messing-Gusslegierungen
- Bor-Nitrat-Gemische als Zünder für Airbags
- Kristallines Bor und Borfasern für Anwendungen mit extrem hoher Festigkeit und Steifigkeit: Bauteile für Helikopterrotoren, Tennisrackets, Golfschläger, Angelruten, Panzerungen und schusssichere Westen; wegen des geringen Radarechos findet es Verwendung in den Stealth-Kampfflugzeugen F-117 und B-2.
- Feuerwerksartikel und Leuchtspurmunition (wegen intensiv grüner Flamme)
- p-Dotierung in Silicium
- Thermochemische Randschichthärtung, siehe Borieren
- Nadelträger bei sehr hochwertigen Tonabnehmersystemen von Plattenspielern, als Ersatz für Aluminium
- Die Kernfusion von 11B-Atomkernen mit Protonen wäre eine – technisch noch sehr ferne – Möglichkeit zur Energiegewinnung. ⓘ
Borverbindungen
- Waschmittel (Perborate)
- Lichtwellenleiter
- Organische Synthesen
- Feuerfestes Borosilikatglas
- Glasfritten
- Keramikglasuren
- Pflanzenschutzmittel
- Schleifmittel und Schneidstoff zur Bearbeitung von Stahl (Borcarbid, Bornitrid); weitere Anwendungen siehe dort
- Neodym-Eisen-Borverbindungen zur Herstellung stärkster Magnete. Sie werden genutzt für Kernspintomographen, Mikromotoren und Festplatten (Positionierung der Schreib-/Leseköpfe), Dauermagnet-Rotoren (z. B. Schritt- und Servomotoren), Linearmotoren für Positionierachsen, hochwertige Lautsprecher und Kopfhörer. Gegenüber den Cobalt-Samarium-Magneten sind sie wesentlich preiswerter.
- Abtastnadelträger bei hochwertigen Tonabnehmern für Schallplatten
- Brems- und Kupplungsbeläge
- Panzerungen, kugelsichere Westen
- Nuklearanwendungen von Borverbindungen, meist Borcarbid B4C:
- Neutronenabschirmung aufgrund des sehr hohen Wirkungsquerschnitts für thermische Neutronen bei der Kernreaktion 10B(n,)7Li (3837 Barn); für Bor mit natürlicher Isotopenzusammensetzung gelten demnach 764 Barn. Borverbindungen werden deshalb Strahlenschutzkleidung und -wänden, Stählen für Lagergefäße von Kernbrennstoffen und der dem Strahlenschutz dienenden Betonhülle hinzugefügt.
- Steuerstäbe zur Regelung und zum Abschalten der Kettenreaktion in Kernreaktoren.
- Bei Druckwasserreaktoren wird dafür dem Kühlwasser eine variable Menge von Borsäure zugemischt.
- Detektion von Neutronen auf Basis der gleichen Reaktion
- Neutronenquelle durch die Kernreaktion 11B(,n)14N
- Neutronenabschirmung aufgrund des sehr hohen Wirkungsquerschnitts für thermische Neutronen bei der Kernreaktion 10B(n,)7Li (3837 Barn); für Bor mit natürlicher Isotopenzusammensetzung gelten demnach 764 Barn. Borverbindungen werden deshalb Strahlenschutzkleidung und -wänden, Stählen für Lagergefäße von Kernbrennstoffen und der dem Strahlenschutz dienenden Betonhülle hinzugefügt.
- Flussmittel zum Löten (Borsäure)
- Boraxperle als grobe chemische Analysemethode für Metallionen
- Kühlschmierstoffe in der Zerspanung
- Holzschutzmittel (wegen geringer Giftigkeit)
- Flammschutzmittel für Platinen
- Kosmetikindustrie
- Düngemittel
- Borane
- Diboran
- Boroxin Herstellung von Elektrolyten
- Boride
- Bornitrid
- Borhalogenide
- Nachweis von niederen Alkoholen mit Borsäure (s. Borsäuretrimethylester)
- BNCT (Boron Neutron Capture Therapy)
- Magnesiumdiborid (MgB2)
- Rheniumdiborid (ReB2) ist ein Feststoff härter als Diamant
- Strontiumborid (SrB6)wird in Steuerstäben für Kernreaktoren eingesetzt
- Lanthanhexaborid (LaB6) wird in hochergiebigen Kathoden als Elektronenemitter genutzt ⓘ
Sicherheitshinweise
Elementares Bor ist in geringen Dosen nicht giftig. Für Bor gibt es keine Hinweise auf genotoxische oder kanzerogene Wirkungen; von der Deutschen Gesellschaft für Ernährung ist kein Referenzwert für Bor als Zufuhrempfehlung aufgeführt. ⓘ
Dosen über 100 mg/Tag können jedoch Vergiftungserscheinungen hervorrufen. Die US-amerikanische Behörde EPA gibt einen täglichen Grenzwert (RfD – Reference Dose) von 0,2 mg pro Kilogramm Körpergewicht für Bor und Borate an, geht jedoch nicht von einer Karzinogenität aus. ⓘ
Bortrioxid, Borsäure und Borate werden mit der 30. ATP in der EU seit Sommer 2009 als fortpflanzungsgefährdend eingestuft. Bei Borsäure und Borax wurde dieser Effekt bislang jedoch lediglich bei der Verabreichung von höheren Dosen an Mäuse beobachtet. ⓘ
Einige Borverbindungen wie die Borane (Borwasserstoffverbindungen) sind hochgradig toxisch und müssen mit größter Sorgfalt gehandhabt werden. ⓘ








