Kohlenstoff
 Graphit (links) und Diamant (rechts), zwei Allotrope des Kohlenstoffs | ||||||||||||||||||||||||||
| Kohlenstoff | ||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allotrope | Graphit, Diamant und mehr (siehe Allotrope des Kohlenstoffs) | |||||||||||||||||||||||||
| Erscheinungsbild |
| |||||||||||||||||||||||||
| Standard-Atomgewicht Ar°(C) |
| |||||||||||||||||||||||||
| Kohlenstoff im Periodensystem | ||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
| Ordnungszahl (Z) | 6 | |||||||||||||||||||||||||
| Gruppe | Gruppe 14 (Kohlenstoffgruppe) | |||||||||||||||||||||||||
| Periode | Periode 2 | |||||||||||||||||||||||||
| Block | p-Block | |||||||||||||||||||||||||
| Elektronen-Konfiguration | [[[Helium|He]]] 2s2 2p2 | |||||||||||||||||||||||||
| Elektronen pro Schale | 2, 4 | |||||||||||||||||||||||||
| Physikalische Eigenschaften | ||||||||||||||||||||||||||
| Phase bei STP | fest | |||||||||||||||||||||||||
| Sublimationspunkt | 3915 K (3642 °C, 6588 °F) | |||||||||||||||||||||||||
| Dichte (nahe r.t.) | amorph: 1,8-2,1 g/cm3 Graphit: 2,267 g/cm3 Diamant: 3,515 g/cm3 | |||||||||||||||||||||||||
| Tripelpunkt | 4600 K, 10.800 kPa | |||||||||||||||||||||||||
| Schmelzwärme | Graphit: 117 kJ/mol | |||||||||||||||||||||||||
| Molare Wärmekapazität | Graphit: 8,517 J/(mol-K) Diamant: 6,155 J/(mol-K) | |||||||||||||||||||||||||
| Atomare Eigenschaften | ||||||||||||||||||||||||||
| Oxidationsstufen | -4, -3, -2, -1, 0, +1, +2, +3, +4 (ein leicht saures Oxid) | |||||||||||||||||||||||||
| Elektronegativität | Pauling-Skala: 2,55 | |||||||||||||||||||||||||
| Ionisierungsenergien |
| |||||||||||||||||||||||||
| Kovalenter Radius | sp3: 77 pm sp2: 73 pm sp: 69 pm | |||||||||||||||||||||||||
| Van-der-Waals-Radius | 170 pm | |||||||||||||||||||||||||
| Spektrallinien von Kohlenstoff | ||||||||||||||||||||||||||
| Andere Eigenschaften | ||||||||||||||||||||||||||
| Natürliches Vorkommen | primordial | |||||||||||||||||||||||||
| Kristallstruktur | Graphit: einfach hexagonal (schwarz) | |||||||||||||||||||||||||
| Kristallstruktur | Diamant: flächenzentriert diamantkubisch (klar) | |||||||||||||||||||||||||
| Schallgeschwindigkeit dünner Stab | Diamant: 18.350 m/s (bei 20 °C) | |||||||||||||||||||||||||
| Thermische Ausdehnung | Diamant: 0,8 µm/(m⋅K) (bei 25 °C) | |||||||||||||||||||||||||
| Wärmeleitfähigkeit | Graphit: 119-165 W/(m⋅K) Diamant: 900-2300 W/(m⋅K) | |||||||||||||||||||||||||
| Elektrischer Widerstand | Graphit: 7,837 µΩ⋅m | |||||||||||||||||||||||||
| Magnetische Ordnung | diamagnetisch | |||||||||||||||||||||||||
| Molare magnetische Suszeptibilität | Diamant: -5,9×10-6 cm3/mol | |||||||||||||||||||||||||
| Elastizitätsmodul | Diamant: 1050 GPa | |||||||||||||||||||||||||
| Schermodul | Diamant: 478 GPa | |||||||||||||||||||||||||
| Elastizitätsmodul | Diamant: 442 GPa | |||||||||||||||||||||||||
| Poissonzahl | Diamant: 0,1 | |||||||||||||||||||||||||
| Mohs-Härte | Graphit: 1-2 Diamant: 10 | |||||||||||||||||||||||||
| CAS-Nummer |
| |||||||||||||||||||||||||
| Geschichte | ||||||||||||||||||||||||||
| Entdeckung | Ägypter und Sumerer (3750 v. Chr.) | |||||||||||||||||||||||||
| Anerkannt als ein Element durch | Antoine Lavoisier (1789) | |||||||||||||||||||||||||
| Hauptisotope von Kohlenstoff | ||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
Kohlenstoff (aus dem Lateinischen: carbo "Kohle") ist ein chemisches Element mit dem Symbol C und der Ordnungszahl 6. Es ist nichtmetallisch und vierwertig, d. h. es stehen vier Elektronen zur Verfügung, um kovalente chemische Bindungen einzugehen. Es gehört zur Gruppe 14 des Periodensystems. Kohlenstoff macht nur etwa 0,025 Prozent der Erdkruste aus. Drei Isotope kommen in der Natur vor: 12C und 13C sind stabil, während 14C ein Radionuklid ist, das mit einer Halbwertszeit von etwa 5.730 Jahren zerfällt. Kohlenstoff ist eines der wenigen Elemente, die seit dem Altertum bekannt sind. ⓘ
Kohlenstoff ist das 15. häufigste Element in der Erdkruste und nach Wasserstoff, Helium und Sauerstoff das vierthäufigste Element im Universum. Die Häufigkeit von Kohlenstoff, seine einzigartige Vielfalt an organischen Verbindungen und seine ungewöhnliche Fähigkeit, bei den auf der Erde üblichen Temperaturen Polymere zu bilden, machen dieses Element zu einem gemeinsamen Element allen bekannten Lebens. Es ist nach Sauerstoff das zweithäufigste Element im menschlichen Körper (etwa 18,5 %). ⓘ
Die Atome des Kohlenstoffs können sich auf unterschiedliche Weise miteinander verbinden, was zu verschiedenen Allotropen des Kohlenstoffs führt. Zu den bekanntesten Allotropen gehören Graphit, Diamant, amorpher Kohlenstoff und Fullerene. Die physikalischen Eigenschaften von Kohlenstoff variieren stark mit der allotropen Form. So ist Graphit beispielsweise undurchsichtig und schwarz, während Diamant sehr transparent ist. Graphit ist weich genug, um auf Papier einen Streifen zu bilden (daher sein Name, der vom griechischen Verb "γράφειν" abgeleitet ist, was "schreiben" bedeutet), während Diamant das härteste natürlich vorkommende Material ist. Graphit ist ein guter elektrischer Leiter, während Diamant eine geringe elektrische Leitfähigkeit aufweist. Unter normalen Bedingungen haben Diamant, Kohlenstoff-Nanoröhren und Graphen die höchsten Wärmeleitfähigkeiten aller bekannten Materialien. Alle Kohlenstoff-Allotrope sind unter normalen Bedingungen Feststoffe, wobei Graphit bei Standardtemperatur und -druck die thermodynamisch stabilste Form ist. Sie sind chemisch beständig und benötigen hohe Temperaturen, um selbst mit Sauerstoff zu reagieren. ⓘ
Die häufigste Oxidationsstufe von Kohlenstoff in anorganischen Verbindungen ist +4, während +2 in Kohlenmonoxid und Übergangsmetallcarbonylkomplexen vorkommt. Die größten Quellen für anorganischen Kohlenstoff sind Kalksteine, Dolomite und Kohlendioxid, aber auch in organischen Ablagerungen von Kohle, Torf, Öl und Methanclathraten kommen erhebliche Mengen vor. Kohlenstoff bildet eine riesige Anzahl von Verbindungen, mehr als jedes andere Element. Bis heute wurden fast zehn Millionen Verbindungen beschrieben, und doch ist diese Zahl nur ein Bruchteil der theoretisch möglichen Verbindungen unter Standardbedingungen. Aus diesem Grund wird Kohlenstoff oft als der "König der Elemente" bezeichnet. ⓘ
Kohlenstoff (von urgerm. kul-a-, kul-ō(n)- ,Kohle‘) oder Carbon (von lat. carbō ,Holzkohle‘, latinisiert Carboneum oder Carbonium) ist ein chemisches Element mit dem Elementsymbol C und der Ordnungszahl 6. Im Periodensystem steht es in der vierten Hauptgruppe bzw. der 14. IUPAC-Gruppe oder Kohlenstoffgruppe sowie der zweiten Periode. ⓘ
Es kommt in der Natur sowohl in gediegener (reiner) Form (Diamant, Graphit, Chaoit) als auch chemisch gebunden (z. B. in Form von Carbiden, Carbonaten, Kohlenstoffdioxid, Erdöl, Erdgas und Kohle) vor. Aufgrund seiner besonderen Elektronenkonfiguration (halbgefüllte L-Schale) besitzt es die Fähigkeit zur Bildung komplexer Moleküle und weist von allen chemischen Elementen die größte Vielfalt an chemischen Verbindungen auf. Diese Eigenschaft macht Kohlenstoff und seine Verbindungen zur Grundlage des Lebens auf der Erde. ⓘ
Eigenschaften

Zu den Allotropen des Kohlenstoffs gehören Graphit, eine der weichsten bekannten Substanzen, und Diamant, die härteste natürlich vorkommende Substanz. Er verbindet sich leicht mit anderen kleinen Atomen, einschließlich anderer Kohlenstoffatome, und ist in der Lage, mehrere stabile kovalente Bindungen mit geeigneten mehrwertigen Atomen einzugehen. Es ist bekannt, dass Kohlenstoff fast zehn Millionen Verbindungen bilden kann, was die große Mehrheit aller chemischen Verbindungen darstellt. Kohlenstoff hat außerdem den höchsten Sublimationspunkt aller Elemente. Bei Atmosphärendruck hat er keinen Schmelzpunkt, da sein Tripelpunkt bei 10,8 ± 0,2 Megapascal (106,6 ± 2,0 atm; 1.566 ± 29 psi) und 4.600 ± 300 K (4.330 ± 300 °C; 7.820 ± 540 °F) liegt, so dass er bei etwa 3.900 K (3.630 °C; 6.560 °F) sublimiert. Graphit ist unter Standardbedingungen viel reaktiver als Diamant, obwohl er thermodynamisch stabiler ist, da sein delokalisiertes pi-System viel anfälliger für Angriffe ist. So kann Graphit beispielsweise durch heiße konzentrierte Salpetersäure unter Standardbedingungen zu Mellitsäure, C6(CO2H)6, oxidiert werden, die die hexagonalen Einheiten des Graphits bewahrt, während die größere Struktur aufgebrochen wird. ⓘ
Kohlenstoff sublimiert in einem Kohlenstoffbogen, der eine Temperatur von etwa 5800 K (5.530 °C oder 9.980 °F) hat. Unabhängig von seiner allotropen Form bleibt Kohlenstoff also bei höheren Temperaturen fest als die höchstschmelzenden Metalle wie Wolfram oder Rhenium. Obwohl er thermodynamisch zur Oxidation neigt, widersteht Kohlenstoff der Oxidation besser als Elemente wie Eisen und Kupfer, die bei Raumtemperatur schwächere Reduktionsmittel sind. ⓘ
Kohlenstoff ist das sechste Element mit einer Grundzustandselektronenkonfiguration von 1s22s22p2, wobei die vier Außenelektronen Valenzelektronen sind. Seine ersten vier Ionisierungsenergien, 1086,5, 2352,6, 4620,5 und 6222,7 kJ/mol, sind viel höher als die der schwereren Elemente der Gruppe 14. Die Elektronegativität von Kohlenstoff liegt bei 2,5 und damit deutlich höher als die der schwereren Gruppe-14-Elemente (1,8-1,9), aber nahe bei den meisten benachbarten Nichtmetallen sowie einigen der Übergangsmetalle der zweiten und dritten Reihe. Die kovalenten Radien von Kohlenstoff werden normalerweise mit 77,2 pm (C-C), 66,7 pm (C=C) und 60,3 pm (C≡C) angegeben, obwohl diese Werte je nach Koordinationszahl und Bindungsart variieren können. Im Allgemeinen nimmt der kovalente Radius mit geringerer Koordinationszahl und höherer Bindungsordnung ab. ⓘ
Verbindungen auf Kohlenstoffbasis bilden die Grundlage allen bekannten Lebens auf der Erde, und der Kohlenstoff-Stickstoff-Zyklus liefert einen Teil der von der Sonne und anderen Sternen erzeugten Energie. Obwohl er eine außerordentliche Vielfalt von Verbindungen bildet, sind die meisten Formen von Kohlenstoff unter normalen Bedingungen vergleichsweise reaktionslos. Bei Standardtemperatur und -druck widersteht er allen außer den stärksten Oxidationsmitteln. Er reagiert nicht mit Schwefelsäure, Salzsäure, Chlor oder Alkalien. Bei höheren Temperaturen reagiert Kohlenstoff mit Sauerstoff unter Bildung von Kohlenstoffoxiden und entzieht Metalloxiden den Sauerstoff, so dass das elementare Metall übrig bleibt. Diese exotherme Reaktion wird in der Eisen- und Stahlindustrie zum Schmelzen von Eisen und zur Kontrolle des Kohlenstoffgehalts von Stahl verwendet:
- Fe
3O
4 + 4 C(s) + 2 O
2 → 3 Fe(s) + 4 CO
2(g). ⓘ
Kohlenstoff reagiert mit Schwefel unter Bildung von Schwefelkohlenstoff und mit Wasserdampf in der bei der Kohlevergasung verwendeten Kohle-Gas-Reaktion:
- C(s) + H2O(g) → CO(g) + H2(g). ⓘ
Bei hohen Temperaturen verbindet sich Kohlenstoff mit einigen Metallen zu Metallcarbiden, wie z. B. dem Eisenkarbid Zementit in Stahl und Wolframcarbid, das häufig als Schleifmittel und zur Herstellung harter Spitzen für Schneidwerkzeuge verwendet wird. ⓘ
Das System der Kohlenstoff-Allotrope umfasst eine Reihe von Extremen:
| Graphit ist eines der weichsten bekannten Materialien. | Synthetischer nanokristalliner Diamant ist das härteste bekannte Material. ⓘ |
| Graphit ist ein sehr gutes Schmiermittel und weist eine Superschmierfähigkeit auf. | Diamant ist das ultimative Schleifmittel. |
| Graphit ist ein elektrischer Leiter. | Diamant ist ein hervorragender elektrischer Isolator und hat das höchste elektrische Durchschlagsfeld aller bekannten Materialien. |
| Einige Formen von Graphit werden für die thermische Isolierung verwendet (z. B. als Feuerschutz und Hitzeschild), aber auch andere Formen sind gute Wärmeleiter. | Diamant ist der bekannteste natürlich vorkommende Wärmeleiter. |
| Graphit ist undurchsichtig. | Diamant ist hochtransparent. |
| Graphit kristallisiert im hexagonalen System. | Diamant kristallisiert im kubischen System. |
| Amorpher Kohlenstoff ist völlig isotrop. | Kohlenstoff-Nanoröhren gehören zu den anisotropesten bekannten Materialien. |
Allotrope
Da atomarer Kohlenstoff eine sehr kurzlebige Spezies ist, wird er in verschiedenen mehratomigen Strukturen mit unterschiedlichen Molekülkonfigurationen, den so genannten Allotropen, stabilisiert. Die drei relativ bekannten Allotrope des Kohlenstoffs sind amorpher Kohlenstoff, Graphit und Diamant. Fullerene, die früher als exotisch galten, werden heute häufig synthetisiert und in der Forschung verwendet; sie umfassen Buckyballs, Kohlenstoff-Nanoröhren, Kohlenstoff-Nanoknospen und Nanofasern. Es wurden auch mehrere andere exotische Allotrope entdeckt, wie Lonsdaleit, glasartiger Kohlenstoff, Kohlenstoff-Nanoschaum und linearer acetylenischer Kohlenstoff (Carbyne). ⓘ
Graphen ist ein zweidimensionales Blatt aus Kohlenstoff, dessen Atome in einem hexagonalen Gitter angeordnet sind. Seit 2009 scheint Graphen das stärkste jemals getestete Material zu sein. Das Verfahren zur Abtrennung von Graphen aus Graphit erfordert noch einige technologische Entwicklungen, bevor es für industrielle Prozesse wirtschaftlich ist. Im Erfolgsfall könnte Graphen für den Bau eines Weltraumfahrstuhls verwendet werden. Es könnte auch zur sicheren Speicherung von Wasserstoff für den Einsatz in einem wasserstoffbasierten Motor in Autos verwendet werden. ⓘ

Die amorphe Form ist eine Ansammlung von Kohlenstoffatomen in einem nicht kristallinen, unregelmäßigen, glasartigen Zustand, der nicht in einer kristallinen Makrostruktur vorliegt. Er liegt als Pulver vor und ist der Hauptbestandteil von Substanzen wie Holzkohle, Lampenruß und Aktivkohle. Bei normalem Druck nimmt Kohlenstoff die Form von Graphit an, bei dem jedes Atom trigonal an drei andere in einer Ebene aus verschmolzenen hexagonalen Ringen gebunden ist, genau wie bei den aromatischen Kohlenwasserstoffen. Das sich daraus ergebende Netzwerk ist zweidimensional, und die daraus resultierenden flachen Blätter sind gestapelt und durch schwache Van-der-Waals-Kräfte lose miteinander verbunden. Dies verleiht dem Graphit seine Weichheit und seine Spaltungseigenschaften (die Schichten gleiten leicht aneinander vorbei). Aufgrund der Delokalisierung eines der Außenelektronen jedes Atoms zur Bildung einer π-Wolke leitet Graphit Elektrizität, allerdings nur in der Ebene der einzelnen kovalent gebundenen Schichten. Daraus ergibt sich für Kohlenstoff eine geringere elektrische Leitfähigkeit als für die meisten Metalle. Die Delokalisierung ist auch der Grund für die energetische Stabilität von Graphit gegenüber Diamant bei Raumtemperatur. ⓘ
Bei sehr hohem Druck bildet Kohlenstoff das kompaktere Allotrop Diamant, dessen Dichte fast doppelt so hoch ist wie die von Graphit. Hier ist jedes Atom tetraedrisch mit vier anderen Atomen verbunden und bildet ein dreidimensionales Netz aus verschlungenen sechsgliedrigen Atomringen. Diamant hat die gleiche kubische Struktur wie Silizium und Germanium, und aufgrund der Stärke der Kohlenstoff-Kohlenstoff-Bindungen ist er der härteste natürlich vorkommende Stoff, gemessen an der Kratzfestigkeit. Entgegen der landläufigen Meinung, dass "Diamanten ewig sind", sind sie unter normalen Bedingungen (298 K, 105 Pa) thermodynamisch instabil (ΔfG°(Diamant, 298 K) = 2,9 kJ/mol) und müssten sich theoretisch in Graphit umwandeln. Aufgrund einer hohen Aktivierungsenergiebarriere ist der Übergang in Graphit bei normaler Temperatur jedoch so langsam, dass er nicht wahrnehmbar ist. Bei sehr hohen Temperaturen verwandelt sich Diamant jedoch in Graphit, und Diamanten können in einem Hausbrand verglühen. Die untere linke Ecke des Phasendiagramms für Kohlenstoff wurde noch nicht experimentell untersucht. Obwohl eine rechnerische Studie mit Methoden der Dichtefunktionaltheorie zu dem Ergebnis kam, dass Diamant bei T → 0 K und p → 0 Pa um etwa 1,1 kJ/mol stabiler ist als Graphit, zeigen neuere und endgültige experimentelle und rechnerische Studien, dass Graphit bei T < 400 K ohne Druckeinwirkung um 2,7 kJ/mol stabiler ist als Diamant. 7 kJ/mol bei T = 0 K und 3,2 kJ/mol bei T = 298,15 K. Unter bestimmten Bedingungen kristallisiert Kohlenstoff als Lonsdaleit, ein hexagonales Kristallgitter, bei dem alle Atome kovalent gebunden sind und das ähnliche Eigenschaften wie Diamant aufweist. ⓘ
Fullerene sind eine synthetische kristalline Formation mit einer graphitähnlichen Struktur, aber anstelle von flachen hexagonalen Zellen können einige der Zellen, aus denen Fullerene gebildet werden, Fünfecke, nicht planare Sechsecke oder sogar Heptagone aus Kohlenstoffatomen sein. Die Platten werden so zu Kugeln, Ellipsen oder Zylindern verformt. Die Eigenschaften von Fullerenen (unterteilt in Buckyballs, Buckytubes und Nanobuds) sind noch nicht vollständig analysiert und stellen ein intensives Forschungsgebiet im Bereich der Nanomaterialien dar. Die Namen Fulleren und Buckyballs sind nach Richard Buckminster Fuller benannt, dem Erfinder der geodätischen Kuppeln, die der Struktur der Fullerene ähneln. Die Buckyballs sind ziemlich große Moleküle, die vollständig aus trigonal gebundenem Kohlenstoff bestehen und Kugeln bilden (das bekannteste und einfachste ist das fußballförmige C60-Buckminsterfulleren). Kohlenstoff-Nanoröhren (Buckytubes) ähneln strukturell den Buckyballs, mit dem Unterschied, dass jedes Atom trigonal in einem gebogenen Blatt gebunden ist, das einen Hohlzylinder bildet. Nanobuds wurden erstmals 2007 beschrieben und sind hybride Buckytubes/Buckyballs (Buckyballs sind kovalent an die Außenwand eines Nanotubes gebunden), die die Eigenschaften beider Materialien in einer einzigen Struktur vereinen. ⓘ

Bei den anderen entdeckten Allotropen handelt es sich um Kohlenstoff-Nanoschaum, ein ferromagnetisches Allotrop, das 1997 entdeckt wurde. Es besteht aus einer Ansammlung von Kohlenstoffatomen mit geringer Dichte, die in einem lockeren dreidimensionalen Netz aneinandergereiht sind, in dem die Atome trigonal in sechs- und siebengliedrigen Ringen gebunden sind. Mit einer Dichte von etwa 2 kg/m3 gehört er zu den leichtesten bekannten Feststoffen. Auch glasartiger Kohlenstoff weist einen hohen Anteil an geschlossenen Poren auf, aber im Gegensatz zu normalem Graphit sind die Graphitschichten nicht wie Buchseiten übereinander gestapelt, sondern haben eine eher zufällige Anordnung. Linearer acetylenischer Kohlenstoff hat die chemische Struktur -(C:::C)n-. Der Kohlenstoff in dieser Modifikation ist linear mit sp-Orbital-Hybridisierung und ist ein Polymer mit abwechselnden Einfach- und Dreifachbindungen. Dieses Carbyne ist für die Nanotechnologie von großem Interesse, da sein Elastizitätsmodul 40-mal so hoch ist wie das des härtesten bekannten Materials - Diamant. ⓘ
Im Jahr 2015 gab ein Team der North Carolina State University die Entwicklung eines anderen Allotrops bekannt, das sie Q-Kohlenstoff nannten und das durch einen hochenergetischen Laserpuls mit geringer Dauer auf amorphem Kohlenstoffstaub erzeugt wurde. Q-Kohlenstoff soll Ferromagnetismus, Fluoreszenz und eine Härte aufweisen, die der von Diamanten überlegen ist. ⓘ
In der Dampfphase liegt ein Teil des Kohlenstoffs in Form von Dikohlenstoff (C
2). Wenn er angeregt wird, leuchtet dieses Gas grün. ⓘ

Sind nur 2 der 3 p-Orbitale an der Hybridisierung beteiligt, entstehen die so genannten sp2-Orbitale. Die sp2- Orbitale richten sich zweidimensional (als Fläche bzw. Ebene) aus; ober- und unterhalb dieser Fläche formt das übrigbleibende p-Orbital jeweils einen Orbitallappen. Steht beispielsweise das p-Orbital senkrecht auf der xy-Ebene, liegen die sp2- Orbitale trigonal in der xy-Ebene. Sie haben den gleichen Winkel von 120° zueinander. Das Bild links veranschaulicht die Situation. Das unhybridisierte p-Orbital ist der Übersichtlichkeit halber weggelassen. ⓘ
sp2-Kohlenstoff-Atome können miteinander kovalente Bindungen bilden, die dann in einer Ebene liegen. Ihre Struktur ist trigonal; dies ist die Grundstruktur der Planarebenen des Graphits (siehe Kristallgitterstruktur dort). Die übriggebliebenen p-Orbitale wechselwirken ebenfalls untereinander. Sie formen die pi-Bindungen mit deutlich geringeren Bindungsenergien als die sigma-Bindungen der sp2 beziehungsweise sp3-Orbitale und bilden ober- und unterhalb der sigma-Bindungsebene ein sogenanntes Elektronengas in Form atomrumpfunabhängiger („delokalisierter“) pi-Elektronen. ⓘ
Chemisch spricht man von einer Doppelbindung. Die Schreibweise C=C vernachlässigt den unterschiedlichen Charakter beider Bindungen. Die Bindungsenergie der diamantartigen tetraedrischen sp3-Einfachbindung 'C–C' liegt bei 350 kJ/mol, die der graphitartigen trigonalen sp2-Doppelbindung C=C nur um 260 kJ/mol höher. In einem hexagonalen Kohlenstoff-Ring mit sechs Kohlenstoff-Atomen stabilisiert sich die pi-Bindung durch Delokalisierung der Elektronen innerhalb des Rings (mehr dazu siehe Benzol). ⓘ
Vorkommen


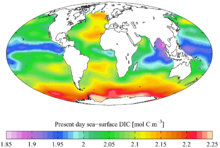
Kohlenstoff ist nach Wasserstoff, Helium und Sauerstoff das vierthäufigste chemische Element im beobachtbaren Universum. Kohlenstoff ist in der Sonne, in Sternen, Kometen und in den Atmosphären der meisten Planeten reichlich vorhanden. Einige Meteoriten enthalten mikroskopisch kleine Diamanten, die entstanden sind, als das Sonnensystem noch eine protoplanetare Scheibe war. Mikroskopische Diamanten können auch durch den intensiven Druck und die hohen Temperaturen an den Einschlagstellen von Meteoriten entstehen. ⓘ
Im Jahr 2014 kündigte die NASA eine stark verbesserte Datenbank zur Verfolgung polyzyklischer aromatischer Kohlenwasserstoffe (PAK) im Universum an. Mehr als 20 % des Kohlenstoffs im Universum sind möglicherweise mit PAK verbunden, komplexen Verbindungen aus Kohlenstoff und Wasserstoff ohne Sauerstoff. Diese Verbindungen sind Teil der PAK-Welt-Hypothese, die ihnen eine Rolle bei der Abiogenese und der Entstehung von Leben zuschreibt. PAK scheinen "ein paar Milliarden Jahre" nach dem Urknall entstanden zu sein, sind im gesamten Universum verbreitet und werden mit neuen Sternen und Exoplaneten in Verbindung gebracht. ⓘ
Man schätzt, dass die feste Erde insgesamt 730 ppm Kohlenstoff enthält, davon 2000 ppm im Kern und 120 ppm im Mantel und in der Kruste zusammen. Da die Masse der Erde 5,972×1024 kg beträgt, würde dies 4360 Millionen Gigatonnen Kohlenstoff bedeuten. Das ist viel mehr als die Menge an Kohlenstoff in den Ozeanen oder der Atmosphäre (siehe unten). ⓘ
Zusammen mit dem Sauerstoff im Kohlendioxid befindet sich der Kohlenstoff in der Erdatmosphäre (ca. 900 Gigatonnen Kohlenstoff - jedes ppm entspricht 2,13 Gt) und in allen Gewässern gelöst (ca. 36 000 Gigatonnen Kohlenstoff). Der Kohlenstoff in der Biosphäre wird auf 550 Gigatonnen geschätzt, allerdings mit einer großen Unsicherheit, die vor allem auf die große Ungewissheit über die Menge der terrestrischen Bakterien im tiefen Untergrund zurückzuführen ist. Kohlenwasserstoffe (wie Kohle, Erdöl und Erdgas) enthalten ebenfalls Kohlenstoff. Die Kohle-"Reserven" (nicht die "Ressourcen") belaufen sich auf etwa 900 Gigatonnen mit vielleicht 18.000 Gt an Ressourcen. Die Ölreserven belaufen sich auf etwa 150 Gigatonnen. Die nachgewiesenen Erdgasvorkommen belaufen sich auf etwa 175×1012 Kubikmeter (mit etwa 105 Gigatonnen Kohlenstoff), aber Studien gehen von weiteren 900×1012 Kubikmetern an "unkonventionellen" Vorkommen wie Schiefergas aus, was etwa 540 Gigatonnen Kohlenstoff entspricht. ⓘ
Kohlenstoff findet sich auch in Methanhydraten in den Polarregionen und unter den Meeren. Verschiedene Schätzungen gehen von 500, 2500 oder 3.000 Gigatonnen Kohlenstoff aus. ⓘ
In der Vergangenheit waren die Mengen an Kohlenwasserstoffen noch größer. Einer Quelle zufolge wurden im Zeitraum von 1751 bis 2008 durch die Verbrennung fossiler Brennstoffe etwa 347 Gigatonnen Kohlenstoff in Form von Kohlendioxid in die Atmosphäre abgegeben. Eine andere Quelle beziffert die Menge, die der Atmosphäre seit 1750 hinzugefügt wurde, auf 879 Gt, und die Gesamtmenge, die in die Atmosphäre, das Meer und das Land (z. B. Torfmoore) gelangt ist, auf fast 2.000 Gt. ⓘ
Kohlenstoff ist ein Bestandteil (etwa 12 % der Masse) der sehr großen Massen von Karbonatgestein (Kalkstein, Dolomit, Marmor usw.). Kohle ist sehr kohlenstoffreich (Anthrazit enthält 92-98 %) und stellt mit 4.000 Gigatonnen oder 80 % der fossilen Brennstoffe die größte kommerzielle Quelle für mineralischen Kohlenstoff dar. ⓘ
Was einzelne Kohlenstoff-Allotrope betrifft, so wird Graphit in großen Mengen in den Vereinigten Staaten (vor allem in New York und Texas), Russland, Mexiko, Grönland und Indien gefunden. Natürliche Diamanten kommen in dem Gestein Kimberlit vor, das in alten vulkanischen "Hälsen" oder "Röhren" vorkommt. Die meisten Diamantenvorkommen befinden sich in Afrika, vor allem in Südafrika, Namibia, Botswana, der Republik Kongo und Sierra Leone. Diamantvorkommen wurden auch in Arkansas, Kanada, der russischen Arktis, Brasilien sowie in Nord- und Westaustralien gefunden. Inzwischen werden Diamanten auch vom Meeresboden vor dem Kap der Guten Hoffnung gewonnen. Diamanten kommen in der Natur vor, aber etwa 30 % aller in den USA verwendeten Industriediamanten werden heute hergestellt. ⓘ
Kohlenstoff-14 wird in den oberen Schichten der Troposphäre und der Stratosphäre in 9-15 km Höhe durch eine Reaktion gebildet, die durch kosmische Strahlung ausgelöst wird. Dabei werden thermische Neutronen erzeugt, die mit den Kernen von Stickstoff-14 zusammenstoßen und Kohlenstoff-14 und ein Proton bilden. So enthält 1,5%×10-10 des atmosphärischen Kohlendioxids Kohlenstoff-14. ⓘ
Kohlenstoffreiche Asteroiden sind relativ häufig in den äußeren Teilen des Asteroidengürtels im Sonnensystem anzutreffen. Diese Asteroiden wurden bisher noch nicht direkt von Wissenschaftlern beprobt. Die Asteroiden können für den hypothetischen weltraumgestützten Kohlenstoffabbau genutzt werden, der in der Zukunft möglich sein könnte, aber derzeit technologisch unmöglich ist. ⓘ
Isotope
Es sind insgesamt 15 Isotope zwischen 8C und 23C des Kohlenstoffs bekannt. Von diesen sind zwei, die Isotope 12C und 13C stabil und kommen in der Natur vor. Das Isotop mit dem größeren Anteil an der natürlichen Isotopenzusammensetzung ist 12C mit 98,93 %, 13C hat einen Anteil von 1,07 %. Die langlebigsten instabilen Isotope sind 11C, das mit einer Halbwertszeit von 20,364 Minuten unter β+-Strahlung in 11B übergeht und 14C, das mit einer Halbwertszeit von 5730 Jahren unter Betazerfall zu 14N zerfällt. Alle anderen Isotope haben nur kurze Halbwertszeiten von Sekunden oder Millisekunden. ⓘ
12C ist laut Definition der Bezugspunkt für die Einheit der Atommasse. 13C kann man in NMR-spektroskopischen Untersuchungen detektieren, da es, anders als 12C, über ein magnetisches Moment verfügt. Das Verhältnis dieser beiden Isotope heißt Δ13C und wird in der Geochemie, Paläoklimatologie und Paläozeanographie benutzt. ⓘ
14C entsteht durch die Reaktion von 14N mit kosmischer Strahlung. Lebewesen, die am Kohlenstoffzyklus teilnehmen, zeigen den gleichen Anteil an 14C bezüglich der gesamten enthaltenen Kohlenstoffmenge wie die Atmosphäre. Nach dem Ende des Stoffwechsels, also beispielsweise nach der Fällung eines Baums, verringert sich dieser Anteil allmählich durch den radioaktiven Zerfall. Die Bestimmung des Anteils von 14C zum gesamten Kohlenstoffgehalt erlaubt daher eine Altersbestimmung an Gegenständen aus organischem Material, die Radiokarbonmethode, die vor allem in der Archäologie Verwendung findet. ⓘ
Aus Erdgas oder Erdöl gewonnenes, und aus dem Erdmantel stammendes CO2 enthält so gut wie kein 14C, das mit einer Halbwertszeit von 5730 Jahren zerfällt, im Vergleich zum CO2 aus der Luft, wo das 14C-Isotop laufend nachgebildet wird. 14C kann daher als eine Art Tracer verwendet werden, um mithilfe von Szintillationsspektrometern den Weg oder den Gehalt von Molekülen, die auf Erdöl basieren oder aus dem Erdmantel stammen, in Pflanzen zu bestimmen. Beispielsweise den CO2-Transport in der Atmungskette. ⓘ
Das kurzlebige Isotop 11C findet Anwendung als PET-Nuklid. Dazu wird es an einem Zyklotron erzeugt und mittels geeigneter chemischer Verfahren zu Radiopharmaka wie [11C]-Cholin umgesetzt. ⓘ
Kohlenstoff-14 (14C) ist ein natürlich vorkommendes Radioisotop, das in der oberen Atmosphäre (untere Stratosphäre und obere Troposphäre) durch Wechselwirkung von Stickstoff mit kosmischer Strahlung entsteht. Es kommt auf der Erde in Spurenmengen von 1 Teil pro Billion (0,0000000001%) oder mehr vor und ist meist auf die Atmosphäre und oberflächliche Ablagerungen, insbesondere Torf und andere organische Materialien, beschränkt. Dieses Isotop zerfällt durch 0,158 MeV β- Emission. Aufgrund seiner relativ kurzen Halbwertszeit von 5730 Jahren ist 14C in alten Gesteinen praktisch nicht vorhanden. Der 14C-Gehalt in der Atmosphäre und in lebenden Organismen ist nahezu konstant, nimmt aber nach dem Tod vorhersehbar im Körper ab. Dieses Prinzip wird bei der 1949 erfundenen Radiokohlenstoffdatierung angewandt, die in großem Umfang zur Bestimmung des Alters von kohlenstoffhaltigen Materialien mit einem Alter von bis zu 40.000 Jahren verwendet wird. ⓘ
Es gibt 15 bekannte Kohlenstoffisotope, von denen das kurzlebigste 8C ist, das durch Protonenemission und Alphazerfall zerfällt und eine Halbwertszeit von 1,98739 × 10-21 s hat. Das exotische 19C weist einen Kernhalo auf, d. h. sein Radius ist deutlich größer, als man erwarten würde, wenn der Kern eine Kugel mit konstanter Dichte wäre. ⓘ
Bildung in Sternen
Die Bildung des Kohlenstoff-Atomkerns erfolgt in einem Riesen- oder Überriesenstern durch den Triple-Alpha-Prozess. Dazu ist ein nahezu gleichzeitiger Zusammenstoß von drei Alphateilchen (Heliumkernen) erforderlich, da die Produkte weiterer Kernfusionsreaktionen von Helium mit Wasserstoff oder einem anderen Heliumkern Lithium-5 bzw. Beryllium-8 erzeugen, die beide sehr instabil sind und fast sofort wieder in kleinere Kerne zerfallen. Der Triple-Alpha-Prozess findet bei Temperaturen von über 100 Megakelvin und einer Heliumkonzentration statt, die durch die rasche Ausdehnung und Abkühlung des frühen Universums nicht möglich waren, so dass während des Urknalls kein nennenswerter Kohlenstoff entstanden ist. ⓘ
Nach der aktuellen physikalischen Kosmologietheorie bildet sich Kohlenstoff im Inneren von Sternen auf dem horizontalen Ast. Wenn massereiche Sterne als Supernova sterben, wird der Kohlenstoff als Staub in den Weltraum verstreut. Dieser Staub wird zum Ausgangsmaterial für die Bildung der nächsten Generation von Sternensystemen mit hinzukommenden Planeten. Das Sonnensystem ist ein solches Sternsystem mit einem Überfluss an Kohlenstoff, der die Existenz von Leben, wie wir es kennen, ermöglicht. ⓘ
Der CNO-Zyklus ist ein zusätzlicher Wasserstofffusionsmechanismus, der Sterne antreibt und bei dem Kohlenstoff als Katalysator fungiert. ⓘ
Rotationsübergänge verschiedener Isotopenformen von Kohlenmonoxid (z. B. 12CO, 13CO und 18CO) sind im Submillimeter-Wellenlängenbereich nachweisbar und werden bei der Untersuchung neu entstehender Sterne in Molekülwolken verwendet. ⓘ
Kohlenstoffkreislauf

Unter terrestrischen Bedingungen ist die Umwandlung von einem Element in ein anderes sehr selten. Daher ist die Menge an Kohlenstoff auf der Erde praktisch konstant. Prozesse, die Kohlenstoff nutzen, müssen ihn also von irgendwoher beziehen und an anderer Stelle wieder abgeben. Die Wege des Kohlenstoffs in der Umwelt bilden den Kohlenstoffkreislauf. So ziehen beispielsweise photosynthetische Pflanzen Kohlendioxid aus der Atmosphäre (oder dem Meerwasser) und bauen es zu Biomasse auf, wie im Calvin-Zyklus, einem Prozess der Kohlenstofffixierung. Ein Teil dieser Biomasse wird von Tieren gefressen, während ein Teil des Kohlenstoffs von Tieren als Kohlendioxid wieder ausgeatmet wird. Der Kohlenstoffkreislauf ist wesentlich komplizierter als dieser kurze Kreislauf; beispielsweise ist ein Teil des Kohlendioxids in den Ozeanen gelöst; wenn Bakterien es nicht verbrauchen, kann aus abgestorbenen pflanzlichen oder tierischen Stoffen Erdöl oder Kohle entstehen, die bei der Verbrennung Kohlenstoff freisetzen. ⓘ
Verbindungen
Organische Verbindungen


Kohlenstoff kann sehr lange Ketten aus miteinander verbundenen Kohlenstoff-Kohlenstoff-Bindungen bilden, eine Eigenschaft, die als Verkettung bezeichnet wird. Kohlenstoff-Kohlenstoff-Bindungen sind stark und stabil. Durch Verkettung bildet der Kohlenstoff eine Vielzahl von Verbindungen. Eine Aufzählung der einzelnen Verbindungen zeigt, dass mehr Kohlenstoff enthalten ist als nicht. Ähnliches gilt für Wasserstoff, denn die meisten organischen Verbindungen enthalten Wasserstoff, der chemisch an Kohlenstoff oder ein anderes allgemeines Element wie Sauerstoff oder Stickstoff gebunden ist. ⓘ
Die einfachste Form eines organischen Moleküls ist der Kohlenwasserstoff - eine große Familie von organischen Molekülen, die aus Wasserstoffatomen bestehen, die an eine Kette von Kohlenstoffatomen gebunden sind. Ein Kohlenwasserstoffgerüst kann durch andere Atome, so genannte Heteroatome, ersetzt werden. Häufige Heteroatome in organischen Verbindungen sind Sauerstoff, Stickstoff, Schwefel, Phosphor und die nicht radioaktiven Halogene sowie die Metalle Lithium und Magnesium. Organische Verbindungen, die Bindungen zu Metallen enthalten, werden als metallorganische Verbindungen bezeichnet (siehe unten). Bestimmte Gruppierungen von Atomen, oft einschließlich Heteroatomen, kommen in einer großen Anzahl organischer Verbindungen vor. Diese Ansammlungen, die als funktionelle Gruppen bezeichnet werden, verleihen gemeinsame Reaktivitätsmuster und ermöglichen die systematische Untersuchung und Kategorisierung organischer Verbindungen. Kettenlänge, Form und funktionelle Gruppen beeinflussen alle die Eigenschaften organischer Moleküle. ⓘ
In den meisten stabilen Kohlenstoffverbindungen (und fast allen stabilen organischen Verbindungen) gehorcht der Kohlenstoff der Oktettregel und ist vierwertig, d. h. ein Kohlenstoffatom bildet insgesamt vier kovalente Bindungen (zu denen auch Doppel- und Dreifachbindungen gehören können). Zu den Ausnahmen gehören eine kleine Anzahl stabilisierter Carbokationen (drei Bindungen, positive Ladung), Radikale (drei Bindungen, neutral), Carbanionen (drei Bindungen, negative Ladung) und Carbene (zwei Bindungen, neutral), obwohl diese Spezies eher als instabile, reaktive Zwischenstufen anzutreffen sind. ⓘ
Kohlenstoff kommt in allen bekannten organischen Lebewesen vor und ist die Grundlage der organischen Chemie. In Verbindung mit Wasserstoff bildet er verschiedene Kohlenwasserstoffe, die für die Industrie als Kühl-, Schmier- und Lösungsmittel, als chemisches Ausgangsmaterial für die Herstellung von Kunststoffen und Petrochemikalien sowie als fossile Brennstoffe wichtig sind. ⓘ
In Verbindung mit Sauerstoff und Wasserstoff kann Kohlenstoff viele Gruppen wichtiger biologischer Verbindungen bilden, darunter Zucker, Lignane, Chitine, Alkohole, Fette und aromatische Ester, Carotinoide und Terpene. Mit Stickstoff bildet es Alkaloide, und mit Schwefel werden Antibiotika, Aminosäuren und Gummiprodukte gebildet. Zusammen mit Phosphor bildet es die DNA und RNA, die Träger des chemischen Codes des Lebens, und Adenosintriphosphat (ATP), das wichtigste Energieübertragungsmolekül in allen lebenden Zellen. ⓘ
Anorganische Verbindungen
Üblicherweise werden kohlenstoffhaltige Verbindungen, die mit Mineralien assoziiert sind oder keine Bindungen zu den anderen Kohlenstoffatomen, Halogenen oder Wasserstoff enthalten, getrennt von den klassischen organischen Verbindungen behandelt; die Definition ist nicht starr, und die Klassifizierung einiger Verbindungen kann von Autor zu Autor variieren (siehe Referenzartikel oben). Zu diesen Verbindungen gehören die einfachen Oxide des Kohlenstoffs. Das bekannteste Oxid ist Kohlendioxid (CO2). Es war einst der Hauptbestandteil der Paläoatmosphäre, ist aber heute nur noch ein kleiner Bestandteil der Erdatmosphäre. In Wasser gelöst, bildet es Kohlensäure (H
2CO
3), aber wie die meisten Verbindungen mit mehreren einfach gebundenen Sauerstoffatomen an einem einzigen Kohlenstoff ist sie instabil. Durch dieses Zwischenprodukt werden jedoch resonanzstabilisierte Karbonationen erzeugt. Einige wichtige Minerale sind Karbonate, vor allem Calcit. Kohlenstoffdisulfid (CS
2) ist ähnlich. Aufgrund seiner physikalischen Eigenschaften und seiner Verbindung zur organischen Synthese wird Schwefelkohlenstoff jedoch manchmal als organisches Lösungsmittel eingestuft. ⓘ
Das andere häufige Oxid ist Kohlenmonoxid (CO). Es wird durch unvollständige Verbrennung gebildet und ist ein farb- und geruchloses Gas. Die Moleküle enthalten jeweils eine Dreifachbindung und sind ziemlich polar, so dass sie dazu neigen, sich dauerhaft an Hämoglobinmoleküle zu binden und den Sauerstoff zu verdrängen, der eine geringere Bindungsaffinität hat. Cyanid (CN-) hat eine ähnliche Struktur, verhält sich aber eher wie ein Halogenid-Ion (Pseudohalogen). Es kann zum Beispiel das Nitrid Cyanogenmolekül ((CN)2) bilden, ähnlich wie zweiatomige Halogenide. Auch das schwerere Analogon von Cyanid, Cyaphid (CP-), wird als anorganisch betrachtet, obwohl die meisten einfachen Derivate sehr instabil sind. Andere seltene Oxide sind Kohlenstoffsuboxid (C
3O
2), das instabile Dikohlenmonoxid (C2O), Kohlentrioxid (CO3), Cyclopentanpenton (C5O5), Cyclohexanhexon (C6O6) und Mellitsäureanhydrid (C12O9). Mellitsäureanhydrid ist jedoch das dreifache Acylanhydrid der Mellitsäure; außerdem enthält es einen Benzolring. Viele Chemiker betrachten es daher als organisch. ⓘ
Mit reaktiven Metallen, wie Wolfram, bildet Kohlenstoff entweder Carbide (C4-) oder Acetylide (C2-
2), um Legierungen mit hohem Schmelzpunkt zu bilden. Diese Anionen sind auch mit Methan und Acetylen verbunden, beides sehr schwache Säuren. Mit einer Elektronegativität von 2,5 geht der Kohlenstoff bevorzugt kovalente Bindungen ein. Einige Karbide sind kovalente Gitter, wie Karborund (SiC), das dem Diamant ähnelt. Dennoch sind selbst die polarsten und salzartigsten Carbide keine vollständig ionischen Verbindungen. ⓘ
Metallorganische Verbindungen
Metallorganische Verbindungen enthalten per Definition mindestens eine kovalente Kohlenstoff-Metall-Bindung. Es gibt eine Vielzahl solcher Verbindungen; zu den wichtigsten Klassen gehören einfache Alkyl-Metall-Verbindungen (z. B. Tetraethylblei), η2-Alken-Verbindungen (z. B. Zeise-Salz) und η3-Allyl-Verbindungen (z. B. Allylpalladiumchlorid-Dimer), Metallocene mit Cyclopentadienyl-Liganden (z. B. Ferrocen) und Übergangsmetall-Carben-Komplexe. Es gibt viele Metallcarbonyl- und Metallcyanidkomplexe (z. B. Tetracarbonylnickel und Kaliumferricyanid); einige Fachleute betrachten Metallcarbonyl- und Cyanidkomplexe ohne andere Kohlenstoffliganden als rein anorganisch und nicht als metallorganisch. Die meisten metallorganischen Chemiker betrachten jedoch Metallkomplexe mit einem beliebigen Kohlenstoffliganden, auch mit "anorganischem Kohlenstoff" (z. B. Carbonyle, Cyanide und bestimmte Arten von Carbiden und Acetyliden), als metallorganisch. Metallkomplexe, die organische Liganden ohne kovalente Kohlenstoff-Metall-Bindung enthalten (z. B. Metallcarboxylate), werden als metallorganische Verbindungen bezeichnet. ⓘ
Es wird davon ausgegangen, dass Kohlenstoff die Bildung von vier kovalenten Bindungen stark bevorzugt, aber es sind auch andere exotische Bindungsschemata bekannt. Carborane sind sehr stabile dodekaedrische Derivate der [B12H12]2- Einheit, bei denen ein BH durch ein CH+ ersetzt ist. Somit ist der Kohlenstoff an fünf Boratome und ein Wasserstoffatom gebunden. Das Kation [(Ph3PAu)6C]2+ enthält einen oktaedrischen Kohlenstoff, der an sechs Phosphin-Gold-Fragmente gebunden ist. Dieses Phänomen wird auf die Aurophilie der Goldliganden zurückgeführt, die für eine zusätzliche Stabilisierung einer ansonsten labilen Spezies sorgen. In der Natur hat der Eisen-Molybdän-Cofaktor (FeMoco), der für die mikrobielle Stickstofffixierung verantwortlich ist, ebenfalls ein oktaedrisches Kohlenstoffzentrum (formell ein Karbid, C(-IV)), das an sechs Eisenatome gebunden ist. Im Jahr 2016 wurde bestätigt, dass das Hexamethylbenzol-Dikation in Übereinstimmung mit früheren theoretischen Vorhersagen ein Kohlenstoffatom mit sechs Bindungen enthält. Genauer gesagt konnte das Dikation strukturell durch die Formulierung [MeC(η5-C5Me5)]2+ beschrieben werden, was es zu einem "organischen Metallocen" macht, bei dem ein MeC3+-Fragment über alle fünf Kohlenstoffatome des Rings an ein η5-C5Me5-Fragment gebunden ist. ⓘ
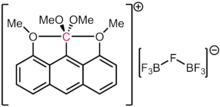
Es ist wichtig zu beachten, dass in den oben genannten Fällen jede der Bindungen zum Kohlenstoff weniger als zwei formale Elektronenpaare enthält. Die Anzahl der formalen Elektronen dieser Spezies übersteigt also nicht ein Oktett. Dies macht sie hyperkoordiniert, aber nicht hypervalent. Selbst in Fällen von angeblichen 10-C-5-Spezies (d. h. ein Kohlenstoff mit fünf Liganden und einer formalen Elektronenzahl von zehn), wie von Akiba und Mitarbeitern berichtet, kommen Berechnungen der elektronischen Struktur zu dem Schluss, dass die Elektronenpopulation um den Kohlenstoff immer noch weniger als acht beträgt, wie dies auch für andere Verbindungen mit Vier-Elektronen-Dreizentren-Bindungen gilt. ⓘ
Geschichte und Etymologie

Der englische Name Carbon stammt vom lateinischen carbo für Kohle und Holzkohle ab, woraus sich auch das französische charbon für Holzkohle ableitet. Im Deutschen, Niederländischen und Dänischen heißen Kohlenstoff, koolstof bzw. kulstof, was wörtlich übersetzt "Kohle" bedeutet. ⓘ
Kohlenstoff wurde in der Vorgeschichte entdeckt und war in Form von Ruß und Holzkohle bereits den frühesten menschlichen Zivilisationen bekannt. Diamanten waren wahrscheinlich schon 2500 v. Chr. in China bekannt, während Kohlenstoff in Form von Holzkohle um die Zeit der Römer auf die gleiche Weise hergestellt wurde wie heute, nämlich durch Erhitzen von Holz in einer mit Lehm bedeckten Pyramide, um die Luft auszuschließen. ⓘ

1722 wies René Antoine Ferchault de Réaumur nach, dass Eisen durch die Absorption einer Substanz, die heute als Kohlenstoff bekannt ist, in Stahl umgewandelt wird. 1772 wies Antoine Lavoisier nach, dass Diamanten eine Form von Kohlenstoff sind, als er Proben von Holzkohle und Diamanten verbrannte und feststellte, dass bei beiden kein Wasser entstand und beide die gleiche Menge an Kohlendioxid pro Gramm freisetzten. 1779 wies Carl Wilhelm Scheele nach, dass Graphit, den man für eine Form von Blei hielt, stattdessen mit Holzkohle identisch ist, allerdings mit einer kleinen Beimischung von Eisen, und dass es bei der Oxidation mit Salpetersäure "Luftsäure" (sein Name für Kohlendioxid) ergibt. 1786 bestätigten die französischen Wissenschaftler Claude Louis Berthollet, Gaspard Monge und C. A. Vandermonde, dass es sich bei Graphit hauptsächlich um Kohlenstoff handelte, indem sie ihn mit Sauerstoff oxidierten, ähnlich wie es Lavoisier mit Diamant getan hatte. Auch hier blieb etwas Eisen übrig, das nach Ansicht der französischen Wissenschaftler für die Graphitstruktur notwendig war. In ihrer Veröffentlichung schlugen sie den Namen carbone (lat. carbonum) für das Element im Graphit vor, das bei der Verbrennung von Graphit als Gas freigesetzt wurde. Antoine Lavoisier führte daraufhin Kohlenstoff als Element in seinem Lehrbuch von 1789 auf. ⓘ
Ein neues Allotrop des Kohlenstoffs, Fulleren, das 1985 entdeckt wurde, umfasst nanostrukturierte Formen wie Buckyballs und Nanoröhren. Ihre Entdecker - Robert Curl, Harold Kroto und Richard Smalley - erhielten 1996 den Nobelpreis für Chemie. Das daraus resultierende erneute Interesse an neuen Formen führte zur Entdeckung weiterer exotischer Allotrope, darunter glasartiger Kohlenstoff, und zu der Erkenntnis, dass "amorpher Kohlenstoff" nicht unbedingt amorph ist. ⓘ
Herstellung
Graphit
Kommerziell nutzbare natürliche Graphitvorkommen gibt es in vielen Teilen der Welt, aber die wirtschaftlich wichtigsten Quellen liegen in China, Indien, Brasilien und Nordkorea. Graphitvorkommen sind metamorphen Ursprungs und kommen in Verbindung mit Quarz, Glimmer und Feldspat in Schiefer, Gneis und metamorphosierten Sand- und Kalksteinen in Form von Linsen oder Adern vor, die manchmal einen Meter oder mehr dick sind. Die Graphitvorkommen in Borrowdale, Cumberland, England, waren anfangs so groß und rein, dass man bis ins 19. Jahrhundert Bleistifte herstellte, indem man Blöcke aus Naturgraphit in Streifen sägte und diese dann in Holz einbettete. Heute gewinnt man kleinere Graphitvorkommen, indem man das Muttergestein zerkleinert und den leichteren Graphit auf dem Wasser ausschwimmen lässt. ⓘ
Es gibt drei Arten von Naturgraphit: amorphen, flockigen oder kristallinen Graphit und Adern oder Klumpen. Amorpher Graphit ist von geringster Qualität und kommt am häufigsten vor. Im Gegensatz zur Wissenschaft bezieht sich "amorph" in der Industrie auf eine sehr geringe Kristallgröße und nicht auf das völlige Fehlen einer Kristallstruktur. Amorpher Graphit wird für minderwertige Graphitprodukte verwendet und ist der preisgünstigste Graphit. Große amorphe Graphitlagerstätten gibt es in China, Europa, Mexiko und den Vereinigten Staaten. Flockengraphit ist seltener und von höherer Qualität als amorpher Graphit; er kommt in Form separater Platten vor, die in metamorphem Gestein kristallisiert sind. Flockengraphit kann das Vierfache des Preises von amorphem Graphit betragen. Qualitativ hochwertige Flocken können zu expandierbarem Graphit für viele Verwendungszwecke, z. B. als Flammschutzmittel, verarbeitet werden. Die bedeutendsten Vorkommen befinden sich in Österreich, Brasilien, Kanada, China, Deutschland und Madagaskar. Ader- oder Klumpengraphit ist die seltenste, wertvollste und hochwertigste Art von Naturgraphit. Er kommt in Adern entlang von Intrusionskontakten in festen Klumpen vor und wird nur in Sri Lanka kommerziell abgebaut. ⓘ
Nach Angaben des USGS belief sich die Weltproduktion von Naturgraphit im Jahr 2010 auf 1,1 Millionen Tonnen, zu denen China 800.000 t, Indien 130.000 t, Brasilien 76.000 t, Nordkorea 30.000 t und Kanada 25.000 t beitrugen. In den Vereinigten Staaten wurde kein Naturgraphit abgebaut, aber 2009 wurden 118.000 t synthetischer Graphit mit einem geschätzten Wert von 998 Mio. $ produziert. ⓘ
Diamanten

Die Lieferkette für Diamanten wird von einer begrenzten Anzahl mächtiger Unternehmen kontrolliert und ist zudem stark auf einige wenige Standorte in der Welt konzentriert (siehe Abbildung). ⓘ
Nur ein sehr kleiner Teil des Diamantenerzes besteht aus echten Diamanten. Das Erz wird zerkleinert, wobei darauf geachtet werden muss, dass größere Diamanten bei diesem Prozess nicht zerstört werden, und anschließend werden die Partikel nach ihrer Dichte sortiert. Heute werden die Diamanten in der diamantenreichen Dichtefraktion mit Hilfe der Röntgenfluoreszenz aufgespürt, und die letzten Sortierschritte werden von Hand durchgeführt. Bevor der Einsatz von Röntgenstrahlen üblich wurde, erfolgte die Trennung mit Fettbändern; Diamanten neigen stärker dazu, am Fett zu haften als die anderen Mineralien im Erz. ⓘ
In der Vergangenheit wurden Diamanten nur in alluvialen Lagerstätten in Südindien gefunden. Indien war von der Zeit ihrer Entdeckung im 9. Jahrhundert v. Chr. bis zur Mitte des 18. Jahrhunderts n. Chr. weltweit führend in der Diamantenproduktion, aber das kommerzielle Potenzial dieser Vorkommen war Ende des 18. Jahrhunderts erschöpft, und zu diesem Zeitpunkt wurde Indien von Brasilien verdrängt, wo 1725 die ersten nichtindischen Diamanten gefunden wurden. ⓘ
Die Diamantenproduktion aus Primärlagerstätten (Kimberlite und Lamproite) begann erst in den 1870er Jahren nach der Entdeckung der Diamantenfelder in Südafrika. Die Produktion hat im Laufe der Zeit zugenommen, und insgesamt wurden seither über 4,5 Milliarden Karat gefördert. Die meisten kommerziell nutzbaren Diamantenvorkommen befanden sich in Russland, Botswana, Australien und der Demokratischen Republik Kongo. Bis 2005 produzierte Russland fast ein Fünftel der weltweiten Diamantenproduktion (hauptsächlich in Jakutien, z. B. im Mir-Pipe und im Udachnaya-Pipe), aber die Argyle-Mine in Australien wurde mit einer Produktion von 14 Millionen Karat im Jahr 2018 zur größten Einzelquelle. Neue Funde, die kanadischen Minen in Diavik und Ekati, werden voraussichtlich noch wertvoller werden, da sie Steine in Edelsteinqualität produzieren. ⓘ
In den Vereinigten Staaten wurden Diamanten in Arkansas, Colorado und Montana gefunden. Im Jahr 2004 führte die überraschende Entdeckung eines mikroskopisch kleinen Diamanten in den Vereinigten Staaten dazu, dass im Januar 2008 in einem abgelegenen Teil von Montana eine Großprobe von Kimberlit-Röhren genommen wurde. ⓘ
Anwendungen





Kohlenstoff ist für alle bekannten lebenden Systeme unerlässlich, und ohne ihn könnte das Leben, wie wir es kennen, nicht existieren (siehe alternative Biochemie). Abgesehen von Nahrungsmitteln und Holz wird Kohlenstoff in erster Linie in Form von Kohlenwasserstoffen wirtschaftlich genutzt, vor allem in Form des fossilen Brennstoffs Methangas und Rohöl (Petroleum). Rohöl wird in Raffinerien von der petrochemischen Industrie destilliert, um Benzin, Kerosin und andere Produkte herzustellen. Zellulose ist ein natürliches, kohlenstoffhaltiges Polymer, das von Pflanzen in Form von Holz, Baumwolle, Leinen und Hanf produziert wird. Zellulose wird in erster Linie für die Aufrechterhaltung der Struktur von Pflanzen verwendet. Kommerziell wertvolle Kohlenstoffpolymere tierischen Ursprungs sind Wolle, Kaschmir und Seide. Kunststoffe werden aus synthetischen Kohlenstoffpolymeren hergestellt, bei denen häufig Sauerstoff- und Stickstoffatome in regelmäßigen Abständen in die Hauptpolymerkette eingebaut sind. Die Rohstoffe für viele dieser synthetischen Stoffe werden aus Erdöl gewonnen. ⓘ
Die Verwendungsmöglichkeiten von Kohlenstoff und seinen Verbindungen sind äußerst vielfältig. Er kann mit Eisen Legierungen bilden, von denen die häufigste Kohlenstoffstahl ist. Graphit wird mit Tonen kombiniert, um die "Mine" zu bilden, die in Bleistiften zum Schreiben und Zeichnen verwendet wird. Es wird auch als Schmiermittel und Pigment, als Formmaterial in der Glasherstellung, in Elektroden für Trockenbatterien und in der Galvanotechnik und Galvanoplastik, in Bürsten für Elektromotoren und als Neutronenmoderator in Kernreaktoren verwendet. ⓘ
Holzkohle wird als Zeichenmaterial in der Kunst, beim Grillen, in der Eisenverhüttung und in vielen anderen Bereichen verwendet. Holz, Kohle und Öl werden als Brennstoff für die Energieerzeugung und zum Heizen verwendet. Diamanten in Edelsteinqualität werden in der Schmuckherstellung verwendet, und Industriediamanten werden in Bohr-, Schneid- und Polierwerkzeugen für die Bearbeitung von Metallen und Stein eingesetzt. Kunststoffe werden aus fossilen Kohlenwasserstoffen hergestellt, und Kohlenstofffasern, die durch Pyrolyse synthetischer Polyesterfasern gewonnen werden, dienen zur Verstärkung von Kunststoffen und zur Herstellung moderner, leichter Verbundwerkstoffe. ⓘ
Kohlenstofffasern werden durch Pyrolyse von extrudierten und verstreckten Filamenten aus Polyacrylnitril (PAN) und anderen organischen Substanzen hergestellt. Die kristallografische Struktur und die mechanischen Eigenschaften der Faser hängen von der Art des Ausgangsmaterials und von der anschließenden Verarbeitung ab. Kohlenstofffasern aus PAN haben eine Struktur, die an schmale Graphitfäden erinnert, aber durch die thermische Verarbeitung kann die Struktur zu einem kontinuierlichen, gewalzten Blatt umgestaltet werden. Das Ergebnis sind Fasern mit einer höheren spezifischen Zugfestigkeit als Stahl. ⓘ
Ruß wird als schwarzes Pigment in Druckfarben, Öl- und Wasserfarben, Kohlepapier, Autolacken, Tusche und Laserdruckertoner verwendet. Ruß wird auch als Füllstoff in Gummiprodukten wie Reifen und in Kunststoffmischungen verwendet. Aktivkohle wird als Absorptions- und Adsorptionsmittel in Filtermaterialien für so unterschiedliche Anwendungen wie Gasmasken, Wasseraufbereitung und Küchenabzugshauben sowie in der Medizin zur Absorption von Toxinen, Giften oder Gasen aus dem Verdauungssystem verwendet. Kohlenstoff wird bei der chemischen Reduktion bei hohen Temperaturen verwendet. Koks wird verwendet, um Eisenerz zu Eisen zu reduzieren (Schmelzen). Das Einsatzhärten von Stahl wird durch Erhitzen fertiger Stahlteile in Kohlenstoffpulver erreicht. Karbide aus Silizium, Wolfram, Bor und Titan gehören zu den härtesten bekannten Materialien und werden als Schleifmittel in Schneid- und Schleifwerkzeugen verwendet. Kohlenstoffverbindungen bilden die meisten Materialien für Kleidung, wie natürliche und synthetische Textilien und Leder, und fast alle Innenoberflächen in der gebauten Umwelt, mit Ausnahme von Glas, Stein und Metall. ⓘ
Diamanten
Die Diamantenindustrie lässt sich in zwei Kategorien einteilen: die eine befasst sich mit Diamanten in Edelsteinqualität, die andere mit Diamanten in Industriequalität. Obwohl beide Arten von Diamanten in großem Umfang gehandelt werden, unterscheiden sich die beiden Märkte grundlegend. ⓘ
Im Gegensatz zu Edelmetallen wie Gold oder Platin werden Schmuckdiamanten nicht als Ware gehandelt: Beim Verkauf von Diamanten wird ein erheblicher Aufschlag erhoben, und es gibt keinen sehr aktiven Markt für den Weiterverkauf von Diamanten. ⓘ
Industriediamanten werden vor allem wegen ihrer Härte und Wärmeleitfähigkeit geschätzt, wobei die gemmologischen Eigenschaften Klarheit und Farbe meist keine Rolle spielen. Etwa 80 % der geförderten Diamanten (das entspricht etwa 100 Millionen Karat oder 20 Tonnen pro Jahr) sind für die Verwendung als Edelsteine ungeeignet und werden für industrielle Zwecke verwendet (bekannt als Bort). Synthetische Diamanten, die in den 1950er Jahren erfunden wurden, fanden fast sofort industrielle Anwendungen; jährlich werden 3 Milliarden Karat (600 Tonnen) synthetische Diamanten hergestellt. ⓘ
In der Industrie werden Diamanten hauptsächlich zum Schneiden, Bohren, Schleifen und Polieren verwendet. Für die meisten dieser Anwendungen sind keine großen Diamanten erforderlich; tatsächlich können die meisten Diamanten von Edelsteinqualität, abgesehen von ihrer geringen Größe, industriell verwendet werden. Diamanten werden in Bohrspitzen oder Sägeblätter eingebettet oder zu einem Pulver gemahlen, das beim Schleifen und Polieren verwendet wird. Zu den spezialisierten Anwendungen gehören der Einsatz in Labors als Behälter für Hochdruckexperimente (siehe Diamant-Ambosszelle), Hochleistungslager und in begrenztem Umfang auch Spezialfenster. Mit den kontinuierlichen Fortschritten bei der Herstellung von synthetischen Diamanten werden neue Anwendungen möglich. Für viel Aufsehen sorgt die mögliche Verwendung von Diamant als Halbleiter für Mikrochips und wegen seiner außergewöhnlichen Wärmeleitfähigkeit als Kühlkörper in der Elektronik. ⓘ
Vorsichtsmaßnahmen
Reiner Kohlenstoff hat eine äußerst geringe Toxizität für den Menschen und kann in Form von Graphit oder Holzkohle sicher gehandhabt werden. Er ist resistent gegen Auflösung oder chemische Angriffe, selbst im sauren Inhalt des Verdauungstrakts. Wenn er also einmal in das Körpergewebe gelangt ist, kann er dort auf unbestimmte Zeit verbleiben. Ruß war wahrscheinlich eines der ersten Pigmente, die zum Tätowieren verwendet wurden, und bei Ötzi, dem Mann aus dem Eis, wurden Ruß-Tätowierungen gefunden, die während seines Lebens und 5200 Jahre nach seinem Tod erhalten blieben. Das Einatmen von Kohlenstaub oder Ruß (Carbon Black) in großen Mengen kann gefährlich sein, da es das Lungengewebe reizt und die Lungenkrankheit Kohlenarbeiter-Pneumokoniose verursacht. Diamantstaub, der als Schleifmittel verwendet wird, kann schädlich sein, wenn er verschluckt oder eingeatmet wird. In den Abgasen von Dieselmotoren entstehen mikroskopisch kleine Kohlenstoffpartikel, die sich in der Lunge ansammeln können. In diesen Beispielen kann die Schädigung durch Verunreinigungen (z. B. organische Chemikalien, Schwermetalle) und nicht durch den Kohlenstoff selbst verursacht werden. ⓘ
Kohlenstoff hat im Allgemeinen eine geringe Toxizität für das Leben auf der Erde, aber Kohlenstoff-Nanopartikel sind für Drosophila tödlich. ⓘ
Kohlenstoff kann in Gegenwart von Luft bei hohen Temperaturen stark und hell brennen. Große Kohleansammlungen, die in Abwesenheit von Sauerstoff über Hunderte von Millionen von Jahren inert geblieben sind, können sich spontan entzünden, wenn sie in Abraumhalden von Kohlebergwerken, Schiffsladeräumen, Kohlebunkern und Lagerstätten der Luft ausgesetzt werden. ⓘ
Bei nuklearen Anwendungen, bei denen Graphit als Neutronenmoderator eingesetzt wird, kann es zu einer Akkumulation von Wigner-Energie mit anschließender plötzlicher, spontaner Freisetzung kommen. Durch Glühen auf mindestens 250 °C kann die Energie sicher freigesetzt werden, doch beim Brand in Windscale ging das Verfahren schief, so dass andere Reaktormaterialien in Brand gerieten. ⓘ
Zu den zahlreichen Kohlenstoffverbindungen gehören tödliche Gifte wie Tetrodotoxin, das Lektin Ricin aus den Samen der Rizinuspflanze Ricinus communis, Cyanid (CN-) und Kohlenmonoxid, aber auch lebenswichtige Stoffe wie Glukose und Eiweiß. ⓘ
Atommodell des Kohlenstoffs

Das Modell der Atom- und Molekülorbitale veranschaulicht, wie es zu der unterschiedlichen Ausprägung der Erscheinungsformen des Kohlenstoffs kommt. ⓘ
Kohlenstoff besitzt sechs Elektronen. Nach dem Schalenmodell besetzen zwei Elektronen die innere 1s-Schale. Das 2s-Niveau der zweiten Schale nimmt ebenfalls zwei Elektronen auf, zwei weitere das 2px- und 2py- Niveau. Nur die vier äußeren Elektronen der zweiten Schale treten chemisch in Erscheinung. Die Aufenthaltswahrscheinlichkeit der Elektronen in einem s-Niveau ist kugelförmig. In einem p-Niveau ist sie anisotrop. Die Elektronen bevölkern einen sanduhrförmigen Raum, jeweils eine Sanduhrhälfte links und rechts vom Zentrum entlang der x-Achse, wenn man sich das Atom im Zentrum eines kartesischen Koordinatensystems platziert vorstellt. Senkrecht dazu stehen das py- und pz-Orbital (gemäß y- und z-Achse). ⓘ
Erscheinungsformen des Kohlenstoffs
Modifikationen
Chaoit
Chaoit ist eine sehr seltene Modifikation, die ähnlich wie Graphit im hexagonalen Kristallsystem kristallisiert, jedoch mit anderen Gitterparametern und leicht abweichender Kristallstruktur. Er entsteht ähnlich wie Lonsdaleit durch Schock-Metamorphose in graphitischem Gneis. ⓘ
Cyclo[18]carbon
Cyclo[18]carbon ist eine 2019 entdeckte cyclische Modifikation des Kohlenstoffs mit der Summenformel C18, die bei tiefen Temperaturen nahe dem absoluten Nullpunkt stabil ist. [18carbon ⓘ]
Weitere Formen des Kohlenstoffs
Amorpher Kohlenstoff
In amorphem Kohlenstoff (a-C) sind die Atome ohne langreichweitige Ordnung vernetzt. Das Material lässt sich mit nahezu beliebigen sp2:sp3-Hybridisierungsverhältnissen herstellen, wobei die Materialeigenschaften fließend von denen des Graphits zu denen des Diamanten übergehen. In der Industrie wird in diesem Fall häufig der Begriff Diamond-like Coating oder Diamond-like Carbon (DLC) verwendet. Bei einem sp3-Hybridisierungsanteil von über 70 % spricht man von tetraedrisch amorphem Kohlenstoff (ta-C). Dieses Material zeichnet sich durch hohen elektrischen Widerstand, extreme Härte und optische Transparenz aus. Die Herstellung kann mittels PVD- oder PECVD-Methoden erfolgen. Das Material wird dabei als Schicht abgeschieden (amorphe Kohlenstoffschicht). ⓘ
Kohlenstoff-Fasern
Kohlenstoff-Fasern bestehen aus graphitartig sp2-gebundenem Kohlenstoff. Isotrope Fasern verhalten sich ähnlich wie polykristalliner Graphit und besitzen nur geringe Festigkeiten. Fasermatten und -bündel werden für Wärmedichtungen eingesetzt. Durch Strecken bei der Herstellung ist es möglich, die Basalebenen entlang der Faserachse auszurichten. Man erhält hochfeste Fasern mit Eigenschaften, die den theoretischen Werten von Graphit entlang der Basalebenen nahekommen. Anisotrope Kohlenstofffasern sind leicht, außerordentlich steif und fest und werden in Verbundwerkstoffen genutzt. ⓘ
Glaskohlenstoff

Glaskohlenstoff („Glassy Carbon“) ist ein hochtechnologischer Werkstoff aus reinem Kohlenstoff, der glasartige und keramische Eigenschaften mit denen des Graphits vereint. Im Gegensatz zu Graphit besitzt Glaskohlenstoff eine fullerenartige Mikrostruktur. Dadurch ergibt sich eine große Vielfalt positiver Materialeigenschaften. Die Leitfähigkeit ist zum Beispiel geringer als bei Graphit. ⓘ
Graphen
Als Graphen bezeichnet man eine Graphit-Basalebene von sp2-hybridisiertem Kohlenstoff. Man erhält die dünnen Schichten durch chemisches Spalten von Graphit. Eingebettet in Kunststoffen eignet es sich als Ausgangsmaterial für neue Verbundwerkstoffe oder für Untersuchungen von zweidimensionalen Kristallen, außerdem wird an Anwendungen in der Elektronik geforscht. ⓘ
Aktivkohle
Behutsames Graphitieren von organischen Materialien, wie zum Beispiel Kokosnuss-Schalen, führt zu einem porösen Kohlenstoff. Die Hohlräume stehen wie bei einem Schwamm miteinander in Verbindung und bilden eine sehr große innere Oberfläche. Aktivkohle filtert gelöste Stoffe in geringer Konzentration aus Flüssigkeiten und kann Gase adsorbieren. ⓘ
Ruß
Ruß besteht ebenfalls aus Kohlenstoff auf Graphitbasis. Je reiner der Ruß, desto deutlicher treten die Eigenschaften von Graphit hervor. Lampen- oder Kerzenruß ist stark mit organischen Verbindungen verunreinigt, die die Bildung größerer Graphit-Verbände verhindern. ⓘ
Kohlenstoffnanoröhren
Eine weitere Form von Kohlenstoff sind zylindrisch angeordnete, sp2-hybridisierte Kohlenstoffatome. Ihre Geometrie entsteht aus einer planaren Schicht Graphit, die zu einem Zylinder aufgerollt wird. Die entstandene Röhre kann zusätzlich noch verdreht sein, wodurch sich die elektrischen Eigenschaften ändern. Es können mehrere einwandige Röhren konzentrisch ineinander liegen, so dass man von multiwalled carbon nanotubes (MWCNT) spricht, im Gegensatz zu single-walled carbon nanotubes (SWCNT). ⓘ
Carbon nanobuds
Carbon nanobuds kombinieren die Eigenschaften von Kohlenstoffnanoröhren und Fullerenen. ⓘ
Kohlenstoffnanoschaum
Kohlenstoffnanoschaum, ein Aerogel, ist eine zufällig orientierte, netzartige Anordnung von Kohlenstoff-Graphitebenen. Er ähnelt dem Glaskohlenstoff, nur mit deutlich größeren vernetzten Hohlräumen. Ihr durchschnittlicher Durchmesser liegt bei sechs bis neun Nanometern. ⓘ
Davon zu unterscheiden ist Kohlenstoff-Aerogel, das aus zusammengewachsenen Nanopartikeln besteht. Seine Dichte liegt bei 200 bis 1000 kg/m3. ⓘ
Aerographit
Aerographit besteht aus einem Netzwerk poröser Kohlenstoffröhrchen und ist mit einer Dichte von 0,2 Milligramm pro Kubikzentimeter einer der leichtesten Feststoffe der Welt. Aerographit lässt sich um bis zu 95 % komprimieren und wieder in die ursprüngliche Form auseinanderziehen. ⓘ
Nicht-graphitischer Kohlenstoff
„Nicht-graphitischer Kohlenstoff besteht aus Schichten von hexagonal angeordneten, sp2-hybridisierten Kohlenstoffatomen. Diese Schichten sind ohne jegliche dreidimensionale Fernordnung annähernd parallel gestapelt.“ Dieses Material besteht aus gegeneinander verdrehten und verschobenen Stapeln aus Graphenschichten. Diese Anordnung wird auch als turbostratisch bezeichnet. Hierbei kann der Abstand der Schichten untereinander deutlich von dem in Graphit gefundenen Schichtabstand abweichen. Die Mikrostrukturanalyse des Materials ist unter anderem mittels WAXS möglich, aufgrund der durch die signifikante Unordnung bedingten breiten und sich überlappenden Maxima können jedoch Standard-Verfahren wie die Scherrer-Gleichung nicht angewandt werden. ⓘ
Carbin (Perlenketten)
Innerhalb doppelwandiger Nanoröhrchen ist es im Jahre 2016 gelungen, als Carbin bezeichnete geradlinige Ketten zu synthetisieren, die aus mehr als 6000 Atomen bestehen. ⓘ
Q-carbon
Q-Carbon ist eine künstlich hergestellte diamantartige allotrope Form des Kohlenstoffs, die als ferromagnetisch und härter als Diamant beschrieben wird. ⓘ







