Alkaloide
Alkaloide sind eine Klasse von basischen, natürlich vorkommenden organischen Verbindungen, die mindestens ein Stickstoffatom enthalten. Zu dieser Gruppe gehören auch einige verwandte Verbindungen mit neutralen und sogar schwach sauren Eigenschaften. Einige synthetische Verbindungen mit ähnlicher Struktur können ebenfalls als Alkaloide bezeichnet werden. Neben Kohlenstoff, Wasserstoff und Stickstoff können Alkaloide auch Sauerstoff, Schwefel und, seltener, andere Elemente wie Chlor, Brom und Phosphor enthalten. ⓘ
Alkaloide werden von einer Vielzahl von Organismen wie Bakterien, Pilzen, Pflanzen und Tieren produziert. Sie können aus Rohextrakten dieser Organismen durch Säure-Base-Extraktion oder Lösungsmittelextraktion mit anschließender Kieselgelsäulenchromatographie gereinigt werden. Alkaloide haben ein breites Spektrum pharmakologischer Wirkungen, darunter Malariamittel (z. B. Chinin), Antiasthma (z. B. Ephedrin), Krebsmittel (z. B. Homoharringtonin), Cholinomimetika (z. B. Galantamin), gefäßerweiternde (z. B. Vincamin), antiarrhythmische (z. B. Chinidin), schmerzstillende (z. B. Morphin), antibakterielle (z. B. Chelerythrin) und blutzuckersenkende Wirkungen (z. B. Piperin). Viele von ihnen werden in der traditionellen oder modernen Medizin verwendet oder dienen als Ausgangspunkt für die Entdeckung neuer Arzneimittel. Andere Alkaloide besitzen psychotrope (z. B. Psilocin) und stimulierende Wirkungen (z. B. Kokain, Koffein, Nikotin, Theobromin) und wurden in entheogenen Ritualen oder als Freizeitdrogen verwendet. Alkaloide können auch giftig sein (z. B. Atropin, Tubocurarin). Obwohl Alkaloide auf eine Vielzahl von Stoffwechselsystemen bei Menschen und anderen Tieren wirken, rufen sie fast einheitlich einen bitteren Geschmack hervor. ⓘ
Die Grenze zwischen Alkaloiden und anderen stickstoffhaltigen Naturstoffen ist nicht klar gezogen. Verbindungen wie Aminosäurepeptide, Proteine, Nukleotide, Nukleinsäuren, Amine und Antibiotika werden normalerweise nicht als Alkaloide bezeichnet. Natürliche Verbindungen, die Stickstoff in der exozyklischen Position enthalten (Meskalin, Serotonin, Dopamin usw.), werden in der Regel als Amine und nicht als Alkaloide eingestuft. Einige Autoren betrachten Alkaloide jedoch als einen Sonderfall der Amine. ⓘ

Alkaloide (Wortbildung aus arabisch القلية, DMG al-qalya ‚die Pflanzenasche‘ und griechisch -oides: „ähnlich“) sind natürlich vorkommende, chemisch heterogene, meist alkalische, stickstoffhaltige organische Verbindungen des Sekundärstoffwechsels, die auf den tierischen, also auch menschlichen Organismus wirken. ⓘ
Über 10.000 verschiedene pflanzliche, tierische oder von Mikroorganismen produzierte Substanzen werden dieser Stoffgruppe zugeordnet. Der Begriff wurde 1819 zuerst für „alkaliähnliche“ Pflanzenstoffe wie Morphin, Strychnin und Solanin verwendet. Eine zufriedenstellende und allgemein akzeptierte Definition für den Begriff „Alkaloid“ existiert jedoch bis heute nicht. ⓘ
Benennung

Der Name "Alkaloide" wurde 1819 von dem deutschen Chemiker Carl Friedrich Wilhelm Meißner eingeführt und leitet sich von der spätlateinischen Wurzel alkali und dem Suffix -οειδής - ("wie") ab. Der Begriff wurde jedoch erst nach der Veröffentlichung eines Übersichtsartikels von Oscar Jacobsen im chemischen Wörterbuch von Albert Ladenburg in den 1880er Jahren allgemein verwendet. ⓘ
Für die Benennung von Alkaloiden gibt es keine einheitliche Methode. Viele Einzelnamen werden durch Anhängen des Suffixes "ine" an den Art- oder Gattungsnamen gebildet. So wird beispielsweise Atropin aus der Pflanze Atropa belladonna isoliert; Strychnin wird aus dem Samen des Strychninbaums (Strychnos nux-vomica L.) gewonnen. Wenn mehrere Alkaloide aus einer Pflanze gewonnen werden, werden die Namen oft durch unterschiedliche Suffixe unterschieden: "Idin", "Anin", "Alin", "Inin" usw. Außerdem gibt es mindestens 86 Alkaloide, deren Namen die Wurzel "vin" enthalten, weil sie aus Vinca-Pflanzen wie Vinca rosea (Catharanthus roseus) gewonnen werden; diese werden Vinca-Alkaloide genannt. ⓘ
Geschichte

Alkaloidhaltige Pflanzen werden von den Menschen seit der Antike zu therapeutischen und erholsamen Zwecken verwendet. So sind beispielsweise in Mesopotamien seit etwa 2000 v. Chr. Heilpflanzen bekannt. In der Odyssee von Homer wird auf ein Geschenk der ägyptischen Königin an Helena verwiesen, eine Droge, die Vergessenheit bringt. Es wird angenommen, dass es sich bei dem Geschenk um eine opiumhaltige Droge handelte. In einem chinesischen Buch über Zimmerpflanzen aus dem 1. bis 3. Jahrhundert v. Chr. wird eine medizinische Verwendung von Ephedra und Schlafmohn erwähnt. Auch Kokablätter werden von den südamerikanischen Indianern seit dem Altertum verwendet. ⓘ
Extrakte aus Pflanzen, die giftige Alkaloide wie Aconitin und Tubocurarin enthalten, wurden seit der Antike zur Vergiftung von Pfeilen verwendet. ⓘ
Die Erforschung der Alkaloide begann im 19. Jahrhundert. Jahrhundert. 1804 isolierte der deutsche Chemiker Friedrich Sertürner aus Opium ein "schlafförderndes Prinzip" (lateinisch: principium somniferum), das er in Anlehnung an den griechischen Gott der Träume Morpheus "Morphium" nannte; im Deutschen und in einigen anderen mitteleuropäischen Sprachen ist dies noch heute der Name der Droge. Der im Englischen und Französischen verwendete Begriff "Morphine" stammt von dem französischen Physiker Joseph Louis Gay-Lussac. ⓘ
Einen wichtigen Beitrag zur Chemie der Alkaloide leisteten in den ersten Jahren ihrer Entwicklung die französischen Forscher Pierre Joseph Pelletier und Joseph Bienaimé Caventou, die Chinin (1820) und Strychnin (1818) entdeckten. Zu dieser Zeit wurden mehrere andere Alkaloide entdeckt, darunter Xanthin (1817), Atropin (1819), Koffein (1820), Coniin (1827), Nikotin (1828), Colchicin (1833), Spartein (1851) und Kokain (1860). Die Entwicklung der Chemie der Alkaloide wurde durch das Aufkommen der spektroskopischen und chromatographischen Methoden im 20. Jahrhundert beschleunigt, so dass bis 2008 mehr als 12 000 Alkaloide identifiziert wurden. ⓘ
Die erste vollständige Synthese eines Alkaloids gelang im Jahr 1886 dem deutschen Chemiker Albert Ladenburg. Er stellte Coniin her, indem er 2-Methylpyridin mit Acetaldehyd umsetzte und das entstandene 2-Propenylpyridin mit Natrium reduzierte. ⓘ

Klassifizierungen

Im Vergleich zu den meisten anderen Klassen von Naturstoffen zeichnen sich die Alkaloide durch eine große strukturelle Vielfalt aus. Es gibt keine einheitliche Klassifizierung. Ursprünglich, als das Wissen über die chemischen Strukturen noch nicht vorhanden war, stützte man sich auf die botanische Klassifizierung der Ausgangspflanzen. Diese Klassifizierung gilt heute als veraltet. ⓘ
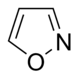
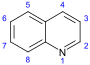
Neuere Klassifizierungen beruhen auf der Ähnlichkeit des Kohlenstoffgerüsts (z. B. Indol-, Isochinolin- und Pyridin-ähnlich) oder der biochemischen Vorstufe (Ornithin, Lysin, Tyrosin, Tryptophan usw.). Sie erfordern jedoch in Grenzfällen Kompromisse; so enthält Nikotin ein Pyridinfragment aus Nikotinamid und einen Pyrrolidinanteil aus Ornithin und kann daher beiden Klassen zugeordnet werden. ⓘ
Alkaloide werden häufig in die folgenden Hauptgruppen eingeteilt:
- "Echte Alkaloide" enthalten Stickstoff im Heterozyklus und stammen von Aminosäuren ab. Ihre charakteristischen Beispiele sind Atropin, Nikotin und Morphin. Zu dieser Gruppe gehören auch einige Alkaloide, die neben dem Stickstoffheterozyklus Terpene (z. B. Evonin) oder Peptidfragmente (z. B. Ergotamin) enthalten. Die Piperidinalkaloide Coniin und Conicin können als echte Alkaloide (und nicht als Pseudoalkaloide: siehe unten) betrachtet werden, obwohl sie nicht von Aminosäuren abstammen.
- "Protoalkaloide", die Stickstoff enthalten (aber nicht den Stickstoff-Heterozyklus) und ebenfalls aus Aminosäuren stammen. Beispiele hierfür sind Meskalin, Adrenalin und Ephedrin.
- Polyaminalkaloide - Derivate von Putrescin, Spermidin und Spermin.
- Peptid- und Cyclopeptidalkaloide.
- Pseudoalkaloide - alkaloidähnliche Verbindungen, die nicht von Aminosäuren abstammen. Zu dieser Gruppe gehören terpenartige und steroidartige Alkaloide sowie purinartige Alkaloide wie Koffein, Theobromin, Theacrin und Theophyllin. Einige Autoren stufen Verbindungen wie Ephedrin und Cathinon als Pseudoalkaloide ein. Diese stammen von der Aminosäure Phenylalanin ab, erhalten ihr Stickstoffatom aber nicht von der Aminosäure, sondern durch Transaminierung. ⓘ
Einige Alkaloide haben nicht das für ihre Gruppe charakteristische Kohlenstoffgerüst. So enthalten Galanthamin und Homoaporphine kein Isochinolinfragment, werden aber im Allgemeinen den Isochinolinalkaloiden zugerechnet. ⓘ
Die Hauptklassen der monomeren Alkaloide sind in der nachstehenden Tabelle aufgeführt:
| Klasse | Wichtigste Gruppen | Wichtigste Syntheseschritte | Beispiele ⓘ |
|---|---|---|---|
| Alkaloide mit Stickstoffheterozyklen (echte Alkaloide) | |||
| Pyrrolidin-Derivate | Ornithin oder Arginin → Putrescin → N-Methylputrescin → N-Methyl-Δ1-pyrrolin | Cuscohygrin, Hygrin, Hygrolin, Stachydrin | |
| Tropan-Derivate | Atropin-Gruppe Substitution in den Stellungen 3, 6 oder 7 |
Ornithin oder Arginin → Putrescin → N-Methylputrescin → N-Methyl-Δ1-pyrrolin | Atropin, Scopolamin, Hyoscyamin |
| Kokaingruppe Substitution in den Stellungen 2 und 3 |
Kokain, Ecgonin | ||
| Pyrrolizidin-Derivate | Nicht-Ester | In Pflanzen: Ornithin oder Arginin → Putrescin → Homospermidin → Retronecin | Retronecin, Heliotridin, Laburnin |
| Komplexe Ester von Monocarbonsäuren | Indicin, Lindelophin, Sarrazin | ||
| Makrozyklische Diester | Platyphyllin, Trichodesmin | ||
| 1-Aminopyrrolizidine (Loline) | Bei Pilzen: L-Prolin + L-Homoserin → N-(3-Amino-3-carboxypropyl)prolin → Norlolin | Lolin, N-Formyllolin, N-Acetyllolin | |
| Piperidin-Derivate | Lysin → Kadaverin → Δ1-Piperidin | Sedamin, Lobelin, Anaferin, Piperin | |
| Octansäure → Conicein → Coniin | Coniin, Conicin | ||
| Quinolizidin-Derivate | Lupinin-Gruppe | Lysin → Kadaverin → Δ1-Piperidin | Lupinin, Nupharidin |
| Cytisin-Gruppe | Cytisin | ||
| Spartein-Gruppe | Spartein, Lupanin, Anahygrin | ||
| Matrin-Gruppe. | Matrin, Oxymatrin, Allomatridin | ||
| Ormosanin-Gruppe | Ormosanin, Piptantin | ||
| Indolizidin-Derivate | Lysin → δ-Semialdehyd der α-Aminoadipinsäure → Pipecolsäure → 1 Indolizidinon | Swainsonin, Castanospermin | |
| Pyridin-Derivate | Einfache Derivate von Pyridin | Nicotinsäure → Dihydronicotinsäure → 1,2-Dihydropyridin | Trigonellin, Ricinin, Arecolin |
| Polyzyklische nicht kondensierende Pyridinderivate | Nikotin, Nornikotin, Anabasin, Anatabin | ||
| Polyzyklische kondensierte Pyridin-Derivate | Actinidin, Enzianin, Pediculinin | ||
| Sesquiterpene Pyridinderivate | Nicotinsäure, Isoleucin | Evonin, Hippocratein, Triptonin | |
| Isochinolinderivate und verwandte Alkaloide | Einfache Derivate von Isochinolin | Tyrosin oder Phenylalanin → Dopamin oder Tyramin (für Alkaloide Amarillis) | Salsolin, Lophocerin |
| Derivate von 1- und 3-Isochinolinen | N-Methylcoridaldin, Noroxyhydrastinin | ||
| Derivate von 1- und 4-Phenyltetrahydroisochinolinen | Kryptostilin | ||
| Derivate des 5-Naftil-Isochinolins | Ancistrocladin | ||
| Derivate von 1- und 2-Benzyl-Isochinolinen | Papaverin, Laudanosin, Sendaverin | ||
| Cularin-Gruppe | Cularin, Yagonin | ||
| Pavine und Isopavine | Argemonin, Amurensin | ||
| Benzopyrrokoline | Kryptaustoline | ||
| Protoberberberine | Berberin, Canadin, Ophiocarpin, Mecambridin, Corydalin | ||
| Phthalidisochinoline | Hydrastin, Narkotin (Noscapin) | ||
| Spirobenzylisochinoline | Fumaricin | ||
| Ipecacuanha-Alkaloide | Emetin, Protoemetin, Ipecosid | ||
| Benzophenanthridine | Sanguinarin, Oxynitidin, Corynoloxin | ||
| Aporphine | Glaucin, Coridin, Liriodenin | ||
| Proaporphine | Pronuciferin, Glaziovin | ||
| Homoaporphine | Kreysiginin, Multifloramin | ||
| Homoproaporphine | Bulbocodin | ||
| Morphine | Morphin, Codein, Thebain, Sinomenin | ||
| Homomorphine | Kreysiginin, Androcymbin | ||
| Tropoloisochinoline | Imerubrin | ||
| Azofluoranthene | Rufescin, Imelutein | ||
| Amaryllis-Alkaloide | Lycorin, Ambellin, Tazettin, Galantamin, Montanin | ||
| Erythrina-Alkaloide | Erysodin, Erythroidin | ||
| Phenanthren-Derivate | Atherospermine | ||
| Protopine | Protopin, Oxomuramin, Corycavidin | ||
| Aristolactam | Doriflavin | ||
| Oxazol-Derivate | Tyrosin → Tyramin | Annulolin, Halfordinol, Texalin, Texamin | |
| Isoxazol-Derivate | Ibotensäure → Muscimol | Ibotensäure, Muscimol | |
| Thiazol-Derivate | 1-Desoxy-D-xylulose-5-phosphat (DOXP), Tyrosin, Cystein | Nostocyclamid, Thiostrepton | |
| Quinazolin-Derivate | 3,4-Dihydro-4-Chinazolon-Derivate | Anthranilsäure oder Phenylalanin oder Ornithin | Febrifugin |
| 1,4-Dihydro-4-Chinazolon-Derivate | Glycorin, Arborin, Glycosminin | ||
| Pyrrolidin- und Piperidin-Chinazolin-Derivate | Vazicin (Peganin) | ||
| Acridin-Derivate | Anthranilsäure | Rutacridon, Acronin | |
| Chinolinderivate | Einfache Chinolinderivate Derivate von 2-Chinolonen und 4-Chinolonen | Anthranilsäure → 3-Carboxychinolin | Cusparin, Echinopsin, Evocarpin |
| Trizyklische Terpenoide | Flindersin | ||
| Furanochinolin-Derivate | Dictamnin, Fagarin, Skimmianin | ||
| Chinine | Tryptophan → Tryptamin → Strictosidin (mit Secologanin) → Korinanteal → Cinhoninon | Chinin, Chinidin, Cinchonin, Cinhonidin | |
| Indol-Derivate | Nicht-Isopren-Indolalkaloide | ||
| Einfache Indolderivate | Tryptophan → Tryptamin oder 5-Hydroxytryptophan | Serotonin, Psilocybin, Dimethyltryptamin (DMT), Bufotenin | |
| Einfache Derivate von β-Carbolin | Harman, Harmin, Harmalin, Eleagnin | ||
| Pyrroloindol-Alkaloide | Physostigmin (Esterin), Etheramin, Physovenin, Eptastigmin | ||
| Semiterpenoide Indolalkaloide | |||
| Ergot-Alkaloide | Tryptophan → Chanoclavin → Agroclavin → Elimoclavin → Paspalinsäure → Lysergsäure | Ergotamin, Ergobasin, Ergosin | |
| Monoterpenoide Indolalkaloide | |||
| Alkaloide vom Corynanthe-Typ | Tryptophan → Tryptamin → Strictosidin (mit Secologanin) | Ajmalicin, Sarpagin, Vobasin, Ajmalin, Yohimbin, Reserpin, Mitragynin, Strychnin-Gruppe und (Strychnin-Brucin, Aquamcin, Vomicin) | |
| Iboga-artige Alkaloide | Ibogamin, Ibogain, Voacangin | ||
| Alkaloide vom Aspidosperma-Typ | Vincamin, Vinca-Alkaloide, Vincotin, Aspidospermin | ||
| Imidazol-Derivate | Direkt aus Histidin | Histamin, Pilocarpin, Pilosin, Stevensin | |
| Purin-Derivate | Xanthosin (entsteht bei der Purinbiosynthese) → 7-Methylxantosin → 7-Methyl-Xanthin → Theobromin → Koffein | Koffein, Theobromin, Theophyllin, Saxitoxin | |
| Alkaloide mit Stickstoff in der Seitenkette (Protoalkaloide) | |||
| β-Phenylethylamin-Derivate | Tyrosin oder Phenylalanin → Dioxyphenilalanin → Dopamin → Adrenalin und Meskalin Tyrosin → Tyramin Phenylalanin → 1-Phenylpropan-1,2-dion → Cathinon → Ephedrin und Pseudoephedrin | Tyramin, Ephedrin, Pseudoephedrin, Meskalin, Cathinon, Katecholamine (Adrenalin, Noradrenalin, Dopamin) | |
| Colchicin-Alkaloide | Tyrosin oder Phenylalanin → Dopamin → Herbstalin → Colchicin | Colchicin, Colchamin | |
| Muscarin | Glutaminsäure → 3-Ketoglutaminsäure → Muscarin (mit Brenztraubensäure) | Muscarin, Allomuscarin, Epimuscarin, Epiallomuscarin | |
| Benzylamin | Phenylalanin mit Valin, Leucin oder Isoleucin | Capsaicin, Dihydrocapsaicin, Nordihydrocapsaicin, Vanillylamin | |
| Polyamin-Alkaloide | |||
| Putrescin-Derivate | Ornithin → Putrescin → Spermidin → Spermin | Paucin | |
| Spermidin-Derivate | Lunarin, Codonocarpin | ||
| Spermien-Derivate | Verbascenin, Aphelandrin | ||
| Peptid-(Cyclopeptid-)Alkaloide | |||
| Peptidalkaloide mit einem 13-gliedrigen Zyklus | Nummularin C-Typ | Aus verschiedenen Aminosäuren | Nummularin C, Nummularin S |
| Ziziphin-Typ | Ziziphin A, Sativanin H | ||
| Peptidalkaloide mit einem 14-gliedrigen Zyklus | Frangulanin-Typ | Frangulanin, Scutianin J | |
| Scutianin A-Typ | Scutianin A | ||
| Integerin-Typ | Integerin, Diskarin D | ||
| Amphibin F-Typ | Amphibin F, Spinanin A | ||
| Amfibin B-Typ | Amphibin B, Lotosin C | ||
| Peptidalkaloide mit einem 15-gliedrigen Zyklus | Mucronin A-Typ | Mucronin A | |
| Pseudoalkaloide (Terpene und Steroide) | |||
| Diterpene | Lycoctonin-Typ | Mevalonsäure → Isopentenylpyrophosphat → Geranylpyrophosphat | Aconitin, Delphinin |
| Steroidale Alkaloide | Cholesterin, Arginin | Solanidin, Cyclopamin, Batrachotoxin | |
Eigenschaften

Die meisten Alkaloide enthalten Sauerstoff in ihrer Molekularstruktur; diese Verbindungen sind bei Umgebungsbedingungen normalerweise farblose Kristalle. Sauerstofffreie Alkaloide, wie Nikotin oder Coniin, sind in der Regel flüchtige, farblose, ölige Flüssigkeiten. Einige Alkaloide sind farbig, wie Berberin (gelb) und Sanguinarin (orange). ⓘ
Die meisten Alkaloide sind schwache Basen, aber einige, wie Theobromin und Theophyllin, sind amphoter. Viele Alkaloide lösen sich schlecht in Wasser, aber leicht in organischen Lösungsmitteln, wie Diethylether, Chloroform oder 1,2-Dichlorethan. Koffein, Kokain, Codein und Nikotin sind in Wasser schwer löslich (mit einer Löslichkeit von ≥1 g/L), während andere, darunter Morphin und Yohimbin, nur sehr schwach wasserlöslich sind (0,1-1 g/L). Alkaloide und Säuren bilden Salze in unterschiedlicher Stärke. Diese Salze sind in der Regel gut löslich in Wasser und Ethanol und schlecht löslich in den meisten organischen Lösungsmitteln. Ausnahmen sind Scopolaminhydrobromid, das in organischen Lösungsmitteln löslich ist, und das wasserlösliche Chininsulfat. ⓘ
Die meisten Alkaloide haben einen bitteren Geschmack oder sind giftig, wenn sie eingenommen werden. Die Alkaloidproduktion in Pflanzen scheint sich als Reaktion auf die Ernährung durch pflanzenfressende Tiere entwickelt zu haben; einige Tiere haben jedoch die Fähigkeit entwickelt, Alkaloide zu entgiften. Einige Alkaloide können bei den Nachkommen von Tieren, die die Alkaloide aufnehmen, aber nicht entgiften können, Entwicklungsstörungen hervorrufen. Ein Beispiel ist das Alkaloid Cyclopamin, das in den Blättern der Kornblume vorkommt. In den 1950er Jahren wiesen bis zu 25 % der Lämmer von Schafen, die Maislilie gefressen hatten, schwere Gesichtsverformungen auf. Diese reichten von deformierten Kiefern bis hin zur Zyklopie (siehe Abbildung). Nach jahrzehntelanger Forschung wurde in den 1980er Jahren die für diese Missbildungen verantwortliche Verbindung als das Alkaloid 11-Desoxyjervin identifiziert, das später in Cyclopamin umbenannt wurde. ⓘ
Verbreitung in der Natur
Alkaloide werden von verschiedenen lebenden Organismen gebildet, insbesondere von höheren Pflanzen - etwa 10 bis 25 % dieser Pflanzen enthalten Alkaloide. Daher wurde in der Vergangenheit der Begriff "Alkaloid" mit Pflanzen in Verbindung gebracht. ⓘ
Der Alkaloidgehalt in Pflanzen liegt in der Regel im Bereich weniger Prozent und ist über das Pflanzengewebe inhomogen. Je nach Art der Pflanze ist die höchste Konzentration in den Blättern (z. B. Bilsenkraut), den Früchten oder Samen (Strychninbaum), der Wurzel (Rauvolfia serpentina) oder der Rinde (Cinchona) zu finden. Außerdem können verschiedene Gewebe derselben Pflanzen unterschiedliche Alkaloide enthalten. ⓘ
Außer in Pflanzen finden sich Alkaloide auch in bestimmten Pilzarten, wie Psilocybin im Pilz der Gattung Psilocybe, und in Tieren, wie Bufotenin in der Haut einiger Kröten und einer Reihe von Insekten, insbesondere Ameisen. Auch viele Meeresorganismen enthalten Alkaloide. Einige Amine, wie Adrenalin und Serotonin, die bei höheren Tieren eine wichtige Rolle spielen, ähneln in ihrer Struktur und Biosynthese den Alkaloiden und werden manchmal als Alkaloide bezeichnet. ⓘ
Extraktion
Aufgrund der strukturellen Vielfalt der Alkaloide gibt es keine einheitliche Methode für ihre Extraktion aus natürlichen Rohstoffen. Die meisten Methoden machen sich die Eigenschaft der meisten Alkaloide zunutze, in organischen Lösungsmitteln, nicht aber in Wasser löslich zu sein, und die gegenteilige Tendenz ihrer Salze. ⓘ
Die meisten Pflanzen enthalten mehrere Alkaloide. Ihr Gemisch wird zuerst extrahiert und dann werden die einzelnen Alkaloide abgetrennt. Die Pflanzen werden vor der Extraktion gründlich gemahlen. Die meisten Alkaloide liegen in den Rohpflanzen in Form von Salzen organischer Säuren vor. Die extrahierten Alkaloide können Salze bleiben oder sich in Basen umwandeln. Bei der Basenextraktion wird das Rohmaterial mit alkalischen Lösungen verarbeitet und die Alkaloidbasen mit organischen Lösungsmitteln wie 1,2-Dichlorethan, Chloroform, Diethylether oder Benzol extrahiert. Anschließend werden die Verunreinigungen durch schwache Säuren aufgelöst; dabei werden die Alkaloidbasen in Salze umgewandelt, die mit Wasser ausgewaschen werden. Falls erforderlich, wird eine wässrige Lösung der Alkaloidsalze erneut alkalisch gemacht und mit einem organischen Lösungsmittel behandelt. Der Vorgang wird so lange wiederholt, bis die gewünschte Reinheit erreicht ist. ⓘ
Bei der sauren Extraktion wird das pflanzliche Rohmaterial mit einer schwach sauren Lösung (z. B. Essigsäure in Wasser, Ethanol oder Methanol) behandelt. Anschließend wird eine Base zugegeben, um die Alkaloide in basische Formen umzuwandeln, die mit einem organischen Lösungsmittel extrahiert werden (wenn die Extraktion mit Alkohol durchgeführt wurde, wird dieser zuerst entfernt und der Rest in Wasser gelöst). Die Lösung wird wie oben beschrieben gereinigt. ⓘ
Die Alkaloide werden aufgrund ihrer unterschiedlichen Löslichkeit in bestimmten Lösungsmitteln und ihrer unterschiedlichen Reaktivität mit bestimmten Reagenzien oder durch Destillation von ihrem Gemisch getrennt. ⓘ
Eine Reihe von Alkaloiden wurde aus Insekten identifiziert, von denen die als Solenopsine bekannten Alkaloide aus dem Gift der Feuerameisen die größte Aufmerksamkeit der Forscher auf sich gezogen haben. Diese Insektenalkaloide können durch Eintauchen lebender Feuerameisen in Lösungsmittel oder durch Zentrifugieren lebender Ameisen und anschließende Reinigung durch Kieselgelchromatographie effizient extrahiert werden. Der Nachweis und die Dosierung der extrahierten Solenopsin-Ameisenalkaloide wurde anhand ihres Absorptionspeaks bei 232 Nanometern als möglich beschrieben. ⓘ
Die im biologischen Material hauptsächlich in Form ihrer Essig-, Oxal-, Milch-, Wein-, Aconit- oder Chinasäure-Salze, seltener in Reinform oder als Ester vorliegenden Alkaloide werden auf klassische Weise durch Extraktion gewonnen. Das Verfahren der Extraktion hängt von den physikochemischen Eigenschaften der zu isolierenden Alkaloide ab. Für die meisten Alkaloide hat sich die Verwendung des polaren Lösungsmittels Methanol unter Zusatz von Essigsäure bewährt. Nach Eindampfen und Aufnahme in einem wässrigen sauren Medium (z. B. verdünnte Salzsäure) können Fremdbestandteile, wie Fette und andere lipophile Stoffe, durch Extraktion mit dem lipophilen Lösungsmittel Ether entfernt werden. Für die Extraktion der Alkaloide aus der wässrigen Phase hat sich Chloroform nach Alkalisierung mit Natronlauge oder einer anderen geeigneten Base bewährt. Aus der Chloroformphase geht nach Trocknen und Eindampfen in der Regel ein Alkaloidgemisch hervor, das bevorzugt durch Chromatographie aufgetrennt werden kann. Zur Isolierung lipidunlöslicher Alkaloide mit einer quartären Ammoniumstruktur kann eine Fällung mit Pikrin- oder Reineckesäure dienen. ⓘ
Zudem ist für zahlreiche Alkaloide eine Partialsynthese oder chemische Totalsynthese möglich. Diese wendet man insbesondere an, wenn sie preisgünstiger als die Extraktion sind. Ein Beispiel für üblicherweise synthetisch hergestellte Alkaloide ist Theophyllin. ⓘ
Biosynthese
Biologische Vorläufer der meisten Alkaloide sind Aminosäuren, wie Ornithin, Lysin, Phenylalanin, Tyrosin, Tryptophan, Histidin, Asparaginsäure und Anthranilsäure. Nicotinsäure kann aus Tryptophan oder Asparaginsäure synthetisiert werden. Die Wege der Alkaloidbiosynthese sind zu zahlreich und lassen sich nicht einfach klassifizieren. Es gibt jedoch einige typische Reaktionen, die bei der Biosynthese der verschiedenen Alkaloidklassen ablaufen, darunter die Synthese von Schiffschen Basen und die Mannich-Reaktion. ⓘ
Synthese von Schiffschen Basen
Schiffsche Basen können durch Reaktion von Aminen mit Ketonen oder Aldehyden gewonnen werden. Diese Reaktionen sind eine gängige Methode zur Herstellung von C=N-Bindungen. ⓘ
Bei der Biosynthese von Alkaloiden können solche Reaktionen innerhalb eines Moleküls ablaufen, wie z. B. bei der Synthese von Piperidin:
Mannich-Reaktion
Integraler Bestandteil der Mannich-Reaktion ist neben einem Amin und einer Carbonylverbindung ein Carbanion, das bei der nukleophilen Addition an das durch die Reaktion von Amin und Carbonyl gebildete Ion die Rolle des Nukleophils spielt. ⓘ
Die Mannich-Reaktion kann sowohl intermolekular als auch intramolekular ablaufen:
Dimere Alkaloide
Neben den oben beschriebenen monomeren Alkaloiden gibt es auch dimere und sogar trimere und tetrameren Alkaloide, die durch Kondensation von zwei, drei und vier monomeren Alkaloiden entstehen. Dimere Alkaloide werden in der Regel aus Monomeren desselben Typs durch die folgenden Mechanismen gebildet:
- Mannich-Reaktion, die z. B. zu Voacamin führt
- Michael-Reaktion (Villalstonin)
- Kondensation von Aldehyden mit Aminen (Toxiferin)
- Oxidative Addition von Phenolen (Dauricin, Tubocurarin)
- Lactonisierung (Carpaine). ⓘ
Carpaine ⓘ
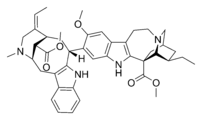
Es gibt auch dimere Alkaloide, die aus zwei verschiedenen Monomeren gebildet werden, wie die Vinca-Alkaloide Vinblastin und Vincristin, die aus der Kopplung von Catharanthin und Vindolin entstehen. Das neuere halbsynthetische Chemotherapeutikum Vinorelbin wird bei der Behandlung von nicht-kleinzelligem Lungenkrebs eingesetzt. Es ist ein weiteres Dimer-Derivat von Vindolin und Catharanthin und wird aus Anhydrovinblastin synthetisiert, entweder ausgehend von Leurosin oder den Monomeren selbst. ⓘ


Biologische Rolle
Alkaloide gehören zu den wichtigsten und bekanntesten Sekundärmetaboliten, d. h. zu den biogenen Stoffen, die nicht direkt am normalen Wachstum, der Entwicklung oder der Fortpflanzung des Organismus beteiligt sind. Stattdessen vermitteln sie im Allgemeinen ökologische Wechselwirkungen, die dem Organismus einen Selektionsvorteil verschaffen können, indem sie seine Überlebensfähigkeit oder Fruchtbarkeit erhöhen. In einigen Fällen bleibt ihre Funktion, wenn überhaupt, unklar. Eine frühe Hypothese, wonach Alkaloide die Endprodukte des Stickstoffmetabolismus in Pflanzen sind, wie Harnstoff und Harnsäure in Säugetieren, wurde durch die Feststellung widerlegt, dass ihre Konzentration eher schwankt als stetig zunimmt. ⓘ
Die meisten der bekannten Funktionen von Alkaloiden stehen im Zusammenhang mit dem Schutz. So schützt beispielsweise das Aporphinalkaloid Liriodenin, das vom Tulpenbaum produziert wird, diesen vor parasitären Pilzen. Außerdem hält das Vorhandensein von Alkaloiden in der Pflanze Insekten und Chordatiere davon ab, sie zu fressen. Einige Tiere sind jedoch an Alkaloide angepasst und verwenden sie sogar in ihrem eigenen Stoffwechsel. Alkaloidverwandte Substanzen wie Serotonin, Dopamin und Histamin sind wichtige Neurotransmitter bei Tieren. Es ist auch bekannt, dass Alkaloide das Pflanzenwachstum regulieren. Ein Beispiel für einen Organismus, der Alkaloide zum Schutz einsetzt, ist die Utetheisa ornatrix, besser bekannt als die Ornate Motte. Pyrrolizidin-Alkaloide machen die Larven und erwachsenen Motten für viele ihrer natürlichen Feinde wie Cocinelid-Käfer, Florfliegen, insektenfressende Hemiptera und insektenfressende Fledermäuse ungenießbar. Ein weiteres Beispiel für die Verwendung von Alkaloiden ist die Giftschierlingmotte (Agonopterix alstroemeriana). Diese Motte ernährt sich während ihres Larvenstadiums von ihrer hochgiftigen und alkaloidreichen Wirtspflanze, dem giftigen Schierling (Conium maculatum). A. alstroemeriana profitiert möglicherweise in zweifacher Hinsicht von der Toxizität der natürlich vorkommenden Alkaloide, zum einen durch die Ungenießbarkeit der Art für Fressfeinde und zum anderen durch die Fähigkeit von A. alstroemeriana, Conium maculatum als den richtigen Ort für die Eiablage zu erkennen. Ein als Solenopsin bekanntes Feuerameisengift-Alkaloid schützt nachweislich die Königinnen invasiver Feuerameisen bei der Gründung neuer Nester und spielt somit eine zentrale Rolle bei der weltweiten Ausbreitung dieser Schädlingsameisenart. ⓘ
Anwendungen
In der Medizin
Die medizinische Verwendung von alkaloidhaltigen Pflanzen hat eine lange Geschichte, und als im 19. Jahrhundert die ersten Alkaloide isoliert wurden, fanden sie sofort Anwendung in der klinischen Praxis. Viele Alkaloide werden immer noch in der Medizin verwendet, meist in Form von Salzen, zu denen die folgenden gehören:
| Alkaloid | Wirkung ⓘ |
|---|---|
| Ajmalin | Antiarrhythmikum |
| Emetin | antiprotozoisches Mittel,
Erbrechen |
| Ergot-Alkaloide | Vasokonstriktion, halluzinogen, Uterotonikum |
| Glaucine | Antitussivum |
| Morphium | Analgetikum |
| Nikotin | Stimulans, Agonist des nikotinischen Acetylcholinrezeptors |
| Physostigmin | Hemmstoff der Acetylcholinesterase |
| Quinidin | Antiarrhythmikum |
| Chinin | Fiebersenkend, Malariamittel |
| Reserpin | blutdrucksenkend |
| Tubocurarin | Muskelrelaxans |
| Vinblastin, Vincristin | Antitumormittel |
| Vincamin | gefäßerweiternd, blutdrucksenkend |
| Yohimbin | Stimulans, Aphrodisiakum |
Bei vielen synthetischen und halbsynthetischen Arzneimitteln handelt es sich um strukturelle Abwandlungen der Alkaloide, die die Hauptwirkung der Droge verstärken oder verändern und unerwünschte Nebenwirkungen verringern sollen. So ist beispielsweise Naloxon, ein Opioidrezeptor-Antagonist, ein Derivat des im Opium enthaltenen Thebain. ⓘ
In der Landwirtschaft
Vor der Entwicklung eines breiten Spektrums relativ gering toxischer synthetischer Pestizide wurden einige Alkaloide, wie z. B. Nikotinsalze und Anabasin, als Insektizide eingesetzt. Ihre Verwendung wurde durch ihre hohe Toxizität für den Menschen eingeschränkt. ⓘ
Verwendung als psychoaktive Drogen
Zubereitungen aus alkaloidhaltigen Pflanzen und deren Extrakten, später auch reine Alkaloide, werden seit langem als psychoaktive Substanzen verwendet. Kokain, Koffein und Cathinon sind Stimulanzien für das zentrale Nervensystem. Meskalin und viele Indolalkaloide (wie Psilocybin, Dimethyltryptamin und Ibogain) haben eine halluzinogene Wirkung. Morphin und Codein sind starke narkotische Schmerzmittel. ⓘ
Es gibt Alkaloide, die selbst keine starke psychoaktive Wirkung haben, aber Vorstufen für halbsynthetische psychoaktive Drogen sind. So werden beispielsweise Ephedrin und Pseudoephedrin zur Herstellung von Methcathinon und Methamphetamin verwendet. Thebain wird für die Synthese vieler Schmerzmittel wie Oxycodon verwendet. ⓘ
Siehe auch
- Amin
- Base (Chemie)
- Liste der giftigen Pflanzen
- Mayersches Reagenz
- Natürliche Produkte
- Palau'amin
- Sekundärer Metabolit ⓘ
Allgemeine und zitierte Referenzen
- Aniszewski, Tadeusz (2007). Alkaloide: Geheimnisse des Lebens. Amsterdam: Elsevier. ISBN 978-0-444-52736-3.
- Begley, Tadhg P. (2009). Enzyklopädie der chemischen Biologie. ChemBioChem. Vol. 10. Wiley. pp. 1569-1570. doi:10.1002/cbic.200900262. ISBN 978-0-471-75477-0.
- Brossi, Arnold (1989). Die Alkaloide: Chemie und Pharmakologie. Academic Press.
- Dewick, Paul M. (2002). Medizinische Naturprodukte: A Biosynthetic Approach (Zweite Auflage). Wiley. ISBN 978-0-471-49640-3.
- Fattorusso, E.; Taglialatela-Scafati, O. (2008). Moderne Alkaloide: Struktur, Isolierung, Synthese und Biologie. Wiley-VCH. ISBN 978-3-527-31521-5.
- Grinkevich NI; Safronich LN, eds. (1983). Die chemische Analyse von Heilpflanzen (in русский). Moskau: Vysshaya Shkola.
- Hesse, Manfred (2002). Alkaloide: Fluch oder Segen der Natur? Wiley-VCH. ISBN 978-3-906390-24-6.
- Knunyants, IL (1988). Chemische Enzyklopädie. Sowjetische Enzyklopädie.
- Orekhov, AP (1955). Chemie der Alkaloide (Acad. 2nd ed.). Moskau.
- Plemenkov, VV (2001). Einführung in die Chemie der Naturstoffe. Kasan.
- Saxton, J. E. (1971). Die Alkaloide: A Specialist Periodical Report. London: The Chemical Society.
- Veselovskaya, N. B.; Kovalenko, A. E. (2000). Drogen. Moskau: Triada-X.
- Wink, M. (2009). "Wirkungsweise und Toxikologie von Pflanzentoxinen und Giftpflanzen". Mitt. Julius Kühn-Inst. 421: 93-112x. ⓘ
Definitionen
Der Begriff Alkaloid war ursprünglich eine allgemeine Bezeichnung für aus Pflanzen isolierte basische Stoffe. Später wurden Alkaloide auch aus anderen Organismen, wie Pilzen (z. B. Mutterkornalkaloide) und Tieren (z. B. das Krötenalkaloid Bufotenin) isoliert, sodass die Definition erweitert wurde. Des Weiteren wurde der Alkaloidbegriff teilweise auch auf einige nicht basische Naturstoffe, wie das Herbstzeitlosen-Alkaloid Colchicin, das Capsaicin des Cayennepfeffers oder die Purin-Alkaloide Coffein, Theophyllin und Theobromin, ausgedehnt. ⓘ
Alle Alkaloide wirken charakteristisch auf den tierischen und menschlichen Organismus. Die meisten sind giftig und haben einen bitteren Geschmack. Die Basizität ist ein häufiges, aber nicht essenzielles Merkmal dieser Substanzgruppe. Basische Antibiotika, wie beispielsweise Streptomycin, die auf Mikroorganismen wirken, werden in der Regel nicht als Alkaloide bezeichnet. Darüber hinaus sind alle Alkaloide Produkte des Sekundärstoffwechsels. Sie werden für den Grundstoffwechsel der sie bildenden Organismen nicht benötigt, sondern dienen häufig als Schutz vor Fressfeinden. Basische Aminosäuren oder Peptide, die Primärstoffwechselprodukte sind, werden daher nicht den Alkaloiden zugeordnet. ⓘ
Einige strenge Definitionen fordern, dass der Stickstoff Teil eines heterocyclischen, biogenetisch von Aminosäuren abgeleiteten Systems ist. Diese Definition gliedert beispielsweise die Protoalkaloide Ephedrin und Mescalin sowie die Pseudoalkaloide Coniin und Coffein aus der Familie der Alkaloide aus. Auch Atropin ist als künstliches Racemisierungsprodukt des (S)-Hyoscyamins nach strenger Auslegung kein Alkaloid. ⓘ
Einteilung
Alkaloide können nach verschiedenen Kriterien unterteilt werden. Üblich sind Kategorisierungen nach chemischer Struktur, Herkunft, Biogenese und pharmakologischer Wirkung. ⓘ
Einteilung nach chemischer Struktur
Die in der Literatur am häufigsten verwendete Einteilung der Alkaloide ist die Kategorisierung entsprechend ihrer chemischen Struktur. Namensgebend ist der Teil des Moleküls, der das Stickstoffatom enthält.
- Alkaloide mit heterocyclischem Stickstoff
- Pyrrolidin-Alkaloide: z. B. Hygrin
- Pyrrolizidin-Alkaloide: z. B. Senezionin
- Steroid-Alkaloide: z. B. Solanin
- Pyridin-Alkaloide: z. B. Nicotin, Anabasin
- Piperidin-Alkaloide: z. B. Piperin
- Tropan-Alkaloide: z. B. Hyoscyamin, Scopolamin, Kokain
- Chinolin-Alkaloide: z. B. Chinin, Chinidin
- Isochinolin-Alkaloide: z. B. Morphin, Codein, Papaverin, Berberin, Tubocurarin
- Indolalkaloide: z. B. Ajmalin, Ergotamin, Yohimbin, Reserpin, Strychnin
- Purinalkaloide: z. B. Coffein, Theophyllin, Theobromin
- Imidazolalkaloide: z. B. Pilocarpin, Cynodin, Cynometrin, Odilin
- Acridon-Alkaloide: z. B. Acronycin, Melicopicin, Rutacridon
- Chinolizidin-Alkaloide: z. B. Lupinin, Spartein
- Benzylisochinolinalkaloide: z. B. Papaverin, Reticulin, Laudanosin
- Alkaloide mit acyclischem Stickstoff: z. B. Ephedrin, Mescalin ⓘ
Einteilung nach Biogenese
Eine weitere Einteilung der Alkaloide kann anhand von Gemeinsamkeiten und Unterschieden der Biosynthese erfolgen. Dabei werden Alkaloide entsprechend den Aminosäuren geordnet, die als Stickstoffquelle in der Biosynthese genutzt werden.
- Von Asparaginsäure oder Lysin abgeleitete Alkaloide: z. B. Nicotin, Lupinin
- Von Glycin abgeleitete Alkaloide: z. B. Coffein, Theophyllin, Theobromin
- Von Histidin abgeleitete Alkaloide: z. B. Pilocarpin
- Von Ornithin abgeleitete Alkaloide: z. B. Hyoscyamin, Scopolamin, Kokain
- Von Phenylalanin oder Tyrosin abgeleitete Alkaloide: z. B. Colchicin, Morphin, Codein, Papaverin, Tubocurarin, Berberin
- Von Tryptophan abgeleitete Alkaloide: z. B. Ergotamin, Ergometrin, Ajmalin, Reserpin, Strychnin ⓘ
Demgegenüber weist der Sammelbegriff Terpenalkaloide, zu denen beispielsweise das Diterpenalkaloid Aconitin und die Steroidalkaloide zählen, auf die biogenetische Herkunft des Kohlenstoffgrundgerüstes aus dem Terpenstoffwechsel hin. ⓘ
Einteilung nach pharmakologischer Wirkung
- Nach pharmakologischer Wirkung; z. B. Halluzinogene ⓘ
Analytik
Als klassisches Nachweisreagenz für Alkaloide wird Dragendorff-Reagenz verwendet. In Gegenwart von Alkaloiden bildet es ein Ionenpaar mit der Zusammensetzung [BiI4]−[NHR3]+, das, je nach Alkaloid, als gelboranges bis braunes Präzipitat zu erkennen ist. Alternativ dazu werden auch Mayers Reagenz (Tetraiodomercurat), Silicowolframsäure, Wagners Reagenz (Iod-Kaliumiodid), Sonnenscheins Reagenz (Phosphomolybdänsäure), Iodoplatinat und weitere als Nachweisreagenz verwendet. Die Selektivität dieser Nachweisreagenzien variiert stark und ist innerhalb der Gruppe der Alkaloide begrenzt. Um die Selektivität zu erhöhen, kombiniert man sie in der Regel mit chromatographischen Verfahren wie der Dünnschichtchromatographie. ⓘ