Graphit
| Graphit ⓘ | |
|---|---|
| Sehr reiner Graphit aus dem ehemaligen Ceylon, heute Sri Lanka | |
| Allgemeines und Klassifikation | |
| Andere Namen |
Grafit |
| Chemische Formel | C |
| Mineralklasse (und ggf. Abteilung) |
Elemente – Halbmetalle (Metalloide) und Nichtmetalle |
| System-Nr. nach Strunz und nach Dana |
1.CB.05a (8. Auflage: I/B.02a) 01.03.06.02 |
| Ähnliche Minerale | Molybdänit (Molybdänglanz) |
| Kristallographische Daten | |
| Kristallsystem | hexagonal |
| Kristallklasse; Symbol | dihexagonal-dipyramidal; 6/m 2/m 2/m |
| Raumgruppe | P63/mmc (Nr. 194) |
| Gitterparameter | a = 2,46 Å; c = 6,71 Å |
| Häufige Kristallflächen | {001} |
| Physikalische Eigenschaften | |
| Mohshärte | 1 bis 2 |
| Dichte (g/cm3) | 2,1 bis 2,3, beim idealen Einkristall 2,26 |
| Spaltbarkeit | vollkommen, Schichtabstand 3,35 Å beim idealen Einkristall |
| Bruch; Tenazität | uneben, biegsam |
| Farbe | grau bis schwarz |
| Strichfarbe | grauschwarz |
| Transparenz | undurchsichtig |
| Glanz | Metallglanz, matt |
| Magnetismus | diamagnetisch |
| Kristalloptik | |
| Brechungsindex | n = 1,93 bis 2,07 (rot) |
| Optischer Charakter | einachsig negativ |
| Pleochroismus | stark rot |
| Weitere Eigenschaften | |
| Chemisches Verhalten | unlöslich in nicht-oxidierenden Säuren |
| Besondere Merkmale | hohe Anisotropie (z. B. Härte, Leitfähigkeit) |
Graphit (auch Grafit) ist ein sehr häufig vorkommendes Mineral aus der Mineralklasse der „Elemente“. Er ist eine der natürlichen Erscheinungsformen des chemischen Elements Kohlenstoff in Reinform und kristallisiert äußerlich gesehen im hexagonalen Kristallsystem (genaueres siehe Kristallstruktur). ⓘ
Graphit bildet undurchsichtige, graue bis schwarze Kristalle in sechseckiger, tafeliger, schuppiger oder stängeliger Form, die auf den Kristallflächen Metallglanz aufweisen. Massige oder körnige Aggregate sind dagegen matt. Seine Mohshärte beträgt zwischen 1 und 2, seine Dichte etwa 2,1 bis 2,3 g/cm³, und er hat eine grauschwarze Strichfarbe. ⓘ
| Graphit ⓘ | |
|---|---|
 Graphit-Probe | |
| Allgemein | |
| Kategorie | Einheimisches Mineral |
| Formel (Wiederholungseinheit) | C |
| IMA-Symbol | Gr |
| Strunz-Klassifizierung | 1.CB.05a |
| Kristallsystem | Sechseckig |
| Kristallklasse | Dihexagonal dipyramidal (6/mmm) Hermann-Mauguin-Schreibweise: (6/m 2/m 2/m) |
| Raumgruppe | P63mc (geknickt) P63/mmc (flach) |
| Einheitszelle | a = 2,461, c = 6,708 [Å]; Z = 4 |
| Kennzeichnung | |
| Farbe | eisenschwarz bis stahlgrau; tiefblau im Durchlicht |
| Kristallform | tafelförmige, sechsseitig blättrige Massen, körnige bis verdichtete Massen |
| Verzwillingung | Vorhanden |
| Spaltbarkeit | Basal - perfekt auf {0001} |
| Bruch | Schuppig, sonst rau, wenn nicht auf der Spaltfläche |
| Zähigkeit | Flexibel, nicht elastisch, sektil |
| Härte nach Mohs-Skala | 1–2 |
| Glanz | Metallisch, erdig |
| Schlieren | Schwarz |
| Diaphanie | Undurchsichtig, transparent nur bei extrem dünnen Flocken |
| Spezifisches Gewicht | 1.9–2.3 |
| Dichte | 2,09-2,23 g/cm3 |
| Optische Eigenschaften | Uniaxial (-) |
| Pleochroismus | Stark |
| Löslichkeit | Löslich in geschmolzenem Nickel, warmer Chlorschwefelsäure |
| Andere Eigenschaften | stark anisotrop, leitet Elektrizität, fühlt sich fettig an, markiert leicht |
| Referenzen | |
Graphit (/ˈɡræfaɪt/) ist eine kristalline Form des Elements Kohlenstoff. Er besteht aus gestapelten Schichten von Graphen. Graphit kommt in der Natur vor und ist unter Standardbedingungen die stabilste Form des Kohlenstoffs. Synthetischer und natürlicher Graphit werden in großem Umfang (300 kt/Jahr im Jahr 1989) für die Herstellung von Bleistiften, Schmiermitteln und Elektroden verbraucht. Unter hohem Druck und bei hohen Temperaturen wandelt es sich in Diamant um. Er ist ein schwacher Wärme- und Stromleiter. ⓘ
Arten und Sorten
Naturgraphit
Die wichtigsten Arten von Naturgraphit, die jeweils in verschiedenen Erzlagerstätten vorkommen, sind ⓘ
- Kristalline kleine Graphitflocken (oder Flockengraphit) treten als isolierte, flache, plättchenförmige Partikel mit hexagonalen Kanten auf, wenn sie ungebrochen sind. Im gebrochenen Zustand können die Kanten unregelmäßig oder kantig sein;
- Amorpher Graphit: Sehr feiner Flockengraphit wird manchmal als amorph bezeichnet;
- Klumpengraphit (oder Adergraphit) tritt in Spaltadern oder Brüchen auf und erscheint als massives plattiges Einwachsen von faserigen oder nadelförmigen kristallinen Aggregaten und ist wahrscheinlich hydrothermalen Ursprungs.
- Hochgeordneter pyrolytischer Graphit ist Graphit mit einer Winkelspreizung zwischen den Graphitplatten von weniger als 1°.
- Die Bezeichnung "Graphitfaser" wird manchmal auch für Kohlenstofffasern oder kohlenstofffaserverstärkte Polymere verwendet. ⓘ
Vorkommen
Graphit kommt in metamorphen Gesteinen als Ergebnis der Reduktion von sedimentären Kohlenstoffverbindungen während der Metamorphose vor. Er kommt auch in Eruptivgestein und in Meteoriten vor. Zu den mit Graphit vergesellschafteten Mineralien gehören Quarz, Calcit, Glimmer und Turmalin. Die wichtigsten Exportquellen für abgebauten Graphit sind in der Reihenfolge der Tonnage: China, Mexiko, Kanada, Brasilien und Madagaskar. ⓘ
In Meteoriten kommt Graphit zusammen mit Troilit und Silikatmineralien vor. Kleine Graphitkristalle in meteoritischem Eisen werden als Cliftonit bezeichnet. Einige mikroskopisch kleine Körner weisen eine besondere Isotopenzusammensetzung auf, was darauf hindeutet, dass sie vor dem Sonnensystem entstanden sind. Sie gehören zu den etwa 12 bekannten Mineralienarten, die vor dem Sonnensystem entstanden sind und auch in Molekülwolken nachgewiesen wurden. Diese Minerale bildeten sich in den Auswürfen, wenn Supernovae explodierten oder Sterne geringer bis mittlerer Größe ihre äußeren Hüllen spät in ihrem Leben ausstießen. Graphit ist möglicherweise das zweit- oder drittälteste Mineral im Universum. ⓘ
Struktur
Graphit besteht aus Schichten aus trigonalem, planarem Kohlenstoff. Die einzelnen Schichten werden als Graphen bezeichnet. In jeder Schicht sind die Kohlenstoffatome in einem Bienenwabengitter mit einer Bindungslänge von 0,142 nm angeordnet, und der Abstand zwischen den Ebenen beträgt 0,335 nm. Die Bindungen zwischen den Schichten sind relativ schwache van-der-Waals-Bindungen und werden häufig von Gasen besetzt, wodurch sich die graphenartigen Schichten leicht voneinander trennen und aneinander vorbeigleiten lassen. ⓘ
Die elektrische Leitfähigkeit senkrecht zu den Schichten ist folglich etwa 1000-mal geringer. ⓘ
Die beiden Formen von Graphit heißen alpha (hexagonal) und beta (rhomboedrisch). Ihre Eigenschaften sind sehr ähnlich. Sie unterscheiden sich durch die Stapelung der Graphenschichten: Die Stapelung im Alpha-Graphit ist ABA, im Gegensatz zur ABC-Stapelung im energetisch weniger stabilen und selteneren Beta-Graphit. Die Alpha-Form kann durch mechanische Behandlung in die Beta-Form umgewandelt werden, und die Beta-Form kehrt in die Alpha-Form zurück, wenn sie über 1300 °C erhitzt wird. ⓘ
Einheitszelle von Alphagraphit ⓘ
Thermodynamik

Die Gleichgewichtsdruck- und -temperaturbedingungen für einen Übergang zwischen Graphit und Diamant sind theoretisch und experimentell gut belegt. Der Druck ändert sich linear zwischen 1,7 GPa bei 0 K und 12 GPa bei 5000 K (dem Tripelpunkt von Diamant/Graphit/Flüssigkeit). Die Phasen haben jedoch einen breiten Bereich um diese Linie, in dem sie koexistieren können. Bei normaler Temperatur und normalem Druck, d. h. bei 20 °C (293 K) und 1 Standardatmosphäre (0,10 MPa), ist die stabile Phase des Kohlenstoffs Graphit, während Diamant metastabil ist und seine Umwandlungsrate in Graphit vernachlässigbar ist. Bei Temperaturen über etwa 4500 K wandelt sich Diamant jedoch schnell in Graphit um. Für eine schnelle Umwandlung von Graphit in Diamant sind Drücke erforderlich, die weit über der Gleichgewichtslinie liegen: bei 2000 K ist ein Druck von 35 GPa erforderlich. ⓘ
Andere Eigenschaften

Die akustischen und thermischen Eigenschaften von Graphit sind in hohem Maße anisotrop, da sich Phononen schnell entlang der fest gebundenen Ebenen ausbreiten, aber langsamer von einer Ebene zur anderen wandern. Die hohe thermische Stabilität sowie die elektrische und thermische Leitfähigkeit von Graphit erleichtern seinen weit verbreiteten Einsatz als Elektroden und feuerfeste Materialien in der Hochtemperaturverarbeitung. In sauerstoffhaltigen Atmosphären oxidiert Graphit jedoch bei Temperaturen von 700 °C und darüber leicht zu Kohlendioxid. ⓘ
Graphit ist ein elektrischer Leiter und wird daher z. B. als Elektrode für Bogenlampen verwendet. Er kann Strom leiten, weil die Elektronen in den Kohlenstoffschichten stark delokalisiert sind (ein Phänomen, das als Aromatizität bezeichnet wird). Diese Valenzelektronen können sich frei bewegen und sind daher in der Lage, Strom zu leiten. Der Strom wird jedoch hauptsächlich in der Ebene der Schichten geleitet. Die leitfähigen Eigenschaften von pulverförmigem Graphit ermöglichen seine Verwendung als Drucksensor in Kohlenstoffmikrofonen. ⓘ
Graphit und Graphitpulver werden in industriellen Anwendungen wegen ihrer selbstschmierenden und trockenschmierenden Eigenschaften geschätzt. Häufig wird angenommen, dass die Schmiereigenschaften von Graphit ausschließlich auf die lockere interlamellare Kopplung zwischen den Schichten der Struktur zurückzuführen sind. Es hat sich jedoch gezeigt, dass Graphit in einer Vakuumumgebung (wie z. B. in Technologien für den Einsatz im Weltraum) aufgrund der hypoxischen Bedingungen als Schmiermittel abbaut. Diese Beobachtung führte zu der Hypothese, dass die Schmierung auf das Vorhandensein von Flüssigkeiten zwischen den Schichten, wie Luft und Wasser, zurückzuführen ist, die auf natürliche Weise aus der Umgebung adsorbiert werden. Diese Hypothese wurde durch Studien widerlegt, die zeigen, dass Luft und Wasser nicht absorbiert werden. Neuere Studien deuten darauf hin, dass die Schmiereigenschaften von Graphit auch auf einen Effekt namens Superlubricity zurückzuführen sind. Die Verwendung von Graphit wird dadurch eingeschränkt, dass er die Lochfraßkorrosion in einigen nichtrostenden Stählen begünstigt und die galvanische Korrosion zwischen ungleichen Metallen (aufgrund seiner elektrischen Leitfähigkeit) fördert. In Gegenwart von Feuchtigkeit wirkt es außerdem korrosiv auf Aluminium. Aus diesem Grund hat die US Air Force die Verwendung von Graphit als Schmiermittel in Aluminiumflugzeugen verboten und von der Verwendung in aluminiumhaltigen automatischen Waffen abgeraten. Selbst Graphitstiftmarkierungen auf Aluminiumteilen können die Korrosion fördern. Ein weiteres Hochtemperatur-Schmiermittel, hexagonales Bornitrid, hat die gleiche Molekularstruktur wie Graphit. Aufgrund seiner ähnlichen Eigenschaften wird es manchmal auch als weißer Graphit bezeichnet. ⓘ
Wenn eine große Anzahl kristallographischer Defekte diese Ebenen miteinander verbindet, verliert Graphit seine Schmiereigenschaften und wird zu so genanntem pyrolytischem Graphit. Außerdem ist er stark anisotrop und diamagnetisch, so dass er in der Luft über einem starken Magneten schwebt. Wird er in einer Wirbelschicht bei 1000-1300 °C hergestellt, ist er isotrop und turbostratisch und wird in Geräten verwendet, die mit Blut in Berührung kommen, wie z. B. mechanische Herzklappen, und wird pyrolytischer Kohlenstoff genannt. Pyrolytischer Graphit und pyrolytischer Kohlenstoff werden oft verwechselt, sind aber sehr unterschiedliche Materialien. ⓘ
Natürliche und kristalline Graphite werden aufgrund ihrer Scherflächen, ihrer Sprödigkeit und ihrer unbeständigen mechanischen Eigenschaften nicht oft in reiner Form als Konstruktionsmaterial verwendet. ⓘ
Geschichte der Verwendung von Naturgraphit

Im 4. Jahrtausend v. Chr., während der Jungsteinzeit in Südosteuropa, verwendete die Marița-Kultur Graphit in einer Keramikfarbe zur Verzierung von Töpferwaren. ⓘ
Irgendwann vor 1565 (manche Quellen sprechen von 1500) wurde an der Zufahrt zu Grey Knotts vom Weiler Seathwaite in der Gemeinde Borrowdale, Cumbria, England, aus ein riesiges Graphitvorkommen entdeckt, das die Einheimischen zur Kennzeichnung von Schafen nutzten. Während der Herrschaft von Elisabeth I. (1558-1603) wurde Borrowdale-Graphit als feuerfestes Material zum Auskleiden von Formen für Kanonenkugeln verwendet, was zu runderen, glatteren Kugeln führte, die weiter abgefeuert werden konnten und zur Stärke der englischen Marine beitrugen. Dieses besondere Graphitvorkommen war äußerst rein und weich und konnte leicht in Stöcke geschnitten werden. Aufgrund ihrer militärischen Bedeutung wurden diese einzigartige Mine und ihre Produktion von der Krone streng kontrolliert. ⓘ
Im 19. Jahrhundert wurden die Verwendungsmöglichkeiten von Graphit stark erweitert und umfassten Ofenpolitur, Schmiermittel, Farben, Schmelztiegel, Gießereiverkleidungen und Bleistifte, ein wichtiger Faktor bei der Verbreitung von Lehrmitteln während des ersten großen Aufschwungs der Bildung für die Massen. Das britische Empire kontrollierte den größten Teil der Weltproduktion (vor allem aus Ceylon), aber die Produktion aus österreichischen, deutschen und amerikanischen Lagerstätten expandierte bis Mitte des Jahrhunderts. Die 1845 von Joseph Dixon und seinem Partner Orestes Cleveland gegründete Dixon Crucible Company aus Jersey City, New Jersey, eröffnete beispielsweise Minen im Bezirk Lake Ticonderoga in New York, baute dort eine Verarbeitungsanlage und eine Fabrik zur Herstellung von Bleistiften, Tiegeln und anderen Produkten in New Jersey, die im Engineering & Mining Journal vom 21. Dezember 1878 beschrieben wurde. Der Dixon-Bleistift wird immer noch hergestellt. ⓘ

Die Anfänge des revolutionären Schaumflotationsverfahrens sind mit dem Graphitabbau verbunden. Der E&MJ-Artikel über die Dixon Crucible Company enthält eine Skizze der "schwimmenden Tanks", die bei dem uralten Verfahren zur Graphitgewinnung verwendet werden. Da Graphit so leicht ist, wurde das Gemisch aus Graphit und Abfällen durch eine letzte Reihe von Wassertanks geleitet, in denen ein sauberer Graphit "schwamm", während die Abfälle herausfielen. In einem Patent aus dem Jahr 1877 gingen die beiden Brüder Bessel (Adolph und August) aus Dresden noch einen Schritt weiter und fügten den Tanks eine kleine Menge Öl hinzu und kochten das Gemisch - ein Rühr- oder Schaumschritt -, um den Graphit aufzufangen, der erste Schritt zum späteren Flotationsverfahren. Adolph Bessel erhielt die Wohler-Medaille für das patentierte Verfahren, mit dem die Gewinnung von Graphit aus der deutschen Lagerstätte auf 90 % gesteigert werden konnte. Im Jahr 1977 veranstaltete die Deutsche Gesellschaft für Bergbauingenieure und Metallurgen ein spezielles Symposium, das ihrer Entdeckung und damit dem 100-jährigen Bestehen der Flotation gewidmet war. ⓘ
In den Vereinigten Staaten ließ sich Hezekiah Bradford aus Philadelphia 1885 ein ähnliches Verfahren patentieren, aber es ist ungewiss, ob sein Verfahren in den nahe gelegenen Graphitlagerstätten von Chester County, Pennsylvania, einem bedeutenden Produzenten in den 1890er Jahren, erfolgreich eingesetzt wurde. Das Bessel-Verfahren wurde nur in begrenztem Umfang eingesetzt, vor allem wegen der reichlich vorhandenen saubereren Lagerstätten auf der ganzen Welt, bei denen nicht viel mehr als eine manuelle Sortierung erforderlich war, um den reinen Graphit zu gewinnen. Der Stand der Technik um 1900 wird im Bericht des kanadischen Bergbauministeriums über Graphitminen und -bergbau beschrieben, als die kanadischen Lagerstätten zu wichtigen Graphitproduzenten wurden. ⓘ
Andere Namen

In der Vergangenheit wurde Graphit auch als Schwarzblei oder Plumbago bezeichnet. Plumbago wurde üblicherweise in seiner massiven mineralischen Form verwendet. Beide Bezeichnungen sind auf Verwechslungen mit den ähnlich aussehenden Bleierzen, insbesondere Bleiglanz, zurückzuführen. Das lateinische Wort für Blei, plumbum, war Namensgeber für die englische Bezeichnung dieses grauen, metallisch glänzenden Minerals und sogar für die Bleikräuter oder plumbagos, Pflanzen mit Blüten, die dieser Farbe ähneln. ⓘ
Der Begriff Schwarzblei bezieht sich in der Regel auf einen pulverisierten oder verarbeiteten Graphit von mattschwarzer Farbe. ⓘ
Abraham Gottlob Werner prägte 1789 den Namen Graphit ("Schreibstein"). Er versuchte, die Verwirrung zwischen Molybdän, Blei und Schwarzblei zu klären, nachdem Carl Wilhelm Scheele 1778 nachgewiesen hatte, dass es mindestens drei verschiedene Minerale gibt. Die Analyse von Scheele zeigte, dass es sich bei den chemischen Verbindungen Molybdänsulfid (Molybdänit), Blei(II)-sulfid (Bleiglanz) und Graphit um drei verschiedene weiche schwarze Minerale handelt. ⓘ
Verwendungszwecke von Naturgraphit
Naturgraphit wird hauptsächlich für feuerfeste Materialien, Batterien, die Stahlerzeugung, expandierten Graphit, Bremsbeläge, Gießereibeläge und Schmiermittel verwendet. ⓘ
Feuerfeste Materialien
Die Verwendung von Graphit als feuerfester (hitzebeständiger) Werkstoff begann vor 1900 mit Graphittiegeln, die zur Aufnahme von geschmolzenem Metall verwendet wurden; heute ist dies nur noch ein kleiner Teil der feuerfesten Materialien. Mitte der 1980er Jahre gewann der Kohlenstoff-Magnesit-Stein an Bedeutung, und etwas später die Tonerde-Graphit-Form. Ab 2017 lautet die Reihenfolge: Tonerde-Graphit-Steine, Kohlenstoff-Magnesit-Steine, Monolithen (Spritz- und Stampfmassen) und dann Tiegel. ⓘ
Für Tiegel wurde anfangs sehr großer Flockengraphit verwendet, während für Kohlenstoff-Magnesit-Steine nicht ganz so großer Flockengraphit erforderlich war. Für diese und andere Produkte gibt es jetzt viel mehr Flexibilität bei der erforderlichen Flockengröße, und amorpher Graphit ist nicht mehr auf Feuerfestmaterialien des unteren Marktsegments beschränkt. Formteile aus Aluminiumoxid-Graphit werden für Stranggussprodukte wie Düsen und Tröge verwendet, um den geschmolzenen Stahl von der Pfanne zur Form zu befördern, und Kohlenstoffmagnesitsteine dienen der Auskleidung von Stahlkonvertern und Elektrolichtbogenöfen, um extremen Temperaturen standzuhalten. Graphitblöcke werden auch in Teilen von Hochofenauskleidungen verwendet, wo die hohe Wärmeleitfähigkeit des Graphits entscheidend ist, um eine angemessene Kühlung des Bodens und des Herdes des Ofens zu gewährleisten. Hochreine Monolithen werden häufig als kontinuierliche Ofenauskleidung anstelle von Kohlenstoff-Magnesit-Steinen verwendet. ⓘ
Die US-amerikanische und europäische Feuerfestindustrie befand sich in den Jahren 2000-2003 in einer Krise, die durch einen gleichgültigen Stahlmarkt und einen rückläufigen Feuerfestverbrauch pro Tonne Stahl ausgelöst wurde und zu Firmenübernahmen und zahlreichen Werksschließungen führte. Viele der Werksschließungen resultierten aus der Übernahme von Harbison-Walker Refractories durch die RHI AG, und bei einigen Werken wurden die Anlagen versteigert. Da ein Großteil der verlorenen Kapazitäten für Kohlenstoff-Magnesit-Steine bestimmt war, verlagerte sich der Graphitverbrauch im Feuerfestbereich auf Aluminiumoxid-Graphit-Formteile und Monolithics und weg von Steinen. Der größte Teil der Kohlenstoff-Magnesit-Steine wird jetzt aus China importiert. Fast alle der oben genannten feuerfesten Materialien werden für die Stahlherstellung verwendet und machen 75 % des Feuerfestverbrauchs aus; der Rest wird von einer Vielzahl von Industriezweigen, z. B. der Zementindustrie, verwendet. ⓘ
Nach Angaben des USGS belief sich der Verbrauch von Naturgraphit für feuerfeste Materialien in den USA im Jahr 2010 auf 12.500 Tonnen. ⓘ
Batterien
Die Verwendung von Graphit in Batterien hat seit den 1970er Jahren zugenommen. Natürlicher und synthetischer Graphit wird als Anodenmaterial für den Bau von Elektroden in den wichtigsten Batterietechnologien verwendet. ⓘ
Die Nachfrage nach Batterien, vor allem Nickel-Metallhydrid- und Lithium-Ionen-Batterien, führte in den späten 1980er und frühen 1990er Jahren zu einem Anstieg der Graphitnachfrage - ein Wachstum, das durch tragbare Elektronikgeräte wie tragbare CD-Player und Elektrowerkzeuge angetrieben wurde. Laptops, Mobiltelefone, Tablets und Smartphone-Produkte haben die Nachfrage nach Batterien erhöht. Es wird erwartet, dass die Batterien für Elektrofahrzeuge die Nachfrage nach Graphit erhöhen werden. So enthält beispielsweise eine Lithium-Ionen-Batterie in einem vollelektrischen Nissan Leaf fast 40 kg Graphit. ⓘ
Radioaktiver Graphit aus alten Kernreaktoren wird als Brennstoff erforscht. Die nukleare Diamantbatterie hat das Potenzial für eine lang anhaltende Energieversorgung für Elektronik und das Internet der Dinge. ⓘ
Stahlherstellung
Naturgraphit wird bei der Stahlerzeugung hauptsächlich zur Erhöhung des Kohlenstoffgehalts im geschmolzenen Stahl verwendet; er kann auch zur Schmierung der Matrizen dienen, die zum Strangpressen von heißem Stahl verwendet werden. Kohlenstoffzusätze stehen im Wettbewerb mit Alternativen wie synthetischem Graphitpulver, Petrolkoks und anderen Formen von Kohlenstoff. Ein Kohlenstoff-Raiser wird zugesetzt, um den Kohlenstoffgehalt des Stahls auf ein bestimmtes Niveau zu erhöhen. Nach einer Schätzung, die sich auf die Graphitverbrauchsstatistiken des USGS stützt, haben die Stahlhersteller in den USA im Jahr 2005 10.500 Tonnen auf diese Weise verwendet. ⓘ
Bremsbeläge
Natürlicher amorpher und feinblättriger Graphit wird in Bremsbelägen oder Bremsbacken für schwerere (nicht automobilbetriebene) Fahrzeuge verwendet und gewann an Bedeutung, als Asbest ersetzt werden musste. Diese Verwendung ist schon seit geraumer Zeit wichtig, aber die organischen Zusammensetzungen ohne Asbest (NAO) beginnen, den Marktanteil von Graphit zu verringern. Ein Umbruch in der Bremsbelagindustrie mit einigen Werksschließungen hat sich ebenso wenig positiv ausgewirkt wie ein indifferenter Automobilmarkt. Nach Angaben des USGS belief sich der Verbrauch von Naturgraphit für Bremsbeläge in den USA im Jahr 2005 auf 6.510 Tonnen. ⓘ
Gießereibeläge und Schmiermittel
Ein Gießerei-Formputz ist eine Farbe auf Wasserbasis aus amorphem oder feinem Flockengraphit. Wenn man die Innenseite einer Form damit bestreicht und trocknen lässt, bleibt eine feine Graphitschicht zurück, die die Trennung des Gussobjekts nach dem Abkühlen des heißen Metalls erleichtert. Graphitschmiermittel sind Spezialprodukte für den Einsatz bei sehr hohen oder sehr niedrigen Temperaturen, als Schmiermittel für Schmiedegesenke, als Antiseize-Mittel, als Getriebeschmiermittel für Bergbaumaschinen und zum Schmieren von Schlössern. Graphit mit geringer Körnung oder besser noch ohne Körnung (ultrahochreiner Graphit) ist äußerst wünschenswert. Er kann als trockenes Pulver, in Wasser oder Öl oder als kolloidaler Graphit (eine permanente Suspension in einer Flüssigkeit) verwendet werden. Nach einer Schätzung, die sich auf die Graphitverbrauchsstatistiken des USGS stützt, wurden im Jahr 2005 2 200 Tonnen auf diese Weise verwendet. Graphit kann auch mit Metall imprägniert werden, um eine selbstschmierende Legierung für den Einsatz unter extremen Bedingungen zu schaffen, z. B. für Lager von Maschinen, die hohen oder niedrigen Temperaturen ausgesetzt sind. ⓘ
Bleistifte

Die Fähigkeit, Spuren auf Papier und anderen Gegenständen zu hinterlassen, gab dem Graphit seinen Namen, der 1789 von dem deutschen Mineralogen Abraham Gottlob Werner vergeben wurde. Der Name leitet sich von γράφειν ("graphein") ab, was auf Altgriechisch schreiben oder zeichnen bedeutet. ⓘ
Ab dem 16. Jahrhundert wurden alle Bleistifte mit Minen aus englischem Naturgraphit hergestellt, aber die moderne Bleistiftmine ist meist eine Mischung aus pulverisiertem Graphit und Ton; sie wurde 1795 von Nicolas-Jacques Conté erfunden. Sie ist chemisch nicht mit dem Metall Blei verwandt, dessen Erze ein ähnliches Aussehen hatten, daher die Weiterführung des Namens. Plumbago ist eine weitere ältere Bezeichnung für Naturgraphit, der zum Zeichnen verwendet wird, typischerweise als Klumpen des Minerals ohne Holzummantelung. Der Begriff Plumbago-Zeichnung ist normalerweise auf Werke des 17. und 18. Jahrhunderts, meist Porträts, beschränkt. ⓘ
Heute sind Bleistifte immer noch ein kleiner, aber bedeutender Markt für Naturgraphit. Etwa 7 % der 2011 produzierten 1,1 Millionen Tonnen wurden für die Herstellung von Bleistiften verwendet. Verwendet wird minderwertiger amorpher Graphit, der hauptsächlich aus China bezogen wird. ⓘ
Andere Verwendungen
Naturgraphit wird in Zink-Kohle-Batterien, Bürsten für Elektromotoren und verschiedenen Spezialanwendungen eingesetzt. Graphit von unterschiedlicher Härte oder Weichheit ergibt unterschiedliche Qualitäten und Farbtöne, wenn er als künstlerisches Medium verwendet wird. Bei den Eisenbahnen wurde Graphitpulver oft mit Altöl oder Leinöl gemischt, um eine hitzebeständige Schutzschicht für die freiliegenden Teile des Kessels einer Dampflokomotive zu schaffen, z. B. für die Rauchkammer oder den unteren Teil der Feuerbüchse. ⓘ
Expandierter Graphit
Expandierter Graphit wird durch Eintauchen von natürlichem Flockengraphit in ein Bad mit Chromsäure und anschließend konzentrierter Schwefelsäure hergestellt, wodurch die Kristallgitterebenen auseinandergedrückt werden und der Graphit expandiert. Der expandierte Graphit kann zur Herstellung von Graphitfolien oder direkt als "Hot Top"-Verbindung verwendet werden, um geschmolzenes Metall in einer Pfanne oder rotglühende Stahlblöcke zu isolieren und den Wärmeverlust zu verringern, oder als Brandschutzvorrichtungen, die um eine Brandschutztür oder in Blechmanschetten, die Kunststoffrohre umgeben, angebracht werden (während eines Brandes dehnt sich der Graphit aus und verkohlt, um dem Eindringen und der Ausbreitung des Feuers entgegenzuwirken), oder zur Herstellung von Hochleistungsdichtungsmaterial für Hochtemperaturanwendungen. Nach der Herstellung von Graphitfolien werden diese maschinell bearbeitet und in die Bipolarplatten von Brennstoffzellen eingebaut. Aus der Folie werden Kühlkörper für Laptops hergestellt, die sie kühl halten und gleichzeitig Gewicht sparen, und sie wird zu einem Folienlaminat verarbeitet, das in Ventilpackungen verwendet oder zu Dichtungen verarbeitet werden kann. Ein kleineres Mitglied dieser Gruppe sind die Dichtungen alten Stils: feiner Flockengraphit in Ölen oder Fetten für Anwendungen, die Hitzebeständigkeit erfordern. Eine GAN-Schätzung des derzeitigen US-Naturgraphitverbrauchs für diese Endverwendung beläuft sich auf 7.500 Tonnen. ⓘ
Interkalierter Graphit
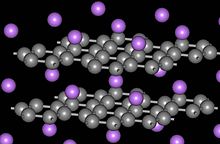
Graphit bildet Einlagerungsverbindungen mit einigen Metallen und kleinen Molekülen. Bei diesen Verbindungen wird das Wirtsmolekül oder -atom zwischen den Graphitschichten "eingeklemmt", was zu einer Art von Verbindung mit variabler Stöchiometrie führt. Ein bekanntes Beispiel für eine Interkalationsverbindung ist Kaliumgraphit mit der Formel KC8. Einige Graphit-Einlagerungsverbindungen sind Supraleiter. Die höchste Übergangstemperatur (Stand Juni 2009) Tc = 11,5 K wird in CaC6 erreicht, und sie steigt unter Druck weiter an (15,1 K bei 8 GPa). Die Fähigkeit von Graphit, Lithiumionen ohne nennenswerte Quellungsschäden einzulagern, macht ihn zum dominierenden Anodenmaterial in Lithium-Ionen-Batterien. ⓘ
Verwendungen von synthetischem Graphit
Durch Verkoken kohlenstoffhaltiger Materialien entstehen graphitierbare Kohlenstoffe. Ausgangssubstanzen sind zum Beispiel Braunkohle, Steinkohle, Erdöl und Peche, aber auch Kunststoffe. Bei der Graphitierung erfolgt durch Erhitzen unter Luftabschluss auf etwa 3000 °C eine Umwandlung vom amorphen Kohlenstoff zum polykristallinen Graphit. ⓘ
Künstlich hergestellter Graphit ist auch als Acheson-Graphit bekannt. Bedeutende Hersteller sind unter anderem Showa Denko Carbon, SGL Carbon, Schunk Kohlenstofftechnik (Deutschland), Imerys (Schweiz), Tōkai Carbon (Japan), Morgan Advanced Materials (Großbritannien) und Tōyō Tanso (Japan). ⓘ
Highly ordered pyrolytic graphite (HOPG) ist eine sehr reine Form von Graphit. ⓘ
Erfindung eines Verfahrens zur Herstellung von synthetischem Graphit
Im Jahr 1893 entdeckte Charles Street von Le Carbone ein Verfahren zur Herstellung von künstlichem Graphit. Mitte der 1890er Jahre erfand Edward Goodrich Acheson (1856-1931) zufällig eine weitere Methode zur Herstellung von synthetischem Graphit, nachdem er Karborund (Siliziumkarbid oder SiC) synthetisiert hatte. Er entdeckte, dass die Überhitzung von Karborundum im Gegensatz zu reinem Kohlenstoff fast reinen Graphit ergab. Bei der Untersuchung der Auswirkungen hoher Temperaturen auf Karborundum hatte er festgestellt, dass Silizium bei etwa 4.150 °C verdampft und den Kohlenstoff als Graphit zurücklässt. Dieser Graphit wurde als Schmiermittel wertvoll. ⓘ
Achesons Technik zur Herstellung von Siliziumkarbid und Graphit wird als Acheson-Verfahren bezeichnet. 1896 erhielt Acheson ein Patent für seine Methode der Graphitsynthese, und 1897 begann er mit der kommerziellen Produktion. Im Jahr 1899 wurde die Acheson Graphite Co. gegründet. ⓘ
Synthetischer Graphit kann auch aus Polyimid hergestellt und vermarktet werden. ⓘ
Wissenschaftliche Forschung
Hochorientierter pyrolytischer Graphit (HOPG) ist die hochwertigste synthetische Form von Graphit. Er wird in der wissenschaftlichen Forschung verwendet, insbesondere als Längenstandard für die Kalibrierung von Rastersondenmikroskopen. ⓘ
Elektroden
Graphitelektroden leiten den Strom, der Eisen- und Stahlschrott und manchmal auch direkt reduziertes Eisen (DRI) in Elektrolichtbogenöfen schmilzt, die die große Mehrheit der Stahlöfen ausmachen. Sie werden aus Petrolkoks hergestellt, nachdem dieser mit Steinkohlenteerpech gemischt wurde. Anschließend werden sie extrudiert und geformt, dann gebrannt, um das Bindemittel (Pech) zu verkohlen, und schließlich durch Erhitzen auf Temperaturen von annähernd 3000 °C, bei denen sich die Kohlenstoffatome zu Graphit anordnen, graphitiert. Sie können bis zu 3,5 m lang und 75 cm im Durchmesser sein. Ein zunehmender Anteil des weltweiten Stahls wird mit Hilfe von Elektrolichtbogenöfen hergestellt, und der Elektrolichtbogenofen selbst wird immer effizienter, so dass mehr Stahl pro Tonne Elektrode erzeugt wird. Einer Schätzung auf der Grundlage von USGS-Daten zufolge belief sich der Graphitelektrodenverbrauch im Jahr 2005 auf 197.000 Tonnen. ⓘ
Bei der elektrolytischen Aluminiumschmelze werden ebenfalls Graphitkohlenstoffelektroden verwendet. In wesentlich geringerem Umfang werden Elektroden aus synthetischem Graphit bei der Funkenerosion (EDM) verwendet, in der Regel zur Herstellung von Spritzgussformen für Kunststoffe. ⓘ
Pulver und Schrott
Das Pulver wird durch Erhitzen von Petrolkokspulver über die Graphitierungstemperatur hergestellt, manchmal mit geringfügigen Änderungen. Der Graphitschrott stammt aus Stücken von unbrauchbarem Elektrodenmaterial (in der Herstellungsphase oder nach der Verwendung) und Drehspänen, in der Regel nach dem Zerkleinern und Kalibrieren. Der größte Teil des synthetischen Graphitpulvers wird zur Erhöhung des Kohlenstoffgehalts in Stahl verwendet (und konkurriert mit natürlichem Graphit), ein Teil wird in Batterien und Bremsbelägen eingesetzt. Nach Angaben des USGS belief sich die Produktion von synthetischem Graphitpulver und -schrott in den USA im Jahr 2001 auf 95.000 Tonnen (neueste Daten). ⓘ
Neutronenmoderator
Spezielle Qualitäten von synthetischem Graphit, wie z. B. Gilsocarbon, werden auch als Matrix und Neutronenmoderator in Kernreaktoren verwendet. Sein geringer Neutronenquerschnitt empfiehlt ihn auch für den Einsatz in geplanten Fusionsreaktoren. Es muss darauf geachtet werden, dass Graphit in Reaktorqualität frei von neutronenabsorbierenden Materialien wie Bor ist, das in kommerziellen Graphitabscheidungssystemen häufig als Seed-Elektrode verwendet wird - dies war die Ursache für das Scheitern der graphitbasierten Kernreaktoren der Deutschen im Zweiten Weltkrieg. Da sie das Problem nicht isolieren konnten, waren sie gezwungen, weitaus teurere Schwerwassermoderatoren zu verwenden. Graphit, der für Kernreaktoren verwendet wird, wird oft auch als Kerngraphit bezeichnet. Herbert G. McPherson, ein in Berkeley ausgebildeter Physiker bei National Carbon, einer Abteilung von Union Carbide, war maßgeblich an der Bestätigung einer Vermutung von Leo Szilard beteiligt, wonach Borverunreinigungen selbst in "reinem" Graphit für einen Neutronenabsorptionsquerschnitt in Graphit verantwortlich sind, der U-235-Kettenreaktionen beeinträchtigt. McPherson war sich des Vorhandenseins von Verunreinigungen in Graphit bewusst, da mit der Verwendung von Technicolor in der Kinematographie die Spektren der Graphitelektrodenbögen in Filmprojektoren Verunreinigungen benötigten, um die Emission von Licht im roten Bereich zu verstärken und damit wärmere Hauttöne auf der Leinwand darzustellen. Hätte es also keine Farbfilme gegeben, wäre für die erste anhaltende natürliche U-Kettenreaktion wahrscheinlich ein mit schwerem Wasser moderierter Reaktor erforderlich gewesen. ⓘ
Andere Verwendungen
Graphitfasern (Kohlenstoff) und Kohlenstoffnanoröhren werden auch in kohlenstofffaserverstärkten Kunststoffen und in hitzebeständigen Verbundwerkstoffen wie verstärktem Kohlenstoff-Kohlenstoff (RCC) verwendet. Zu den kommerziellen Strukturen, die aus Kohlenstofffaser-Graphit-Verbundwerkstoffen hergestellt werden, gehören Angelruten, Golfschlägerschäfte, Fahrradrahmen, Karosserieteile von Sportwagen, der Rumpf des Boeing 787 Dreamliners und Billardqueue-Stöcke, und sie wurden erfolgreich in Stahlbeton eingesetzt. Die mechanischen Eigenschaften von kohlenstofffaserverstärkten Kunststoffverbundwerkstoffen und Grauguss werden stark von der Rolle des Graphits in diesen Werkstoffen beeinflusst. In diesem Zusammenhang wird der Begriff "(100 %) Graphit" oft lose verwendet, um eine reine Mischung aus Kohlenstoffverstärkung und Harz zu bezeichnen, während der Begriff "Verbundwerkstoff" für Verbundwerkstoffe mit zusätzlichen Bestandteilen verwendet wird. ⓘ
Modernes rauchloses Pulver ist mit Graphit beschichtet, um den Aufbau statischer Aufladung zu verhindern. ⓘ
Graphit wurde in mindestens drei radarabsorbierenden Materialien verwendet. In Sumpf und Schornsteinfeger wurde es mit Kautschuk gemischt, um den Radarquerschnitt der Schnorchel von U-Booten zu verringern. Es wurde auch in Kacheln der frühen F-117 Nighthawk Stealth-Jagdflugzeuge verwendet. ⓘ
Graphitverbundwerkstoffe werden als Absorber für hochenergetische Teilchen verwendet, z. B. im Strahlenkanal des Large Hadron Collider. ⓘ
In Form gefeilte Graphitstäbe werden in der Glasverarbeitung als Werkzeug zur Bearbeitung von heißem geschmolzenem Glas verwendet. ⓘ
Recycling
Auch bei Graphit spielt Recycling eine wichtige Rolle, recycelter Graphit von Gussformen, Ofenauskleidungen und Graphitelektroden wird vor allem für Bremsbeläge und thermische Isolierungen verwendet. Das Recyclingpotential ist noch ausbaufähig, wird derzeit aber auf Grund reichlich vorhandener weltweiter Graphitmengen nicht ausgeschöpft. ⓘ
Graphitabbau, -aufbereitung und -vermahlung

Graphit wird sowohl im Tagebau als auch unter Tage abgebaut. Graphit muss in der Regel aufbereitet werden. Dies kann durch manuelles Heraussuchen der Gangart (Gestein) und manuelles Sieben des Produkts oder durch Zerkleinern des Gesteins und Ausschwimmen des Graphits erfolgen. Die Aufbereitung durch Flotation stößt auf die Schwierigkeit, dass Graphit sehr weich ist und die Ganggesteinspartikel "markiert" (überzieht). Dies führt dazu, dass die "markierten" Gangpartikel mit dem Graphit abschwimmen und ein unreines Konzentrat entsteht. Es gibt zwei Möglichkeiten, ein handelsübliches Konzentrat oder Produkt zu erhalten: wiederholtes Nachmahlen und Flotieren (bis zu sieben Mal), um das Konzentrat zu reinigen, oder durch saures Auslaugen (Auflösen) des Ganggesteins mit Flusssäure (bei einem Silikatgangestein) oder Salzsäure (bei einem Karbonatgangestein). ⓘ
Beim Mahlen können die eingehenden Graphitprodukte und -konzentrate gemahlen werden, bevor sie klassifiziert (sortiert oder gesiebt) werden, wobei die gröberen Flockengrößenfraktionen (unter 8 Mesh, 8-20 Mesh, 20-50 Mesh) sorgfältig aufbewahrt werden, und anschließend wird der Kohlenstoffgehalt bestimmt. Aus den verschiedenen Fraktionen können einige Standardmischungen hergestellt werden, die jeweils eine bestimmte Flockengrößenverteilung und einen bestimmten Kohlenstoffgehalt aufweisen. Für einzelne Kunden, die eine bestimmte Flockengrößenverteilung und einen bestimmten Kohlenstoffgehalt wünschen, können auch individuelle Mischungen hergestellt werden. Wenn die Flockengröße keine Rolle spielt, kann das Konzentrat freier gemahlen werden. Zu den typischen Endprodukten gehören ein feines Pulver zur Verwendung als Aufschlämmung bei Ölbohrungen, Beschichtungen für Gießereiformen und Kohlenstoffverstärker in der Stahlindustrie (synthetisches Graphitpulver und pulverisierter Petrolkoks können ebenfalls als Kohlenstoffverstärker verwendet werden). Die Umweltauswirkungen der Graphitfabriken bestehen in der Luftverschmutzung, einschließlich der Feinstaubbelastung der Arbeiter, und in der Verunreinigung des Bodens durch verschüttetes Pulver, was zu einer Schwermetallverschmutzung des Bodens führt. ⓘ

Nach Angaben des United States Geological Survey (USGS) belief sich die Weltproduktion von Naturgraphit im Jahr 2016 auf 1.200.000 Tonnen, von denen die folgenden Hauptexporteure sind: China (780.000 t), Indien (170.000 t), Brasilien (80.000 t), Türkei (32.000 t) und Nordkorea (6.000 t). In den Vereinigten Staaten wird noch kein Graphit abgebaut. Westwater Resources befindet sich jedoch derzeit in der Entwicklungsphase zur Errichtung einer Pilotanlage für ihre Coosa-Graphitmine in der Nähe von Sylacauga, Alabama. Die US-Produktion von synthetischem Graphit belief sich 2010 auf 134.000 t im Wert von 1,07 Mrd. $. ⓘ
Sicherheit am Arbeitsplatz
Menschen können am Arbeitsplatz Graphit ausgesetzt sein, indem sie es einatmen oder mit der Haut oder den Augen in Berührung kommen. ⓘ
Vereinigte Staaten
Die Occupational Safety and Health Administration (OSHA) hat den gesetzlichen Grenzwert (zulässiger Expositionsgrenzwert) für die Graphitexposition am Arbeitsplatz auf einen zeitlich gewichteten Durchschnitt (TWA) von 15 Millionen Partikeln pro Kubikfuß (1,5 mg/m3) an einem 8-Stunden-Arbeitstag festgelegt. Das National Institute for Occupational Safety and Health (NIOSH) hat einen empfohlenen Expositionsgrenzwert (REL) von 2,5 mg/m3 lungengängigen Staubes über einen 8-Stunden-Arbeitstag festgelegt. Bei einer Konzentration von 1250 mg/m3 ist Graphit unmittelbar lebens- und gesundheitsgefährlich. ⓘ
Graphit-Recycling
Am häufigsten wird Graphit recycelt, wenn Elektroden aus synthetischem Graphit hergestellt und Teile davon abgeschnitten oder Drehspäne zur Wiederverwendung weggeworfen werden, oder wenn die Elektrode (oder andere Materialien) bis zum Elektrodenhalter verwendet werden. Eine neue Elektrode ersetzt die alte, aber ein beträchtliches Stück der alten Elektrode bleibt übrig. Dieses wird zerkleinert und zerkleinert, und das dabei entstehende Graphitpulver wird meist zur Erhöhung des Kohlenstoffgehalts im geschmolzenen Stahl verwendet. Graphithaltige feuerfeste Materialien werden manchmal ebenfalls recycelt, oft aber nicht, weil ihr Graphitgehalt zu gering ist: Die größten Mengen, wie Kohlenstoff-Magnesit-Steine, die nur 15-25 % Graphit enthalten, enthalten in der Regel zu wenig Graphit, um sich für das Recycling zu lohnen. Ein Teil der recycelten Kohlenstoff-Magnesit-Steine wird jedoch als Grundlage für Ofenreparaturmaterial verwendet, und auch zerkleinerte Kohlenstoff-Magnesit-Steine werden in Schlackenkonditionierern eingesetzt. Tiegel haben zwar einen hohen Graphitanteil, doch ist die Menge der verwendeten und anschließend recycelten Tiegel sehr gering. ⓘ
Ein hochwertiges Flockengraphitprodukt, das dem natürlichen Flockengraphit sehr ähnlich ist, kann aus Stahlwerkskies hergestellt werden. Kish ist ein großvolumiger, fast geschmolzener Abfall, der aus der Eisenschmelze eines Sauerstoffschmelzofens abgeschöpft wird und aus einer Mischung aus Graphit (ausgefällt aus dem übersättigten Eisen), kalkreicher Schlacke und etwas Eisen besteht. Das Eisen wird vor Ort recycelt, wobei eine Mischung aus Graphit und Schlacke zurückbleibt. Das beste Rückgewinnungsverfahren ist die hydraulische Klassierung (bei der ein Wasserstrom zur Trennung der Mineralien nach ihrem spezifischen Gewicht verwendet wird: Graphit ist leicht und setzt sich fast als letztes ab), um ein Graphit-Rohkonzentrat von 70 % zu erhalten. Durch Auslaugen dieses Konzentrats mit Salzsäure erhält man ein 95 %iges Graphitprodukt mit einer Flockengröße von 10 mesh abwärts. ⓘ
Klassifikation
Bereits in der veralteten 8. Auflage der Mineralsystematik nach Strunz gehörte der Graphit zur Mineralklasse der „Elemente“ und dort zur Abteilung der „Halbmetalle und Nichtmetalle“, wo er als einziges Mitglied die Gruppe I/B.02a bildete. ⓘ
Im zuletzt 2018 überarbeiteten und aktualisierten Lapis-Mineralienverzeichnis nach Stefan Weiß, das sich aus Rücksicht auf private Sammler und institutionelle Sammlungen noch nach dieser klassischen Systematik von Karl Hugo Strunz richtet, erhielt das Mineral die System- und Mineral-Nr. I/B.02-10. In der „Lapis-Systematik“ entspricht dies ebenfalls der Abteilung „Halbmetalle und Nichtmetalle“, wo Graphit zusammen mit Chaoit, Diamant, Fullerit (Mineralstatus bisher zweifelhaft), Lonsdaleit und Moissanit eine eigenständige, aber unbenannte Gruppe bildet. ⓘ
Auch die seit 2001 gültige und von der IMA bis 2009 aktualisierte 9. Auflage der Strunz’schen Mineralsystematik ordnet den Graphit in die Abteilung der „Halbmetalle (Metalloide) und Nichtmetalle“ ein. Diese ist allerdings weiter unterteilt nach den Hauptelementen der eingruppierten Minerale, so dass Graphit entsprechend in der Unterabteilung „Kohlenstoff-Silicium-Familie“ zu finden ist, wo es als einziges Mitglied die unbenannte Gruppe 1.CB.05a bildet. ⓘ
Die vorwiegend im englischen Sprachraum gebräuchliche Systematik der Minerale nach Dana ordnet den Graphit ebenfalls in die Klasse und dort in die gleichnamige Abteilung der „Elemente“ ein. Hier ist er zusammen mit Diamant, Lonsdaleit, Chaoit und Fullerit in der Gruppe der „Kohlenstoffpolymorphe“ mit der System-Nr. 01.03.06 innerhalb der Unterabteilung „Elemente: Halbmetalle und Nichtmetalle“ zu finden. ⓘ
Eigenschaften
Bei einer Temperatur von über 2500 °C wird Graphit plastisch verformbar und sublimiert in einer sauerstofffreien Umgebung bei einer Temperatur von 3750 °C. Unter Sauerstoffeinwirkung entzündet sich Graphit bei etwa 600 °C. ⓘ
Graphit ist beständig gegen nichtoxidierende Säuren und ist diamagnetisch. Auffällig ist das stark anisotrope Verhalten von Graphit, insbesondere hinsichtlich Härte und elektrischer Leitfähigkeit. ⓘ
Magnetische Suszeptibilität
Graphit hat eine negative magnetische Suszeptibilität und ist daher diamagnetisch. Der Betrag der Suszeptibilität und damit das Ausmaß an Diamagnetismus von Graphit hängt von der Qualität des Graphits und seiner Orientierung im Magnetfeld ab. ⓘ
Bei Ausrichtung senkrecht zu den Atomlagen liegt sie bei = −450 · 10−6 für pyrolytischen Graphit (vgl. pyrolytic graphit (en)) bis zu = −595 · 10−6 für hoch-orientierte Formen. Bei Ausrichtung parallel zu den Atomlagen liegt die Suszeptibilität bei = −85 · 10−6 für pyrolytischen Graphit. Bei polykristallinem Graphit (z. B. Ruß, Glaskohlenstoff) ist die Suszeptibilität isotrop und die Werte mitteln sich über die verschieden ausgerichteten Einkristalle. Für Ruß ergibt sich z. B. eine Suszeptibilität von = −204 · 10−6 . ⓘ
Graphit ist damit bei senkrechter Ausrichtung das am stärksten diamagnetische Element. Es ist aber immer noch rund 2000 Mal schwächer als ideale Diamagneten – wie z. B. Supraleiter – mit einer magnetischen Suszeptibilität von = −1. Je nach Form ist Graphit auch in polykristalliner Form noch stärker diamagnetisch als das nächststärkste diamagnetische Element Bismut. ⓘ
Modifikationen und Varietäten
Graphit ist neben Diamant und Fulleren die dritte unter irdischen Normalbedingungen stabile Form (Modifikation) des Kohlenstoffs. Eine weitere Modifikation, der Lonsdaleit, entsteht nur durch außergewöhnliche Schockereignisse wie beispielsweise bei einem Meteoriteneinschlag. ⓘ
Bildung und Fundorte

Natürlicher Graphit entsteht durch eine Kombination aus Diagenese und Metamorphose (Kontakt- und Regionalmetamorphose) und durchläuft dabei die Prozesse der Inkohlung. Bedingungen dafür sind organischer Kohlenstoff und hohe Temperaturen und Drücke über Zeiträume von Jahrmillionen. ⓘ
Das Ausgangsmaterial des Graphits sind kohlenstoffhaltige Sedimente (z. B. Pflanzen- oder Faulschlammasse) dessen Kohlenstoffgehalt durch Inkohlung auf bis zu 90 % angereichert wird. Die Anreicherungsprozesse können unter relativ niedrigen Drücken und Temperaturen ablaufen (Diagenese). Für die endgültige Entstehung von Graphit bedarf es aber hoher Temperaturen und Drücke, um den amorphen Kohlenstoff in kristallinen Kohlenstoff umzuwandeln. Solche Bedingungen können ausschließlich durch metamorphe oder magmatische Prozesse erreicht werden, und müssen anoxisch ablaufen, da Kohlenstoff bei erhöhten Temperaturen ansonsten Verbindungen mit Sauerstoff eingeht und als Kohlenstoffmonoxid oder Kohlenstoffdioxid entweicht. ⓘ
Graphit kommt daher bevorzugt in metamorphen Gesteinen vor, die in plattentektonischen Kollisionsgebieten während der Gebirgsbildung aus sedimentären Ausgangsgesteinen entstanden sind. Durch Regionalmetamorphose gebildete Graphitvorkommen befinden sich linsen- oder nestartig abgetrennt im Umgebungsgestein, durch Kontaktmetamorphose gebildetes Graphit kann auch in Pegmatiten sowie in Kalk- und Sandsteinen vorkommen. Weiterhin kann Graphit Bestandteil von Meteoriten sein. ⓘ
Nach der Entstehung wird Graphit in drei Arten eingeteilt: Flockengraphit (flake graphite), amorphen Graphit (amorphous graphite) und Ganggraphit (vein graphite). Der Flockengraphit ist die häufigste Graphitvariante, er besteht aus Plättchen und kommt in metamorphen Gesteinen, wie z. B. Marmor, Gneis oder Schiefern, vor. Der amorphe Graphit ist ein sehr feinkörniger Graphit, der in Kohleflözen, Tonsteinen und Schiefern vorkommt. Der Ganggraphit ist der seltenste Graphit, er bildet sich in Pegmatigängen und Spalten, in denen bei bereits relativ niedrigen Temperaturen von etwa 500–600 °C verschiedene Minerale kristallisieren. Seine Entstehung ist noch umstritten, jedoch gilt die Lösung von kohlenwasserstoffhaltigem Material in wässrigen Fluide mit anschließender Auskristallisation für am wahrscheinlichsten. ⓘ
Es existieren zahlreiche Graphitfundorte weltweit. Von wirtschaftlicher Bedeutung sind aber vor allem die Volksrepublik China, Korea, Madagaskar, Simbabwe, Brasilien und Indien sowohl im Tagebau als auch unter Tage. Im Jahr 2020 wurden ca. 940.000 Tonnen gefördert. ⓘ
In Europa gibt es zurzeit nur noch wenige aktive Graphitbergwerke. In der Ukraine, in Norwegen und in Tschechien wird makrokristalliner Graphit in unterschiedlicher Qualität unter Tage abgebaut. Bei dem makrokristallinen Graphit sind die einzelnen Graphitkristallitpakete (Flocken) gut erhalten und sichtbar. In Österreich wurden dagegen mikrokristalline Graphite gewonnen, deren Kristalle nicht so deutlich ausgeprägt sind. ⓘ
Österreich nahm in den 1960er-Jahren den nach Südkorea zweiten Platz unter den graphitfördernden Ländern ein (Höchststand 1964 mit etwa 100.000 Tonnen Förderung). Der größte Bergbau befand sich in Kaisersberg bei Sankt Stefan ob Leoben in der Steiermark. Er wurde 1997 stillgelegt; seit Frühjahr 2008 wird im dortigen „Marie-Stollen“ wieder gearbeitet. Bis 1991 bestand in Sunk bei Trieben im Paltental (Steiermark) ein Bergbau, in dem Graphit mit einem sehr hohen Kohlenstoffanteil von zum Teil über 85 % gewonnen wurde. Weitere kleine Graphitbergbaue bestanden bis in die 1970er-Jahre am Semmering, im Liesingtal (Steiermark), im Dunkelsteiner Wald (Niederösterreich) sowie im Waldviertel, wo das seit 1831 in Abbau stehende Vorkommen in Mühldorf am bedeutendsten war. Aktuell (2022) ist der Untertagbergbau in Sankt Stefan ob Leoben der einzige aktive Graphitbergbau in den Alpen, wobei die dort abgebaute Menge je nach Quelle mit 100 t und einmal mit 500 t für das Jahr 2020 angegeben wird. ⓘ
In Deutschland war und ist der Graphit-Bergbau von Kropfmühl/Landkreis Passau bedeutsam. Am 21. Juni 2012 wurde das Graphitbergwerk am Standort Kropfmühl offiziell wieder eröffnet. Der Abbau ist, laut einer Pressemitteilung des Unternehmens, aufgrund der steigenden Nachfrage nach Graphit und der Preisentwicklung am Weltmarkt wieder rentabel geworden. Die in Deutschland abgebauten Mengen betrugen 2020 je nach Quelle 108 t bis 300 t. ⓘ
Die weltweit größte Graphitmine befand sich 2022 in Mozambique und soll 50 Jahre lang betrieben werden. Weltweit verteilten sich die Fördermengen wie folgt:
| Land | 2018 | 2019 | 2020 ⓘ |
|---|---|---|---|
| (in Tonnen) | |||
| 150 | 100 | 100 | |
| 78.981 | 81.770 | 67.020 | |
| 222 | 207 | 108 | |
| 630.000 | 700.000 | 665.000 | |
| 39.030 | 34.674 | 30.168 | |
| 11.000 | 11.045 | 11.937 | |
| 0 | 135 | 0 | |
| 47.900 | 53.400 | 48.055 | |
| 4.130 | 2.342 | 2.033 | |
| 104.000 | 153.000 | 18.159 | |
| 3.456 | |||
| 45.000 | 45.000 | 45.000 | |
| 10.000 | 9.780 | 5.549 | |
| 11.900 | 17.500 | 12.900 | |
| 3.800 | 3.100 | 2.500 | |
| 670 | 302 | 3.052 | |
| 16.752 | 9.990 | 15.205 | |
| 15.000 | 10.000 | 10.000 | |
| 1.500 | 3.500 | 3.700 | |
| Gesamt | 1.023.491 | 1.135.845 | 940.486 |
Verwendung
Graphitelektroden
2011 wurden 42 % aller synthetischen Graphite zu Elektroden verarbeitet. So werden für die Herstellung einer Tonne Elektrostahl im Durchschnitt 2–2,5 kg Graphit verbraucht. ⓘ
- Elektrode im Lichtbogenofen (zur Elektrostahlgewinnung)
- Elektrode in Kohlebogenlampen
- Kohlebürste in elektrischen Motoren
- negative Elektrode von Lithium-Ionen-Zellen
- positive Elektrode von Zink-Kohle-Primärzellen
- Elektrode beim Senkerodieren
- Schleifleisten auf dem Stromabnehmer von Schienenfahrzeugen
- Raderdungskontakte auf Schienenfahrzeugen ⓘ
Nukleargraphit
Graphit wurde und wird in hochgereinigter Form in manchen Kernreaktor-Typen als Moderator eingesetzt. In den deutschen, inzwischen stillgelegten „Kugelhaufenreaktoren“ Versuchsreaktor Jülich und THTR-300 diente Graphit zugleich als Moderator und Brennelementmatrix. Die guten Moderationseigenschaften und die hohe Temperaturstabilität waren für den Einsatz in der Nukleartechnik ausschlaggebend. ⓘ
Die Graphitbrände des britischen Windscale-Reaktors 1957 in Sellafield sowie des RBMK-Reaktors in Tschernobyl 1986 führten jedoch zu Bedenken wegen der Sicherheit von Graphit in Reaktoren. Als Probleme kommen die Reaktionsfähigkeit mit Wasserdampf (> 900 °C) unter Bildung brennbarer Gase und die Neigung zu energetischen Instabilitäten (siehe Wigner-Energie) hinzu. ⓘ
2006 gab es weltweit 250.000 t bestrahlten Nukleargraphit (Deutschland ca. 1000 t), für den es wegen seines hohen Gehalts an C-14 (radioaktives Isotop mit einer Halbwertszeit von 5700 Jahren) noch keine ökonomisch akzeptable Endlagerstrategie gibt. ⓘ
Weitere Verwendungsmöglichkeiten


Graphit wird vielfältig genutzt als ⓘ
- Bleistiftmine, auch ohne Holzumhüllung für künstlerische Grafik
- Festschmierstoff
- Werkstoff für selbstschmierende Lager und Dichtungen
- Füller zur Verbesserung der elektrischen Leitfähigkeit und zum Herabsetzen des Reibbeiwertes von Kunststoffen
- Schmelztiegel
- Gießform
- thermisch hochbelastbare Ofenauskleidung
- Ablator (z. B. im SpaceX Merlin 1A Raketentriebwerk)
- Monochromator im Einkristalldiffraktometer
- Standardsubstrat in der Rastertunnelmikroskopie unter Umgebungsbedingungen.
- Waffe in Form von Graphitfäden zum Kurzschließen der feindlichen Stromversorgung (Graphitbombe)
- korrosionsbeständiger Werkstoff in der chemischen Industrie
- Wanne und Elektroden bei der Aluminiumherstellung (Schmelzflusselektrolyse)
- Legierungselement in Gusseisen – metallurgische Ausscheidungsphase (Kugelgraphit, Lamellengraphit)
- Phasenwechselmaterial
- Diabon ist ein aus Graphit bestehender Werkstoff
- Absorbermaterial für hochenergetische Teilchen (z. B. am LHC)
- Zur Verbesserung der Wärmedämmung bei EPS, wie Neopor. ⓘ





