Cobalamine
 Skeletal formula of a generic cobalamin | |
 Stick model of cyanocobalamin (R = CN) based on the crystal structure | |
| Clinical data | |
|---|---|
| Other names | Vitamin B12, vitamin B-12, cobalamin |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a605007 |
| License data |
|
| Routes of administration | By mouth, sublingual, intravenous (IV), intramuscular (IM), intranasal |
| ATC code |
|
| Legal status | |
| Legal status |
|
| Pharmacokinetic data | |
| Bioavailability | Readily absorbed in distal half of the ileum. |
| Protein binding | Very high to specific transcobalamins plasma proteins. Binding of hydroxocobalamin is slightly higher than cyanocobalamin. |
| Metabolism | liver |
| Eliminationshalbwertszeit | Ungefähr 6 Tage (400 Tage in der Leber). |
| Ausscheidung | Niere |
| Bezeichner | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| Chemische und physikalische Daten | |
| Formel | C63H88CoN14O14P |
| Molare Masse | 1355,388 g-mol-1 |
| 3D-Modell (JSmol) | |
SMILES
| |
InChI
| |
Vitamin B12, auch bekannt als Cobalamin, ist ein wasserlösliches Vitamin, das am Stoffwechsel beteiligt ist. Es ist eines der acht B-Vitamine. Es wird von Tieren benötigt, die es als Cofaktor bei der DNA-Synthese und im Fettsäure- und Aminosäurestoffwechsel verwenden. Es ist wichtig für das normale Funktionieren des Nervensystems durch seine Rolle bei der Synthese von Myelin und im Kreislaufsystem bei der Reifung der roten Blutkörperchen im Knochenmark. Pflanzen benötigen kein Cobalamin und führen die Reaktionen mit Enzymen durch, die nicht von Cobalamin abhängig sind. ⓘ
Vitamin B12 ist das chemisch komplexeste aller Vitamine und für den Menschen das einzige Vitamin, das über tierische Lebensmittel oder Nahrungsergänzungsmittel zugeführt werden muss. Nur einige Archaeen und Bakterien können Vitamin B12 synthetisieren. Die meisten Menschen in den Industrieländern erhalten genügend B12 durch den Verzehr von Fleisch oder Lebensmitteln tierischen Ursprungs. Zu den Lebensmitteln, die Vitamin B12 enthalten, gehören Fleisch, Muscheln, Leber, Fisch, Geflügel, Eier und Milchprodukte. Getreidehaltige Lebensmittel können mit dem Vitamin angereichert werden. Zur Behandlung und Vorbeugung von Vitamin-B12-Mangel gibt es Nahrungsergänzungsmittel und Medikamente. Sie werden durch den Mund eingenommen, können aber zur Behandlung eines Mangels auch als intramuskuläre Injektion verabreicht werden. ⓘ
Die häufigste Ursache für einen Vitamin-B12-Mangel in den Industrieländern ist eine gestörte Absorption aufgrund eines Verlusts des gastrischen Intrinsic Factors (IF), der an eine B12-Quelle in der Nahrung gebunden sein muss, damit die Absorption erfolgen kann. Eine zweite wichtige Ursache ist die altersbedingte Abnahme der Magensäureproduktion (Achlorhydrie), da die Säureexposition das proteingebundene Vitamin freisetzt. Aus demselben Grund sind Menschen, die eine Langzeittherapie mit Antazida, Protonenpumpenhemmern, H2-Blockern oder anderen Antazida durchführen, einem erhöhten Risiko ausgesetzt. Die Ernährung von Vegetariern und Veganern liefert möglicherweise nicht genügend B12, es sei denn, sie nehmen ein Nahrungsergänzungsmittel zu sich. Ein Mangel an Vitamin B12 kann sich durch eine Neuropathie der Gliedmaßen oder eine Blutkrankheit namens perniziöse Anämie, eine Art megaloblastische Anämie, bemerkbar machen, die ein Gefühl von Müdigkeit und Schwäche, Benommenheit, Kopfschmerzen, Kurzatmigkeit, Appetitlosigkeit, Kribbeln, Veränderungen der Beweglichkeit, starke Gelenkschmerzen, Muskelschwäche, Gedächtnisstörungen, Bewusstseinsstörungen, Gehirnnebel und vieles mehr verursacht. Bleibt der Mangel bei Säuglingen unbehandelt, kann er zu neurologischen Schäden und Anämie führen. Der individuelle Folsäurespiegel kann den Verlauf der pathologischen Veränderungen und die Symptomatik des Vitamin-B12-Mangels beeinflussen. ⓘ
Vitamin B12 wurde als Folge der perniziösen Anämie entdeckt, einer Autoimmunerkrankung, bei der die Zahl der roten Blutkörperchen im Blut aufgrund eines Mangels an Vitamin B12 geringer ist als normal. Die Fähigkeit, das Vitamin zu absorbieren, nimmt mit dem Alter ab, insbesondere bei Menschen über 60 Jahren. ⓘ
| Strukturformel ⓘ | |||||||||
|---|---|---|---|---|---|---|---|---|---|
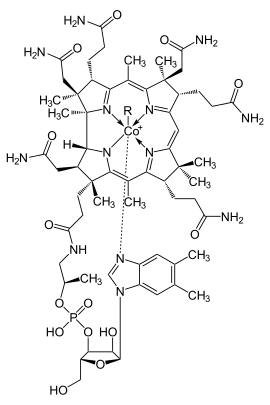
| |||||||||
| Adenosylcobalamin (AdoCbl, Coenzym B12): R = 5′-Desoxyadenosyl Cyanocobalamin: R = –C≡N Aquocobalamin (Vitamin B12a): R = –OH2 Hydroxycobalamin (Vitamin B12b): R = –OH Methylcobalamin (MeCbl, MeB12): R = –CH3 Nitritocobalamin (Vitamin B12c): R = –O–N=O | |||||||||
| Allgemeines | |||||||||
| Trivialname | Vitamin B12 | ||||||||
| Andere Namen |
| ||||||||
| Summenformel |
| ||||||||
| CAS-Nummer |
| ||||||||
| PubChem | 16072210 | ||||||||
| ATC-Code |
B03BA04 | ||||||||
| DrugBank | DB00115 | ||||||||
| Kurzbeschreibung | roter, kristalliner Feststoff (Cyanocobalamin, Hydroxocobalamin, Methylcobalamin) | ||||||||
| Vorkommen | tierische Produkte (Adenosylcobalamin, Hydroxocobalamin, Methylcobalamin), Dickdarm (durch bakterielle Produktion) | ||||||||
| Physiologie | |||||||||
| Funktion | Zellteilung, Blutbildung, Funktion des Nervensystems | ||||||||
| Täglicher Bedarf | 4 µg | ||||||||
| Folgen bei Mangel | Perniziöse Anämie, neurologische Erkrankungen (z. B. funikuläre Myelose), Glossitis, Diarrhöen | ||||||||
| Überdosis | nicht bekannt | ||||||||
| Eigenschaften | |||||||||
| Molare Masse | |||||||||
| Aggregatzustand | fest | ||||||||
| Schmelzpunkt |
zersetzt sich ab 392 °C (Cyanocobalamin) | ||||||||
| Löslichkeit | wenig löslich in Wasser: 12 g·l−1 (Cyanocobalamin), 20 g·l−1 (Hydroxocobalamin), unlöslich in Ether, Aceton und Chloroform (Cyanocobalamin), löslich in Alkohol (Cyanocobalamin) | ||||||||
| Sicherheitshinweise | |||||||||
| |||||||||
| Toxikologische Daten |
| ||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||
Cobalamine sind chemische Verbindungen, die in allen Lebewesen vorkommen und auch als Vitamin-B12-Gruppe (vereinfachend Vitamin B12) bezeichnet werden. Der wichtigste Vertreter aus der Cobalamin-Gruppe ist das umgangssprachlich ebenfalls als Vitamin B12 bezeichnete Adenosylcobalamin, welches auch als Coenzym B12 bekannt ist. Es ist als Kofaktor (Coenzym) Teil mehrerer Enzyme. Beim Menschen sind zwei Cobalamin-abhängige Enzyme bekannt, die am Stoffwechsel der Aminosäuren teilnehmen. Cobalamine enthalten das Spurenelement Cobalt als Zentralatom. ⓘ
Zur Vitamin-B12-Gruppe gehören auch die Speicherformen
- Aquocobalamin bzw. Aquacobalamin (Vitamin B12a, die konjugierte Säure des Hydroxocobalamins),
- Hydroxocobalamin bzw. Hydroxycobalamin (Vitamin B12b) und
- Nitritocobalamin (Vitamin B12c). ⓘ
Die Medizin verwendet die biologisch inaktiven Formen Cyanocobalamin und Hydroxocobalamin zur Vitamin-B12-Supplementierung und für andere therapeutische Zwecke. Im menschlichen Organismus werden diese Vorstufen in Adenosylcobalamin und Methylcobalamin umgewandelt. Beide sind als Coenzyme biologisch aktiv. ⓘ
Definition
Vitamin B12 ist ein Koordinationskomplex aus Kobalt, der das Zentrum eines Corrin-Liganden einnimmt und darüber hinaus an einen Benzimidazol-Liganden und eine Adenosylgruppe gebunden ist. Es ist ein tiefroter Feststoff, der sich in Wasser auflöst und rote Lösungen ergibt. ⓘ
Es ist eine Reihe von verwandten Arten bekannt, die sich ähnlich verhalten und insbesondere alle als Vitamine fungieren. Diese Verbindungen, zu denen auch Vitamin B12 gehört, werden häufig als "Cobalamine" bezeichnet. Diese chemischen Verbindungen haben eine ähnliche Molekülstruktur, von denen jede einzelne in einem biologischen System mit Vitaminmangel eine Vitaminaktivität aufweist; sie werden als "Vitamere" bezeichnet. Das Vitamin wirkt als Coenzym, was bedeutet, dass seine Anwesenheit für einige enzymkatalysierte Reaktionen erforderlich ist.
- Adenosylcobalamin
- Cyanocobalamin, der Adenosyl-Ligand in Vitamin B12 wird durch Cyanid ersetzt.
- Hydroxocobalamin, der Adenosyl-Ligand in Vitamin B12 wird durch Hydroxid ersetzt.
- Methylcobalamin: Der Adenosyl-Ligand in Vitamin B12 wird durch Methyl ersetzt. ⓘ
Cyanocobalamin ist eine hergestellte Form von B12. Durch bakterielle Fermentation entstehen AdoB12 und MeB12, die durch Zugabe von Kaliumcyanid in Gegenwart von Natriumnitrit und Hitze in Cyanocobalamin umgewandelt werden. Nach dem Verzehr wird das Cyanocobalamin in das biologisch aktive AdoB12 und MeB12 umgewandelt. Die beiden bioaktiven Formen von Vitamin B
12 sind Methylcobalamin im Cytosol und Adenosylcobalamin in den Mitochondrien. ⓘ
Cyanocobalamin ist die häufigste Form, die in Nahrungsergänzungsmitteln und zur Anreicherung von Lebensmitteln verwendet wird, da Cyanid das Molekül gegen Abbau stabilisiert. Methylcobalamin wird ebenfalls als Nahrungsergänzungsmittel angeboten. Die Verwendung von Adenosylcobalamin oder Methylcobalamin zur Behandlung von Vitamin-B12-Mangel ist nicht von Vorteil. ⓘ
Hydroxocobalamin kann zur Behandlung eines Vitamin-B12-Mangels intramuskulär gespritzt werden. Es kann auch intravenös zur Behandlung von Cyanidvergiftungen injiziert werden, da die Hydroxylgruppe durch Cyanid verdrängt wird, wodurch ein ungiftiges Cyanocobalamin entsteht, das mit dem Urin ausgeschieden wird. ⓘ
"Pseudovitamin B12" bezieht sich auf Verbindungen, die Corrinoide mit einer vitaminähnlichen Struktur, aber ohne Vitaminaktivität sind. Pseudovitamin B12 ist das Hauptcorrinoid in Spirulina, einem Algennahrungsmittel, von dem manchmal fälschlicherweise behauptet wird, es habe diese Vitaminaktivität. ⓘ
Mangel
Ein Mangel an Vitamin B12 kann zu schweren und irreversiblen Schäden führen, insbesondere am Gehirn und am Nervensystem. Bei einem nur geringfügig unter dem Normalwert liegenden Spiegel können eine Reihe von Symptomen auftreten, wie z. B. Müdigkeit und Schwäche, Ohnmachtsgefühle, Schwierigkeiten beim Gehen (taumelnde Gleichgewichtsstörungen), Depressionen, Gedächtnisschwäche, schlechte Reflexe, Verwirrtheit, Atemnot, Kopfschmerzen, blasse Haut und abnorme Empfindungen, insbesondere bei Menschen über 60 Jahren. Ein Vitamin-B12-Mangel kann auch Symptome von Manie und Psychose hervorrufen. Neben anderen Problemen können eine geschwächte Immunität, eine verminderte Fruchtbarkeit und eine Unterbrechung des Blutkreislaufs bei Frauen auftreten. ⓘ
Die Hauptform der Vitamin-B12-Mangelanämie ist die perniziöse Anämie. Sie ist durch einen Dreiklang von Symptomen gekennzeichnet:
- Anämie mit Promegaloblastose des Knochenmarks (megaloblastische Anämie). Dies ist auf die Hemmung der DNA-Synthese (insbesondere Purine und Thymidin) zurückzuführen.
- Gastrointestinale Symptome: Veränderung der Darmmotilität, z. B. leichter Durchfall oder Verstopfung, und Verlust der Kontrolle über Blase und Darm. Man nimmt an, dass diese Symptome auf eine gestörte DNA-Synthese zurückzuführen sind, die die Replikation an Gewebestellen mit hohem Zellumsatz hemmt. Dies kann auch auf den Autoimmunangriff auf die Parietalzellen des Magens bei perniziöser Anämie zurückzuführen sein. Es besteht ein Zusammenhang mit der antralen vaskulären Ektasie des Magens (die auch als Wassermelonenmagen bezeichnet werden kann) und der perniziösen Anämie.
- Neurologische Symptome: sensorische oder motorische Defizite (fehlende Reflexe, vermindertes Vibrations- oder Berührungsempfinden) und subakute kombinierte Degeneration des Rückenmarks. Zu den Mangelsymptomen bei Kindern gehören Entwicklungsverzögerung, Regression, Reizbarkeit, unwillkürliche Bewegungen und Hypotonie. ⓘ
Ein Vitamin-B12-Mangel wird am häufigsten durch Malabsorption verursacht, kann aber auch durch eine zu geringe Aufnahme, eine immunologische Gastritis, ein geringes Vorhandensein von Bindungsproteinen oder die Einnahme bestimmter Medikamente entstehen. Veganer - Menschen, die sich dafür entscheiden, keine tierischen Lebensmittel zu verzehren - sind gefährdet, weil pflanzliche Lebensmittel das Vitamin nicht in ausreichender Menge enthalten, um einen Vitaminmangel zu verhindern. Vegetarier - Menschen, die tierische Nebenprodukte wie Milchprodukte und Eier, aber kein Fleisch von Tieren verzehren - sind ebenfalls gefährdet. Ein Vitamin-B12-Mangel wurde bei 40 % bis 80 % der vegetarischen Bevölkerung beobachtet, die nicht zusätzlich ein Vitamin-B12-Präparat einnehmen oder mit Vitamin angereicherte Lebensmittel verzehren. In Hongkong und Indien wurde ein Vitamin-B12-Mangel bei etwa 80 % der veganen Bevölkerung festgestellt. Wie Vegetarier können auch Veganer dem vorbeugen, indem sie ein Nahrungsergänzungsmittel einnehmen oder mit B12 angereicherte Lebensmittel wie Getreide, pflanzliche Milch und Nährhefe regelmäßig zu sich nehmen. Ältere Menschen sind einem erhöhten Risiko ausgesetzt, da sie mit zunehmendem Alter dazu neigen, weniger Magensäure zu produzieren, ein Zustand, der als Achlorhydrie bekannt ist, wodurch sich die Wahrscheinlichkeit eines B12-Mangels aufgrund einer verminderten Aufnahme erhöht. ⓘ
Schwangerschaft, Stillzeit und frühe Kindheit
Die U.S. Recommended Dietary Allowance (RDA) für die Schwangerschaft beträgt 2,6 µg/Tag, für die Stillzeit 2,8 µg/Tag. Bei der Festlegung dieser Werte wurde die RDA von 2,4 µg/Tag für nicht schwangere Frauen zugrunde gelegt, zuzüglich der Menge, die während der Schwangerschaft auf den Fötus übertragen wird und der Menge, die mit der Muttermilch abgegeben wird. Die Europäische Behörde für Lebensmittelsicherheit (EFSA) hat jedoch auf der Grundlage derselben wissenschaftlichen Erkenntnisse eine angemessene Zufuhr (AI) von 4,5 μg/Tag für die Schwangerschaft und 5,0 μg/Tag für die Stillzeit festgelegt. Ein niedriger mütterlicher Vitamin-B12-Spiegel, definiert als Serumkonzentration von weniger als 148 pmol/l, erhöht das Risiko einer Fehlgeburt, einer Frühgeburt und eines niedrigen Geburtsgewichts des Neugeborenen. Während der Schwangerschaft konzentriert die Plazenta B12, so dass Neugeborene eine höhere Serumkonzentration haben als ihre Mütter. Da das kürzlich aufgenommene Vitamin die Plazenta besser erreicht, ist das von der werdenden Mutter aufgenommene Vitamin wichtiger als das im Lebergewebe enthaltene. Frauen, die wenig tierische Lebensmittel zu sich nehmen oder sich vegetarisch oder vegan ernähren, haben ein höheres Risiko, während der Schwangerschaft einen Vitaminmangel zu erleiden, als Frauen, die mehr tierische Produkte zu sich nehmen. Dieser Mangel kann zu Anämie führen und erhöht auch das Risiko, dass ihr gestilltes Kind einen Vitaminmangel entwickelt. ⓘ
Niedrige Vitaminkonzentrationen in der Muttermilch treten in Familien mit niedrigem sozioökonomischem Status oder geringem Verzehr von tierischen Erzeugnissen auf. Nur in wenigen Ländern, vor allem in Afrika, gibt es Programme zur obligatorischen Anreicherung von Lebensmitteln mit Weizen- oder Maismehl; in Indien gibt es ein freiwilliges Anreicherungsprogramm. Was die stillende Mutter zu sich nimmt, ist wichtiger als der Gehalt in ihrem Lebergewebe, da das Vitamin, das erst kürzlich aufgenommen wurde, besser in die Muttermilch gelangt. Der B12-Gehalt der Muttermilch nimmt im Laufe der Stillzeit sowohl bei gut ernährten als auch bei Müttern mit Vitaminmangel ab. Ausschließliches oder fast ausschließliches Stillen über sechs Monate hinaus ist ein starker Indikator für einen niedrigen Serumvitaminstatus bei stillenden Kindern. Dies gilt insbesondere dann, wenn der Vitaminstatus während der Schwangerschaft schlecht war und wenn die früh eingeführten Nahrungsmittel, mit denen der noch gestillte Säugling gefüttert wird, vegan sind. Das Risiko eines Mangels bleibt bestehen, wenn die Ernährung nach dem Abstillen arm an tierischen Produkten ist. Zu den Anzeichen eines niedrigen Vitaminspiegels bei Säuglingen und Kleinkindern können Anämie, schlechtes körperliches Wachstum und Verzögerungen in der neurologischen Entwicklung gehören. Kinder, bei denen ein niedriger B12-Serumspiegel diagnostiziert wird, können mit intramuskulären Injektionen behandelt werden und dann auf eine orale Nahrungsergänzung umgestellt werden. ⓘ
Magenbypass-Operation
Zur Behandlung von krankhafter Fettleibigkeit werden verschiedene Methoden der Magenbypass- oder Magenbeschränkungsoperation eingesetzt. Die Roux-en-Y-Magenbypass-Operation (RYGB), nicht aber die Sleeve-Magenbypass-Operation oder das Magenband, erhöht das Risiko eines Vitamin-B12-Mangels und erfordert eine präventive postoperative Behandlung entweder mit einer Injektion oder einer hochdosierten oralen Supplementierung. Bei einer postoperativen oralen Supplementierung können 1000 μg/Tag erforderlich sein, um einen Vitaminmangel zu verhindern. ⓘ
Diagnose
In einer Übersichtsarbeit heißt es: "Derzeit gibt es keinen 'Goldstandard'-Test für die Diagnose eines Vitamin-B12-Mangels, so dass für die Diagnose sowohl der klinische Zustand des Patienten als auch die Ergebnisse von Untersuchungen berücksichtigt werden müssen." Ein Vitaminmangel wird in der Regel vermutet, wenn ein routinemäßiges vollständiges Blutbild eine Anämie mit einem erhöhten mittleren korpuskulären Volumen (MCV) zeigt. Außerdem können im peripheren Blutausstrich Makrozyten und hypersegmentierte polymorphnukleare Leukozyten zu sehen sein. Die Diagnose wird auf der Grundlage von Vitamin-B12-Blutspiegeln unter 150-180 pmol/L (200-250 pg/ml) bei Erwachsenen unterstützt. Die Serumwerte können jedoch aufrechterhalten werden, während die B12-Speicher im Gewebe erschöpft werden. Daher bestätigen Serum-B12-Werte über dem Grenzwert für einen Mangel nicht unbedingt einen ausreichenden B12-Status. Aus diesem Grund werden erhöhte Serumhomocysteinwerte über 15 Mikromol/L und Methylmalonsäure (MMA) über 0,271 Mikromol/L als bessere Indikatoren für einen B12-Mangel angesehen, als sich nur auf die B12-Konzentration im Blut zu verlassen. Erhöhte MMA-Werte sind jedoch nicht beweiskräftig, da sie bei Menschen mit B12-Mangel, aber auch bei älteren Menschen mit Niereninsuffizienz auftreten, und erhöhte Homocystein-Werte sind nicht beweiskräftig, da sie auch bei Menschen mit Folatmangel auftreten. Darüber hinaus können erhöhte Methylmalonsäurewerte auch mit Stoffwechselstörungen wie Methylmalonsäureanämie zusammenhängen. Liegt eine Schädigung des Nervensystems vor und ist der Bluttest nicht aussagekräftig, kann eine Lumbalpunktion durchgeführt werden, um den B12-Spiegel im Liquor zu messen. ⓘ
Medizinische Anwendungen
Behebung eines Mangels
Ein schwerer Vitamin-B12-Mangel wird durch häufige intramuskuläre Injektionen hoher Dosen des Vitamins behoben, gefolgt von Erhaltungsdosen von Injektionen oder oraler Einnahme in größeren Abständen. Im Vereinigten Königreich besteht die anfängliche Standardtherapie aus intramuskulären Injektionen von 1000 μg Hydroxocobalamin dreimal wöchentlich für zwei Wochen oder bis zur Besserung der neurologischen Symptome, gefolgt von 1000 μg alle zwei oder drei Monate. Zu den Nebenwirkungen der Injektion gehören Hautausschlag, Juckreiz, Schüttelfrost, Fieber, Hitzewallungen, Übelkeit und Schwindelgefühl. ⓘ
Zyanidvergiftung
Bei Cyanidvergiftungen kann eine große Menge Hydroxocobalamin intravenös verabreicht werden, manchmal in Kombination mit Natriumthiosulfat. Der Wirkungsmechanismus ist einfach: Der Hydroxycobalamin-Hydroxid-Ligand wird durch das giftige Cyanid-Ion verdrängt, und das daraus resultierende ungiftige Cyanocobalamin wird mit dem Urin ausgeschieden. ⓘ
Empfehlungen für die Ernährung
Die meisten Menschen in den Vereinigten Staaten und im Vereinigten Königreich nehmen ausreichend Vitamin B12 zu sich. Der Anteil der Menschen mit niedrigen oder geringen Vitamin-B12-Spiegeln beträgt in der westlichen Welt jedoch bis zu 40 %. Getreidehaltige Lebensmittel können durch den Zusatz des Vitamins angereichert werden. Vitamin-B12-Ergänzungen sind als Einzel- oder Multivitamintabletten erhältlich. Pharmazeutische Zubereitungen von Vitamin B12 können durch intramuskuläre Injektion verabreicht werden. Da es nur wenige nicht-tierische Quellen für das Vitamin gibt, wird Veganern empfohlen, ein Nahrungsergänzungsmittel oder angereicherte Lebensmittel zur B12-Aufnahme zu verwenden, da sie sonst ernsthafte gesundheitliche Folgen riskieren. Kinder in einigen Regionen der Entwicklungsländer sind aufgrund des erhöhten Bedarfs während des Wachstums in Verbindung mit einer Ernährung, die wenig tierische Lebensmittel enthält, besonders gefährdet. ⓘ
Die US National Academy of Medicine aktualisierte 1998 die geschätzten durchschnittlichen Anforderungen (EARs) und die empfohlenen Tagesdosen (RDAs) für Vitamin B12. Der EAR-Wert für Vitamin B12 für Frauen und Männer ab 14 Jahren beträgt 2,0 μg/Tag; die RDA liegt bei 2,4 μg/Tag. Die RDA ist höher als die EAR, um Mengen zu ermitteln, die den überdurchschnittlichen Bedarf von Menschen decken. Die RDA für die Schwangerschaft beträgt 2,6 μg/Tag. Die RDA für die Stillzeit beträgt 2,8 μg/Tag. Für Säuglinge bis zu 12 Monaten beträgt die angemessene Zufuhr (AI) 0,4-0,5 μg/Tag (AI wird festgelegt, wenn keine ausreichenden Informationen zur Bestimmung der EAR und RDA vorliegen). Für Kinder im Alter von 1-13 Jahren steigt die RDA mit dem Alter von 0,9 auf 1,8 μg/Tag. Da 10 bis 30 % der älteren Menschen möglicherweise nicht in der Lage sind, das natürlich in Lebensmitteln vorkommende Vitamin B12 wirksam aufzunehmen, ist es für Personen über 50 Jahre ratsam, ihre RDA hauptsächlich durch den Verzehr von mit Vitamin B12 angereicherten Lebensmitteln oder durch ein Vitamin-B12-haltiges Ergänzungsmittel zu decken. Was die Sicherheit anbelangt, so werden für Vitamine und Mineralien tolerierbare Höchstmengen (UL) festgelegt, wenn es genügend Beweise gibt. Im Falle von Vitamin B12 gibt es keinen UL, da es keine Humandaten über schädliche Auswirkungen hoher Dosen gibt. Die EAR-, RDA-, AI- und UL-Werte werden zusammen als Referenzzufuhrwerte für die Ernährung (DRI) bezeichnet. ⓘ
Die Europäische Behörde für Lebensmittelsicherheit (EFSA) bezeichnet die kollektiven Informationen als "Referenzwerte für die Ernährung", wobei die Bevölkerungsreferenzzufuhr (PRI) anstelle der RDA und der durchschnittliche Bedarf anstelle der EAR steht. AI und UL werden von der EFSA genauso definiert wie in den Vereinigten Staaten. Für Frauen und Männer über 18 Jahren wird die angemessene Aufnahme (AI) auf 4,0 μg/Tag festgelegt. Die AI für die Schwangerschaft beträgt 4,5 μg/Tag, für die Stillzeit 5,0 μg/Tag. Für Kinder im Alter von 1-17 Jahren steigen die AIs mit dem Alter von 1,5 bis 3,5 μg/Tag. Diese AIs sind höher als die RDAs in den USA. Die EFSA überprüfte auch die Frage der Sicherheit und kam zu demselben Schluss wie die Vereinigten Staaten: Es gibt keine ausreichenden Beweise für die Festlegung eines UL für Vitamin B12. ⓘ
Das japanische National Institute of Health and Nutrition hat die RDA für Menschen ab 12 Jahren auf 2,4 μg/Tag festgelegt. Auch die Weltgesundheitsorganisation verwendet 2,4 μg/Tag als empfohlene Nährstoffzufuhr für dieses Vitamin für Erwachsene. ⓘ
Bei der Kennzeichnung von Lebensmitteln und Nahrungsergänzungsmitteln in den USA wird die Menge in einer Portion als "Prozent des Tageswertes" (%DV) angegeben. Für die Kennzeichnung von Vitamin B12 betrug 100 % des Tageswerts 6,0 μg, wurde aber am 27. Mai 2016 auf 2,4 μg herabgesetzt. Die Einhaltung der aktualisierten Kennzeichnungsvorschriften war bis zum 1. Januar 2020 für Hersteller mit einem jährlichen Lebensmittelumsatz von 10 Millionen US-Dollar oder mehr und bis zum 1. Januar 2021 für Hersteller mit einem geringeren Lebensmittelumsatz erforderlich. Eine Tabelle mit den alten und neuen Tageswerten für Erwachsene finden Sie unter Reference Daily Intake. ⓘ
Quellen
Bakterien und Archaeen
Vitamin B12 wird in der Natur von bestimmten Bakterien und Archaeen produziert. Es wird von einigen Bakterien in der Darmmikrobiota von Menschen und anderen Tieren synthetisiert, aber man ging lange davon aus, dass der Mensch es nicht aufnehmen kann, da es im Dickdarm gebildet wird, der dem Dünndarm nachgeschaltet ist, wo die Aufnahme der meisten Nährstoffe erfolgt. Wiederkäuer wie Kühe und Schafe sind Vormagenfermenter, d. h., pflanzliche Nahrung wird im Pansen mikrobiell fermentiert, bevor sie in den eigentlichen Magen (Labmagen) gelangt, und so nehmen sie das von Bakterien produzierte Vitamin B12 auf. Andere Säugetierarten (Beispiele: Kaninchen, Pika, Biber, Meerschweinchen) verzehren ballaststoffreiche Pflanzen, die den Darm passieren und im Blinddarm und Dickdarm bakteriell fermentiert werden. Die bei dieser Fermentation im Hinterdarm anfallenden Fäkalien der ersten Passage, die so genannten "Cecotropen", werden wieder aufgenommen, was als Cecotrophie oder Koprophagie bezeichnet wird. Die Wiederaufnahme ermöglicht die Absorption von Nährstoffen, die durch die bakterielle Verdauung verfügbar gemacht wurden, sowie von Vitaminen und anderen Nährstoffen, die von den Darmbakterien synthetisiert werden, einschließlich Vitamin B12. Pflanzenfresser, die keine Wiederkäuer sind, können einen vergrößerten Vormagen und/oder Dünndarm haben, um Platz für die bakterielle Fermentation und die Produktion von B-Vitaminen, einschließlich B12, zu schaffen. Damit die Darmbakterien Vitamin B12 produzieren können, muss das Tier ausreichende Mengen an Kobalt zu sich nehmen. Böden mit Kobaltmangel können zu einem B12-Mangel führen, so dass B12-Injektionen oder eine Kobaltergänzung für Nutztiere erforderlich sein können. ⓘ
Aus Tieren gewonnene Lebensmittel
Tiere speichern das mit der Nahrung aufgenommene Vitamin B12 in ihren Lebern und Muskeln, und einige geben das Vitamin in ihre Eier und Milch ab. Fleisch, Leber, Eier und Milch sind daher Quellen des Vitamins für andere Tiere, einschließlich des Menschen. Für den Menschen liegt die Bioverfügbarkeit von Eiern bei weniger als 9 %, während sie bei Fisch, Geflügel und Fleisch 40 bis 60 % beträgt. Insekten sind eine B12-Quelle für Tiere (einschließlich anderer Insekten und des Menschen). Zu den tierischen Nahrungsquellen mit einer hohen Konzentration an Vitamin B12 gehören Leber und anderes Organfleisch von Lamm, Kalb, Rind und Truthahn sowie Schalentiere und Krebsfleisch. ⓘ
Pflanzen und Algen
Zu den natürlichen Vitamin-B12-Quellen aus Pflanzen und Algen gehören fermentierte pflanzliche Lebensmittel wie Tempeh und aus Algen gewonnene Lebensmittel wie Nori und Seetang. Andere Algenarten sind reich an B12, wobei einige Arten, wie Porphyra yezoensis, so viel Cobalamin wie Leber enthalten. Methylcobalamin wurde in Chlorella vulgaris nachgewiesen. Da nur Bakterien und einige Archaeen die Gene und Enzyme besitzen, die für die Synthese von Vitamin B12 erforderlich sind, erhalten alle Pflanzen und Algen das Vitamin sekundär durch Symbiose mit verschiedenen Bakterienarten oder, im Falle von fermentierten pflanzlichen Lebensmitteln, durch bakterielle Fermentation. ⓘ
Die Academy of Nutrition and Dietetics hält pflanzliche Quellen und Algen für "unzuverlässig" und empfiehlt Veganern, stattdessen auf angereicherte Lebensmittel und Nahrungsergänzungsmittel zurückzugreifen. ⓘ
Angereicherte Lebensmittel
Zu den Lebensmitteln, für die mit Vitamin B12 angereicherte Versionen erhältlich sind, gehören Frühstückscerealien, pflanzliche Milchersatzprodukte wie Soja- und Hafermilch, Energieriegel und Nährhefe. Der Anreicherungsbestandteil ist Cyanocobalamin. Durch mikrobielle Fermentation wird Adenosylcobalamin gewonnen, das dann durch Zugabe von Kaliumcyanid oder Thiocyanat in Gegenwart von Natriumnitrit und Hitze in Cyanocobalamin umgewandelt wird. ⓘ
Ab 2019 ist in neunzehn Ländern die Anreicherung von Weizenmehl, Maismehl oder Reis mit Vitamin B12 vorgeschrieben. Die meisten davon befinden sich in Südostafrika oder Mittelamerika. ⓘ
Vegane Organisationen empfehlen unter anderem, dass jeder Veganer B12 entweder über angereicherte Lebensmittel oder über Nahrungsergänzungsmittel zu sich nimmt. ⓘ
Ergänzungen

Vitamin B12 ist in Multivitamintabletten enthalten; in einigen Ländern werden Lebensmittel auf Getreidebasis, wie Brot und Nudeln, mit B12 angereichert. In den USA sind nicht verschreibungspflichtige Produkte erhältlich, die jeweils bis zu 5.000 µg enthalten, und es ist ein gängiger Bestandteil von Energydrinks und Energy Shots, die in der Regel ein Vielfaches der empfohlenen Tagesdosis an B12 enthalten. Das Vitamin kann auch als verschreibungspflichtiges Produkt durch Injektion oder auf anderem Wege verabreicht werden. ⓘ
Sublinguales Methylcobalamin, das kein Cyanid enthält, ist in Tabletten zu 5 mg erhältlich. Es ist davon auszugehen, dass der Stoffwechsel und die biologische Verteilung von Methylcobalamin ähnlich sind wie bei anderen Vitamin-B12-Quellen in der Ernährung. Die Menge an Cyanid in Cyanocobalamin ist im Allgemeinen nicht besorgniserregend, auch nicht in der 1.000-µg-Dosis, da die Menge an Cyanid (20 µg in einer 1.000-µg-Cyanocobalamin-Tablette) geringer ist als die tägliche Aufnahme von Cyanid aus der Nahrung und Cyanocobalamin daher nicht als Gesundheitsrisiko angesehen wird. Menschen mit Nierenproblemen sollten keine hohen Dosen von Cyanocobalamin einnehmen, da sie Cyanid nicht effizient verstoffwechseln können. ⓘ
Intramuskuläre oder intravenöse Injektion
Eine Injektion von Hydroxycobalamin wird häufig verwendet, wenn die Absorption im Verdauungstrakt beeinträchtigt ist. Bei hochdosierten oralen Ergänzungspräparaten (z. B. 0,5-1,0 mg oder mehr) ist diese Vorgehensweise jedoch möglicherweise nicht erforderlich, da bei großen Mengen des oral eingenommenen Vitamins sogar die 1 % bis 5 % des freien kristallinen B12, die im gesamten Darm durch passive Diffusion absorbiert werden, ausreichen können, um die erforderliche Menge zu liefern. ⓘ
Eine Person mit Cobalamin-C-Krankheit (die zu einer kombinierten Methylmalonsäureurie und Homocystinurie führt) muss möglicherweise mit intravenösem oder intramuskulärem Hydroxocobalamin oder transdermalem B12 behandelt werden, da orales Cyanocobalamin für die Behandlung der Cobalamin-C-Krankheit unzureichend ist. ⓘ
Bei der Vitamin-B12-Supplementierung verwendete Nanotechnologien
Die herkömmliche Verabreichung gewährleistet keine spezifische Verteilung und kontrollierte Freisetzung von Vitamin B12. Darüber hinaus erfordern therapeutische Protokolle, die Injektionen beinhalten, medizinisches Personal und das Pendeln der Patienten zum Krankenhaus, was die Kosten der Behandlung erhöht und die Lebensweise der Patienten beeinträchtigt. Die gezielte Verabreichung von Vitamin B12 ist ein Schwerpunkt der modernen Verordnungen. So würde beispielsweise die Zufuhr des Vitamins zum Knochenmark und zu den Nervenzellen die Wiederherstellung des Myelins unterstützen. Derzeit werden mehrere Nanoträger-Strategien zur Verbesserung der Verabreichung von Vitamin B12 entwickelt, um die Verabreichung zu vereinfachen, die Kosten zu senken, die Pharmakokinetik zu verbessern und die Lebensqualität der Patienten zu erhöhen. ⓘ
Pseudovitamin-B12
Pseudovitamin-B12 bezieht sich auf B12-ähnliche Analoga, die beim Menschen biologisch inaktiv sind. Es wurde festgestellt, dass die meisten Cyanobakterien, einschließlich Spirulina, und einige Algen wie Porphyra tenera (die in Japan zur Herstellung eines getrockneten Algennahrungsmittels namens Nori verwendet wird) hauptsächlich Pseudovitamin-B12 anstelle von biologisch aktivem B12 enthalten. Diese Pseudovitaminverbindungen finden sich in einigen Arten von Schalentieren, in essbaren Insekten und manchmal auch als metabolische Abbauprodukte von Cyanocobalamin, das Nahrungsergänzungsmitteln und angereicherten Lebensmitteln zugesetzt wird. ⓘ
Pseudovitamin-B12 kann sich als biologisch aktives Vitamin B12 erweisen, wenn ein mikrobiologischer Test mit Lactobacillus delbrueckii subsp. lactis durchgeführt wird, da die Bakterien das Pseudovitamin verwerten können, obwohl es für den Menschen nicht verfügbar ist. Um den B12-Gehalt zuverlässig zu bestimmen, gibt es fortschrittlichere Techniken. Eine dieser Techniken umfasst die Vorabtrennung durch Kieselgel und die anschließende Bewertung mit B12-abhängigen E. coli-Bakterien. ⓘ
Ein verwandtes Konzept sind Antivitamin-B12-Verbindungen (oft synthetische B12-Analoga), die nicht nur keine Vitaminwirkung haben, sondern auch die Aktivität des echten Vitamin B12 aktiv stören. Bei der Entwicklung dieser Verbindungen wurde hauptsächlich das Metallion ersetzt. Diese Verbindungen haben das Potenzial, zur Analyse der B12-Verwertungswege oder sogar zur Bekämpfung von B12-abhängigen Krankheitserregern eingesetzt zu werden. ⓘ
Wechselwirkungen mit Medikamenten
H2-Rezeptor-Antagonisten und Protonenpumpenhemmer
Die Magensäure wird benötigt, um Vitamin B12 aus Proteinen freizusetzen und zu absorbieren. Eine verringerte Sekretion von Magensäure und Pepsin aufgrund der Einnahme von H2-Blockern oder Protonenpumpeninhibitoren (PPI) kann die Absorption von proteingebundenem (diätetischem) Vitamin B12 verringern, nicht jedoch die von zusätzlichem Vitamin B12. Beispiele für H2-Rezeptor-Antagonisten sind Cimetidin, Famotidin, Nizatidin und Ranitidin. Beispiele für PPIs sind Omeprazol, Lansoprazol, Rabeprazol, Pantoprazol und Esomeprazol. Ein klinisch signifikanter Vitamin-B12-Mangel und eine megaloblastische Anämie sind unwahrscheinlich, es sei denn, diese medikamentösen Therapien werden über zwei oder mehr Jahre fortgesetzt oder die Nahrungsaufnahme liegt unter den empfohlenen Werten. Ein symptomatischer Vitaminmangel ist wahrscheinlicher, wenn die Person achlorhydrisch wird (ein vollständiges Fehlen der Magensäuresekretion), was bei Protonenpumpenhemmern häufiger vorkommt als bei H2-Blockern. ⓘ
Metformin
Erniedrigte Serumspiegel von Vitamin B12 treten bei bis zu 30 % der Personen auf, die langfristig das Antidiabetikum Metformin einnehmen. Ein Mangel tritt nicht auf, wenn die Vitamin-B12-Aufnahme über die Nahrung ausreichend ist oder prophylaktisch eine B12-Supplementierung erfolgt. Wird ein Mangel festgestellt, kann Metformin weiter eingenommen werden, während der Mangel mit B12-Ergänzungspräparaten behoben wird. ⓘ
Andere Medikamente
Bestimmte Medikamente können die Absorption von oral eingenommenem Vitamin B12 vermindern, darunter: Colchizin, Kaliumpräparate mit verlängerter Wirkstofffreisetzung und Antibiotika wie Gentamicin, Neomycin und Tobramycin. Die Medikamente gegen Krampfanfälle Phenobarbital, Pregabalin, Primidon und Topiramat werden mit niedrigeren als den normalen Vitamin-Serumkonzentrationen in Verbindung gebracht. Bei Personen, denen Valproat verschrieben wurde, waren die Serumspiegel jedoch höher. Darüber hinaus können bestimmte Arzneimittel die Labortests für das Vitamin beeinträchtigen, z. B. Amoxicillin, Erythromycin, Methotrexat und Pyrimethamin. ⓘ
Chemie

Vitamin B12 ist von allen Vitaminen das chemisch komplexeste. Die Struktur von B12 basiert auf einem Corrin-Ring, der dem Porphyrin-Ring des Häms ähnelt. Das zentrale Metallion ist Kobalt. Als luftstabiler Feststoff isoliert und im Handel erhältlich, liegt Kobalt in Vitamin B12 (Cyanocobalamin und anderen Vitaminen) in der Oxidationsstufe +3 vor. Biochemisch gesehen kann das Kobaltzentrum sowohl an reduktiven Prozessen mit zwei als auch mit einem Elektron teilnehmen, um die "reduzierten" (B12r, +2 Oxidationsstufe) und "superreduzierten" (B12s, +1 Oxidationsstufe) Formen zu erreichen. Die Fähigkeit, zwischen den Oxidationsstufen +1, +2 und +3 hin- und herzuwechseln, ist für die vielseitige Chemie von Vitamin B12 verantwortlich, die es ihm ermöglicht, als Spender von Desoxyadenosyl-Radikalen (radikalische Alkylquelle) und als Äquivalent eines Methylkations (elektrophile Alkylquelle) zu dienen. Vier der sechs Koordinationsstellen werden durch den Corrinring bereitgestellt, eine fünfte durch eine Dimethylbenzimidazolgruppe. Die sechste Koordinationsstelle, das reaktive Zentrum, ist variabel und kann eine Cyanogruppe (-CN), eine Hydroxylgruppe (-OH), eine Methylgruppe (-CH3) oder eine 5′-Desoxyadenosylgruppe sein. Historisch gesehen ist die kovalente Kohlenstoff-Kobalt-Bindung eines der ersten Beispiele für Kohlenstoff-Metall-Bindungen, die in der Biologie entdeckt wurden. Die Hydrogenasen und zwangsläufig auch die Enzyme, die mit der Nutzung von Kobalt in Verbindung stehen, gehen Metall-Kohlenstoff-Bindungen ein. Tiere sind in der Lage, Cyanocobalamin und Hydroxocobalamin in die bioaktiven Formen Adenosylcobalamin und Methylcobalamin umzuwandeln, indem sie die Cyano- oder Hydroxylgruppen enzymatisch ersetzen. ⓘ

Methoden für die Analyse von Vitamin B12 in Lebensmitteln
Zur Bestimmung des Vitamin-B12-Gehalts in Lebensmitteln wurden verschiedene Methoden angewandt, darunter mikrobiologische Tests, Chemilumineszenz-Tests, polarographische, spektrophotometrische und Hochleistungsflüssigkeitschromatographie-Verfahren. Der mikrobiologische Assay war die am häufigsten verwendete Methode zur Bestimmung von Lebensmitteln, bei der bestimmte Vitamin B12 benötigende Mikroorganismen wie Lactobacillus delbrueckii subsp. lactis ATCC7830 verwendet wurden. Aufgrund der hohen Messunsicherheit von Vitamin B12 ist sie jedoch nicht mehr die Referenzmethode. Außerdem erfordert dieser Test eine Inkubation über Nacht und kann falsche Ergebnisse liefern, wenn inaktive Vitamin-B12-Analoga in den Lebensmitteln vorhanden sind. Gegenwärtig werden zur Bestimmung des Vitamin-B12-Gehalts in Lebensmitteln der Radioisotopen-Verdünnungstest (RIDA) mit markiertem Vitamin B12 und Schweine-Infusion verwendet. Aus früheren Berichten geht hervor, dass mit der RIDA-Methode höhere Konzentrationen von Vitamin B12 in Lebensmitteln nachgewiesen werden können als mit der mikrobiologischen Testmethode. ⓘ
Seit der Jahrtausendwende wird zur Bestimmung des Cobalamin-Spiegels im Blut ein CBLA-Assay durchgeführt (competitive-binding luminescence assay), der die früheren mikrobiologischen und Radioisotopen-Dilutions-Assays der 1970er Jahre abgelöst hat. Einzelfallberichte und kleinere Studien deuten darauf hin, dass diese neueren Assays bei Patienten mit perniziöser Anämie systematische Fehler aufweisen. Kleine klinische Serien bestätigten, dass die Assays eine hohe Rate falsch-negativer Ergebnisse (zwischen 22 und 35 %) produzieren, d. h., in einem von drei bis fünf Fällen wird statt eines Cobalamin-Mangels fälschlicherweise ein Normalspiegel ermittelt. ⓘ
Biochemie
Funktion des Coenzyms
Vitamin B12 fungiert als Coenzym, was bedeutet, dass seine Anwesenheit bei einigen enzymkatalysierten Reaktionen erforderlich ist. Im Folgenden sind die drei Enzymklassen aufgeführt, die manchmal B12 benötigen, um zu funktionieren (bei Tieren):
- Isomerasen
- Umlagerungen, bei denen ein Wasserstoffatom direkt zwischen zwei benachbarten Atomen übertragen wird, wobei gleichzeitig der zweite Substituent X ausgetauscht wird, der ein Kohlenstoffatom mit Substituenten, ein Sauerstoffatom eines Alkohols oder ein Amin sein kann. Dabei wird die adoB12-Form (Adenosylcobalamin) des Vitamins verwendet.
- Methyltransferasen
- Übertragungen von Methylgruppen (-CH3) zwischen zwei Molekülen. Sie verwenden die MeB12 (Methylcobalamin)-Form des Vitamins.
- Dehalogenasen
- Einige Arten von anaeroben Bakterien synthetisieren B12-abhängige Dehalogenasen, die potenziell für den Abbau von chlorierten Schadstoffen eingesetzt werden können. Die Mikroorganismen sind entweder zur De-novo-Biosynthese von Corrinoiden fähig oder sind von exogenem Vitamin B12 abhängig. ⓘ
Beim Menschen sind zwei große Coenzym-B12-abhängige Enzymfamilien bekannt, die den ersten beiden Reaktionstypen entsprechen. Diese werden durch die beiden folgenden Enzyme verkörpert:

Die Methylmalonyl-Coenzym-A-Mutase (MUT) ist ein Isomerase-Enzym, das die AdoB12-Form und den Reaktionstyp 1 verwendet, um L-Methylmalonyl-CoA in Succinyl-CoA umzuwandeln, ein wichtiger Schritt beim katabolischen Abbau einiger Aminosäuren zu Succinyl-CoA, das dann über den Zitronensäurezyklus in die Energiegewinnung eingeht. Diese Funktion geht bei Vitamin-B12-Mangel verloren und kann klinisch als erhöhte Methylmalonsäurekonzentration (MMA) im Serum gemessen werden. Die MUT-Funktion ist für eine ordnungsgemäße Myelinsynthese erforderlich. Ausgehend von Tierversuchen geht man davon aus, dass die erhöhte Methylmalonyl-CoA-Konzentration zu Methylmalonat (Methylmalonsäure) hydrolysiert, einer neurotoxischen Dicarbonsäure, die neurologische Schäden verursacht. ⓘ
Die Methionin-Synthase, die vom MTR-Gen kodiert wird, ist ein Methyltransferase-Enzym, das mit Hilfe von MeB12 und dem Reaktionstyp 2 eine Methylgruppe von 5-Methyltetrahydrofolat auf Homocystein überträgt und so Tetrahydrofolat (THF) und Methionin erzeugt. Diese Funktion geht bei Vitamin-B12-Mangel verloren, was zu einem erhöhten Homocysteinspiegel und zum Abfangen von Folat als 5-Methyltetrahydrofolat führt, aus dem THF (die aktive Form von Folat) nicht wiedergewonnen werden kann. THF spielt eine wichtige Rolle bei der DNA-Synthese, so dass eine verminderte Verfügbarkeit von THF zu einer ineffektiven Produktion von Zellen mit schnellem Umsatz führt, insbesondere von roten Blutkörperchen und auch von Darmwandzellen, die für die Resorption verantwortlich sind. THF kann über MTR regeneriert oder aus frischem Folat in der Nahrung gewonnen werden. So lösen sich alle DNA-synthetischen Effekte des B12-Mangels, einschließlich der megaloblastischen Anämie der perniziösen Anämie, auf, wenn ausreichend Folat in der Nahrung vorhanden ist. Die bekannteste "Funktion" von B12 (die an der DNA-Synthese, der Zellteilung und der Anämie beteiligt ist) ist also in Wirklichkeit eine fakultative Funktion, die durch die B12-Erhaltung einer aktiven Form von Folat vermittelt wird, die für eine effiziente DNA-Produktion erforderlich ist. Andere Cobalamin benötigende Methyltransferase-Enzyme sind auch in Bakterien bekannt, wie z.B. Me-H4-MPT, Coenzym-M-Methyltransferase. ⓘ
Vereinfachend zusammengefasst ist Vitamin B12 wichtig für die Zellteilung und Blutbildung sowie die Funktion des Nervensystems. ⓘ
Coenzym B12 nimmt im humanen Organismus als Coenzym an nur zwei enzymatischen Reaktionen teil:
- N5-Methyl-Tetrahydrofolat-Homocystein-S-Methyltransferase (Methionin-Synthase, EC 2.1.1.13) und
- Methylmalonyl-CoA-Mutase (EC 5.4.99.2) ⓘ
Ist dieser Schritt gehemmt, kommt es zu einem Anstieg von Methylmalonsäure im Plasma und vor allem im Urin. Dieser Stoffwechselweg spielt offenbar eine besondere Rolle im ZNS, da sich ein Vitamin-B12-Mangel bisweilen sogar vor der typischen Anämie mit Symptomen wie z. B. der funikulären Myelose, einer Störung der Pyramidenbahn und der Hinterstränge, aber auch scheinbaren Altersdemenzen und anderem bemerkbar macht. Daher sollte insbesondere bei älteren Patienten mit neurologischer Symptomatik ein Vitamin-B12-Mangel als mögliche (Mit-)Ursache ausgeschlossen und ggf. behandelt werden. Erste neurologische Symptome äußern sich als so genannte Polyneuropathie in Form von Kribbelparästhesien oder anderen Missempfindungen (z. B. leichtes Brennen) in verschiedenen Körperregionen, die anfangs nur vorübergehend sind. ⓘ
Physiologie
Absorption
Die Aufnahme von B12 aus der Nahrung erfolgt über zwei Prozesse. Der erste ist ein Vitamin B12-spezifischer Darmmechanismus mit Hilfe des intrinsischen Faktors, durch den alle paar Stunden 1-2 Mikrogramm absorbiert werden können, wodurch der größte Teil des mit der Nahrung aufgenommenen Vitamins absorbiert wird. Der zweite ist ein passiver Diffusionsprozess. Die menschliche Physiologie der aktiven Vitamin-B12-Aufnahme aus der Nahrung ist komplex. Das proteingebundene Vitamin B12 muss durch die Wirkung von Verdauungsproteasen sowohl im Magen als auch im Dünndarm aus den Proteinen freigesetzt werden. Die Magensäure löst das Vitamin aus den Nahrungspartikeln; daher können Antazida und säurehemmende Medikamente (insbesondere Protonenpumpenhemmer) die Aufnahme von B12 hemmen. Nachdem B12 durch Pepsin im Magen von den Proteinen in der Nahrung befreit wurde, bindet sich das R-Protein (auch bekannt als Haptocorrin und Transcobalamin-1), ein B12-bindendes Protein, das in den Speicheldrüsen produziert wird, an B12. Dadurch wird das Vitamin vor dem Abbau in der sauren Umgebung des Magens geschützt. Dieses Muster der B12-Übertragung auf ein spezielles Bindungsprotein, das in einem früheren Verdauungsschritt abgesondert wurde, wird vor der Absorption noch einmal wiederholt. Das nächste Bindungsprotein für B12 ist der Intrinsic Factor (IF), ein von den parietalen Zellen des Magens synthetisiertes Protein, das als Reaktion auf Histamin, Gastrin und Pentagastrin sowie auf das Vorhandensein von Nahrung ausgeschüttet wird. Im Zwölffingerdarm verdauen Proteasen R-Proteine und setzen ihr gebundenes B12 frei, das sich dann an IF bindet und einen Komplex (IF/B12) bildet. B12 muss an IF gebunden sein, damit es effizient absorbiert werden kann, da die Rezeptoren auf den Enterozyten im terminalen Ileum des Dünndarms nur den B12-IF-Komplex erkennen; außerdem schützt der Intrinsic Factor das Vitamin vor dem Abbau durch Darmbakterien. ⓘ
Die Aufnahme von Vitamin B12 aus der Nahrung erfordert also einen intakten und funktionierenden Magen, ein exokrines Pankreas, einen Intrinsic-Faktor und einen Dünndarm. Probleme mit einem dieser Organe machen einen Vitamin-B12-Mangel möglich. Menschen, denen der Intrinsic Factor fehlt, haben eine verminderte Fähigkeit, B12 zu absorbieren. Bei der perniziösen Anämie liegt ein Mangel an IF aufgrund einer autoimmunen atrophischen Gastritis vor, bei der sich Antikörper gegen Parietalzellen bilden. Die Antikörper können sich abwechselnd gegen die IF bilden und an sie binden, wodurch sie an der Ausübung ihrer B12-Schutzfunktion gehindert werden. Aufgrund der Komplexität der B12-Absorption haben geriatrische Patienten, von denen viele aufgrund einer eingeschränkten Funktion der Parietalzellen hypoazid sind, ein erhöhtes Risiko für einen B12-Mangel. Dies führt dazu, dass 80-100 % der oral eingenommenen Dosen mit den Fäkalien ausgeschieden werden, im Gegensatz zu 30-60 %, die bei Personen mit adäquaten IF mit den Fäkalien ausgeschieden werden. ⓘ
Sobald der IF/B12-Komplex von spezialisierten ilealen Rezeptoren erkannt wird, wird er in den portalen Kreislauf transportiert. Das Vitamin wird dann auf Transcobalamin II (TC-II/B12) übertragen, das als Plasmatransporter dient. Erbliche Defekte in der Produktion der Transcobalamine und ihrer Rezeptoren können zu einem funktionellen B12-Mangel und zu einer infantilen megaloblastischen Anämie sowie zu einer anormalen B12-bezogenen Biochemie führen, selbst in einigen Fällen mit normalen B12-Werten im Blut. Damit das Vitamin in den Zellen wirken kann, muss der TC-II/B12-Komplex an einen Zellrezeptor binden und endozytiert werden. Das Transcobalamin II wird in einem Lysosom abgebaut, und das freie B12 wird schließlich in das Zytoplasma freigesetzt, wo es von bestimmten zellulären Enzymen in das richtige Coenzym umgewandelt werden kann (siehe oben). ⓘ
Untersuchungen zur intestinalen Absorption von B12 zeigen, dass die obere Grenze der Absorption pro oraler Einzeldosis unter normalen Bedingungen bei etwa 1,5 µg liegt. Der passive Diffusionsprozess der B12-Absorption - normalerweise ein sehr kleiner Teil der Gesamtabsorption des Vitamins aus der Nahrung - kann die R-Protein- und IF-vermittelte Absorption übersteigen, wenn die oralen B12-Dosen sehr hoch sind (tausend oder mehr µg pro Dosis), wie es bei der oralen B12-Supplementierung in Tablettenform üblich ist. Auf diese Weise können perniziöse Anämie und bestimmte andere Störungen der B12-Absorption mit oralen Megadosen von B12 behandelt werden, ohne dass die zugrunde liegenden Absorptionsstörungen behoben werden. Siehe den Abschnitt über Nahrungsergänzungsmittel weiter oben. ⓘ
Lagerung und Ausscheidung
Wie schnell sich der B12-Spiegel verändert, hängt vom Gleichgewicht zwischen der Menge an B12, die mit der Nahrung aufgenommen wird, der Menge, die ausgeschieden wird, und der Menge, die absorbiert wird, ab. Die Gesamtmenge des im Körper gespeicherten Vitamin B12 beträgt bei Erwachsenen etwa 2-5 mg. Etwa 50 % davon sind in der Leber gespeichert. Etwa 0,1 % davon gehen täglich durch Ausscheidungen in den Darm verloren, da nicht alle diese Ausscheidungen resorbiert werden. Die Galle ist die wichtigste Form der B12-Ausscheidung; der größte Teil des in der Galle ausgeschiedenen B12 wird über den enterohepatischen Kreislauf recycelt. Überschüssiges B12, das die Bindungskapazität des Blutes übersteigt, wird normalerweise mit dem Urin ausgeschieden. Aufgrund des äußerst effizienten enterohepatischen Kreislaufs von B12 kann die Leber Vitamin B12 für 3 bis 5 Jahre speichern; daher ist ein ernährungsbedingter Mangel an diesem Vitamin bei Erwachsenen selten, wenn keine Malabsorptionsstörungen vorliegen. Bei fehlender enterohepatischer Rückresorption wird Vitamin B12 nur für Monate bis ein Jahr gespeichert. ⓘ
Synthese
Biosynthese
Vitamin B12 wird aus einem tetrapyrrolischen Gerüst gewonnen, das durch die Enzyme Deaminase und Cosynthetase gebildet wird, die Aminolävulinsäure über Porphobilinogen und Hydroxymethylbilan in Uroporphyrinogen III umwandeln. Letzteres ist das erste makrozyklische Zwischenprodukt, das Häm, Chlorophyll, Sirohäm und B12 selbst gemeinsam haben. Spätere Schritte, insbesondere der Einbau der zusätzlichen Methylgruppen seiner Struktur, wurden unter Verwendung von 13C-Methyl-markiertem S-Adenosylmethionin untersucht. Erst mit Hilfe eines gentechnisch veränderten Stammes von Pseudomonas denitrificans, in dem acht der an der Biosynthese des Vitamins beteiligten Gene überexprimiert worden waren, konnte die vollständige Abfolge der Methylierung und anderer Schritte bestimmt werden, so dass alle Zwischenstufen des Weges vollständig bekannt waren. ⓘ
Es ist bekannt, dass Arten aus den folgenden Gattungen und die folgenden einzelnen Arten B12 synthetisieren: Propionibacterium shermanii, Pseudomonas denitrificans, Streptomyces griseus, Acetobacterium, Aerobacter, Agrobacterium, Alcaligenes, Azotobacter, Bacillus, Clostridium, Corynebacterium, Flavobacterium, Lactobacillus, Micromonospora, Mycobacterium, Nocardia, Proteus, Rhizobium, Salmonella, Serratia, Streptococcus und Xanthomonas. ⓘ
Industriell
Die industrielle Produktion von B12 wird durch Fermentation ausgewählter Mikroorganismen erreicht. Streptomyces griseus, ein Bakterium, das früher für einen Pilz gehalten wurde, war viele Jahre lang die kommerzielle Quelle für Vitamin B12. Die Arten Pseudomonas denitrificans und Propionibacterium freudenreichii subsp. shermanii werden heute häufiger verwendet. Sie werden unter speziellen Bedingungen gezüchtet, um den Ertrag zu steigern. Rhone-Poulenc verbesserte den Ertrag durch gentechnische Veränderung von P. denitrificans. Propionibacterium, die anderen üblicherweise verwendeten Bakterien, produzieren keine Exotoxine oder Endotoxine und werden von der US-amerikanischen Food and Drug Administration allgemein als sicher anerkannt (GRAS-Status). ⓘ
Die weltweite Gesamtproduktion von Vitamin B12 belief sich 2008 auf 35 000 kg (77 175 lb). ⓘ
Labor
Die vollständige Laborsynthese von B12 wurde 1972 von Robert Burns Woodward und Albert Eschenmoser durchgeführt und ist nach wie vor eine der klassischen Leistungen der organischen Synthese. Sie erforderte den Einsatz von 91 Postdocs (hauptsächlich in Harvard) und 12 Doktoranden (an der ETH Zürich) aus 19 Nationen. Die Synthese stellt eine formale Totalsynthese dar, da die Forschergruppen nur das bekannte Zwischenprodukt Brenztraubensäure herstellten, über dessen chemische Umwandlung in Vitamin B12 bereits berichtet wurde. Obwohl die Eschenmoser-Woodward-Synthese von Vitamin B12 eine intellektuelle Höchstleistung darstellt, ist sie aufgrund ihrer Länge von 72 chemischen Schritten und einer chemischen Gesamtausbeute von deutlich unter 0,01 % von keiner praktischen Bedeutung. Und obwohl es seit 1972 sporadische Syntheseversuche gegeben hat, bleibt die Eschenmoser-Woodward-Synthese die einzige abgeschlossene (formale) Totalsynthese. ⓘ
Geschichte
Beschreibungen von Mangelerscheinungen
Zwischen 1849 und 1887 beschrieb Thomas Addison einen Fall von perniziöser Anämie, William Osler und William Gardner beschrieben erstmals einen Fall von Neuropathie, Hayem beschrieb große Erythrozyten im peripheren Blut bei diesem Zustand, die er "Riesenblutkörperchen" nannte (heute Makrozyten genannt), Paul Ehrlich identifizierte Megaloblasten im Knochenmark und Ludwig Lichtheim beschrieb einen Fall von Myelopathie. ⓘ
Identifizierung der Leber als Anti-Anämie-Nahrungsmittel
In den 1920er Jahren entdeckte George Whipple, dass die Einnahme großer Mengen roher Leber die Blutarmut bei Hunden am schnellsten zu heilen schien, und stellte die Hypothese auf, dass der Verzehr von Leber die perniziöse Anämie behandeln könnte. Edwin Cohn stellte einen Leberextrakt her, der bei der Behandlung der perniziösen Anämie 50- bis 100-mal wirksamer war als die natürlichen Leberprodukte. William Castle wies nach, dass Magensaft einen "intrinsischen Faktor" enthält, der in Verbindung mit Fleischverzehr die Aufnahme des Vitamins in diesem Zustand fördert. 1934 erhielt George Whipple gemeinsam mit William P. Murphy und George Minot den Nobelpreis für Physiologie oder Medizin für die Entdeckung einer wirksamen Behandlung der perniziösen Anämie mit Leberkonzentrat, das später einen hohen Gehalt an Vitamin B12 aufwies. ⓘ
Identifizierung des Wirkstoffs
Während ihrer Tätigkeit im Bureau of Dairy Industry, U.S. Department of Agriculture, wurde Mary Shaw Shorb mit der Erforschung des Bakterienstamms Lactobacillus lactis Dorner (LLD) beauftragt, der zur Herstellung von Joghurt und anderen Milchprodukten verwendet wurde. Für das Nährmedium von LLD wurde Leberextrakt benötigt. Shorb wusste, dass derselbe Leberextrakt zur Behandlung der perniziösen Anämie verwendet wurde (ihr Schwiegervater war an dieser Krankheit gestorben), und schloss daraus, dass LLD als Testmethode zur Identifizierung des Wirkstoffs entwickelt werden könnte. Während ihrer Zeit an der University of Maryland erhielt sie ein kleines Stipendium von Merck und entwickelte in Zusammenarbeit mit Karl Folkers von diesem Unternehmen den LLD-Test. Dieser identifizierte den "LLD-Faktor" als wesentlich für das Wachstum der Bakterien. Shorb, Folker und Alexander R. Todd von der Universität Cambridge nutzten den LLD-Test, um den Faktor gegen perniziöse Anämie aus Leberextrakten zu extrahieren, ihn zu reinigen und ihm den Namen Vitamin B12 zu geben. 1955 trug Todd zur Aufklärung der Struktur des Vitamins bei, wofür er 1957 den Nobelpreis für Chemie erhielt. Die vollständige chemische Struktur des Moleküls wurde 1956 von Dorothy Hodgkin auf der Grundlage kristallographischer Daten bestimmt. Für diese und andere kristallographische Analysen erhielt sie 1964 den Nobelpreis für Chemie. Hodgkin entschlüsselte später auch die Struktur von Insulin. ⓘ
Fünf Personen wurden mit Nobelpreisen für direkte und indirekte Studien über Vitamin B12 ausgezeichnet: George Whipple, George Minot und William Murphy (1934), Alexander R. Todd (1957) und Dorothy Hodgkin (1964). ⓘ
Dorothy Hodgkin ⓘ
Kommerzielle Produktion
Die industrielle Produktion von Vitamin B12 erfolgt durch Fermentation ausgewählter Mikroorganismen. Wie bereits erwähnt, gelang Robert Burns Woodward und Albert Eschenmoser 1972 die vollständig synthetische Laborsynthese von B12. Dieses Verfahren hat jedoch kein kommerzielles Potenzial, da es fast 70 Schritte erfordert und eine Ausbeute von weit unter 0,01 % aufweist. ⓘ
Gesellschaft und Kultur
In den 1970er Jahren entwickelte John A. Myers, ein in Baltimore ansässiger Arzt, ein Programm zur intravenösen Injektion von Vitaminen und Mineralien bei verschiedenen Erkrankungen. Die Formel enthielt 1000 µg Cyanocobalamin. Dies wurde als Myers-Cocktail bekannt. Nach seinem Tod im Jahr 1984 verschrieben andere Ärzte und Naturheilkundler die "intravenöse Mikronährstofftherapie" mit unbelegten gesundheitsbezogenen Behauptungen zur Behandlung von Müdigkeit, Energiemangel, Stress, Angstzuständen, Migräne, Depressionen, Immunschwäche, zur Förderung der Gewichtsabnahme und mehr. Abgesehen von einem Bericht über Fallstudien gibt es jedoch keine in der wissenschaftlichen Literatur bestätigten Vorteile. Ärzte in Kliniken und Kurbädern verschreiben Versionen dieser intravenösen Kombinationspräparate, aber auch intramuskuläre Injektionen nur von Vitamin B12. Eine Untersuchung der Mayo Clinic kam zu dem Schluss, dass es keine stichhaltigen Beweise dafür gibt, dass Vitamin-B12-Injektionen einen Energieschub oder eine Gewichtsabnahme bewirken. ⓘ
Es gibt Hinweise darauf, dass Ärzte bei älteren Menschen häufig Cyanocobalamin-Injektionen in unangemessener Weise verschreiben und verabreichen, was dadurch belegt wird, dass die meisten Probanden in einer großen Studie entweder normale Serumkonzentrationen aufwiesen oder vor den Injektionen nicht getestet worden waren. ⓘ
Definitionen
Das Lexikon der medizinischen Laboratoriumsdiagnostik definiert Vitamin B12 als „wasserlösliche Vitamine, welche in Form von zwei Coenzymen im zellulären Stoffwechsel von Fettsäuren und aliphatischen Aminosäuren eine wesentliche Rolle spielen“. Demnach werden unter dem Begriff substituierte Corrinoide bzw. Cobalamine mit biologischer Wirkung zusammengefasst. Forschungsgeschichtlich bedingte Synonymbezeichnungen des Vitamin B12 sind Antiperniziosa-Faktor und Extrinisic-Faktor. Die Definition des Pschyrembel betont die Beteiligung der Vitamingruppe an der Zellteilung, der Erythropoese und der Myelinbildung. ⓘ
Die International Union of Nutritional Sciences (IUNS) und die International Union of Pure and Applied Chemistry (IUAPC) geben an, dass „Vitamin B12“ als allgemeine Beschreibung für alle Corrinoide verwendet werden sollte, die qualitativ die biologische Aktivität von Cyanocobalamin aufweisen. ⓘ
In PubChem steht Vitamin B12 synonym für das Cyanocobalamin, ebenso in verschiedener Fachliteratur. ⓘ
Nicht zu verwechseln mit den eigentlichen Cobalaminen sind die Trans-Cobalamine, bei denen es sich lediglich um Transportproteine für Vitamin B12 handelt. ⓘ
Vorkommen
| Lebensmittel | Gehalt in µg/100 g (siehe Hinweis) |
|---|---|
| Rinderleber | 65 |
| Kalbsleber | 60 |
| Spirulina maxima | (57) |
| Schweineleber | 40 |
| Kalbsniere | 25 |
| Hühnerleber | 20 |
| Schweineniere | 15 |
| Austern | 14,6 |
| Hering | 11 |
| Makrele | 9 |
| Rindfleisch (Muskel) | 5,0 |
| Thunfisch | 4,3 |
| Camembert 30 % Fett i. Tr. | 3,1 |
| Lachs | 2,9 |
| Steppengrille | 2,9 |
| Emmentaler 45 % Fett i. Tr. | 2,2 |
| Hühnereigelb | 2,0 |
| Totentrompete, Echter Pfifferling (Wildform) | 1,1–2,7 |
| Aal | 1 |
| Blutwurst | 1 |
| Schweinefleisch (Muskel) | 0,8 |
| Speisequark 20 % Fett i. Tr. | 0,8 |
| Kabeljau | 0,5–0,8 |
| Kuhmilch 3,5 % Fett | 0,4 |
| Sojasauce | 0,3 |
| Tempeh | 0,3 |
| Ingwer | 0,16 |
| Hühnereiweiß | 0,1 |
| Gemüse | 0,01 |
| Sauerkraut | 0 |
Herstellung
Für die chemische Reindarstellung von Vitamin B12 aus Streptomyces-Kulturen oder aus Leber wird Cyanid hinzugesetzt. Die chemische Synthese von Vitamin B12 ist wegen der Komplexität der Cobalamine sehr aufwendig. Supplemente für den menschlichen Verzehr oder zum Einsatz in Tiernahrung (Geflügel und Schweine) werden daher meist mittels gentechnisch veränderten Mikroorganismen hergestellt. Da lediglich das gereinigte Endprodukt auf den Markt kommt, besteht hierfür keine Kennzeichnungspflicht. ⓘ
Überdosierung (Hypervitaminose)
Therapeutische – meist intravenöse – Überdosen werden mit lokalen allergischen Beschwerden sowie einer Form der Akne (Acne medicamentosa) in Verbindung gebracht. Auch die extrem hoch dosierte Verwendung als Gegengift von bis zu 5 g (entspricht 5.000.000 µg) Hydroxocobalamin ist laut EFSA erprobt und sicher. ⓘ
Die wissenschaftlichen Einschätzungen einer täglichen Höchsteinnahmemenge (engl. UL, Tolerable Upper Intake Level) variieren und basieren auf einfachen Schätzungen, weil – so u. a. das Bundesinstitut für Risikobewertung (BfR) – Untersuchungen mit sehr hohen Einnahmedosen „keine nachteiligen gesundheitlichen Effekte gezeigt haben“ bzw. die zur Berechnung benötigten Toxizitätswerte NOAEL und LOAEL nicht vorliegen. Einen UL hatte der frühere Wissenschaftliche Lebensmittelausschuss der EU-Kommission (SCF) 2000 bzw. die Europäische Behörde für Lebensmittelsicherheit (EFSA) 2006 nicht festgelegt. ⓘ
Für Nahrungsergänzungsmittel hat das BfR 2021 die Einnahme von 25 μg Vitamin B12 pro Tag (2004 noch 9 μg) als sichere Obergrenze angegeben. Gemäß EFSA von 2006 waren von einer zusätzlichen Aufnahme von bis zu 1.000 µg pro Tag bei Patienten mit eingeschränkter Vitamin-B12-Aufnahme keine unerwünschten Wirkungen bekannt, diese wurden aber auch nicht erfasst. Die Datenlage nach Stand 2004 ließ außerdem keine Risikoabschätzung zur oralen Verabreichung explizit von Cyanocobalamin zu. ⓘ
Nach Einschätzung des Arbeitskreises Nahrungsergänzungsmittel (AK NEM) des Bund für Lebensmittelrecht und Lebensmittelkunde ist die rein theoretische Einstufung des BfR von 2004 spekulativ und basiert nicht auf realen Einnahme-Daten. 2005 stuften die WHO bzw. die FAO Vitamin B12 als Substanz ohne bekannten negativen Gesundheitseffekt ein („Nutrient substances with no identified adverse health effects“). Bei solchen Substanzen wird für die Risikobewertung der „highest observed intake“ („höchste beobachtete Einnahme“) als Richtlinie für die sichere Obergrenze gewählt. Der AK NEM verwies in seiner Stellungnahme auf D. Richardson, der basierend auf der WHO-Einstufung, einen Wert von 2.000 µg täglicher Einnahme als Richtlinie („guidance level“) ermittelte, also einen deutlich höheren Wert als der BfR. Der in Italien gewählte obere Grenzwert liegt laut AK NEM bei 1.000 µg. ⓘ
Im Rahmen einer 2018 veröffentlichten Studie wurden die Daten aus 20 vorhergegangenen Einzelstudien analysiert sowie eine Mendelsche Randomisierung durchgeführt. Die Autoren konnten die Korrelation zwischen erhöhten Cobalamin-Spiegeln und bestimmten Tumoren (Adenokarzinom, kleinzelliges Bronchialkarzinom) nachweisen und vertreten die Auffassung, dass ihre Ergebnisse die Hypothese eines kausalen Zusammenhangs unterstützen. Die in die Studie eingeschlossenen Patienten wiesen vor allem aufgrund diverser genetischer Varianten erhöhte Cobalamin-Spiegel auf. Unklar bleibt daher, inwiefern risikobehaftete Cobalamin-Spiegel auch durch orale Supplementation erreicht werden können. Unklar bleibt auch, ob ein kausaler Zusammenhang zwischen einem hohen Spiegel und dem Risiko besteht oder ob ein hoher Cobalamin-Spiegel nur ein Indikator für andere Risikofaktoren wie z. B. erhöhten Fleischkonsum und Entzündungen wegen chronischer Erkrankungen ist oder weil die Nahrungsergänzungsmittel wegen anderer Leiden genommen werden. ⓘ
Weitere Verwendung
Verwendung als Gegengift
Hydroxycobalamin ist ein Antidot bei Vergiftungen durch Cyanide bzw. Blausäure. Cyanidvergiftungen kommen hauptsächlich im Rahmen von Kunststoffbränden vor. Weitere Ursachen können die versehentliche oder absichtliche Einnahme, das Einatmen oder ein Hautkontakt bei Industrieunfällen sein. ⓘ
Die klinische Symptomatik Koma, Bradykardie und Hypotonie von Rauchgasexponierten im Rahmen eines Brandes sollte an eine Cyanidintoxikation denken lassen. Wie Kohlenmonoxid und Nitrose-Gase ist auch Blausäure im Rahmen der Brandbekämpfung messbar und erhärtet den Verdacht auf eine Intoxikation. Die Therapie mit 4-Dimethylaminophenol (4-DMAP) ist bei Rauchgasexponierten zu meiden, da dies als Met-Hämoglobinbildner die Oxigenierung negativ beeinflusst. ⓘ
Unter dem Handelsnamen Cyanokit erhielt die Firma Merck KGaA am 29. November 2007 für Hydroxocobalamin über das zentralisierte Verfahren von der Europäischen Kommission die Marktzulassung zur Behandlung erwiesener oder vermuteter Cyanidvergiftung bei Erwachsenen und Kindern. Hydroxocobalamin ist eine Form von Vitamin B12, das Cyanid-Ionen bindet. Dabei entsteht Cyanocobalamin, das über die Nieren mit dem Urin ausgeschieden wird. So wird die Bindung des Cyanids an die Cytochrom-c-Oxidase verhindert. Die Anfangsdosis für Cyanokit bei Erwachsenen liegt bei 5 g des Wirkstoffes, die als intravenöse Infusion zu verabreichen ist. In Abhängigkeit von der Schwere der Vergiftung und der klinischen Reaktion kann eine zweite Dosis von 5 g bis zu einer Gesamtdosis von 10 g verabreicht werden. ⓘ
Das Risiko-Nutzen-Verhältnis im Rahmen der Behandlung der Cyanidvergiftung mit Hydroxocobalamin ist gut. Als häufige Nebenwirkung kommt es zu einer harmlosen ca. eine Woche andauernden Rotfärbung der Haut und des Urins sowie zu einem leichten Blutdruckanstieg. ⓘ
Topische Anwendung auf der Haut
Cyanocobalamin wird alternativmedizinisch zur Behandlung des atopischen Ekzems (Neurodermitis) und der Schuppenflechte (Psoriasis) in Form von Salben mit 0,07%igem Vitamin-B12 auf Grundlage von Avocadoöl eingesetzt. Bevor die Salbe im November 2009 unter dem Markennamen Regividerm als Medizinprodukt auf den Markt gebracht wurde, fand sie durch die Fernsehdokumentation Heilung unerwünscht – Wie Pharmakonzerne ein Medikament verhindern, die am 19. Oktober 2009 von der ARD gesendet wurde, ein großes und im Verlauf auch kritisches Medieninteresse. Peter Schönhöfer, ein klinischer Pharmakologe, der vom WDR im Rahmen der Produktion dieser Dokumentation mit der Begutachtung der Studien beauftragt worden war, zog deren Aussagekraft kurz nach der Sendung in Zweifel, da aufgrund der niedrigen Patientenzahlen überhaupt keine belastbare Aussage darstellbar sei. Seine schon während der Produktion dem WDR gegenüber ausgesprochenen Warnungen seien ignoriert worden. Der Dermatologe und Studien-Koautor Peter Altmeyer äußerte gegenüber FOCUS, seine kleine Seitenvergleichsstudie ohne Kontrollgruppe mit 13 Psoriasis- und 49 Neurodermitispatienten sei von der ARD hochgejubelt und falsch interpretiert worden. Für einen Beweis der Wirksamkeit wäre ein Feldversuch mit einigen tausend Patienten notwendig. ⓘ
Seit März 2010 darf das besagte Produkt nicht mehr unter dem Namen Regividerm vertrieben werden, es heißt nun Mavena B12 Salbe. ⓘ
In der gültigen S2K-Leitlinie „Neurodermitis“ ist eine Supplementierung von Vitamin B12 nicht als wirksame Therapie gelistet. ⓘ




