Natriumthiosulfat

| |
| |

| |
| Bezeichnungen | |
|---|---|
| IUPAC-Bezeichnung
Natriumthiosulfat
| |
| Andere Namen
Natriumhyposulfit
Hyposulfit von Soda Hypo | |
| Bezeichner | |
| |
3D-Modell (JSmol)
|
|
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| EC-Nummer |
|
PubChem CID
|
|
| RTECS-Nummer |
|
| UNII |
|
InChI
| |
SMILES
| |
| Eigenschaften | |
Chemische Formel
|
Na2S2O3 |
| Molekulare Masse | 158,11 g/mol (wasserfrei) 248,18 g/mol (Pentahydrat) |
| Erscheinungsbild | Weiße Kristalle |
| Geruch | Geruchlos |
| Dichte | 1,667 g/cm3 |
| Schmelzpunkt | 48,3 °C (118,9 °F; 321,4 K) (Pentahydrat) |
| Siedepunkt | 100 °C (212 °F; 373 K) (Pentahydrat, - 5H2O Zersetzung) |
Löslichkeit in Wasser
|
70,1 g/100 mL (20 °C) 231 g/100 mL (100 °C) |
| Löslichkeit | vernachlässigbar in Alkohol |
Brechungsindex (nD)
|
1.489 |
| Struktur | |
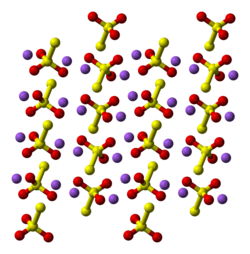
Kristallstruktur
|
monoklin |
| Gefahren | |
| GHS-Kennzeichnung: | |
Piktogramme
|

|
Signalwort
|
Warnhinweis |
Gefahrenhinweise
|
H315, H319, H335 |
Sicherheitshinweise
|
P261, P264, P271, P280, P302+P352, P304+P340, P305+P351+P338, P312, P321, P332+P313, P337+P313, P362, P403+P233, P405, P501 |
| NFPA 704 (Feuerdiamant) | |
| Flammpunkt | Nicht brennbar |
| Sicherheitsdatenblatt (SDS) | Externes SDB |
| Verwandte Verbindungen | |
Andere Kationen
|
Thioschwefelsäure Lithium-Thiosulfat Kaliumthiosulfat |
Wenn nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |
Natriumthiosulfat (Natriumthiosulfat) ist eine anorganische Verbindung mit der Formel Na2S2O3.xH2O. Normalerweise ist es als weißes oder farbloses Pentahydrat Na2S2O3-5H2O erhältlich. Der Feststoff ist eine kristalline, effloreszierende (leicht wasserabgebende) Substanz, die sich gut in Wasser löst. ⓘ
Natriumthiosulfat wird im Goldbergbau, bei der Wasseraufbereitung, in der analytischen Chemie, bei der Entwicklung von fotografischen Filmen und Abzügen auf Silberbasis und in der Medizin verwendet. In der Medizin wird Natriumthiosulfat unter anderem zur Behandlung von Zyanidvergiftungen und Pityriasis eingesetzt. Es steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation. ⓘ
Natriumthiosulfat (Na2S2O3) ist das stabile Natriumsalz der in freiem Zustand instabilen Thioschwefelsäure. ⓘ
Verwendungen
Natriumthiosulfat wird vor allem in der Industrie verwendet. Es wird zum Beispiel verwendet, um Farbstoffe in ihre lösliche Leukoform umzuwandeln. Es wird auch zum Bleichen von "Wolle, Baumwolle, Seide, ... Seifen, Klebstoffen, Ton, Sand, Bauxit und ... Speiseölen, Speisefetten und Gelatine" verwendet. ⓘ
Medizinische Verwendungen
Natriumthiosulfat wird zur Behandlung von Zyanidvergiftungen eingesetzt. Weitere Verwendungszwecke sind die örtliche Behandlung von Ringelflechte und Tinea versicolor sowie die Behandlung einiger Nebenwirkungen von Hämodialyse und Chemotherapie. ⓘ
Fotografische Verarbeitung
Silberhalogenide, z. B. AgBr, typische Bestandteile fotografischer Emulsionen, lösen sich bei der Behandlung mit wässrigem Thiosulfat auf; diese Anwendung als fotografisches Fixiermittel wurde von John Herschel entdeckt. Es wird sowohl für die Entwicklung von Filmen als auch von Fotopapier verwendet; das Natriumthiosulfat ist als fotografisches Fixiermittel bekannt und wird oft als "Hypo" bezeichnet, nach der ursprünglichen chemischen Bezeichnung "Hyposulfit von Soda". Für diese Anwendung wird in der Regel Ammoniumthiosulfat gegenüber Natriumthiosulfat bevorzugt. ⓘ
Neutralisierung von gechlortem Wasser
Ammoniumthiosulfat wird zur Entchlorung von Leitungswasser und zur Senkung des Chlorgehalts in Aquarien, Schwimmbädern und Spas (z. B. nach einer Superchlorierung) sowie in Wasseraufbereitungsanlagen zur Behandlung von abgesetztem Rückspülwasser vor der Einleitung in Flüsse verwendet. Die Reduktionsreaktion verläuft analog zur Jodreduktionsreaktion. ⓘ
Bei der Prüfung des pH-Werts von Bleichmitteln neutralisiert Natriumthiosulfat die farbentfernende Wirkung von Bleichmitteln und ermöglicht die Prüfung des pH-Werts von Bleichlösungen mit flüssigen Indikatoren. Die betreffende Reaktion ist mit der Jodreaktion vergleichbar: Thiosulfat reduziert das Hypochlorit (Wirkstoff in Bleichmitteln) und wird dabei zu Sulfat oxidiert. Die vollständige Reaktion ist:
- 4 NaClO + Na2S2O3 + 2 NaOH → 4 NaCl + 2 Na2SO4 + H2O ⓘ
In ähnlicher Weise reagiert Natriumthiosulfat mit Brom, wobei das freie Brom aus der Lösung entfernt wird. Lösungen von Natriumthiosulfat werden in Chemielabors häufig als Vorsichtsmaßnahme bei der Arbeit mit Brom und zur sicheren Entsorgung von Brom, Jod oder anderen starken Oxidationsmitteln verwendet. ⓘ
Struktur
Vom Pentahydrat sind zwei Polymorphien bekannt. Das wasserfreie Salz kommt in mehreren Polymorphen vor. Im festen Zustand ist das Thiosulfat-Anion tetraedrisch und entsteht durch Ersetzen eines der Sauerstoffatome durch ein Schwefelatom in einem Sulfat-Anion. Der S-S-Abstand deutet auf eine Einfachbindung hin, was bedeutet, dass der terminale Schwefel eine signifikante negative Ladung trägt und die S-O-Wechselwirkungen eher Doppelbindungscharakter haben. ⓘ
Herstellung
Im industriellen Maßstab wird Natriumthiosulfat vor allem aus flüssigen Abfallprodukten der Natriumsulfid- oder Schwefelfarbstoffherstellung hergestellt. ⓘ
Im Labor kann dieses Salz durch Erhitzen einer wässrigen Lösung von Natriumsulfit mit Schwefel oder durch Sieden von wässrigem Natriumhydroxid und Schwefel nach der folgenden Gleichung hergestellt werden:
- 6 NaOH + 4 S → 2 Na2S + Na2S2O3 + 3 H2O ⓘ
Natriumthiosulfat wird durch Erhitzen von fein verteiltem Schwefel in einer Natriumsulfitlösung unter Druck hergestellt:
Alternativ kann das Natriumsulfit auch mit Natriumdisulfid umgesetzt werden. ⓘ
Wichtigste Reaktionen

Natriumthiosulfat bildet unter Normalbedingungen mit 5 Äquivalenten Kristallwasser farblose Kristalle, welche gut wasserlöslich sind. Beim Lösungsvorgang kühlt sich die Flüssigkeit stark ab, da die Hydratationsenthalpie kleiner ist als die Gitterenergie und die fehlende Wärmemenge dem System entzogen wird. Das Pentahydrat Na2S2O3·5H2O ist auch unter dem Namen Fixiersalz bekannt, da es bei der Filmentwicklung zur Fixierung dient. Unter dem Namen Antichlor wird es nach dem Bleichen von Papier- und Textilfasern verwendet, um überschüssiges Chlor zu entfernen.
Die Pentahydrat-Kristalle haben einen Schmelzpunkt von 48,5 °C, die Schmelze kann unterkühlt werden und gibt beim Erstarren eine große Menge von Kristallisationswärme ab. ⓘ
Wasserfreies Natriumthiosulfat tritt in vier polymorphen Kristallformen auf. Die bei Raumtemperatur stabile α–Form kristalliert in einem monoklinen Kristallgitter. Bei 330 °C wandelt sie sich in die trikline β–Form um. Diese bildet beim weiteren Erhitzen bei 388 °C eine kubische γ–Form. Alle Phasenübergänge sind reversibel und die Formen stehen enantiotrop zueinander. Eine metastabile orthorhombische α'–Form kann durch die Dehydratation des Pentahydrats oder Abkühlung der β–Form erhalten werden. Diese wandelt sich um 155 °C exotherm in die α–Form um und steht somit monotrop zu dieser. Die γ–Form zersetzt sich ab 444 °C in einer exothermen Reaktion zu Natriumsulfat und Natriumpentasulfid. ⓘ
Wird zur wässrigen Natriumthiosulfat-Lösung Säure hinzugefügt, so scheidet sich nach kurzer Zeit Schwefel in Form einer gelblichen Trübung aus. Die freigesetzte, instabile Thioschwefelsäure (H2S2O3) zerfällt nämlich rasch zu Schwefel und Schwefeldioxid:
Die wasserunlöslichen Silberhalogenide (AgCl, AgBr) werden durch eine Fixiersalzlösung aufgelöst. Durch die Bildung des wasserlöslichen Natriumdithiosulfatoargentat(I)-Komplexes wird der entwickelte Film lichtunempfindlich:
Natriumthiosulfat ist ein Reduktionsmittel und reagiert daher leicht mit dem Oxidationsmittel Kaliumpermanganat. ⓘ
Thiosulfatsalze zersetzen sich typischerweise bei der Behandlung mit Säuren. Die anfängliche Protonierung erfolgt am Schwefel. Wenn die Protonierung in Diethylether bei -78 °C durchgeführt wird, erhält man H2S2O3 (Thioschwefelsäure). Es handelt sich um eine relativ starke Säure mit pKas-Werten von 0,6 bzw. 1,7 für die erste und zweite Dissoziation. ⓘ
Koordinationschemie
Thiosulfat ist ein starker Ligand für weiche Metallionen. Ein typischer Komplex ist [Pd(S2O3)2(Ethylendiamin)]2-, der ein Paar S-gebundener Thiosulfatliganden aufweist. Natriumthiosulfat und Ammoniumthiosulfat wurden als Alternative zu Cyanid für die Extraktion von Gold vorgeschlagen. Die Vorteile dieses Ansatzes bestehen darin, dass (i) Thiosulfat weitaus weniger toxisch ist als Cyanid und (ii) dass Erze, die für die Goldcyanidierung refraktär sind (z. B. kohlenstoffhaltige oder Carlin-Erze), mit Thiosulfat gelaugt werden können. Zu den Problemen dieses alternativen Verfahrens gehören der hohe Verbrauch von Thiosulfat und das Fehlen einer geeigneten Rückgewinnungstechnik, da [Au(S2O3)2]3- nicht an Aktivkohle adsorbiert, die bei der Goldcyanidierung standardmäßig zur Abtrennung des Goldkomplexes aus der Erzaufschlämmung verwendet wird. ⓘ
Iodometrie
In der analytischen Chemie ist die wichtigste Verwendung, dass das Thiosulfat-Anion in wässriger Lösung stöchiometrisch mit Iod reagiert und es zu Iodid reduziert, während das Thiosulfat zu Tetrathionat oxidiert wird:
- 2 S2O2-3 + I2 → S4O2-6 + 2 I- ⓘ
Aufgrund des quantitativen Charakters dieser Reaktion und der ausgezeichneten Haltbarkeit von Na2S2O3-5H2O wird es als Titriermittel für die Iodometrie verwendet. Na2S2O3-5H2O ist auch ein Bestandteil von Joduhr-Experimenten. ⓘ
Diese besondere Verwendung kann zur Messung des Sauerstoffgehalts von Wasser durch eine lange Reihe von Reaktionen im Winkler-Test für gelösten Sauerstoff eingerichtet werden. Es wird auch zur volumetrischen Schätzung der Konzentrationen bestimmter Verbindungen in Lösung (z. B. Wasserstoffperoxid) und zur Schätzung des Chlorgehalts in handelsüblichem Bleichpulver und Wasser verwendet. ⓘ
Reaktion mit Aluminiumkationen
Natriumthiosulfat wird in der analytischen Chemie verwendet. Es kann beim Erhitzen mit einer Probe, die Aluminiumkationen enthält, einen weißen Niederschlag bilden:
- 2 Al3+ + 3 S2O2-3 + 3 H2O → 3 SO2 + 3 S + 2 Al(OH)3 ⓘ
Organische Chemie
Die Alkylierung von Natriumthiosulfat führt zu S-Alkylthiosulfaten, die als Buntes Salze bezeichnet werden. Die Alkylthiosulfate sind hydrolysefähig, so dass das Thiol entsteht. Diese Reaktion wird durch eine Synthese von Thioglykolsäure veranschaulicht:
- ClCH2CO2H + Na2S2O3 → Na[O3S2CH2CO2H] + NaCl
- Na[O3S2CH2CO2H] + H2O → HSCH2CO2H + NaHSO4 ⓘ
Verwendung
Natriumthiosulfat kann in der Analogfotografie als Fixiersalz dienen, im Bergbau zur Extraktion von Silberchlorid aus Silbererzen und in der Galvanotechnik zur Herstellung von Gold- und Silberbädern. In der Medizin wird es als Gegenmittel bei Cyanidvergiftungen verwendet, dabei wird weniger gefährliches Thiocyanat gebildet. ⓘ
Natriumthiosulfat dient als Antichlor zum Beenden von Bleich- oder Desinfektionsprozessen mit Chlor. Dabei wird das Chlor zu Chlorid (bzw. Salzsäure) reduziert, und es entsteht Hydrogensulfat:
- Fehler beim Parsen (Syntaxfehler): {\displaystyle \ce{S2O3^2- + 4 Cl2 + 13 H2O -> 2 HSO4- + 8 H3O+ + 8 Cl- <span title="Aus: Deutsche Wikipedia, Abschnitt "Verwendung"" class="plainlinks">[https://de.wikipedia.org/wiki/Natriumthiosulfat#Verwendung <span style="color:#dddddd">ⓘ</span>]</span>}}
In der Chemie wird es zur Bestimmung der Iodzahl verwendet, in der Iodometrie wird Thiosulfat zu Tetrathionat oxidiert:
- . ⓘ
Weitere Verwendung findet es als Pentahydrat in sogenannten Wärmekissen. Durch das Biegen eines Metallplättchens entsteht ein Kristallisationskeim, der die exotherme Kristallisation auslöst. Die Regeneration des Kissens erfolgt durch Erwärmen in kochendem Wasser, wobei die Kristalle wieder geschmolzen (gelöst) werden. ⓘ
Im Rahmen von Studien erfolgt die Anwendung von Thiosulfat zur Verhinderung von Hörverlusten, die im Rahmen einer cisplatinhaltigen Chemotherapie speziell bei Kindern auftreten können. ⓘ





![{\displaystyle \mathrm {2\ Na_{2}S_{2}O_{3}+AgCl\rightarrow Na_{3}[Ag(S_{2}O_{3})_{2}]+NaCl} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/bfb0ab7aad92851dce645ab6aa3774f8bb601209)
