Stoffwechsel
| Teil einer Serie über ⓘ |
| Biochemie |
|---|
 |
|
|
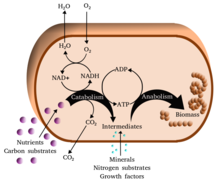
Der Stoffwechsel (/məˈtæbəlɪzəm/, von griechisch μεταβολή metabolē, "Veränderung") ist die Gesamtheit der lebenserhaltenden chemischen Reaktionen in Organismen. Die drei Hauptzwecke des Stoffwechsels sind: die Umwandlung der in der Nahrung enthaltenen Energie in Energie, die für den Betrieb zellulärer Prozesse zur Verfügung steht; die Umwandlung der Nahrung in Bausteine für Proteine, Lipide, Nukleinsäuren und einige Kohlenhydrate; und die Beseitigung von Stoffwechselabfällen. Diese enzymkatalysierten Reaktionen ermöglichen es den Organismen, zu wachsen und sich zu vermehren, ihre Strukturen zu erhalten und auf ihre Umwelt zu reagieren. Das Wort Stoffwechsel kann sich auch auf die Summe aller chemischen Reaktionen beziehen, die in lebenden Organismen ablaufen, einschließlich der Verdauung und des Transports von Stoffen in und zwischen verschiedenen Zellen; in diesem Fall wird die oben beschriebene Reihe von Reaktionen innerhalb der Zellen als intermediärer (oder intermediärer) Stoffwechsel bezeichnet. ⓘ
Stoffwechselreaktionen können als katabolisch - der Abbau von Verbindungen (z. B. von Glukose zu Pyruvat durch Zellatmung) - oder anabolisch - der Aufbau (Synthese) von Verbindungen (wie Proteinen, Kohlenhydraten, Lipiden und Nukleinsäuren) - kategorisiert werden. Beim Katabolismus wird in der Regel Energie freigesetzt, während beim Anabolismus Energie verbraucht wird. ⓘ
Die chemischen Reaktionen des Stoffwechsels sind in Stoffwechselwegen organisiert, in denen eine Chemikalie in einer Reihe von Schritten in eine andere Chemikalie umgewandelt wird, wobei jeder Schritt durch ein bestimmtes Enzym erleichtert wird. Enzyme sind für den Stoffwechsel von entscheidender Bedeutung, da sie es den Organismen ermöglichen, erwünschte Reaktionen, die Energie benötigen und nicht von selbst ablaufen, durch Kopplung mit spontanen Reaktionen, die Energie freisetzen, in Gang zu setzen. Enzyme wirken als Katalysatoren - sie ermöglichen es, dass eine Reaktion schneller abläuft - und sie ermöglichen auch die Regulierung der Geschwindigkeit einer Stoffwechselreaktion, zum Beispiel als Reaktion auf Veränderungen in der Zellumgebung oder auf Signale von anderen Zellen. ⓘ
Das Stoffwechselsystem eines bestimmten Organismus bestimmt, welche Stoffe er als nahrhaft und welche als giftig empfindet. Einige Prokaryonten nutzen beispielsweise Schwefelwasserstoff als Nährstoff, doch ist dieses Gas für Tiere giftig. Der Grundumsatz eines Organismus ist das Maß für die Energiemenge, die durch all diese chemischen Reaktionen verbraucht wird. ⓘ
Ein auffälliges Merkmal des Stoffwechsels ist die Ähnlichkeit der grundlegenden Stoffwechselwege bei sehr unterschiedlichen Arten. So sind beispielsweise die Carbonsäuren, die als Zwischenprodukte des Zitronensäurezyklus am bekanntesten sind, in allen bekannten Organismen vorhanden, und zwar in so unterschiedlichen Arten wie dem einzelligen Bakterium Escherichia coli und riesigen mehrzelligen Organismen wie Elefanten. Diese Ähnlichkeiten in den Stoffwechselwegen sind wahrscheinlich auf ihr frühes Auftreten in der Evolutionsgeschichte zurückzuführen, und ihre Beibehaltung ist wahrscheinlich auf ihre Wirksamkeit zurückzuführen. Bei verschiedenen Krankheiten, wie Typ-II-Diabetes, metabolischem Syndrom und Krebs, ist der normale Stoffwechsel gestört. Der Stoffwechsel von Krebszellen unterscheidet sich ebenfalls vom Stoffwechsel normaler Zellen, und diese Unterschiede können genutzt werden, um Angriffspunkte für therapeutische Maßnahmen bei Krebs zu finden. ⓘ
Als Stoffwechsel oder Metabolismus (altgriechisch μεταβολισμός metabolismós, deutsch ‚Stoffwechsel‘, mit lateinischer Endung -us) bezeichnet man alle chemischen Umwandlungen von Stoffen im Körper von Lebewesen, beispielsweise die Umwandlung von Nahrungsmitteln in Zwischenprodukte (Metaboliten) und Endprodukte. Diese biochemischen Vorgänge dienen dem Aufbau, Abbau und Ersatz bzw. Erhalt der Körpersubstanz (Baustoffwechsel) sowie der Energiegewinnung für energieverbrauchende Aktivitäten (Energiestoffwechsel) und damit der Aufrechterhaltung der Körperfunktionen und somit des Lebens. Wesentlich für den Stoffwechsel sind Enzyme, die chemische Stoffumsetzungen beschleunigen und lenken (katalysieren). ⓘ
Werden von außen aufgenommene, fremde Stoffe umgesetzt, so spricht man auch von Fremdstoffmetabolismus. Der Umbau organismenfremder Stoffe in organismeneigene Stoffe wird Assimilation genannt. Das Gegenteil ist die Dissimilation (Abbau organismuseigener Stoffe). Zum Stoffwechsel gehört auch die Umwandlung schädlicher Stoffe in ausscheidbare Stoffe (Biotransformation). ⓘ
Stoffwechselvorgänge werden vor allem in der Biochemie erforscht. In der Medizin und Physiologie sind sie von großer Bedeutung (siehe auch Stoffwechselstörung). Sie können aber auch physikalisch gedeutet werden, als Austausch von freier Energie gegen Ordnung: Lebewesen erhöhen in sich die Ordnung und verbrauchen dabei Energie. Im Organismus nimmt die Entropie (Unordnung) ab, in der Umgebung nimmt sie zu. ⓘ
Biochemische Schlüsselstoffe
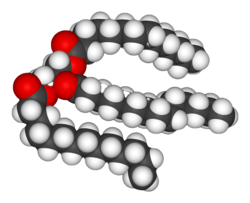
Die meisten Strukturen, aus denen Tiere, Pflanzen und Mikroben bestehen, sind aus vier grundlegenden Molekülklassen aufgebaut: Aminosäuren, Kohlenhydrate, Nukleinsäuren und Lipide (oft Fette genannt). Da diese Moleküle lebenswichtig sind, konzentrieren sich die Stoffwechselreaktionen entweder auf die Herstellung dieser Moleküle beim Aufbau von Zellen und Geweben oder auf ihren Abbau und ihre Verwendung zur Energiegewinnung durch ihre Verdauung. Diese biochemischen Stoffe können zu Polymeren wie DNA und Proteinen zusammengefügt werden, die zu den wichtigsten Makromolekülen des Lebens gehören. ⓘ
| Art des Moleküls | Name der Monomerformen | Bezeichnung der Polymerformen | Beispiele für polymere Formen ⓘ |
|---|---|---|---|
| Aminosäuren | Aminosäuren | Proteine (bestehend aus Polypeptiden) | Faserproteine und kugelförmige Proteine |
| Kohlenhydrate | Monosaccharide | Mehrfachzucker (Polysaccharide) | Stärke, Glykogen und Zellulose |
| Nukleinsäuren | Nukleotide | Polynukleotide | DNA und RNA |
Aminosäuren und Proteine
Proteine bestehen aus Aminosäuren, die in einer linearen Kette durch Peptidbindungen verbunden sind. Viele Proteine sind Enzyme, die die chemischen Reaktionen im Stoffwechsel katalysieren. Andere Proteine haben strukturelle oder mechanische Funktionen, wie z. B. diejenigen, die das Zytoskelett bilden, ein System von Gerüsten, das die Zellform aufrechterhält. Proteine spielen auch eine wichtige Rolle bei der Zellsignalisierung, bei Immunreaktionen, der Zelladhäsion, dem aktiven Transport durch Membranen und dem Zellzyklus. Aminosäuren tragen auch zum zellulären Energiestoffwechsel bei, indem sie eine Kohlenstoffquelle für den Eintritt in den Zitronensäurezyklus (Tricarbonsäurezyklus) bereitstellen, insbesondere wenn eine primäre Energiequelle wie Glukose knapp ist oder wenn Zellen metabolischem Stress ausgesetzt sind. ⓘ
Lipide
Lipide sind die vielfältigste Gruppe von Biochemikalien. Ihre wichtigsten strukturellen Verwendungszwecke sind Teil biologischer Membranen, sowohl interner als auch externer, wie z. B. der Zellmembran. Ihre chemische Energie kann ebenfalls genutzt werden. Lipide sind Polymere von Fettsäuren, die eine lange, unpolare Kohlenwasserstoffkette mit einem kleinen polaren Bereich mit Sauerstoff enthalten. Lipide werden in der Regel als hydrophobe oder amphipathische biologische Moleküle definiert, lösen sich jedoch in organischen Lösungsmitteln wie Ethanol, Benzol oder Chloroform. Die Fette sind eine große Gruppe von Verbindungen, die Fettsäuren und Glycerin enthalten; ein Glycerinmolekül, das durch Esterbindungen an drei Fettsäuren gebunden ist, wird als Triacylglycerid bezeichnet. Es gibt mehrere Variationen dieser Grundstruktur, darunter Rückgratstrukturen wie Sphingosin in Sphingomyelin und hydrophile Gruppen wie Phosphat in Phospholipiden. Steroide wie Sterol sind eine weitere wichtige Klasse von Lipiden. ⓘ
Kohlenhydrate

Kohlenhydrate sind Aldehyde oder Ketone, an die viele Hydroxylgruppen gebunden sind und die in geraden Ketten oder Ringen vorliegen können. Kohlenhydrate sind die am häufigsten vorkommenden biologischen Moleküle und erfüllen zahlreiche Aufgaben, z. B. die Speicherung und den Transport von Energie (Stärke, Glykogen) und strukturelle Komponenten (Zellulose in Pflanzen, Chitin in Tieren). Die grundlegenden Kohlenhydrateinheiten werden als Monosaccharide bezeichnet und umfassen Galaktose, Fruktose und vor allem Glukose. Monosaccharide können auf nahezu unbegrenzte Weise zu Polysacchariden verknüpft werden. ⓘ
Nukleotide
Die beiden Nukleinsäuren, DNA und RNA, sind Polymere aus Nukleotiden. Jedes Nukleotid besteht aus einem Phosphat, das an eine Ribose- oder Desoxyribose-Zuckergruppe gebunden ist, die wiederum an eine stickstoffhaltige Base gebunden ist. Nukleinsäuren sind von entscheidender Bedeutung für die Speicherung und Nutzung der genetischen Information und deren Interpretation durch die Prozesse der Transkription und der Proteinbiosynthese. Diese Informationen werden durch DNA-Reparaturmechanismen geschützt und durch DNA-Replikation weitergegeben. Viele Viren haben ein RNA-Genom, wie z. B. HIV, das mithilfe der reversen Transkription eine DNA-Vorlage aus seinem viralen RNA-Genom erstellt. RNA in Ribozymen wie Spleißosomen und Ribosomen ähnelt den Enzymen, da sie chemische Reaktionen katalysieren kann. Einzelne Nukleoside werden durch Anhängen einer Nukleobase an einen Ribosezucker hergestellt. Diese Basen sind heterozyklische Ringe mit Stickstoff, die als Purine oder Pyrimidine klassifiziert werden. Nukleotide fungieren auch als Coenzyme in Stoffwechselgruppen-Transferreaktionen. ⓘ
Coenzyme

Der Stoffwechsel umfasst eine Vielzahl chemischer Reaktionen, die meisten lassen sich jedoch einigen wenigen Grundtypen von Reaktionen zuordnen, bei denen funktionelle Gruppen von Atomen und deren Bindungen innerhalb von Molekülen übertragen werden. Diese gemeinsame Chemie ermöglicht es den Zellen, eine kleine Anzahl von Stoffwechselzwischenprodukten zu verwenden, um chemische Gruppen zwischen verschiedenen Reaktionen zu übertragen. Diese Gruppentransfer-Zwischenprodukte werden als Coenzyme bezeichnet. Jede Klasse von Gruppenübertragungsreaktionen wird von einem bestimmten Coenzym durchgeführt, das das Substrat für eine Reihe von Enzymen ist, die es herstellen, und für eine Reihe von Enzymen, die es verbrauchen. Diese Coenzyme werden also ständig hergestellt, verbraucht und wiederverwertet. ⓘ
Ein zentrales Coenzym ist Adenosintriphosphat (ATP), die universelle Energiewährung der Zellen. Dieses Nukleotid wird verwendet, um chemische Energie zwischen verschiedenen chemischen Reaktionen zu übertragen. In den Zellen ist nur eine geringe Menge ATP vorhanden, aber da es ständig regeneriert wird, kann der menschliche Körper pro Tag etwa sein eigenes Gewicht an ATP verbrauchen. ATP fungiert als Brücke zwischen Katabolismus und Anabolismus. Beim Katabolismus werden Moleküle abgebaut, beim Anabolismus werden sie wieder zusammengesetzt. Bei katabolen Reaktionen wird ATP erzeugt, bei anabolen Reaktionen wird es verbraucht. Es dient auch als Träger von Phosphatgruppen bei Phosphorylierungsreaktionen. ⓘ
Ein Vitamin ist eine organische Verbindung, die in kleinen Mengen benötigt wird und nicht in den Zellen hergestellt werden kann. In der menschlichen Ernährung fungieren die meisten Vitamine nach einer Modifikation als Coenzyme; so werden beispielsweise alle wasserlöslichen Vitamine phosphoryliert oder an Nukleotide gekoppelt, wenn sie in den Zellen verwendet werden. Nicotinamid-Adenin-Dinukleotid (NAD+), ein Derivat von Vitamin B3 (Niacin), ist ein wichtiges Coenzym, das als Wasserstoffakzeptor fungiert. Hunderte von verschiedenen Arten von Dehydrogenasen entziehen ihren Substraten Elektronen und reduzieren NAD+ zu NADH. Diese reduzierte Form des Coenzyms ist dann ein Substrat für alle Reduktasen in der Zelle, die Wasserstoffatome auf ihre Substrate übertragen müssen. Nicotinamid-Adenin-Dinukleotid kommt in der Zelle in zwei verwandten Formen vor: NADH und NADPH. Die Form NAD+/NADH ist wichtiger für katabole Reaktionen, während NADP+/NADPH für anabole Reaktionen verwendet wird. ⓘ
Mineralien und Cofaktoren
Anorganische Elemente spielen eine entscheidende Rolle im Stoffwechsel; einige sind reichlich vorhanden (z. B. Natrium und Kalium), während andere in sehr geringen Konzentrationen vorkommen. Etwa 99 % des Körpergewichts eines Menschen bestehen aus den Elementen Kohlenstoff, Stickstoff, Kalzium, Natrium, Chlor, Kalium, Wasserstoff, Phosphor, Sauerstoff und Schwefel. Organische Verbindungen (Proteine, Lipide und Kohlenhydrate) enthalten den größten Teil des Kohlenstoffs und Stickstoffs; der größte Teil des Sauerstoffs und Wasserstoffs liegt in Form von Wasser vor. ⓘ
Die reichlich vorhandenen anorganischen Elemente wirken als Elektrolyte. Die wichtigsten Ionen sind Natrium, Kalium, Calcium, Magnesium, Chlorid, Phosphat und das organische Ion Bicarbonat. Durch die Aufrechterhaltung eines präzisen Ionengradienten über die Zellmembranen werden der osmotische Druck und der pH-Wert aufrechterhalten. Ionen sind auch für die Funktion von Nerven und Muskeln von entscheidender Bedeutung, da Aktionspotenziale in diesen Geweben durch den Austausch von Elektrolyten zwischen der extrazellulären Flüssigkeit und der Zellflüssigkeit, dem Zytosol, erzeugt werden. Elektrolyte gelangen durch Proteine in der Zellmembran, die als Ionenkanäle bezeichnet werden, in die Zellen und verlassen sie wieder. So hängt beispielsweise die Muskelkontraktion von der Bewegung von Kalzium, Natrium und Kalium durch Ionenkanäle in der Zellmembran und den T-Tubuli ab. ⓘ
Übergangsmetalle sind in der Regel als Spurenelemente in Organismen vorhanden, wobei Zink und Eisen am häufigsten vorkommen. Metall-Cofaktoren sind fest an spezifische Stellen in Proteinen gebunden; obwohl Enzym-Cofaktoren während der Katalyse verändert werden können, kehren sie am Ende der katalysierten Reaktion immer in ihren ursprünglichen Zustand zurück. Metallische Mikronährstoffe werden von spezifischen Transportern in den Organismus aufgenommen und an Speicherproteine wie Ferritin oder Metallothionein gebunden, wenn sie nicht benötigt werden. ⓘ
Katabolismus
Katabolismus ist die Gesamtheit der Stoffwechselprozesse, die große Moleküle abbauen. Dazu gehören der Abbau und die Oxidation von Nahrungsmolekülen. Der Zweck der katabolen Reaktionen besteht darin, die Energie und die Komponenten bereitzustellen, die für die anabolen Reaktionen benötigt werden, bei denen Moleküle aufgebaut werden. Die genaue Art dieser katabolen Reaktionen unterscheidet sich von Organismus zu Organismus, und die Organismen können anhand ihrer Energie-, Wasserstoff- und Kohlenstoffquellen (ihrer primären Nährstoffgruppen) klassifiziert werden, wie in der folgenden Tabelle dargestellt. Organotrophe Organismen nutzen organische Moleküle als Quelle für Wasserstoffatome oder Elektronen, während lithotrophe Organismen anorganische Substrate nutzen. Während Phototrophe das Sonnenlicht in chemische Energie umwandeln, sind Chemotrophe auf Redoxreaktionen angewiesen, bei denen Elektronen von reduzierten Donatormolekülen wie organischen Molekülen, Wasserstoff, Schwefelwasserstoff oder Eisenionen auf Sauerstoff, Nitrat oder Sulfat übertragen werden. Bei Tieren sind an diesen Reaktionen komplexe organische Moleküle beteiligt, die zu einfacheren Molekülen wie Kohlendioxid und Wasser abgebaut werden. Photosynthetische Organismen, wie Pflanzen und Cyanobakterien, nutzen ähnliche Elektronenübertragungsreaktionen, um die vom Sonnenlicht aufgenommene Energie zu speichern. ⓘ
| Energiequelle | Sonnenlicht | Foto- | -troph | ||
| Vorgebildete Moleküle | chemo- | ||||
| Wasserstoff- oder Elektronendonator | organische Verbindung | organo- | |||
| anorganische Verbindung | litho- | ||||
| Kohlenstoffquelle | organische Verbindung | hetero- | |||
| anorganische Verbindung | auto- | ||||
Die am häufigsten vorkommenden katabolischen Reaktionen bei Tieren lassen sich in drei Hauptphasen unterteilen. In der ersten Phase werden große organische Moleküle wie Proteine, Polysaccharide oder Lipide außerhalb der Zellen in ihre kleineren Bestandteile zerlegt. Anschließend werden diese kleineren Moleküle von den Zellen aufgenommen und in kleinere Moleküle, in der Regel Acetyl-Coenzym A (Acetyl-CoA), umgewandelt, wodurch ein Teil der Energie freigesetzt wird. Schließlich wird die Acetylgruppe des CoA im Zitronensäurezyklus und in der Elektronentransportkette zu Wasser und Kohlendioxid oxidiert, wodurch weitere Energie freigesetzt wird, während das Coenzym Nicotinamid-Adenin-Dinukleotid (NAD+) zu NADH reduziert wird. ⓘ
Verdauung
Makromoleküle können von den Zellen nicht direkt verarbeitet werden. Makromoleküle müssen in kleinere Einheiten zerlegt werden, bevor sie im Zellstoffwechsel verwendet werden können. Um diese Polymere zu verdauen, werden verschiedene Enzymklassen eingesetzt. Zu diesen Verdauungsenzymen gehören Proteasen, die Proteine in Aminosäuren aufspalten, sowie Glykosidhydrolasen, die Polysaccharide in Einfachzucker, die so genannten Monosaccharide, aufspalten. ⓘ
Mikroben scheiden Verdauungsenzyme einfach in ihre Umgebung aus, während Tiere diese Enzyme nur von spezialisierten Zellen in ihren Eingeweiden, einschließlich des Magens und der Bauchspeicheldrüse, und in Speicheldrüsen absondern. Die von diesen extrazellulären Enzymen freigesetzten Aminosäuren oder Zucker werden dann durch aktive Transportproteine in die Zellen gepumpt. ⓘ
Energie aus organischen Verbindungen
Der Kohlenhydratabbau ist die Zerlegung von Kohlenhydraten in kleinere Einheiten. Kohlenhydrate werden normalerweise in die Zellen aufgenommen, nachdem sie in Monosaccharide aufgespalten wurden. Dort werden sie hauptsächlich durch die Glykolyse abgebaut, bei der Zucker wie Glukose und Fruktose in Pyruvat umgewandelt und etwas ATP erzeugt wird. Pyruvat ist ein Zwischenprodukt in mehreren Stoffwechselwegen, aber der größte Teil wird durch aerobe (mit Sauerstoff) Glykolyse in Acetyl-CoA umgewandelt und dem Zitronensäurezyklus zugeführt. Obwohl im Zitronensäurezyklus etwas mehr ATP erzeugt wird, ist das wichtigste Produkt NADH, das bei der Oxidation von Acetyl-CoA aus NAD+ gebildet wird. Bei dieser Oxidation wird Kohlendioxid als Abfallprodukt freigesetzt. Unter anaeroben Bedingungen entsteht bei der Glykolyse Laktat, wobei das Enzym Laktatdehydrogenase NADH zu NAD+ reoxidiert, um es erneut in der Glykolyse zu verwenden. Ein alternativer Weg für den Glukoseabbau ist der Pentosephosphatweg, bei dem das Coenzym NADPH reduziert wird und Pentosezucker wie Ribose, die Zuckerkomponente der Nukleinsäuren, entsteht. ⓘ
Fette werden durch Hydrolyse zu freien Fettsäuren und Glycerin abgebaut. Das Glycerin geht in die Glykolyse ein, und die Fettsäuren werden durch Beta-Oxidation abgebaut, um Acetyl-CoA freizusetzen, das dann dem Zitronensäurezyklus zugeführt wird. Fettsäuren setzen bei der Oxidation mehr Energie frei als Kohlenhydrate. Auch Steroide werden von einigen Bakterien in einem der Beta-Oxidation ähnlichen Prozess abgebaut, und bei diesem Abbauprozess werden erhebliche Mengen an Acetyl-CoA, Propionyl-CoA und Pyruvat freigesetzt, die alle von der Zelle zur Energiegewinnung genutzt werden können. M. tuberculosis kann auch auf dem Lipid Cholesterin als einziger Kohlenstoffquelle wachsen, und Gene, die am Cholesterin-Verwertungsweg beteiligt sind, wurden als wichtig für verschiedene Stadien des Infektionslebenszyklus von M. tuberculosis bestätigt. ⓘ
Aminosäuren werden entweder zur Synthese von Proteinen und anderen Biomolekülen verwendet oder zur Energiegewinnung zu Harnstoff und Kohlendioxid oxidiert. Der Oxidationsweg beginnt mit der Entfernung der Aminogruppe durch eine Transaminase. Die Aminogruppe wird dem Harnstoffzyklus zugeführt, wobei ein desaminiertes Kohlenstoffgerüst in Form einer Ketosäure zurückbleibt. Mehrere dieser Ketosäuren sind Zwischenprodukte im Zitronensäurezyklus, zum Beispiel α-Ketoglutarat, das durch Desaminierung von Glutamat entsteht. Die glucogenen Aminosäuren können auch durch Gluconeogenese in Glucose umgewandelt werden (siehe unten). ⓘ
Energieumwandlungen
Oxidative Phosphorylierung

Grün: Membranständige Oxidoreduktase (links) und ATP-Synthase (rechts). Zurückströmende Kationen versetzen den unteren Teil der ATP-Synthase in Rotation. Aus dort aufgenommenem Phosphat und ADP wird Wasser „herausgequetscht“. Am Stator, der in der Membran verankert ist, wird das fertige ATP freigesetzt.
Rot: Ionentransport durch Membran-Enzyme. Eine Oxidoreduktase (links) pumpt H+-Ionen von innen durch die Membran nach außen und verstärkt die elektrische Ladung der Membran und den Protonengradienten.
Blau: Elektronentransfer. Die Energie für die Oxidoreduktasen stammt aus einem Elektronenfluss von e−-Donoren (wie z. B. Zuckern) zu einem e−-Akzeptor (vermittelt über Coenzyme wie NADH), die als e−-Überträger fungieren. ⓘ
Zell- und Biomembranen sind keineswegs nur „Beutel“, in denen sich Enzyme und ihre Reaktionspartner frei bewegen können. Vielmehr bilden sie für geladene Moleküle (Ionen) eine undurchdringliche Barriere. In den Membranen finden sich allerdings Membranproteine, die selektiv Ionen durch die Membran durchlassen oder sogar aktiv transportieren. Letztere sorgen durch den Export von Kationen dafür, dass die Membranen außen positiv und innen negativ elektrisch geladen sind (Membranpotential). In dieser Ladung steckt Energie. Sie wird für eine Reihe von Transport- und Bewegungsprozessen frei, wenn die Kationen zurück fließen. ⓘ
So fließt durch die Membranen praktisch aller lebenden Zellen ständig ein Strom von positiv geladenen Teilchen. ⓘ
Angetrieben wird dieser Strom durch exergone chemische Reaktionen. So verbrauchen Nervenzellen kontinuierlich ATP, um ihr Membranpotential aufrechtzuerhalten. Das geschieht dort durch ATPasen, die als Natrium-Kalium-Pumpen fungieren. ⓘ
Die Regenerierung von verbrauchtem ATP basiert bei nahezu allen Lebewesen fast ausschließlich auf der Nutzung des Membranpotentials durch das Enzym ATP-Synthase (Abb.). In dafür spezialisierten Organellen (den Mitochondrien) von Tieren und Pflanzen sowie in nahezu allen Archaeen und Bakterien fungieren Oxidoreduktasen als Kationen-Pumpen, die das Membranpotential aufrechterhalten. Beim Menschen sind das die Enzyme der Atmungskette. Pflanzen verwenden dafür auch ihren Photosynthese-Apparat in den Chloroplasten. ⓘ
Bei der oxidativen Phosphorylierung werden die Elektronen, die organischen Molekülen in Bereichen wie dem Zitronensäurezyklus entzogen werden, auf Sauerstoff übertragen, und die freigesetzte Energie wird zur Herstellung von ATP verwendet. Bei Eukaryonten geschieht dies durch eine Reihe von Proteinen in den Membranen der Mitochondrien, die so genannte Elektronentransportkette. Bei Prokaryonten befinden sich diese Proteine in der inneren Membran der Zelle. Diese Proteine nutzen die Energie aus reduzierten Molekülen wie NADH, um Protonen durch die Membran zu pumpen. ⓘ

Wenn Protonen aus den Mitochondrien herausgepumpt werden, entsteht ein Unterschied in der Protonenkonzentration an der Membran und ein elektrochemischer Gradient. Diese Kraft treibt Protonen über die Basis eines Enzyms namens ATP-Synthase zurück in das Mitochondrium. Durch den Protonenstrom wird die Stiel-Untereinheit in Rotation versetzt, wodurch die aktive Stelle der Synthase-Domäne ihre Form ändert und Adenosindiphosphat phosphoryliert und in ATP umgewandelt wird. ⓘ
Energie aus anorganischen Verbindungen
Chemolithotrophie ist eine Art des Stoffwechsels bei Prokaryonten, bei der die Energie aus der Oxidation anorganischer Verbindungen gewonnen wird. Diese Organismen können Wasserstoff, reduzierte Schwefelverbindungen (wie Sulfid, Schwefelwasserstoff und Thiosulfat), Eisen (Fe(II)) oder Ammoniak als Quellen für Reduktionskraft nutzen und gewinnen Energie aus der Oxidation dieser Verbindungen. Diese mikrobiellen Prozesse sind wichtig für globale biogeochemische Kreisläufe wie Acetogenese, Nitrifikation und Denitrifikation und sind entscheidend für die Bodenfruchtbarkeit. ⓘ
Energie aus Licht
Die Energie des Sonnenlichts wird von Pflanzen, Cyanobakterien, Purpurbakterien, grünen Schwefelbakterien und einigen Protisten aufgefangen. Dieser Prozess ist häufig mit der Umwandlung von Kohlendioxid in organische Verbindungen im Rahmen der Photosynthese gekoppelt, die weiter unten behandelt wird. Bei Prokaryonten können die Systeme der Energiegewinnung und der Kohlenstofffixierung jedoch auch getrennt voneinander ablaufen, da Purpurbakterien und grüne Schwefelbakterien das Sonnenlicht als Energiequelle nutzen und dabei zwischen Kohlenstofffixierung und Fermentation organischer Verbindungen wechseln können. ⓘ
In vielen Organismen ähnelt die Nutzung der Sonnenenergie im Prinzip der oxidativen Phosphorylierung, da die Energie in Form eines Protonenkonzentrationsgradienten gespeichert wird. Die Elektronen, die zum Antrieb dieser Elektronentransportkette benötigt werden, stammen von Proteinen, die Licht sammeln und als photosynthetische Reaktionszentren bezeichnet werden. Die Reaktionszentren werden je nach Art der vorhandenen photosynthetischen Pigmente in zwei Typen eingeteilt, wobei die meisten photosynthetischen Bakterien nur einen Typ haben, während Pflanzen und Cyanobakterien zwei Typen besitzen. ⓘ
In Pflanzen, Algen und Cyanobakterien nutzt das Photosystem II die Lichtenergie, um dem Wasser Elektronen zu entziehen, wobei Sauerstoff als Abfallprodukt freigesetzt wird. Die Elektronen fließen dann zum Cytochrom b6f-Komplex, der ihre Energie nutzt, um Protonen durch die Thylakoidmembran im Chloroplasten zu pumpen. Diese Protonen bewegen sich durch die Membran zurück und treiben wie zuvor die ATP-Synthase an. Die Elektronen fließen dann durch das Photosystem I und können zur Reduktion des Coenzyms NADP+ verwendet werden. Dieses Coenzym kann in den Calvin-Zyklus eintreten, der weiter unten behandelt wird, oder zur weiteren ATP-Erzeugung recycelt werden. ⓘ
Anabolismus
Der Anabolismus ist die Gesamtheit der konstruktiven Stoffwechselprozesse, bei denen die durch den Katabolismus freigesetzte Energie zur Synthese komplexer Moleküle verwendet wird. Im Allgemeinen werden die komplexen Moleküle, aus denen die zellulären Strukturen bestehen, Schritt für Schritt aus kleineren und einfacheren Vorläufern aufgebaut. Der Anabolismus umfasst drei grundlegende Phasen. Erstens die Herstellung von Vorläufersubstanzen wie Aminosäuren, Monosacchariden, Isoprenoiden und Nukleotiden, zweitens ihre Aktivierung in reaktive Formen unter Verwendung von ATP-Energie und drittens der Zusammenbau dieser Vorläufersubstanzen zu komplexen Molekülen wie Proteinen, Polysacchariden, Lipiden und Nukleinsäuren. ⓘ
Der Anabolismus in Organismen kann je nach der Quelle der aufgebauten Moleküle in ihren Zellen unterschiedlich sein. Autotrophe Organismen wie Pflanzen können die komplexen organischen Moleküle in ihren Zellen, wie Polysaccharide und Proteine, aus einfachen Molekülen wie Kohlendioxid und Wasser aufbauen. Heterotrophe Organismen hingegen benötigen eine Quelle für komplexere Stoffe wie Monosaccharide und Aminosäuren, um diese komplexen Moleküle herzustellen. Die Organismen können weiter nach der endgültigen Energiequelle eingeteilt werden: Photoautotrophe und Photoheterotrophe gewinnen Energie aus Licht, während Chemoautotrophe und Chemoheterotrophe Energie aus Oxidationsreaktionen gewinnen. ⓘ
Kohlenstofffixierung

Unter Photosynthese versteht man die Synthese von Kohlenhydraten aus Sonnenlicht und Kohlendioxid (CO2). In Pflanzen, Cyanobakterien und Algen spaltet die sauerstoffhaltige Photosynthese Wasser auf, wobei Sauerstoff als Abfallprodukt entsteht. Bei diesem Prozess werden das von den photosynthetischen Reaktionszentren erzeugte ATP und NADPH, wie oben beschrieben, verwendet, um CO2 in Glycerat-3-Phosphat umzuwandeln, das dann in Glukose umgewandelt werden kann. Diese Kohlenstoff-Fixierungsreaktion wird durch das Enzym RuBisCO im Rahmen des Calvin-Benson-Zyklus durchgeführt. In Pflanzen gibt es drei Arten der Photosynthese: C3-Kohlenstofffixierung, C4-Kohlenstofffixierung und CAM-Photosynthese. Diese unterscheiden sich durch den Weg, den das Kohlendioxid zum Calvin-Zyklus nimmt, wobei C3-Pflanzen das CO2 direkt fixieren, während C4- und CAM-Photosynthese das CO2 zuerst in andere Verbindungen einbauen, um mit intensivem Sonnenlicht und trockenen Bedingungen fertig zu werden. ⓘ
Bei den photosynthetischen Prokaryonten sind die Mechanismen der Kohlenstofffixierung vielfältiger. Hier kann das Kohlendioxid durch den Calvin-Benson-Zyklus, einen umgekehrten Zitronensäurezyklus oder die Carboxylierung von Acetyl-CoA gebunden werden. Prokaryotische Chemoautotrophe fixieren CO2 ebenfalls über den Calvin-Benson-Zyklus, verwenden aber Energie aus anorganischen Verbindungen, um die Reaktion anzutreiben. ⓘ
Kohlenhydrate und Glykane
Im Kohlenhydratanabolismus können einfache organische Säuren in Monosaccharide wie Glukose umgewandelt und dann zum Aufbau von Polysacchariden wie Stärke verwendet werden. Die Erzeugung von Glukose aus Verbindungen wie Pyruvat, Laktat, Glycerin, Glycerat-3-Phosphat und Aminosäuren wird als Gluconeogenese bezeichnet. Bei der Gluconeogenese wird Pyruvat über eine Reihe von Zwischenstufen, von denen viele mit der Glykolyse gemeinsam sind, in Glucose-6-phosphat umgewandelt. Allerdings handelt es sich bei diesem Stoffwechselweg nicht einfach um eine umgekehrte Glykolyse, da mehrere Schritte von nicht-glykolytischen Enzymen katalysiert werden. Dies ist wichtig, da so die Bildung und der Abbau von Glukose getrennt geregelt werden können und verhindert wird, dass beide Wege gleichzeitig in einem sinnlosen Zyklus ablaufen. ⓘ
Fett ist zwar eine gängige Art der Energiespeicherung, aber bei Wirbeltieren wie dem Menschen können die Fettsäuren in diesen Speichern nicht durch Gluconeogenese in Glukose umgewandelt werden, da diese Organismen Acetyl-CoA nicht in Pyruvat umwandeln können; Pflanzen können dies, aber Tiere verfügen nicht über den erforderlichen enzymatischen Mechanismus. Daher müssen Wirbeltiere nach längerem Hungertod Ketonkörper aus Fettsäuren herstellen, um Glukose in Geweben wie dem Gehirn zu ersetzen, die keine Fettsäuren verstoffwechseln können. In anderen Organismen wie Pflanzen und Bakterien wird dieses Stoffwechselproblem durch den Glyoxylatzyklus gelöst, der den Decarboxylierungsschritt im Zitronensäurezyklus umgeht und die Umwandlung von Acetyl-CoA in Oxalacetat ermöglicht, wo es zur Herstellung von Glukose verwendet werden kann. Mit Ausnahme von Fett wird Glukose in den meisten Geweben als Energieressource gespeichert, die im Gewebe durch Glykogenese zur Verfügung steht und normalerweise zur Aufrechterhaltung des Glukosespiegels im Blut verwendet wird. ⓘ
Polysaccharide und Glykane werden durch die sequentielle Addition von Monosacchariden durch Glykosyltransferase von einem reaktiven Zucker-Phosphat-Donor wie Uridindiphosphat-Glukose (UDP-Glc) an eine Akzeptor-Hydroxylgruppe auf dem wachsenden Polysaccharid hergestellt. Da jede der Hydroxylgruppen am Ring des Substrats ein Akzeptor sein kann, können die hergestellten Polysaccharide gerade oder verzweigte Strukturen aufweisen. Die gebildeten Polysaccharide können selbst strukturelle oder metabolische Funktionen haben oder durch Oligosaccharyltransferasen genannte Enzyme auf Lipide und Proteine übertragen werden. ⓘ
Fettsäuren, Isoprenoide und Sterol

Fettsäuren werden durch Fettsäuresynthasen hergestellt, die Acetyl-CoA-Einheiten polymerisieren und dann reduzieren. Die Acylketten in den Fettsäuren werden durch einen Zyklus von Reaktionen verlängert, bei denen die Acylgruppe hinzugefügt, zu einem Alkohol reduziert, zu einer Alkengruppe dehydriert und dann wieder zu einer Alkangruppe reduziert wird. Die Enzyme der Fettsäurebiosynthese werden in zwei Gruppen eingeteilt: Bei Tieren und Pilzen werden alle diese Fettsäuresynthasereaktionen von einem einzigen multifunktionellen Typ-I-Protein durchgeführt, während in Pflanzenplastiden und Bakterien getrennte Typ-II-Enzyme jeden Schritt des Weges ausführen. ⓘ
Terpene und Isoprenoide sind eine große Klasse von Lipiden, zu denen auch die Carotinoide gehören, und bilden die größte Klasse pflanzlicher Naturprodukte. Diese Verbindungen werden durch den Zusammenbau und die Modifizierung von Isopreneinheiten hergestellt, die aus den reaktiven Vorläufern Isopentenylpyrophosphat und Dimethylallylpyrophosphat stammen. Diese Vorstufen können auf unterschiedliche Weise hergestellt werden. In Tieren und Archaeen werden diese Verbindungen über den Mevalonatweg aus Acetyl-CoA hergestellt, während in Pflanzen und Bakterien der Nicht-Mevalonatweg Pyruvat und Glyceraldehyd-3-Phosphat als Substrate verwendet. Eine wichtige Reaktion, bei der diese aktivierten Isopren-Donatoren verwendet werden, ist die Sterol-Biosynthese. Hier werden die Isopren-Einheiten zu Squalen verbunden und dann zu einer Reihe von Ringen gefaltet und geformt, um Lanosterin zu bilden. Lanosterin kann dann in andere Sterine wie Cholesterin und Ergosterin umgewandelt werden. ⓘ
Proteine
Organismen sind unterschiedlich gut in der Lage, die 20 häufigsten Aminosäuren zu synthetisieren. Die meisten Bakterien und Pflanzen können alle zwanzig synthetisieren, aber Säugetiere können nur elf nicht-essentielle Aminosäuren synthetisieren, so dass neun essentielle Aminosäuren mit der Nahrung aufgenommen werden müssen. Einige einfache Parasiten, wie z. B. das Bakterium Mycoplasma pneumoniae, können keine Aminosäuren synthetisieren und nehmen ihre Aminosäuren direkt von ihren Wirten auf. Alle Aminosäuren werden aus Zwischenprodukten der Glykolyse, des Zitronensäurezyklus oder des Pentosephosphatweges synthetisiert. Der Stickstoff wird durch Glutamat und Glutamin bereitgestellt. Die Synthese von nicht essentiellen Aminosäuren hängt von der Bildung der entsprechenden Alpha-Ketosäure ab, die dann zur Bildung einer Aminosäure transaminiert wird. ⓘ
Aminosäuren werden zu Proteinen aufgebaut, indem sie zu einer Kette von Peptidbindungen verbunden werden. Jedes unterschiedliche Protein hat eine einzigartige Abfolge von Aminosäureresten: Dies ist seine Primärstruktur. So wie sich die Buchstaben des Alphabets zu einer schier unendlichen Vielfalt von Wörtern zusammensetzen lassen, können Aminosäuren in unterschiedlicher Reihenfolge miteinander verbunden werden, um eine riesige Vielfalt von Proteinen zu bilden. Proteine werden aus Aminosäuren hergestellt, die durch Anhängen an ein Transfer-RNA-Molekül über eine Esterbindung aktiviert wurden. Dieser Aminoacyl-tRNA-Vorläufer wird in einer ATP-abhängigen Reaktion hergestellt, die von einer Aminoacyl-tRNA-Synthetase durchgeführt wird. Diese Aminoacyl-tRNA ist dann ein Substrat für das Ribosom, das die Aminosäure unter Verwendung der Sequenzinformation in einer Boten-RNA an die sich verlängernde Proteinkette anfügt. ⓘ
Nukleotid-Synthese und -Rückgewinnung
Nukleotide werden aus Aminosäuren, Kohlendioxid und Ameisensäure auf Wegen hergestellt, die große Mengen an metabolischer Energie erfordern. Folglich verfügen die meisten Organismen über effiziente Systeme zur Rückgewinnung von vorgebildeten Nukleotiden. Purine werden als Nukleoside synthetisiert (an Ribose gebundene Basen). Sowohl Adenin als auch Guanin werden aus dem Vorläufernukleosid Inosinmonophosphat hergestellt, das mit Hilfe von Atomen aus den Aminosäuren Glycin, Glutamin und Asparaginsäure sowie Formiat aus dem Coenzym Tetrahydrofolat synthetisiert wird. Die Pyrimidine hingegen werden aus der Base Orotat synthetisiert, die aus Glutamin und Aspartat gebildet wird. ⓘ
Xenobiotika und Redox-Stoffwechsel
Alle Organismen sind ständig Verbindungen ausgesetzt, die sie nicht als Nahrung verwenden können und die schädlich wären, wenn sie sich in den Zellen anreichern würden, da sie keine metabolische Funktion haben. Diese potenziell schädlichen Verbindungen werden als Xenobiotika bezeichnet. Xenobiotika wie synthetische Drogen, natürliche Gifte und Antibiotika werden durch eine Reihe von Enzymen entgiftet, die Xenobiotika verstoffwechseln. Beim Menschen gehören dazu Cytochrom-P450-Oxidasen, UDP-Glucuronosyltransferasen und Glutathion-S-Transferasen. Dieses System von Enzymen wirkt in drei Stufen, um zunächst das Xenobiotikum zu oxidieren (Phase I) und dann wasserlösliche Gruppen an das Molekül zu konjugieren (Phase II). Das veränderte wasserlösliche Xenobiotikum kann dann aus den Zellen herausgepumpt werden und in mehrzelligen Organismen weiter verstoffwechselt werden, bevor es ausgeschieden wird (Phase III). In der Ökologie sind diese Reaktionen besonders wichtig für den mikrobiellen biologischen Abbau von Schadstoffen und die Bioremediation von kontaminierten Böden und Ölverschmutzungen. Viele dieser mikrobiellen Reaktionen laufen auch bei mehrzelligen Organismen ab, aber aufgrund der unglaublichen Vielfalt an Mikrobenarten sind diese Organismen in der Lage, ein weitaus breiteres Spektrum an Xenobiotika zu bewältigen als mehrzellige Organismen und können sogar persistente organische Schadstoffe wie Organochloridverbindungen abbauen. ⓘ
Ein verwandtes Problem für aerobe Organismen ist der oxidative Stress. Bei Prozessen wie der oxidativen Phosphorylierung und der Bildung von Disulfidbindungen während der Proteinfaltung entstehen reaktive Sauerstoffspezies wie Wasserstoffperoxid. Diese schädlichen Oxidantien werden durch antioxidative Stoffwechselprodukte wie Glutathion und Enzyme wie Katalasen und Peroxidasen entfernt. ⓘ
Thermodynamik von lebenden Organismen
Lebende Organismen müssen den Gesetzen der Thermodynamik gehorchen, die die Übertragung von Wärme und Arbeit beschreiben. Der zweite Hauptsatz der Thermodynamik besagt, dass in jedem isolierten System die Entropie (Unordnung) nicht abnehmen kann. Obwohl die erstaunliche Komplexität der lebenden Organismen diesem Gesetz zu widersprechen scheint, ist Leben möglich, da alle Organismen offene Systeme sind, die Materie und Energie mit ihrer Umgebung austauschen. Lebende Systeme befinden sich nicht im Gleichgewicht, sondern sind dissipative Systeme, die ihren Zustand hoher Komplexität dadurch aufrechterhalten, dass sie einen größeren Anstieg der Entropie in ihrer Umgebung verursachen. Der Stoffwechsel einer Zelle erreicht dies, indem er die spontanen Prozesse des Katabolismus mit den nicht-spontanen Prozessen des Anabolismus koppelt. Thermodynamisch ausgedrückt, erhält der Stoffwechsel die Ordnung aufrecht, indem er Unordnung schafft. ⓘ
Regulierung und Kontrolle
Da sich die Umwelt der meisten Organismen ständig verändert, müssen die Stoffwechselreaktionen genau reguliert werden, um konstante Bedingungen in den Zellen aufrechtzuerhalten, ein Zustand, der als Homöostase bezeichnet wird. Die Regulierung des Stoffwechsels ermöglicht es den Organismen auch, auf Signale zu reagieren und aktiv mit ihrer Umwelt zu interagieren. Zwei eng miteinander verbundene Konzepte sind wichtig, um zu verstehen, wie Stoffwechselwege gesteuert werden. Erstens: Die Regulierung eines Enzyms in einem Stoffwechselweg ist die Art und Weise, wie seine Aktivität als Reaktion auf Signale erhöht oder verringert wird. Zweitens ist die von diesem Enzym ausgeübte Kontrolle die Auswirkung, die diese Veränderungen in seiner Aktivität auf die Gesamtrate des Stoffwechselwegs (den Fluss durch den Stoffwechselweg) haben. Ein Enzym kann zum Beispiel große Aktivitätsänderungen aufweisen (d. h. es ist stark reguliert), aber wenn diese Änderungen nur geringe Auswirkungen auf den Fluss eines Stoffwechselwegs haben, dann ist dieses Enzym nicht an der Kontrolle des Weges beteiligt. ⓘ

Es gibt mehrere Ebenen der Stoffwechselregulation. Bei der intrinsischen Regulation reguliert sich der Stoffwechselweg selbst, um auf Veränderungen der Substrat- oder Produktmengen zu reagieren; so kann beispielsweise eine Verringerung der Produktmenge den Fluss durch den Weg erhöhen, um dies auszugleichen. Diese Art der Regulierung beinhaltet häufig eine allosterische Regulierung der Aktivitäten mehrerer Enzyme in dem Stoffwechselweg. Bei der extrinsischen Kontrolle ändert eine Zelle in einem mehrzelligen Organismus ihren Stoffwechsel als Reaktion auf Signale von anderen Zellen. Diese Signale liegen in der Regel in Form von wasserlöslichen Botenstoffen wie Hormonen und Wachstumsfaktoren vor und werden von spezifischen Rezeptoren auf der Zelloberfläche erkannt. Diese Signale werden dann im Inneren der Zelle durch Second-Messenger-Systeme weitergeleitet, an denen häufig die Phosphorylierung von Proteinen beteiligt ist. ⓘ
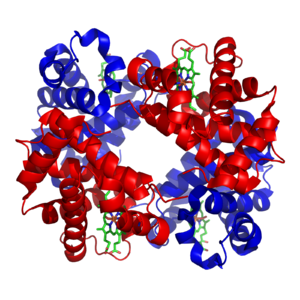
Ein sehr gut verstandenes Beispiel für die extrinsische Kontrolle ist die Regulierung des Glukosestoffwechsels durch das Hormon Insulin. Insulin wird als Reaktion auf einen Anstieg des Blutzuckerspiegels produziert. Die Bindung des Hormons an Insulinrezeptoren auf den Zellen aktiviert dann eine Kaskade von Proteinkinasen, die die Zellen veranlassen, Glukose aufzunehmen und in Speichermoleküle wie Fettsäuren und Glykogen umzuwandeln. Der Stoffwechsel des Glykogens wird durch die Aktivität der Phosphorylase, dem Enzym, das Glykogen abbaut, und der Glykogensynthase, dem Enzym, das es herstellt, gesteuert. Diese Enzyme werden auf gegenseitige Weise reguliert, wobei die Phosphorylierung die Glykogensynthase hemmt, die Phosphorylase jedoch aktiviert. Insulin bewirkt die Glykogensynthese, indem es die Proteinphosphatasen aktiviert und eine Abnahme der Phosphorylierung dieser Enzyme bewirkt. ⓘ
Entwicklung

Die oben beschriebenen zentralen Stoffwechselwege, wie die Glykolyse und der Zitronensäurezyklus, sind in allen drei Bereichen der Lebewesen zu finden und waren auch beim letzten gemeinsamen Vorfahren vorhanden. Diese universelle Vorläuferzelle war prokaryotisch und wahrscheinlich ein Methanogen, das über einen umfangreichen Aminosäure-, Nukleotid-, Kohlenhydrat- und Lipidstoffwechsel verfügte. Die Beibehaltung dieser alten Stoffwechselwege im Laufe der späteren Evolution könnte darauf zurückzuführen sein, dass diese Reaktionen eine optimale Lösung für die jeweiligen Stoffwechselprobleme darstellten, wobei Stoffwechselwege wie die Glykolyse und der Zitronensäurezyklus ihre Endprodukte hocheffizient und in einer minimalen Anzahl von Schritten erzeugen. Die ersten Wege des enzymbasierten Stoffwechsels waren möglicherweise Teil des Purinnukleotid-Stoffwechsels, während frühere Stoffwechselwege Teil der alten RNA-Welt waren. ⓘ
Es wurden viele Modelle vorgeschlagen, um die Mechanismen zu beschreiben, durch die sich neue Stoffwechselwege entwickeln. Dazu gehören die sequentielle Hinzufügung neuer Enzyme zu einem kurzen Vorläuferstoffwechselweg, die Verdopplung und anschließende Divergenz ganzer Stoffwechselwege sowie die Rekrutierung bereits vorhandener Enzyme und deren Zusammenführung zu einem neuen Reaktionsweg. Die relative Bedeutung dieser Mechanismen ist unklar, aber genomische Studien haben gezeigt, dass die Enzyme in einem Stoffwechselweg wahrscheinlich einen gemeinsamen Vorfahren haben, was darauf hindeutet, dass sich viele Stoffwechselwege schrittweise entwickelt haben, wobei neue Funktionen aus bereits bestehenden Schritten in dem Stoffwechselweg entstanden sind. Ein alternatives Modell ergibt sich aus Studien, die die Entwicklung von Proteinstrukturen in Stoffwechselnetzwerken nachverfolgen. Dies legt nahe, dass Enzyme durchgängig rekrutiert werden, wobei Enzyme ausgeliehen werden, um ähnliche Funktionen in verschiedenen Stoffwechselwegen zu erfüllen (wie in der MANET-Datenbank ersichtlich). Eine dritte Möglichkeit ist, dass einige Teile des Stoffwechsels als "Module" existieren, die in verschiedenen Stoffwechselwegen wiederverwendet werden können und ähnliche Funktionen an verschiedenen Molekülen erfüllen. ⓘ
Neben der Entwicklung neuer Stoffwechselwege kann die Evolution auch den Verlust von Stoffwechselfunktionen bewirken. So gehen beispielsweise bei einigen Parasiten Stoffwechselprozesse verloren, die nicht überlebenswichtig sind, und vorgebildete Aminosäuren, Nukleotide und Kohlenhydrate können stattdessen vom Wirt abgefangen werden. Ähnliche reduzierte Stoffwechselfähigkeiten sind bei endosymbiotischen Organismen zu beobachten. ⓘ
Der Stoffwechsel ist ein komplexes Netzwerk von einzelnen Reaktionen. Gruppen von Reaktionen, die unmittelbar aufeinander folgen, werden Stoffwechselwege genannt. Diese können linear (z. B. Glycolyse) oder zyklisch (z. B. Citratzyklus) sein. ⓘ
Die meisten Stoffwechselwege sind amphibol, das heißt, sie laufen in verschiedenen Schritten katabol und anabol ab. Auch wenn viele Einzelschritte reversibel sind, ist der ganze Stoffwechselweg immer irreversibel, da mindestens ein Reaktionsschritt nur in anabole oder katabole Richtung verläuft. ⓘ
Untersuchung und Manipulation

Klassischerweise wird der Stoffwechsel mit einem reduktionistischen Ansatz untersucht, der sich auf einen einzigen Stoffwechselweg konzentriert. Besonders wertvoll ist der Einsatz radioaktiver Tracer auf der Ebene des gesamten Organismus, des Gewebes und der Zellen, mit denen die Wege von den Vorstufen zu den Endprodukten durch die Identifizierung radioaktiv markierter Zwischen- und Endprodukte definiert werden. Die Enzyme, die diese chemischen Reaktionen katalysieren, können dann gereinigt und ihre Kinetik und Reaktionen auf Hemmstoffe untersucht werden. Ein paralleler Ansatz besteht darin, die kleinen Moleküle in einer Zelle oder einem Gewebe zu identifizieren; der vollständige Satz dieser Moleküle wird als Metabolom bezeichnet. Insgesamt geben diese Studien einen guten Überblick über die Struktur und Funktion einfacher Stoffwechselwege, sind aber unzureichend, wenn sie auf komplexere Systeme wie den Stoffwechsel einer ganzen Zelle angewendet werden. ⓘ
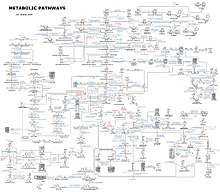
Eine Vorstellung von der Komplexität der Stoffwechselnetzwerke in Zellen, die Tausende verschiedener Enzyme enthalten, vermittelt die Abbildung rechts, die die Interaktionen zwischen nur 43 Proteinen und 40 Metaboliten zeigt: Die Sequenzen der Genome liefern Listen mit bis zu 26.500 Genen. Heute ist es jedoch möglich, diese genomischen Daten zu nutzen, um komplette Netzwerke biochemischer Reaktionen zu rekonstruieren und ganzheitlichere mathematische Modelle zu erstellen, die deren Verhalten erklären und vorhersagen können. Diese Modelle sind besonders leistungsfähig, wenn sie die mit klassischen Methoden gewonnenen Daten über Stoffwechselwege und Metaboliten mit Daten über die Genexpression aus Proteom- und DNA-Mikroarray-Studien kombinieren. Mit Hilfe dieser Techniken wurde nun ein Modell des menschlichen Stoffwechsels erstellt, das für die künftige Arzneimittelentdeckung und die biochemische Forschung von Nutzen sein wird. Diese Modelle werden nun in der Netzwerkanalyse verwendet, um menschliche Krankheiten in Gruppen zu klassifizieren, die gemeinsame Proteine oder Metaboliten aufweisen. ⓘ
Bakterielle Stoffwechselnetzwerke sind ein eindrucksvolles Beispiel für eine "bow-tie"-Organisation, eine Architektur, die in der Lage ist, eine breite Palette von Nährstoffen aufzunehmen und eine große Vielfalt von Produkten und komplexen Makromolekülen unter Verwendung relativ weniger gemeinsamer Zwischenwährungen zu produzieren. ⓘ
Eine wichtige technologische Anwendung dieser Informationen ist das Metabolic Engineering. Dabei werden Organismen wie Hefe, Pflanzen oder Bakterien gentechnisch verändert, um sie für die Biotechnologie nützlicher zu machen und die Produktion von Medikamenten wie Antibiotika oder Industriechemikalien wie 1,3-Propandiol und Shikimisäure zu unterstützen. Diese gentechnischen Veränderungen zielen in der Regel darauf ab, den Energieaufwand für die Herstellung des Produkts zu verringern, die Erträge zu steigern und die Produktion von Abfällen zu reduzieren. ⓘ
Geschichte
Der Begriff Stoffwechsel leitet sich vom französischen "métabolisme" oder vom altgriechischen μεταβολή - "Metabole" für "eine Veränderung" ab, das wiederum von μεταβάλλ - "Metaballein" bedeutet "sich verändern". ⓘ
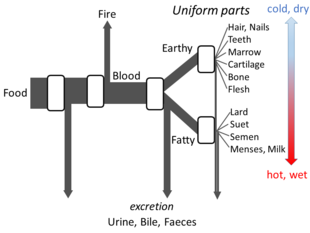
Griechische Philosophie
Aristoteles' Die Teile der Tiere enthält genügend Details seiner Ansichten über den Stoffwechsel, um ein Modell des offenen Flusses zu erstellen. Er ging davon aus, dass in jeder Phase des Prozesses Stoffe aus der Nahrung umgewandelt werden, wobei Wärme als klassisches Element des Feuers freigesetzt und Reststoffe als Urin, Galle oder Fäkalien ausgeschieden werden. ⓘ
Islamische Medizin
Ibn al-Nafis beschrieb den Stoffwechsel in seinem 1260 n. Chr. erschienenen Werk mit dem Titel Al-Risalah al-Kamiliyyah fil Siera al-Nabawiyyah (Die Abhandlung von Kamil über die Biographie des Propheten) mit folgendem Satz: "Sowohl der Körper als auch seine Teile befinden sich in einem ständigen Zustand der Auflösung und der Ernährung, so dass sie unweigerlich einer ständigen Veränderung unterliegen." ⓘ
Anwendung der wissenschaftlichen Methode
Die Geschichte der wissenschaftlichen Erforschung des Stoffwechsels erstreckt sich über mehrere Jahrhunderte und hat sich von der Untersuchung ganzer Tiere in frühen Studien bis zur Untersuchung einzelner Stoffwechselreaktionen in der modernen Biochemie entwickelt. Die ersten kontrollierten Experimente zum menschlichen Stoffwechsel wurden 1614 von Santorio Santorio in seinem Buch Ars de statica medicina veröffentlicht. Er beschrieb, wie er sich vor und nach dem Essen, Schlafen, Arbeiten, Sex, Fasten, Trinken und Ausscheiden wog. Er stellte fest, dass der größte Teil der aufgenommenen Nahrung durch das, was er "unempfindliches Schwitzen" nannte, verloren ging. ⓘ

In diesen frühen Studien waren die Mechanismen dieser Stoffwechselprozesse noch nicht bekannt, und man ging davon aus, dass das lebende Gewebe durch eine Lebenskraft belebt wird. Im 19. Jahrhundert kam Louis Pasteur bei der Untersuchung der Gärung von Zucker zu Alkohol durch Hefe zu dem Schluss, dass die Gärung durch Substanzen innerhalb der Hefezellen katalysiert wird, die er "Fermente" nannte. Er schrieb, dass "die alkoholische Gärung ein Akt ist, der mit dem Leben und der Organisation der Hefezellen zusammenhängt, nicht mit dem Tod oder der Fäulnis der Zellen". Diese Entdeckung und die Veröffentlichung einer Arbeit über die chemische Synthese von Harnstoff durch Friedrich Wöhler im Jahr 1828 sind bemerkenswert, da es sich um die erste organische Verbindung handelt, die aus rein anorganischen Ausgangsstoffen hergestellt wurde. Damit war bewiesen, dass sich die organischen Verbindungen und die chemischen Reaktionen in den Zellen im Prinzip nicht von allen anderen Bereichen der Chemie unterscheiden. ⓘ
Erst die Entdeckung der Enzyme zu Beginn des 20. Jahrhunderts durch Eduard Buchner trennte die Untersuchung der chemischen Reaktionen des Stoffwechsels von der biologischen Untersuchung der Zellen und markierte den Beginn der Biochemie. Zu Beginn des 20. Jahrhunderts wuchs der Umfang des biochemischen Wissens rasch an. Einer der produktivsten dieser modernen Biochemiker war Hans Krebs, der große Beiträge zur Erforschung des Stoffwechsels leistete. Er entdeckte den Harnstoffzyklus und später, in Zusammenarbeit mit Hans Kornberg, den Zitronensäurezyklus und den Glyoxylatzyklus. Die moderne biochemische Forschung wurde durch die Entwicklung neuer Techniken wie Chromatographie, Röntgenbeugung, NMR-Spektroskopie, radioisotopische Markierung, Elektronenmikroskopie und Molekulardynamiksimulationen erheblich gefördert. Diese Techniken haben die Entdeckung und detaillierte Analyse der vielen Moleküle und Stoffwechselwege in den Zellen ermöglicht. ⓘ
Kataboler und anaboler Stoffwechsel
Der gesamte Stoffwechsel kann eingeteilt werden in katabole Reaktionen, welche durch den Abbau von chemisch komplexen Nahrungsstoffen zu einfacheren Stoffen Energie liefern (Katabolismus), und anabole Reaktionen, welche unter Energieverbrauch körpereigene Stoffe aus einfachen Bausteinen aufbauen (Anabolismus). ⓘ
Katabolismus und Anabolismus haben eine gemeinsame Schnittstelle: Im Intermediärstoffwechsel werden relativ einfache Moleküle umgebaut, die als Zwischenprodukte (Metaboliten) sowohl vom katabolen als auch vom anabolen Stoffwechsel bereitgestellt werden können. ⓘ
|
<imagemap>-Fehler: Am Ende von Zeile 20 wurde kein gültiger Link gefunden |
| Einige Stoffwechselwege und ihre Verknüpfung (Substanzen zum Anklicken) |
Stoffwechselrate
Die Geschwindigkeit der Energiebereitstellung durch den Energiestoffwechsel wird Stoffwechselrate oder Metabolismusrate genannt. Sie ist als Energieumsatz des Organismus pro Zeiteinheit definiert. Die basale Stoffwechselrate ist der Energieverbrauch bei völliger Ruhe; insbesondere beim Menschen spricht man vom Grundumsatz. ⓘ
Reaktionstypen
Enzymatisch katalysierte Reaktionen
Nach dem IUPAC/IUBMB Enzym-Klassifikationssystem gibt es sechs Hauptgruppen von Enzymreaktionen. Dadurch kann auch der Stoffwechsel, in dem Reaktionen durch Enzyme katalysiert werden, ebenfalls in sechs Gruppen von Reaktionen unterteilt werden, nämlich in Redoxreaktionen, Gruppenübertragungsreaktionen, Hydrolysereaktionen, Lyase-Reaktionen (Addition, Hydratisierung), Isomerisierungsreaktionen und Ligationsreaktionen. ⓘ
Transport
Der Transport von Stoffen durch Transportproteine kann innerhalb von Zellkompartimenten, außerhalb von Zellen, oder über Kompartimentgrenzen (Biomembrane) hinweg geschehen. Es kann sich um reine Diffusionsprozesse, erleichterte Diffusion oder aktiven, ATP verbrauchenden Membrantransport handeln. ⓘ
Mit der Transporter Classification Database (TCDB) steht eine von der IUBMB sanktionierte Klassifikation der Transportproteine zur Verfügung, die sich zusätzlich zur Funktion an der Abstammung der Proteine orientiert. Bei dieser Definition von Transport werden allerdings alle Proteine, die Stoffe zeitweilig nur binden und in dieser Zeit selbst transportiert werden (beispielsweise mit dem Blutkreislauf), nicht erfasst. Die Hauptgruppen in der TCDB sind Porine und Ionenkanäle, potenzialgetriebene Transporter, primär aktive Transporter, Phosphotransferasen, Transmembran-Elektronencarrier, Hilfstransporter und andere. ⓘ
Stoffwechseltypen bei verschiedenen Gruppen von Lebewesen
Pflanzen, Algen, einige Bakterien und Archaea betreiben Photosynthese. Sie verwenden die Energie des Lichts, um Kohlenstoffdioxid (bei Landpflanzen aus der Luft stammend), Wasser und andere Ausgangsstoffe in körpereigenes Material umzuwandeln. Dieses dient entweder sofort dem weiteren Aufbau und Wachstum des Organismus, oder es dient als Speicherstoff, wie zum Beispiel Kohlenhydrate (siehe auch Calvin-Zyklus). Die Reservestoffe können später im Baustoffwechsel oder im Energiestoffwechsel verarbeitet werden. Sekundäre Pflanzenstoffe sind chemische Verbindungen, die von Pflanzen produziert werden, aber weder im Baustoffwechsel noch im Energiestoffwechsel benötigt werden. ⓘ
Tiere verstoffwechseln (metabolisieren) bei ihrer Verdauung andere Organismen oder deren Speicherstoffe (etwa Kohlenhydrate, Proteine oder Fette), siehe auch Chemotrophie. ⓘ
Bei Mikroorganismen finden sich weitere Typen des Stoffwechsels. ⓘ
Darüber hinaus ist in der Ratgeberliteratur zu Ernährung und Diäten gelegentlich von verschiedenen „Stoffwechseltypen“ beim Menschen die Rede, siehe Metabolic Typing. Mit der oben genannten Einteilung der Lebewesen haben individuelle Besonderheiten innerhalb einzelner Arten nichts zu tun. Menschen unterscheiden sich in Merkmalen ihres Stoffwechsels ebenso wie in anderen Merkmalen. Die Lehre von bestimmten „Typen“ gilt jedoch als spekulativ und unwissenschaftlich. ⓘ

