Pregabalin
 | |
 | |
| Klinische Daten | |
|---|---|
| Aussprache | /priˈɡæbəlɪn/ |
| Handelsnamen | Lyrica, andere |
| Andere Bezeichnungen | 3-Isobutyl-GABA, (S)-3-Isobutyl-γ-aminobuttersäure |
| AHFS/Drugs.com | Monographie |
| MedlinePlus | a605045 |
| Lizenz-Daten |
|
| Schwangerschaft Kategorie |
|
| Abhängigkeit Haftung | Körperlich: Mäßig Psychologisch: Mäßig |
| Sucht Haftung | Gering |
| Wege der Verabreichung | Durch den Mund |
| Wirkstoffklasse | Gabapentinoid |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | Oral: Hoch (≥90% werden schnell resorbiert; die Verabreichung mit der Nahrung hat keinen signifikanten Einfluss auf die Bioverfügbarkeit) |
| Proteinbindung | <1% |
| Metaboliten | N-Methylpregabalin |
| Beginn der Wirkung | Kann innerhalb einer Woche eintreten (Schmerzen) |
| Eliminationshalbwertszeit | 4,5-7 Stunden mit einer mittleren Eliminationshalbwertszeit von 6,3 Stunden |
| Dauer der Wirkung | Unbekannt |
| Ausscheidung | Niere |
| Bezeichner | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Chemische und physikalische Daten | |
| Formel | C8H17NO2 |
| Molare Masse | 159,229 g-mol-1 |
| 3D-Modell (JSmol) | |
SMILES
| |
InChI
| |
| (Überprüfen) | |
Pregabalin, das unter anderem unter dem Markennamen Lyrica vertrieben wird, ist ein Antikonvulsivum und Anxiolytikum zur Behandlung von Epilepsie, neuropathischen Schmerzen, Fibromyalgie, Restless-Leg-Syndrom, Opioid-Entzug und generalisierter Angststörung (GAD). Bei Epilepsie wird es als Zusatztherapie bei partiellen Anfällen eingesetzt. Vor chirurgischen Eingriffen wirkt es schmerzlindernd, führt jedoch zu einer stärkeren Sedierung und zu Sehstörungen. Es wird durch den Mund eingenommen. ⓘ
Häufige Nebenwirkungen sind Kopfschmerzen, Schwindel, Schläfrigkeit, Verwirrung, Gedächtnisstörungen, Koordinationsstörungen, Mundtrockenheit, Sehstörungen und Gewichtszunahme. Schwerwiegende Nebenwirkungen können Angioödeme, Medikamentenmissbrauch und ein erhöhtes Selbstmordrisiko sein. Wenn Pregabalin in hohen Dosen über einen längeren Zeitraum eingenommen wird, kann es zu einer Abhängigkeit kommen, doch ist das Risiko gering, wenn es in üblichen Dosen eingenommen wird. Die Sicherheit der Einnahme während der Schwangerschaft oder Stillzeit ist unklar. Pregabalin ist ein Gabapentinoid und wirkt durch Hemmung bestimmter Kalziumkanäle. ⓘ
Pregabalin wurde 2004 in den Vereinigten Staaten für die medizinische Verwendung zugelassen. Es wurde als Nachfolger von Gabapentin entwickelt. Es ist als Generikum in einer Reihe von Ländern erhältlich, ab 2019 auch in den Vereinigten Staaten. Eine generische Version der Formulierung mit verlängerter Wirkstofffreisetzung ist in den Vereinigten Staaten ab April 2021 erhältlich. Im Jahr 2019 war es mit mehr als 9 Millionen Verschreibungen das am häufigsten verschriebene Medikament in den Vereinigten Staaten (Platz 81). In den USA ist Pregabalin eine kontrollierte Substanz nach Schedule V des Controlled Substances Act von 1970. Im Vereinigten Königreich ist es eine kontrollierte Substanz der Klasse C. ⓘ
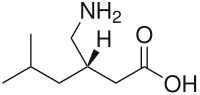
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Pregabalin | ||||||||||||||||||
| Andere Namen |
(S)-3-(Aminomethyl)-5-methylhexansäure (IUPAC) | ||||||||||||||||||
| Summenformel | C8H17NO2 | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code |
N03AX16 | ||||||||||||||||||
| Wirkstoffklasse |
Antiepileptikum | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 159,23 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
186–188 °C | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Pregabalin ist ein Arzneistoff aus der Gruppe der Gabapentinoide und gehört als Wirkstoff zu den Antikonvulsiva. Zugelassen ist es EU-weit seit 2004 zur Behandlung neuropathischer Schmerzen, der Epilepsie sowie der Generalisierten Angststörung. Die bekannteste Handelsmarke ist Lyrica. Seit dem 1. Dezember 2014 sind in Deutschland Generika verfügbar. ⓘ
Pregabalin war 2009 auf Platz 12 der umsatzstärksten patentgeschützten Arzneimittel in Deutschland, mit einem Umsatz von ca. 220 Millionen Euro. Das Medikament wurde von Richard Bruce Silverman entwickelt. ⓘ
Medizinische Anwendungen

Krampfanfälle
Pregabalin ist nützlich, wenn es zu anderen Behandlungen hinzugefügt wird, wenn diese anderen Behandlungen die partielle Epilepsie nicht kontrollieren. Die alleinige Anwendung von Pregabalin ist weniger wirksam als die einiger anderer Anfallsmedikamente. Es ist unklar, wie Pregabalin im Vergleich zu Gabapentin bei dieser Anwendung abschneidet. ⓘ
Neuropathische Schmerzen
Die European Federation of Neurological Societies empfiehlt Pregabalin als Mittel der ersten Wahl für die Behandlung von Schmerzen im Zusammenhang mit diabetischer Neuropathie, postherpetischer Neuralgie und zentralen neuropathischen Schmerzen. Eine Minderheit erzielt einen erheblichen Nutzen, eine größere Zahl einen mäßigen Nutzen. Als Mittel der ersten Wahl ist es Gabapentin und trizyklischen Antidepressiva gleichgestellt, wobei letztere seit 2010 preiswerter sind. ⓘ
Studien haben gezeigt, dass höhere Dosen von Pregabalin mit einer größeren Wirksamkeit verbunden sind. ⓘ
Der Einsatz von Pregabalin bei krebsbedingten neuropathischen Schmerzen ist umstritten, wird aber häufig angewendet. Es wurde zur Vorbeugung von chronischen Schmerzen nach Operationen untersucht, aber sein Nutzen für diesen Zweck ist umstritten. ⓘ
Pregabalin wird allgemein als nicht wirksam bei der Behandlung akuter Schmerzen angesehen. In Studien, die den Nutzen von Pregabalin bei der Behandlung akuter postoperativer Schmerzen untersuchten, wurde keine Wirkung auf die Gesamtschmerzstärke beobachtet, aber die Patienten benötigten weniger Morphin und hatten weniger opioidbedingte Nebenwirkungen. Es wurden mehrere mögliche Mechanismen für die Schmerzverbesserung diskutiert. ⓘ
Angstzustände
Pregabalin ist mäßig wirksam und sicher in der Behandlung der generalisierten Angststörung. Die World Federation of Biological Psychiatry empfiehlt Pregabalin als eines von mehreren Medikamenten der ersten Wahl für die Behandlung von generalisierten Angststörungen, empfiehlt jedoch andere Medikamente wie SSRIs als erste Wahl für die Behandlung von Zwangsstörungen und posttraumatischen Belastungsstörungen. Pregabalin scheint eine ähnliche angstlösende Wirkung wie Benzodiazepine zu haben, wobei das Risiko einer Abhängigkeit geringer ist. ⓘ
Die Wirkung von Pregabalin tritt nach einer Woche der Einnahme ein und ist ähnlich wirksam wie die von Lorazepam, Alprazolam und Venlafaxin, aber Pregabalin hat sich als überlegen erwiesen, da es eine beständigere therapeutische Wirkung bei psychosomatischen Angstsymptomen zeigt. Langzeitstudien haben eine anhaltende Wirksamkeit ohne Toleranzentwicklung gezeigt. Darüber hinaus hat Pregabalin im Gegensatz zu Benzodiazepinen eine positive Wirkung auf den Schlaf und die Schlafarchitektur, die durch eine Verbesserung des Langsamschlafs gekennzeichnet ist. Im Vergleich zu Benzodiazepinen führt es zu weniger schweren kognitiven und psychomotorischen Beeinträchtigungen. ⓘ
In einer Übersichtsarbeit aus dem Jahr 2019 wurde festgestellt, dass Pregabalin die Symptome lindert und im Allgemeinen gut verträglich ist. ⓘ
Andere Verwendungen
Für die Anwendung von Pregabalin bei Ischias und Kreuzschmerzen gibt es keine Belege und kein signifikantes Risiko. Der Nutzen von Pregabalin beim Alkoholentzug sowie beim Entzug von bestimmten anderen Arzneimitteln ist nur begrenzt belegt (Stand: 2016). ⓘ
Es gibt keine Belege für die Verwendung von Pregabalin zur Vorbeugung von Migräne, und auch Gabapentin hat sich nicht als nützlich erwiesen. ⓘ
Unerwünschte Wirkungen
Zu den häufigsten Nebenwirkungen zählen Schwindel, Müdigkeit, Benommenheit, nachlassende Aufmerksamkeit, Trunkenheitsgefühl, insbesondere zu Beginn der Behandlung. Des Weiteren kann es zu verschwommenem Sehen, Doppeltsehen, Gleichgewichtsstörungen, Erektionsstörungen, Ödemen, Übelkeit und Erbrechen kommen. Eine Gewichtszunahme ist häufig. Gelegentliche Nebenwirkungen sind Muskelzucken, Muskelkrämpfe, Herzrhythmusstörungen, Kraftlosigkeit und Stürze. Selten auftretende Nebenwirkungen sind Schluckbeschwerden, hoher Blutzucker, Muskelschäden, Nierenversagen, Brustschmerzen und Veränderungen der Sicht (Tiefenwahrnehmung, Lichtblitze, optische Helligkeit). Weitere Nebenwirkungen, die nach Markteinführung berichtet wurden und deren Häufigkeit nicht bestimmt werden kann, sind Herzmuskelschwäche (Herzinsuffizienz), Änderung der Aufnahme von elektrischen Veränderungen (EKG) des Herzens, die mit Herzrhythmusstörungen zusammenhängen, Flüssigkeit in der Lunge, Verlust des Bewusstseins, Krampfanfälle sowie Überempfindlichkeits- und allergische Reaktionen. ⓘ
Nach Absetzen einer Pregabalin-Therapie wurden bei einigen Patienten zum Teil schwere Entzugs-Symptome festgestellt. Pregabalin sollte deshalb nicht plötzlich abgesetzt, sondern ausschleichend dosiert werden, da es sonst auch zu einer Häufung epileptischer Anfälle kommen kann. Benommenheit und Schläfrigkeit können vor allem bei älteren Patienten zu Stürzen führen. ⓘ
Es bestehen Hinweise auf ein Abhängigkeitspotenzial von Pregabalin, entsprechende Berichte gibt es aus Deutschland und Schweden. Die Fachinformationen wurden um den Hinweis erweitert: „Fälle von nicht bestimmungsgemäßem Gebrauch, Missbrauch und Abhängigkeit wurden berichtet. Bei Patienten mit Drogenmissbrauch in der Vorgeschichte ist Vorsicht geboten und der Patient sollte hinsichtlich Symptomen eines nicht bestimmungsgemäßen Gebrauchs, des Missbrauchs oder der Abhängigkeit von Pregabalin (…) überwacht werden.“ ⓘ
Der Wirkstoff Pregabalin kann die Wirkung von ZNS-dämpfenden Substanzen wie Lorazepam und Alkohol verstärken, bis hin zu Atemschwäche (respiratorischer Insuffizienz) und Koma. Er verstärkt vermutlich auch kognitive und grobmotorische Beeinträchtigungen nach Einnahme von Oxycodon. ⓘ
Eine gleichzeitige Verwendung von Pregabalin und oralen hormonellen Kontrazeptiva („Antibabypille“) ist möglich. ⓘ
Bei Niereninsuffizienz muss die Dosierung reduziert werden. ⓘ
Die Einnahme von Pregabalin wird mit Gewichtszunahme, Schläfrigkeit und Müdigkeit, Schwindel, Schwellungen der Beine, Sehstörungen, Koordinationsverlust und Euphorie in Verbindung gebracht. Das Nebenwirkungsprofil von Pregabalin ähnelt dem anderer Mittel zur Depression des zentralen Nervensystems. Zu den unerwünschten Arzneimittelwirkungen im Zusammenhang mit der Einnahme von Pregabalin gehören:
- Sehr häufig (>10 % der Pregabalin-Patienten): Schwindel, Schläfrigkeit.
- Häufig (1-10 % der Patienten mit Pregabalin): Verschwommenes Sehen, Diplopie, gesteigerter Appetit und anschließende Gewichtszunahme, Euphorie, Verwirrtheit, lebhafte Träume, Veränderungen der Libido (Zunahme oder Abnahme), Reizbarkeit, Ataxie, Veränderungen der Aufmerksamkeit, Rauschzustände, abnorme Koordination, Gedächtnisstörungen, Zittern, Dysarthrie, Parasthesie, Schwindel, Mundtrockenheit und Verstopfung, Erbrechen und Blähungen, erektile Dysfunktion, Müdigkeit, periphere Ödeme, Gefühl der Auswirkungen von Trunkenheit, abnormales Gehen, Asthenie, Nasopharyngitis, erhöhter Kreatinkinasewert.
- Selten (0,1-1% der Patienten mit Pregabalin): Depression, Lethargie, Unruhe, Anorgasmie, Halluzinationen, Myoklonus, Hypoästhesie, Hyperästhesie, Tachykardie, übermäßiger Speichelfluss, Hypoglykämie, Schwitzen, Flush, Hautausschlag, Muskelkrämpfe, Myalgie, Arthralgie, Harninkontinenz, Dysurie, Thrombozytopenie, Nierensteine
- Selten (<0,1 % der Personen, die Pregabalin einnehmen): Neutropenie, Herzblock ersten Grades, Hypotonie, Hypertonie, Pankreatitis, Dysphagie, Oligurie, Rhabdomyolyse, Suizidgedanken oder -verhalten. ⓘ
Es wurde über Fälle von Freizeitkonsum mit den damit verbundenen unerwünschten Wirkungen berichtet. ⓘ
Entzugssymptome
Nach abruptem oder schnellem Absetzen von Pregabalin berichteten einige Personen über Symptome, die auf eine körperliche Abhängigkeit hindeuten. Die FDA stellte fest, dass das Substanzabhängigkeitsprofil von Pregabalin, gemessen anhand einer persönlichen körperlichen Entzugscheckliste, quantitativ geringer ist als bei Benzodiazepinen. Selbst bei Personen, die die kurzfristige Einnahme von Pregabalin abgebrochen haben, traten Entzugssymptome auf, darunter Schlaflosigkeit, Kopfschmerzen, Übelkeit, Angstzustände, Durchfall, grippeähnliche Symptome, Nervosität, schwere Depressionen, Schmerzen, Krämpfe, Hyperhidrosis und Schwindel. ⓘ
Schwangerschaft
Es ist unklar, ob die Einnahme in der Schwangerschaft sicher ist; einige Studien haben mögliche Schäden aufgezeigt. ⓘ
Atmen
Im Dezember 2019 warnte die US-amerikanische Arzneimittelzulassungsbehörde (FDA) vor schwerwiegenden Atemproblemen bei der Einnahme von Gabapentin oder Pregabalin in Verbindung mit ZNS-Depressiva oder bei Personen mit Lungenproblemen. ⓘ
Die FDA verlangte, dass neue Warnhinweise über das Risiko einer Atemdepression in die Verschreibungsinformationen der Gabapentinoide aufgenommen werden. Außerdem forderte die FDA die Arzneimittelhersteller auf, klinische Studien durchzuführen, um das Missbrauchspotenzial der Gabapentinoide, insbesondere in Kombination mit Opioiden, weiter zu untersuchen, da der Missbrauch dieser Produkte zunimmt und der gemeinsame Gebrauch das Risiko einer Atemdepression erhöhen kann. ⓘ
Unter den 49 Fallberichten, die der FDA über den Fünfjahreszeitraum von 2012 bis 2017 vorgelegt wurden, starben zwölf Menschen an Atemdepression durch Gabapentinoide, die alle mindestens einen Risikofaktor aufwiesen. ⓘ
Die FDA überprüfte die Ergebnisse von zwei randomisierten, doppelblinden, placebokontrollierten klinischen Studien an gesunden Menschen, drei Beobachtungsstudien und mehreren Studien an Tieren. Eine Studie zeigte, dass die alleinige Anwendung von Pregabalin und die gleichzeitige Anwendung mit einem opioiden Schmerzmittel die Atemfunktion beeinträchtigen kann. Die andere Studie zeigte, dass Gabapentin allein die Atempausen während des Schlafs erhöht. Die drei Beobachtungsstudien an einem akademischen medizinischen Zentrum zeigten einen Zusammenhang zwischen Gabapentinoiden, die vor einer Operation verabreicht wurden, und Atemdepression nach verschiedenen Operationen. Die FDA überprüfte auch mehrere Tierstudien, die zeigten, dass Pregabalin allein und Pregabalin zusammen mit Opioiden die Atemfunktion beeinträchtigen kann. ⓘ
Überdosierung
Mehrere Personen mit Nierenversagen entwickelten während der Behandlung mit Pregabalin einen Myoklonus, offenbar als Folge einer allmählichen Anreicherung des Arzneimittels. Eine akute Überdosierung kann sich durch Somnolenz, Tachykardie und Hypertonie äußern. Die Plasma-, Serum- oder Blutkonzentration von Pregabalin kann zur Überwachung der Therapie oder zur Bestätigung einer Vergiftungsdiagnose bei hospitalisierten Personen gemessen werden. ⓘ
Pharmakologie
Wechselwirkungen
In vivo sind keine Wechselwirkungen nachgewiesen worden. Der Hersteller weist auf einige potenzielle pharmakologische Wechselwirkungen mit Opioiden, Benzodiazepinen, Barbituraten, Ethanol (Alkohol) und anderen Arzneimitteln hin, die das zentrale Nervensystem dämpfen. ACE-Hemmer können die schädliche/toxische Wirkung von Pregabalin verstärken. Pregabalin kann die flüssigkeitsrückhaltende Wirkung bestimmter Antidiabetika (Thiazolidindione) verstärken. ⓘ
Pharmakodynamik

Pregabalin ist ein Gabapentinoid und wirkt durch Hemmung bestimmter Kalziumkanäle. Insbesondere ist es ein Ligand der α2δ-Hilfsuntereinheit bestimmter spannungsabhängiger Kalziumkanäle (VDCCs) und wirkt somit als Inhibitor der α2δ-Untereinheit enthaltenden VDCCs. Es gibt zwei arzneimittelbindende α2δ-Untereinheiten, α2δ-1 und α2δ-2, und Pregabalin zeigt eine ähnliche Affinität für diese beiden Stellen (und somit keine Selektivität zwischen ihnen). Pregabalin ist selektiv in seiner Bindung an die α2δ-VDCC-Untereinheit. Obwohl Pregabalin ein GABA-Analogon ist, bindet es nicht an die GABA-Rezeptoren, wird in vivo nicht in GABA oder einen anderen GABA-Rezeptor-Agonisten umgewandelt und moduliert nicht direkt den GABA-Transport oder -Metabolismus. Es wurde jedoch festgestellt, dass Pregabalin die Expression von L-Glutaminsäure-Decarboxylase (GAD), dem für die GABA-Synthese verantwortlichen Enzym, im Gehirn dosisabhängig erhöht und daher möglicherweise indirekte GABA-erge Wirkungen hat, indem es den GABA-Spiegel im Gehirn erhöht. Es gibt derzeit keine Hinweise darauf, dass die Wirkungen von Pregabalin über einen anderen Mechanismus als die Hemmung von α2δ-haltigen VDCCs vermittelt werden. Demnach scheint die Hemmung der α2δ-1-haltigen VDCCs durch Pregabalin für seine antikonvulsiven, analgetischen und anxiolytischen Wirkungen verantwortlich zu sein. ⓘ
Die endogenen α-Aminosäuren L-Leucin und L-Isoleucin, die Pregabalin und den anderen Gabapentinoiden in ihrer chemischen Struktur sehr ähnlich sind, sind offensichtlich Liganden der α2δ-VDCC-Untereinheit mit ähnlicher Affinität wie die Gabapentinoide (z. B., IC50 = 71 nM für L-Isoleucin) und sind in der menschlichen Zerebrospinalflüssigkeit in mikromolaren Konzentrationen vorhanden (z. B. 12,9 μM für L-Leucin, 4,8 μM für L-Isoleucin). Es wurde die Theorie aufgestellt, dass sie die endogenen Liganden der Untereinheit sein könnten und dass sie die Wirkungen von Gabapentinoiden kompetitiv antagonisieren könnten. Während Gabapentinoide wie Pregabalin und Gabapentin nanomolare Affinitäten für die α2δ-Untereinheit aufweisen, liegen ihre Potenzen in vivo im niedrigen mikromolaren Bereich, und es wird angenommen, dass die Konkurrenz um die Bindung durch endogene L-Aminosäuren wahrscheinlich für diese Diskrepanz verantwortlich ist. ⓘ
In einer Studie wurde festgestellt, dass Pregabalin eine 6-fach höhere Affinität als Gabapentin für α2δ-Untereinheiten enthaltende VDCCs besitzt. In einer anderen Studie wurde jedoch festgestellt, dass Pregabalin und Gabapentin eine ähnliche Affinität für die menschliche rekombinante α2δ-1-Untereinheit aufweisen (Ki = 32 nM bzw. 40 nM). In jedem Fall ist Pregabalin als Analgetikum 2- bis 4-mal stärker als Gabapentin und scheint bei Tieren als Antikonvulsivum 3- bis 10-mal stärker als Gabapentin zu sein. ⓘ
Pharmakokinetik
Absorption
Pregabalin wird aus dem Darm durch einen aktiven Transportprozess aufgenommen, der über den großen neutralen Aminosäuretransporter 1 (LAT1, SLC7A5), einen Transporter für Aminosäuren wie L-Leucin und L-Phenylalanin, vermittelt wird. Es sind nur sehr wenige Medikamente (weniger als 10) bekannt, die über diesen Transporter transportiert werden. Im Gegensatz zu Gabapentin, das ausschließlich von LAT1 transportiert wird, scheint Pregabalin nicht nur von LAT1, sondern auch von anderen Carriern transportiert zu werden. Der LAT1 ist leicht sättigbar, so dass die Pharmakokinetik von Gabapentin dosisabhängig ist, mit verminderter Bioverfügbarkeit und verzögerten Spitzenwerten bei höheren Dosen. Im Gegensatz dazu ist dies bei Pregabalin nicht der Fall, das eine lineare Pharmakokinetik und keine Sättigung der Absorption aufweist. ⓘ
Die orale Bioverfügbarkeit von Pregabalin beträgt über den gesamten klinischen Dosisbereich (75 bis 900 mg/Tag) mehr als oder gleich 90 %. Die Nahrung hat keinen signifikanten Einfluss auf die orale Bioverfügbarkeit von Pregabalin. Pregabalin wird schnell resorbiert, wenn es auf nüchternen Magen verabreicht wird, mit einer Tmax (Zeit bis zum Erreichen der Höchstwerte) von im Allgemeinen weniger als oder gleich 1 Stunde bei Dosen von 300 mg oder weniger. Es hat sich jedoch gezeigt, dass Nahrung die Absorption von Pregabalin erheblich verzögert und die Spitzenwerte signifikant reduziert, ohne die Bioverfügbarkeit des Arzneimittels zu beeinträchtigen; die Tmax-Werte für Pregabalin liegen bei 0,6 Stunden im nüchternen Zustand und bei 3,2 Stunden im gefütterten Zustand (5-facher Unterschied), und die Cmax ist im gefütterten Zustand gegenüber dem nüchternen Zustand um 25-31% reduziert. ⓘ
Verteilung
Pregabalin überwindet die Blut-Hirn-Schranke und gelangt in das zentrale Nervensystem. Aufgrund seiner geringen Lipophilie erfordert Pregabalin jedoch einen aktiven Transport über die Blut-Hirn-Schranke. Das LAT1 wird an der Blut-Hirn-Schranke in hohem Maße exprimiert und transportiert Pregabalin in das Gehirn. Es wurde nachgewiesen, dass Pregabalin bei Ratten die Plazenta passiert und in der Milch säugender Ratten vorhanden ist. Beim Menschen beträgt das Verteilungsvolumen einer oral verabreichten Dosis von Pregabalin etwa 0,56 l/kg. Pregabalin ist nicht signifikant an Plasmaproteine gebunden (<1%). ⓘ
Stoffwechsel
Pregabalin wird kaum oder gar nicht verstoffwechselt. In Experimenten mit nuklearmedizinischen Techniken wurde festgestellt, dass es sich bei etwa 98 % der im Urin wiedergefundenen Radioaktivität um unverändertes Pregabalin handelt. Der Hauptmetabolit ist N-Methylpregabalin. ⓘ
Ausscheidung
Pregabalin wird über die Nieren mit dem Urin ausgeschieden, hauptsächlich in unveränderter Form. Es hat eine relativ kurze Eliminationshalbwertszeit, die mit 6,3 Stunden angegeben wird. Aufgrund seiner kurzen Eliminationshalbwertszeit wird Pregabalin 2 bis 3 Mal pro Tag verabreicht, um therapeutische Spiegel aufrechtzuerhalten. Die Nieren-Clearance von Pregabalin beträgt 73 mL/Minute. ⓘ
Chemie

Pregabalin ist ein GABA-Analogon, das sowohl ein 3-substituiertes Derivat als auch eine γ-Aminosäure ist. Genauer gesagt handelt es sich bei Pregabalin um (S)-(+)-3-Isobutyl-GABA. Pregabalin ist auch den α-Aminosäuren L-Leucin und L-Isoleucin sehr ähnlich, was für seine Pharmakodynamik möglicherweise von größerer Bedeutung ist als seine strukturelle Ähnlichkeit mit GABA. ⓘ
In wässrigen Medien ist es bei pH-Werten unterhalb von 3,7 leicht löslich. ⓘ
Synthese
Bei der enantioselektiven Synthese von Pregabalin wird zunächst ausgehend von Isobutyraldehyd und Acrylnitril mehrstufig das Salz aus dem tert-Butylammonium-Kation und dem Anion 3-Cyano-5-methyl-3-hexenoat hergestellt, dessen C=C-Doppelbindung dann einer enantioselektiven Hydrierung unterworfen wird und (S)-3-Cyano-5-methylhexansäure liefert. Die Reduktion der Nitrilgruppe liefert dann Pregabalin. Es gibt auch alternative Synthesen, bei denen eine Racematspaltung der Schlüsselschritt ist. ⓘ
Geschichte
| Externes Video ⓘ | |
|---|---|
 | |
Pregabalin wurde 1990 als Antikonvulsivum synthetisiert. Erfunden wurde es von dem medizinischen Chemiker Richard Bruce Silverman an der Northwestern University in Evanston, Illinois. Silverman ist vor allem dafür bekannt, dass er den Wirkstoff Pregabalin als mögliches Mittel zur Behandlung von epileptischen Anfällen identifiziert hat. Zwischen 1988 und 1990 synthetisierte Ryszard Andruszkiewicz, ein Gastwissenschaftler, eine Reihe von Molekülen für Silverman. Eines davon sah besonders vielversprechend aus. Das Molekül war so geformt, dass es in das Gehirn transportiert werden konnte, wo es das Enzym L-Glutaminsäure-Decarboxylase aktivierte. Silverman hoffte, dass das Enzym die Produktion des hemmenden Neurotransmitters GABA erhöhen und Krämpfe blockieren würde. Schließlich wurden die Moleküle zur Prüfung an Parke-Davis Pharmaceuticals geschickt. Im Jahr 2004 wurde das Medikament in der Europäischen Union zugelassen. In den USA erhielt es im Dezember 2004 die FDA-Zulassung für die Behandlung von Epilepsie, diabetischen neuropathischen Schmerzen und postherpetischer Neuralgie. Pregabalin kam dann im Herbst 2005 unter dem Markennamen Lyrica auf den US-Markt. Im Jahr 2017 genehmigte die US-Arzneimittelbehörde (FDA) Pregabalin Lyrica CR mit verlängerter Wirkstofffreisetzung, aber im Gegensatz zur Formulierung mit sofortiger Wirkstofffreisetzung wurde es nicht für die Behandlung von Fibromyalgie oder als Zusatztherapie für Erwachsene mit partiellen Anfällen zugelassen. ⓘ
Gesellschaft und Kultur
Kosten
Pregabalin ist als Generikum in einer Reihe von Ländern erhältlich, ab Juli 2019 auch in den Vereinigten Staaten. In den Vereinigten Staaten liegen die Großhandels-/Apothekenkosten für generisches Pregabalin ab Juli 2019 bei 0,17-0,22 US-Dollar pro 150-mg-Kapsel. ⓘ
Rechtlicher Status
- Vereinigte Staaten: Während der klinischen Studien berichtete eine kleine Anzahl von Anwendern (~4 %) über Euphorie nach der Einnahme, was zu einer Kontrolle in den USA führte. Die Drug Enforcement Administration (DEA) stufte Pregabalin als Depressivum ein und ordnete Pregabalin, einschließlich seiner Salze, sowie alle Produkte, die Pregabalin enthalten, in Schedule V des Controlled Substances Act ein.
- Norwegen: Pregabalin steht in der Liste B für verschreibungspflichtige Arzneimittel, neben Benzodiazepinen.
- Vereinigtes Königreich: Am 14. Januar 2016 richtete der Beirat für Drogenmissbrauch (Advisory Council on the Misuse of Drugs, ACMD) ein Schreiben an die Minister des Innenministeriums, in dem er empfahl, dass Pregabalin zusammen mit Gabapentin gemäß dem Misuse of Drugs Act 1971 kontrolliert werden sollte. Im Oktober 2018 wurde bekannt gegeben, dass Pregabalin ab April 2019 als kontrollierte Substanz der Klasse C neu eingestuft wird. ⓘ
Zulassung
In den Vereinigten Staaten hat die Food and Drug Administration (FDA) Pregabalin als Zusatztherapie für Erwachsene mit partiellen Anfällen, zur Behandlung von postherpetischer Neuralgie und neuropathischen Schmerzen im Zusammenhang mit Rückenmarksverletzungen und diabetischer peripherer Neuropathie sowie zur Behandlung von Fibromyalgie zugelassen. Pregabalin ist außerdem in der Europäischen Union, im Vereinigten Königreich und in Russland für die Behandlung der generalisierten Angststörung zugelassen worden. ⓘ
Vermarktung
Seit 2008 führt Pfizer umfangreiche Werbekampagnen direkt beim Verbraucher durch, um sein Markenprodukt Lyrica für die Indikationen Fibromyalgie und diabetische Nervenschmerzen zu bewerben. Im Januar 2016 gab das Unternehmen eine Rekordsumme von 24,6 Mio. USD für ein einzelnes Medikament für Fernsehwerbung aus und erzielte damit weltweit einen Umsatz von 14 Mrd. USD, davon mehr als die Hälfte in den Vereinigten Staaten. ⓘ
Bis 2009 bewarb Pfizer Lyrica für andere Anwendungen, die von den medizinischen Aufsichtsbehörden nicht genehmigt worden waren. Für Lyrica und drei weitere Medikamente wurde Pfizer vom Justizministerium zu einer Rekordstrafe in Höhe von 2,3 Milliarden US-Dollar verurteilt, nachdem das Unternehmen sich der Werbung und des Brandings mit der Absicht des Betrugs oder der Irreführung" schuldig bekannt hatte. Pfizer warb illegal für die Medikamente, indem es Ärzte zu Beratertreffen einlud, von denen viele an Urlaubsorten stattfanden; die Teilnehmer erhielten eine Aufwandsentschädigung und ein Honorar nur für ihre Anwesenheit", so Staatsanwalt Michael Loucks. ⓘ
Geistiges Eigentum
Professor Richard "Rick" Silverman von der Northwestern University entwickelte dort Pregabalin. Die Universität hält ein Patent darauf, das exklusiv an Pfizer lizenziert ist. Dieses und andere Patente wurden von Generikaherstellern angefochten und 2014 bestätigt, so dass Pfizer bis 2018 Exklusivität für Lyrica in den USA genießt. ⓘ
Im Oktober 2017 wurde Pregabalin unter vielen Markennamen in anderen Ländern vermarktet: Algerika, Alivax, Alyse, Alzain, Andogablin, Aprion, Averopreg, Axual, Balifibro, Brieka, Clasica, Convugabalin, Dapapalin, Dismedox, Dolgenal, Dolica, Dragonor, Ecubalin, Epica, Epiron, Gaba-P, Gabanext, Gabarol, Gabica, Gablin, Gablovac, Gabrika, Gavin, Gialtyn, Glonervya, Helimon, Hexgabalin, Irenypathic, Kabian, Kemirica, Kineptia, Lecaent, Lingabat, Linprel, Lyribastad, Lyric, Lyrica, Lyrineur, Lyrolin, Lyzalon, Martesia, Maxgalin, Mystika, Neuragabalin, Neugaba, Neurega, Neurica, Neuristan, Neurolin, Neurovan, Neurum, Newrica, Nuramed, Paden, Pagadin, Pagamax, Painica, Pevesca, PG, Plenica, Pragiola, Prebalin, Prebanal, Prebel, Prebictal, Prebien, Prefaxil, Pregaba, Pregabalin, Pregabalina, Pregabaline, Prégabaline, Pregabalinum, Pregabateg, Pregaben, Pregabid, Pregabin, Pregacent, Pregadel, Pregagamma, Pregalex, Pregalin, Pregalodos, Pregamid, Pregan, Preganerve, Pregastar, Pregatrend, Pregavalex, Pregdin Apex, Pregeb, Pregobin, Prejunate, Prelin, Preludyo, Prelyx, Premilin, Preneurolin, Prestat, Pretor, Priga, Provelyn, Regapen, Resenz, Rewisca, Serigabtin, Symra, Vronogabic, Xablin, und Xil. ⓘ
Es wurde auch in mehreren Ländern als Kombinationspräparat mit Mecobalamin unter den Markennamen Agemax-P, Alphamix-PG, Freenerve-P, Gaben, Macraberin-P, Mecoblend-P, Mecozen-PG, Meex-PG, Methylnuron-P, Nervolin, Nervopreg, Neurica-M, Neuroprime-PG, Neutron-OD, Nuroday-P, Nurodon-PG, Nuwin-P, Pecomin-PG, Prebel-M, Predic-GM, Pregacent-M, Pregamet, Preganerv-M, Pregeb-M OD, Pregmic, Prejunate Plus, Preneurolin Plus, Pretek-GM, Rejusite, Renerve-P, Safyvit-PR, und Vitcobin-P, Voltanerv mit Methylcobalamin und ALA von Cogentrix Pharma. ⓘ
Das Hauptpatent von Pfizer für Lyrica zur Behandlung von Anfallsleiden im Vereinigten Königreich lief 2013 aus. Im November 2018 entschied der Oberste Gerichtshof des Vereinigten Königreichs, dass das zweite Patent von Pfizer für das Medikament zur Behandlung von Schmerzen ungültig ist, weil es für die von ihm abgedeckten Erkrankungen - zentrale und periphere neuropathische Schmerzen - keine Beweise gibt. Ab Oktober 2015 waren die Hausärzte gezwungen, die Patienten von Pregabalin-Generika auf Markenpräparate umzustellen, bis das zweite Patent im Juli 2017 auslief. Dies kostete den NHS 502 Millionen Pfund. ⓘ
Medizinische Verwendung
Klinische Wirksamkeit und Sicherheit
Zusatztherapie bei Epilepsie
Pregabalin wurde in drei kontrollierten klinischen Studien sowohl bei zweimal täglicher als auch bei dreimal täglicher Gabe über jeweils 12 Wochen untersucht. Insgesamt war das Verträglichkeits- und Wirksamkeitsprofil bei zweimal und bei dreimal täglicher Gabe ähnlich. Eine Reduktion der Anfallshäufigkeit wurde innerhalb der ersten Woche beobachtet. ⓘ
Die Wirksamkeit und Sicherheit von Pregabalin als Zusatztherapie von Epilepsie wurden bei pädiatrischen Patienten unter 12 Jahren und Jugendlichen nicht nachgewiesen. Die Nebenwirkungen, die in einer Studie zur Pharmakokinetik und Verträglichkeit unter Beteiligung von Patienten ab einem Alter von 3 Monaten bis 16 Jahren (n = 65) beobachtet wurden, waren jenen, die bei Erwachsenen beobachtet wurden, ähnlich. Die Ergebnisse einer einjährigen unverblindeten Sicherheitsstudie unter Beteiligung von 54 pädiatrischen Epilepsiepatienten ab einem Alter von 3 Monaten bis 16 Jahren zeigen, dass die Nebenwirkungen Fieber und Infektionen der oberen Atemwege häufiger als in Studien bei Erwachsenen beobachtet wurden. Monotherapie (neu diagnostizierte Patienten): In einer kontrollierten klinischen Studie über 56 Wochen wurde Pregabalin bei zweimal täglicher Gabe untersucht. Bezogen auf den Endpunkt einer sechsmonatigen Anfallsfreiheit zeigte Pregabalin im Vergleich zu Lamotrigin keine Nichtunterlegenheit. Pregabalin und Lamotrigin waren gleichermaßen sicher und gut verträglich. ⓘ
Generalisierte Angststörungen
Pregabalin wurde in 6 kontrollierten Studien über einen Zeitraum von 4 bis 6 Wochen sowie in einer 8-wöchigen Studie mit älteren Patienten und in einer Langzeitstudie zur Rückfallprävention mit einer doppelblinden Rückfallpräventionsphase von 6 Monaten untersucht. Eine Besserung der Symptome von generalisierten Angststörungen gemäß der Hamilton-Angst-Skala (HAM-A) wurde innerhalb der 1. Woche beobachtet. In kontrollierten klinischen Studien über 4 bis 8 Wochen zeigten 52 % der mit Pregabalin behandelten Patienten und 38 % der Patienten unter Placebo eine im Vergleich zu den Ausgangswerten mindestens 50%ige Verbesserung des HAM-A-Gesamt-Scores. ⓘ
Anwendung bei Kindern und Jugendlichen
Es liegen keine Untersuchungen zur Anwendung bei Kindern und Jugendlichen unter 18 Jahren vor. Es kann deswegen nicht empfohlen werden, dass diese Personengruppen Pregabalin anwenden. ⓘ
Anwendung bei Schwangeren und in der Stillzeit
Es gibt keine kontrollierten klinischen Studien zur Anwendung von Pregabalin bei schwangeren Frauen. Tierversuche lassen jedoch vermuten, dass möglicherweise Gefahren für den Fötus bestehen könnten. Pregabalin sollte deshalb in der Schwangerschaft nur angewendet werden, wenn es unbedingt notwendig ist. Nach Angabe des Herstellers Pfizer ist die Anwendung bei Schwangerschaft ausgeschlossen, es wird explizit darauf hingewiesen, dass gebärfähige Frauen eine „wirksame Verhütungsmethode“ anwenden müssen. ⓘ
Auswirkungen auf die Fahrtüchtigkeit
Durch die Einnahme von Pregabalin kann es zu Benommenheit und Schläfrigkeit kommen. Deshalb wird Patienten davon abgeraten, Auto zu fahren, komplexe Maschinen zu bedienen oder andere potenziell gefährliche Tätigkeiten auszuführen, solange nicht bekannt ist, ob die Fähigkeit zur Ausübung solcher Tätigkeiten beeinträchtigt wird. ⓘ
Tiermedizinische Verwendung
Unter dem Namen Bonqat ist Pregabalin in der EU zugelassen zur Linderung akuter Angstzustände und Ängsten im Zusammenhang mit Transporten und Tierarztbesuchen bei Katzen. ⓘ