Histamin

| |
| |
| Bezeichnungen | |
|---|---|
| IUPAC-Bezeichnung
2-(1H-Imidazol-4-yl)ethanamin
| |
| Bezeichner | |
3D-Modell (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Arzneimittelbank | |
IUPHAR/BPS
|
|
| KEGG | |
| MeSH | Histamin |
PubChem CID
|
|
| UNII | |
InChI
| |
SMILES
| |
| Eigenschaften | |
Chemische Formel
|
C5H9N3 |
| Molare Masse | 111,148 g-mol-1 |
| Schmelzpunkt | 83,5 °C (182,3 °F; 356,6 K) |
| Siedepunkt | 209,5 °C (409,1 °F; 482,6 K) |
Löslichkeit in Wasser
|
Leicht löslich in kaltem Wasser, heißem Wasser |
| Löslichkeit in anderen Lösungsmitteln | Leicht löslich in Methanol. Sehr schwach löslich in Diethylether. Leicht löslich in Ethanol. |
| log P | −0.7 |
| Acidität (pKa) | Imidazol: 6.04 Endständiges NH2: 9,75 |
| Pharmakologie | |
ATC-Code
|
L03AX14 (WHO) V04CG03 (WHO) (Phosphat) |
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |
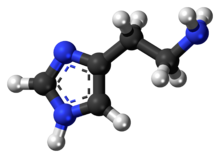
Histamin ist eine organische stickstoffhaltige Verbindung, die an lokalen Immunreaktionen beteiligt ist, physiologische Funktionen im Darm reguliert und als Neurotransmitter für Gehirn, Rückenmark und Gebärmutter fungiert. Seit seiner Entdeckung im Jahr 1910 wurde Histamin als lokales Hormon (Autokoid) betrachtet, da es nicht über die klassischen endokrinen Drüsen verfügt, die es absondern; in den letzten Jahren wurde Histamin jedoch als zentraler Neurotransmitter anerkannt. Histamin ist an der Entzündungsreaktion beteiligt und spielt eine zentrale Rolle als Vermittler von Juckreiz. Als Teil einer Immunreaktion auf fremde Krankheitserreger wird Histamin von Basophilen und Mastzellen in nahe gelegenen Bindegeweben produziert. Histamin erhöht die Durchlässigkeit der Kapillaren für die weißen Blutkörperchen und einige Proteine, damit diese die Krankheitserreger in den infizierten Geweben angreifen können. Es besteht aus einem Imidazolring, der an eine Ethylaminkette gebunden ist; unter physiologischen Bedingungen ist die Aminogruppe der Seitenkette protoniert. ⓘ
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemeines | |||||||||||||||||||
| Name | Histamin | ||||||||||||||||||
| Andere Namen |
2-(1H-Imidazol-4-yl)-ethanamin (IUPAC) | ||||||||||||||||||
| Summenformel | C5H9N3 | ||||||||||||||||||
| Kurzbeschreibung |
weißer, hygroskopischer Feststoff | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 111,15 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
83–84 °C | ||||||||||||||||||
| Siedepunkt |
167 °C (1,1 hPa) | ||||||||||||||||||
| Löslichkeit |
leicht löslich in Wasser und Ethanol, unlöslich in Diethylether | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
| ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Histamin (altgr. ἱστός histos ‚Gewebe‘) – in der Nomenklatur: 2-(4-Imidazolyl)-ethylamin – ist ein Naturstoff, der im menschlichen oder tierischen Organismus als Gewebshormon und Neurotransmitter wirkt und auch im Pflanzenreich und in Bakterien weit verbreitet ist. Beim Menschen und anderen Säugetieren spielt Histamin eine zentrale Rolle bei allergischen Reaktionen und ist am Immunsystem, d. h. an der Abwehr körperfremder Stoffe, beteiligt. So dient es als einer der Botenstoffe in der Entzündungsreaktion, um eine Anschwellung des Gewebes zu bewirken. Auch im Magen-Darm-Trakt, bei der Regulation der Magensäureproduktion und der Motilität sowie im Zentralnervensystem bei der Steuerung des Schlaf-Wach-Rhythmus und der Appetitkontrolle wirkt Histamin als wichtiger Regulator. Biochemisch ist es, wie auch Tyramin, Serotonin, Dopamin, Adrenalin, Noradrenalin oder Octopamin, ein biogenes Amin. Es wird durch Abspaltung von Kohlenstoffdioxid (Decarboxylierung) aus der Aminosäure Histidin gebildet und insbesondere in Mastzellen, basophilen Granulozyten und Nervenzellen gespeichert. ⓘ
Eigenschaften
Histaminbase, die als Mineralölmull gewonnen wird, schmilzt bei 83-84 °C. Die Hydrochlorid- und Phosphorsalze bilden weiße, hygroskopische Kristalle und lassen sich leicht in Wasser oder Ethanol, nicht aber in Ether lösen. In wässriger Lösung liegt der Imidazolring von Histamin in zwei tautomeren Formen vor, die sich dadurch unterscheiden, welches der beiden Stickstoffatome protoniert ist. Der Stickstoff, der weiter von der Seitenkette entfernt ist, ist der "tele"-Stickstoff und wird durch ein kleines tau-Zeichen gekennzeichnet, der Stickstoff, der näher an der Seitenkette liegt, ist der "pros"-Stickstoff und wird durch das pi-Zeichen gekennzeichnet. Das tele-Tautomer, Nτ-H-Histamin, wird in Lösung gegenüber dem pros-Tautomer, Nπ-H-Histamin, bevorzugt. ⓘ

Histamin hat zwei basische Zentren, nämlich die aliphatische Aminogruppe und dasjenige Stickstoffatom des Imidazolrings, das nicht bereits ein Proton enthält. Unter physiologischen Bedingungen wird die aliphatische Aminogruppe (mit einem pKa von etwa 9,4) protoniert, während der zweite Stickstoff des Imidazolrings (pKa ≈ 5,8) nicht protoniert wird. Daher wird Histamin normalerweise zu einem einfach geladenen Kation protoniert. Da menschliches Blut leicht basisch ist (mit einem normalen pH-Bereich von 7,35 bis 7,45), ist die vorherrschende Form des Histamins im menschlichen Blut am aliphatischen Stickstoff monoprotisch. Histamin ist ein Monoamin-Neurotransmitter. ⓘ
Synthese und Metabolismus
Histamin wird aus der Decarboxylierung der Aminosäure Histidin gewonnen, eine Reaktion, die durch das Enzym L-Histidin-Decarboxylase katalysiert wird. Es ist ein hydrophiles vasoaktives Amin. ⓘ
Einmal gebildet, wird Histamin entweder gespeichert oder durch seine primären Abbauenzyme, die Histamin-N-Methyltransferase oder die Diaminoxidase, rasch inaktiviert. Im zentralen Nervensystem wird das in die Synapsen freigesetzte Histamin hauptsächlich durch die Histamin-N-Methyltransferase abgebaut, während in anderen Geweben beide Enzyme eine Rolle spielen können. Mehrere andere Enzyme, darunter MAO-B und ALDH2, verarbeiten die unmittelbaren Metaboliten von Histamin weiter, um sie auszuscheiden oder zu recyceln. ⓘ
Auch Bakterien sind in der Lage, Histamin mit Hilfe von Histidindecarboxylase-Enzymen zu produzieren, die nicht mit denen von Tieren verwandt sind. Eine nicht ansteckende Form der lebensmittelbedingten Krankheit, die Scombroid-Vergiftung, ist auf die Histaminproduktion durch Bakterien in verdorbenen Lebensmitteln, insbesondere Fisch, zurückzuführen. Fermentierte Lebensmittel und Getränke enthalten von Natur aus geringe Mengen an Histamin, was auf eine ähnliche Umwandlung durch fermentierende Bakterien oder Hefen zurückzuführen ist. Sake enthält Histamin im Bereich von 20-40 mg/l, Weine im Bereich von 2-10 mg/l. ⓘ
Lagerung und Freisetzung

Histamin kommt in erhöhter Konzentration in den Mastzellen, den basophilen Granulozyten sowie in histaminspeichernden Zellen der Schleimhäute, der Bronchien und des Magen-Darm-Trakts vor. In diesen Zellen wird Histamin in Vesikeln an Heparin gebunden gespeichert. Aus diesen Vesikeln wird Histamin bei IgE-vermittelten allergischen Reaktionen vom „Soforttyp“ (Typ I) oder durch Komplementfaktoren (z. B. bei einem Endotoxin-bedingten Schock) freigesetzt. Neben Gewebshormonen können auch Arzneistoffe, wie beispielsweise Opiate, Muskelrelaxantien sowie Plasmaexpander und Röntgenkontrastmittel, eine Freisetzung von Histamin hervorrufen. Ein weiterer wichtiger Speicherort von Histamin sind die ECL-Zellen der Magenschleimhaut, aus denen Histamin durch Hormone und Gewebshormone, wie z. B. Gastrin, Acetylcholin und PACAP (pituitary adenylate cyclase activating polypeptide) freigesetzt werden kann. ⓘ
Erhöhte Histaminkonzentrationen können auch in Teilen des Zentralnervensystems und der Gehirn-Rückenmarks-Flüssigkeit (Liquor cerebrospinalis) nachgewiesen werden. Die höchste Histaminkonzentration kann dabei im Hypothalamus gefunden werden. Innerhalb des Zentralnervensystems fungiert Histamin auch als Neurotransmitter in histaminergen Neuronen. Eine Freisetzung von Histamin in den synaptischen Spalt wird durch Acetylcholin, Noradrenalin und Histamin selbst über präsynaptische Rezeptoren gehemmt. ⓘ
Das meiste Histamin im Körper wird in Granula in Mastzellen und in weißen Blutkörperchen (Leukozyten), den Basophilen, gebildet. Mastzellen sind besonders zahlreich an Stellen, an denen es zu Verletzungen kommen kann - in der Nase, im Mund und an den Füßen, an inneren Körperoberflächen und in Blutgefäßen. Histamin, das nicht in Mastzellen vorkommt, findet sich in verschiedenen Geweben, unter anderem im Hypothalamus des Gehirns, wo es als Neurotransmitter wirkt. Ein weiterer wichtiger Ort für die Speicherung und Freisetzung von Histamin ist die enterochromaffinähnliche (ECL) Zelle des Magens. ⓘ
Der wichtigste pathophysiologische Mechanismus der Histaminfreisetzung durch Mastzellen und Basophile ist immunologischer Natur. Wenn diese Zellen durch an ihren Membranen gebundene IgE-Antikörper sensibilisiert sind, degranulieren sie, wenn sie dem entsprechenden Antigen ausgesetzt werden. Bestimmte Amine und Alkaloide, darunter Medikamente wie Morphin und Curare-Alkaloide, können Histamin in den Granula verdrängen und seine Freisetzung bewirken. Auch Antibiotika wie Polymyxin können die Histaminfreisetzung stimulieren. ⓘ
Die Histaminfreisetzung erfolgt, wenn Allergene an mastzellgebundene IgE-Antikörper binden. Eine Verringerung der IgE-Überproduktion kann die Wahrscheinlichkeit verringern, dass Allergene genügend freies IgE finden, um eine Mastzellfreisetzung von Histamin auszulösen. ⓘ
Abbau
Histamin wird von Mastzellen als Immunreaktion freigesetzt und später hauptsächlich durch zwei Enzyme abgebaut: Diaminoxidase (DAO), die durch AOC1-Gene kodiert wird, und Histamin-N-Methyltransferase (HNMT), die durch das HNMT-Gen kodiert wird. Das Vorhandensein von Einzelnukleotid-Polymorphismen (SNPs) in diesen Genen wird mit einer Vielzahl von Erkrankungen in Verbindung gebracht, die durch ein überaktives Immunsystem verursacht werden, von Colitis ulcerosa bis hin zu Autismus-Spektrum-Störungen (ASD). Der Histaminabbau ist von entscheidender Bedeutung für die Verhinderung von allergischen Reaktionen auf ansonsten harmlose Substanzen. ⓘ
DAO wird typischerweise in Epithelzellen an der Spitze der Zotten der Dünndarmschleimhaut exprimiert. Eine verminderte DAO-Aktivität wird mit gastrointestinalen Störungen und weit verbreiteten Nahrungsmittelunverträglichkeiten in Verbindung gebracht. Dies ist auf eine erhöhte Histaminabsorption durch die Enterozyten zurückzuführen, wodurch die Histaminkonzentration im Blutkreislauf ansteigt. Eine Studie ergab, dass bei Migränepatienten mit Glutensensitivität ein positiver Zusammenhang mit niedrigeren DAO-Serumspiegeln bestand. Eine niedrige DAO-Aktivität kann noch schwerwiegendere Folgen haben, da Mutationen in den ABP1-Allelen des AOC1-Gens mit Colitis ulcerosa in Verbindung gebracht wurden. Heterozygote oder homozygote rezessive Genotypen an den Allelen rs2052129, rs2268999, rs10156191 und rs1049742 erhöhen das Risiko für eine verminderte DAO-Aktivität. Personen mit einem Genotyp für eine verminderte DAO-Aktivität können histaminreiche Lebensmittel wie Alkohol, fermentierte Lebensmittel und gealterte Lebensmittel meiden, um allergische Reaktionen abzuschwächen. Außerdem sollten sie darauf achten, ob Probiotika, die sie einnehmen, histaminproduzierende Stämme enthalten, und ihren Arzt konsultieren, um eine angemessene Unterstützung zu erhalten. ⓘ
HNMT wird im zentralen Nervensystem exprimiert, wo ein Mangel nachweislich zu aggressivem Verhalten und abnormalen Schlaf-Wach-Zyklen bei Mäusen führt. Da Histamin als Neurotransmitter im Gehirn eine Reihe von neurophysiologischen Funktionen reguliert, hat man sich auf die Entwicklung von Medikamenten konzentriert, die auf die Histaminregulierung abzielen. Yoshikawa et al. untersuchen, wie sich die Polymorphismen C314T, A939G, G179A und T632C auf die enzymatische Aktivität von HNMT und die Pathogenese verschiedener neurologischer Störungen auswirken. Diese Mutationen können sich entweder positiv oder negativ auswirken. Bei einigen ADHS-Patienten hat sich gezeigt, dass sich die Symptome als Reaktion auf Lebensmittelzusatzstoffe und Konservierungsmittel verschlimmern, was zum Teil auf die Freisetzung von Histamin zurückzuführen ist. In einer doppelblinden, placebokontrollierten Crossover-Studie wiesen Kinder mit ADHS, die nach dem Verzehr eines herausfordernden Getränks mit verschlimmerten Symptomen reagierten, mit größerer Wahrscheinlichkeit die HNMT-Polymorphismen T939C und Thr105Ile auf. Die Rolle von Histamin bei Neuroinflammation und Kognition hat es zu einem Untersuchungsziel für viele neurologische Störungen gemacht, darunter auch Autismus-Spektrum-Störungen (ASD). De-novo-Deletionen im HNMT-Gen wurden ebenfalls mit ASD in Verbindung gebracht. ⓘ
Mastzellen erfüllen eine wichtige immunologische Aufgabe, indem sie den Körper vor Antigenen schützen und die Homöostase des Darmmikrobioms aufrechterhalten. Sie wirken wie ein Alarmsignal und lösen Entzündungsreaktionen des Immunsystems aus. Ihre Anwesenheit im Verdauungssystem ermöglicht es ihnen, als frühe Barriere gegen das Eindringen von Krankheitserregern in den Körper zu dienen. Menschen, die unter weit verbreiteten Empfindlichkeiten und allergischen Reaktionen leiden, können an einem Mastzellenaktivierungssyndrom (MCAS) leiden, bei dem übermäßige Mengen an Histamin aus den Mastzellen freigesetzt werden, die nicht ordnungsgemäß abgebaut werden können. Die anormale Histaminfreisetzung kann entweder durch dysfunktionale interne Signale von defekten Mastzellen oder durch die Entwicklung klonaler Mastzellpopulationen durch Mutationen im Tyrosinkinase-Kit verursacht werden. In solchen Fällen ist der Körper möglicherweise nicht in der Lage, ausreichend abbauende Enzyme zu produzieren, um das überschüssige Histamin ordnungsgemäß zu beseitigen. Da die MCAS-Symptomatik so breit gefächert ist, ist die Diagnose schwierig und kann als eine Vielzahl von Krankheiten, einschließlich Reizdarmsyndrom und Fibromyalgie, missverstanden werden. ⓘ
Histamin wird häufig als mögliche Ursache für Krankheiten untersucht, die mit einer Überempfindlichkeit des Immunsystems zusammenhängen. Bei Asthmapatienten wird eine abnorme Histaminrezeptoraktivierung in der Lunge mit Bronchospasmus, Atemwegsobstruktion und übermäßiger Schleimproduktion in Verbindung gebracht. Mutationen im Histaminabbau sind bei Patienten mit einer Kombination aus Asthma und Allergenüberempfindlichkeit häufiger als bei Patienten, die nur an Asthma leiden. HNMT-464 TT und HNMT-1639 TT sind bei Kindern mit allergischem Asthma deutlich häufiger anzutreffen, wobei letzteres bei afroamerikanischen Kindern überrepräsentiert ist. ⓘ

Histamin wird im Körper über zwei verschiedene Wege abgebaut. Insbesondere im Zentralnervensystem erfolgt eine Inaktivierung zum Nτ-Methylhistamin durch das Enzym Histamin-N-Methyltransferase. Nτ-Methylhistamin wird nachfolgend oxidativ über Monoaminooxidasen, Diaminoxidasen und Aldehydoxidasen zur Nτ-Methylimidazolylessigsäure abgebaut. In der Peripherie hingegen spielt die Histaminmethylierung eine untergeordnete Rolle. Hier erfolgt der Abbau vorwiegend über Diaminoxidasen und Aldehydoxidasen zur Imidazolylessigsäure. Diese wird nach Ribosylierung über die Nieren ausgeschieden. ⓘ
Mechanismus der Wirkung
Beim Menschen entfaltet Histamin seine Wirkung vor allem durch Bindung an G-Protein-gekoppelte Histaminrezeptoren, die als H1 bis H4 bezeichnet werden. Seit 2015 wird davon ausgegangen, dass Histamin ligandengesteuerte Chloridkanäle im Gehirn und im Darmepithel aktiviert. ⓘ
| G-Protein-gekoppelter Rezeptor | Ort | Funktion | Quellen |
|---|---|---|---|
| Histamin-H1-Rezeptor |
- ZNS: Ausgedrückt auf den Dendriten der Ausgangsneuronen des histaminergen tuberomammillären Kerns, der in den dorsalen Raphe, den Locus coeruleus und weitere Strukturen projiziert. |
- ZNS: Schlaf-Wach-Zyklus (fördert Wachsein), Körpertemperatur, Nozizeption, endokrine Homöostase, Appetitregulierung, Kognition |
|
| Histamin H2-Rezeptor |
- ZNS: Dorsalstriatum (Nucleus caudatus und Putamen), Großhirnrinde (äußere Schichten), Hippocampusformation, Nucleus dentatus des Kleinhirns |
- ZNS: Nicht nachgewiesen (Hinweis: Die meisten bekannten H2-Rezeptor-Liganden können die Blut-Hirn-Schranke nicht in ausreichenden Konzentrationen überwinden, um neuropsychologische und Verhaltenstests zu ermöglichen) |
|
| Histamin-H3-Rezeptor | Im zentralen Nervensystem und in geringerem Maße im Gewebe des peripheren Nervensystems angesiedelt | Autorezeptor- und Heterorezeptorfunktionen: verminderte Neurotransmitterfreisetzung von Histamin, Acetylcholin, Noradrenalin, Serotonin. Moduliert die Nozizeption, die Magensäuresekretion und die Nahrungsaufnahme. | |
| Histamin-H4-Rezeptor | Befindet sich hauptsächlich auf Basophilen und im Knochenmark. Er wird auch in Thymus, Dünndarm, Milz und Dickdarm exprimiert. | Spielt eine Rolle bei der Chemotaxis von Mastzellen, der Juckreizwahrnehmung, der Zytokinproduktion und -sekretion sowie der viszeralen Überempfindlichkeit. Andere mutmaßliche Funktionen (z. B. Entzündung, Allergie, Kognition usw.) sind noch nicht vollständig geklärt. | |
| Ligandengesteuerter Ionenkanal | Ort | Funktion | Quellen |
| Histamingesteuerter Chloridkanal | Vermutlich: ZNS (Hypothalamus, Thalamus) und Darmepithel | Gehirn: Erzeugt schnelle hemmende postsynaptische Potentiale Darmepithel: Chloridsekretion (verbunden mit sekretorischer Diarrhöe) |
Rolle im Körper
Obwohl Histamin im Vergleich zu anderen biologischen Molekülen klein ist (es enthält nur 17 Atome), spielt es eine wichtige Rolle im Körper. Es ist bekannt, dass es an 23 verschiedenen physiologischen Funktionen beteiligt ist. Dass Histamin an vielen physiologischen Funktionen beteiligt ist, liegt an seinen chemischen Eigenschaften, die ihm eine vielseitige Bindung ermöglichen. Es ist coulombisch (in der Lage, eine Ladung zu tragen), konformationsfähig und flexibel. Dadurch kann es leichter interagieren und binden. ⓘ
Vasodilatation und Senkung des Blutdrucks
Seit mehr als hundert Jahren ist bekannt, dass eine intravenöse Injektion von Histamin einen Blutdruckabfall bewirkt. Der zugrunde liegende Mechanismus betrifft sowohl die Hyperpermeabilität der Gefäße als auch die Gefäßerweiterung. Durch die Bindung von Histamin an die Endothelzellen ziehen sich diese zusammen, wodurch die Durchlässigkeit der Gefäße erhöht wird. Außerdem stimuliert es die Synthese und Freisetzung verschiedener Entspannungsmittel für die glatten Gefäßmuskelzellen, wie Stickstoffmonoxid, vom Endothel abgeleitete hyperpolarisierende Faktoren und andere Verbindungen, was zu einer Erweiterung der Blutgefäße führt. Diese beiden Mechanismen spielen eine Schlüsselrolle in der Pathophysiologie der Anaphylaxie. ⓘ
Auswirkungen auf die Nasenschleimhaut
Eine erhöhte Gefäßpermeabilität führt dazu, dass Flüssigkeit aus den Kapillaren in das Gewebe entweicht, was zu den klassischen Symptomen einer allergischen Reaktion führt: eine laufende Nase und tränende Augen. Allergene können an IgE-beladene Mastzellen in den Schleimhäuten der Nasenhöhle binden. Dies kann zu drei klinischen Reaktionen führen:
- Niesen aufgrund einer histaminassoziierten sensorischen Nervenstimulation
- Übersekretion aus dem Drüsengewebe
- Verstopfung der Nase aufgrund einer Gefäßverengung, die mit einer Vasodilatation und einer erhöhten Kapillardurchlässigkeit einhergeht ⓘ
Schlaf-Wach-Regulierung
Histamin ist ein Neurotransmitter, der von histaminergen Neuronen freigesetzt wird, die aus dem Hypothalamus von Säugetieren hervorgehen. Die Zellkörper dieser Neuronen befinden sich in einem Teil des hinteren Hypothalamus, der als tuberomammillärer Nukleus (TMN) bezeichnet wird. Die Histaminneuronen in dieser Region bilden das Histaminsystem des Gehirns, das weit in das gesamte Gehirn projiziert und axonale Projektionen zum Kortex, zum medialen Vorderhirnbündel, zu anderen Hypothalamuskernen, zum medialen Septum, zum Kern des diagonalen Bandes, zum ventralen tegmentalen Bereich, zur Amygdala, zum Striatum, zur Substantia nigra, zum Hippocampus, zum Thalamus und zu anderen Orten umfasst. Die Histamin-Neuronen im TMN sind an der Regulierung des Schlaf-Wach-Zyklus beteiligt und fördern bei Aktivierung die Erregung. Die neuronale Feuerungsrate der Histamin-Neuronen im TMN ist stark positiv mit dem Erregungszustand einer Person korreliert. Diese Neuronen feuern in Wachphasen schnell, in Phasen der Entspannung/Müdigkeit langsamer und hören während des REM- und NREM-Schlafs (Non-REM) ganz auf zu feuern. ⓘ
H1-Antihistaminika der ersten Generation (d. h. Antagonisten des Histaminrezeptors H1) sind in der Lage, die Blut-Hirn-Schranke zu überwinden und Schläfrigkeit zu erzeugen, indem sie die Histamin-H1-Rezeptoren im Nucleus tuberomammillaris antagonisieren. Die neuere Klasse der H1-Antihistaminika der zweiten Generation durchdringt die Blut-Hirn-Schranke nicht so leicht und verursacht daher weniger wahrscheinlich eine Sedierung, obwohl individuelle Reaktionen, Begleitmedikationen und Dosierung die Wahrscheinlichkeit einer sedierenden Wirkung erhöhen können. Im Gegensatz dazu erhöhen Histamin-H3-Rezeptor-Antagonisten die Wachheit. Ähnlich wie bei der sedierenden Wirkung der H1-Antihistaminika der ersten Generation kann die Unfähigkeit, die Wachsamkeit aufrechtzuerhalten, durch die Hemmung der Histaminbiosynthese oder den Verlust (d. h. die Degeneration oder Zerstörung) von histaminfreisetzenden Neuronen im TMN entstehen. ⓘ
Freisetzung von Magensäure
Enterochromaffin-ähnliche Zellen, die sich in den Magendrüsen des Magens befinden, setzen Histamin frei, das die nahe gelegenen Parietalzellen durch Bindung an den apikalen H2-Rezeptor stimuliert. Die Stimulation der Parietalzellen führt zur Aufnahme von Kohlendioxid und Wasser aus dem Blut, das dann durch das Enzym Kohlensäureanhydrase in Kohlensäure umgewandelt wird. Im Zytoplasma der Parietalzelle dissoziiert die Kohlensäure leicht in Wasserstoff- und Bicarbonat-Ionen. Die Bicarbonat-Ionen diffundieren durch die Basilarmembran zurück in den Blutkreislauf, während die Wasserstoff-Ionen über eine K+/H+-ATPase-Pumpe in das Lumen des Magens gepumpt werden. Die Histaminfreisetzung wird gestoppt, wenn der pH-Wert des Magens zu sinken beginnt. Antagonistische Moleküle wie Ranitidin blockieren den H2-Rezeptor und verhindern die Bindung von Histamin, wodurch die Wasserstoffionensekretion verringert wird. ⓘ
Schützende Wirkungen
Histamin hat nicht nur stimulierende Auswirkungen auf die Neuronen, sondern auch unterdrückende, die vor der Anfälligkeit für Krämpfe, Medikamentensensibilisierung, Überempfindlichkeit gegen Denervierung, ischämische Läsionen und Stress schützen. Es wurde auch vermutet, dass Histamin die Mechanismen steuert, durch die Erinnerungen und Lernprozesse vergessen werden. ⓘ
Erektion und sexuelle Funktion
Libidoverlust und Erektionsstörungen können während der Behandlung mit Histamin-H2-Rezeptor-Antagonisten wie Cimetidin, Ranitidin und Risperidon auftreten. Die Injektion von Histamin in den Schwellkörper bei Männern mit psychogener Impotenz führt bei 74 % von ihnen zu vollständigen oder teilweisen Erektionen. Es wurde vermutet, dass H2-Antagonisten sexuelle Schwierigkeiten verursachen können, indem sie die funktionelle Bindung von Testosteron an seine endogenen Rezeptoren verringern. ⓘ
Schizophrenie
Die Metaboliten von Histamin sind im Liquor von Menschen mit Schizophrenie erhöht, während die Effizienz der H1-Rezeptor-Bindungsstellen verringert ist. Viele atypische antipsychotische Medikamente haben die Wirkung, die Histaminproduktion zu erhöhen, da der Histaminspiegel bei Menschen mit dieser Störung unausgewogen zu sein scheint. ⓘ
Multiple Sklerose
Die Histamintherapie zur Behandlung von Multipler Sklerose wird derzeit untersucht. Es ist bekannt, dass die verschiedenen H-Rezeptoren unterschiedliche Auswirkungen auf die Behandlung dieser Krankheit haben. Die H1- und H4-Rezeptoren haben sich in einer Studie als kontraproduktiv für die Behandlung von MS erwiesen. Es wird angenommen, dass die H1- und H4-Rezeptoren die Durchlässigkeit der Blut-Hirn-Schranke erhöhen und damit das Eindringen unerwünschter Zellen in das zentrale Nervensystem fördern. Dies kann zu Entzündungen und einer Verschlimmerung der MS-Symptome führen. Es wird angenommen, dass die H2 und H3-Rezeptoren bei der Behandlung von MS-Patienten hilfreich sind. Es hat sich gezeigt, dass Histamin die Differenzierung der T-Zellen unterstützt. Dies ist wichtig, da das körpereigene Immunsystem bei MS die körpereigenen Myelinscheiden der Nervenzellen angreift (was zum Verlust der Signalfunktion und schließlich zur Degeneration der Nerven führt). Indem die T-Zellen bei der Differenzierung unterstützt werden, ist es weniger wahrscheinlich, dass die T-Zellen körpereigene Zellen angreifen und stattdessen Eindringlinge attackieren. ⓘ
Störungen
Als integraler Bestandteil des Immunsystems kann Histamin bei Störungen des Immunsystems und Allergien eine Rolle spielen. Mastozytose ist eine seltene Krankheit, bei der es zu einer Vermehrung von Mastzellen kommt, die übermäßig viel Histamin produzieren. ⓘ
Bei manchen Menschen kann sich infolge einer Histaminintoleranz übermäßiges Histamin aus der Nahrung im Körper ansammeln. Dies kann zu Symptomen wie Nesselsucht, juckender oder geröteter Haut, geröteten Augen, Schwellungen im Gesicht, laufender Nase und Verstopfung, Kopfschmerzen oder Asthmaanfällen führen. ⓘ
Geschichte
Die Geschichte der Erforschung des Histamins begann im Jahr 1907 mit seiner Synthese als chemische Kuriosität durch die deutschen Chemiker Adolf Windaus und W. Vogt. Bereits drei Jahre später gelang Henry H. Dale und George Barger der Nachweis von Histamin im Mutterkorn und somit die Entdeckung von Histamin als Naturstoff. Im gleichen Jahr wiesen Henry H. Dale und P. P. Laidlaw Histamin als körpereigene Substanz nach. Dale und Laidlaw klärten gleichzeitig einige grundlegende Funktionen des Histamins auf. Die Biosynthese des Histamins aus der Aminosäure Histidin konnte durch Dankwart Ackermann ebenfalls 1910 aufgeklärt werden. ⓘ
Daniel Bovet und Anne-Marie Staub entdeckten im Jahr 1937 erste Substanzen, die die Wirkung von Histamin hemmen (Antihistaminika). Bereits fünf Jahre später wurden mit Phenbenzamin und Mepyramin die ersten Antihistaminika in der Therapie eingesetzt. Anfang der 1950er Jahre wurden von der französischen Pharmafirma Rhône-Poulenc im Rahmen der Anti-Histaminforschung die ersten Neuroleptika entwickelt. Im Jahr 1972 gelang James W. Black und Mitarbeitern die Unterscheidung zwischen H1- und H2-Rezeptoren. Als weitere Subtypen des Histaminrezeptors wurden 1983 der H3-Rezeptor durch Jean-Michel Arrang mit Hilfe pharmakologischer Methoden und 2000 der H4-Rezeptor durch Entschlüsselung des menschlichen Genoms entdeckt. ⓘ
In der medizinischen Literatur werden gelegentlich die Bezeichnungen "H-Substanz" oder "Substanz H" für Histamin oder eine hypothetische histaminähnliche diffusionsfähige Substanz verwendet, die bei allergischen Reaktionen der Haut und bei Entzündungsreaktionen des Gewebes freigesetzt wird. ⓘ
Funktion
Im menschlichen Organismus besitzt Histamin vielfältige Funktionen, wobei insbesondere seine Beteiligung an Abwehrreaktionen im Vordergrund steht. Auf molekularer Ebene vermittelt Histamin seine Funktionen über eine Aktivierung der Histamin-Rezeptoren H1, H2, H3 und H4, die zur Familie der G-Protein-gekoppelten Rezeptoren gehören. ⓘ
Abwehrreaktionen
Wichtige Mitwirkungen des Histamins sind seine Funktion an der Abwehr körperfremder Stoffe und seine pathologische Beteiligung an der Symptomatik von Allergien und Asthma. Ebenso ist Histamin eine der Mediatorsubstanzen bei Entzündungen und Verbrennungen. Hierbei führt Histamin zu Jucken, Schmerz und Kontraktion der glatten Muskulatur (beispielsweise in den Bronchien). Es bewirkt eine erhöhte Permeabilität der Gefäßwände kleiner Blutgefäße und führt so zur Nesselsucht. An diesem Prozess ist auch eine durch Histamin induzierte Aktivierung des Transkriptionsfaktors NF-κB und eine damit verbundene vermehrte Freisetzung weiterer Entzündungsmediatoren beteiligt. Histamin führt ebenfalls zu einer Freisetzung von Adrenalin aus den Nebennieren. Diese Effekte werden insbesondere über eine Aktivierung von H1-Rezeptoren vermittelt. ⓘ
Histamin wirkt chemotaktisch auf verschiedene, an der Abwehr körperfremder Stoffe beteiligte Zellen, beispielsweise die eosinophilen Granulozyten und die T-Zellen. Für diese Effekte wird vor allem eine Aktivierung von H4-Rezeptoren verantwortlich gemacht. ⓘ
Anders als beim Menschen spielt Histamin bei Hunden und Katzen bei der Entstehung von Juckreiz nur eine untergeordnete Rolle. ⓘ
Magen-Darm-Trakt
Im Magen-Darm-Trakt ist Histamin an der Regulation der Magensäureproduktion und (über seine erregende Wirkung auf die glatte Muskulatur) der Motilität beteiligt. Die durch Histamin über eine Aktivierung von H2-Rezeptoren vermittelte Steigerung der Magensäureproduktion kann dabei als ein Bestandteil einer Histamin-vermittelten Abwehrreaktion interpretiert werden. ⓘ
Herz-Kreislaufsystem
Ebenfalls als Bestandteil einer Abwehrreaktion kann die Wirkung von Histamin auf die Blutgefäße interpretiert werden. Es kontrahiert H1-Rezeptor-vermittelt die großen Blutgefäße (Durchmesser von mehr als 80 µm) und führt zu einer Erweiterung kleinerer Blutgefäße verbunden mit Hautrötung. Am Herzen besitzt Histamin über eine Aktivierung von H2-Rezeptoren eine positiv inotrope (die Schlagkraft steigernde) und positiv chronotrope (die Schlagfrequenz steigernde) Wirkung. ⓘ
Zentralnervensystem
Im Zentralnervensystem ist Histamin über eine Aktivierung von H1-Rezeptoren an der Auslösung des Erbrechens sowie der Regulation des Schlaf-Wach-Rhythmus beteiligt. Basierend auf tierexperimentellen Befunden wird eine antidepressive, antikonvulsive und appetitzügelnde Wirkung des Histamins diskutiert. Ebenso scheint es an der Regulation der Körpertemperatur, der zentralen Kontrolle des Blutdrucks und der Schmerzempfindung beteiligt zu sein. Über präsynaptische Rezeptoren (insbesondere H3-Rezeptoren) besitzt Histamin durch Hemmung der Neurotransmitterfreisetzung im Zentralnervensystem und im peripheren Nervensystem einen regulatorischen Einfluss auf noradrenerge, serotoninerge, cholinerge, dopaminerge und glutaminerge Neuronen. Histamin beeinflusst somit indirekt die Wirkung dieser Neurotransmitter. ⓘ
Aktuell laufen Studien in Europa mit Histamin als Arzneistoff mit wachmachender (vigilanzsteigernder) Wirkung. Zum Einsatz könnte das Medikament in einiger Zeit z. B. bei krankhaften Schlaf-Wach-Regulationsstörungen kommen. ⓘ
Toxikologie
Die Verträglichkeitsgrenze von Histamin liegt bei erwachsenen Primaten ungefähr bei 10 mg. Größere Mengen Histamin führen zu einer Vergiftung, die durch akute Beschwerden wie Atemnot, Blutdruckabfall, Rötung der Haut, Nesselausschlag, Übelkeit, Erbrechen, Kopfschmerzen und Durchfall gekennzeichnet ist. Eine Menge von 100 mg Histamin führt bereits zu deutlichen Vergiftungserscheinungen. Die Verträglichkeitsgrenze könnte bei Patienten mit einer Histamin-Intoleranz deutlich herabgesetzt sein. Die Einnahme größerer Mengen an histaminhaltigen Nahrungsmitteln, z. B. bei einer bestimmten Form der Fischvergiftung, kann dementsprechend ebenso zu Vergiftungssymptomen führen wie die gleichzeitige Einnahme von MAO-Hemmern und tyramin- oder histaminhaltigen Lebensmitteln wie Fisch, Fleisch, Käse, Gemüse und Wein. ⓘ
Im Tierversuch zeigte Histamin bei verschiedenen Tierarten (Hund, Maus, Meerschweinchen, Ratte, Hase) negative Effekte auf die Lunge und das gesamte Atmungssystem. Bei Hunden führten intravenöse Gaben von 7 mg/kg zu Störungen bei der Herzfunktion, subkutane Dosen führten ab 28,5 mg/kg zu Durchfall und Koma. ⓘ
Verwendung
Histamin wird zur medizinischen Diagnostik, v. a. von Atopien und Allergien, sowie im inhalativen Provokationstest und zur Positivkontrolle beim Intrakutantest eingesetzt. Darüber hinaus werden auch Arzneistoffe, welche die Freisetzung von Histamin aus Mastzellen (Mastzellstabilisatoren) oder die Wirkung von Histamin an Histaminrezeptoren blockieren (Antihistaminika), in der Therapie verwendet. Mit Mastzellenstabilisatoren (beispielsweise Cromoglicinsäure (DNCG), Nedocromil oder Lodoxamid) und mit H1-Antihistaminika (z. B. Diphenhydramin, Loratadin oder Cetirizin) werden allergische Beschwerden symptomatisch behandelt. Außerdem werden Schlafstörungen, Angststörungenen, Übelkeit und Erbrechen mit H1-Antihistaminika behandelt. H2-Antihistaminika (wie Cimetidin, Ranitidin oder Famotidin) sind als Hemmer der Magensäureproduktion bedeutende Antazida. ⓘ
Ein Analogon des Histamins ist das vasodilatatorische Betahistin, welches als Antiemetikum und Antivertiginosum (also gegen Schwindel) v. a. bei Morbus Menière und Hydrops cochleae eingesetzt wird. ⓘ
Verwendung als Arzneimittel
Histamin wird unter dem Handelsnamen Ceplene in der Krebsimmuntherapie als Injektionslösung in Kombination mit Interleukin-2 als Arzneistoff zur Behandlung akuter myeloischer Leukämie (AML) eingesetzt, einer seltenen Krebserkrankung, von der die weißen Blutkörperchen betroffen sind. Da nur wenige Patienten unter dieser Krebsform leiden, wurde Ceplene 2005 als Arzneimittel für seltene Leiden („Orphan-Arzneimittel“) ausgewiesen. Die arzneimittelrechtliche Zulassung folgte 2008. ⓘ
Klinische Angaben
Anwendungsgebiete (Indikationen)
Histamin ist zur Behandlung der akuten myeloischen Leukämie in Kombination mit Interleukin-2 bei Krebspatienten in der ersten Remission zugelassen. Die Zulassung beschränkt sich auf erwachsene Patienten, wobei eine Wirksamkeit bei Patienten über 60 Jahre nicht vollständig nachgewiesen wurde. ⓘ
Gegenanzeigen (Kontraindikationen)
Als absolute Kontraindikation für die Anwendung von Histamin in der Krebsimmuntherapie gelten Überempfindlichkeitsreaktionen, mittelschwere und schwere Herzinsuffizienz (NYHA III und IV) sowie die gleichzeitige systemische Anwendung von Steroiden, des Blutdrucksenkers Clonidin oder magensäuresekretionshemmender Arzneimittel aus der Gruppe der H2-Antihistaminika. Ebenso ist die Krebsimmuntherapie mit Histamin und Interleukin-2 bei Patienten mit einer allogenen Stammzelltransplantation kontraindiziert. Da in präklinischen Studien an Nagetieren nach einer Anwendung von Histamin Hinweise auf schädigende Wirkungen auf die Nachkommen gefunden wurden, ist die Anwendung bei Schwangeren und Stillenden kontraindiziert. ⓘ
Histamin als Abwehrstoff

Histamin wird in einigen Pflanzen und Tieren auch als Abwehrsubstanz produziert und gespeichert. Beispielsweise speichert die Große Brennnessel in ihren Brennhaaren neben anderen Substanzen Histamin, das bei Berührung abgegeben wird. Die Heuschrecke Poekilocerus bufonius (Pyrgomorphidae) gibt bei Gefahr ein Sekret ab, das neben Cardenoliden ca. 1 % Histamin enthält. Histamin ist auch im Hautdrüsensekret der Südfrösche enthalten. Darüber hinaus können tierische und pflanzliche Abwehrstoffe, wie beispielsweise das Mastzelldegranulierende Peptid (MCD-Peptid) des Bienengifts, Histamin aus den Mastzellen höherer Tiere freisetzen und somit eine Entzündungsreaktion auslösen. ⓘ



