Insulin

Insulin (/ˈɪn.sjʊ.lɪn/, von lateinisch insula, "Insel") ist ein Peptidhormon, das von den Betazellen der Bauchspeicheldrüseninseln produziert wird und beim Menschen durch das INS-Gen kodiert wird. Es gilt als das wichtigste anabole Hormon des Körpers. Es reguliert den Stoffwechsel von Kohlenhydraten, Fetten und Proteinen, indem es die Aufnahme von Glukose aus dem Blut in Leber-, Fett- und Skelettmuskelzellen fördert. In diesen Geweben wird die aufgenommene Glukose entweder über die Glykogenese in Glykogen oder über die Lipogenese in Fette (Triglyceride) umgewandelt, oder, im Falle der Leber, in beides. Die Produktion und Sekretion von Glukose durch die Leber wird durch hohe Insulinkonzentrationen im Blut stark gehemmt. Das zirkulierende Insulin beeinflusst auch die Synthese von Proteinen in einer Vielzahl von Geweben. Es ist also ein anaboles Hormon, das die Umwandlung kleiner Moleküle im Blut in große Moleküle in den Zellen fördert. Niedrige Insulinspiegel im Blut haben den gegenteiligen Effekt, indem sie den weit verbreiteten Katabolismus, insbesondere den Abbau von Körperfettreserven, fördern. ⓘ
Die Betazellen reagieren empfindlich auf den Blutzuckerspiegel, so dass sie bei einem hohen Glukosespiegel Insulin ins Blut absondern und bei einem niedrigen Glukosespiegel die Insulinausschüttung hemmen. Insulin fördert die Glukoseaufnahme und den Stoffwechsel in den Zellen und senkt so den Blutzuckerspiegel. Die benachbarten Alphazellen, die sich an den Betazellen orientieren, geben Glukagon in umgekehrter Weise ins Blut ab: eine erhöhte Sekretion bei niedrigem Blutzuckerspiegel und eine verringerte Sekretion bei hoher Glukosekonzentration. Glucagon erhöht den Blutzuckerspiegel, indem es die Glykogenolyse und die Gluconeogenese in der Leber stimuliert. Die Sekretion von Insulin und Glukagon in das Blut als Reaktion auf die Blutglukosekonzentration ist der wichtigste Mechanismus der Glukosehomöostase. ⓘ
Eine verringerte oder fehlende Insulinaktivität führt zu Diabetes mellitus, einem Zustand mit hohem Blutzuckerspiegel (Hyperglykämie). Es gibt zwei Arten dieser Krankheit. Bei Diabetes mellitus Typ 1 werden die Betazellen durch eine Autoimmunreaktion zerstört, so dass kein Insulin mehr synthetisiert oder in das Blut abgegeben werden kann. Bei Diabetes mellitus Typ 2 ist die Zerstörung der Betazellen weniger stark ausgeprägt als bei Typ 1 und ist nicht auf einen Autoimmunprozess zurückzuführen. Stattdessen kommt es zu einer Anhäufung von Amyloid in den Inseln der Bauchspeicheldrüse, wodurch wahrscheinlich deren Anatomie und Physiologie gestört werden. Die Pathogenese des Typ-2-Diabetes ist noch nicht ganz geklärt, aber es ist bekannt, dass eine verminderte Population von Beta-Zellen in den Inselzellen, eine verminderte Sekretionsfunktion der überlebenden Beta-Zellen in den Inselzellen und eine Insulinresistenz im peripheren Gewebe eine Rolle spielen. Typ-2-Diabetes ist durch eine erhöhte Glukagonsekretion gekennzeichnet, die nicht von der Blutzuckerkonzentration abhängt und auf diese nicht reagiert. Als Reaktion auf den Blutzuckerspiegel wird jedoch weiterhin Insulin ins Blut ausgeschüttet. Infolgedessen sammelt sich die Glukose im Blut an. ⓘ
Das menschliche Insulinprotein besteht aus 51 Aminosäuren und hat eine Molekularmasse von 5808 Da. Es ist ein Heterodimer aus einer A-Kette und einer B-Kette, die durch Disulfidbindungen miteinander verbunden sind. Die Struktur des Insulins variiert leicht zwischen den einzelnen Tierarten. Insulin aus tierischen Quellen unterscheidet sich aufgrund dieser Unterschiede in seiner Wirksamkeit (in Bezug auf die Auswirkungen auf den Kohlenhydratstoffwechsel) etwas vom menschlichen Insulin. Schweineinsulin ist dem menschlichen Insulin besonders ähnlich und wurde häufig zur Behandlung von Typ-1-Diabetikern eingesetzt, bevor Humaninsulin in großen Mengen durch rekombinante DNA-Technologien hergestellt werden konnte. ⓘ
Insulin war das erste Peptidhormon, das entdeckt wurde. Frederick Banting und Charles Herbert Best, die im Labor von J. J. R. Macleod an der Universität von Toronto arbeiteten, isolierten 1921 als erste Insulin aus der Bauchspeicheldrüse von Hunden. Frederick Sanger sequenzierte 1951 die Aminosäurestruktur, womit Insulin das erste Protein war, das vollständig sequenziert wurde. Die Kristallstruktur des Insulins im festen Zustand wurde 1969 von Dorothy Hodgkin bestimmt. Insulin ist auch das erste Protein, das chemisch synthetisiert und durch rekombinante DNA-Technologie hergestellt wurde. Es steht auf der WHO-Modellliste der unentbehrlichen Arzneimittel, den wichtigsten Medikamenten, die in einem grundlegenden Gesundheitssystem benötigt werden. ⓘ
| Insulin ⓘ | ||
|---|---|---|
| ||
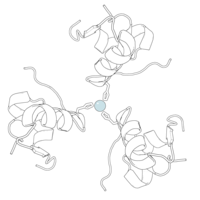
| Zwei Modelldarstellungen des Insulinmoleküls. Links das einfache Molekül (Monomer) als ein Kalottenmodell aus dem die Oberflächenform hervorgeht. Rechts das sechsfache Molekül (Hexamer) als so genanntes Bändermodell, bei dem die innere Struktur deutlich wird. Bei letzterem sind α-Helices durch Schrauben und β-Faltblätter durch Pfeile dargestellt. | ||
|
Vorhandene Strukturdaten: 1ai0, 3ins, 4ins, 6ins, 7ins, 9ins | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 5,8 kDa / 51 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Heterodimer (21 + 30 aa) | |
| Präkursor | Proinsulin | |
| Bezeichner | ||
| Gen-Name | INS | |
| Externe IDs | ||
| Arzneistoffangaben | ||
| ATC-Code | A10AB01 | |
| DrugBank | DB00030 | |
| Vorkommen | ||
| Homologie-Familie | CLU_140421_1_0 | |
| Übergeordnetes Taxon | Wirbeltiere | |
| Orthologe | ||
| Mensch | Maus | |
| Entrez | 3630 | 16334 |
| Ensembl | ENSG00000129965 | ENSMUSG00000000215 |
| UniProt | P01308 | Q5EEX1 |
| Refseq (mRNA) | NM_000207 | NM_008387 |
| Refseq (Protein) | NP_000198 | NP_032413 |
| Genlocus | Chr 11: 2.14 – 2.14 Mb | Chr 7: 142.49 – 142.49 Mb |
| PubMed-Suche | 3630 | 16334 |
Insulin (andere Namen: Insulinum, Insulinhormon, Inselhormon) ist ein für alle Wirbeltiere lebenswichtiges Proteohormon (Polypeptidhormon), das in den β-Zellen der Bauchspeicheldrüse gebildet wird. Diese spezialisierten Zellen befinden sich in den Langerhans-Inseln. Von diesen Inseln leitet sich auch der Name „Insulin“ ab (von lateinisch insula „Insel“). Insulin ist an der Regulation des Stoffwechsels, insbesondere dem der Kohlenhydrate, beteiligt. Insulin senkt den Blutzuckerspiegel, indem es Körperzellen dazu anregt, Glucose aus dem Blut aufzunehmen. ⓘ
Evolution und Artenvielfalt
Insulin ist möglicherweise vor mehr als einer Milliarde Jahren entstanden. Die molekularen Ursprünge des Insulins reichen mindestens bis zu den einfachsten einzelligen Eukaryonten zurück. Neben den Tieren sind insulinähnliche Proteine auch aus dem Reich der Pilze und der Protista bekannt. ⓘ
Insulin wird bei den meisten Wirbeltieren von den Betazellen der Pankreasinseln und bei einigen Teleostfischen vom Brockmann-Körper produziert. Die Kegelschnecken Conus geographus und Conus tulipa, giftige Meeresschnecken, die Jagd auf kleine Fische machen, verwenden modifizierte Formen von Insulin in ihren Giftcocktails. Das Insulintoxin, das in seiner Struktur dem Insulin der Fische ähnlicher ist als dem nativen Insulin der Schnecken, bremst die Beutefische, indem es ihren Blutzuckerspiegel senkt. ⓘ
Herstellung

Insulin wird bei Säugetieren ausschließlich in den Betazellen der Pankreasinseln und bei einigen Fischen im Brockmann-Körper produziert. Das menschliche Insulin wird vom INS-Gen auf Chromosom 11 produziert. Nagetiere haben zwei funktionsfähige Insulin-Gene; das eine ist das Homolog der meisten Säugetiergene (Ins2), das andere ist eine retroposierte Kopie, die die Promotorsequenz enthält, der aber ein Intron fehlt (Ins1). Die Transkription des Insulin-Gens steigt als Reaktion auf einen erhöhten Blutzuckerspiegel. Dies wird in erster Linie durch Transkriptionsfaktoren gesteuert, die Enhancer-Sequenzen in den ~400 Basenpaaren vor der Transkriptionsstartstelle des Gens binden. ⓘ
Die wichtigsten Transkriptionsfaktoren, die die Insulinsekretion beeinflussen, sind PDX1, NeuroD1 und MafA. ⓘ
Bei niedrigem Blutzuckerspiegel befindet sich PDX1 (Pankreas- und Duodenal-Homeobox-Protein 1) aufgrund der Interaktion mit HDAC1 und 2 in der Kernperipherie, was zu einer Herunterregulierung der Insulinsekretion führt. Ein Anstieg des Blutzuckerspiegels bewirkt eine Phosphorylierung von PDX1, was dazu führt, dass es eine Translokation in den Zellkern erfährt und das A3-Element innerhalb des Insulinpromotors bindet. Nach der Translokation interagiert es mit den Koaktivatoren HAT p300 und SETD7. PDX1 beeinflusst die Histonmodifikationen durch Acetylierung und Deacetylierung sowie Methylierung. Es soll auch Glucagon unterdrücken. ⓘ
NeuroD1, auch bekannt als β2, reguliert die Insulinexozytose in β-Zellen des Pankreas, indem es direkt die Expression von Genen induziert, die an der Exozytose beteiligt sind. Es ist im Zytosol lokalisiert, wird aber als Reaktion auf hohe Glukose durch OGT glykosyliert und/oder durch ERK phosphoryliert, was eine Translokation in den Zellkern bewirkt. Im Zellkern heterodimerisiert β2 mit E47, bindet an das E1-Element des Insulinpromotors und rekrutiert den Co-Aktivator p300, der β2 acetyliert. Es ist in der Lage, bei der Aktivierung des Insulin-Gens auch mit anderen Transkriptionsfaktoren zu interagieren. ⓘ
MafA wird bei niedrigem Blutzuckerspiegel durch Proteasomen abgebaut. Erhöhte Glukosespiegel führen zur Glykosylierung eines unbekannten Proteins. Dieses Protein wirkt auf unbekannte Weise als Transkriptionsfaktor für MafA und MafA wird aus der Zelle transportiert. MafA wird dann zurück in den Zellkern verlagert, wo es an das C1-Element des Insulinpromotors bindet. ⓘ
Diese Transkriptionsfaktoren wirken synergistisch und in einer komplexen Anordnung. Ein erhöhter Blutzuckerspiegel kann nach einiger Zeit die Bindungskapazitäten dieser Proteine zerstören und damit die Insulinausschüttung verringern, was zu Diabetes führt. Die verringerten Bindungsaktivitäten können durch glukosebedingten oxidativen Stress vermittelt werden, und Antioxidantien sollen die verringerte Insulinsekretion in glukotoxischen β-Zellen des Pankreas verhindern. Stresssignalmoleküle und reaktive Sauerstoffspezies hemmen das Insulin-Gen, indem sie die Cofaktoren, die die Transkriptionsfaktoren binden, und die Transkriptionsfaktoren selbst beeinträchtigen. ⓘ
Mehrere regulatorische Sequenzen in der Promotorregion des menschlichen Insulin-Gens binden an Transkriptionsfaktoren. Im Allgemeinen binden die A-Boxen an Pdx1-Faktoren, die E-Boxen an NeuroD, die C-Boxen an MafA und die cAMP-Response-Elemente an CREB. Es gibt auch Silencer, die die Transkription hemmen. ⓘ
Synthese

Insulin wird als inaktives Vorläufermolekül, ein 110 Aminosäuren langes Protein namens "Präproinsulin", synthetisiert. Präproinsulin wird direkt in das raue endoplasmatische Retikulum (RER) übersetzt, wo sein Signalpeptid durch Signalpeptidase entfernt wird, um "Proinsulin" zu bilden. Bei der Faltung des Proinsulins werden die gegenüberliegenden Enden des Proteins, die so genannte "A-Kette" und die "B-Kette", durch drei Disulfidbindungen miteinander verschmolzen. Das gefaltete Proinsulin durchläuft dann den Golgi-Apparat und wird in spezielle sekretorische Vesikel verpackt. Im Granulum wird das Proinsulin durch die Proprotein-Convertase 1/3 und die Proprotein-Convertase 2 gespalten, wobei der mittlere Teil des Proteins, das so genannte "C-Peptid", entfernt wird. Schließlich entfernt die Carboxypeptidase E zwei Aminosäurepaare von den Enden des Proteins, wodurch aktives Insulin entsteht - die Insulin-A- und -B-Ketten, die nun durch zwei Disulfidbindungen verbunden sind. ⓘ
Das so entstandene reife Insulin ist in reifen Granula verpackt und wartet auf Stoffwechselsignale (wie Leucin, Arginin, Glukose und Mannose) und die Stimulation des Vagusnervs, um aus der Zelle in den Blutkreislauf exozytiert zu werden. ⓘ
Es ist erwiesen, dass Insulin und seine verwandten Proteine im Gehirn produziert werden, und ein verminderter Spiegel dieser Proteine wird mit der Alzheimer-Krankheit in Verbindung gebracht. ⓘ
Die Insulinfreisetzung wird auch durch die Stimulation des Beta-2-Rezeptors angeregt und durch die Stimulation des Alpha-1-Rezeptors gehemmt. Darüber hinaus wirken Cortisol, Glucagon und Wachstumshormon der Wirkung von Insulin in Stresssituationen entgegen. Insulin hemmt auch die Freisetzung von Fettsäuren durch die hormonsensitive Lipase im Fettgewebe. ⓘ
Aufbau

Entgegen der anfänglichen Annahme, dass Hormone im Allgemeinen kleine chemische Moleküle sind, erwies sich Insulin als das erste Peptidhormon, dessen Struktur bekannt war, als recht groß. Ein einzelnes Protein (Monomer) des menschlichen Insulins besteht aus 51 Aminosäuren und hat eine Molekularmasse von 5808 Da. Die Molekularformel von Humaninsulin lautet C257H383N65O77S6. Es ist eine Kombination aus zwei Peptidketten (Dimer), der A-Kette und der B-Kette, die durch zwei Disulfidbindungen miteinander verbunden sind. Die A-Kette besteht aus 21 Aminosäuren, während die B-Kette aus 30 Resten besteht. Die verbindenden (interchain) Disulfidbindungen werden an Cysteinresten zwischen den Positionen A7-B7 und A20-B19 gebildet. Innerhalb der A-Kette gibt es eine zusätzliche (ketteninterne) Disulfidbindung zwischen den Cysteinresten an den Positionen A6 und A11. Die A-Kette weist zwei α-helikale Regionen an A1-A8 und A12-A19 auf, die antiparallel zueinander sind, während die B-Kette eine zentrale α-Helix (die die Reste B9-B19 bedeckt) aufweist, die von der Disulfidbindung auf beiden Seiten und zwei β-Sheets (die B7-B10 und B20-B23 bedecken) flankiert wird. ⓘ
Die Aminosäuresequenz des Insulins ist stark konserviert und variiert nur geringfügig zwischen den Arten. Rinderinsulin unterscheidet sich vom menschlichen Insulin nur in drei Aminosäureresten, das Schweineinsulin in einem. Selbst das Insulin einiger Fischarten ist dem menschlichen Insulin ähnlich genug, um beim Menschen klinisch wirksam zu sein. Das Insulin einiger wirbelloser Tiere ähnelt in seiner Sequenz dem menschlichen Insulin und hat ähnliche physiologische Wirkungen. Die starke Homologie in der Insulinsequenz verschiedener Arten deutet darauf hin, dass sie über einen großen Teil der Evolutionsgeschichte der Tiere hinweg erhalten geblieben ist. Das C-Peptid des Proinsulins unterscheidet sich jedoch sehr viel stärker zwischen den Arten; es ist ebenfalls ein Hormon, allerdings ein sekundäres. ⓘ
Insulin wird im Körper als Hexamer (eine Einheit aus sechs Insulinmolekülen) produziert und gespeichert, während die aktive Form das Monomer ist. Das Hexamer hat eine Größe von etwa 36000 Da. Die sechs Moleküle sind als drei dimere Einheiten miteinander verbunden und bilden ein symmetrisches Molekül. Ein wichtiges Merkmal ist das Vorhandensein von Zinkatomen (Zn2+) auf der Symmetrieachse, die von drei Wassermolekülen und drei Histidinresten an Position B10 umgeben sind. ⓘ
Das Hexamer ist eine inaktive, langzeitstabile Form, die dazu dient, das hochreaktive Insulin geschützt, aber dennoch leicht verfügbar zu halten. Die Hexamer-Monomer-Umwandlung ist einer der zentralen Aspekte von Insulinformulierungen zur Injektion. Das Hexamer ist weitaus stabiler als das Monomer, was aus praktischen Gründen wünschenswert ist; das Monomer ist jedoch ein sehr viel schneller reagierendes Arzneimittel, da die Diffusionsgeschwindigkeit umgekehrt proportional zur Partikelgröße ist. Ein schnell reagierendes Medikament bedeutet, dass Insulininjektionen nicht stundenlang vor den Mahlzeiten erfolgen müssen, was wiederum Diabetikern mehr Flexibilität in ihren Tagesplänen bietet. Insulin kann aggregieren und fibrilläre, ineinander verschachtelte Betafasern bilden. Dies kann zu einer Injektionsamyloidose führen und verhindert die Speicherung von Insulin über längere Zeiträume. ⓘ
Funktion
Ausschüttung
Die Betazellen in den Langerhans-Inseln setzen Insulin in zwei Phasen frei. Die erste Phase wird als Reaktion auf einen erhöhten Blutzuckerspiegel rasch ausgelöst und dauert etwa 10 Minuten. Die zweite Phase ist eine anhaltende, langsame Freisetzung von neu gebildeten Bläschen, die unabhängig vom Zucker ausgelöst wird und nach 2 bis 3 Stunden ihren Höhepunkt erreicht. Die beiden Phasen der Insulinfreisetzung deuten darauf hin, dass die Insulinkörnchen in verschiedenen Populationen oder "Pools" vorhanden sind. In der ersten Phase der Insulinexozytose werden die meisten der für die Exozytose prädisponierten Granula nach der Kalziuminternalisierung freigesetzt. Dieser Pool wird als Readily Releasable Pool (RRP) bezeichnet. Die RRP-Granula machen 0,3-0,7 % der gesamten insulinhaltigen Granula-Population aus und befinden sich in unmittelbarer Nähe der Plasmamembran. Während der zweiten Phase der Exozytose benötigen die Insulinkörnchen eine Mobilisierung der Körnchen zur Plasmamembran und eine vorherige Vorbereitung, damit sie freigesetzt werden können. Die zweite Phase der Insulinfreisetzung wird also von der Geschwindigkeit bestimmt, mit der die Granula für die Freisetzung vorbereitet werden. Dieser Pool wird als Reserve-Pool (RP) bezeichnet. Der RP wird langsamer freigesetzt als der RRP (RRP: 18 Körnchen/min; RP: 6 Körnchen/min). Eine verminderte Insulinfreisetzung in der ersten Phase kann der früheste nachweisbare Betazelldefekt sein, der das Auftreten von Typ-2-Diabetes vorhersagt. Die Erstphasenfreisetzung und die Insulinsensitivität sind unabhängige Prädiktoren für Diabetes. ⓘ
Die Freisetzung in der ersten Phase wird wie folgt beschrieben:
- Glukose gelangt über den Glukosetransporter GLUT 2 in die β-Zellen. Bei niedrigem Blutzuckerspiegel gelangt nur wenig Glukose in die β-Zellen; bei hohen Blutzuckerkonzentrationen gelangen große Mengen an Glukose in diese Zellen.
- Die Glukose, die in die β-Zelle gelangt, wird von der Glukokinase (Hexokinase IV) zu Glukose-6-Phosphat (G-6-P) phosphoryliert, das von G-6-P nicht in der Weise gehemmt wird, wie die Hexokinasen in anderen Geweben (Hexokinase I - III) von diesem Produkt betroffen sind. Dies bedeutet, dass die intrazelluläre G-6-P-Konzentration proportional zur Blutzuckerkonzentration bleibt.
- Glukose-6-Phosphat gelangt in den glykolytischen Stoffwechselweg und dann über die Pyruvat-Dehydrogenase-Reaktion in den Krebs-Zyklus, wo durch die Oxidation von Acetyl-CoA (dem Substrat des Krebs-Zyklus) mehrere energiereiche ATP-Moleküle erzeugt werden, was zu einem Anstieg des ATP:ADP-Verhältnisses in der Zelle führt.
- Ein erhöhtes intrazelluläres ATP:ADP-Verhältnis schließt den ATP-empfindlichen Kaliumkanal SUR1/Kir6.2 (siehe Sulfonylharnstoff-Rezeptor). Dadurch werden Kaliumionen (K+) daran gehindert, die Zelle durch erleichterte Diffusion zu verlassen, was zu einer Anhäufung intrazellulärer Kaliumionen führt. Infolgedessen wird das Innere der Zelle gegenüber dem Äußeren weniger negativ, was zu einer Depolarisierung der Zelloberflächenmembran führt.
- Nach der Depolarisierung öffnen sich spannungsabhängige Kalziumionenkanäle (Ca2+), so dass Kalziumionen durch erleichterte Diffusion in die Zelle gelangen können.
- Die zytosolische Kalziumionenkonzentration kann auch durch die Freisetzung von Kalzium aus intrazellulären Speichern über die Aktivierung von Ryanodinrezeptoren erhöht werden.
- Die Kalziumionenkonzentration im Zytosol der Betazellen kann auch bzw. zusätzlich durch die Aktivierung von Phospholipase C erhöht werden, die durch die Bindung eines extrazellulären Liganden (Hormon oder Neurotransmitter) an einen G-Protein-gekoppelten Membranrezeptor entsteht. Phospholipase C spaltet das Membranphospholipid, Phosphatidyl-Inositol-4,5-Bisphosphat, in Inositol-1,4,5-Trisphosphat und Diacylglycerol. Inositol-1,4,5-Trisphosphat (IP3) bindet dann an Rezeptorproteine in der Plasmamembran des endoplasmatischen Retikulums (ER). Dies ermöglicht die Freisetzung von Ca2+-Ionen aus dem ER über IP3-gesteuerte Kanäle, wodurch die zytosolische Konzentration von Kalziumionen unabhängig von den Auswirkungen einer hohen Blutzuckerkonzentration ansteigt. Die parasympathische Stimulation der Bauchspeicheldrüseninseln wirkt über diesen Weg, um die Insulinsekretion in das Blut zu erhöhen.
- Die deutlich erhöhte Menge an Kalziumionen im Zytoplasma der Zellen bewirkt die Freisetzung von zuvor synthetisiertem Insulin, das in intrazellulären sekretorischen Vesikeln gespeichert wurde, in das Blut. ⓘ
Dies ist der wichtigste Mechanismus für die Freisetzung von Insulin. Andere Substanzen, von denen bekannt ist, dass sie die Insulinfreisetzung stimulieren, sind die Aminosäuren Arginin und Leucin, die parasympathische Freisetzung von Acetylcholin (über den Phospholipase-C-Weg), Sulfonylharnstoffe, Cholecystokinin (CCK, ebenfalls über Phospholipase C) und die gastrointestinalen Inkretine wie Glucagon-like Peptide-1 (GLP-1) und glukoseabhängiges insulinotropes Peptid (GIP). ⓘ
Die Freisetzung von Insulin wird durch Noradrenalin stark gehemmt, was zu einem Anstieg des Blutzuckerspiegels bei Stress führt. Es scheint, dass die Freisetzung von Katecholaminen durch das sympathische Nervensystem widersprüchliche Einflüsse auf die Insulinfreisetzung durch Betazellen hat, da die Insulinfreisetzung durch α2-adrenerge Rezeptoren gehemmt und durch β2-adrenerge Rezeptoren stimuliert wird. Der Nettoeffekt von Noradrenalin aus den sympathischen Nerven und Epinephrin aus den Nebennieren auf die Insulinfreisetzung ist eine Hemmung aufgrund der Dominanz der α-adrenergen Rezeptoren. ⓘ
Wenn der Glukosespiegel auf den üblichen physiologischen Wert sinkt, verlangsamt sich die Insulinfreisetzung aus den β-Zellen oder hört auf. Sinkt der Blutzuckerspiegel unter diesen Wert, insbesondere auf gefährlich niedrige Werte, erzwingt die Freisetzung hyperglykämischer Hormone (vor allem Glukagon aus den Alphazellen der Langerhans-Inseln) die Freisetzung von Glukose aus den Glykogenspeichern der Leber ins Blut, die durch Glukoneogenese ergänzt wird, wenn die Glykogenspeicher erschöpft sind. Durch den Anstieg des Blutzuckerspiegels verhindern oder korrigieren die hyperglykämischen Hormone eine lebensbedrohliche Hypoglykämie. ⓘ
Hinweise auf eine gestörte Insulinfreisetzung in der ersten Phase liefert der Glukosetoleranztest, der sich durch einen deutlich erhöhten Blutzuckerspiegel 30 Minuten nach der Aufnahme einer Glukoselast (75 oder 100 g Glukose) zeigt, gefolgt von einem langsamen Abfall über die nächsten 100 Minuten, um zwei Stunden nach Testbeginn noch über 120 mg/100 ml zu liegen. Bei einer normalen Person ist der Blutzuckerspiegel am Ende des Tests korrigiert (und kann sogar leicht überkorrigiert sein). Ein Insulinspike ist eine "erste Reaktion" auf einen Blutzuckeranstieg. Diese Reaktion ist individuell und dosisabhängig, obwohl früher immer angenommen wurde, dass sie nur nahrungsmittelspezifisch ist. ⓘ


Die Ausschüttung von Insulin ins Blut erfolgt durch Exozytose. ⓘ
Das C-Peptid wird erst bei Anstieg des Blutzuckerspiegels aus dem Proinsulin durch Peptidasen herausgeschnitten und gemeinsam mit dem aktiven Insulin und Zink ausgeschüttet. Durch den Nachweis von C-Peptid im Serum kann die endogene Insulinproduktion gemessen werden. So kann bei Diabetikern eine Aussage darüber getroffen werden, wie viel Insulin noch vom Körper selbst hergestellt wird, da das synthetische Produkt keine C-Sequenz enthält. ⓘ
Oszillationen

Selbst während der Verdauung, im Allgemeinen ein oder zwei Stunden nach einer Mahlzeit, ist die Insulinfreisetzung aus der Bauchspeicheldrüse nicht kontinuierlich, sondern oszilliert mit einer Periode von 3-6 Minuten, wobei sie von der Erzeugung einer Blutinsulinkonzentration von mehr als etwa 800 pmol/l auf weniger als 100 pmol/l (bei Ratten) wechselt. Man nimmt an, dass dies dazu dient, eine Herunterregulierung der Insulinrezeptoren in den Zielzellen zu vermeiden und die Leber bei der Gewinnung von Insulin aus dem Blut zu unterstützen. Diese Oszillation ist bei der Verabreichung von insulinstimulierenden Medikamenten zu berücksichtigen, da im Idealfall die oszillierende Blutkonzentration der Insulinfreisetzung erreicht werden sollte und nicht eine konstant hohe Konzentration. Dies kann durch die rhythmische Abgabe von Insulin in die Pfortader, durch eine lichtaktivierte Abgabe oder durch eine Inselzelltransplantation in die Leber erreicht werden. ⓘ
Insulinspiegel im Blut
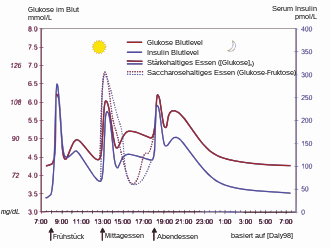
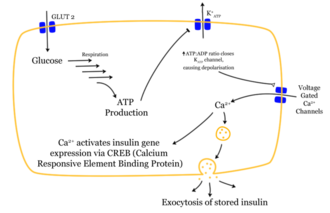
Das Eindringen eines Glucose-Moleküls in die β-Zelle setzt eine Wirkungskette in Gang. Nachdem die Glucose durch den GLUT1-Transporter in die Zelle gelangt ist, wird sie durch Glycolyse verstoffwechselt. Das dabei entstehende ATP hemmt den Ausstrom von Kalium-Ionen (ATP-sensitive Kaliumkanäle). So kommt es durch den stark verminderten Kaliumausstrom zur Depolarisation, weil die Stabilität des Membranpotentials nicht weiter durch Kaliumausstrom erhalten wird. Das depolarisierte Membranpotential bewirkt eine Öffnung spannungsabhängiger Calcium-Kanäle. Der Einstrom der Calciumionen ist der entscheidende Reiz für die Verschmelzung der insulinhaltigen Vesikel mit der Zellmembran. ⓘ
Die gespeicherten Insulinmoleküle werden durch Verschmelzen der Membranen (Exozytose) aus den β-Zellen in den Extrazellularraum und weiter in den Blutkreislauf freigesetzt. Dabei werden die Speicher-Hexamere aufgetrennt. Der Insulinspiegel im Blut steigt an. ⓘ
Der Insulinspiegel im Blut kann in internationalen Einheiten wie µIU/mL oder in der molaren Konzentration wie pmol/L gemessen werden, wobei 1 µIU/mL 6,945 pmol/L entspricht. Ein typischer Blutspiegel zwischen den Mahlzeiten beträgt 8-11 μIU/mL (57-79 pmol/L). ⓘ
Signaltransduktion
Die Wirkungen des Insulins werden durch seine Bindung an einen Rezeptor, den Insulinrezeptor (IR), ausgelöst, der sich in der Zellmembran befindet. Das Rezeptormolekül enthält eine α- und eine β-Untereinheit. Zwei Moleküle sind miteinander verbunden und bilden ein so genanntes Homodimer. Das Insulin bindet an die α-Untereinheiten des Homodimers, das der extrazellulären Seite der Zellen zugewandt ist. Die β-Untereinheiten haben eine Tyrosinkinase-Enzymaktivität, die durch die Insulinbindung ausgelöst wird. Diese Aktivität provoziert die Autophosphorylierung der β-Untereinheiten und anschließend die Phosphorylierung von Proteinen innerhalb der Zelle, die als Insulinrezeptorsubstrate (IRS) bekannt sind. Die Phosphorylierung des IRS aktiviert eine Signaltransduktionskaskade, die zur Aktivierung anderer Kinasen sowie von Transkriptionsfaktoren führt, die die intrazellulären Wirkungen von Insulin vermitteln. ⓘ
Die Kaskade, die zum Einbau der GLUT4-Glukosetransporter in die Zellmembranen von Muskel- und Fettzellen und zur Glykogensynthese im Leber- und Muskelgewebe sowie zur Umwandlung von Glukose in Triglyceride im Leber-, Fett- und Milchdrüsengewebe führt, funktioniert über die Aktivierung der Phosphoinositol-3-Kinase (PI3K) durch IRS-1. Dieses Enzym wandelt ein Phospholipid in der Zellmembran, das Phosphatidylinositol-4,5-bisphosphat (PIP2), in Phosphatidylinositol-3,4,5-Triphosphat (PIP3) um, das wiederum die Proteinkinase B (PKB) aktiviert. Aktivierte PKB erleichtert die Fusion von GLUT4-haltigen Endosomen mit der Zellmembran, was zu einer Zunahme der GLUT4-Transporter in der Plasmamembran führt. PKB phosphoryliert auch die Glykogensynthase-Kinase (GSK), wodurch dieses Enzym inaktiviert wird. Das bedeutet, dass sein Substrat, die Glykogensynthase (GS), nicht phosphoryliert werden kann, sondern dephosphoryliert und damit aktiv bleibt. Das aktive Enzym, die Glykogensynthase (GS), katalysiert den geschwindigkeitsbegrenzenden Schritt bei der Synthese von Glykogen aus Glukose. Ähnliche Dephosphorylierungen betreffen die Enzyme, die die Geschwindigkeit der Glykolyse steuern, die zur Fettsynthese über Malonyl-CoA in den Geweben führt, die Triglyceride erzeugen können, und auch die Enzyme, die die Geschwindigkeit der Glukoneogenese in der Leber steuern. Die Gesamtwirkung dieser letzten Enzymdephosphorylierungen besteht darin, dass in den Geweben, die diese Reaktionen durchführen können, die Glykogen- und Fettsynthese aus Glukose stimuliert und die Glukoseproduktion in der Leber durch Glykogenolyse und Glukoneogenese gehemmt wird. Der Abbau von Triglyceriden durch das Fettgewebe in freie Fettsäuren und Glycerin wird ebenfalls gehemmt. ⓘ
Nachdem das intrazelluläre Signal, das aus der Bindung des Insulins an seinen Rezeptor resultiert, erzeugt worden ist, muss die Signalübertragung beendet werden. Wie weiter unten im Abschnitt über den Abbau erwähnt, ist die Endozytose und der Abbau des an das Insulin gebundenen Rezeptors ein Hauptmechanismus zur Beendigung der Signalübertragung. Darüber hinaus wird der Signalweg auch durch Dephosphorylierung der Tyrosinreste in den verschiedenen Signalwegen durch Tyrosinphosphatasen beendet. Serin-/Threonin-Kinasen sind ebenfalls dafür bekannt, die Aktivität von Insulin zu verringern. ⓘ
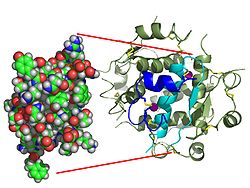
Die Struktur des Insulin-Insulin-Rezeptor-Komplexes wurde mit Hilfe der Röntgenkristallographie bestimmt. ⓘ
Physiologische Wirkungen


Zu den Wirkungen des Insulins auf den gesamten menschlichen Stoffwechsel gehören:
- Erhöhung der zellulären Aufnahme bestimmter Stoffe, vor allem von Glukose im Muskel- und Fettgewebe (etwa zwei Drittel der Körperzellen)
- Steigerung der DNA-Replikation und der Proteinsynthese durch Kontrolle der Aminosäureaufnahme
- Modifizierung der Aktivität zahlreicher Enzyme. ⓘ
Zu den (indirekten und direkten) Wirkungen des Insulins auf die Zellen gehören:
- Stimulierung der Glukoseaufnahme - Insulin senkt die Glukosekonzentration im Blut, indem es die Aufnahme von Glukose durch die Zellen anregt. Dies ist möglich, weil Insulin den Einbau des GLUT4-Transporters in die Zellmembranen des Muskel- und Fettgewebes bewirkt, wodurch Glukose in die Zelle gelangen kann.
- Erhöhte Fettsynthese - Insulin zwingt die Fettzellen zur Aufnahme von Glukose aus dem Blut, die in Triglyceride umgewandelt wird; ein Rückgang des Insulins bewirkt das Gegenteil.
- Vermehrte Veresterung von Fettsäuren - zwingt das Fettgewebe, aus Fettsäuren neutrale Fette (d. h. Triglyceride) herzustellen; ein Rückgang des Insulins bewirkt das Gegenteil.
- Verminderte Lipolyse - erzwingt eine Verringerung der Umwandlung von Lipidspeichern in den Fettzellen in Fettsäuren und Glycerin im Blut; ein Rückgang des Insulins bewirkt das Gegenteil.
- Induzierte Glykogensynthese - Bei hohem Glukosespiegel induziert Insulin die Bildung von Glykogen durch die Aktivierung des Enzyms Hexokinase, das der Glukose eine Phosphatgruppe hinzufügt, so dass ein Molekül entsteht, das die Zelle nicht verlassen kann. Gleichzeitig hemmt das Insulin das Enzym Glukose-6-Phosphatase, das die Phosphatgruppe entfernt. Diese beiden Enzyme sind entscheidend für die Bildung von Glykogen. Außerdem aktiviert Insulin die Enzyme Phosphofructokinase und Glykogensynthase, die für die Glykogensynthese verantwortlich sind.
- Verminderte Glukoneogenese und Glykogenolyse - verringert die Produktion von Glukose aus Nicht-Kohlenhydrat-Substraten, vor allem in der Leber (der größte Teil des endogenen Insulins, der in der Leber ankommt, verlässt die Leber nie); ein Rückgang des Insulins bewirkt, dass die Leber Glukose aus verschiedenen Substraten produziert.
- Verminderte Proteolyse - verminderter Abbau von Proteinen
- Verminderte Autophagie - verminderter Abbau von beschädigten Organellen. Postprandiale Werte hemmen die Autophagie vollständig.
- Erhöhte Aminosäureaufnahme - zwingt die Zellen, zirkulierende Aminosäuren zu absorbieren; ein Rückgang des Insulins hemmt die Aufnahme.
- Arterieller Muskeltonus - zwingt die Arterienwandmuskulatur zur Entspannung, was den Blutfluss erhöht, insbesondere in den Mikroarterien; ein Insulinabfall verringert den Blutfluss, indem er die Kontraktion dieser Muskeln ermöglicht.
- Erhöhte Sekretion von Salzsäure durch die Parietalzellen im Magen.
- Erhöhte Kaliumaufnahme - zwingt die Zellen, die Glykogen synthetisieren (eine sehr schwammige, "feuchte" Substanz, die den Gehalt an intrazellulärem Wasser und den damit einhergehenden K+-Ionen erhöht), Kalium aus den extrazellulären Flüssigkeiten aufzunehmen; ein Mangel an Insulin hemmt die Aufnahme. Durch die erhöhte zelluläre Kaliumaufnahme durch Insulin wird der Kaliumspiegel im Blutplasma gesenkt. Dies geschieht möglicherweise durch die insulininduzierte Verlagerung der Na+/K+-ATPase an die Oberfläche der Skelettmuskelzellen.
- Verminderte renale Natriumausscheidung. ⓘ
Insulin beeinflusst auch andere Körperfunktionen, wie z. B. die vaskuläre Compliance und die Kognition. Sobald Insulin in das menschliche Gehirn gelangt, verbessert es die Lern- und Gedächtnisleistung und wirkt sich insbesondere auf das verbale Gedächtnis aus. Die Verstärkung der Insulinsignalisierung im Gehirn durch intranasale Insulinverabreichung verbessert auch die akute thermoregulatorische und glukoregulatorische Reaktion auf die Nahrungsaufnahme, was darauf hindeutet, dass Insulin im Zentralnervensystem zur Koordinierung einer Vielzahl von homöostatischen oder regulatorischen Prozessen im menschlichen Körper beiträgt. Insulin hat auch eine stimulierende Wirkung auf das Gonadotropin-Releasing-Hormon aus dem Hypothalamus und fördert so die Fruchtbarkeit. ⓘ
Abbau
Die biologische Halbwertszeit einzelner Insulinmoleküle im Blutkreislauf liegt bei circa fünf Minuten. ⓘ
Das Insulin wird über manche Insulinrezeptoren in die Zellen aufgenommen, dort abgebaut und somit verbraucht. In der Leber und in der Niere wird Insulin durch Insulinase inaktiviert, die Insulinase oder genauer Glutathion-Insulin-Transhydrogenase spaltet die Disulfidbrücken zwischen der A- und der B-Kette auf, wodurch das Insulin in zwei Teile zerfällt und wirkungslos wird. Die Abbauprodukte werden durch die Niere ausgeschieden, ebenso 1,5 % des noch intakten Insulins. Die kurze Zeitspanne der Aktivität des Insulins zeigt, dass die physiologische Steuerung des Zuckerstoffwechsels im gesunden Körper sehr schnell funktioniert; diese Geschwindigkeit kann bei der Behandlung des Diabetes mellitus praktisch nicht erreicht werden. ⓘ
Regulator des Endocannabinoid-Stoffwechsels
Insulin ist ein wichtiger Regulator des Endocannabinoid-Stoffwechsels (EC), und es hat sich gezeigt, dass eine Insulinbehandlung zu einer Verringerung der intrazellulären EC, des 2-Arachidonoylglycerins (2-AG) und des Anandamids (AEA) führt, was mit insulinempfindlichen Expressionsänderungen bei Enzymen des EC-Stoffwechsels einhergeht. In insulinresistenten Adipozyten sind die Muster der insulininduzierten Enzymexpression in einer Weise gestört, die mit einer erhöhten EG-Synthese und einem verringerten EG-Abbau übereinstimmt. Die Ergebnisse deuten darauf hin, dass insulinresistente Adipozyten den EC-Stoffwechsel nicht regulieren und die intrazellulären EC-Spiegel als Reaktion auf die Insulinstimulation verringern, wodurch fettleibige insulinresistente Personen erhöhte EC-Konzentrationen aufweisen. Diese Dysregulation trägt zu einer übermäßigen Ansammlung von viszeralem Fett und einer verminderten Freisetzung von Adiponektin aus dem abdominalen Fettgewebe bei, was wiederum zur Entstehung mehrerer kardiometabolischer Risikofaktoren beiträgt, die mit Fettleibigkeit und Typ-2-Diabetes in Verbindung gebracht werden. ⓘ
Hypoglykämie
Hypoglykämie, auch bekannt als "Unterzuckerung", liegt vor, wenn der Blutzuckerspiegel unter den Normalwert sinkt. Dies kann zu einer Vielzahl von Symptomen führen, darunter Ungeschicklichkeit, Schwierigkeiten beim Sprechen, Verwirrung, Bewusstlosigkeit, Krampfanfälle oder Tod. Auch ein Hungergefühl, Schweißausbrüche, Zittern und Schwäche können auftreten. Die Symptome treten in der Regel schnell auf. ⓘ
Die häufigste Ursache für eine Hypoglykämie sind Medikamente zur Behandlung von Diabetes mellitus wie Insulin und Sulfonylharnstoffe. Das Risiko ist bei Diabetikern größer, die weniger als üblich gegessen, mehr als üblich Sport getrieben oder Alkohol konsumiert haben. Weitere Ursachen für eine Hypoglykämie sind Nierenversagen, bestimmte Tumore wie Insulinome, Lebererkrankungen, Schilddrüsenunterfunktion, Hunger, angeborene Stoffwechselstörungen, schwere Infektionen, reaktive Hypoglykämie und eine Reihe von Medikamenten einschließlich Alkohol. Ein niedriger Blutzuckerspiegel kann bei ansonsten gesunden Säuglingen auftreten, die einige Stunden lang nichts gegessen haben. ⓘ
Krankheiten und Syndrome
Es gibt mehrere Erkrankungen, bei denen eine Insulinstörung pathologisch ist:
- Diabetes mellitus - allgemeiner Begriff, der sich auf alle Zustände bezieht, die durch Hyperglykämie gekennzeichnet sind. Es gibt die folgenden Typen:
- Typ 1 - autoimmunvermittelte Zerstörung der insulinproduzierenden β-Zellen in der Bauchspeicheldrüse, was zu einem absoluten Insulinmangel führt
- Typ 2 - entweder unzureichende Insulinproduktion durch die β-Zellen oder Insulinresistenz oder beides aus nicht vollständig geklärten Gründen.
- Es besteht ein Zusammenhang mit der Ernährung, mit Bewegungsmangel, mit Fettleibigkeit, mit dem Alter und mit dem metabolischen Syndrom. Die Kausalität wurde bei mehreren Modellorganismen, darunter Mäusen und Affen, nachgewiesen; wichtig ist, dass auch nicht fettleibige Menschen aufgrund von Ernährung, sitzender Lebensweise und unbekannten Risikofaktoren an Typ-2-Diabetes erkranken, auch wenn es sich dabei nicht unbedingt um einen kausalen Zusammenhang handelt.
- Es ist wahrscheinlich, dass es eine genetische Anfälligkeit für die Entwicklung von Typ-2-Diabetes unter bestimmten Umweltbedingungen gibt.
- Andere Arten der gestörten Glukosetoleranz (siehe Diabetes)
- Insulinom - ein Tumor der Betazellen, der überschüssiges Insulin oder reaktive Hypoglykämie produziert.
- Metabolisches Syndrom - ein schlecht verstandener Zustand, der zuerst von Gerald Reaven als Syndrom X bezeichnet wurde. Es ist nicht klar, ob das Syndrom eine einzige, behandelbare Ursache hat oder das Ergebnis von Körperveränderungen ist, die zu Typ-2-Diabetes führen. Es ist gekennzeichnet durch erhöhten Blutdruck, Dyslipidämie (Störungen der Cholesterinwerte und anderer Blutfette) und einen erhöhten Taillenumfang (zumindest in weiten Teilen der entwickelten Welt). Die grundlegende Ursache ist möglicherweise die Insulinresistenz, die dem Typ-2-Diabetes vorausgeht, d. h. eine verminderte Fähigkeit zur Insulinreaktion in bestimmten Geweben (z. B. Muskeln, Fett). Häufig entwickeln sich Krankheiten wie essenzieller Bluthochdruck, Fettleibigkeit, Typ-2-Diabetes und Herz-Kreislauf-Erkrankungen (CVD).
- Polyzystisches Ovarsyndrom - ein komplexes Syndrom bei Frauen in den reproduktiven Jahren, bei dem sich Anovulation und Androgenüberschuss häufig als Hirsutismus zeigen. In vielen Fällen von PCOS liegt eine Insulinresistenz vor. ⓘ
Medizinische Anwendungen
Biosynthetisches Humaninsulin (Humaninsulin rDNA, INN) für den klinischen Gebrauch wird durch rekombinante DNA-Technologie hergestellt. Biosynthetisches Humaninsulin weist im Vergleich zu extraktivem tierischem Insulin eine höhere Reinheit auf, wodurch die Bildung von Antikörpern verringert wird. Forschern ist es gelungen, das Gen für Humaninsulin in Pflanzen einzuschleusen und so eine weitere Methode zur Insulinproduktion ("Biopharming") in Färberdistel zu entwickeln. Es wird erwartet, dass diese Technik die Produktionskosten senken wird. ⓘ
Es sind mehrere Analoga des Humaninsulins erhältlich. Diese Insulinanaloga sind eng mit der Struktur des Humaninsulins verwandt und wurden für spezifische Aspekte der Blutzuckerkontrolle in Bezug auf eine schnelle Wirkung (prandiale Insuline) und eine lange Wirkung (Basalinsuline) entwickelt. Das erste biosynthetische Insulinanalogon wurde für den klinischen Einsatz zu den Mahlzeiten (prandiales Insulin) entwickelt: Humalog (Insulin lispro) wird nach der subkutanen Injektion schneller absorbiert als normales Insulin und wirkt 15 Minuten nach der Injektion. Andere schnell wirkende Analoga sind NovoRapid und Apidra, die ein ähnliches Profil aufweisen. Alle werden aufgrund von Aminosäuresequenzen, die die Bildung von Dimeren und Hexameren reduzieren, schnell resorbiert (monomere Insuline werden schneller resorbiert). Schnell wirkende Insuline erfordern nicht das Intervall zwischen Injektion und Mahlzeit, das früher für Humaninsulin und tierische Insuline empfohlen wurde. Der andere Typ ist das langwirksame Insulin; das erste dieser Insuline war Lantus (Insulin Glargin). Diese Insuline haben eine gleichmäßige Wirkung über einen längeren Zeitraum von 18 bis 24 Stunden. Ein weiteres langwirksames Insulinanalogon (Levemir) basiert ebenfalls auf einem Fettsäureacylierungsansatz. An dieses Analogon wird ein Myristinsäuremolekül angehängt, das das Insulinmolekül mit dem reichlich vorhandenen Serumalbumin verbindet, was wiederum die Wirkung verlängert und das Risiko einer Hypoglykämie verringert. Beide langwirksamen Analoga müssen nur einmal täglich eingenommen werden und werden bei Typ-1-Diabetikern als Basalinsulin verwendet. Es gibt auch eine Kombination aus einem schnell wirkenden und einem protrahierten Insulin, die es den Patienten ermöglicht, ein Insulinprofil zu erreichen, das dem der körpereigenen Insulinausschüttung ähnelt. Insulin wird auch in vielen Zelllinien, wie CHO-s, HEK 293 oder Sf9, für die Herstellung von monoklonalen Antikörpern, Virusimpfstoffen und Gentherapieprodukten verwendet. ⓘ
Insulin wird in der Regel als subkutane Injektion mit Einwegspritzen mit Nadeln, über eine Insulinpumpe oder mit Insulin-Pens mit Einwegnadeln zur wiederholten Verwendung verabreicht. Inhalatives Insulin ist ebenfalls auf dem US-Markt erhältlich. ⓘ
Im Gegensatz zu vielen anderen Arzneimitteln kann Insulin nicht über den Mund eingenommen werden, da es, wie fast alle anderen Proteine, die in den Magen-Darm-Trakt gelangen, in Bruchstücke zerlegt wird, wodurch es seine Wirkung verliert. Es wurde an Möglichkeiten geforscht, Insulin vor dem Verdauungstrakt zu schützen, so dass es oral oder sublingual verabreicht werden kann. ⓘ
Im Jahr 2021 nahm die Weltgesundheitsorganisation Insulin in ihre Modellliste der unentbehrlichen Arzneimittel auf. ⓘ

In der Insulintherapie werden verschiedene Insulinpräparate verwendet. Die häufigste und älteste Verabreichungsart ist die subkutane Injektion. Für diesen Zweck steht eine Reihe von kurz-, mittel- und langwirkenden Humaninsulinen und Insulinanaloga zur Verfügung. Werden diese zur Therapie kombiniert, so ist auf die unterschiedliche Halbwertzeit besonders zu achten. ⓘ

Peroral ist Insulin unwirksam, da die Eiweißketten im Magen-Darm-Trakt von körpereigenen Enzymen abgebaut werden, bevor sie ihre Wirkung entfalten können. Untersucht wird, inwieweit sich Insuline in Nanopartikel verkapseln lassen, um auf diesem Wege „unverdaut“ in den Blutkreislauf eingeschleust werden zu können. Jüngere Entwicklungen wie Präparate zur Inhalation, die das Insulin über die Atemwege zuführen, haben sich auf dem Markt bisher nicht behaupten können. ⓘ
In der Vergangenheit wurde Insulin im Rahmen der Insulinschocktherapie zur Behandlung von Menschen mit psychischen Krankheiten eingesetzt. Diese Methode der Behandlung wurde zum Beispiel im biografischen Film A Beautiful Mind an John Nash gezeigt. Dieses Verfahren wird nicht mehr praktiziert. ⓘ
Geschichte der Studie
Entdeckung
Als der Berliner Medizinstudent Paul Langerhans 1869 die Struktur der Bauchspeicheldrüse unter dem Mikroskop untersuchte, entdeckte er einige bis dahin unbemerkte Gewebeklümpchen, die über den Großteil der Bauchspeicheldrüse verstreut waren. Die Funktion dieser "kleinen Zellhaufen", die später als Langerhans-Inseln bekannt wurden, blieb zunächst unbekannt, aber Édouard Laguesse schlug später vor, dass sie Sekrete produzieren könnten, die eine regulierende Rolle bei der Verdauung spielen. Der Sohn von Paul Langerhans, Archibald, trug ebenfalls dazu bei, diese regulierende Rolle zu verstehen. ⓘ
1889 entfernte der Arzt Oskar Minkowski in Zusammenarbeit mit Joseph von Mering die Bauchspeicheldrüse eines gesunden Hundes, um ihre vermutete Rolle bei der Verdauung zu testen. Bei der Untersuchung des Urins fanden sie Zucker, womit zum ersten Mal ein Zusammenhang zwischen der Bauchspeicheldrüse und Diabetes hergestellt wurde. 1901 gelang dem amerikanischen Arzt und Wissenschaftler Eugene Lindsay Opie ein weiterer wichtiger Schritt, als er die Rolle der Bauchspeicheldrüse auf die Langerhans-Inseln beschränkte: "Diabetes mellitus als Folge einer Verletzung der Bauchspeicheldrüse wird durch die Zerstörung der Langerhans-Inseln verursacht und tritt nur auf, wenn diese Körper teilweise oder ganz zerstört sind". ⓘ
In den folgenden zwei Jahrzehnten unternahmen die Forscher mehrere Versuche, die Sekrete der Inselchen zu isolieren. Im Jahr 1906 erzielte Georg Ludwig Zülzer einen Teilerfolg bei der Behandlung von Hunden mit Pankreasextrakt, konnte seine Arbeit jedoch nicht fortsetzen. Zwischen 1911 und 1912 versuchte E.L. Scott an der Universität von Chicago wässrige Pankreasextrakte und stellte "eine leichte Verminderung der Glykosurie" fest, konnte aber seinen Direktor nicht vom Wert seiner Arbeit überzeugen; sie wurde eingestellt. Israel Kleiner wies 1915 an der Rockefeller University ähnliche Wirkungen nach, doch wurde seine Arbeit durch den Ersten Weltkrieg unterbrochen und er kehrte nicht mehr dorthin zurück. ⓘ
1916 entwickelte Nicolae Paulescu einen wässrigen Bauchspeicheldrüsenextrakt, der, wenn er einem zuckerkranken Hund injiziert wurde, eine normalisierende Wirkung auf den Blutzuckerspiegel hatte. Wegen des Ersten Weltkriegs musste er seine Experimente unterbrechen. 1921 schrieb er vier Abhandlungen über seine in Bukarest durchgeführten Arbeiten und seine Versuche an einem diabetischen Hund. Später im selben Jahr veröffentlichte er "Research on the Role of the Pancreas in Food Assimilation". ⓘ
Der Name "Insulin" wurde 1916 von Edward Albert Sharpey-Schafer für ein hypothetisches Molekül geprägt, das von den Langerhansschen Inseln der Bauchspeicheldrüse (lateinisch insula für Insel oder Insel) produziert wird und den Glukosestoffwechsel steuert. Ohne dass Sharpey-Schafer dies wusste, hatte Jean de Meyer 1909 den sehr ähnlichen Begriff "Insulin" für dasselbe Molekül eingeführt. ⓘ
Extraktion und Reinigung
Im Oktober 1920 kam der Kanadier Frederick Banting zu dem Schluss, dass die Verdauungssekrete, die Minkowski ursprünglich untersucht hatte, das Inselsekret zersetzen und damit eine erfolgreiche Extraktion unmöglich machen. Als ausgebildeter Chirurg wusste Banting, dass eine Verstopfung des Pankreasgangs zu einer Verkümmerung des größten Teils der Bauchspeicheldrüse führen würde, während die Langerhans-Inseln intakt blieben. Er ging davon aus, dass aus den Inseln ein relativ reines Extrakt gewonnen werden könnte, wenn der Rest der Bauchspeicheldrüse größtenteils verschwunden war. Er machte sich eine Notiz: "Pankreasgänge des Hundes ligieren. Hunde am Leben lassen, bis die Azini degenerieren und die Inseln übrig bleiben. Versuchen Sie, die innere Sekretion dieser Inseln zu isolieren und die Glykosurie zu lindern." ⓘ

Im Frühjahr 1921 reiste Banting nach Toronto, um J.J.R. Macleod, Professor für Physiologie an der Universität von Toronto, seine Idee vorzustellen. Macleod war zunächst skeptisch, da Banting keine Erfahrung in der Forschung hatte und mit der neuesten Literatur nicht vertraut war, aber er erklärte sich bereit, Banting einen Laborraum zur Verfügung zu stellen, um seine Ideen zu testen. Macleod arrangierte auch zwei Studenten als Bantings Laborassistenten für diesen Sommer, aber Banting brauchte nur einen Laborassistenten. Charles Best und Clark Noble warfen eine Münze; Best gewann den Münzwurf und übernahm die erste Schicht. Dies erwies sich als unglücklich für Noble, denn Banting behielt Best den ganzen Sommer über und teilte schließlich die Hälfte seines Nobelpreisgeldes und die Anerkennung für die Entdeckung mit Best. Am 30. Juli 1921 isolierten Banting und Best erfolgreich einen Extrakt ("Isleton") aus den Inseln eines gefesselten Hundes und injizierten ihn einem diabetischen Hund, wobei sie feststellten, dass der Extrakt den Blutzucker innerhalb einer Stunde um 40 % senkte. ⓘ
Banting und Best präsentierten Macleod bei seiner Rückkehr nach Toronto im Herbst 1921 ihre Ergebnisse, doch Macleod wies auf Mängel in der Versuchsanordnung hin und schlug vor, die Experimente mit mehr Hunden und besserer Ausrüstung zu wiederholen. Er versetzte Banting und Best in ein besseres Labor und begann, Banting ein Gehalt aus seinen Forschungsgeldern zu zahlen. Einige Wochen später war auch die zweite Versuchsreihe ein Erfolg, und Macleod trug dazu bei, dass die Ergebnisse noch im November in Toronto veröffentlicht wurden. Banting, dem die zeitaufwändige Aufgabe des Anbindens von Hunden und die mehrwöchige Wartezeit für die Insulinextraktion ein Dorn im Auge war, kam auf die Idee, Insulin aus der Bauchspeicheldrüse fötaler Kälber zu gewinnen, die noch keine Verdauungsdrüsen entwickelt hatten. Im Dezember gelang es ihnen auch, Insulin aus der Bauchspeicheldrüse einer erwachsenen Kuh zu gewinnen. Macleod stellte alle anderen Forschungen in seinem Labor ein, um sich auf die Reinigung des Insulins zu konzentrieren. Er lud den Biochemiker James Collip ein, ihm bei dieser Aufgabe zu helfen, und das Team fühlte sich innerhalb eines Monats bereit für einen klinischen Test. ⓘ

Am 11. Januar 1922 erhielt Leonard Thompson, ein 14-jähriger Diabetiker, der im Toronto General Hospital im Sterben lag, die erste Insulininjektion. Der Extrakt war jedoch so unrein, dass Thompson eine schwere allergische Reaktion zeigte und weitere Injektionen abgesagt wurden. In den folgenden 12 Tagen arbeitete Collip Tag und Nacht an der Verbesserung des Ochsenspeicheldrüsenextrakts. Am 23. Januar wurde eine zweite Dosis injiziert, die die für Diabetes typische Glykosurie beseitigte, ohne offensichtliche Nebenwirkungen zu verursachen. Die erste amerikanische Patientin war Elizabeth Hughes, die Tochter des US-Außenministers Charles Evans Hughes. Der erste in den USA behandelte Patient war der spätere Holzschnittkünstler James D. Havens; Dr. John Ralston Williams importierte Insulin aus Toronto nach Rochester, New York, um Havens zu behandeln. ⓘ
Banting und Best arbeiteten nie gut mit Collip zusammen, da sie ihn als eine Art Eindringling betrachteten, und Collip verließ das Projekt bald darauf. Im Laufe des Frühjahrs 1922 gelang es Best, seine Techniken so weit zu verbessern, dass große Mengen Insulin bei Bedarf extrahiert werden konnten, aber das Präparat blieb unrein. Die Arzneimittelfirma Eli Lilly and Company hatte bereits kurz nach den ersten Veröffentlichungen im Jahr 1921 ihre Unterstützung angeboten, und im April nahm Lilly das Angebot an. Im November entdeckte der Chefchemiker von Lilly, George B. Walden, die isoelektrische Fällung und konnte große Mengen an hochveredeltem Insulin herstellen. Kurz darauf wurde das Insulin der breiten Öffentlichkeit zum Kauf angeboten. ⓘ
Patent
Gegen Ende Januar 1922 kam es zu Spannungen zwischen den vier "Mitentdeckern" des Insulins, und Collip drohte kurz damit, sein Reinigungsverfahren separat patentieren zu lassen. John G. FitzGerald, Direktor der nichtkommerziellen öffentlichen Gesundheitseinrichtung Connaught Laboratories, schaltete sich daher als Friedensstifter ein. Die daraus resultierende Vereinbarung vom 25. Januar 1922 stellte zwei wesentliche Bedingungen: Erstens, dass die Mitarbeiter einen Vertrag unterzeichnen, in dem sie sich verpflichten, während einer anfänglichen Arbeitsperiode mit Connaught kein Patent mit einem kommerziellen Pharmaunternehmen abzuschließen, und zweitens, dass keine Änderungen in der Forschungspolitik erlaubt sind, die nicht zuvor zwischen FitzGerald und den vier Mitarbeitern besprochen wurden. Dies trug dazu bei, Meinungsverschiedenheiten einzudämmen und die Forschung an den öffentlichen Auftrag von Connaught zu binden. ⓘ
Anfangs zögerten Macleod und Banting aus medizinethischen Gründen besonders, ihr Verfahren für Insulin patentieren zu lassen. Es bestanden jedoch weiterhin Bedenken, dass ein privater Dritter die Forschung an sich reißen und monopolisieren könnte (wie Eli Lilly and Company angedeutet hatte), und dass eine sichere Verteilung ohne Kapazitäten für die Qualitätskontrolle schwer zu gewährleisten wäre. Zu diesem Zweck gab Edward Calvin Kendall wertvolle Ratschläge. Er hatte 1914 in der Mayo-Klinik Thyroxin isoliert und das Verfahren durch eine Vereinbarung zwischen ihm, den Brüdern Mayo und der Universität von Minnesota patentieren lassen, wobei er das Patent auf die öffentliche Universität übertrug. Am 12. April schrieben Banting, Best, Collip, Macleod und FitzGerald gemeinsam an den Präsidenten der Universität von Toronto und schlugen eine ähnliche Vereinbarung vor, mit dem Ziel, ein Patent an den Verwaltungsrat der Universität zu übertragen. In dem Schreiben wurde betont, dass:
Das Patent würde zu keinem anderen Zweck verwendet werden als zur Verhinderung der Erlangung eines Patents durch andere Personen. Wenn die Einzelheiten der Zubereitungsmethode veröffentlicht würden, stünde es jedem frei, den Extrakt herzustellen, aber niemand könne sich ein gewinnbringendes Monopol sichern.
Der Auftrag an den Obersten Rat der Universität Toronto wurde am 15. Januar 1923 gegen eine symbolische Zahlung von 1,00 Dollar abgeschlossen. Die Vereinbarung wurde 1923 in The World's Work als "ein Fortschritt in der medizinischen Ethik" gewürdigt. Auch in den 2010er Jahren hat sie im Zusammenhang mit der Gesundheitsversorgung und der Erschwinglichkeit von Medikamenten viel Aufmerksamkeit in den Medien gefunden. ⓘ
Nach weiteren Bedenken hinsichtlich der Versuche von Eli Lilly, Teile des Herstellungsprozesses separat zu patentieren, führte der stellvertretende Direktor und Leiter der Insulinabteilung von Connaught, Robert Defries, eine Patent-Pooling-Politik ein, die von den Herstellern verlangen würde, dass sie alle Verbesserungen des Herstellungsprozesses frei miteinander teilen, ohne die Erschwinglichkeit zu gefährden. ⓘ
Strukturanalyse und Synthese
Gereinigtes tierisches Insulin war zunächst die einzige Insulinart, die für Experimente und Diabetiker zur Verfügung stand. John Jacob Abel war der erste, der 1926 die kristallisierte Form herstellte. Der Nachweis, dass es sich um ein Protein handelt, wurde erstmals von Michael Somogyi, Edward A. Doisy und Philip A. Shaffer im Jahr 1924 erbracht. Vollständig bewiesen wurde sie, als Hans Jensen und Earl A. Evans Jr. 1935 die Aminosäuren Phenylalanin und Prolin isolierten. ⓘ
Die Aminosäurestruktur von Insulin wurde erstmals 1951 von Frederick Sanger charakterisiert, und das erste synthetische Insulin wurde Mitte der 1960er Jahre gleichzeitig in den Labors von Panayotis Katsoyannis an der Universität Pittsburgh und Helmut Zahn an der RWTH Aachen hergestellt. Synthetisches kristallines Rinderinsulin wurde 1965 von chinesischen Forschern hergestellt. Die vollständige dreidimensionale Struktur von Insulin wurde 1969 im Labor von Dorothy Hodgkin durch Röntgenkristallographie bestimmt. ⓘ
Dr. Hans E. Weber entdeckte Präproinsulin, als er 1974 als Forschungsstipendiat an der University of California Los Angeles arbeitete. In den Jahren 1973-1974 erlernte Weber die Techniken zur Isolierung, Reinigung und Übersetzung von Boten-RNA. Zur weiteren Untersuchung von Insulin erhielt er Bauchspeicheldrüsengewebe aus einem Schlachthof in Los Angeles und später aus Tierbeständen der UCLA. Er isolierte und reinigte die gesamte Boten-RNA aus den Inselzellen der Bauchspeicheldrüse, die dann in Eizellen von Xenopus laevis übersetzt und mit Anti-Insulin-Antikörpern ausgefällt wurde. Als das gesamte translatierte Protein auf einer SDS-Polyacrylamid-Gelelektrophorese und einem Saccharosegradienten untersucht wurde, wurden Peaks isoliert, die Insulin und Proinsulin entsprechen. Zur Überraschung von Dr. Weber wurde jedoch ein dritter Peak isoliert, der einem Molekül entspricht, das größer ist als Proinsulin. Nach mehrmaliger Wiederholung des Experiments stellte er immer wieder diesen großen Peak vor dem Proinsulin fest, bei dem es sich seiner Meinung nach um ein größeres Vorläufermolekül vor dem Proinsulin handeln musste. Im Mai 1975 hielt Weber auf der Tagung der American Diabetes Association in New York einen Vortrag über seine Arbeit, in dem er dieses Vorläufermolekül als erster "Präproinsulin" nannte. Im Anschluss an diesen Vortrag wurde Weber von Dr. Donald Steiner, einem Forscher, der zur Charakterisierung von Proinsulin beigetragen hatte, zu einem Abendessen eingeladen, um seine Arbeit und seine Ergebnisse zu diskutieren. Ein Jahr später, im April 1976, wurde dieses Molekül von Steiner unter Bezugnahme auf die Arbeit und Entdeckung von Hans Weber weiter charakterisiert und sequenziert. Präproinsulin wurde zu einem wichtigen Molekül, um den Prozess der Transkription und Translation zu untersuchen. ⓘ
Das erste gentechnisch hergestellte, synthetische "menschliche" Insulin wurde 1978 von Arthur Riggs und Keiichi Itakura am Beckman Research Institute of the City of Hope in Zusammenarbeit mit Herbert Boyer von Genentech in E. coli hergestellt. Genentech, das von Swanson, Boyer und Eli Lilly and Company gegründet wurde, verkaufte 1982 das erste kommerziell erhältliche biosynthetische Humaninsulin unter dem Markennamen Humulin. Die überwiegende Mehrheit des weltweit verwendeten Insulins ist biosynthetisches rekombinantes "Humaninsulin" oder seine Analoga. In jüngster Zeit hat eine kanadische Forschergruppe, die Pionierarbeit geleistet hat, einen anderen Ansatz verfolgt, bei dem eine leicht zu züchtende Färberdistelpflanze für die Herstellung von viel billigerem Insulin verwendet wird. ⓘ
Rekombinantes Insulin wird entweder in Hefe (gewöhnlich Saccharomyces cerevisiae) oder in E. coli hergestellt. In Hefe kann Insulin als ein einkettiges Protein mit einer KexII-Endoprotease-Stelle (ein Hefe-Homolog von PCI/PCII) hergestellt werden, die die Insulin-A-Kette von einer C-terminal verkürzten Insulin-B-Kette trennt. Ein chemisch synthetisierter C-terminaler Schwanz wird dann durch umgekehrte Proteolyse mit der kostengünstigen Protease Trypsin auf das Insulin aufgepfropft; typischerweise wird das Lysin am C-terminalen Schwanz mit einer chemischen Schutzgruppe geschützt, um Proteolyse zu verhindern. Die Einfachheit der modularen Synthese und die relative Sicherheit von Modifikationen in diesem Bereich sind der Grund für die weit verbreiteten Insulinanaloga mit C-terminalen Modifikationen (z. B. Lispro, Aspart, Glulisin). Die Genentech-Synthese und vollständig chemische Synthesen wie die von Bruce Merrifield werden nicht bevorzugt, da die Effizienz der Rekombination der beiden Insulinketten gering ist, vor allem aufgrund der Konkurrenz mit der Ausfällung der Insulin-B-Kette. ⓘ
Nobelpreise

Das Nobelpreiskomitee schrieb 1923 die praktische Gewinnung von Insulin einem Team der Universität von Toronto zu und verlieh den Nobelpreis an zwei Männer: Frederick Banting und J.J.R. Macleod. Sie wurden 1923 für die Entdeckung des Insulins mit dem Nobelpreis für Physiologie oder Medizin ausgezeichnet. Banting, verärgert darüber, dass Best nicht erwähnt wurde, teilte seinen Preis mit ihm, und Macleod teilte seinen Preis sofort mit James Collip. Das Patent für Insulin wurde für einen Dollar an die Universität von Toronto verkauft. ⓘ
Zwei weitere Nobelpreise wurden für Arbeiten über Insulin vergeben. Der britische Molekularbiologe Frederick Sanger, der 1955 die Primärstruktur des Insulins bestimmte, erhielt 1958 den Nobelpreis für Chemie. Rosalyn Sussman Yalow erhielt den Nobelpreis für Medizin 1977 für die Entwicklung des Radioimmunoassays für Insulin. ⓘ
Mehrere Nobelpreise stehen auch in einem indirekten Zusammenhang mit Insulin. George Minot, Mitpreisträger des Nobelpreises 1934 für die Entwicklung der ersten wirksamen Behandlung der perniziösen Anämie, litt an Diabetes mellitus. Dr. William Castle stellte fest, dass die Entdeckung des Insulins im Jahr 1921, die gerade noch rechtzeitig kam, um Minot am Leben zu erhalten, daher auch für die Entdeckung eines Heilmittels für perniziöse Anämie verantwortlich war. Dorothy Hodgkin erhielt 1964 den Nobelpreis für Chemie für die Entwicklung der Kristallographie, mit der sie 1969 die vollständige Molekularstruktur des Insulins entschlüsselte. ⓘ
Kontroverse

Die von Banting, Best, Collip und Macleod veröffentlichten Arbeiten stellten die Herstellung eines gereinigten Insulinextrakts dar, der für die Verwendung bei menschlichen Patienten geeignet war. Obwohl Paulescu die Prinzipien der Behandlung entdeckte, konnte sein Kochsalzextrakt nicht am Menschen angewendet werden; er wurde bei der Verleihung des Nobelpreises 1923 nicht erwähnt. Professor Ian Murray setzte sich besonders dafür ein, das "historische Unrecht" gegen Nicolae Paulescu zu korrigieren. Murray war Professor für Physiologie am Anderson College of Medicine in Glasgow, Schottland, Leiter der Abteilung für Stoffwechselkrankheiten an einem führenden Krankenhaus in Glasgow, Vizepräsident der British Association of Diabetes und Gründungsmitglied der International Diabetes Federation. Murray schrieb:
Paulescu, der angesehene rumänische Wissenschaftler, dem es zu dem Zeitpunkt, als das Team in Toronto mit seinen Forschungen begann, bereits gelungen war, das antidiabetische Hormon der Bauchspeicheldrüse zu extrahieren und seine Wirksamkeit bei der Verringerung der Hyperglykämie bei diabetischen Hunden zu beweisen, ist nicht ausreichend gewürdigt worden. ⓘ
In einer privaten Mitteilung brachte Professor Arne Tiselius, ehemaliger Leiter des Nobel-Instituts, seine persönliche Meinung zum Ausdruck, dass Paulescu den Preis 1923 ebenfalls verdient hatte. ⓘ
Funktion und Wirkung
Die Regulation der Konzentration von Glucose im Blut erfolgt durch einen Regelkreis aus zwei Hormonen, die abhängig von der Blutzuckerkonzentration ausgeschüttet werden. Insulin ist das einzige Hormon, das den Blutzuckerspiegel senken kann. Sein Gegenspieler ist das Glucagon, dessen Hauptaufgabe es ist, den Blutzuckerspiegel zu erhöhen. Auch Adrenalin, Kortisol und Schilddrüsenhormone haben blutzuckersteigernde Wirkungen. ⓘ
Der Blutzuckerspiegel steigt vor allem nach der Aufnahme von kohlenhydratreicher Nahrung. Als Reaktion darauf wird von den β-Zellen Insulin ins Blut ausgeschüttet. Insulin senkt den Blutzuckerspiegel dadurch, dass es mittels seiner „Schlüsselfunktion“ der Glucose aus dem Blutplasma und der Gewebsflüssigkeit den Durchtritt durch die Zellmembran in das Zellinnere ermöglicht. Vor allem die Leber- und Muskelzellen können in kurzer Zeit große Mengen Glucose aufnehmen und sie in Form von Glycogen speichern oder zur Energiegewinnung abbauen (siehe Glycolyse). ⓘ
Auch auf andere Zellen wirkt das Hormon, so hat es Einfluss auf den Fett- und Aminosäurestoffwechsel sowie auf den Kaliumhaushalt. ⓘ
Das Hormon ist wesentlicher Faktor folgender Erkrankungen:
- Diabetes mellitus
- Hyperinsulinismus
- Insulinom
- Insulinresistenz
- Metabolisches Syndrom ⓘ



Das im Blut zirkulierende Insulin entfaltet seine Wirkung durch Bindung an Insulinrezeptoren. ⓘ
Insulinrezeptor
Letztlich löst die Bindung dieses Hormons an seinen Rezeptor eine Reihe von Kinase-Kaskaden (Kaskade von Phosphorylierungsreaktionen) aus, die durch Signalwege beschrieben werden können. ⓘ
Diese Signalwege bewirken ein Sinken des Blutglucosespiegels durch
- Förderung der Glucose-Aufnahme (GLUT4-Translokation zur Zelloberfläche)
- Förderung der Glucose-Speicherung (Glycogensynthese) in der Leber und den Muskeln ⓘ
Dieses Signal wird durch die Aktivierung glucoseverbrauchender Wege unterstützt. Weitere unterstützende Maßnahmen bestehen in der Unterdrückung glucoseliefernder Wege, so zum Beispiel durch Abbau des second messenger cAMP über eine Phosphodiesterase. ⓘ
Glucoseaufnahme im Muskelgewebe
Das Hormon erhöht in der Muskulatur und im Fettgewebe die Permeabilität (Durchlässigkeit) der Zellmembran für Glucose. Dabei ist zu beachten, dass nicht die Membran selbst permeabler wird, sondern dass vermehrt Carrier-Proteine für Glucose aktiviert werden. Dieses Carrier-Protein ist GLUT4, ein hochaffiner, insulinabhängiger Glucose-Transporter, welcher die Glucose durch erleichterte Diffusion (passiver Transport) in die Zelle transportiert. Folgende physikalische Eigenschaften sind für GLUT4 relevant: sättigbar, nicht aktivierbar oder inaktivierbar, also Regulation nur durch insulinabhängigen Einbau oder Ausbau. ⓘ
Glucoseaufnahme und Stoffwechsel im Gehirn
Nervenzellen (und Erythrozyten) nehmen Glucose insulinunabhängig auf. Deshalb nehmen die insulinabhängigen Zellen bei einem erhöhten Insulinspiegel mehr Glucose auf, und für die insulinunabhängigen bleibt weniger übrig. ⓘ
Im Allgemeinen besteht bei Hypoglykämie die Gefahr, dass das auf Glucose angewiesene Nervensystem geschädigt wird. Insulin wird, verabreicht als Nasenspray in direktem Kontakt mit dem ZNS, zur Behandlung der Alzheimer-Krankheit untersucht. ⓘ
Auf- und Abbau von Fettgewebe
Das Hormon hemmt die Lipolyse im Fettgewebe und somit den Abbau von Fett. Ein Insulinmangel führt daher zu einer gesteigerten Lipolyse mit Bildung von Ketokörpern und einer daraus resultierenden Ketose. ⓘ
Förderung des Zellwachstums
Eine weitere zentrale Funktion des Peptidhormons Insulin besteht in der Regulation von Zellwachstum und Proliferation durch die Aktivierung der Transkription von Genen, die für Kontrolle und Ablauf des Zellzyklus von großer Bedeutung sind. Diese Insulinwirkung ist bei Diskursen über Insulinpräparate ein Thema. ⓘ
Tryptophan-Aufnahme im Gehirn
Höhere Insulinspiegel haben einen leicht steigernden Einfluss auf die Aufnahme von Tryptophan ins Gehirn. ⓘ
Gegenspieler
Fällt der Blutzuckerspiegel im Körper unter einen Wert von 80 mg/dl ab, wird die Insulinproduktion bereits stark reduziert. ⓘ
Sinkt der Blutzucker weiter ab, treten verschiedene Gegenspieler des Insulins auf:
Die Spiegel dieser gegenregulierenden Hormone steigen bereits deutlich an, wenn der Blutzucker unter 60 mg/dl absinkt. ⓘ
Beim Typ 1-Diabetes ist oft auch der Gegenregulationmechanismus gestört, was zu zusätzlichen Problemen mit Hypoglykämien führt. ⓘ
Somatostatin hat einen hemmenden Einfluss auf die Sekretion von Insulin und Glucagon, da er als allgemeiner Hemmer im Körper fungiert. ⓘ
Wirkung auf den Kaliumspiegel
Insulin senkt den Kaliumspiegel im Blut, indem es dafür sorgt, dass Kalium in das Zellinnere von Hepatozyten und Skelettmuskelzellen verlagert wird, also von extrazellulär nach intrazellulär. Dies erfolgt durch Aktivierung der Natrium-Kalium-ATPase durch Insulin. Insulinpräparate werden daher gemeinsam mit Glucose (zur Vermeidung einer Hypoglykämie) zur Behandlung einer Hyperkaliämie verwendet. ⓘ
Vorkommen
Insulinsequenzen von mehr als 100 verschiedenen Spezies sind bekannt. Die Proteinsequenzen der jeweiligen Insuline sind sich ähnlich – sie zeigen Sequenzhomologie – sind aber nicht identisch. Über die Unterschiede im chemischen Aufbau von Humaninsulin gegenüber den Insulinen einiger Säugetiere sowie Informationen zu künstlich hergestelltem Insulin siehe Insulinpräparat. ⓘ
Insulin und Evolution: Genotypen, die in Jäger- und Sammlergesellschaften einen raschen Abbau von Energiereserven bei Nahrungsmangel verhinderten, prädisponieren beim heutigen Lebensstil mit Bewegungsmangel und Nahrungsüberangebot zu Adipositas und Typ-2-Diabetes. ⓘ
Inwieweit Gene den Glucosestoffwechsel und die damit verbundene Wirkung von Insulin beeinflussen, ist noch nicht zur Gänze geklärt. ⓘ
Die Homologe des Insulins in Insekten sind die Drosophila Insulin-like Peptides. ⓘ
Bildung, Speicherung, Freisetzung und Regulierung
Speicherung

Die Insulinmoleküle werden in den Vesikeln des Golgi-Apparats, der an der Zellmembran der β-Zelle liegt, durch Zink-Ionen zu Hexameren gebunden und so stabilisiert gespeichert (Zink-Insulin-Komplex). ⓘ
Die hohe Bindungsfreudigkeit von Insulinmolekülen an Zink hat mehrere wichtige Auswirkungen. Insulin ist in der Form von Hexameren und nach dem Zerfall in Dimere noch nicht wirksam, sondern nur als Einzelmolekül. Diese Eigenschaft spielt bei den Insulinpräparaten eine wichtige Rolle. Bei schnellwirkenden Insulinpräparaten ist der zu langsame Zerfall der Molekülverbände unerwünscht und es wird nach Möglichkeiten gesucht den Zerfall zu beschleunigen. Bei langwirkenden Insulinpräparaten wird die Zinkbindung zur Verlängerung der Wirkdauer durch hohe Zinkkonzentrationen gezielt verstärkt. Bei der Entwicklung von oralen Insulinpräparaten wird die Zinkbindung zur Kopplung von Insulin an Transportmoleküle genutzt. ⓘ
Missbrauch von Insulin
Insulin steht auf der Liste der verbotenen Doping-Substanzen, da es zu mehreren Zwecken missbraucht werden kann. Da Insulin der durch Somatropin verringerten Glucoseaufnahme in die Muskelzellen entgegenwirkt, wird es oft zur Kompensation dessen unerwünschter Nebenwirkung verwendet (siehe Anabolikum). Andere Anwendungen sind die Förderung der Füllung der Glycogenspeicher bei Ausdauersportlern und die Unterstützung des Aufbaus von Muskelmasse. ⓘ
Die missbräuchliche Selbstverabreichung von Insulin, um den Blutzuckerspiegel übermäßig abzusenken, führt zum Krankheitsbild der Hypoglycaemia factitia. ⓘ
Im März 2008 wurde der Krankenpfleger Colin Norris in Newcastle zu einer Freiheitsstrafe von 30 Jahren verurteilt, weil er vier seiner Patientinnen durch Injektion zu hoher Insulindosen ermordet hatte. ⓘ