Herzinsuffizienz
| Herzversagen ⓘ | |
|---|---|
| Andere Bezeichnungen | Kongestive Herzinsuffizienz (CHF), kongestive Herzinsuffizienz (CCF) |
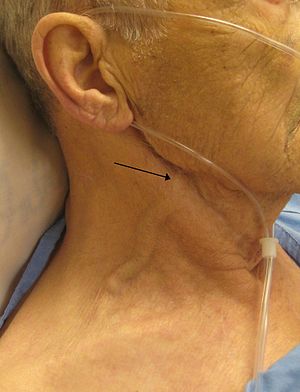 | |
| Ein Mann mit kongestiver Herzinsuffizienz und ausgeprägter Dehnung der Jugularvenen. Die äußere Jugularvene ist durch einen Pfeil markiert. | |
| Fachgebiet | Kardiologie |
| Symptome | Kurzatmigkeit, Müdigkeitsgefühl, Beinschwellung |
| Dauer | In der Regel lebenslang |
| Ursachen | Herzinfarkt, Bluthochdruck, Herzrhythmusstörungen, übermäßiger Alkoholkonsum, Infektionen, Herzschäden |
| Risikofaktoren | Rauchen, Bewegungsmangel, Passivrauchen |
| Diagnostische Methode | Echokardiogramm |
| Differentialdiagnose | Nierenversagen, Schilddrüsenerkrankung, Lebererkrankung, Anämie, Fettleibigkeit |
| Medikation | Diuretika, Herzmedikamente |
| Häufigkeit | 40 Millionen (2015), 1-2 % der Erwachsenen (entwickelte Länder) |
| Todesfälle | 35% Sterberisiko im ersten Jahr |
Herzinsuffizienz (HF), auch bekannt als kongestive Herzinsuffizienz (CHF) und (kongestive) Herzinsuffizienz (CCF), ist eine Reihe von Symptomen, die durch das Versagen der Pumpfunktion des Herzens zur Unterstützung des Blutflusses durch den Körper verursacht werden. Die Anzeichen und Symptome der Herzinsuffizienz sind auf eine strukturelle und/oder funktionelle Anomalie des Herzens zurückzuführen. Durch diese Anomalie wird das Herz daran gehindert, sich bei jedem Herzschlag mit Blut zu füllen und Blut auszustoßen. Zu den Anzeichen und Symptomen einer Herzinsuffizienz gehören in der Regel Kurzatmigkeit, übermäßige Müdigkeit und Beinschwellungen. Die Kurzatmigkeit verschlimmert sich in der Regel bei Bewegung oder im Liegen und kann die Betroffenen nachts aufwecken. Auch eine eingeschränkte Belastbarkeit ist ein häufiges Merkmal. Schmerzen in der Brust, einschließlich Angina pectoris, treten in der Regel nicht aufgrund einer Herzinsuffizienz auf. ⓘ
Häufige Ursachen für eine Herzinsuffizienz sind koronare Herzkrankheiten, einschließlich eines früheren Myokardinfarkts (Herzinfarkts), Bluthochdruck, Vorhofflimmern, Herzklappenerkrankungen, übermäßiger Alkoholkonsum, Infektionen und eine Kardiomyopathie unbekannter Ursache. Diese verursachen eine Herzinsuffizienz, indem sie entweder die Struktur oder die Funktion des Herzens verändern. Es gibt zwei Arten der linksventrikulären Herzinsuffizienz: die Herzinsuffizienz mit reduzierter Auswurffraktion (HFrEF oder systolische Herzinsuffizienz) und die Herzinsuffizienz mit erhaltener Auswurffraktion (HFpEF oder diastolische Herzinsuffizienz). Diese Arten der Herzinsuffizienz werden von einer medizinischen Fachkraft anhand der Kontraktions- und Entspannungsfunktion der linken Herzkammer eines Patienten diagnostiziert. Der Schweregrad der Herzinsuffizienz wird nach der Schwere der Symptome bei körperlicher Belastung eingestuft. ⓘ
Herzinsuffizienz ist nicht dasselbe wie ein Herzinfarkt (bei dem ein Teil des Herzmuskels aufgrund eines Gerinnsels in den Arterien, die das Herz versorgen, abstirbt) oder ein Herzstillstand (bei dem der Blutfluss aufgrund der Unfähigkeit des Herzens, effektiv zu pumpen, vollständig zum Stillstand kommt). Andere Krankheiten, die ähnliche Symptome wie eine Herzinsuffizienz aufweisen können, sind Fettleibigkeit, Nierenversagen, Leberprobleme, Anämie und Schilddrüsenerkrankungen. Die Diagnose basiert auf Symptomen, körperlichen Befunden und einer Echokardiografie. Bluttests, Elektrokardiographie und Röntgenaufnahmen des Brustkorbs können nützlich sein, um die zugrunde liegende Ursache zu ermitteln. ⓘ
Die Behandlung richtet sich nach dem Schweregrad und der Ursache der Erkrankung. Bei Menschen mit chronischer, stabiler und leichter Herzinsuffizienz besteht die Behandlung in der Regel aus einer Änderung der Lebensweise, wie z. B. dem Verzicht auf das Rauchen, körperlicher Bewegung und einer Umstellung der Ernährung, sowie aus Medikamenten. Bei einer Herzinsuffizienz aufgrund einer linksventrikulären Dysfunktion werden Angiotensin-Converting-Enzym-Hemmer, Angiotensin-Rezeptorblocker oder Valsartan/Sacubitril zusammen mit Betablockern empfohlen. Bei schwerer Erkrankung können Aldosteronantagonisten oder Hydralazin mit einem Nitrat eingesetzt werden. Diuretika sind nützlich, um Flüssigkeitsansammlungen und die daraus resultierende Kurzatmigkeit zu verhindern. Je nach Ursache kann manchmal ein implantiertes Gerät wie ein Herzschrittmacher oder ein implantierbarer Herzdefibrillator empfohlen werden. In einigen mittelschweren oder schweren Fällen kann eine kardiale Resynchronisationstherapie (CRT) oder eine Modulation der kardialen Kontraktilität von Nutzen sein. Bei einer schweren Erkrankung, die trotz aller anderen Maßnahmen fortbesteht, kann ein Herzunterstützungssystem (für die linke, rechte oder beide Herzkammern) oder gelegentlich eine Herztransplantation empfohlen werden. ⓘ
Herzinsuffizienz ist eine häufige, kostspielige und potenziell tödliche Erkrankung, die bei älteren Erwachsenen die häufigste Ursache für Krankenhausaufenthalte und Wiedereinweisungen ist. Eine Herzinsuffizienz führt oft zu drastischeren gesundheitlichen Beeinträchtigungen als das Versagen anderer, ähnlich komplexer Organe wie Nieren oder Leber. Im Jahr 2015 waren weltweit etwa 40 Millionen Menschen davon betroffen. Insgesamt leiden etwa 2 % der Erwachsenen an Herzinsuffizienz, bei den über 65-Jährigen sind es sogar 6-10 %. Prognosen zufolge werden die Raten weiter steigen. Das Sterberisiko liegt im ersten Jahr nach der Diagnose bei etwa 35 %, während das Sterberisiko im zweiten Jahr bei denjenigen, die noch leben, unter 10 % liegt. Dieses Sterberisiko ist ähnlich hoch wie bei anderen Krebsarten. Im Vereinigten Königreich ist die Krankheit der Grund für 5 % der Notfalleinlieferungen in Krankenhäuser. Die Herzinsuffizienz ist bereits seit dem Altertum bekannt und wurde bereits um 1550 v. Chr. im Papyrus Ebers beschrieben. ⓘ
| Klassifikation nach ICD-10 ⓘ | |
|---|---|
| I11.0- | Hypertensive Herzkrankheit mit (kongestiver) Herzinsuffizienz |
| I13.0- | Hypertensive Herz- und Nierenkrankheit mit (kongestiver) Herzinsuffizienz |
| I50.0- | Rechtsherzinsuffizienz |
| I50.1- | Linksherzinsuffizienz |
| I50.9 | Herzinsuffizienz, nicht näher bezeichnet |
| R57.0 | Kardiogener Schock |
| ICD-10 online (WHO-Version 2019) | |
Die Herzinsuffizienz (von „Insuffizienz“ im Sinne von „Unzulänglichkeit“; in der Medizin unter anderem ungenügende Leistungsfähigkeit eines Organs; lateinisch Insufficientia cordis) oder Herzschwäche ist die krankhafte Unfähigkeit des Herzens, das vom Körper benötigte Herzzeitvolumen ohne Anstieg des enddiastolischen Drucks zu fördern. Die „Pumpschwäche“ äußert sich in reduzierter körperlicher und geistiger Leistungsfähigkeit, man spricht auch von Vorwärtsversagen. ⓘ
Nicht weniger relevant sind die Symptome des Rückwärtsversagens: Zur Steigerung der Herzleistung vergrößert der Körper seinen Wasserbestand, was bei Schwäche des rechten Herzens zu Wassereinlagerungen in den Beinen führt. Bei Schwäche des linken Herzens sammelt sich Wasser in der Lunge an, das sich, insbesondere im Liegen, als Atemnot bemerkbar macht und in schweren Fällen die Sauerstoffaufnahme lebensbedrohlich einschränkt. Deswegen bezeichnete man die Herzinsuffizienz und auch die darauf basierende Niereninsuffizienz früher gemeinsam als Wassersucht oder Hydrops. ⓘ
Die Herzinsuffizienz ist die gemeinsame Endstrecke vieler Herzerkrankungen, wobei langjähriger Bluthochdruck und atherosklerotische Verengungen der herzversorgenden Gefäße (also koronare Herzkrankheit und abgelaufene Herzinfarkte) die häufigsten Ursachen sind. In der Therapie spielen neben der Behandlung und Beseitigung von zugrundeliegenden Krankheiten und Risikofaktoren bestimmte Blutdrucksenker eine große Rolle, da sie nachweislich die Überlebenszeit verlängern. ⓘ
Die fortgeschrittene Herzinsuffizienz zeigt oft einen schubartigen Verlauf mit wiederkehrenden Dekompensationen, bei denen die Betroffenen bedrohlich viel Wasser einlagern und damit auch ihr Herz „überladen“. Diese kardiale Dekompensation ist ein häufiger Grund für Krankenhausbehandlungen. Sie kann oft mit harntreibenden Medikamenten und gegebenenfalls mit intensivmedizinischer Behandlung beherrscht werden, aber auch zum Tod aus relativer Gesundheit heraus führen. Die Herzinsuffizienz ist eine häufige Krankheit mit hoher Sterblichkeit und zählt entsprechend zu den häufigsten Todesursachen. ⓘ
Klassifizierung
Bei der Herzinsuffizienz handelt es sich nicht um eine Krankheit, sondern um ein Syndrom, d. h. um ein Bündel von Anzeichen und Symptomen, die durch die Beeinträchtigung der Pumpfunktion des Herzens zur Unterstützung des Kreislaufs in Ruhe oder bei Belastung verursacht werden. Es entwickelt sich, wenn sich das Herz während der Diastole nicht richtig mit Blut füllen kann, was zu einem Anstieg des intrakardialen Drucks oder zum Ausstoßen des Blutes während der Systole führt, wodurch die Herzleistung für den Rest des Körpers verringert wird. Eine Füllungsstörung und ein hoher intrakardialer Druck können zu Flüssigkeitsansammlungen in den Venen und Geweben führen. Dies äußert sich in Wassereinlagerungen und Schwellungen aufgrund von Flüssigkeitsansammlungen (Ödemen), die als Stauung bezeichnet werden. Eine gestörte Auswurfleistung kann zu einer unzureichenden Durchblutung des Körpergewebes führen und eine Ischämie verursachen. ⓘ
Anzeichen und Symptome
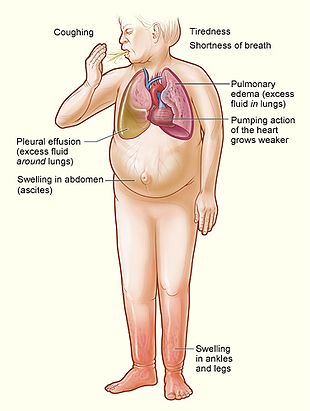
Herzinsuffizienz ist ein pathophysiologischer Zustand, bei dem die Herzleistung nicht ausreicht, um die Bedürfnisse des Körpers und der Lungen zu erfüllen. Der Begriff "kongestive Herzinsuffizienz" wird häufig verwendet, da eines der häufigsten Symptome eine Stauung oder Flüssigkeitsansammlung im Gewebe und in den Venen der Lunge oder anderer Körperteile ist. Die Stauung äußert sich insbesondere in Form von Wassereinlagerungen und Schwellungen (Ödemen), sowohl in Form von peripheren Ödemen (die geschwollene Gliedmaßen und Füße verursachen) als auch in Form von Lungenödemen (die Atembeschwerden verursachen) und Aszites (geschwollener Bauch). ⓘ
Die Symptome der Herzinsuffizienz werden traditionell in links- und rechtsseitig eingeteilt, da die linke und die rechte Herzkammer unterschiedliche Teile des Kreislaufs versorgen, doch treten bei den Betroffenen häufig beide Arten von Anzeichen und Symptomen auf. ⓘ
Die linke Seite des Herzens nimmt sauerstoffreiches Blut aus den Lungen auf und pumpt es in den systemischen Kreislauf (den Rest des Körpers mit Ausnahme des Lungenkreislaufs) weiter. Ein Versagen der linken Herzhälfte führt zu einem Rückstau des Blutes in die Lunge, was aufgrund der unzureichenden Versorgung mit sauerstoffreichem Blut Atembeschwerden und Müdigkeit verursacht. Häufige Anzeichen für die Atmung sind eine erhöhte Atemfrequenz und eine erhöhte Atemarbeit (unspezifische Anzeichen für Atemnot). Rasselgeräusche oder Knistergeräusche, die zunächst in den Lungenbasen und bei starker Ausprägung in allen Lungenfeldern zu hören sind, deuten auf die Entwicklung eines Lungenödems (Flüssigkeit in den Alveolen) hin. Zyanose, die auf einen schweren Sauerstoffmangel im Blut hinweist, ist ein spätes Anzeichen für ein extrem schweres Lungenödem. ⓘ
Weitere Anzeichen, die auf eine linksventrikuläre Insuffizienz hinweisen, sind ein seitlich verschobener Apex-Schlag (der auftritt, wenn das Herz vergrößert ist) und ein Gallop-Rhythmus (zusätzliche Herztöne), der als Zeichen eines erhöhten Blutflusses oder eines erhöhten intrakardialen Drucks gehört werden kann. Herzgeräusche können auf das Vorliegen einer Herzklappenerkrankung hinweisen, entweder als Ursache (z. B. Aortenstenose) oder als Folge (z. B. Mitralinsuffizienz) einer Herzinsuffizienz. ⓘ
Die Rückwärtsinsuffizienz der linken Herzkammer führt zu einer Verstopfung der Blutgefäße in der Lunge, so dass die Symptome vorwiegend respiratorischer Natur sind. Die Rückwärtsinsuffizienz kann unterteilt werden in das Versagen des linken Vorhofs, der linken Herzkammer oder beider im linken Kreislauf. Die Betroffenen leiden unter Dyspnoe (Kurzatmigkeit) bei Anstrengung und in schweren Fällen auch unter Dyspnoe in Ruhe. Es kommt zu einer zunehmenden Atemnot im Liegen, die als Orthopnoe bezeichnet wird. Sie wird oft an der Anzahl der Kissen gemessen, die erforderlich sind, um bequem zu liegen, und bei Orthopnoe kann der Betroffene darauf zurückgreifen, im Sitzen zu schlafen. Ein weiteres Symptom der Herzinsuffizienz ist die paroxysmale nächtliche Dyspnoe: ein plötzlicher nächtlicher Anfall von schwerer Atemnot, meist mehrere Stunden nach dem Einschlafen. Leichte Ermüdbarkeit und Belastungsunverträglichkeit sind ebenfalls häufige Beschwerden im Zusammenhang mit der Atemwegserkrankung. ⓘ
"Eine Beeinträchtigung der linksventrikulären Vorwärtsfunktion kann zu Symptomen einer schlechten systemischen Zirkulation wie Schwindel, Verwirrtheit und kühlen Extremitäten in Ruhe führen. ⓘ
Rechtsseitiges Versagen
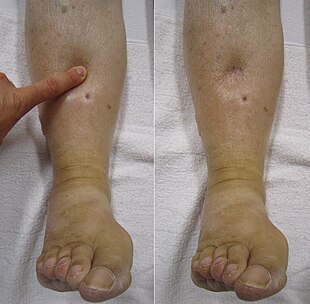
Die rechtsseitige Herzinsuffizienz wird häufig durch eine pulmonale Herzerkrankung (Cor pulmonale) verursacht, die typischerweise durch Störungen des Lungenkreislaufs, wie z. B. pulmonale Hypertonie oder Pulmonalstenose, hervorgerufen wird. Bei der körperlichen Untersuchung kann man ein peripheres Lochödem, Aszites, eine vergrößerte Leber und eine vergrößerte Milz feststellen. Der juguläre Venendruck wird häufig als Marker für den Flüssigkeitsstatus bestimmt, der durch Auslösen eines hepato-jugulären Refluxes verstärkt werden kann. Wenn der rechtsventrikuläre Druck erhöht ist, kann eine parasternale Hebung vorliegen, die auf eine kompensatorische Erhöhung der Kontraktionskraft hinweist. ⓘ
Die Rückwärtsinsuffizienz des rechten Ventrikels führt zu einer Verstopfung der systemischen Kapillaren. Dies führt zu einer übermäßigen Ansammlung von Flüssigkeit im Körper. Dies führt zu Schwellungen unter der Haut (als periphere Ödeme oder Anasarka bezeichnet) und betrifft in der Regel zuerst die abhängigen Körperteile (Fuß- und Knöchelschwellungen bei Menschen, die aufrecht stehen, und Sakralödeme bei Menschen, die überwiegend liegen). Nachturie (häufiges nächtliches Wasserlassen) kann auftreten, wenn nachts im Liegen Flüssigkeit aus den Beinen in den Blutkreislauf zurückgeführt wird. In zunehmend schweren Fällen kann es zu Aszites (Flüssigkeitsansammlung in der Bauchhöhle, die eine Schwellung verursacht) und einer Lebervergrößerung kommen. Eine erhebliche Leberstauung kann zu einer Beeinträchtigung der Leberfunktion (kongestive Hepatopathie) führen, und es können Gelbsucht und sogar Koagulopathie (Probleme mit verminderter oder erhöhter Blutgerinnung) auftreten. ⓘ
Biventrikuläres Versagen
Dumpfheit der Lungenfelder beim Abklopfen mit dem Finger und verminderte Atemgeräusche an der Lungenbasis können auf die Entwicklung eines Pleuraergusses (Flüssigkeitsansammlung zwischen Lunge und Brustwand) hinweisen. Obwohl er bei isolierter links- oder rechtsseitiger Herzinsuffizienz auftreten kann, ist er bei biventrikulärer Insuffizienz häufiger, da Pleuralvenen sowohl in das systemische als auch in das pulmonale Venensystem entwässern. Bei einseitigem Auftreten sind die Ergüsse häufig rechtsseitig. ⓘ
Wenn eine Person mit einem Versagen eines Ventrikels lange genug lebt, neigt sie dazu, ein Versagen beider Ventrikel zu entwickeln. Bei einer Linksherzinsuffizienz können beispielsweise ein Lungenödem und eine pulmonale Hypertonie auftreten, die die Belastung des rechten Ventrikels erhöhen. Eine rechtsventrikuläre Insuffizienz ist für die andere Seite nicht so schädlich, aber auch nicht harmlos. ⓘ
Ursachen
Es ist wichtig zu wissen, dass die Herzinsuffizienz keine eigenständige Krankheit ist, sondern ein Syndrom, das durch eine andere Krankheit verursacht wird. Daher ist es für die Diagnose und Behandlung von entscheidender Bedeutung, die Ursache der Herzinsuffizienz zu ermitteln. Der Herzmuskel ist entweder zu schwach, um effizient zu pumpen, oder nicht elastisch genug. ⓘ
Die Herzinsuffizienz ist das potenzielle Endstadium aller Erkrankungen des Herzens. Häufige Ursachen für eine Herzinsuffizienz sind koronare Herzkrankheiten, einschließlich eines früheren Myokardinfarkts (Herzinfarkts), Bluthochdruck, Vorhofflimmern, Herzklappenerkrankungen, übermäßiger Alkoholkonsum, Infektionen und Kardiomyopathie mit unbekannter Ursache. Darüber hinaus können Virusinfektionen des Herzens zu einer Entzündung der Herzmuskelschicht führen und in der Folge zur Entwicklung einer Herzinsuffizienz beitragen. Die genetische Veranlagung spielt eine wichtige Rolle. Liegt mehr als eine Ursache vor, ist ein Fortschreiten der Krankheit wahrscheinlicher und die Prognose ist schlechter. Herzschäden können eine Person dazu prädisponieren, später im Leben eine Herzinsuffizienz zu entwickeln, und haben viele Ursachen, darunter systemische Virusinfektionen (z. B. HIV), Chemotherapeutika wie Daunorubicin, Cyclophosphamid, Trastuzumab und Störungen durch den Konsum von Substanzen wie Alkohol, Kokain und Methamphetamin. Eine seltene Ursache ist die Exposition gegenüber bestimmten Toxinen wie Blei und Kobalt. Auch infiltrative Erkrankungen wie Amyloidose und Bindegewebserkrankungen wie systemischer Lupus erythematodes haben ähnliche Folgen. Obstruktive Schlafapnoe (eine Schlafstörung, bei der sich Atemstörungen mit Fettleibigkeit, Bluthochdruck und/oder Diabetes überlagern) gilt als unabhängige Ursache für Herzversagen. Jüngste Berichte aus klinischen Studien haben auch einen Zusammenhang zwischen Blutdruckschwankungen und Herzinsuffizienz sowie kardialen Veränderungen, die zu einer Herzinsuffizienz führen können, hergestellt. ⓘ
Hochgradige Herzinsuffizienz
Zu einer Herzinsuffizienz kann es auch kommen, wenn die gepumpte Blutmenge über das normale Maß hinausgeht und das Herz nicht in der Lage ist, damit Schritt zu halten. Dies kann bei Überlastungssituationen (z. B. Blut- oder Seruminfusionen), Nierenerkrankungen, chronischer schwerer Anämie, Beriberi (Vitamin-B1/Thiamin-Mangel), Schilddrüsenüberfunktion, Leberzirrhose, Morbus Paget, Multiplem Myelom, arteriovenösen Fisteln oder arteriovenösen Malformationen auftreten. ⓘ
Akute Dekompensation

Eine chronisch stabile Herzinsuffizienz kann leicht dekompensieren. Dies ist meist die Folge einer gleichzeitigen Erkrankung (z. B. eines Myokardinfarkts (Herzinfarkts) oder einer Lungenentzündung), von Herzrhythmusstörungen, unkontrolliertem Bluthochdruck oder der Nichteinhaltung einer Flüssigkeitsrestriktion, einer Diät oder von Medikamenten. Weitere Faktoren, die die Herzinsuffizienz verschlimmern können, sind: Anämie, Schilddrüsenüberfunktion, übermäßige Flüssigkeits- oder Salzzufuhr und Medikamente wie NSAIDs und Thiazolidindione. NSAIDs erhöhen das Risiko um das Doppelte. ⓘ
Medikamente
Eine Reihe von Medikamenten kann die Krankheit auslösen oder verschlimmern. Dazu gehören NSAIDS, COX-2-Hemmer, eine Reihe von Narkosemitteln wie Ketamin, Thiazolidindione, einige Krebsmedikamente, verschiedene Antiarrhythmika, Pregabalin, Alpha-2-Adrenorezeptor-Agonisten, Minoxidil, Itraconazol, Cilostazol, Anagrelid, Stimulanzien (z. B., Methylphenidat), trizyklische Antidepressiva, Lithium, Antipsychotika, Dopamin-Agonisten, TNF-Hemmer, Kalziumkanalblocker (insbesondere Verapamil und Diltiazem), Salbutamol und Tamsulosin. ⓘ
Indem sie die Bildung von Prostaglandinen hemmen, können NSAIDs die Herzinsuffizienz durch mehrere Mechanismen verschlimmern, einschließlich der Förderung von Flüssigkeitsretention, der Erhöhung des Blutdrucks und der Verringerung des Ansprechens auf harntreibende Medikamente. In ähnlicher Weise empfiehlt die ACC/AHA die Einnahme von COX-2-Hemmern bei Menschen mit Herzinsuffizienz nicht. Thiazolidindione werden stark mit neuen Fällen von Herzinsuffizienz und der Verschlimmerung einer bereits bestehenden Herzinsuffizienz in Verbindung gebracht, da sie mit einer Gewichtszunahme und Flüssigkeitsretention einhergehen. Bestimmte Kalziumkanalblocker wie Diltiazem und Verapamil sind dafür bekannt, dass sie die Kraft, mit der das Herz das Blut ausstößt, vermindern und werden daher bei Menschen mit Herzinsuffizienz mit verminderter Auswurffraktion nicht empfohlen. ⓘ
Ergänzungen
Bestimmte alternative Arzneimittel bergen das Risiko, eine bestehende Herzinsuffizienz zu verschlimmern, und werden daher nicht empfohlen. Dazu gehören Eisenhut, Ginseng, Gossypol, Gynura, Süßholz, Maiglöckchen, Tetrandrin und Yohimbin. Eisenhut kann eine abnorm langsame Herzfrequenz und abnormale Herzrhythmen wie ventrikuläre Tachykardie verursachen. Ginseng kann zu anormal niedrigem oder hohem Blutdruck führen und die Wirkung von harntreibenden Medikamenten beeinträchtigen. Gossypol kann die Wirkung von Diuretika verstärken, was zu Toxizität führen kann. Gynura kann zu niedrigem Blutdruck führen. Süßholz kann eine Herzinsuffizienz verschlimmern, indem es den Blutdruck erhöht und die Flüssigkeitsretention fördert. Maiglöckchen können über einen ähnlichen Mechanismus wie Digoxin eine abnorm langsame Herzfrequenz verursachen. Tetrandrin kann durch Hemmung der L-Typ-Calciumkanäle zu niedrigem Blutdruck führen. Yohimbin kann eine Herzinsuffizienz verschlimmern, indem es über einen Alpha-2-Adrenorezeptor-Antagonismus den Blutdruck erhöht. ⓘ
Pathomechanismus

Durch das im Zuge der Herzinsuffizienz abnehmende Herzzeitvolumen kommt es zu einer unzureichenden Durchblutung der Organe. Als Reaktion darauf werden Kompensationsmechanismen aktiviert, die die Versorgung der Organe mit sauerstoffreichem Blut gewährleisten sollen. Dazu zählt die vermehrte Ausschüttung von Hormonen wie Adrenalin und Noradrenalin, die die Schlagkraft des Herzens steigern und über eine Engstellung der Gefäße den Blutdruck erhöhen. Angiotensin II und Aldosteron, die Effektorhormone des Renin-Angiotensin-Aldosteron-Systems (RAAS), führen zu einer Steigerung des Blutvolumens und ebenfalls zur Erhöhung des Blutdrucks. Obwohl die genannten Mechanismen vorübergehend zum Erhalt der Organdurchblutung notwendig sind, führen sie doch langfristig zu einer Schädigung des Herzens und einem Fortschreiten der Erkrankung. So führen sie im Herzen zu einer Verdickung der Muskulatur (Hypertrophie; „Die Hypertrophie bewirkt die Kompensation eines Klappenfehlers.“). Diese ist zunächst hilfreich, um eine vermehrte Pumparbeit leisten zu können. Daneben kommt es zu vermehrtem Einbau von Bindegewebe (Fibrose). Beide Prozesse gemeinsam werden auch als kardiales Remodeling bezeichnet. Die zellulären Mechanismen, die dem Remodeling zu Grunde liegen, sind Gegenstand intensiver Forschung. Unter anderem werden eine veränderte Genexpression, die Aktivierung intrazellulärer Signalwege, z. B. von MAP-Kinasen, und die Veränderung des Calcium-Stoffwechsels sowie des Energiestoffwechsels untersucht. Neuere Untersuchungen lieferten außerdem Hinweise auf eine Beteiligung von epigenetischen Veränderungen. Aldosteron-Antagonisten wie Spironolacton werden in der Therapie der Herzinsuffizienz eingesetzt, da sie dem Remodeling entgegenwirken. ⓘ
Solange das Herz der erhöhten Anforderung gerecht werden kann, spricht man von kompensierter Herzinsuffizienz. Die Vergrößerung des Blutvolumens bewirkt eine stärkere Füllung des Herzens und damit über den Frank-Starling-Mechanismus ein größeres Schlagvolumen. Dieser Mechanismus ist allerdings durch das Laplace-Gesetz begrenzt, nach dem eine größere Herzweite eine größere Muskelspannung erfordert. Im Ergebnis führt ab einem bestimmten Punkt eine Zunahme der Herzfüllung zu einer Abnahme des Schlagvolumens. Während ein gesundes Herz stets unterhalb dieses Punkts operiert, wird diese Reserve bei einer unbehandelten Herzinsuffizienz ausgeschöpft. Bei einer dekompensierten Herzinsuffizienz wird das Herz über den Punkt des maximalen Schlagvolumens hinaus beladen, sodass sich das Herzzeitvolumen in diesem Fall durch eine Verkleinerung des Blutvolumens steigern lässt. Kurzzeitig lässt sich die Füllung des Herzens über eine aufrechte Körperhaltung (keine Schocklagerung!) oder einen unblutigen Aderlass mindern, letztlich muss das Blutvolumen über eine Therapie mit entwässernden Medikamenten verringert werden. ⓘ
Bei Überdehnung schüttet das Herz natriuretische Peptide aus. Diese wirken gefäßerweiternd und harntreibend und stellen somit ein Gegengewicht zum Renin-Angiotensin-Aldosteron-System dar. Die natriuretischen Peptide werden von dem Enzym Neprilysin abgebaut. Mit dem Neprilysin-Hemmer Sacubitril steht neuerdings ein Arzneistoff zur Verfügung, der den körpereigenen Schutzmechanismus gegen eine Überlastung des Herzens verstärkt. ⓘ
Eine Herzinsuffizienz wird durch jeden Zustand verursacht, der die Leistungsfähigkeit des Herzmuskels durch Schädigung oder Überlastung verringert. Im Laufe der Zeit führt diese erhöhte Arbeitsbelastung, die durch eine langfristige Aktivierung neurohormonaler Systeme wie dem Renin-Angiotensin-System vermittelt wird, zu Fibrose, Dilatation und strukturellen Veränderungen der Form des linken Ventrikels von elliptisch zu kugelförmig. ⓘ
Das Herz eines Menschen mit Herzinsuffizienz kann aufgrund einer Überlastung des Ventrikels eine verminderte Kontraktionskraft aufweisen. Bei einem normalen Herzen führt eine verstärkte Füllung des Ventrikels zu einer erhöhten Kontraktionskraft durch das Frank-Starling-Gesetz des Herzens und damit zu einem Anstieg des Herzzeitvolumens. Bei einer Herzinsuffizienz versagt dieser Mechanismus, da der Ventrikel so stark mit Blut gefüllt ist, dass die Kontraktion des Herzmuskels weniger effizient wird. Dies ist auf die verminderte Fähigkeit zurückzuführen, die Aktin- und Myosinfilamente im überdehnten Herzmuskel zu vernetzen. ⓘ
Diagnose
Es gibt keine Diagnosekriterien, die als Goldstandard für Herzinsuffizienz gelten. Das National Institute for Health and Care Excellence empfiehlt die Messung des natriuretischen Hirnpeptids (BNP) und bei positivem Ergebnis eine Ultraschalluntersuchung des Herzens. Dies wird für Patienten mit Kurzatmigkeit empfohlen. Bei Patienten mit einer sich verschlimmernden Herzinsuffizienz werden sowohl ein BNP- als auch ein Troponin-Test empfohlen, um den wahrscheinlichen Ausgang der Erkrankung zu bestimmen. ⓘ
Klassifizierung
Eine historische Methode zur Kategorisierung der Herzinsuffizienz ist die Einteilung nach der betroffenen Herzseite (Linksherzinsuffizienz versus Rechtsherzinsuffizienz). Man ging davon aus, dass die Rechtsherzinsuffizienz die Durchblutung der Lunge beeinträchtigt, während die Linksherzinsuffizienz die Durchblutung der Aorta und damit des Gehirns und des übrigen Körperkreislaufs beeinträchtigt. Allerdings sind Mischformen häufig, und die Linksherzinsuffizienz ist eine häufige Ursache der Rechtsherzinsuffizienz. ⓘ
Eine genauere Klassifizierung der Art der Herzinsuffizienz erfolgt durch die Messung der Auswurffraktion, d. h. des Anteils des Blutes, das während einer einzigen Kontraktion aus dem Herzen gepumpt wird. Die Auswurffraktion wird als Prozentsatz angegeben, wobei der normale Bereich zwischen 50 und 75 % liegt. Es werden zwei Arten unterschieden: 1) Herzinsuffizienz aufgrund einer reduzierten Auswurffraktion (HFrEF): Nicht mehr empfohlene Synonyme sind "Herzinsuffizienz aufgrund einer linksventrikulären systolischen Dysfunktion" und "systolische Herzinsuffizienz". HFrEF ist mit einer Auswurffraktion von weniger als 40 % verbunden. ⓘ
2) Herzinsuffizienz mit erhaltener Auswurffraktion (HFpEF): Zu den nicht mehr empfohlenen Synonymen gehören "diastolische Herzinsuffizienz" und "Herzinsuffizienz mit normaler Auswurffraktion". HFpEF tritt auf, wenn sich der linke Ventrikel während der Systole normal kontrahiert, aber der Ventrikel steif ist und sich während der Diastole nicht normal entspannt, was die Füllung beeinträchtigt. ⓘ
Die Herzinsuffizienz kann auch als akut oder chronisch eingestuft werden. Die chronische Herzinsuffizienz ist ein langfristiger Zustand, der in der Regel durch die Behandlung der Symptome stabil gehalten wird. Die akute dekompensierte Herzinsuffizienz ist eine Verschlimmerung der Symptome einer chronischen Herzinsuffizienz, die zu akuter Atemnot führen kann. Eine hochgradige Herzinsuffizienz kann auftreten, wenn eine erhöhte kardiale Belastung vorliegt, die zu einem erhöhten diastolischen Druck in der linken Herzkammer führt, der sich zu einer Lungenstauung (Lungenödem) entwickeln kann. ⓘ
Mehrere Begriffe stehen in engem Zusammenhang mit der Herzinsuffizienz und können die Ursache für die Herzinsuffizienz sein, sollten aber nicht mit ihr verwechselt werden. Herzstillstand und Asystolie beziehen sich auf Situationen, in denen überhaupt keine Herzleistung mehr erbracht wird. Ohne dringende Behandlung führen sie zum plötzlichen Tod. Myokardinfarkt ("Herzinfarkt") bezeichnet eine Schädigung des Herzmuskels aufgrund unzureichender Blutzufuhr, in der Regel als Folge einer verstopften Koronararterie. Kardiomyopathie bezieht sich speziell auf Probleme innerhalb des Herzmuskels, und diese Probleme können zu Herzversagen führen. Ischämische Kardiomyopathie bedeutet, dass die Ursache der Muskelschädigung eine koronare Herzkrankheit ist. Dilatative Kardiomyopathie bedeutet, dass die Muskelschädigung zu einer Vergrößerung des Herzens geführt hat. Bei der hypertrophen Kardiomyopathie kommt es zu einer Vergrößerung und Verdickung des Herzmuskels. ⓘ
Ultraschall
Zur Untermauerung der klinischen Diagnose einer Herzinsuffizienz wird in der Regel die Echokardiographie eingesetzt. Bei diesem Verfahren werden mit Ultraschall das Schlagvolumen (SV, die Blutmenge im Herzen, die bei jedem Schlag die Herzkammern verlässt), das enddiastolische Volumen (EDV, die Gesamtblutmenge am Ende der Diastole) und das SV im Verhältnis zum EDV bestimmt, ein Wert, der als Auswurffraktion (EF) bezeichnet wird. In der Pädiatrie ist die Verkürzungsfraktion das bevorzugte Maß für die systolische Funktion. Normalerweise sollte die EF zwischen 50 und 70 % liegen; bei systolischer Herzinsuffizienz sinkt sie unter 40 %. Mit der Echokardiographie können auch Herzklappenerkrankungen erkannt und der Zustand des Herzbeutels (der das Herz umgebende Bindegewebesack) beurteilt werden. Die Echokardiografie kann auch bei der Entscheidung helfen, welche Behandlungen dem Betroffenen helfen können, z. B. Medikamente, der Einsatz eines implantierbaren Kardioverter-Defibrillators oder eine kardiale Resynchronisationstherapie. Mit Hilfe der Echokardiographie kann auch festgestellt werden, ob eine akute Myokardischämie die auslösende Ursache ist, die sich als regionale Wandbewegungsanomalien auf dem Echo zeigen kann. ⓘ
Ultraschalluntersuchung bei schwerer systolischer Herzinsuffizienz
Ultraschalluntersuchung bei schwerer systolischer Herzinsuffizienz
Ultraschalluntersuchung der Lunge, die ein Ödem aufgrund einer schweren systolischen Herzinsuffizienz zeigt
Ultraschalluntersuchung bei schwerer systolischer Herzinsuffizienz
Ultraschalluntersuchung bei schwerer systolischer Herzinsuffizienz ⓘ
Röntgenaufnahme des Brustkorbs

Röntgenaufnahmen des Brustkorbs werden häufig zur Unterstützung der Diagnose von Herzinsuffizienz eingesetzt. Bei kompensierter Herzinsuffizienz kann eine Kardiomegalie (sichtbare Vergrößerung des Herzens) festgestellt werden, die als Cardiothorax-Ratio (Verhältnis der Herzgröße zum Brustkorb) quantifiziert wird. Bei linksventrikulärer Insuffizienz können Anzeichen für eine Gefäßumverteilung (Blutumleitung im Oberlappen oder Kephalisation), Kerley-Linien, Manschetten um die Bronchien und interstitielle Ödeme vorliegen. Im Ultraschall der Lunge lassen sich möglicherweise auch Kerley-Linien erkennen. ⓘ
Kerley-B-Linien ⓘ
Die Röntgenaufnahme des Brustkorbes (Röntgen-Thorax) bildet u. a. das Herz und die Lunge ab. Bei leichteren Formen der Herzinsuffizienz zeigt sie in der Regel noch einen normalen Befund. Ist das Herz auf mehr als die Hälfte der Brustkorbbreite verbreitert, spricht man von einer Kardiomegalie; durch Erweiterung der linken Herzkammer kann das Herz eine charakteristische „Holzschuhform“ annehmen. Ein Rückstau des Blutes im Lungenkreislauf stellt sich als vermehrte Gefäßzeichnung dar. Ein Lungenödem zeigt sich als Verschattung im Zentrum („Schmetterlingsödem“); beim interstitiellen Lungenödem treten am Rand Kerley-Linien auf. Auch ein Pleuraerguss ist im Röntgenbild des Brustkorbs gut darstellbar. ⓘ
Um eine koronare Herzkrankheit als Ursache der Herzinsuffizienz zu diagnostizieren und zu behandeln, wird oft eine Herzkatheteruntersuchung mit Koronarangiografie (Koronarographie) durchgeführt. Dabei können die Druckverhältnisse im und am Herzen direkt gemessen und Verengungen der Herzkranzgefäße beurteilt und mit Stents behandelt werden. ⓘ
Elektrophysiologie
Mit Hilfe eines Elektrokardiogramms (EKG/EKG) können Herzrhythmusstörungen, ischämische Herzerkrankungen, rechts- und linksventrikuläre Hypertrophie sowie Leitungsverzögerungen oder -anomalien (z. B. Linksschenkelblock) festgestellt werden. Obwohl diese Befunde nicht spezifisch für die Diagnose einer Herzinsuffizienz sind, schließt ein normales EKG eine linksventrikuläre systolische Dysfunktion praktisch aus. ⓘ
Blutuntersuchungen
Zu den routinemäßig durchgeführten Blutuntersuchungen gehören Elektrolyte (Natrium, Kalium), Messungen der Nierenfunktion, Leberfunktionstests, Schilddrüsenfunktionstests, ein komplettes Blutbild und bei Verdacht auf eine Infektion häufig das C-reaktive Protein. Ein erhöhtes natriuretisches Hirnpeptid (BNP) ist ein spezifischer Test, der auf eine Herzinsuffizienz hinweist. Außerdem kann BNP verwendet werden, um die Ursachen der Dyspnoe aufgrund einer Herzinsuffizienz von anderen Ursachen der Dyspnoe zu unterscheiden. Besteht der Verdacht auf einen Herzinfarkt, können verschiedene kardiale Marker verwendet werden. ⓘ
BNP ist ein besserer Indikator als N-terminales pro-BNP für die Diagnose von symptomatischer Herzinsuffizienz und linksventrikulärer systolischer Dysfunktion. Bei symptomatischen Personen hat BNP eine Sensitivität von 85 % und eine Spezifität von 84 % bei der Erkennung von Herzinsuffizienz; die Leistung nimmt mit zunehmendem Alter ab. ⓘ
Eine Hyponatriämie (niedrige Serumnatriumkonzentration) ist bei Herzinsuffizienz häufig. Der Vasopressinspiegel ist in der Regel zusammen mit Renin, Angiotensin II und Katecholaminen erhöht, um das verringerte zirkulierende Volumen aufgrund einer unzureichenden Herzleistung auszugleichen. Dies führt zu einer erhöhten Flüssigkeits- und Natriumretention im Körper; die Rate der Flüssigkeitsretention ist höher als die Rate der Natriumretention im Körper, dieses Phänomen verursacht eine hypervolämische Hyponatriämie (niedrige Natriumkonzentration aufgrund hoher Flüssigkeitsretention im Körper). Dieses Phänomen tritt häufiger bei älteren Frauen mit geringer Körpermasse auf. Eine schwere Hyponatriämie kann zu einer Flüssigkeitsansammlung im Gehirn führen, die ein Hirnödem und eine intrakranielle Blutung verursacht. ⓘ
Angiographie
Die Angiografie ist die Röntgendarstellung von Blutgefäßen, bei der über einen dünnen Kunststoffschlauch (Katheter), der direkt in das Blutgefäß eingeführt wird, Kontrastmittel in die Blutbahn injiziert wird. Die Röntgenbilder werden Angiogramme genannt. Herzinsuffizienz kann die Folge einer koronaren Herzkrankheit sein, und ihre Prognose hängt zum Teil von der Fähigkeit der Koronararterien ab, den Herzmuskel (Myokard) mit Blut zu versorgen. Daher kann die Koronarkatheterisierung dazu dienen, Möglichkeiten für eine Revaskularisierung durch eine perkutane Koronarintervention oder eine Bypass-Operation zu ermitteln. ⓘ
Algorithmen
Für die Diagnose der Herzinsuffizienz werden verschiedene Algorithmen verwendet. Der von der Framingham Heart Study verwendete Algorithmus beispielsweise addiert Kriterien, die hauptsächlich aus der körperlichen Untersuchung stammen. Im Gegensatz dazu gewichtet der umfassendere Algorithmus der Europäischen Gesellschaft für Kardiologie den Unterschied zwischen unterstützenden und gegensätzlichen Parametern aus der Anamnese, der körperlichen Untersuchung, weiteren medizinischen Tests und dem Ansprechen auf die Therapie. ⓘ
Framingham-Kriterien
Nach den Framingham-Kriterien erfordert die Diagnose einer kongestiven Herzinsuffizienz (Herzinsuffizienz mit eingeschränkter Pumpleistung) das gleichzeitige Vorhandensein von mindestens zwei der folgenden Hauptkriterien oder eines Hauptkriteriums in Verbindung mit zwei der Nebenkriterien. Zu den Hauptkriterien gehören ein vergrößertes Herz auf dem Röntgenbild der Brust, ein S3-Galopp (ein drittes Herzgeräusch), ein akutes Lungenödem, ein Aufwachen aus dem Schlaf mit Luftnot, Knistern bei der Lungenauskultation, ein zentraler Venendruck von mehr als 16 cm H
2O im rechten Vorhof, eine Dehnung der Jugularvene, ein positiver abdominojugulärer Test und ein Gewichtsverlust von mehr als 4,5 kg in 5 Tagen als Reaktion auf die Behandlung (manchmal als Nebenkriterium eingestuft). Zu den leichteren Kriterien gehören eine abnorm schnelle Herzfrequenz von mehr als 120 Schlägen pro Minute, nächtlicher Husten, Atembeschwerden bei körperlicher Aktivität, Pleuraerguss, eine Abnahme der Vitalkapazität um ein Drittel gegenüber dem gemessenen Maximum, Lebervergrößerung und beidseitige Knöchelödeme. ⓘ
Geringfügige Kriterien sind nur dann akzeptabel, wenn sie nicht auf eine andere Erkrankung wie pulmonale Hypertonie, chronische Lungenerkrankung, Zirrhose, Aszites oder das nephrotische Syndrom zurückgeführt werden können. Die Kriterien der Framingham Heart Study haben eine Sensitivität von 100 % und eine Spezifität von 78 % für die Identifizierung von Personen mit definitiver Herzinsuffizienz. ⓘ
ESC-Algorithmus
Der ESC-Algorithmus gewichtet diese Parameter bei der Feststellung der Diagnose einer Herzinsuffizienz:
| Bewertung | Diagnose der Herzinsuffizienz | |
|---|---|---|
| Befürworter, wenn vorhanden | spricht dagegen, wenn normal oder nicht vorhanden | |
| Kompatible Symptome | ++ | ++ |
| Kompatible Anzeichen | ++ | + |
| Herzfunktionsstörung in der Echokardiographie | +++ | +++ |
| Ansprechen der Symptome oder Zeichen auf die Therapie | +++ | ++ |
| EKG | ||
| Normal | ++ | |
| Abnormal | ++ | + |
| Herzrhythmusstörungen | +++ | + |
| Labor | ||
| Erhöhtes BNP/NT-proBNP | +++ | + |
| Niedriges/normales BNP/NT-proBNP | + | +++ |
| Niedriger Natriumgehalt im Blut | + | + |
| Nierenfunktionsstörung | + | + |
| Leichte Erhöhungen von Troponin | + | + |
| Röntgenaufnahme des Brustkorbs | ||
| Pulmonale Stauung | +++ | + |
| Verminderte körperliche Leistungsfähigkeit | +++ | ++ |
| Abnorme Lungenfunktionstests | + | + |
| Abnorme Hämodynamik in Ruhe | +++ | ++ |
| + = einige Bedeutung; ++ = mittlere Bedeutung; +++ = große Bedeutung. | ||
Einteilung
Die Herzinsuffizienz wird in der Regel nach dem Grad der funktionellen Beeinträchtigung eingeteilt, der sich aus dem Schweregrad der Herzinsuffizienz ergibt (wie in der Funktionsklassifikation der New York Heart Association (NYHA) dargestellt). Die NYHA-Funktionsklassen (I-IV) beginnen mit der Klasse I, die als eine Person definiert ist, die keine Einschränkungen bei irgendwelchen Aktivitäten erfährt und keine Symptome bei gewöhnlichen Aktivitäten hat. Menschen mit Herzinsuffizienz der NYHA-Klasse II haben leichte, milde Einschränkungen bei alltäglichen Aktivitäten; die Person fühlt sich in Ruhe oder bei leichter Anstrengung wohl. Bei einer Herzinsuffizienz der NYHA-Klasse III kommt es zu einer deutlichen Einschränkung bei allen Aktivitäten; der Betroffene fühlt sich nur in Ruhe wohl. Eine Person mit Herzinsuffizienz der NYHA-Klasse IV ist in Ruhe symptomatisch und fühlt sich bei jeder körperlichen Aktivität sehr unwohl. Dieser Score dokumentiert den Schweregrad der Symptome und kann zur Beurteilung des Ansprechens auf die Behandlung herangezogen werden. Obwohl der NYHA-Score weit verbreitet ist, ist er nicht sehr reproduzierbar und sagt nicht zuverlässig die Gehstrecke oder die Belastungstoleranz bei formalen Tests voraus. ⓘ
In ihren Leitlinien von 2001 hat die Arbeitsgruppe des American College of Cardiology/American Heart Association vier Stadien der Herzinsuffizienz eingeführt:
- Stadium A: Menschen mit einem hohen Risiko, in der Zukunft eine HF zu entwickeln, aber ohne funktionelle oder strukturelle Herzstörung
- Stadium B: Eine strukturelle Herzerkrankung, aber keine Symptome in irgendeinem Stadium
- Stadium C: Frühere oder aktuelle Symptome einer Herzinsuffizienz im Zusammenhang mit einem zugrundeliegenden strukturellen Herzproblem, die jedoch mit Medikamenten behandelt werden
- Stadium D: Fortgeschrittene Erkrankung, die stationäre Unterstützung, eine Herztransplantation oder Palliativmedizin erfordert ⓘ
Das ACC-Stadiensystem ist nützlich, da das Stadium A die "Vorstufe der Herzinsuffizienz" umfasst - ein Stadium, in dem durch eine Behandlung das Fortschreiten der Krankheit mit offenen Symptomen vermutlich verhindert werden kann. Das ACC-Stadium A hat keine entsprechende NYHA-Klasse. ACC-Stadium B würde der NYHA-Klasse I entsprechen. ACC-Stadium C entspricht den NYHA-Klassen II und III, während sich ACC-Stadium D mit der NYHA-Klasse IV überschneidet.
- Der Grad der gleichzeitig bestehenden Erkrankungen: z. B. Herzinsuffizienz/systemische Hypertonie, Herzinsuffizienz/pulmonale Hypertonie, Herzinsuffizienz/Diabetes, Herzinsuffizienz/Niereninsuffizienz usw.
- ob das Problem in erster Linie ein erhöhter venöser Rückstau (Vorlast) oder eine unzureichende arterielle Durchblutung (Nachlast) ist
- ob die Anomalie auf ein niedriges Herzzeitvolumen mit hohem systemischen Gefäßwiderstand oder auf ein hohes Herzzeitvolumen mit niedrigem Gefäßwiderstand zurückzuführen ist (Herzinsuffizienz mit niedrigem Output vs. Herzinsuffizienz mit hohem Output) ⓘ
Früher ergänzte man: „Die Angabe der Grade (classes) I bis IV bezieht sich auf die funktionelle, die Grade A bis E auf die therapeutische Klassifikation“ der NYHA. ⓘ
Histopathologie

Die Histopathologie kann bei Autopsien eine Herzinsuffizienz diagnostizieren. Das Vorhandensein von Siderophagen weist auf eine chronische linksseitige Herzinsuffizienz hin, ist aber nicht spezifisch für diese. Sie wird auch durch eine Stauung des Lungenkreislaufs angezeigt. ⓘ
Vorbeugung
Das Risiko einer Person, eine Herzinsuffizienz zu entwickeln, steht in umgekehrtem Verhältnis zum Grad der körperlichen Aktivität. Diejenigen, die mindestens 500 MET-Minuten/Woche erreichten (das empfohlene Minimum der US-Leitlinien), hatten ein geringeres Risiko für eine Herzinsuffizienz als Personen, die angaben, in ihrer Freizeit keinen Sport zu treiben; die Verringerung des Risikos für eine Herzinsuffizienz war sogar noch größer bei denjenigen, die ein höheres Maß an körperlicher Aktivität als das empfohlene Minimum ausübten. Eine Herzinsuffizienz kann auch durch die Senkung von Bluthochdruck und hohen Cholesterinwerten sowie durch die Kontrolle von Diabetes verhindert werden. Die Beibehaltung eines gesunden Gewichts und die Verringerung des Natrium-, Alkohol- und Zuckerkonsums können ebenfalls helfen. Darüber hinaus hat sich gezeigt, dass der Verzicht auf Tabakkonsum das Risiko einer Herzinsuffizienz senkt. Nach Angaben von Johns Hopkins und der American Heart Association gibt es einige Möglichkeiten, einem kardialen Ereignis vorzubeugen. Johns Hopkins weist darauf hin, dass die Beendigung des Tabakkonsums, die Vermeidung von Bluthochdruck, körperliche Betätigung und die Ernährung das Risiko einer Herzerkrankung drastisch senken können. Hoher Blutdruck ist für die meisten kardiovaskulären Todesfälle verantwortlich. Die Senkung des Bluthochdrucks in den Normalbereich kann durch Ernährungsentscheidungen wie z. B. weniger Salzkonsum erreicht werden, und auch körperliche Bewegung trägt zur Senkung des Blutdrucks bei. Eine der besten Möglichkeiten zur Vermeidung von Herzinsuffizienz besteht darin, gesündere Ernährungsgewohnheiten zu fördern, z. B. mehr Gemüse, Obst, Getreide und mageres Eiweiß zu essen. ⓘ
Diabetes ist ein wichtiger Risikofaktor für Herzinsuffizienz. Bei Frauen mit koronarer Herzkrankheit (KHK) war Diabetes der stärkste Risikofaktor für Herzversagen. Diabetikerinnen mit niedriger Kreatinin-Clearance oder erhöhtem BMI hatten das höchste Risiko für eine Herzinsuffizienz. Während die jährliche Inzidenzrate der Herzinsuffizienz bei nicht-diabetischen Frauen ohne Risikofaktoren 0,4 % beträgt, lag die jährliche Inzidenzrate bei diabetischen Frauen mit erhöhtem Body-Mass-Index (BMI) und verminderter Kreatinin-Clearance bei 7 % bzw. 13 %. ⓘ
Behandlung
Die Behandlung konzentriert sich auf die Verbesserung der Symptome und die Verhinderung des Fortschreitens der Krankheit. Reversible Ursachen der Herzinsuffizienz müssen ebenfalls behandelt werden (z. B. Infektionen, Alkoholkonsum, Anämie, Thyreotoxikose, Herzrhythmusstörungen und Bluthochdruck). Die Behandlungen umfassen Lebensstil und pharmakologische Maßnahmen sowie gelegentlich verschiedene Formen der Gerätetherapie. In seltenen Fällen wird eine Herztransplantation als wirksame Behandlung eingesetzt, wenn die Herzinsuffizienz das Endstadium erreicht hat. ⓘ
Akute Dekompensation
Bei akuter dekompensierter Herzinsuffizienz besteht das unmittelbare Ziel darin, eine angemessene Durchblutung und Sauerstoffversorgung der Endorgane wiederherzustellen. Dazu muss sichergestellt werden, dass die Atemwege, die Atmung und der Kreislauf ausreichend sind. Die Sofortbehandlung umfasst in der Regel eine Kombination aus gefäßerweiternden Mitteln wie Nitroglyzerin, harntreibenden Mitteln wie Furosemid und möglicherweise nichtinvasiver Überdruckbeatmung. Zusätzlicher Sauerstoff ist bei Patienten mit einer Sauerstoffsättigung von unter 90 % angezeigt, wird aber bei Patienten mit normalem Sauerstoffgehalt in normaler Atmosphäre nicht empfohlen. ⓘ
Chronische Behandlung
Die Ziele der Behandlung von Menschen mit chronischer Herzinsuffizienz sind die Verlängerung des Lebens, die Verhinderung einer akuten Dekompensation und die Linderung der Symptome, so dass eine größere Aktivität möglich ist. ⓘ
Eine Herzinsuffizienz kann durch eine Vielzahl von Erkrankungen verursacht werden. Bei der Prüfung der therapeutischen Optionen ist der Ausschluss reversibler Ursachen von größter Bedeutung, darunter Schilddrüsenerkrankungen, Anämie, chronische Tachykardie, Alkoholmissbrauch, Bluthochdruck und Funktionsstörungen einer oder mehrerer Herzklappen. Die Behandlung der zugrunde liegenden Ursache ist in der Regel der erste Ansatz zur Behandlung der Herzinsuffizienz. In den meisten Fällen wird jedoch entweder keine primäre Ursache gefunden oder die Behandlung der primären Ursache führt nicht zur Wiederherstellung einer normalen Herzfunktion. In diesen Fällen gibt es verhaltenstherapeutische, medizinische und gerätetechnische Behandlungsstrategien, die zu einer deutlichen Verbesserung der Ergebnisse führen können, einschließlich der Linderung der Symptome, der Belastbarkeit und einer Verringerung der Wahrscheinlichkeit eines Krankenhausaufenthalts oder des Todes. Die Rehabilitation von Atemnot bei chronisch obstruktiver Lungenerkrankung und Herzinsuffizienz wurde vorgeschlagen, wobei das Bewegungstraining eine zentrale Komponente darstellt. Die Rehabilitation sollte auch andere Maßnahmen zur Bewältigung der Kurzatmigkeit umfassen, einschließlich der psychologischen und pädagogischen Bedürfnisse der Betroffenen und der Bedürfnisse der Pflegekräfte. Eine Eisensupplementierung scheint bei Menschen mit Eisenmangelanämie und Herzinsuffizienz sinnvoll zu sein. ⓘ
Vorausschauende Pflegeplanung
Die neuesten Erkenntnisse deuten darauf hin, dass eine vorausschauende Pflegeplanung (Advance Care Planning, ACP) dazu beitragen kann, die Dokumentation der Gespräche mit den Teilnehmern durch das medizinische Personal zu verbessern und die Depressivität der Betroffenen zu mindern. Dabei wird die künftige Pflegeplanung einer Person unter Berücksichtigung ihrer Präferenzen und Werte besprochen. Die Ergebnisse beruhen jedoch auf minderwertiger Evidenz. ⓘ
Überwachung
Zu den verschiedenen Maßnahmen, die häufig zur Beurteilung des Fortschritts von Patienten mit Herzinsuffizienz eingesetzt werden, gehören die Flüssigkeitsbilanz (Berechnung der Flüssigkeitsaufnahme und -ausscheidung) und die Überwachung des Körpergewichts (das kurzfristig die Flüssigkeitsverschiebung widerspiegelt). Die Fernüberwachung kann wirksam sein, um Komplikationen bei Menschen mit Herzinsuffizienz zu verringern. ⓘ
Lebensstil
Bei der Behandlung der chronischen Herzinsuffizienz steht die Änderung des Verhaltens im Vordergrund, mit Ernährungsrichtlinien für die Flüssigkeits- und Salzaufnahme. Die Einschränkung der Flüssigkeitszufuhr ist wichtig, um die Flüssigkeitsretention im Körper zu verringern und den hyponatriämischen Zustand des Körpers zu korrigieren. Die Belege für den Nutzen einer Salzreduzierung sind jedoch im Jahr 2018 gering. ⓘ
Bewegung und körperliche Aktivität
Bewegung sollte gefördert und an die individuellen Fähigkeiten angepasst werden. Eine Meta-Analyse ergab, dass von einem Physiotherapeuten durchgeführte, zentrumsbasierte Gruppeninterventionen hilfreich sind, um die körperliche Aktivität bei HF zu fördern. Physiotherapeuten müssen für die Durchführung von Interventionen zur Verhaltensänderung in Verbindung mit einem Bewegungsprogramm zusätzlich geschult werden. Es ist davon auszugehen, dass eine Intervention zur Förderung der körperlichen Aktivität wirksamer ist als die übliche Versorgung, wenn sie Aufforderungen und Hinweise zum Gehen oder zur Bewegung enthält, z. B. einen Telefonanruf oder eine Textnachricht. Es ist äußerst hilfreich, wenn ein vertrauenswürdiger Arzt ausdrücklich zu körperlicher Betätigung rät (glaubwürdige Quelle). Eine weitere sehr wirksame Strategie ist die Platzierung von Objekten in der alltäglichen Umgebung des Patienten, die als Anreiz für körperliche Aktivität dienen (Hinzufügen eines Objekts zur Umgebung; z. B. eine Trainingsstufe oder ein Laufband). Die Ermutigung zum Gehen oder zur körperlichen Betätigung in verschiedenen Umgebungen außerhalb von CR (z. B. zu Hause, in der Nachbarschaft, in Parks) ist ebenfalls vielversprechend (Generalisierung des Zielverhaltens). Weitere vielversprechende Strategien sind abgestufte Aufgaben (z. B. allmähliche Steigerung von Intensität und Dauer des Bewegungstrainings), Selbstbeobachtung, Beobachtung der körperlichen Aktivität durch andere ohne Rückmeldung, Aktionsplanung und Zielsetzung. Regelmäßiges körperliches Training als Teil eines kardialen Rehabilitationsprogramms kann die Lebensqualität deutlich verbessern und das Risiko einer Krankenhauseinweisung aufgrund einer Verschlechterung der Symptome verringern. Darüber hinaus ist unklar, ob diese Erkenntnisse auch für Menschen mit HFpEF oder für diejenigen gelten, deren Trainingsprogramm ausschließlich zu Hause stattfindet. ⓘ
Hausbesuche und regelmäßige Überwachung in Herzinsuffizienz-Kliniken verringern die Notwendigkeit einer Krankenhauseinweisung und verbessern die Lebenserwartung. ⓘ
Medikation
Eine vierfache medikamentöse Therapie mit einer Kombination aus Angiotensin-Rezeptor-Neprilysin-Inhibitoren (ARNI), Betablockern, Mineralokortikoidrezeptor-Antagonisten (MRA) und Natrium-Glukose-Cotransporter-2-Inhibitoren (SGLT2-Inhibitoren) ist ab 2021 der Standard der Behandlung. ⓘ
Medikamente der ersten Wahl
Die Erstlinientherapie für Menschen mit Herzinsuffizienz aufgrund einer eingeschränkten systolischen Funktion sollte Angiotensin-Converting-Enzym-(ACE-)Hemmer (ACE-I) oder Angiotensin-Rezeptorblocker (ARB) umfassen, wenn der Betroffene als Nebenwirkung des ACE-I einen Langzeithusten entwickelt. Der Einsatz von Arzneimitteln aus diesen Klassen wird mit einer verbesserten Überlebensrate, weniger Krankenhausaufenthalten aufgrund von Exazerbationen der Herzinsuffizienz und einer verbesserten Lebensqualität bei Menschen mit Herzinsuffizienz in Verbindung gebracht. ⓘ
ARNI Sacubitril/Valsartan sollte bei Patienten eingesetzt werden, die auch unter der Behandlung mit einem ACE-I oder ARB, einem Betablocker und einem Mineralokortikoidrezeptor-Antagonisten noch Symptome haben, da es das Risiko für kardiovaskuläre Mortalität und Krankenhausaufenthalte wegen Herzinsuffizienz um weitere 4,7 % (absolute Risikoreduktion) verringert. Die Anwendung dieser Kombination erfordert jedoch die Beendigung der ACE-i oder ARB-Therapie 48 Stunden vor deren Beginn. ⓘ
Betablocker gehören ebenfalls zur ersten Behandlungslinie und tragen zur Verbesserung der Symptome und der Sterblichkeit durch ACE-I/ARB bei. Der Nutzen von Betablockern für die Sterblichkeit ist bei Menschen mit systolischer Dysfunktion, die auch an Vorhofflimmern leiden, geringer als bei Menschen, die nicht an Vorhofflimmern leiden. Ist die Ejektionsfraktion nicht vermindert (HFpEF), ist der Nutzen von Betablockern bescheidener; es wurde zwar ein Rückgang der Sterblichkeit, aber keine Verringerung der Krankenhauseinweisungen wegen unkontrollierter Symptome beobachtet. ⓘ
Bei Patienten, die ACE-I und ARB nicht vertragen oder die eine erhebliche Nierenfunktionsstörung haben, ist die kombinierte Anwendung von Hydralazin und einem lang wirkenden Nitrat wie Isosorbiddinitrat eine wirksame Alternativstrategie. Diese Behandlung senkt nachweislich die Sterblichkeitsrate bei Patienten mit mittelschwerer Herzinsuffizienz. Sie ist besonders für die schwarze Bevölkerung von Vorteil. ⓘ
Bei symptomatischer Herzinsuffizienz mit deutlich reduzierter Ejektionsfraktion (alle Patienten mit einer Ejektionsfraktion von 35 % oder weniger bzw. weniger als 40 % nach einem Herzinfarkt) kann der Einsatz eines Mineralokortikoid-Antagonisten wie Spironolacton oder Eplerenon zusätzlich zu Betablockern und ACE-I (nach Titrierung auf die Zieldosis oder die maximal verträgliche Dosis) die Symptome verbessern und die Sterblichkeit senken. ⓘ
Der SGLT2-Hemmer ist das neueste Medikament zur Behandlung der Herzinsuffizienz. ⓘ
Andere Medikamente
Medikamente der zweiten Wahl zur Behandlung der Herzinsuffizienz bringen keinen Vorteil für die Sterblichkeit. Digoxin ist ein solches Medikament. Sein enges therapeutisches Fenster, ein hohes Maß an Toxizität und die Tatsache, dass in mehreren Studien kein Nutzen für die Sterblichkeit nachgewiesen werden konnte, haben seine Rolle in der klinischen Praxis eingeschränkt. Es wird heute nur noch bei einer kleinen Anzahl von Patienten mit refraktären Symptomen, Vorhofflimmern und/oder chronischer Hypotonie eingesetzt. ⓘ
Diuretika sind eine Hauptstütze der Behandlung von Symptomen der Flüssigkeitsansammlung und umfassen Diuretika-Klassen wie Schleifendiuretika (z. B. Furosemid), thiazidartige Diuretika und kaliumsparende Diuretika. Obwohl sie weit verbreitet sind, sind die Erkenntnisse über ihre Wirksamkeit und Sicherheit begrenzt, mit Ausnahme der Mineralokortikoid-Antagonisten wie Spironolacton. Mineralokortikoid-Antagonisten scheinen bei Personen unter 75 Jahren das Sterberisiko zu senken. ⓘ
Anämie ist ein unabhängiger Faktor für die Sterblichkeit von Menschen mit chronischer Herzinsuffizienz. Die Behandlung der Anämie verbessert die Lebensqualität von Menschen mit Herzinsuffizienz erheblich, oft mit einer Verringerung des Schweregrads der NYHA-Klassifikation, und verbessert auch die Sterblichkeitsrate. Die Leitlinie der Europäischen Gesellschaft für Kardiologie aus dem Jahr 2016 empfiehlt ein Screening auf Eisenmangelanämie und eine Behandlung mit intravenösem Eisen, wenn ein Mangel festgestellt wird. ⓘ
Die Entscheidung über die Antikoagulation von Menschen mit HF, typischerweise mit einer linksventrikulären Ejektionsfraktion <35 %, ist umstritten, aber im Allgemeinen gilt sie für Menschen mit gleichzeitigem Vorhofflimmern, einem früheren embolischen Ereignis oder Erkrankungen, die das Risiko eines embolischen Ereignisses erhöhen, wie Amyloidose, linksventrikuläre Nichtkompaktion, familiäre dilatative Kardiomyopathie oder ein thromboembolisches Ereignis bei einem Verwandten ersten Grades. ⓘ
Vasopressin-Rezeptor-Antagonisten können auch zur Behandlung von Herzinsuffizienz eingesetzt werden. Conivaptan ist das erste von der US Food and Drug Administration zugelassene Medikament zur Behandlung der euvolemischen Hyponatriämie bei Herzinsuffizienz. In seltenen Fällen kann hypertone 3%ige Kochsalzlösung zusammen mit Diuretika zur Korrektur einer Hyponatriämie eingesetzt werden. ⓘ
Ivabradin wird für Patienten mit symptomatischer Herzinsuffizienz mit reduzierter linksventrikulärer Ejektionsfraktion empfohlen, die eine optimierte leitliniengerechte Therapie (wie oben beschrieben) einschließlich der maximal verträglichen Dosis eines Betablockers erhalten, einen normalen Herzrhythmus haben und weiterhin eine Ruheherzfrequenz von über 70 Schlägen pro Minute aufweisen. Es hat sich gezeigt, dass Ivabradin das Risiko einer Krankenhauseinweisung wegen einer Verschlimmerung der Herzinsuffizienz in dieser Untergruppe von Patienten mit Herzinsuffizienz verringert. ⓘ
Implantierte Geräte
Bei Patienten mit schwerer Kardiomyopathie (linksventrikuläre Ejektionsfraktion unter 35 %) oder bei Patienten mit rezidivierenden ventrikulären Tachykardien oder malignen Arrhythmien ist die Behandlung mit einem automatischen implantierbaren Kardioverter-Defibrillator (AICD) angezeigt, um das Risiko schwerer lebensbedrohlicher Arrhythmien zu verringern. Der AICD verbessert weder die Symptome noch verringert er die Häufigkeit bösartiger Herzrhythmusstörungen, aber er verringert die Sterblichkeit aufgrund dieser Herzrhythmusstörungen, häufig in Verbindung mit Antiarrhythmika. Bei Menschen mit einer linksventrikulären Ejektionskraft (LVEF) von weniger als 35 % ist die Inzidenz von Kammertachykardien oder plötzlichem Herztod hoch genug, um den Einsatz eines AICD zu rechtfertigen. In den AHA/ACC-Leitlinien wird daher der Einsatz von AICDs empfohlen. ⓘ
Die kardiale Kontraktilitätsmodulation (CCM) ist eine Behandlung für Menschen mit mittelschwerer bis schwerer linksventrikulärer systolischer Herzinsuffizienz (NYHA-Klasse II-IV), die sowohl die Stärke der ventrikulären Kontraktion als auch die Pumpleistung des Herzens verbessert. Der CCM-Mechanismus basiert auf der Stimulation des Herzmuskels durch nicht erregende elektrische Signale, die von einem schrittmacherähnlichen Gerät abgegeben werden. CCM eignet sich besonders für die Behandlung von Herzinsuffizienz mit normaler QRS-Komplexdauer (120 ms oder weniger) und verbessert nachweislich die Symptome, die Lebensqualität und die Belastungstoleranz. CCM ist in Europa zugelassen und wurde 2019 von der Food and Drug Administration für den Einsatz in den Vereinigten Staaten genehmigt. ⓘ
Bei etwa einem Drittel der Menschen mit einem LVEF unter 35 % ist die Erregungsleitung zu den Herzkammern deutlich verändert, was zu einer dysynchronen Depolarisation der rechten und linken Herzkammern führt. Besonders problematisch ist dies bei Menschen mit Linksschenkelblock (Blockade eines der beiden primären Leitungsfaserbündel, die an der Herzbasis entspringen und depolarisierende Impulse zur linken Herzkammer leiten). Mithilfe eines speziellen Stimulationsalgorithmus kann die biventrikuläre kardiale Resynchronisationstherapie (CRT) eine normale Sequenz der ventrikulären Depolarisation einleiten. Bei Menschen mit einem LVEF von weniger als 35 % und einer verlängerten QRS-Dauer im EKG (LBBB oder QRS von 150 ms oder mehr) kommt es zu einer Verbesserung der Symptome und der Sterblichkeit, wenn die CRT zur medizinischen Standardtherapie hinzugefügt wird. Bei den zwei Dritteln der Patienten ohne verlängerte QRS-Dauer kann die CRT jedoch sogar schädlich sein. ⓘ
Chirurgische Therapien
Menschen mit schwerster Herzinsuffizienz können Kandidaten für ventrikuläre Unterstützungssysteme sein, die üblicherweise als Überbrückung bis zur Herztransplantation verwendet wurden, in letzter Zeit aber auch als Zielbehandlung für fortgeschrittene Herzinsuffizienz eingesetzt werden. ⓘ
In ausgewählten Fällen kann auch eine Herztransplantation in Betracht gezogen werden. Damit können zwar die mit der Herzinsuffizienz verbundenen Probleme gelöst werden, doch muss der Betroffene in der Regel eine immunsuppressive Behandlung beibehalten, um eine Abstoßung zu verhindern, was wiederum mit erheblichen Nachteilen verbunden ist. Eine wesentliche Einschränkung dieser Behandlungsoption ist die Knappheit der für eine Transplantation verfügbaren Herzen. ⓘ
Palliativmedizin
Menschen mit Herzinsuffizienz haben oft erhebliche Symptome wie Kurzatmigkeit und Brustschmerzen. Die Palliativmedizin sollte bereits in einem frühen Stadium der Herzinsuffizienz eingeleitet werden und nicht die letzte Option darstellen. Palliativmedizin kann nicht nur die Symptome lindern, sondern auch bei der Pflegeplanung helfen, bei der Festlegung von Pflegezielen für den Fall, dass sich die Lebensqualität deutlich verschlechtert, und sicherstellen, dass die Person eine medizinische Vollmacht hat und ihre Wünsche mit dieser Person besprochen wurden. In einer Untersuchung aus den Jahren 2016 und 2017 wurde festgestellt, dass die Palliativversorgung mit besseren Ergebnissen wie Lebensqualität, Symptombelastung und Zufriedenheit mit der Pflege verbunden ist. ⓘ
Ohne Transplantation ist die Herzinsuffizienz möglicherweise nicht reversibel, und die Herzfunktion verschlechtert sich in der Regel mit der Zeit. Die wachsende Zahl von Menschen mit Herzinsuffizienz im Stadium IV (hartnäckige Symptome wie Müdigkeit, Kurzatmigkeit oder Brustschmerzen in Ruhe trotz optimaler medizinischer Therapie) sollte nach den Richtlinien des American College of Cardiology/American Heart Association für eine Palliativversorgung oder ein Hospiz in Betracht gezogen werden. ⓘ
Prognose
Die Prognose bei Herzinsuffizienz kann auf verschiedene Weise beurteilt werden, einschließlich klinischer Prognoseregeln und kardiopulmonaler Belastungstests. Klinische Prognoseregeln verwenden eine Kombination aus klinischen Faktoren wie Labortests und Blutdruck, um die Prognose abzuschätzen. Unter mehreren klinischen Prognoseregeln für akute Herzinsuffizienz schnitt die 'EFFECT-Regel' bei der Stratifizierung von Personen und der Identifizierung von Personen mit geringem Sterberisiko während des Krankenhausaufenthalts oder innerhalb von 30 Tagen etwas besser ab als andere Regeln. Einfache Methoden zur Identifizierung von Personen mit niedrigem Risiko sind:
- Die ADHERE-Baum-Regel besagt, dass Personen mit einem Harnstoff-Stickstoffwert < 43 mg/dl und einem systolischen Blutdruck von mindestens 115 mm Hg ein Risiko von weniger als 10 % haben, im Krankenhaus zu sterben oder Komplikationen zu erleiden.
- Die BWH-Regel besagt, dass Menschen mit einem systolischen Blutdruck von über 90 mm Hg, einer Atemfrequenz von 30 oder weniger Atemzügen pro Minute, einem Serumnatriumspiegel von über 135 mmol/l und keinen neuen ST-T-Wellenveränderungen eine Wahrscheinlichkeit von weniger als 10 % haben, stationär zu sterben oder Komplikationen zu erleiden. ⓘ
Eine sehr wichtige Methode zur Beurteilung der Prognose bei Menschen mit fortgeschrittener Herzinsuffizienz ist der kardiopulmonale Belastungstest (CPX-Test). CPX-Tests werden in der Regel vor einer Herztransplantation als Indikator für die Prognose verlangt. Die CPX-Untersuchung umfasst die Messung des ausgeatmeten Sauerstoffs und Kohlendioxids während der Belastung. Der maximale Sauerstoffverbrauch (VO2 max) wird als Indikator für die Prognose verwendet. In der Regel deutet ein VO2 max-Wert von weniger als 12-14 cc/kg/min auf eine schlechte Überlebensrate hin und legt nahe, dass die betreffende Person ein Kandidat für eine Herztransplantation sein könnte. Menschen mit einer VO2 max <10 cm³/kg/min haben eine deutlich schlechtere Prognose. In den jüngsten Leitlinien der Internationalen Gesellschaft für Herz- und Lungentransplantation werden zwei weitere Parameter vorgeschlagen, die zur Beurteilung der Prognose bei fortgeschrittener Herzinsuffizienz herangezogen werden können: der Herzinsuffizienz-Survival-Score und die Verwendung eines Kriteriums von VE/VCO2-Steigung > 35 aus dem CPX-Test. Der Überlebensscore für Herzinsuffizienz wird anhand einer Kombination aus klinischen Prädiktoren und der VO2 max des CPX-Tests berechnet. ⓘ
Die Herzinsuffizienz geht mit einer erheblichen Beeinträchtigung der körperlichen und geistigen Gesundheit einher, was zu einer deutlich verringerten Lebensqualität führt. Mit Ausnahme der Herzinsuffizienz, die durch reversible Erkrankungen verursacht wird, verschlechtert sich der Zustand in der Regel mit der Zeit. Obwohl manche Menschen viele Jahre überleben, ist die fortschreitende Krankheit mit einer jährlichen Gesamtsterblichkeitsrate von 10 % verbunden. ⓘ
Etwa 18 von 1000 Personen erleiden innerhalb des ersten Jahres nach der Diagnose der HF einen ischämischen Schlaganfall. Mit zunehmender Dauer der Nachbeobachtung steigt die Schlaganfallrate bis zu 5 Jahren auf fast 50 Schlaganfälle pro 1000 Fälle von HF an. ⓘ
Epidemiologie
Im Jahr 2015 waren weltweit etwa 40 Millionen Menschen von Herzinsuffizienz betroffen. Insgesamt leiden etwa 2 % der Erwachsenen an einer Herzinsuffizienz, und bei den über 65-Jährigen steigt diese Rate auf 6-10 %. Bei den über 75-Jährigen liegt die Rate bei über 10 %. ⓘ
Prognosen zufolge werden die Raten steigen. Die steigenden Raten sind vor allem auf die zunehmende Lebenserwartung zurückzuführen, aber auch auf die Zunahme von Risikofaktoren (Bluthochdruck, Diabetes, Dyslipidämie und Fettleibigkeit) und die verbesserten Überlebensraten bei anderen Arten von Herz-Kreislauf-Erkrankungen (Herzinfarkt, Herzklappenerkrankungen und Herzrhythmusstörungen). Herzinsuffizienz ist die häufigste Ursache für Krankenhausaufenthalte bei Menschen über 65 Jahren. ⓘ
Vereinigte Staaten
In den Vereinigten Staaten sind 5,8 Millionen Menschen von Herzinsuffizienz betroffen, und jedes Jahr werden 550.000 neue Fälle diagnostiziert. Im Jahr 2011 war Herzinsuffizienz der häufigste Grund für Krankenhausaufenthalte bei Erwachsenen im Alter von 85 Jahren und älter und der zweithäufigste bei Erwachsenen im Alter von 65-84 Jahren. Schätzungsweise einer von fünf Erwachsenen im Alter von 40 Jahren wird im Laufe seines Lebens eine Herzinsuffizienz entwickeln, und etwa die Hälfte der Menschen, die eine Herzinsuffizienz entwickeln, stirbt innerhalb von fünf Jahren nach der Diagnose. Bei Afroamerikanern, Hispanoamerikanern, amerikanischen Ureinwohnern und kürzlich eingewanderten Menschen aus Ostblockländern wie Russland ist die Herzinsuffizienz wesentlich häufiger. Diese hohe Prävalenz in diesen ethnischen Minderheiten wurde mit der hohen Inzidenz von Diabetes und Bluthochdruck in Verbindung gebracht. Bei vielen Neueinwanderern in den USA wird die hohe Prävalenz der Herzinsuffizienz größtenteils auf mangelnde Gesundheitsvorsorge oder minderwertige Behandlung zurückgeführt. Fast einer von vier Menschen (24,7 %), die in den USA mit kongestiver Herzinsuffizienz ins Krankenhaus eingeliefert werden, wird innerhalb von 30 Tagen wieder eingewiesen. Darüber hinaus suchen mehr als 50 % der Betroffenen innerhalb von 6 Monaten nach der Behandlung eine Wiedereinweisung, und die durchschnittliche Dauer des Krankenhausaufenthalts beträgt 6 Tage. ⓘ
Herzinsuffizienz ist eine der Hauptursachen für die Wiedereinweisung in ein Krankenhaus in den USA. Im Jahr 2011 wurden Menschen im Alter von 65 Jahren und älter mit einer Rate von 24,5 pro 100 Einweisungen wieder eingewiesen. Im selben Jahr wurden Personen, die unter Medicaid fallen, mit einer Rate von 30,4 pro 100 Aufnahmen wieder aufgenommen, und nicht versicherte Personen wurden mit einer Rate von 16,8 pro 100 Aufnahmen wieder aufgenommen. Dies sind die höchsten Rückübernahmequoten für beide Kategorien. Bemerkenswert ist, dass Herzinsuffizienz nicht unter den Top-10 der Erkrankungen mit den meisten 30-Tage-Wiederaufnahmen bei Privatversicherten zu finden ist. ⓘ
Vereinigtes Königreich
Im Vereinigten Königreich sind die Raten der Herzinsuffizienz trotz moderater Verbesserungen in der Prävention aufgrund des Bevölkerungswachstums und der Alterung der Bevölkerung gestiegen. Die Gesamtraten für Herzinsuffizienz sind ähnlich hoch wie die der vier häufigsten Krebsarten (Brust-, Lungen-, Prostata- und Dickdarmkrebs) zusammen. Bei Menschen aus sozial schwachen Verhältnissen wird die Herzinsuffizienz häufiger und in jüngerem Alter diagnostiziert. ⓘ
Entwicklungsländer
In tropischen Ländern ist die häufigste Ursache von HF eine Herzklappenerkrankung oder eine Art von Kardiomyopathie. Mit dem zunehmenden Wohlstand in den unterentwickelten Ländern hat die Häufigkeit von Diabetes, Bluthochdruck und Fettleibigkeit zugenommen, was wiederum die Häufigkeit von Herzinsuffizienz erhöht. ⓘ
Geschlecht
Männer erkranken häufiger an Herzinsuffizienz, aber die Gesamtprävalenzrate ist bei beiden Geschlechtern ähnlich, da Frauen nach dem Auftreten einer Herzinsuffizienz länger überleben. Frauen sind bei der Diagnose einer Herzinsuffizienz in der Regel älter (nach der Menopause), haben häufiger als Männer eine diastolische Dysfunktion und scheinen nach der Diagnose insgesamt eine geringere Lebensqualität zu haben als Männer. ⓘ
Ethnische Zugehörigkeit
Einigen Quellen zufolge haben Menschen asiatischer Abstammung ein höheres Risiko für eine Herzinsuffizienz als andere ethnische Gruppen. Andere Quellen stellen jedoch fest, dass die Raten der Herzinsuffizienz ähnlich hoch sind wie bei anderen ethnischen Gruppen. ⓘ
Geschichte
Jahrhundertelang wurde die Krankheit, zu der viele Fälle von Herzinsuffizienz gehören, als Wassersucht bezeichnet; der Begriff bezeichnet ein allgemeines Ödem, das eine Hauptmanifestation eines versagenden Herzens ist, aber auch durch andere Krankheiten verursacht werden kann. In den Schriften der antiken Zivilisationen finden sich Hinweise darauf, dass sie mit Wassersucht und Herzinsuffizienz vertraut waren: Die Ägypter waren die ersten, die einen Aderlass durchführten, um Flüssigkeitsansammlungen und Atemnot zu lindern, und sie lieferten die möglicherweise ersten dokumentierten Beobachtungen über Herzinsuffizienz im Ebers-Papur (um 1500 v. Chr.); die Griechen beschrieben Fälle von Atemnot, Flüssigkeitsansammlung und Müdigkeit, die mit Herzinsuffizienz vereinbar waren; die Römer verwendeten die blühende Pflanze Drimia maritima (Seekreuzkraut), die Herzglykoside enthält, zur Behandlung von Wassersucht; Beschreibungen von Herzinsuffizienz sind auch aus den Kulturen des alten Indien und China bekannt. Allerdings wurden die Erscheinungsformen der Herzinsuffizienz im Rahmen der medizinischen Theorien dieser Völker verstanden - einschließlich der altägyptischen Religion, der hippokratischen Theorie der Körpersäfte oder der altindischen und chinesischen Medizin -, und das heutige Konzept der Herzinsuffizienz war noch nicht entwickelt. Obwohl Avicenna um das Jahr 1000 n. Chr. Atemnot mit Herzkrankheiten in Verbindung brachte, waren die Beschreibung des Lungenkreislaufs durch Ibn al-Nafis im 13. Jahrhundert und des systemischen Kreislaufs durch William Harvey im Jahr 1628 entscheidend für das moderne Verständnis der Natur des Zustands. Die Rolle des Herzens bei der Flüssigkeitsretention wurde allmählich besser verstanden, als die Brustwassersucht (Flüssigkeitsansammlung in und um die Lunge, die zu Atemnot führt) bekannter wurde und das heutige Konzept der Herzinsuffizienz, das Schwellungen und Atemnot aufgrund von Flüssigkeitsretention zusammenfasst, im 17. und insbesondere im 18: Richard Lower stellte 1679 eine Verbindung zwischen Dyspnoe und Fußschwellung her, und Giovanni Maria Lancisi brachte 1728 eine Dehnung der Jugularvene mit einem Versagen der rechten Herzkammer in Verbindung. Im 19. Jahrhundert wurde die Dropsie durch andere Ursachen, z. B. Nierenversagen, unterschieden. Das von René Laennec 1819 erfundene Stethoskop, die von Wilhelm Röntgen 1895 entdeckten Röntgenstrahlen und die von Willem Einthoven 1903 beschriebene Elektrokardiographie erleichterten die Untersuchung der Herzinsuffizienz. Das 19. Jahrhundert brachte auch experimentelle und konzeptionelle Fortschritte in der Physiologie der Herzkontraktion, die zur Formulierung des Frank-Starling-Gesetzes des Herzens führten (benannt nach den Physiologen Otto Frank und Ernest Starling), ein bemerkenswerter Fortschritt im Verständnis der Mechanismen der Herzinsuffizienz. ⓘ
Eine der frühesten Behandlungen der Herzinsuffizienz, die Linderung von Schwellungen durch Aderlass mit verschiedenen Methoden, einschließlich Blutegeln, wurde über die Jahrhunderte fortgesetzt. Neben dem Aderlass empfahl Jean-Baptiste de Sénac 1749 Opiate bei akuter Atemnot aufgrund von Herzinsuffizienz. William Withering beschrieb 1785 die therapeutische Verwendung der Fingerhut-Pflanzengattung zur Behandlung von Ödemen; ihr Extrakt enthält Herzglykoside, darunter Digoxin, das noch heute zur Behandlung von Herzinsuffizienz eingesetzt wird. Die harntreibende Wirkung von anorganischen Quecksilbersalzen, die zur Behandlung von Syphilis eingesetzt wurden, war bereits im 16. Jahrhundert von Paracelsus festgestellt worden; im 19. In der Zwischenzeit waren Kanülen (Schläuche), die 1877 von dem englischen Arzt Reginald Southey erfunden wurden, eine weitere Methode zur Entfernung überschüssiger Flüssigkeit durch direktes Einführen in geschwollene Gliedmaßen. Die Verwendung von organischen Quecksilberverbindungen als Diuretika, die über ihre Rolle bei der Syphilisbehandlung hinausgingen, begann 1920, war jedoch durch ihren parenteralen Verabreichungsweg und ihre Nebenwirkungen eingeschränkt. Orale Quecksilberdiuretika wurden in den 1950er Jahren eingeführt, ebenso wie Thiaziddiuretika, die weniger toxisch sind und noch heute verwendet werden. Etwa zur gleichen Zeit begann mit der Erfindung der Echokardiographie durch Inge Edler und Hellmuth Hertz im Jahr 1954 eine neue Ära in der Beurteilung der Herzinsuffizienz. In den 1960er Jahren kamen Schleifendiuretika zur Behandlung der Flüssigkeitsretention hinzu, während Christiaan Barnard einem Patienten mit Herzinsuffizienz die erste Herztransplantation spendete. In den folgenden Jahrzehnten fanden neue Medikamentenklassen ihren Platz in der Therapie der Herzinsuffizienz, darunter Vasodilatatoren wie Hydralazin, Hemmstoffe des Renin-Angiotensin-Systems und Betablocker. ⓘ
Wirtschaft
Im Jahr 2011 gehörte die nicht-hypertensive Herzinsuffizienz zu den 10 teuersten Erkrankungen, die bei stationären Krankenhausaufenthalten in den USA festgestellt wurden, mit Gesamtkosten von über 10,5 Milliarden US-Dollar für stationäre Behandlungen. ⓘ
Herzinsuffizienz ist mit hohen Gesundheitsausgaben verbunden, vor allem wegen der Kosten für Krankenhausaufenthalte; die Kosten werden auf 2 % des Gesamtbudgets des Nationalen Gesundheitsdienstes im Vereinigten Königreich und auf mehr als 35 Milliarden US-Dollar in den Vereinigten Staaten geschätzt. ⓘ
Forschungsrichtungen
Einige Hinweise von geringer Qualität deuten darauf hin, dass die Stammzelltherapie helfen kann. Obwohl diese Belege positiv auf einen Nutzen hinweisen, sind sie von geringerer Qualität als andere Belege, die keinen Nutzen erkennen lassen. Es gibt vorläufige Hinweise auf eine längere Lebenserwartung und eine verbesserte linksventrikuläre Ejektionsfraktion bei Personen, die mit Stammzellen aus dem Knochenmark behandelt wurden. ⓘ
Alltagssprache und Doppeldeutungen
Der gebräuchliche deutsche Begriff Herzschwäche trifft den Sachverhalt nur ungenau, weil nicht nur eine krankhaft verminderte Pumpfunktion (systolische Herzinsuffizienz oder Herzmuskelschwäche), sondern auch eine gestörte Füllung des Herzens (diastolische Herzinsuffizienz) bei unbeeinträchtigter Pumpfunktion zur Herzinsuffizienz führen kann. Eine akute, schwere Herzinsuffizienz wird gelegentlich als Herzversagen bezeichnet, wobei eine allgemein akzeptierte Definition dieses insbesondere in Leichenschauscheinen häufig verwendeten Begriffs fehlt. Kritiker wenden ein, dass Herzversagen wohl auch deshalb als häufigste Todesursache genannt wird, weil das Herz letztlich bei jedem Verstorbenen zum Stillstand gekommen ist und die tatsächlich zum Tode führende Krankheit oft nicht ermittelt wurde. ⓘ
Die Identität von der Herzinsuffizienz als zu kleinem Herzzeitvolumen und dem Syndrom des zu kleinen Herzzeitvolumens (englisch: low cardiac output syndrome) wird in der Fachliteratur oft nicht deutlich. Dabei ist cardiac output (abgekürzt CO) die englische Übersetzung vom Herzzeitvolumen (abgekürzt HZV). Außerdem ist die Herzinsuffizienz keine Krankheit, sondern ein Syndrom, also das Symptom zahlreicher Krankheiten. Auch ist die Herzschwäche bei vergrößertem Herzzeitvolumen (high output failure) immer auch eine Herzinsuffizienz mit einem zu kleinen Herzzeitvolumen bei vergrößertem Bedarf an sauerstoffreichem Blut. ⓘ
Einteilung
Die Herzinsuffizienz wird nach ihrem Verlauf (akut oder chronisch), nach der überwiegend betroffenen Herzhälfte (rechts oder links, andernfalls global) und nach dem Mechanismus unterteilt. ⓘ
Verlauf
Die akute Herzinsuffizienz entwickelt sich im Verlauf von Stunden bis Tagen. Ursachen sind:
- tachykarde (zu hohe Herzfrequenz) oder bradykarde (zu niedrige Herzfrequenz) Herzrhythmusstörungen
- plötzlicher Verlust der Pumpfunktion durch einen Herzinfarkt
- Lungenembolie
- akut und schwer verlaufende Herzmuskelentzündung
- mechanische Behinderung der Herzkammerfüllung, z. B. durch Perikardtamponade
- plötzlich auftretende Klappeninsuffizienzen durch Einriss einer vorgeschädigten Herzklappe. ⓘ
Die chronische Herzinsuffizienz entwickelt sich im Verlauf von Monaten bis Jahren. Sie ist charakterisiert durch Kompensationsprozesse des Organismus (schnellerer Herzschlag, Verdickung des Herzmuskels, Engstellung der Blutgefäße, Vermehrung des Blutvolumens usw.), was die verminderte Pumpleistung des Herzens eine Zeit lang ausgleichen kann. Die kompensierte Herzinsuffizienz zeigt keine oder erst bei stärkerer körperlicher Belastung Symptome. Im dekompensierten Stadium kommt es zu pathologischen Wasseransammlungen (Ödemen) und Luftnot (Dyspnoe). Diese tritt bereits in Ruhe oder unter geringer Belastung auf. ⓘ
Spezielle Formen der Herzinsuffizienz
Die Herzinsuffizienz betrifft häufig nicht beide Herzhälften gleichmäßig. Unabhängig von der Lokalisation der Störung kommt es durch die Wassereinlagerungen zur Gewichtszunahme. In der Nacht (körperliche Ruhe, Hochlagerung der Beine) wird ein Teil der Wassereinlagerungen aus dem Gewebe mobilisiert und über die Nieren ausgeschieden; dadurch tritt vermehrtes nächtliches Wasserlassen auf (Nykturie). ⓘ
Rechtsherzinsuffizienz
Bei Rechtsherzinsuffizienz (auch Rechtsinsuffizienz genannt), dem Kontraktionsversagen der rechten Herzkammer und des rechten Vorhofs, staut sich das Blut zurück in die Körpervenen. Durch den erhöhten Venendruck können sich sowohl Wasseransammlungen (als Transsudat) in den Geweben mit Ödemen vor allem der unteren Körperpartien (Beine) bilden, als auch im Bauchraum (Aszites) und in der Pleurahöhle (Pleuraerguss). ⓘ
Funktionelle Einteilung
Funktionell kann man zwischen einem Vorwärts- und Rückwärtsversagen des Herzens unterscheiden. Beim Vorwärtsversagen kann kein ausreichender Druck in den Arterien aufgebaut werden, während beim Rückwärtsversagen ein Rückstau des Blutes in den Körper- und Lungenvenen stattfindet. ⓘ
High-output-failure
Nicht immer liegt der Herzinsuffizienz ein Pumpversagen mit Verminderung des Herzzeitvolumens zugrunde (Low-output-failure). Die Symptome der Herzinsuffizienz können auch auftreten, wenn ein pathologisch erhöhter Durchblutungsbedarf der Organe nicht mehr gedeckt werden kann (High-output-failure):
- Blutarmut (Anämie) – wegen der schlechten Sauerstofftransportkapazität muss das Herzzeitvolumen steigen, um eine ausreichende Sauerstoffversorgung der Gewebe zu sichern.
- Schilddrüsenüberfunktion (Hyperthyreose) – die Pumpleistung des Herzens ist stark stimuliert, der Stoffwechsel und damit die Durchblutung der Gewebe aber auch. Unter anderem durch die Tachykardie kann es zur (relativen) Herzinsuffizienz kommen.
- Arteriovenöse Fistel – durch eine Kurzschlussverbindung zwischen Arterien und Venen wird ein Teil des Herzzeitvolumens ohne Nutzen verbraucht.
- Sepsis/SIRS – die mit der Ausschüttung von Entzündungsmediatoren einhergehende Weitstellung der kleinen Gefäße und endotheliale Schrankenstörung erfordert eine stark erhöhte Auswurfleistung des Herzens, um den arteriellen Blutdruck aufrechtzuerhalten. ⓘ
Pathophysiologie und Ätiologie

Das rechte Herz nimmt über die obere und untere Hohlvene das Blut aus dem Körper auf und pumpt es durch die Lungenarterie (Arteria pulmonalis) in die Lunge (vergleiche Lungenkreislauf). Sauerstoffreiches Blut fließt von dort durch die Lungenvenen zum linken Herz, von wo es durch die Hauptschlagader (Aorta) in den Körper gepumpt wird. Diese Pumpfunktion des Herzens kann aus verschiedenen Ursachen gestört sein. ⓘ
Auch ohne Herzkrankheit kann es zur Herzinsuffizienz kommen, zum Beispiel bei einer Blutarmut oder wenn eine Lungen- oder Leberkrankheit das Herzzeitvolumen verkleinert. Eine seltene Ursache der Herzinsuffizienz ist das in der Adoleszenz nicht ausreichende Mitwachsen des Spenderherzens nach einer Herztransplantation beim Kleinkind. Analog führt ein zu kleines Herzzeitvolumen eines Kunstherzens zur Herzinsuffizienz. ⓘ
Ursachen der Herzinsuffizienz
- verschlechterte Kontraktionsfähigkeit (Systole) oder Füllung (Diastole) des Herzens durch direkte Schädigung des Herzmuskels, z. B. bei koronarer Herzkrankheit, nach Herzinfarkt oder durch Herzmuskelentzündung und Kardiomyopathien
- erhöhter Pumpwiderstand, z. B. bei Bluthochdruck im Körperkreislauf (arterielle Hypertonie) bzw. im Lungenkreislauf (pulmonale Hypertonie) oder verengter Aortenklappe
- erhöhtes Schlagvolumen bei Herzfehlern, z. B. bei undichter Aortenklappe
- zu niedrige Herzfrequenz bei Bradykardie oder zu geringes Schlagvolumen bei Tachykardie und dadurch Abnahme des Herzzeitvolumens
- Einengung des Herzens durch Flüssigkeit im Herzbeutel
- erhöhter Blutbedarf des Körpers bei schwerer Allgemeinerkrankung
- Blutarmut (Anämie)
- obstruktives Schlafapnoe-Syndrom (OSAS), speziell im Fall der Rechtsherzinsuffizienz
- Nebenwirkungen zahlreicher Medikamente
- Auch kann eine zu große Zähflüssigkeit (Viskosität, Hämokonzentration) des Blutes das Herzzeitvolumen verkleinern.
- Eine Destabilisierung des Transthyretin-Proteins kann eine Transthyretin-Amyloidose mit Kardiomyopathie (ATTR-CM) verursachen. ⓘ
Bei 80 bis 90 % der von Herzinsuffizienz Betroffenen liegt eine Funktionsstörung des Herzmuskels zugrunde, knapp zwei Drittel davon im Sinne einer Herzmuskelschwäche. Die häufigste Ursache der Herzinsuffizienz ist in westlichen Ländern eine Durchblutungsstörung des Herzens (Koronare Herzkrankheit oder KHK) bei 54 bis 70 % der Patienten, bei 35 bis 52 % begleitet von Bluthochdruck. Bei 9 bis 20 % ist der Bluthochdruck (Hypertonie) alleinige Ursache der Herzinsuffizienz. Eine Herzmuskelentzündung (Myokarditis) manifestiert sich bei 60 bis 70 % der betroffenen Patienten als (meist vorübergehende) Herzinsuffizienz. Vitamin-D-Mangel begünstigt Herzinsuffizienz, ebenso ein Eisenmangel, auch ohne gleichzeitig bestehende Anämie. ⓘ
In einer der weltweit größten Beobachtungsstudien mit einer Kohorte von etwa 70.000 erwachsenen Bewohnern Norwegens wurde nun auch festgestellt, dass Patienten mit schweren Schlafstörungen (Einschlafstörung, Durchschlafstörung und fehlende nächtliche Erholung) später deutlich häufiger an einer Herzinsuffizienz erkranken. Dabei konnte ausgeschlossen werden, dass andere Risikofaktoren wie Übergewicht, Diabetes, Bewegungsmangel, Hypertonie, Nikotin oder Alkohol zu der vermehrten Entwicklung einer Herzinsuffizienz geführt haben. ⓘ
Begleiterkrankungen
Herzinsuffizienz tritt selten allein auf. Sie ist vielmehr häufig mit begleitenden Erkrankungen vergesellschaftet, zu denen, je nach Ursache der Herzinsuffizienz, koronare Herzkrankheit, Bluthochdruck, Fettstoffwechselstörungen oder Übergewicht gehören. Ein Vorhofflimmern kann sowohl Folge als auch Ursache einer Herzinsuffizienz sein. Die Häufigkeit der Begleiterkrankungen steht im Zusammenhang mit dem Alter des Patienten, persönlichen Risikofaktoren (z. B. Rauchen) und dem Schweregrad der Herzinsuffizienz selbst, sodass auch von einer Multisystemerkrankung gesprochen wird. Daneben sind Begleiterkrankungen anderer Organsysteme häufig anzutreffen. Dazu gehören chronische Niereninsuffizienz und die Schlafapnoe, die beide fast die Hälfte der Patienten mit Herzinsuffizienz betreffen, Eisenmangel (mehr als 40 %), Anämie (35 bis 40 %), Diabetes mellitus (etwa 30 %), die chronisch obstruktive Lungenerkrankung (COPD, etwa 30 %), Sarkopenie (etwa 20 %) und Kachexie (etwa 10 %) sowie einige andere. Die Symptome der Begleiterkrankungen können mit den eigentlichen Herzinsuffizienz-Symptomen überlappen und gelegentlich schwer zu trennen sein. ⓘ
Diagnostik
Die Diagnose Herzinsuffizienz wird gestellt, wenn typische Symptome (s. o.) und entsprechende objektive Befunde zusammentreffen. ⓘ
Körperliche Untersuchung
Bereits bei der körperlichen Untersuchung können einige klinische Zeichen auf eine Herzinsuffizienz hinweisen. Dazu zählen die Halsvenenstauung, Rasselgeräusche über der Lunge, eine Herzvergrößerung (Kardiomegalie), ein 3. Herzton, Unterschenkelödeme, eine Vergrößerung der Leber (Hepatomegalie), Pleuraergüsse, Nykturie und eine Pulsbeschleunigung (Tachykardie). ⓘ
EKG
Das Elektrokardiogramm ist kaum zur Diagnose einer Herzinsuffizienz geeignet, kann aber zugrundeliegende Krankheiten zeigen, beispielsweise abgelaufene Herzinfarkte oder Herzrhythmusstörungen. Außerdem ergeben sich ggf. andere Therapieempfehlungen, wenn kein Sinusrhythmus oder ein Schenkelblock vorliegt. ⓘ
Ultraschalldiagnostik
Wichtigstes Untersuchungsverfahren bei der Herzinsuffizienz ist die Ultraschalluntersuchung des Herzens (Echokardiografie). Sie erlaubt eine schnelle und risikofreie Beurteilung der Herzmuskelfunktion, der Herzklappen und des Herzbeutels. Einerseits kann so die Verdachtsdiagnose Herzinsuffizienz bestätigt oder ausgeschlossen, andererseits können bereits wesentliche Ursachen festgestellt werden. ⓘ
Eine wesentliche Messgröße in der Echokardiografie ist die Ejektionsfraktion der linken Herzkammer. Die Ejektionsfraktion ist definiert als der Anteil des Schlagvolumens am enddiastolischen Volumen und beschreibt somit, wie vollständig sich das Herz beim Schlagen entleert. Eine geringere Ejektionsfraktion ist mit einer schlechteren Prognose verbunden. Unterschreitet die Ejektionsfraktion 40 %, liegt bei Vorhandensein von Symptomen eine Herzinsuffizienz mit reduzierter Ejektionsfraktion (englisch Heart Failure with reduced Ejection Fraction, HFrEF) vor. Die HFrEF ist die „klassische“, gut erforschte und vergleichsweise gut behandelbare Herzinsuffizienz, wie sie typischerweise bei Männern mit Durchblutungsstörungen des Herzens auftritt. Eine Ejektionsfraktion von mindestens 50 % definiert zusammen mit einigen weiteren Kriterien die Herzinsuffizienz mit erhaltener Ejektionsfraktion (heart failure with preserved ejection fraction, HFpEF), für die Alter, weibliches Geschlecht, Bluthochdruck und Diabetes wesentliche Risikofaktoren sind. Eine Herzinsuffizienz mit erhaltener Ejektionsfraktion kann sich im weiteren Verlauf zu einer Herzinsuffizienz mit reduzierter Ejektionsfraktion verschlechtern. Aufgrund von Fortschritten in der Behandlung von Durchblutungsstörungen des Herzens ist die HFpEF in Industriestaaten heute häufiger als die HFrEF. Zwischen HFrEF und HFpEF ist eine HFmEF (heart failure with mid-range ejection fraction) definiert. Da sich die empfohlene Therapie nach der Ejektionsfraktion richtet, ist eine korrekte Bestimmung besonders wichtig. ⓘ
Die Ejektionsfraktion ist jedoch kein Maß für die Schwere der Herzinsuffizienz. Maßgeblich ist das Herzzeitvolumen. Das Herzzeitvolumen ist das Produkt aus enddiastolischer Ventrikelfüllung, Netto-Ejektionsfraktion und Herzfrequenz. Bei der Berechnung der Ejektionsfraktion muss der Rückfluss von Pendelblut bei Herzklappendefekten und anderen Herzvitien berücksichtigt werden. Dieser Rückfluss heißt Regurgitation oder retrograder Blutfluss und bildet zusammen mit der effektiven Blutejektion die gemessene Brutto-Ejektion. Außerdem muss beachtet werden, dass bei jedem Herzschlag alle vier Herzhöhlen unterschiedliche Füllungsvolumina und damit unterschiedliche Ejektionsfraktionen haben. Bei jedem Herzschlag sind jedoch die vier Schlagvolumina jeweils als Produkt aus Füllungsvolumen und zugehöriger Ejektionsfraktion zwangsläufig identisch. ⓘ
MRT
Beurteilung der Anatomie des Herzens und der großen Gefäße bei komplexen angeborenen Vitien und bei Kardiomyopathien, Vitalitätsnachweis vor ggf. geplanter Wiederherstellung der Durchblutung (Herzkatheter, Bypass-Operation), Stresstest mit Dobutamin oder Adenosin zur Beurteilung und Identifikation relevanter Einengungen (Stenosen) im Bereich der Herzdurchblutung (Koronararterien). ⓘ
Eine neue Studie zeigt, dass die Magnetresonanzspektroskopie dabei helfen kann, das Risiko einer Herzinsuffizienz besser abzuschätzen. ⓘ
Therapie
Kausale Therapie
Wann immer möglich, sollte nach ersten allgemeinen therapeutischen Maßnahmen die Ursache der Herzinsuffizienz beseitigt werden:
- Erhöhter Blutdruck sollte gesenkt werden. Bestimmte blutdrucksenkende Medikamente sind bei Herzinsuffizienz unabhängig vom Vorliegen eines Bluthochdrucks indiziert und sollten deshalb bevorzugt eingesetzt werden.
- Patienten mit einer koronaren Herzkrankheit profitieren oft von einer Ballondilatation der verengten Gefäße mit Stentversorgung oder von einer Bypassoperation.
- Bei einem relevanten Herzklappenfehler sollte eine Klappenrekonstruktion oder ein Klappenersatz erwogen werden.
- Ein obstruktives Schlafapnoe-Syndrom (OSA) sollte behandelt werden.
- Herzrhythmusstörungen (in den meisten Fällen Vorhofflimmern) sollten bei geeigneten Patienten medikamentös oder per Katheterablation behoben werden. Wenn das Herz aufgrund von Erregungsleitungsstörungen nicht gut koordiniert schlägt, kann ein Herzschrittmacher helfen. ⓘ
Nicht-medikamentöse Therapie
Eine Reduktion kardiovaskulärer Risikofaktoren ist anzustreben. Zur nicht-medikamentösen Therapie gehören Gewichtsnormalisierung, reduzierte Kochsalzzufuhr, Limitierung der Flüssigkeitszufuhr (< 2 Liter/Tag) und Alkohol- und Nikotinreduktion bzw. -karenz. In den NYHA-Stadien I-III wird moderates körperliches Training empfohlen, bei dekompensierter Herzinsuffizienz körperliche Schonung bis zur Bettruhe. Reisen in Höhenlagen sowie heißes und feuchtes Klima sollten vermieden werden. Zur dauerhaften Lebensstilveränderung kann der Besuch einer Herzschule sinnvoll sein. ⓘ
Bei durch Herzinsuffizienz verursachte Ateminsuffizienz kann eine Beatmung notwendig werden. Hierbei sollte, wenn möglich, zur Vermeidung einer endotrachealen Intubation zunächst die Anwendung einer nichtinvasen Beatmungsform erfolgen. ⓘ



