Tamsulosin
 | |
 | |
| Klinische Daten | |
|---|---|
| Aussprache | /tæmˈsuːləsɪn/ tam-SOO-lə-sin |
| Handelsnamen | Flomax, andere |
| AHFS/Drugs.com | Monographie |
| MedlinePlus | a698012 |
| Lizenz-Daten |
|
| Schwangerschaft Kategorie |
|
| Wege der Verabreichung | Durch den Mund |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | 100% (durch den Mund) |
| Verstoffwechselung | Leber |
| Eliminationshalbwertszeit | 9-13 Stunden |
| Ausscheidung | 76% Niere |
| Bezeichner | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Chemische und physikalische Daten | |
| Formel | C20H28N2O5S |
| Molare Masse | 408,51 g-mol-1 |
| 3D-Modell (JSmol) | |
SMILES
| |
InChI
| |
| (Überprüfen) | |

Tamsulosin, das unter anderem unter dem Markennamen Flomax vertrieben wird, ist ein Arzneimittel zur Behandlung der symptomatischen gutartigen Prostatahyperplasie (BPH) und der chronischen Prostatitis sowie zur Unterstützung der Passage von Nierensteinen. Der Nutzen bei Nierensteinen ist besser belegt, wenn der Stein größer ist. Das Medikament wird durch den Mund eingenommen. ⓘ
Häufige Nebenwirkungen sind Schwindel, Kopfschmerzen, Schlaflosigkeit, Übelkeit, verschwommenes Sehen und sexuelle Probleme. Andere Nebenwirkungen können Schwindelgefühl im Stehen und Angioödeme sein. Tamsulosin ist ein Alphablocker und wirkt, indem es die Muskeln in der Prostata entspannt. Insbesondere ist es ein α1-Adrenorezeptorblocker. ⓘ
Tamsulosin wurde 1997 für den medizinischen Gebrauch in den Vereinigten Staaten zugelassen. Es ist als Generikum erhältlich. Im Jahr 2019 war es mit mehr als 21 Millionen Verschreibungen das 28. am häufigsten verschriebene Medikament in den Vereinigten Staaten. ⓘ
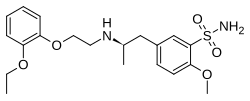
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Tamsulosin | ||||||||||||||||||
| Andere Namen |
(R)-(−)-5-{2-[2-(2-Ethoxyphenoxy)-ethylamino]propyl}-2-methoxy-benzolsulfonamid | ||||||||||||||||||
| Summenformel | C20H28N2O5S | ||||||||||||||||||
| Kurzbeschreibung |
weißes bis fast weißes Pulver (Tamsulosin·Hydrochlorid) | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code |
G04CA02 | ||||||||||||||||||
| Wirkstoffklasse |
Alphablocker | ||||||||||||||||||
| Wirkmechanismus |
α1-Adrenozeptor-Antagonist | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | |||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
228–230 °C (Tamsulosin·Hydrochlorid) | ||||||||||||||||||
| Löslichkeit |
schwer löslich in Wasser, leicht löslich in Ameisensäure, schwer löslich in Ethanol (Tamsulosin·Hydrochlorid) | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
650 mg·kg−1 (LD50, Ratte, oral, Hydrochlorid) | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Tamsulosin ist ein Arzneistoff aus der Klasse der Alpha-Rezeptorenblocker zur Behandlung von Symptomen der benignen Prostatahyperplasie (BPH) und unterliegt der ärztlichen Verschreibungspflicht. Tamsulosin findet als Tamsulosin-Hydrochlorid pharmazeutische Anwendung. ⓘ
Medizinische Anwendungen

Tamsulosin wird hauptsächlich bei gutartiger Prostatahyperplasie und zur Unterstützung der Passage von Nierensteinen eingesetzt. Tamsulosin scheint jedoch nur bei Steinen von mehr als 4 mm und weniger als 10 mm Größe wirksam zu sein. ⓘ
Tamsulosin wird auch als Zusatzbehandlung bei akutem Harnverhalt eingesetzt. Bei Menschen, die Tamsulosin einnehmen, kann die Entleerung nach einer Katheterentfernung erfolgreicher sein. Menschen, die Tamsulosin einnehmen, müssen auch seltener erneut katheterisiert werden. ⓘ
Tamsulosin verringert nicht die Gesamtgröße der Prostata bei Männern mit gutartiger Prostatahyperplasie (BPH) und wird nicht zur Prävention von Prostatakrebs empfohlen. ⓘ
Kombinationstherapie
Tamsulosin ist zur Behandlung von Symptomen des unteren Harntraktes bei der benignen Prostatahyperplasie zugelassen und gilt für diese Indikation als Mittel der ersten Wahl. Es zeigt im Vergleich zu anderen Alphablockern, wie etwa Doxazosin und Alfuzosin, eine geringere Beeinflussung des Blutdruckes (die allerdings nicht immer ausgeschlossen werden kann). ⓘ
Eine klinische Studie mit Nierenstein-Patienten nach ESWL-Behandlung ergab, dass mit Tamsulosin behandelte Patienten besser in der Lage waren, Steintrümmer auszuscheiden. ⓘ
Bei der Behandlung von Prostatakarzinomen mit Low-Dose-Rate-Brachytherapie werden sogenannte Seeds dauerhaft in die Prostata eingesetzt. In den ersten sechs Monaten nach dem Eingriff sind Harndrang, Dysurie und Polyurie häufig. Durch eine prophylaktische Gabe von Tamsulosin können die urologischen Symptome vermindert werden. ⓘ
Die Ergebnisse der CombAT-Studie (Kombination aus Dutasterid (Avodart) und Tamsulosin, Markenname Duodart) aus dem Jahr 2008 haben gezeigt, dass die Behandlung mit der Kombination aus Dutasterid und Tamsulosin bei der Behandlung der gutartigen Prostatahyperplasie einen größeren Nutzen für die Symptome bringt als die Monotherapie mit einem der beiden Wirkstoffe allein. Aus der CombAT-Studie wurde das Medikament Jalyn entwickelt. Es wurde am 14. Juni 2010 von der FDA zugelassen. Diese Kombination kann nützlich sein, da es bei der Anwendung von 5-alpha-Reduktase-Hemmern wie Dutasterid bis zu sechs Monate dauern kann, bis eine Linderung der Symptome eintritt, im Gegensatz zu Alpha-1-Rezeptorblockern, die in einigen Fällen innerhalb von 48 Stunden Linderung verschaffen können. ⓘ
Unerwünschte Wirkungen
- Augen: Bei Patienten, die Tamsulosin einnehmen, kann es während einer Kataraktoperation zu einer Komplikation kommen, die als Floppy-Iris-Syndrom bekannt ist. Wenn der Chirurg über die Vorgeschichte der Person mit diesem Arzneimittel Bescheid weiß und somit die Möglichkeit hat, alternative Techniken anzuwenden, werden die unerwünschten Folgen der Operation erheblich verringert.
- Schwere Hypotension.
- Personen mit Herzerkrankungen, einschließlich Hypotonie, mechanischem Herzversagen (Herzklappen, Lungenembolie, Herzbeutelentzündung) und kongestiver Herzinsuffizienz sollten während der Einnahme von Tamsulosin sorgfältig überwacht werden.
- Alphablocker, einschließlich Prazosin, Terazosin, Doxazosin oder Tamsulosin, scheinen keinen Einfluss auf die Gesamtmortalität bei erneuter Hospitalisierung wegen Herzinsuffizienz bei Patienten zu haben, die auch β-Blocker erhalten.
- Tamsulosin kann auch eine retrograde Ejakulation verursachen, bei der der Samen in die Harnblase umgeleitet wird, anstatt normal ejakuliert zu werden. Dies liegt daran, dass Tamsulosin die Muskeln des Harnröhrenschließmuskels entspannt, die normalerweise während des Samenergusses geschlossen sind. Diese Nebenwirkung kann durch regelmäßiges Beckenbodentraining (Kegel) und Anspannen des Beckenbodens während des Samenergusses gemildert werden. ⓘ
Mechanismus
Tamsulosin ist ein selektiver α1-Rezeptor-Antagonist, der eine bevorzugte Selektivität für den α1A-Rezeptor in der Prostata gegenüber dem α1B-Rezeptor in den Blutgefäßen aufweist. ⓘ
Wenn Alpha-1-Rezeptoren im Blasenhals, in der Prostata, im Harnleiter und in der Harnröhre blockiert werden, kommt es zu einer Entspannung des glatten Muskelgewebes. Dieser Mechanismus verringert den Widerstand gegen den Harnfluss, reduziert die mit BPH verbundenen Beschwerden und erleichtert die Passage von Nierensteinen. ⓘ
Die selektive Wirkung von Tamsulosin an den Alpha-1A/D-Rezeptoren ist umstritten, und mehr als drei Viertel der für Tamsulosin registrierten Humanstudien sind unveröffentlicht. ⓘ
Markennamen
Tamsulosin wurde erstmals 1996 unter dem Handelsnamen Flomax auf den Markt gebracht. Das US-Patent lief im Oktober 2009 aus. Die US-Arzneimittelbehörde FDA (Food and Drug Administration) hat im März 2010 Generika zugelassen. Im Jahr 2010 war Tamsulosin in Großbritannien als rezeptfreies Medikament erhältlich. ⓘ
Es wird von verschiedenen Unternehmen in Lizenz vermarktet, darunter Boehringer Ingelheim und CSL. Tamsulosinhydrochlorid-Kapseln mit verlängerter Wirkstofffreisetzung werden unter den Handelsnamen Urimax 0,4 (Indien), Flomax, Flomaxtra, Contiflo XL, bestflo, Mecir LP (Frankreich), Urimax und Pradif vermarktet, obwohl generische Kapseln mit unveränderter Wirkstofffreisetzung in vielen Ländern (z. B. Kanada) weiterhin zugelassen sind und vermarktet werden. Generische Tabletten mit verlängerter Wirkstofffreisetzung sind in den meisten Ländern des EWR auf dem Markt. In Mexiko wird es als Secotex und in Japan und Indonesien als Harnal D und in Thailand als Harnal OCAS (oral controlled absorption system) vermarktet. In Ägypten, Italien, Russland und Island wird es von Astellas Pharma Europe unter dem Handelsnamen Omnic vertrieben. Der größte Hersteller des Wirkstoffs Tamsulosin ist Synthon BV (Niederlande). Tamsulosinhydrochlorid wird in Bangladesch unter den Handelsnamen Uromax, Prostanil MR, Tamisol MR und Tamsin vermarktet. ⓘ
Pharmakologie
Nebenwirkungen
Trotz der Prostataselektivität dieses Alphablockers können häufig (1 bis 10 %) Schwindel und gelegentlich (< 1 %) Hypotonie und orthostatische Beschwerden auftreten; häufig werden auch Ejakulationsstörungen (retrograde Ejakulation) beobachtet. Durch eine Dosisanpassung kann in vielen Fälle eine Ejakulationsstörung vermieden werden. Selten kann es zu einer vaskulär bedingten Synkope kommen, einem plötzlichen Kräfteverlust mit Bewusstlosigkeit, ferner zu gelegentlichen bis seltenen unspezifischen Beschwerden des Magen-Darm-Traktes, wie Übelkeit, Durchfall oder Verstopfungen. In der Augenheilkunde wurde über einen Zusammenhang mit dem intraoperativen „floppy-iris-syndrome“ bei Katarakt-Operationen berichtet. ⓘ
Wechselwirkungen
Klinisch relevante Wechselwirkungen sind nicht bekannt. ⓘ
Handelsnamen
- Monopräparate
Aglandin (A), Alna (D, A), Flomax (USA), Omnic (D), Omix (CH), Pradif (CH), Prostacure (D), Prostadil (D), Prostalitan (D), Tamsublock (D), Stichtulosin (A), Tadin (D), zahlreiche Generika (D, A, CH) ⓘ