Thiamin
 | |
 Skelettformel und Kugel-Stab-Modell des Kations in Thiamin | |
| Klinische Daten | |
|---|---|
| Aussprache | /ˈθaɪ.əmɪn/ THY-ə-min |
| Andere Bezeichnungen | Vitamin B1, Aneurin, Thiamin |
| AHFS/Drugs.com | Monographie |
| Lizenz-Daten |
|
| Wege der Verabreichung | durch den Mund, IV, IM |
| Wirkstoffklasse | Vitamin |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | 3,7% bis 5,3% |
| Bezeichnungen | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| ChEBI |
|
| ChEMBL |
|
| Chemische und physikalische Daten | |
| Formel | C12H17N4OS+ |
| Molekulare Masse | 265,36 g-mol-1 |
| 3D-Modell (JSmol) |
|
SMILES
| |
InChI
| |
Thiamin, auch bekannt als Thiamin und Vitamin B1, ist ein Vitamin, ein essentieller Mikronährstoff, der vom Körper nicht selbst hergestellt werden kann. Es kommt in Lebensmitteln vor und wird kommerziell als Nahrungsergänzungsmittel oder Medikament synthetisiert. Zu den Nahrungsquellen für Thiamin gehören Vollkorngetreide, Hülsenfrüchte und einige Fleisch- und Fischsorten. Bei der Verarbeitung von Getreide wird ein Großteil des Thiamingehalts entfernt, so dass in vielen Ländern Getreide und Mehl mit Thiamin angereichert werden. Es gibt Nahrungsergänzungsmittel und Medikamente zur Behandlung und Vorbeugung von Thiaminmangel und daraus resultierenden Erkrankungen wie Beriberi und Wernicke-Enzephalopathie. Weitere Anwendungsgebiete sind die Behandlung der Ahornsirup-Urin-Krankheit und des Leigh-Syndroms. Sie werden in der Regel durch den Mund eingenommen, können aber auch intravenös oder intramuskulär injiziert werden. ⓘ
Thiaminzusätze werden im Allgemeinen gut vertragen. Allergische Reaktionen, einschließlich Anaphylaxie, können auftreten, wenn wiederholte Dosen per Injektion verabreicht werden. Thiamin wird für den Stoffwechsel benötigt, unter anderem für den von Glukose, Aminosäuren und Lipiden. Thiamin steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation. Thiamin ist sowohl als Generikum als auch als rezeptfreies Medikament erhältlich. ⓘ
| Strukturformel ⓘ | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Struktur von Thiaminchlorid | |||||||||
| Allgemeines | |||||||||
| Trivialname | Vitamin B1 | ||||||||
| Andere Namen |
| ||||||||
| Summenformel |
| ||||||||
| CAS-Nummer | |||||||||
| ATC-Code |
A11DA01 | ||||||||
| Kurzbeschreibung | farbloses Pulver, charakteristischer Geruch | ||||||||
| Vorkommen | siehe Tabelle im Artikeltext | ||||||||
| Physiologie | |||||||||
| Funktion | Kohlenhydratstoffwechsel, Coenzym bei dehydrierenden Decarboxylierungsreaktionen (z. B. im Pyruvatdehydrogenasekomplex) | ||||||||
| Täglicher Bedarf | 1,0–1,2 mg | ||||||||
| Folgen bei Mangel | Muskelatrophie, Herzinsuffizienz, neurologische Störungen, Beriberi, Wernicke-Enzephalopathie | ||||||||
| Überdosis | nicht bekannt | ||||||||
| Eigenschaften | |||||||||
| Molare Masse | 337,27 g·mol−1 (Hydrochlorid) | ||||||||
| Aggregatzustand | fest | ||||||||
| Schmelzpunkt |
| ||||||||
| Löslichkeit | sehr gut löslich in Wasser (500 g·l−1) | ||||||||
| Sicherheitshinweise | |||||||||
| |||||||||
| Toxikologische Daten | |||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||
Thiamin, Vitamin B1 oder Aneurin ist ein wasserlösliches Vitamin aus dem B-Komplex von schwachem, aber charakteristischem Geruch und ist insbesondere für die Funktion des Nervensystems unentbehrlich. Wird das Vitamin B1 für ca. 14 Tage dem Körper nicht mehr zugeführt, sind die Reserven zu 50 % aufgebraucht. ⓘ
Definition
Thiamin, auch bekannt als Vitamin B1, ist eines der B-Vitamine. Im Gegensatz zu Folat und Vitamin B6, die in mehreren chemisch verwandten Formen, den sogenannten Vitameren, vorkommen, ist Thiamin nur eine einzige chemische Verbindung. Es ist löslich in Wasser, Methanol und Glycerin, aber praktisch unlöslich in weniger polaren organischen Lösungsmitteln. Thiamin wird normalerweise als Chloridsalz geliefert. Es wird durch Einwirkung von Wärme abgebaut. Im Körper ist die am besten charakterisierte Form Thiaminpyrophosphat (TPP), auch Thiamindiphosphat genannt, ein Coenzym beim Abbau von Zuckern und Aminosäuren. ⓘ
Mangel
Zu den unspezifischen Anzeichen eines Thiaminmangels gehören Unwohlsein, Gewichtsverlust, Reizbarkeit und Verwirrtheit. Bekannte Erkrankungen, die durch Thiaminmangel verursacht werden, sind Beriberi, das Wernicke-Korsakoff-Syndrom, die Optikusneuropathie, die Leigh-Krankheit, die afrikanische saisonale Ataxie (oder nigerianische saisonale Ataxie) und die zentrale pontine Myelinolyse. ⓘ
In den westlichen Ländern ist chronischer Alkoholismus eine sekundäre Ursache. Ebenfalls gefährdet sind ältere Erwachsene, Personen mit HIV/AIDS oder Diabetes und Personen, die sich einer bariatrischen Operation unterzogen haben. Unterschiedliche Grade von Thiaminmangel wurden mit der langfristigen Einnahme hoher Dosen von Diuretika in Verbindung gebracht. ⓘ
Chemie
Seine Struktur besteht aus einem Aminopyrimidin und einem Thiazoliumring, die durch eine Methylenbrücke verbunden sind. Das Thiazol ist mit Methyl- und Hydroxyethyl-Seitenketten substituiert. Thiamin ist ein Kation und wird normalerweise als Chloridsalz geliefert. Die Aminogruppe kann mit weiteren Säuren zusätzliche Salze bilden. Es ist bei saurem pH-Wert stabil, aber in alkalischen Lösungen und unter Hitzeeinwirkung instabil. Thiamin reagiert stark in Reaktionen vom Maillard-Typ. ⓘ
Thiamin besteht aus zwei Ringsystemen, die durch eine Methylenbrücke miteinander verbunden sind: einem Pyrimidin- und einem Thiazolring. ⓘ
Funktionen
Thiaminphosphat-Derivate sind an vielen zellulären Prozessen beteiligt. Die am besten charakterisierte Form ist Thiaminpyrophosphat (TPP), ein Coenzym beim Katabolismus von Zuckern und Aminosäuren. Es sind fünf natürliche Thiaminphosphat-Derivate bekannt: Thiaminmonophosphat (ThMP), Thiamindiphosphat (ThDP), auch Thiaminpyrophosphat (TPP) genannt, Thiamintriphosphat (ThTP), Adenosintriamintriphosphat (AThTP) und Adenosintiamindiphosphat (AThDP). Während die Rolle von Thiamindiphosphat als Coenzym bekannt und umfassend charakterisiert ist, kann die nicht-koenzymatische Wirkung von Thiamin und seinen Derivaten durch die Bindung an eine Reihe kürzlich identifizierter Proteine realisiert werden, die die katalytische Wirkung von Thiamindiphosphat nicht nutzen. ⓘ
Thiamin-Diphosphat
Für das Monophosphat ist keine physiologische Rolle bekannt. Das Diphosphat ThPP ist physiologisch relevant. Seine Synthese wird durch das Enzym Thiamin-Diphosphokinase nach der Reaktion Thiamin + ATP → ThDP + AMP (EC 2.7.6.2) katalysiert. ThDP ist ein Coenzym für mehrere Enzyme, die die Übertragung von Zweikohlenstoffeinheiten und insbesondere die Dehydrierung (Decarboxylierung und anschließende Konjugation mit Coenzym A) von 2-Oxosäuren (Alpha-Ketosäuren) katalysieren. Beispiele hierfür sind:
- In den meisten Arten vorhanden
- Pyruvatdehydrogenase und 2-Oxoglutaratdehydrogenase (auch α-Ketoglutaratdehydrogenase genannt)
- verzweigtkettige α-Ketosäure-Dehydrogenase
- 2-Hydroxyphytanoyl-CoA-Lyase
- Transketolase
- In einigen Arten vorhanden:
- Pyruvat-Decarboxylase (in Hefe)
- mehrere zusätzliche bakterielle Enzyme ⓘ
Die Enzyme Transketolase, Pyruvatdehydrogenase (PDH) und 2-Oxoglutaratdehydrogenase (OGDH) sind alle wichtig für den Kohlenhydratstoffwechsel. Das zytosolische Enzym Transketolase ist ein Hauptakteur im Pentosephosphatweg, einem wichtigen Weg für die Biosynthese der Pentosezucker Desoxyribose und Ribose. Die mitochondriale PDH und OGDH sind Teil der biochemischen Wege, die zur Erzeugung von Adenosintriphosphat (ATP) führen, das eine wichtige Energieform für die Zelle darstellt. PDH ist das Bindeglied zwischen der Glykolyse und dem Zitronensäurezyklus, während die von OGDH katalysierte Reaktion ein ratenlimitierender Schritt im Zitronensäurezyklus ist. Im Nervensystem ist die PDH auch an der Produktion von Acetylcholin, einem Neurotransmitter, und an der Myelinsynthese beteiligt. ⓘ
Thiamintriphosphat
ThTP wurde lange Zeit als eine spezifische neuroaktive Form von Thiamin angesehen, die eine Rolle in Chloridkanälen in den Neuronen von Säugetieren und anderen Tieren spielt, obwohl dies nicht vollständig geklärt ist. Es wurde jedoch gezeigt, dass ThTP in Bakterien, Pilzen, Pflanzen und Tieren vorkommt, was auf eine viel allgemeinere zelluläre Rolle schließen lässt. Insbesondere in E. coli scheint es eine Rolle bei der Reaktion auf Aminosäuremangel zu spielen. ⓘ
Adenosin-Thiamin-Diphosphat
AThDP kommt in geringen Mengen in der Leber von Wirbeltieren vor, seine Rolle ist jedoch noch unbekannt. ⓘ
Adenosin-Thiamin-Triphosphat
AThTP kommt in Escherichia coli vor, wo es sich als Folge von Kohlenstoffmangel anreichert. In E. coli kann AThTP bis zu 20 % des gesamten Thiamins ausmachen. In geringeren Mengen kommt es auch in Hefe, Wurzeln höherer Pflanzen und tierischem Gewebe vor. ⓘ
Medizinische Anwendungen
Pränatale Nahrungsergänzung
Schwangere und stillende Frauen haben einen erhöhten Thiaminbedarf, da Thiamin vor allem im dritten Trimester bevorzugt an den Fötus und die Plazenta abgegeben wird. Bei stillenden Frauen geht Thiamin in die Muttermilch über, auch wenn dies zu einem Thiaminmangel bei der Mutter führt. Schwangere mit Hyperemesis gravidarum haben ebenfalls ein erhöhtes Risiko für einen Thiaminmangel, da sie beim Erbrechen Thiamin verlieren. ⓘ
Thiamin ist nicht nur für die Entwicklung der Mitochondrienmembran, sondern auch für die Funktion der Synaptosomenmembran wichtig. Es gibt auch Hinweise darauf, dass Thiaminmangel eine Rolle bei der schlechten Entwicklung des kindlichen Gehirns spielt, die zum plötzlichen Kindstod (SIDS) führen kann. ⓘ
Empfehlungen für die Ernährung
Die Nationale Medizinische Akademie der USA hat 1998 den geschätzten durchschnittlichen Bedarf (Estimated Average Requirements, EARs) und die empfohlenen Tagesdosen (Recommended Dietary Allowances, RDAs) für Thiamin aktualisiert. Die EAR-Werte für Thiamin für Frauen und Männer ab 14 Jahren betragen 0,9 mg/Tag bzw. 1,1 mg/Tag; die RDA-Werte liegen bei 1,1 bzw. 1,2 mg/Tag. Die RDAs sind höher als die EARs, um eine angemessene Zufuhr für Personen mit überdurchschnittlichem Bedarf zu gewährleisten. Die RDA während der Schwangerschaft und für stillende Frauen beträgt 1,4 mg/Tag. Für Säuglinge bis zum Alter von 12 Monaten beträgt die Adequate Intake (AI) 0,2-0,3 mg/Tag und für Kinder im Alter von 1-13 Jahren steigt die RDA mit dem Alter von 0,5 bis 0,9 mg/Tag. Was die Sicherheit anbelangt, so legt die IOM für Vitamine und Mineralstoffe tolerierbare Höchstmengen fest, wenn die Beweise ausreichen. Für Riboflavin gibt es keinen UL, da es keine Humandaten über schädliche Wirkungen hoher Dosen gibt. Die EARs, RDAs, AIs und ULs werden zusammen als Dietary Reference Intakes (DRIs) bezeichnet. ⓘ
Die Europäische Behörde für Lebensmittelsicherheit (EFSA) bezeichnet die Gesamtheit der Informationen als Referenzwerte für die Ernährung (Dietary Reference Values), wobei die Bevölkerungsreferenzzufuhr (PRI) anstelle der RDA und der durchschnittliche Bedarf (Average Requirements) anstelle der EAR verwendet werden. AI und UL sind genauso definiert wie in den Vereinigten Staaten. Für Frauen (einschließlich Schwangere und Stillende), Männer und Kinder beträgt die PRI 0,1 mg Thiamin pro Megajoule (MJ) der aufgenommenen Energie. Da die Umrechnung 1 MJ = 239 kcal beträgt, sollte ein Erwachsener, der 2390 Kilokalorien verbraucht, 1,0 mg Thiamin zu sich nehmen. Dies ist etwas niedriger als der RDA-Wert in den USA. Die Europäische Behörde für Lebensmittelsicherheit (EFSA) prüfte dieselbe Sicherheitsfrage und kam ebenfalls zu dem Schluss, dass es keine ausreichenden Beweise für die Festlegung eines UL für Thiamin gibt. ⓘ
| Vereinigte Staaten ⓘ | ||
| Altersgruppe | RDA (mg/Tag) | Tolerierbare obere Aufnahmemenge |
|---|---|---|
| Säuglinge 0-6 Monate | 0.2* | ND |
| Kleinkinder 6-12 Monate | 0.3* | |
| 1-3 Jahre | 0.5 | |
| 4-8 Jahre | 0.6 | |
| 9-13 Jahre | 0.9 | |
| Frauen 14-18 Jahre | 1.0 | |
| Männer 14+ Jahre | 1.2 | |
| Frauen 19+ Jahre | 1.1 | |
| Schwangere/laktierende Frauen 14-50 | 1.4 | |
| * Angemessene Zufuhr für Säuglinge, da eine RDA noch nicht festgelegt wurde | ||
| Europäische Behörde für Lebensmittelsicherheit | ||
| Altersgruppe | Angemessene Zufuhr (mg/MJ) | Tolerierbare Obergrenze |
| Alle Personen ab 7 Monaten | 0.1 | ND |
Der Bedarf korreliert mit dem täglichen Energieverbrauch. Daher benötigen Männer und junge Erwachsene etwas mehr Vitamin B1. ⓘ
In Südamerika wird häufig Thiamingabe vor Reisen in das Amazonasgebiet als Abwehr gegen Moskitos eingesetzt, da die Mücken den Geruch ablehnen würden. Die Schutzwirkung ist individuell verschieden und wird von zahlreichen Autoren angezweifelt. ⓘ
Thiamin wird im Blut, in der Leber, der Niere, im Gehirn und in den Muskeln gespeichert, wenngleich die Speicherfähigkeit mit 25–30 mg eher niedrig ist. ⓘ
Sicherheit
Thiamin ist bei oraler Verabreichung im Allgemeinen gut verträglich und nicht toxisch. In seltenen Fällen wurde über unerwünschte Nebenwirkungen berichtet, wenn Thiamin intravenös verabreicht wird, darunter allergische Reaktionen, Übelkeit, Lethargie und Koordinationsschwierigkeiten. ⓘ
Kennzeichnung
Bei der Kennzeichnung von Nahrungsmitteln und Nahrungsergänzungsmitteln in den USA wird die Menge in einer Portion als Prozentsatz des Tageswertes (%DV) angegeben. Bei der Kennzeichnung von Thiamin betrug 100 % des Tageswerts 1,5 mg, aber seit dem 27. Mai 2016 wurde dieser Wert auf 1,2 mg geändert, um ihn mit der RDA in Einklang zu bringen. Eine Tabelle mit den alten und neuen Tageswerten für Erwachsene finden Sie unter Reference Daily Intake. ⓘ
Quellen
Thiamin ist hitzeempfindlich, es wird durch Kochen zerstört. Es ist wasserlöslich, dadurch geht beim Kochen in Wasser ein Teil ins Kochwasser verloren. In rohem Fisch und Farnen ist das Enzym Thiaminase enthalten, das Thiamin abbaut und somit vernichtet. Konservierungsstoffe aus der Gruppe der Sulfite (E 220 – E 228) zersetzen ebenfalls Thiamin. ⓘ
Bei der Herstellung von weißem Mehl (z. B. Typ 405) oder weißem Reis wird der braune Keim der Pflanze vom Rest des Samens (Endosperm) entfernt. Der Keim enthält jedoch das gesamte Vitamin B1 des Samens, welches zur Verbrennung der enthaltenen Kohlenhydrate benötigt wird. ⓘ
Im Gegensatz dazu bleibt in Vollkornmehl, braunem Reis oder parboiled Reis das Vitamin B1 weitestgehend enthalten. ⓘ
Thiamin ist in einer Vielzahl von verarbeiteten und vollwertigen Lebensmitteln enthalten. Linsen, Erbsen, Vollkornprodukte, Schweinefleisch und Nüsse sind reichhaltige Quellen. ⓘ
Schwangeren Frauen wird häufig empfohlen, täglich ein pränatales Multivitaminpräparat einzunehmen, um eine angemessene Mikronährstoffzufuhr zu gewährleisten. Die Zusammensetzung der Mikronährstoffe variiert zwar von Vitamin zu Vitamin, aber ein typisches tägliches pränatales Vitaminprodukt enthält etwa 1,5 mg Thiamin. ⓘ
Antagonisten
Thiamin in Lebensmitteln kann auf verschiedene Weise abgebaut werden. Sulfite, die Lebensmitteln in der Regel als Konservierungsmittel zugesetzt werden, greifen Thiamin an der Methylenbrücke in der Struktur an und spalten den Pyrimidinring vom Thiazolring ab. Die Geschwindigkeit dieser Reaktion ist unter sauren Bedingungen erhöht. Thiamin wird durch thermolabile Thiaminasen (die in rohem Fisch und Schalentieren vorkommen) abgebaut. Einige Thiaminasen werden von Bakterien produziert. Bakterielle Thiaminasen sind Zelloberflächenenzyme, die vor ihrer Aktivierung von der Membran dissoziieren müssen; die Dissoziation kann bei Wiederkäuern unter azidotischen Bedingungen erfolgen. Pansenbakterien reduzieren auch Sulfat zu Sulfit, so dass eine hohe Sulfatzufuhr mit der Nahrung thiaminantagonistische Wirkungen haben kann. ⓘ
Pflanzliche Thiaminantagonisten sind hitzestabil und kommen sowohl als ortho- als auch als para-Hydroxyphenole vor. Einige Beispiele für diese Antagonisten sind Kaffeesäure, Chlorogensäure und Gerbsäure. Diese Verbindungen interagieren mit dem Thiamin und oxidieren den Thiazolring, so dass es nicht absorbiert werden kann. Zwei Flavonoide, Quercetin und Rutin, wurden ebenfalls als Thiamin-Antagonisten in Betracht gezogen. ⓘ
Anreicherung von Lebensmitteln
In einigen Ländern ist die Anreicherung von Getreidenahrungsmitteln wie Weizen, Reis oder Mais vorgeschrieben oder empfohlen, da der Vitamingehalt durch die Verarbeitung sinkt. Im Februar 2022 schreiben 59 Länder, vor allem in Nord- und Subsahara-Afrika, die Anreicherung von Weizen, Reis oder Mais mit Thiamin oder Thiaminmononitrat vor. Die vorgeschriebenen Mengen reichen von 2,0 bis 10,0 mg/kg. Weitere 18 Länder haben ein freiwilliges Anreicherungsprogramm. Die indische Regierung empfiehlt beispielsweise 3,5 mg/kg für "Maida" (Weißmehl) und "Atta" (Vollkornmehl). ⓘ
Um den Verlust bei der Verarbeitung auszugleichen, wird in vielen Ländern dem Mehl und Reis das Vitamin B1 wieder künstlich zugesetzt. Inzwischen verfahren 71 Länder bei Mehl so, darunter Großbritannien, USA und Kanada, jedoch nicht Deutschland. Thiaminhydrochlorid ist in der EU durch die Verordnung (EG) Nr. 1334/2008 unter der FL-Nummer 16.027 als Aromastoff zugelassen. ⓘ
Nahrungsergänzungsmittel
In Deutschland und anderen EU-Ländern ist Thiamin in folgender Form in Nahrungsergänzungsmitteln (NEM) erlaubt:
- Thiaminhydrochlorid
- Thiaminmononitrat
- Thiaminmonophosphatchlorid
- Thiaminpyrophosphatchlorid ⓘ
Wenn mindestens 0,17 mg Thiamin pro Tagesdosis (etwa 15 % des Referenzwertes) in NEMs erhalten ist, darf mit der Aufrechterhaltung normaler Körperfunktionen geworben werden: Energiestoffwechsel, psychischen Funktion, Funktion des Nervensystems und Herzfunktion. Eine Werbung für eine angebliche zusätzliche Leistungssteigerung ist nicht belegt. Auch für eine postulierte Wirksamkeit bei Nervenschmerzen (neuropathische Schmerzen) fehlen Wirksamkeitsnachweise und dürfen nicht beworben werden. ⓘ
Synthese
Biosynthese
Die Biosynthese von Thiamin findet in Bakterien, einigen Protozoen, Pflanzen und Pilzen statt. Die Thiazol- und Pyrimidin-Anteile werden getrennt biosynthetisiert und dann durch die Wirkung der Thiamin-Phosphat-Synthase zu Thiaminmonophosphat (ThMP) kombiniert. ⓘ
Das Pyrimidin-Ringsystem wird in einer Reaktion gebildet, die von der Phosphomethylpyrimidin-Synthase (ThiC) katalysiert wird, einem Enzym der radikalen SAM-Superfamilie von Eisen-Schwefel-Proteinen, die S-Adenosylmethionin als Cofaktor verwenden.
Das Ausgangsmaterial ist 5-Aminoimidazol-Ribotid, das eine Umlagerungsreaktion über radikalische Zwischenprodukte durchläuft, die die gezeigten blauen, grünen und roten Fragmente in das Produkt einbauen. ⓘ
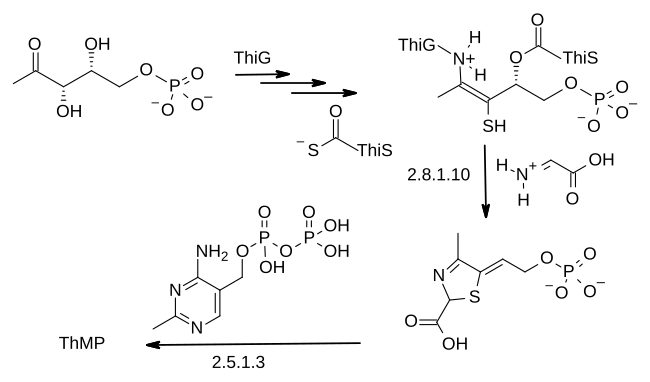
Der Thiazolring wird in einer Reaktion gebildet, die von der Thiazolsynthase katalysiert wird. Die Ausgangsstoffe sind 1-Desoxy-D-xylulose-5-phosphat, 2-Iminoacetat und ein Schwefelträgerprotein namens ThiS. Diese werden durch die Wirkung einer weiteren Proteinkomponente, ThiG, zusammengesetzt.
Der letzte Schritt zur Bildung von ThMP umfasst die Decarboxylierung des Thiazol-Zwischenprodukts, das mit dem Pyrophosphat-Derivat des Phosphomethylpyrimidins reagiert, das wiederum ein Produkt einer Kinase, der Phosphomethylpyrimidin-Kinase, ist. ⓘ

Die Biosynthesewege können sich von Organismus zu Organismus unterscheiden. In E. coli und anderen Enterobakterien kann ThMP durch eine Thiamin-Phosphat-Kinase zu dem Cofaktor Thiamindiphospat (ThDP) phosphoryliert werden (ThMP + ATP → ThDP + ADP). In den meisten Bakterien und in Eukaryonten wird ThMP zu Thiamin hydrolysiert, das dann durch Thiamindiphosphokinase zu ThDP pyrophosphoryliert werden kann (Thiamin + ATP → ThDP + AMP). ⓘ
Die Biosynthesewege werden durch Riboswitches reguliert. Wenn genügend Thiamin in der Zelle vorhanden ist, bindet das Thiamin an die mRNAs für die Enzyme, die in diesem Weg benötigt werden, und verhindert deren Übersetzung. Ist kein Thiamin vorhanden, kommt es zu keiner Hemmung, und die für die Biosynthese erforderlichen Enzyme werden produziert. Der spezifische Riboschalter, der TPP-Riboschalter (oder ThDP), ist der einzige Riboschalter, der sowohl in eukaryotischen als auch in prokaryotischen Organismen identifiziert wurde. ⓘ
Synthese im Labor
Bei der ersten Totalsynthese im Jahr 1936 wurde 3-Ethoxypropanoat mit Ethylformiat behandelt, um eine Dicarbonyl-Zwischenverbindung zu erhalten, die bei der Reaktion mit Acetamidin ein substituiertes Pyrimidin bildete. Die Hydroxylgruppe wurde durch nukleophile aromatische Substitution in eine Aminogruppe umgewandelt, und zwar zunächst mit Phosphoroxychlorid in das Chloridderivat und anschließend mit Ammoniak. Die Ethoxygruppe wurde dann mit Bromwasserstoffsäure in ein Bromderivat umgewandelt, das für die letzte Stufe bereit war, in der Thiamin (als sein Dibromidsalz) in einer Alkylierungsreaktion mit 4-Methyl-5-(2-hydroxyethyl)thiazol gebildet wurde. ⓘ
Industrielle Synthese

Die Synthese im Labormaßstab von 1936 wurde von Merck & Co. entwickelt und ermöglichte ihnen 1937 die Herstellung von Thiamin in Rahway. Ein alternativer Weg unter Verwendung des Zwischenprodukts Grewe-Diamin (5-(Aminomethyl)-2-methyl-4-pyrimidinamin), der erstmals 1937 veröffentlicht wurde, wurde jedoch von Hoffman La Roche untersucht, und es folgten wettbewerbsfähige Herstellungsverfahren. Effiziente Wege zu diesem Diamin sind weiterhin von Interesse. Im Europäischen Wirtschaftsraum ist Thiamin unter der REACH-Verordnung registriert, und es werden dort jährlich zwischen 100 und 1.000 Tonnen hergestellt oder eingeführt. ⓘ
Absorption, Stoffwechsel und Ausscheidung
Thiaminphosphatester in der Nahrung werden im oberen Dünndarm durch die intestinale alkalische Phosphatase zu Thiamin hydrolisiert. Bei niedrigen Konzentrationen erfolgt die Absorption durch Carrier. Bei höheren Konzentrationen erfolgt die Absorption auch über passive Diffusion. Der aktive Transport kann durch Alkoholkonsum oder Folsäuremangel gehemmt werden. ⓘ
Der größte Teil des Thiamins im Serum ist an Proteine, hauptsächlich Albumin, gebunden. Ungefähr 90 % des gesamten Thiamins im Blut befinden sich in den Erythrozyten. In Ratten-Serum wurde ein spezifisches Bindungsprotein namens Thiamin-bindendes Protein (TBP) identifiziert, von dem man annimmt, dass es ein hormonell reguliertes Trägerprotein ist, das für die Verteilung von Thiamin im Gewebe wichtig ist. Die Aufnahme von Thiamin durch Zellen im Blut und in anderen Geweben erfolgt durch aktiven Transport und passive Diffusion. Etwa 80 % des intrazellulären Thiamins ist phosphoryliert und der größte Teil ist an Proteine gebunden. Zwei Mitglieder der SLC-Genfamilie von Transporterproteinen, die von den Genen SLC19A2 und SLC19A3 kodiert werden, sind zum Thiamintransport in der Lage. In einigen Geweben scheint die Thiaminaufnahme und -ausscheidung durch einen löslichen Thiamintransporter vermittelt zu werden, der von Na+ und einem transzellulären Protonengradienten abhängig ist. ⓘ
Der Thiamin-Speicher des Menschen beträgt etwa 25 bis 30 mg, wobei die größten Konzentrationen in Skelettmuskel, Herz, Gehirn, Leber und Nieren zu finden sind. ThMP und freies (unphosphoryliertes) Thiamin ist in Plasma, Milch, Liquor und vermutlich in allen extrazellulären Flüssigkeiten vorhanden. Im Gegensatz zu den hochphosphorylierten Formen von Thiamin sind ThMP und freies Thiamin in der Lage, Zellmembranen zu passieren. Es ist erwiesen, dass Kalzium und Magnesium die Verteilung von Thiamin im Körper beeinflussen, und es hat sich gezeigt, dass Magnesiummangel einen Thiaminmangel verschlimmert. Der Thiamingehalt im menschlichen Gewebe ist geringer als bei anderen Tierarten. ⓘ
Thiamin und seine Metaboliten (2-Methyl-4-amino-5-pyrimidin-carbonsäure, 4-Methyl-thiazol-5-essigsäure und andere) werden hauptsächlich mit dem Urin ausgeschieden. ⓘ
Thiamin wird im Darm über den aktiven Thiamintransporter und in hohen Konzentrationen vorliegend auch durch Diffusion aufgenommen. Es existieren seltene erbliche Mangelkrankheiten dieser Proteine. Bei der Thiamin-responsiblen, megaloblastären Anämie (TRMA) kommt es durch Mutationen im SLC19A2-Gen zur Funktionsunfähigkeit des aktiven Thiamintransporters. Hierdurch kann das in der Nahrung in niedrigen Konzentrationen vorliegende Thiamin nicht mehr ausreichend aufgenommen werden. Dies führt zum charakteristischen Krankheitsbild der TRMA mit einem Diabetes mellitus, Schwerhörigkeit und einer megaloblastären Anämie. Unbehandelt führt die TRMA zum Tode. Durch Verabreichung einer hohen Dosis von Thiamin kann ausreichend Thiamin über den Darm durch Diffusion aufgenommen werden. ⓘ
Thiamin selbst wird im Körper nicht verwendet. Mithilfe des Enzyms Thiaminpyrophosphokinase wird es zunächst zu Thiaminpyrophosphat (TPP, auch Thiamindiphosphat, TDP) umgewandelt. In dieser biologisch aktiven Form ist es Coenzym der Pyruvatdehydrogenase E1, der α-Ketoglutarat-Dehydrogenase, der α-Ketosäure-Dehydrogenase und der Transketolase. ⓘ
Glucosestoffwechsel und Mitochondrien
Mittels Pyruvatdehydrogenase-Komplex (PDC) wird in den Mitochondrien Pyruvat zu Acetyl-CoA umgebaut. TPP dient diesem Enzymkomplex als Coenzym bei der Abspaltung von CO2 und macht damit die aerobe Verwertung von Glucose (und damit auch anderer Kohlenhydrate) erst möglich. ⓘ
Ist dieser Stoffwechselweg blockiert, wird im Cytosol aus Pyruvat durch Milchsäuregärung Lactat erzeugt, was eine vergleichsweise ineffiziente Form der Energiegewinnung darstellt. ⓘ
Geschichte
Thiamin wurde als erstes der wasserlöslichen Vitamine im Jahr 1910 isoliert. Zuvor hatten Beobachtungen am Menschen und an Hühnern gezeigt, dass eine Ernährung mit hauptsächlich poliertem weißem Reis die Krankheit "Beriberi" verursachte, die jedoch nicht auf das Fehlen eines bis dahin unbekannten essenziellen Nährstoffs zurückgeführt wurde. ⓘ
1884 verwarf Takaki Kanehiro, ein Generalarzt der japanischen Marine, die bisherige Keimtheorie für Beriberi und stellte die Hypothese auf, dass die Krankheit stattdessen auf eine unzureichende Ernährung zurückzuführen sei. Als er auf einem Marineschiff die Ernährung umstellte, entdeckte er, dass die Beriberi-Krankheit auf einer neunmonatigen Seereise fast vollständig verschwunden war, wenn man eine Ernährung, die nur aus weißem Reis bestand, durch eine Ernährung mit Gerste, Fleisch, Milch, Brot und Gemüse ersetzte. Allerdings hatte Takaki der erfolgreichen Diät viele Lebensmittel hinzugefügt, und er schrieb den Nutzen fälschlicherweise der erhöhten Proteinzufuhr zu, da Vitamine zu dieser Zeit noch unbekannte Substanzen waren. Die Marine war nicht von der Notwendigkeit eines so kostspieligen Programms zur Verbesserung der Ernährung überzeugt, und viele Männer starben weiterhin an Beriberi, sogar während des russisch-japanischen Krieges von 1904/5. Erst 1905, nachdem der Anti-Beriberi-Faktor in Reiskleie (die durch Polieren zu weißem Reis verarbeitet wurde) und in Gerstenkleie entdeckt worden war, wurde Takakis Experiment mit der Ernennung zum Baron im japanischen Adelssystem belohnt, woraufhin er liebevoll "Barley Baron" genannt wurde. ⓘ
Der spezifische Zusammenhang mit Getreide wurde 1897 von Christiaan Eijkman, einem Militärarzt in Niederländisch-Indien, hergestellt, der entdeckte, dass Hühner, die mit gekochtem, poliertem Reis gefüttert wurden, Lähmungen entwickelten, die durch das Weglassen des Polierens von Reis rückgängig gemacht werden konnten. Er führte die Beriberi darauf zurück, dass der hohe Stärkegehalt im Reis giftig ist. Er glaubte, dass die Toxizität durch eine Verbindung in den polierten Reiskörnern neutralisiert wurde. Ein Mitarbeiter, Gerrit Grijns, interpretierte 1901 den Zusammenhang zwischen dem übermäßigen Verzehr von poliertem Reis und Beriberi richtig: Er kam zu dem Schluss, dass Reis in den äußeren Schichten des Korns einen essenziellen Nährstoff enthält, der durch das Polieren entfernt wird. Eijkman wurde schließlich 1929 mit dem Nobelpreis für Physiologie und Medizin ausgezeichnet, weil seine Beobachtungen zur Entdeckung der Vitamine führten. ⓘ
Im Jahr 1910 isolierte der japanische Agrarchemiker Umetaro Suzuki von der Kaiserlichen Universität Tokio erstmals eine wasserlösliche Thiaminverbindung aus Reiskleie und nannte sie Aberinsäure. (Später benannte er sie in Orizanin um.) Er beschrieb die Verbindung nicht nur als Anti-Beri-Faktor, sondern auch als essentielle Nahrung für den Menschen, doch wurde diese Entdeckung außerhalb Japans nicht bekannt, da bei der Übersetzung aus dem Japanischen ins Deutsche die Behauptung, es handele sich um eine neue Entdeckung, weggelassen wurde. Im Jahr 1911 isolierte der polnische Biochemiker Casimir Funk die antineuritische Substanz aus Reiskleie (das moderne Thiamin), die er als "Vitamin" bezeichnete (weil sie eine Aminogruppe enthält). Seine chemische Struktur hat Funk jedoch nicht vollständig charakterisiert. Die niederländischen Chemiker Barend Coenraad Petrus Jansen und sein engster Mitarbeiter Willem Frederik Donath isolierten und kristallisierten 1926 den Wirkstoff, dessen Struktur 1934 von Robert Runnels Williams bestimmt wurde. Thiamin wurde vom Williams-Team als "Thio" oder "schwefelhaltiges Vitamin" bezeichnet, wobei der Begriff "Vitamin" indirekt über Funk von der Amingruppe des Thiamins selbst herrührte (zu diesem Zeitpunkt, 1936, war bekannt, dass Vitamine nicht immer Amine waren, wie z. B. Vitamin C). Thiamin wurde 1936 von der Williams-Gruppe synthetisiert. ⓘ
Sir Rudolph Peters stellte in Oxford Tauben mit Thiaminmangel als Modell vor, um zu verstehen, wie Thiaminmangel zu den pathologisch-physiologischen Symptomen der Beriberi führen kann. In der Tat führt die Fütterung der Tauben mit poliertem Reis zu einem leicht erkennbaren Verhalten des Zurückziehens des Kopfes, einem Zustand, der Opisthotonos genannt wird. Unbehandelt starben die Tiere nach einigen Tagen. Die Verabreichung von Thiamin im Stadium des Opisthotonos führte innerhalb von 30 Minuten zu einer vollständigen Heilung. Da im Gehirn der Tauben vor und nach der Behandlung mit Thiamin keine morphologischen Veränderungen zu beobachten waren, führte Peters das Konzept einer biochemischen Läsion ein. Als Lohman und Schuster 1937 zeigten, dass das diphosphorylierte Thiaminderivat (Thiamindiphosphat, ThDP) als Cofaktor für die oxydative Decarboxylierung von Pyruvat erforderlich ist, schien der Wirkungsmechanismus von Thiamin im Zellstoffwechsel geklärt zu sein. ⓘ
- Einige Mitwirkende an der Entdeckung von Thiamin
Rudolph Peters ⓘ
Forschung
Benfotiamin, Fursultiamin, Sulbutiamin und andere, die unter Vitamin-B1-Analoga aufgeführt sind, sind synthetische Derivate von Thiamin. Die meisten wurden in den 1950er und 1960er Jahren in Japan als Formen entwickelt, die die Absorption im Vergleich zu Thiamin verbessern sollten. Einige sind in einigen Ländern als Arzneimittel oder nicht verschreibungspflichtiges Nahrungsergänzungsmittel zur Behandlung von diabetischer Neuropathie oder anderen Gesundheitszuständen zugelassen. ⓘ
Vorkommen
Pro 100 g der folgenden Lebensmittel sind laut Bundeslebensmittelschlüssel (BLS) bzw. Römpp Lexikon Chemie die angegebenen Mengen Thiamin enthalten:
| Nahrungsmittel | Thiamin mg/100 g ⓘ |
|---|---|
| Bierhefe, biologisch | 13,0 |
| Weizenkeime | 2,01 |
| Bienenpollen | 0,6 bis 2,2 |
| Sonnenblumenkerne, frisch | 1,9 |
| Back-/Bierhefe, gepresst | 1,0 |
| Sojabohnen, frisch | 0,44 |
| Sesam, geröstet | 0,4 |
| Kamut (Khorasan-Weizen) | 0,40 |
| Vollkorngetreide (Weizen, Gerste, Mais, Reis – nicht erhitzt) | 0,35–0,46 |
| Teff (äthiopisch-eritreisches Süßgras) | 0,3 |
| Erbsen, grün, frisch | 0,3 |
| Macadamianüsse, frisch | 0,28 |
| Schweinefleisch (mittelfett), frisch | 0,23 |
| Löwenzahn, frisch | 0,19 |
| Austernseitling, frisch | 0,17 |
| Bohnen, weiß, gegart | 0,154 |
| Haferflocken, roh | 0,15 |
| Geflügel, gegart | 0,11 |
| Pellkartoffeln gegart | 0,07 |
Mangelerscheinungen (Hypovitaminose)
Bereits 1896 stellte Christiaan Eijkman nach seiner Rückkehr von seiner Asienreise nach Europa fest: „Weißer Reis kann giftig sein!“ Zuvor hatte er in Java gehäuft Fälle von Beriberi beobachtet, die durch eine gründlichere Politur des weißen Reises verursacht wurde. Mangelerscheinungen treten insbesondere in Ländern auf, in denen weißer Reis das Grundnahrungsmittel darstellt und noch einseitig gegessen wird. ⓘ
Symptome:
- Störungen des Kohlenhydratstoffwechsels und Nervensystems (u. a. Polyneuropathie)
- Reizbarkeit und Depressionen
- Müdigkeit, Sehstörungen, Appetitlosigkeit, Konzentrationsschwäche, Muskelatrophie
- Blutarmut (Anämie)
- häufige Kopfschmerzen
- Gedächtnisstörungen (Korsakow-Syndrom), Verwirrungszustände
- Herzversagen, Ödeme, Tachykardie, niedriger Blutdruck, Kurzatmigkeit (Dyspnoe)
- Verringerte Produktion von Antikörpern bei Infektionen
- gestörte Energieproduktion
- schwache Muskulatur (besonders die Wadenmuskulatur)
- Krankheiten:
- Mensch: Beriberi, Wernicke-Enzephalopathie, Strachan-Syndrom
- Tiere: Thiaminmangel-Enzephalopathie der Katze, Zerebrokortikalnekrose, Chastek-Paralyse
In Europa können bestimmte Risikogruppen von einem Mangel betroffen sein, z. B. Alkoholiker, Menschen mit bestimmten Magen-Darm- oder Leberkrankheiten und Frauen mit extremer Schwangerschaftsübelkeit. ⓘ
Alzheimer
Alzheimer-Patienten zeigen eine verminderte Glucose- und Sauerstoffverwertung im Gehirn, die mit einem Thiaminmangel einhergeht. Der Mangel könnte nicht nur die Folge, sondern die Ursache der Krankheit sein. Auch können erniedrigte Thiaminpyrophosphat-Werte in Blut und Gehirn als Diagnosekriterium zur Abgrenzung von Alzheimer zu anderen Formen der Demenz verwendet werden. ⓘ
Folgen einer Überdosierung (Hypervitaminose)
Thiamin besitzt eine große therapeutische Breite. So zeigen tierexperimentelle Befunde bei Ratten, dass selbst eine 100fach über dem täglichen Bedarf liegende Dosis über drei Generationen ohne Nebenwirkungen vertragen wurde. Nach Verabreichung in den Muskel bzw. in die Vene wurden allerdings in Einzelfällen teils schwerste Überempfindlichkeitsreaktionen bis hin zu Atemnot und Schockzuständen beschrieben. Wegen dieser allergischen Reaktionen sollte Vitamin B1 daher nur in Ausnahmefällen parenteral angewendet werden; orale Therapie der Wahl zur Vitamin-B1-Substitution ist die fettlösliche und dadurch hervorragend gewebegängige Thiamin-Prodrug Benfotiamin. ⓘ
Da bei Verzehr auch in hohen Mengen keine nachteiligen gesundheitlichen Folgen beobachtet wurden (oral aufgenommenes Thiamin wird über den Urin ausgeschieden), hat das BfR auf eine Festlegung von Höchstmengen verzichtet. ⓘ