Ketamin
 | |
 | |
| Klinische Daten | |
|---|---|
| Handelsnamen | Ketalar, andere |
| Andere Bezeichnungen | CI-581; CL-369; CM-52372-2 |
| AHFS/Drugs.com | Monographie |
| Lizenz-Daten |
|
| Schwangerschaft Kategorie |
|
| Sucht Haftung | Gering bis mittelschwer |
| Wege der Verabreichung | Beliebig |
| Wirkstoffklasse | NMDA-Rezeptor-Antagonisten; allgemeine Anästhetika; dissoziative Halluzinogene; Analgetika; Antidepressiva |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | |
| Proteinbindung | 23 bis 47%. |
| Stoffwechsel | Leber, Darm (oral):
|
| Stoffwechselprodukte |
|
| Wirkungseintritt |
|
| Eliminationshalbwertszeit |
|
| Dauer der Wirkung |
|
| Ausscheidung |
|
| Bezeichnungen | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Chemische und physikalische Daten | |
| Formel | C13H16ClNO |
| Molekulare Masse | 237,73 g-mol-1 |
| 3D-Modell (JSmol) | |
| Chiralität | Racemisches Gemisch:
|
| Schmelzpunkt | 92 °C (198 °F) |
SMILES
| |
InChI
| |
| (Überprüfen) | |
Ketamin ist ein Medikament, das hauptsächlich zur Einleitung und Aufrechterhaltung von Narkosen verwendet wird. Es löst eine dissoziative Anästhesie aus, einen tranceartigen Zustand, der Schmerzlinderung, Sedierung und Amnesie bewirkt. Kennzeichnend für die Ketaminanästhesie sind erhaltene Atem- und Atemwegsreflexe, eine stimulierte Herzfunktion mit erhöhtem Blutdruck und eine moderate Bronchodilatation. In niedrigeren, nicht narkotisierenden Dosen ist Ketamin ein vielversprechendes Mittel zur Behandlung von Schmerzen und behandlungsresistenten Depressionen. Die antidepressive Wirkung einer einmaligen Verabreichung von Ketamin lässt jedoch mit der Zeit nach, und die Auswirkungen einer wiederholten Anwendung sind nicht ausreichend untersucht worden. ⓘ
Psychiatrische Nebenwirkungen sind häufig, ebenso wie ein erhöhter Blutdruck und Übelkeit. Leber- und Urintoxizität sind bei regelmäßigen Konsumenten hoher Ketamindosen zu Freizeitzwecken häufig. Ketamin ist ein NMDA-Rezeptor-Antagonist, der für die meisten seiner Wirkungen verantwortlich ist, mit Ausnahme der antidepressiven Wirkung, deren Mechanismus Gegenstand zahlreicher Untersuchungen und Diskussionen ist. ⓘ
Ketamin wurde erstmals 1962 synthetisiert und 1970 in den Vereinigten Staaten zugelassen. Es wurde regelmäßig bei Hunden und Pferden eingesetzt und im Vietnamkrieg in großem Umfang zur chirurgischen Anästhesie verwendet. Ketamin wird auch als Freizeitdroge verwendet, sowohl in Pulver- als auch in flüssiger Form, und wird wegen seiner halluzinogenen und dissoziativen Wirkung oft als "Special K" bezeichnet. Es steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation. Es ist als Generikum erhältlich. ⓘ
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Strukturformel ohne Stereochemie | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname |
| ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C13H16ClNO | ||||||||||||||||||
| Kurzbeschreibung |
weißer, kristalliner Feststoff (Ketaminhydrochlorid) | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Wirkstoffklasse |
| ||||||||||||||||||
| Wirkmechanismus |
NMDA-Rezeptor-Lumenblockade | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 237,74 g·mol−1 | ||||||||||||||||||
| Schmelzpunkt |
| ||||||||||||||||||
| pKS-Wert |
7,5 | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
77 mg·kg−1 (LD50, Maus, i.v.) | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Ketamin ist ein in Human- und Tiermedizin eingesetztes dissoziatives Anästhetikum. Seine Wirkung beruht wesentlich auf der nichtkompetitiven Hemmung von NMDA-Rezeptoren. Es bewirkt eine ausreichende Analgesie bei erhaltenem Wachzustand ohne Beeinträchtigung der Vitalfunktionen und ist aufgrund seiner therapeutischen Breite etabliert in der Katastrophenmedizin. Die psychotomimetische Wirkungkomponente veranlasst Zurückhaltung im medizinischen Einsatz, führte aber zur Verwendung als Rauschdroge. Ketamin ist in der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation aufgeführt. ⓘ
Das (S)-Enantiomer Esketamin wurde in jüngerer Zeit in den USA und der Europäischen Union zur Notfallbehandlung behandlungsresistenter Depression zugelassen. ⓘ
Medizinische Anwendungen
Anästhesie
Die Verwendung von Ketamin in der Anästhesie spiegelt seine Eigenschaften wider. Es ist ein Mittel der Wahl für kurzfristige Eingriffe, wenn keine Muskelentspannung erforderlich ist. Die Wirkung von Ketamin auf das Atmungs- und Kreislaufsystem unterscheidet sich von der anderer Anästhetika. Es unterdrückt die Atmung viel weniger als die meisten anderen verfügbaren Anästhetika. Bei der Verwendung von Narkosedosen stimuliert Ketamin in der Regel das Kreislaufsystem, anstatt es zu unterdrücken. Die Schutzreflexe der Atemwege bleiben erhalten, so dass es manchmal möglich ist, eine Ketaminanästhesie ohne Schutzmaßnahmen für die Atemwege durchzuführen. Psychotomimetische Wirkungen schränken die Akzeptanz von Ketamin ein; Lamotrigin und Nimodipin verringern jedoch die psychotomimetischen Wirkungen und können auch durch verabreichte Benzodiazepine oder Propofol ausgeglichen werden. ⓘ
Ketamin wird häufig bei Schwerverletzten eingesetzt und scheint in dieser Gruppe sicher zu sein. Es wurde in großem Umfang bei Notoperationen unter Feldbedingungen in Kriegsgebieten eingesetzt, beispielsweise während des Vietnamkriegs. Eine Leitlinie für die klinische Praxis aus dem Jahr 2011 befürwortet die Verwendung von Ketamin als Sedativum in der Notfallmedizin, auch bei körperlich schmerzhaften Eingriffen. Es ist das Mittel der Wahl für Menschen mit traumatischem Schock, bei denen das Risiko einer Hypotonie besteht. Niedriger Blutdruck ist bei Menschen mit schweren Kopfverletzungen schädlich, und Ketamin verursacht am wenigsten wahrscheinlich einen niedrigen Blutdruck und kann ihn oft sogar verhindern. ⓘ
Ketamin ist eine Option für Kinder, entweder als alleiniges Anästhetikum bei kleineren Eingriffen oder als Induktionsmittel, gefolgt von einem neuromuskulären Blocker und einer Trachealintubation. Insbesondere Kinder mit zyanotischen Herzerkrankungen und neuromuskulären Störungen sind gute Kandidaten für eine Ketaminanästhesie. ⓘ
Aufgrund der bronchienerweiternden Eigenschaften von Ketamin kann es zur Anästhesie bei Menschen mit Asthma, chronisch obstruktiver Atemwegserkrankung und schwerer reaktiver Atemwegserkrankung einschließlich aktivem Bronchospasmus eingesetzt werden. ⓘ
Schmerzen
Ketamininfusionen werden zur akuten Schmerzbehandlung in Notaufnahmen und in der perioperativen Phase bei Personen mit therapieresistenten Schmerzen eingesetzt. Die Dosen sind niedriger als die für die Anästhesie verwendeten; sie werden gewöhnlich als subanästhetische Dosen bezeichnet. Als Zusatz zu Morphin oder allein reduziert Ketamin den Morphinverbrauch, den Schmerzpegel, die Übelkeit und das Erbrechen nach einer Operation. Ketamin ist wahrscheinlich am vorteilhaftesten für chirurgische Patienten, bei denen starke postoperative Schmerzen zu erwarten sind, sowie für Patienten mit Opioid-Toleranz. ⓘ
Aufgrund seiner Wirksamkeit und des geringen Risikos einer Atemdepression ist Ketamin besonders in der prähospitalen Umgebung nützlich. In der Notaufnahme eines Krankenhauses ist Ketamin bei der Behandlung von akuten Schmerzen und bei der Kontrolle von Verfahrensschmerzen ähnlich wirksam wie Opioide. Es kann auch die opioidinduzierte Hyperalgesie und das postanästhetische Zittern verhindern. ⓘ
Bei chronischen Schmerzen wird Ketamin als intravenöses Analgetikum eingesetzt, insbesondere wenn es sich um neuropathische Schmerzen handelt. Es hat den zusätzlichen Vorteil, dass es der spinalen Sensibilisierung oder dem Wind-up-Phänomen, das bei chronischen Schmerzen auftritt, entgegenwirkt. In mehreren klinischen Studien haben Ketamininfusionen zu einer kurzfristigen Schmerzlinderung bei neuropathischen Schmerzdiagnosen, Schmerzen nach traumatischen Wirbelsäulenverletzungen, Fibromyalgie und komplexem regionalen Schmerzsyndrom (CRPS) geführt. Die Konsensus-Leitlinien für chronische Schmerzen aus dem Jahr 2018 kommen jedoch zu dem Schluss, dass es insgesamt nur schwache Belege für den Einsatz von Ketamin bei Schmerzen nach Wirbelsäulenverletzungen, mäßige Belege für Ketamin bei CRPS und schwache oder keine Belege für Ketamin bei gemischten neuropathischen Schmerzen, Fibromyalgie und Krebsschmerzen gibt. Insbesondere gibt es nur für CRPS Hinweise auf eine mittel- bis längerfristige Schmerzlinderung. ⓘ
Depressionen
Ketamin ist ein robustes und schnell wirkendes Antidepressivum, dessen Wirkung jedoch nur vorübergehend ist. Eine intravenöse Ketamininfusion kann bei behandlungsresistenten Depressionen innerhalb von 4 Stunden zu einer Verbesserung der Stimmung führen, die nach 24 Stunden ihren Höhepunkt erreicht. Eine Einzeldosis intravenös verabreichtes Ketamin führt nachweislich bereits 4,5 Stunden nach der Verabreichung zu einer Ansprechrate von mehr als 60 % (mit einer anhaltenden Wirkung nach 24 Stunden) und nach 7 Tagen zu mehr als 40 %. Obwohl es nur wenige Pilotstudien zur Untersuchung der optimalen Dosis gibt, deuten immer mehr Hinweise darauf hin, dass eine Dosis von 0,5 mg/kg, die über 40 Minuten injiziert wird, ein optimales Ergebnis erzielt. Die antidepressive Wirkung von Ketamin lässt nach 7 Tagen nach, und die meisten Patienten erleiden innerhalb von 10 Tagen einen Rückfall, obwohl bei einer erheblichen Minderheit die Besserung 30 Tage und länger anhalten kann. Eine der größten Herausforderungen bei der Ketaminbehandlung kann die Dauer der antidepressiven Wirkung nach Abschluss der Behandlung sein. Eine mögliche Option ist die Erhaltungstherapie mit Ketamin, die in der Regel zweimal pro Woche bis einmal in zwei Wochen durchgeführt wird. Ketamin kann Selbstmordgedanken bis zu drei Tage nach der Injektion verringern. ⓘ
Ketamin ist nicht als Antidepressivum zugelassen, aber das Canadian Network for Mood and Anxiety Treatments (CANMAT) empfiehlt Ketamin als Mittel der dritten Wahl bei Depressionen. Eines der Enantiomere von Ketamin, Esketamin, ist in den Vereinigten Staaten und anderswo als Nasenspray zur Behandlung von behandlungsresistenten Depressionen zugelassen (siehe Esketamin § Depression). ⓘ
Eine Cochrane-Review randomisierter kontrollierter Studien bei Erwachsenen mit unipolaren schweren depressiven Störungen ergab, dass im Vergleich zu Placebo bei den mit Ketamin oder Esketamin behandelten Personen eine Verringerung oder Remission der Symptome über einen Zeitraum von 1 bis 7 Tagen auftrat. 18,7 % (4,1 bis 40,4 %) mehr Personen berichteten über einen gewissen Nutzen und 9,6 % (0,2 bis 39,4 %) mehr erreichten innerhalb von 24 Stunden nach der Ketaminbehandlung eine Remission. Von den Personen, die Esketamin erhielten, hatten 2,1 % (2,5 bis 24,4 %) nach 24 Stunden eine gewisse Linderung und 10,3 % (4,5 bis 18,2 %) wenige oder keine Symptome. Diese Wirkungen hielten nicht länger als eine Woche an, obwohl die höhere Abbrecherquote in einigen Studien bedeutet, dass die Dauer des Nutzens unklar bleibt. ⓘ
Ketamin kann die depressiven Symptome bei Menschen mit bipolarer Depression 24 Stunden nach der Behandlung teilweise verbessern, jedoch nicht 3 oder mehr Tage. Möglicherweise erfahren 10 weitere Personen mit bipolaren Depressionen pro 1000 Personen einen Tag nach der Behandlung eine kurzzeitige Besserung, aber keine Beendigung der Symptome. Diese Schätzungen beruhen auf sehr begrenzten Forschungsergebnissen. ⓘ
Nahtoderfahrung
Die meisten Personen, die sich während der Ketaminanästhesie an ihre Träume erinnern konnten, berichten von Nahtoderfahrungen (NTE), wenn man die weitestmögliche Definition einer NTE zugrunde legt. Ketamin kann Merkmale reproduzieren, die gemeinhin mit NTEs in Verbindung gebracht werden. In einer groß angelegten Studie aus dem Jahr 2019 wurde festgestellt, dass schriftliche Berichte über Ketamin-Erfahrungen im Vergleich zu anderen schriftlichen Berichten über Drogenerfahrungen einen hohen Grad an Ähnlichkeit mit schriftlichen Berichten über NTE aufweisen. ⓘ
Krampfanfälle
Ketamin wird gelegentlich zur Behandlung eines Status epilepticus eingesetzt, der auf die Standardbehandlungen nicht ausreichend anspricht, obwohl es nur begrenzte Belege (Fallstudien und keine randomisierten kontrollierten Studien) für seine Wirksamkeit gibt. ⓘ
Kontraindikationen
Die wichtigsten Kontraindikationen für Ketamin:
- Schwere Herz-Kreislauf-Erkrankungen wie instabile Angina pectoris oder schlecht eingestellter Bluthochdruck
- Erhöhter intrakranieller oder intraokularer Druck. Diese beiden Kontraindikationen sind umstritten
- Unzureichend kontrollierte Psychosen
- Schwere Lebererkrankung wie Zirrhose
- Schwangerschaft
- Aktive Substanzkonsumstörung (bei seriellen Ketamininjektionen)
- Alter von weniger als 3 Monaten ⓘ
Nebenwirkungen
Bei Narkosedosen treten bei 10-20 % der Erwachsenen (1-2 % der Kinder) unerwünschte psychiatrische Reaktionen auf, die während des Auftauchens aus der Narkose auftreten und von Träumen und Dysphorie bis zu Halluzinationen und Auftauch-Delirium reichen. Die psychotomimetischen Wirkungen nehmen durch die Zugabe von Lamotrigin und Nimodipin ab und können durch eine Vorbehandlung mit einem Benzodiazepin oder Propofol ausgeglichen werden. Die Ketaminanästhesie verursacht häufig tonisch-klonische Bewegungen (bei mehr als 10 % der Patienten) und selten Hypertonie. Erbrechen ist bei 5-15 % der Patienten zu erwarten; eine Vorbehandlung mit Propofol mildert es ebenfalls. Ein Laryngospasmus tritt bei Ketamin nur selten auf. Ketamin stimuliert im Allgemeinen die Atmung; in den ersten 2-3 Minuten einer hochdosierten schnellen intravenösen Injektion kann es jedoch eine vorübergehende Atemdepression verursachen. ⓘ
Bei niedrigeren subanästhetischen Dosen sind die psychiatrischen Nebenwirkungen besonders ausgeprägt. Die meisten Menschen fühlen sich seltsam, raumgreifend, benebelt oder haben das Gefühl zu schweben, oder sie haben visuelle Verzerrungen oder Taubheit. Ebenfalls sehr häufig (20-50 %) sind Sprachstörungen, Verwirrung, Euphorie, Schläfrigkeit und Konzentrationsschwierigkeiten. Psychosesymptome wie das Versinken in einem Loch, das Verschwinden, das Gefühl zu schmelzen, das Erleben von Farben und Halluzinationen werden von 6-10 % der Betroffenen beschrieben. Schwindel, verschwommenes Sehen, Mundtrockenheit, Bluthochdruck, Übelkeit, erhöhte oder erniedrigte Körpertemperatur oder Erröten sind die häufigsten (>10 %) nichtpsychiatrischen Nebenwirkungen. Alle diese unerwünschten Wirkungen sind am Ende der Injektion am stärksten ausgeprägt, nehmen 40 Minuten danach drastisch ab und verschwinden innerhalb von 4 Stunden nach der Injektion vollständig. ⓘ
Urin- und Lebertoxizität
Harnwegsintoxizität tritt vor allem bei Personen auf, die routinemäßig große Mengen Ketamin verwenden, wobei 20-30 % der häufigen Anwender Blasenbeschwerden haben. Sie umfasst eine Reihe von Erkrankungen, die von Blasenentzündungen über Hydronephrosen bis hin zum Nierenversagen reichen. Die typischen Symptome einer ketamininduzierten Blasenentzündung sind häufiges Wasserlassen, Dysurie und Harndrang, manchmal begleitet von Schmerzen beim Wasserlassen und Blut im Urin. Die Schädigung der Blasenwand weist Ähnlichkeiten mit der interstitiellen und eosinophilen Zystitis auf. Die Wand ist verdickt, und die funktionelle Blasenkapazität liegt bei nur 10-150 mL. ⓘ
Die Behandlung der ketamininduzierten Zystitis umfasst als ersten Schritt das Absetzen des Ketamins. Anschließend werden NSAIDs und Anticholinergika und bei unzureichender Reaktion Tramadol eingesetzt. Die zweite Behandlungslinie sind epithelschützende Mittel wie orales Pentosanpolysulfat oder die intravesikale (in die Blase) Instillation von Hyaluronsäure. Intravesikales Botulinumtoxin ist ebenfalls nützlich. ⓘ
Die Lebertoxizität von Ketamin tritt bei höheren Dosen und wiederholter Verabreichung auf. In einer Gruppe von chronisch hochdosierten Ketaminkonsumenten wurde die Häufigkeit von Leberschäden mit etwa 10 % angegeben. Es gibt Fallberichte über erhöhte Leberenzymwerte im Zusammenhang mit der Ketaminbehandlung von chronischen Schmerzen. ⓘ
Abhängigkeit und Toleranz
Obwohl die Häufigkeit der Ketaminabhängigkeit nicht bekannt ist, entwickeln einige Personen, die regelmäßig Ketamin verwenden, eine Ketaminabhängigkeit. Auch Tierversuche bestätigen das Risiko eines Missbrauchs. Darüber hinaus kann der schnelle Wirkungseintritt nach der Insufflation den potenziellen Konsum als Freizeitdroge erhöhen. Die kurze Wirkungsdauer begünstigt Rauschzustände. Selbst bei wiederholter medizinischer Anwendung entwickelt sich rasch eine Ketamintoleranz, die den Gebrauch höherer Dosen erforderlich macht. Einige täglich konsumierende Personen berichteten über Entzugserscheinungen, vor allem Angstzustände, Zittern, Schweißausbrüche und Herzklopfen, nachdem sie versucht hatten, den Konsum zu beenden. Bei häufigen Freizeitkonsumenten von Ketamin wurden kognitive Defizite sowie verstärkte Dissoziations- und Wahnsymptome beobachtet. ⓘ
Wechselwirkungen
Ketamin potenziert die sedierende Wirkung von Propofol und Midazolam. Naltrexon verstärkt die psychotomimetischen Wirkungen einer niedrigen Ketamin-Dosis, während Lamotrigin und Nimodipin diese verringern. Clonidin verringert den Anstieg von Speichelfluss, Herzfrequenz und Blutdruck während der Ketaminanästhesie und reduziert das Auftreten von Albträumen. ⓘ
Klinische Beobachtungen deuten darauf hin, dass Benzodiazepine die antidepressive Wirkung von Ketamin vermindern können. Ketamin wird häufig zur Behandlung resistenter Depressionen als Zusatz zu einer Reihe von Antidepressiva eingesetzt. Daher scheinen die meisten herkömmlichen Antidepressiva sicher mit Ketamin kombiniert werden zu können. ⓘ
Pharmakologie
Pharmakodynamik
Mechanismus der Wirkung
Der Antagonismus des NMDA-Rezeptors ist für die anästhesierenden, analgetischen und psychotomimetischen Wirkungen von Ketamin verantwortlich. Der NMDA-Rezeptor-Antagonismus führt zur Analgesie, indem er die zentrale Sensibilisierung der Rückenmarksneuronen verhindert, d. h. die Wirkung von Ketamin greift in die Schmerzübertragung im Rückenmark ein. ⓘ
Der Mechanismus der antidepressiven Wirkung von Ketamin ist unklar. Es ist nicht klar, ob der NMDA-Rezeptor allein für diese Wirkung verantwortlich ist oder ob auch Interaktionen mit anderen Rezeptoren erforderlich sind. Es ist nicht klar, ob Ketamin allein für die antidepressive Wirkung ausreicht oder ob auch seine Metaboliten eine Rolle spielen. In jedem Fall wurde aufgeklärt, dass eine akute Blockade von NMDA-Rezeptoren im Gehirn zu einer Aktivierung von α-Amino-3-hydroxy-5-methyl-4-isoxazolpropionsäure-Rezeptoren (AMPA-Rezeptoren) führt, die wiederum eine Vielzahl nachgeschalteter Signalwege modulieren, um die Neurotransmission im limbischen System zu beeinflussen und die antidepressive Wirkung von NMDA-Rezeptor-Antagonisten wie Ketamin zu vermitteln. Zu diesen nachgeschalteten Wirkungen dieser Aktivierung der AMPA-Rezeptoren gehören die Hochregulierung des neurotrophen Faktors (BDNF) und die Aktivierung seines Signalrezeptors Tropomyosin-Rezeptor-Kinase B (TrkB), die Aktivierung des mTOR-Signalwegs (mammalian target of rapamycin), die Deaktivierung der Glykogensynthase-Kinase 3 (GSK-3) und die Hemmung der Phosphorylierung der eukaryotischen Elongationsfaktor 2 (eEF2)-Kinase. Neben der Blockade des NMDA-Rezeptors ist möglicherweise auch der aktive Metabolit von Ketamin, Hydroxynorketamin, an der schnell einsetzenden antidepressiven Wirkung von Ketamin beteiligt, der zwar nicht wesentlich mit dem NMDA-Rezeptor interagiert, aber indirekt die AMPA-Rezeptoren in ähnlicher Weise aktiviert. Jüngste Forschungen haben ergeben, dass eine akute Hemmung der lateralen Habenula, eines Teils des Gehirns im limbischen System, der als "Anti-Belohnungszentrum" bezeichnet wird (der auf den mesolimbischen Belohnungsweg projiziert und diesen hemmt und andere limbische Bereiche moduliert), an den antidepressiven Wirkungen von Ketamin beteiligt sein könnte. ⓘ
Ketamin ist ein Gemisch aus gleichen Mengen zweier Enantiomere: Esketamin und Arketamin. Esketamin ist ein stärkerer NMDA-Rezeptor-Antagonist und ein stärkeres dissoziatives Halluzinogen als Arketamin. Aufgrund der Hypothese, dass der NMDA-Rezeptor-Antagonismus der antidepressiven Wirkung von Ketamin zugrunde liegt, wurde Esketamin als Antidepressivum entwickelt. Mehrere andere NMDA-Rezeptor-Antagonisten, darunter Memantin, Lanicemin, Rislenemdaz, Rapastinel und 4-Chlorkynurenin, haben jedoch bisher keine ausreichende Wirksamkeit bei Depressionen gezeigt. Darüber hinaus deuten Tierversuche darauf hin, dass Arketamin, das Enantiomer mit einem schwächeren NMDA-Rezeptor-Antagonismus, sowie (2R,6R)-Hydroxynorketamin, der Metabolit mit vernachlässigbarer Affinität für den NMDA-Rezeptor, aber ein potenter Alpha-7-Nikotinrezeptor-Antagonist, antidepressiv wirken können. Es wird nun argumentiert, dass der NMDA-Rezeptor-Antagonismus möglicherweise nicht für die antidepressive Wirkung von Ketamin verantwortlich ist. ⓘ
Molekulare Ziele
| Standort | Wert (μM) | Typ | Wirkung | Spezies | Ref |
|---|---|---|---|---|---|
| NMDA | 0.25–0.66 | Ki | Antagonist | Mensch | |
| MOR | 42 | Ki | Antagonist | Mensch | |
| MOR2 | 12.1 | Ki | Antagonist | Mensch | |
| KOR | 28 25 |
Ki Ki |
Antagonist Agonist |
Mensch | |
| σ2 | 26 | Ki | ND | Ratte | |
| D2 | 0.5 >10 |
Ki Ki |
Agonist ND |
Mensch | |
| M1 | 45 | Ki | ND | Mensch | |
| α2β2 | 92 | IC50 | Antagonist | Mensch | |
| α2β4 | 29 | IC50 | Antagonist | Mensch | |
| α3β2 | 50 | IC50 | Antagonist | Mensch | |
| α3β4 | 9.5 | IC50 | Antagonist | Mensch | |
| α4β2 | 72 | IC50 | Antagonist | Mensch | |
| α4β4 | 18 | IC50 | Antagonist | Mensch | |
| α7 | 3.1 | IC50 | Antagonist | Ratte | |
| ERα | 0.34 | Ki | ND | Mensch | |
| NET | 82–291 | IC50 | Hemmstoff | Mensch | |
| DAT | 63 | Ki | Hemmstoff | Ratte | |
| HCN1 | 8–16 | EC50 | Hemmstoff | Maus | |
| TRPV1 | 1-100 | Ki | Agonist | Ratte | |
| Je kleiner der Wert ist, desto stärker ist die Interaktion mit der Stelle. | |||||
Ketamin wirkt in erster Linie als Antagonist des NMDA-Rezeptors, eines ionotropen Glutamatrezeptors. Die S(+)- und R(-)-Stereoisomere von Ketamin binden mit unterschiedlicher Affinität an die Dizocilpin-Stelle des NMDA-Rezeptors, wobei das erstere eine etwa 3- bis 4-fach höhere Affinität für den Rezeptor aufweist als das letztere. Infolgedessen ist das S-Isomer ein stärkeres Anästhetikum und Analgetikum als sein R-Gegenstück. ⓘ
Ketamin kann mit dem NMDAR über eine andere allosterische Stelle am Rezeptor interagieren und ihn hemmen. ⓘ
Von einigen Ausnahmen abgesehen sind die Wirkungen von Ketamin an anderen Rezeptoren weitaus schwächer als der Antagonismus von Ketamin am NMDA-Rezeptor (siehe die Aktivitätstabelle rechts). ⓘ
Obwohl Ketamin ein sehr schwacher Ligand der Monoamintransporter ist (Ki > 60 μM), wurde vermutet, dass es mit allosterischen Stellen auf den Monoamintransportern interagieren könnte, um eine Hemmung der Wiederaufnahme von Monoaminen zu bewirken. Allerdings wurde mit Ketamin oder seinen Metaboliten bei Konzentrationen von bis zu 10.000 nM keine funktionelle Hemmung (IC50) der menschlichen Monoamintransporter beobachtet. Darüber hinaus wurde in Tierstudien und in mindestens drei Berichten über Fälle beim Menschen keine Wechselwirkung zwischen Ketamin und dem Monoaminoxidase-Hemmer (MAOI) Tranylcypromin festgestellt, was insofern von Bedeutung ist, als die Kombination eines Monoamin-Wiederaufnahmehemmers mit einem MAOI schwere Toxizität wie das Serotonin-Syndrom oder eine hypertensive Krise hervorrufen kann. Insgesamt lassen diese Ergebnisse Zweifel an der Beteiligung der Monoamin-Wiederaufnahmehemmung an den Wirkungen von Ketamin beim Menschen aufkommen. Es wurde festgestellt, dass Ketamin die dopaminerge Neurotransmission im Gehirn steigert, was jedoch nicht auf die Hemmung der Wiederaufnahme von Dopamin zurückzuführen ist, sondern möglicherweise über indirekte/nachgeschaltete Mechanismen erfolgt, nämlich durch Antagonismus des NMDA-Rezeptors. ⓘ
Ob Ketamin ein Agonist von D2-Rezeptoren ist, ist umstritten. Frühe Forschungsarbeiten der Gruppe von Philip Seeman ergaben, dass Ketamin ein partieller D2-Agonist ist, dessen Potenz der seines NMDA-Rezeptorantagonismus ähnelt. Spätere Studien verschiedener Forscher ergaben jedoch eine Affinität von Ketamin von >10 μM für die regulären D2-Rezeptoren von Mensch und Ratte. Während D2-Rezeptor-Agonisten wie Bromocriptin in der Lage sind, die Prolaktinsekretion schnell und stark zu unterdrücken, wurde festgestellt, dass subanästhetische Dosen von Ketamin dies beim Menschen nicht bewirken, sondern den Prolaktinspiegel sogar dosisabhängig erhöhen. Bildgebende Studien haben gemischte Ergebnisse zur Hemmung der striatalen [11C]-Rakloprid-Bindung durch Ketamin beim Menschen ergeben, wobei in einigen Studien eine signifikante Abnahme und in anderen keine solche Wirkung festgestellt wurde. Änderungen der [11C]-Racloprid-Bindung könnten jedoch eher auf durch Ketamin induzierte Änderungen der Dopaminkonzentration als auf die Bindung von Ketamin an den D2-Rezeptor zurückzuführen sein. ⓘ
Zusammenhänge zwischen Spiegeln und Wirkungen
Dissoziation und psychotomimetische Wirkungen werden bei Personen berichtet, die mit Ketamin bei Plasmakonzentrationen von etwa 100 bis 250 ng/ml (0,42-1,1 μM) behandelt werden. Die typische intravenöse antidepressive Dosierung von Ketamin zur Behandlung von Depressionen ist niedrig und führt zu maximalen Plasmakonzentrationen von 70 bis 200 ng/ml (0,29-0,84 μM). Bei ähnlichen Plasmakonzentrationen (70 bis 160 ng/mL; 0,29-0,67 μM) zeigt es auch analgetische Wirkungen. Innerhalb von 1-5 Minuten nach Einleitung der Anästhesie durch eine schnelle intravenöse Injektion von Ketamin erreicht seine Plasmakonzentration 60-110 μM. Wurde die Narkose mit Lachgas zusammen mit einer kontinuierlichen Ketamininjektion aufrechterhalten, stabilisierte sich die Ketaminkonzentration bei etwa 9,3 μM. In einem Experiment mit reiner Ketamin-Narkose begannen die Personen zu erwachen, sobald der Ketamin-Plasmaspiegel auf etwa 2.600 ng/mL (11 μM) sank, und sie orientierten sich in Ort und Zeit, wenn der Spiegel auf 1.000 ng/mL (4 μM) sank. In einer Einzelfallstudie schwankte die Ketaminkonzentration in der Zerebrospinalflüssigkeit, die stellvertretend für die Gehirnkonzentration steht, während der Anästhesie zwischen 2,8 und 6,5 μM und war etwa 40 % niedriger als im Plasma. ⓘ
Pharmakokinetik
Ketamin kann aufgrund seiner Wasser- und Lipidlöslichkeit auf vielen verschiedenen Wegen aufgenommen werden. Die intravenöse Bioverfügbarkeit von Ketamin beträgt definitionsgemäß 100 %, die intramuskuläre Bioverfügbarkeit ist mit 93 % etwas geringer, und die epidurale Bioverfügbarkeit beträgt 77 %. Die subkutane Bioverfügbarkeit wurde noch nie gemessen, wird jedoch als hoch eingeschätzt. Von den weniger invasiven Verabreichungswegen hat die intranasale Verabreichung die höchste Bioverfügbarkeit (45-50 %) und die orale die niedrigste (16-20 %). Die sublinguale und rektale Bioverfügbarkeit liegt mit etwa 25-50 % dazwischen. ⓘ
Nach der Resorption verteilt sich Ketamin rasch im Gehirn und in anderen Geweben. Die Plasmaproteinbindung von Ketamin ist unterschiedlich und liegt zwischen 23 und 47 %. ⓘ
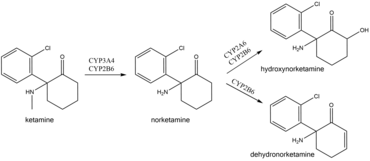
Im Körper unterliegt Ketamin einem umfangreichen Metabolismus. Es wird durch die Isoenzyme CYP3A4 und CYP2B6 in Norketamin biotransformiert, das wiederum durch CYP2A6 und CYP2B6 in Hydroxynorketamin und Dehydronorketamin umgewandelt wird. Die geringe orale Bioverfügbarkeit von Ketamin ist auf den First-Pass-Effekt und möglicherweise auf den intestinalen Metabolismus von Ketamin durch CYP3A4 zurückzuführen. Infolgedessen sind die Plasmaspiegel von Norketamin nach oraler Verabreichung um ein Vielfaches höher als die von Ketamin, und Norketamin spielt möglicherweise eine Rolle bei der anästhetischen und analgetischen Wirkung von oralem Ketamin. Dies erklärt auch, warum die oralen Ketaminspiegel unabhängig von der CYP2B6-Aktivität sind, im Gegensatz zu den subkutanen Ketaminspiegeln. ⓘ
Nach einer intravenösen Injektion von mit Tritium markiertem Ketamin werden 91 % der Radioaktivität aus dem Urin und 3 % aus den Fäkalien wiedergewonnen. Das Medikament wird größtenteils in Form von Metaboliten ausgeschieden, wobei nur 2 % unverändert bleiben. Konjugierte hydroxylierte Derivate von Ketamin (80 %), gefolgt von Dehydronorketamin (16 %), sind die am häufigsten im Urin nachgewiesenen Metaboliten. ⓘ
- Nach etwa 30 Sekunden beginnt Ketamin (wie auch S-Ketamin) bei intravenöser Gabe analgetisch zu wirken. Diese Wirkung hält etwa 5 bis 15 Minuten, bei S-Ketamin 30 bis 40 Minuten, an.
- Plasmahalbwertszeit: bei klinischer Gabe beträgt die terminale Eliminationshalbwertszeit für (S)-Ketaminhydrochlorid zwischen 79 Minuten (nach kontinuierlicher Infusion) und 186 Minuten (nach niedrigdosierter i.v.-Gabe), bei anderen Applikationsformen zwei bis dreieinhalb Stunden.
- Therapeutische Dosis: Abhängig von Zielsetzung (Analgesie, Narkose), Co-Medikation und Kreislaufsituation sowie nach Wirkung im Einzelfall anzupassen.
- Bioverfügbarkeit: oral 17 %, sublingual 33 %, intranasal 25 bis 50 %, intramuskulär 93 %. ⓘ
Chemie
Synthese
2-Chlorbenzonitril wird mit dem Grignard-Reagenz Cyclopentylmagnesiumbromid zu (2-Chlorphenyl)(cyclopentyl)methanon umgesetzt. Dieses wird anschließend mit Brom zum entsprechenden Bromketon bromiert, das dann mit Methylamin in wässriger Lösung unter Hydrolyse des tertiären Bromatoms zum Methyliminoderivat 1-(2-Chlor-N-methylbenzimidoyl)cyclopentanol umgesetzt wird. Dieses Endprodukt wird dann in Decalin oder einem anderen geeigneten hochsiedenden Lösungsmittel erhitzt, woraufhin eine Ringexpansions-Umlagerung stattfindet, bei der Ketamin entsteht. ⓘ

Struktur
Von der chemischen Struktur her ist Ketamin ein Arylcyclohexylaminderivat. Ketamin ist eine chirale Verbindung. Das aktivere Enantiomer, Esketamin (S-Ketamin), ist auch für den medizinischen Gebrauch unter dem Markennamen Ketanest S erhältlich, während das weniger aktive Enantiomer, Arketamin (R-Ketamin), nie als enantioreines Medikament für den klinischen Gebrauch vermarktet wurde. Während S-Ketamin durch den NMDA-Rezeptor-Antagonismus als Analgetikum und Anästhetikum wirksamer ist, hat R-Ketamin eine länger anhaltende Wirkung als Antidepressivum. ⓘ
Die optische Drehung eines bestimmten Enantiomers von Ketamin kann zwischen seinen Salzen und seiner freien Basenform variieren. Die freie Basenform von (S)-Ketamin weist eine Rechtsdrehung auf und wird daher als (S)-(+)-Ketamin bezeichnet. Sein Hydrochloridsalz hingegen weist eine Levorotation auf und wird daher als (S)-(-)-Ketaminhydrochlorid gekennzeichnet. ⓘ
Nachweis
Ketamin kann in Blut oder Plasma quantifiziert werden, um eine Vergiftungsdiagnose bei hospitalisierten Personen zu bestätigen, Beweise bei einer Festnahme wegen Fahrens unter Alkoholeinfluss zu liefern oder bei einer gerichtsmedizinischen Untersuchung eines Todesfalls zu helfen. Die Ketaminkonzentrationen im Blut oder Plasma liegen in der Regel im Bereich von 0,5-5,0 mg/L bei Personen, die die Droge therapeutisch (während einer Vollnarkose) erhalten, 1-2 mg/L bei Personen, die wegen Trunkenheit am Steuer festgenommen wurden, und 3-20 mg/L bei Opfern einer akuten tödlichen Überdosierung. Urin ist häufig die bevorzugte Probe für die routinemäßige Überwachung des Drogenkonsums. Das Vorhandensein von Norketamin, einem pharmakologisch aktiven Metaboliten, ist für die Bestätigung der Einnahme von Ketamin nützlich. ⓘ
Struktur und Stereochemie
Ketamin ist ein chirales Cyclohexanonderivat und Phenylcyclohexylamin mit einem Stereozentrum. ⓘ
| Enantiomere ⓘ | ||
| Name | (R)-Ketamin | (S)-Ketamin |
| Andere Namen | Erketamin | Esketamin |
| Strukturformel | 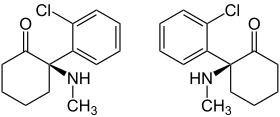
| |
| CAS-Nummer | 33643-49-1 | 33643-46-8 |
| EG-Nummer | – | 811-504-2 |
| ECHA-Infocard | – | 100.242.065 |
| PubChem | – | 182137 |
| Wikidata | Q20707684 | Q2365493 |
Pharmazeutisch werden die Hydrochloride des rac-Ketamins und des Esketamins verwendet. ⓘ
Tracer und nächste Strukturverwandte
Ketamin ist in vielfältiger Weise, insbesondere in seinem aliphatischen Anteil, deuteriert worden, um einerseits Metaboliten massenspektroskopisch ausfindig zu machen und um andererseits Molekülpositionen durch Anwendung des kinetischen Isotopeneffekts gegenüber dem Stoffwechsel zu stabilisieren und das Wirkprofil dieser Verbindungen zu studieren. Diente einst die am Methyl mit 11C markierte Verbindung als provisorischer PET-Tracer, so ist seit dem Jahr 2018 ein Tracer bekannt, der an stoffwechselstabiler Position mit dem Nuklid 14C radioaktiv markiert ist. Das in der Synthese verwendete 14C-Benzonitril ist per Sandmeyer-Reaktion in hoher Ausbeute zugänglich. N-Ethylnorketamin, Deschlorketamin und die 2-Fluor-Entsprechung sind in den 2010er Jahren als NPS identifiziert worden. ⓘ
Geschichte
Ketamin wurde erstmals 1962 von Calvin L. Stevens synthetisiert, einem Chemieprofessor an der Wayne State University und Berater von Parke-Davis. Es war unter dem Entwicklungscode CI-581 bekannt. Nach vielversprechenden präklinischen Untersuchungen an Tieren wurde Ketamin 1964 an menschlichen Gefangenen getestet. Diese Untersuchungen zeigten, dass Ketamin aufgrund seiner kurzen Wirkungsdauer und seiner geringeren Verhaltenstoxizität gegenüber Phencyclidin (PCP) als Narkosemittel die bessere Wahl war. Die Forscher wollten den Zustand der Ketamin-Narkose als "Träumen" bezeichnen, was Parke-Davis jedoch nicht gefiel. Als Mrs. Edward F. Domino, die Ehefrau eines der Pharmakologen, die an Ketamin arbeiteten, von diesem Problem und dem "unzusammenhängenden" Erscheinungsbild der behandelten Personen erfuhr, schlug sie die "dissoziative Anästhesie" vor. Nach der FDA-Zulassung im Jahr 1970 wurde Ketamin erstmals während des Vietnamkriegs an amerikanische Soldaten verabreicht. ⓘ
Die Entdeckung der antidepressiven Wirkung von Ketamin im Jahr 2000 wurde als der wichtigste Fortschritt in der Behandlung von Depressionen seit mehr als 50 Jahren bezeichnet. Sie hat das Interesse an NMDA-Rezeptor-Antagonisten zur Behandlung von Depressionen geweckt und einen Richtungswechsel in der Forschung und Entwicklung von Antidepressiva bewirkt. ⓘ
Im Jahr 1966 erhielt Parke-Davis ein Patent für die Herstellung von Ketamin als Arzneimittel sowohl für die Humanmedizin als auch für die Tiermedizin. Edward Felix Domino, Professor für klinische Pharmakologie an der Universität in Michigan (USA), führte am 3. August 1964 seinen ersten (nichtmedizinischen) Selbstversuch mit Ketamin durch und erkannte dabei das psychedelische Potential der Substanz. Die Bezeichnung dissoziatives Anästhetikum für Ketamin wurde von ihm dann im folgenden Jahr 1965 eingeführt. ⓘ
Im Vietnamkrieg wurde Ketamin an amerikanischen Soldaten erprobt und bald routinemäßig als Anästhetikum bei der Behandlung von Kampfverletzungen eingesetzt. 1970 erfolgte die Zulassung als Arzneimittel durch die Food and Drug Administration. Als Straßendroge verbreitete sich Ketamin etwa ab Mitte der 1970er Jahre. ⓘ
Gesellschaft und Kultur
Rechtlicher Status
Ketamin wird zwar in vielen Ländern weltweit legal vermarktet, ist aber in vielen Ländern auch eine kontrollierte Substanz. ⓘ
- In Australien ist Ketamin in der Giftnorm (Oktober 2015) als kontrollierte Droge nach Liste 8 aufgeführt.
- In Kanada ist Ketamin seit 2005 als Betäubungsmittel der Liste I eingestuft.
- Im Dezember 2013 hat die indische Regierung als Reaktion auf den zunehmenden Freizeitkonsum und die Verwendung von Ketamin als Rendezvous-Vergewaltigungsdroge Ketamin in Liste X des Drogen- und Kosmetikgesetzes aufgenommen, die eine Sondergenehmigung für den Verkauf und die Führung von Aufzeichnungen über alle Verkäufe über zwei Jahre vorschreibt.
- Im Vereinigten Königreich wurde es am 12. Februar 2014 als Droge der Klasse B eingestuft.
- Der zunehmende Freizeitkonsum führte dazu, dass Ketamin im August 1999 in Schedule III des United States Controlled Substance Act aufgenommen wurde. ⓘ
In Deutschland, der Schweiz und Österreich ist Ketamin verschreibungspflichtig. ⓘ
Freizeitsportlicher Konsum
Aufgrund seiner dissoziativen Wirkung wird Ketamin auch weltweit als Rauschdroge verwendet. ⓘ
In niedrigen Dosierungen induziert Ketamin eine Verzerrung des Raum- und Zeitempfindens, Pseudohalluzinationen sowie milde dissoziative Effekte. Ketaminkonsumenten gaben an, dass die besonders erwünschten Effekte in einer „Verschmelzung mit der Umgebung“ (‘melting into the surroundings’), visuellen Halluzinationen, außerkörperlichen Erfahrungen und Albernheit bestanden. Die psychoaktiven Effekte, die mit der Rauschwirkung von Ketamin einhergehen (Derealisation, Depersonalisation, auditive sowie visuelle Halluzinationen, ungewöhnliche Gedankeninhalte, Euphorie, verstärkte Farbwahrnehmung, Verlust des Zeitgefühls sowie neuartige Körperempfindungen) wurden im Allgemeinen als positiv eingestuft. Allerdings gaben 20 % aller Ketaminkonsumenten an, dass derartige Effekte unerwünscht und psychisch belastend seien. Zudem gaben 38 % an, eine Person zu kennen, die bereits schlechte Erfahrung mit Ketamin gemacht hat. John Cunningham Lilly und David Woodard (unter anderem) haben ausführlich über ihre eigenen psychonautischen Erfahrungen mit Ketamin geschrieben. ⓘ
Die Aufwach-Erscheinungen nach einer Anwendung zur Narkose, die bei Ketamin vorkommen, können Wahngedanken, Halluzinationen, Delir, Verwirrtheit, gelegentlich aber auch außerkörperliche Erfahrungen sowie Nahtoderfahrungen beinhalten. Der klinische Einsatz von Ketamin wurde deshalb von jeher durch derartige Symptome eingeschränkt, doch wurde dadurch auch ab den 1960er-Jahren das Interesse an einer Verwendung als Rauschdroge geweckt. Zu den teils erwünschten, teils unangenehmen und angsteinflößenden Wirkungen zählt das K-Hole (Ketamin-Loch), eine etwa 30-minütige komplette Dissoziation von der Realität. Hierbei können Ataxie, Dysarthrie, muskuläre Hypertonie sowie Myoklonie auftreten. Äußerlich gleicht der Zustand häufig einer Bewusstlosigkeit. Das Risiko eines K-Holes wurde mit erhöhtem Ketaminkonsum in Verbindung gebracht, insbesondere bei Nutzern, die Ketamin mehr als 20-mal konsumiert hatten. Die Anwesenheit anderer Personen (etwa Freunde, Personal in Clubs oder auf Festivals) kann dabei helfen, mit der Erfahrung umzugehen. ⓘ
In subanästhetischen Dosen führt Ketamin zu einem dissoziativen Zustand, der durch ein Gefühl der Loslösung vom eigenen Körper und der Außenwelt gekennzeichnet ist und als Depersonalisierung und Derealisierung bezeichnet wird. Bei ausreichend hohen Dosen können die Konsumenten das so genannte "K-Loch" erleben, einen Zustand der Dissoziation mit visuellen und auditiven Halluzinationen, der der Wirkung von LSD ähnelt. John C. Lilly, Marcia Moore, D. M. Turner und David Woodard (u. a.) haben ausführlich über ihren eigenen entheogenen Gebrauch von und ihre psychonautischen Erfahrungen mit Ketamin geschrieben. Turner starb vorzeitig an den Folgen eines Ertrinkens während eines vermutlich unbeaufsichtigten Ketaminkonsums. Im Jahr 2006 wurde die russische Ausgabe von Adam Parfreys Apocalypse Culture II von den Behörden verboten und vernichtet, da sie einen Aufsatz von Woodard über den entheogenen Konsum von Ketamin und psychonautische Erfahrungen mit Ketamin enthielt. Der Freizeitkonsum von Ketamin wurde weltweit mit mehr als 90 Todesfällen in England und Wales in den Jahren 2005-2013 in Verbindung gebracht. Dazu gehören versehentliche Vergiftungen, Ertrinken, Verkehrsunfälle und Selbstmorde. Die meisten Todesfälle waren unter jungen Menschen zu verzeichnen. Aufgrund seiner Fähigkeit, Verwirrung und Amnesie hervorzurufen, wurde Ketamin auch bei Vergewaltigungen eingesetzt. ⓘ
Veterinärmedizin
In der Veterinäranästhesie wird Ketamin häufig wegen seiner narkotisierenden und analgetischen Wirkung bei Katzen, Hunden, Kaninchen, Ratten und anderen Kleintieren eingesetzt. Bei Pferden wird es häufig zur Einleitung und Aufrechterhaltung der Narkose eingesetzt. Es ist ein wichtiger Bestandteil des "Nager-Cocktails", einer Mischung von Arzneimitteln, die zur Betäubung von Nagetieren verwendet werden. Tierärzte verwenden Ketamin häufig zusammen mit Sedativa, um eine ausgewogene Anästhesie und Analgesie zu erreichen, und als Infusion mit konstanter Rate, um ein Abklingen der Schmerzen zu verhindern. Ketamin wird auch zur Schmerzbehandlung bei großen Tieren eingesetzt. Es ist das primäre intravenöse Anästhetikum, das bei chirurgischen Eingriffen an Pferden eingesetzt wird, oft in Verbindung mit Detomidin und Thiopental oder manchmal auch mit Guaifenesin. ⓘ
Ketamin scheint bei Schnecken keine Sedierung oder Anästhesie zu bewirken. Stattdessen scheint es eine erregende Wirkung zu haben. ⓘ
Klinische Anwendung
Anästhesie und Analgesie
Ketamin ist als Allgemeinanästhetikum zur Einleitung und Durchführung einer Vollnarkose, als Ergänzung bei Regionalanästhesien und als Anästhetikum und Analgetikum in der Notfallmedizin zugelassen. Es kann intravenös, intramuskulär und nasal verabreicht werden. In der Allgemeinanästhesie wird es bei Erwachsenen oft in Kombination mit einem Schlafmittel (Hypnotikum), beispielsweise aus der Gruppe der Benzodiazepine, eingesetzt, während in der Kinderchirurgie und in der Notfallmedizin der Einsatz ohne Hypnotika überwiegt. ⓘ
Auf Grund seiner bronchienerweiternden Eigenschaften ist Ketamin in Kombination mit einem Muskelrelaxans auch zur Intubation bei einem therapieresistenten Status asthmaticus zugelassen. Hierbei werden mit 1 bis 2 und bei Bedarf bis zu fünf Milligramm pro Kilogramm Körpergewicht vergleichbar höhere Ketamindosen eingesetzt. Für eine niedrigdosierte Anwendung außerhalb der Zulassung (Off-Label-Use) bei Erwachsenen mit einem akuten Asthmaanfall gibt es keine ausreichenden Belege. Abgesehen von Einzelfallberichten gibt es auch keine Hinweise auf eine Wirksamkeit von Ketamin für eine Anwendung bei einem akuten Asthmaanfall bei Kindern. ⓘ
Ein weiteres zugelassenes Anwendungsgebiet von Ketamin ist die Schmerzbehandlung (Analgesie) intubierter Intensivpatienten. ⓘ
Ketamin findet auch in der Veterinärmedizin (zum Beispiel in Kombination mit Xylazin in der Hellabrunner Mischung) und in der Pädiatrie Anwendung. Ketamin kann nasal, oral, intravenös sowie intramuskulär verabreicht werden. ⓘ
Ketamin ist sowohl ein schlaferzeugendes Mittel (Hypnotikum) als auch ein potentes Analgetikum. Charakteristisch für seine Wirkung ist die Erzeugung einer dissoziativen Anästhesie, d. h. die Erzeugung von Schlaf und Schmerzfreiheit unter weitgehender Erhaltung der Reflextätigkeit, auch der Schutzreflexe. Damit entfällt insbesondere die bei anderen Anästhetika bestehende Gefahr eines lebensbedrohenden Atemstillstands, damit verbunden die Notwendigkeit der Atem- und Kreislaufüberwachung mit entsprechendem Apparate- und Personalaufwand. ⓘ
Neben- und Wechselwirkungen
Als sehr häufige Nebenwirkungen können psychotrope Effekte (Pseudohalluzinationen, unangenehme Träume), Übelkeit und Erbrechen, erhöhter Speichelfluss (Hypersalivation), Sehstörungen, Schwindel und motorische Unruhe auftreten. Daneben wirkt Ketamin als einziges Narkotikum blutdruck- und herzfrequenzsteigernd; dies ist bei spezifischen Indikationen erwünscht. Im Rahmen der Notfallmedizin ist es das einzige Medikament, mit dessen Einsatz kreislaufstabilisierende und narkotische Effekte kombiniert werden können. Der Einsatz bei Patienten mit schwerer koronarer Herzerkrankung (zum Beispiel Herzinfarkt) ist hingegen abzulehnen, weil das Medikament durch Herzfrequenz- und Blutdruckanhebung die Herzarbeit steigert und somit den Sauerstoffverbrauch des Herzmuskels erhöht. ⓘ
Ketamin bewirkt eine Erhöhung von Augen- und Hirndruck, weshalb es bei Verletzungen dort nicht als einziges Anästhetikum eingesetzt werden sollte. Der Muskeltonus der Kehlkopfmuskulatur bleibt unter Ketamin erhalten. Ein sicherer Aspirationsschutz besteht jedoch nicht. In höheren Dosierungen wirkt Ketamin ebenso bronchospasmolytisch. Ketamin als Notfallmedikation kann das Risiko einer Posttraumatischen Belastungsstörung erhöhen. In der Routineanästhesie wird Ketamin aufgrund der psychotropen Nebenwirkungen weitgehend abgelehnt. Die Kombination mit einem Benzodiazepin kann aber das Auftreten von Albträumen und Halluzinationen teilweise verhindern. Eine Reizabschirmung ist ebenfalls sinnvoll. ⓘ
Experimentelle Behandlung der Tollwut
Ketamin gehört wie Midazolam zum sogenannten Milwaukee-Protokoll, einem experimentellen Behandlungsschema bei einer Tollwut-Erkrankung. Dabei wird der Patient in ein künstliches Koma versetzt. Versuche mit Zellkulturen wie auch an Ratten hatten gezeigt, dass Ketamin die virale Gen-Transkription in den Nervenzellen verlangsamt. Wie auch bei anderen Substanzen konnte für Ketamin noch keine klinische Wirksamkeit gegen Tollwut beim Menschen nachgewiesen werden. Dennoch ergeben sich daraus für die pharmakologische Forschung Hinweise auf mögliche Zielmoleküle. ⓘ
Verwendung als Rauschmittel
Risiken
Es besteht das Risiko einer psychischen Abhängigkeit, wenn Ketamin für längere Zeit nichtmedizinisch verwendet wird. Sporadischer Ketaminkonsum ist nicht mit kognitiven Einschränkungen behaftet, chronischer Gebrauch verursacht allerdings erhebliche Beeinträchtigungen des Kurz- und Langzeitgedächtnisses; ob diese reversibel sind, war bis 2013 noch offen. Der Einsatz als K.-o.-Tropfen ist seit langem bekannt. ⓘ
Ketamin hat eine große therapeutische Breite. Die mittlere letale Dosis (LD50), die bei Tieren beobachtet wurde, ist etwa die 100fache der durchschnittlichen menschlichen intravenösen Dosis und das 20fache der durchschnittlichen menschlichen intramuskulären Dosis, die im klinischen Umfeld zur Narkose benutzt wird. ⓘ
Weiterhin kann Ketamin bei längerfristigem Gebrauch die ableitenden Harnwege schädigen. Es kann zu urologischen Beschwerden (LUTS) und zu einer Blasenentzündung mit Bildung von Geschwüren (ulzerative Zystitis) kommen. Die Symptome sind meist reversibel, falls der Ketamingebrauch eingestellt wird, bei chronischem Gebrauch sind jedoch Operationen nötig. ⓘ
Die dissoziative Wirkung von Ketamin kann Nutzer in einen Zustand versetzen, in dem sie verwundbar sind durch Unfälle, Raub, Überfall und Vergewaltigung. In einer Studie mit neunzig Ketamin-Nutzern berichteten 13 %, dass sie als direkte Folge des Ketaminrausches in einen Unfall verwickelt waren, 83 % kannten jemanden, der einen Unfall durch Ketaminkonsum erlitt. ⓘ
Eine magnetresonanztomographische Untersuchung an 21 chronischen Ketaminkonsumenten zeigte bei allen Probanden Hirnschäden, deren Schwere mit Dauer des Konsums korrelierten. Leichte Schäden waren bereits nach einem halben Jahr täglichen Konsums (1 g/Tag) nachweisbar. Während zunächst nur die Weiße Substanz der Großhirnrinde oberflächlich betroffen war, breiteten sich die Läsionen bei längerer Einnahme (ab 1–3 Jahre) auch auf tiefere Hirnareale, wie die Capsula interna und wenig später dem Pons und das Kleinhirn aus. Bei Probanden mit 4–5 Jahren Konsum waren schließlich auch das limbische System und das Stammhirn betroffen. Die Schäden wurden in diesem Stadium – mit fünf oder mehr betroffenen Regionen – als „schwer“ eingestuft. Mischkonsum mit anderen Drogen oder höhere Tagesdosen stehen in Verdacht, die schädigende Wirkung zu verstärken. ⓘ
Statistik
Öffentliche Daten für den Gebrauch von Ketamin als Rauschdroge lagen bis 2011 für Frankreich, Großbritannien, Italien, Tschechien und Ungarn vor. ⓘ
Der Europäische Drogenbericht 2015 der Europäischen Beobachtungsstelle für Drogen und Drogensucht (EMCDDA) erwähnt eine nicht-repräsentative Online-Befragung mit 25.790 Teilnehmern zwischen 15 und 34 Jahren, die regelmäßig an „Veranstaltungen des Nachtlebens“ teilnahmen, nach der in zehn europäischen Ländern die 12-Monats-Prävalenz des Konsums von Ketamin hinter der von Cannabis, MDMA, Kokain und Amphetamin lag. Im Vereinigten Königreich gab es von 1997 bis April 2013 nach amtlicher Statistik 93 Todesfälle in Verbindung mit dem Gebrauch von Ketamin als Rauschmittel. Von den 93 Personen waren 86 % männlich, und das Durchschnittsalter betrug 30,9 Jahre (15,8 bis 60,6 Jahre). Bei 70 dieser Fälle war eine zusätzliche Droge (wie etwa Alkohol) beteiligt. ⓘ
Handelsnamen
Ketalar (CH), Ketanest S (Wirkstoff Esketamin, D), zahlreiche Generika ⓘ
Tiermedizin: Anesketin, Ketaset, Ketavet, Narketan, Ursotamin ⓘ