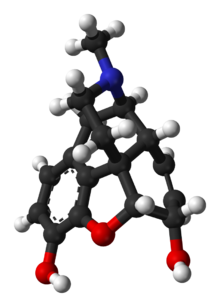
Morphin
 | |
 | |
| Klinische Daten | |
|---|---|
| Aussprache | /ˈmoʊrfiːn/ |
| Handelsnamen | Statex, MS Contin, MST Continus, Oramorph, Sevredol, und andere |
| AHFS/Drugs.com | Monographie |
| Schwangerschaft Kategorie |
|
| Abhängigkeit Haftung | Hoch |
| Abhängigkeit Haftung | Hoch |
| Wege der Verabreichung | Inhalation (Rauchen), Insufflation (Schnupfen), durch den Mund (PO), rektal, subkutan (SC), intramuskulär (IM), intravenös (IV), epidural und intrathekal (IT) |
| Wirkstoffklasse | Opioid |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | 20-40% (durch den Mund), 36-71% (rektal), 100% (IV/IM) |
| Proteinbindung | 30–40% |
| Verstoffwechselung | Hepatisch 90% |
| Beginn der Wirkung | 5 Minuten (IV), 15 Minuten (IM), 20 Minuten (PO) |
| Eliminationshalbwertszeit | 2-3 Stunden |
| Dauer der Wirkung | 3-7 Stunden |
| Ausscheidung | Nieren 90%, Galle 10% |
| Bezeichner | |
IUPAC-Bezeichnung
| |
| CAS-Nummer |
|
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| PDB-Ligand |
|
| Chemische und physikalische Daten | |
| Formel | C17H19NO3 |
| Molekulare Masse | 285,343 g-mol-1 |
| 3D-Modell (JSmol) | |
| Löslichkeit in Wasser | HCl & Schwefel: 60 mg/mL (20 °C) |
SMILES
| |
InChI
| |
| (Überprüfen) | |
Morphin ist ein Schmerzmittel aus der Familie der Opiate, das natürlich im Opium, einem dunkelbraunen Harz des Mohns (Papaver somniferum), vorkommt. Es gibt zahlreiche Methoden zur Verabreichung von Morphin: oral, sublingual, durch Inhalation, durch Injektion in einen Muskel, durch Injektion unter die Haut, intravenös, durch Injektion in den Raum um das Rückenmark, transdermal oder durch rektales Zäpfchen. Es wirkt direkt auf das zentrale Nervensystem (ZNS), um eine Analgesie auszulösen und die Wahrnehmung und emotionale Reaktion auf Schmerzen zu verändern. Bei wiederholter Verabreichung können sich physische und psychische Abhängigkeit und Toleranz entwickeln. Es kann sowohl bei akuten als auch bei chronischen Schmerzen eingenommen werden und wird häufig bei Schmerzen nach Herzinfarkten, Nierensteinen und während der Wehen eingesetzt. Die maximale Wirkung wird bei intravenöser Verabreichung nach etwa 20 Minuten und bei oraler Verabreichung nach 60 Minuten erreicht, während die Wirkungsdauer 3-7 Stunden beträgt. Langwirksame Morphinformulierungen sind als MS-Contin, Kadian und andere Markennamen sowie als Generika erhältlich. ⓘ
Zu den potenziell schwerwiegenden Nebenwirkungen von Morphin gehören verminderte Atemanstrengung, Erbrechen, Übelkeit und niedriger Blutdruck. Morphin macht süchtig und neigt zum Missbrauch. Wird die Dosis nach längerem Gebrauch reduziert, können Opioid-Entzugserscheinungen auftreten. Häufige Nebenwirkungen von Morphin sind Schläfrigkeit, Erbrechen und Verstopfung. Bei der Einnahme von Morphin während der Schwangerschaft oder Stillzeit ist Vorsicht geboten, da es die Gesundheit des Babys beeinträchtigen kann. ⓘ
Morphin wurde erstmals zwischen 1803 und 1805 von dem deutschen Pharmazeuten Friedrich Sertürner isoliert. Es wird allgemein angenommen, dass dies die erste Isolierung eines Wirkstoffs aus einer Pflanze war. Merck begann 1827 mit der kommerziellen Vermarktung des Wirkstoffs. Nach der Erfindung der subkutanen Spritze in den Jahren 1853-1855 wurde Morphin in größerem Umfang verwendet. Sertürner nannte die Substanz ursprünglich Morphium, nach dem griechischen Gott der Träume, Morpheus, da sie dazu neigt, Schlaf zu verursachen. ⓘ
Die wichtigste Quelle für Morphium ist die Isolierung aus dem Mohnstroh des Schlafmohns. Im Jahr 2013 wurden etwa 523 Tonnen Morphin hergestellt. Etwa 45 Tonnen wurden direkt zur Schmerzbehandlung verwendet, was einem Anstieg von 400 % in den letzten zwanzig Jahren entspricht. Das meiste davon wurde in den Industrieländern verwendet. Etwa 70 % des Morphins werden zur Herstellung anderer Opioide wie Hydromorphon, Oxymorphon und Heroin verwendet. In den Vereinigten Staaten ist es eine Droge der Kategorie II, im Vereinigten Königreich der Kategorie A und in Kanada der Kategorie I. Es steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation. Morphin wird unter vielen Handelsnamen verkauft. Im Jahr 2019 war es mit mehr als 3 Millionen Verschreibungen das am häufigsten verschriebene Medikament in den Vereinigten Staaten (Platz 163). ⓘ
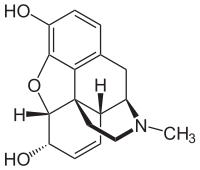
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Morphin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C17H19NO3 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code |
N02AA01 | ||||||||||||||||||
| Wirkstoffklasse |
Opioid-Analgetikum | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 285,34 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
253–254 °C | ||||||||||||||||||
| pKS-Wert |
8,21 (25 °C) | ||||||||||||||||||
| Löslichkeit |
H2O: 40 g·l−1 (20 °C, als Hydrochlorid) | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
335 mg·kg−1 (LD50, Ratte, oral) | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Morphin oder Morphium ist ein Hauptalkaloid des Opiums und zählt damit zu den Opiaten. Es gehört zu der Gruppe der stark wirkenden Opioide der Stufe III im WHO-Stufenschema (Klassifizierung der Schmerztherapie) und ist als Schmerzmittel bei starken und stärksten Schmerzen zugelassen. Morphin ist das erste in Reinform isolierte Alkaloid. Das Opiodanalgetikum ist zudem ein Rauschgift und unterliegt betäubungsmittelrechtlichen Vorschriften gemäß dem Einheitsabkommen über die Betäubungsmittel. ⓘ
Medizinische Anwendungen
Schmerzen
Morphin wird hauptsächlich zur Behandlung von akuten und chronischen starken Schmerzen eingesetzt. Die Dauer der Schmerzlinderung beträgt etwa drei bis sieben Stunden. Nebenwirkungen wie Übelkeit und Verstopfung sind selten so schwerwiegend, dass ein Abbruch der Behandlung gerechtfertigt ist. ⓘ
Es wird bei Schmerzen infolge eines Herzinfarkts und bei Geburtsschmerzen eingesetzt. Es gibt jedoch Bedenken, dass Morphin die Sterblichkeit bei Myokardinfarkten ohne ST-Hebungen erhöhen kann. Morphin wird traditionell auch bei der Behandlung des akuten Lungenödems eingesetzt. Eine Übersichtsarbeit aus dem Jahr 2006 ergab jedoch wenig Belege für diese Praxis. Ein Cochrane-Review aus dem Jahr 2016 kam zu dem Schluss, dass Morphin bei der Linderung von Krebsschmerzen wirksam ist. ⓘ
Kurzatmigkeit
Morphin ist hilfreich bei der Linderung von Symptomen der Kurzatmigkeit, die sowohl durch Krebs als auch durch andere Ursachen verursacht werden können. Bei Kurzatmigkeit in Ruhe oder bei minimaler Anstrengung aufgrund von Erkrankungen wie Krebs im fortgeschrittenen Stadium oder kardiorespiratorischen Erkrankungen im Endstadium führt regelmäßig verabreichtes, niedrig dosiertes Morphin mit verzögerter Wirkstofffreisetzung zu einer signifikanten und sicheren Verringerung der Kurzatmigkeit, wobei der Nutzen über einen längeren Zeitraum erhalten bleibt. ⓘ
Opioidkonsumstörung
Morphin ist in Österreich, Deutschland, Bulgarien, Slowenien und Kanada auch als Retardformulierung für die Opiat-Substitutionstherapie (OST) für opioidabhängige Personen erhältlich, die weder Methadon noch Buprenorphin vertragen. ⓘ
1 Milliliter Ampulle mit 10 mg Morphin ⓘ
Kontraindikationen
Zu den relativen Kontraindikationen für Morphin gehören:
- Atemdepression, wenn keine geeigneten Geräte verfügbar sind
- Obwohl früher angenommen wurde, dass Morphin bei akuter Bauchspeicheldrüsenentzündung kontraindiziert ist, hat eine Überprüfung der Literatur keinen Hinweis darauf ergeben. ⓘ
Unerwünschte Wirkungen
- Häufig und kurzzeitig
- Juckreiz
- Übelkeit
- Erbrechen
- Verstopfung
- Schläfrigkeit
- Trockener Mund
- Depression der Atemwege
- Juckreiz
- Andere
- Opioid-Abhängigkeit
- Schwindel
- Verminderter Sexualtrieb
- Appetitlosigkeit
- Beeinträchtigte sexuelle Funktion
- Verminderter Testosteronspiegel
- Depressionen
- Immunschwäche
- Opioid-induzierte abnorme Schmerzempfindlichkeit
- Unregelmäßige Menstruation
- Erhöhtes Risiko von Stürzen
- Verlangsamte Atmung
- Halluzinationen ⓘ
Verstopfung
Wie Loperamid und andere Opioide wirkt Morphin auf den Plexus myentericus im Verdauungstrakt und reduziert die Darmmotilität, was zu Verstopfung führt. Die gastrointestinalen Wirkungen von Morphin werden hauptsächlich durch μ-Opioidrezeptoren im Darm vermittelt. Durch die Hemmung der Magenentleerung und die Verringerung der treibenden Darmperistaltik verringert Morphin die Geschwindigkeit der Darmpassage. Die Verringerung der Darmsekretion und die erhöhte Aufnahme von Darmflüssigkeit tragen ebenfalls zur verstopfenden Wirkung bei. Opioide können auch indirekt auf den Darm wirken, und zwar durch tonische Darmkrämpfe nach Hemmung der Stickstoffoxidbildung. Diese Wirkung wurde bei Tieren nachgewiesen, als ein Stickoxidvorläufer, L-Arginin, die morphinbedingten Veränderungen der Darmmotilität umkehrte. ⓘ
Ungleichgewicht der Hormone
Klinische Studien kommen übereinstimmend zu dem Schluss, dass Morphin, wie auch andere Opioide, bei chronischen Konsumenten beiderlei Geschlechts häufig Hypogonadismus und Hormonstörungen verursacht. Diese Nebenwirkung ist dosisabhängig und tritt sowohl bei therapeutischen als auch bei Freizeitkonsumenten auf. Morphin kann die Menstruation bei Frauen beeinträchtigen, indem es den Spiegel des luteinisierenden Hormons unterdrückt. Viele Studien deuten darauf hin, dass die Mehrheit (vielleicht sogar 90 %) der chronischen Opioidkonsumenten einen opioidinduzierten Hypogonadismus aufweisen. Dieser Effekt kann die Ursache für die erhöhte Wahrscheinlichkeit von Osteoporose und Knochenbrüchen sein, die bei chronischen Morphinkonsumenten beobachtet wird. Studien deuten darauf hin, dass diese Wirkung nur vorübergehend ist. Seit 2013 ist die Auswirkung einer niedrigen Dosis oder einer akuten Einnahme von Morphin auf das endokrine System unklar. ⓘ
Auswirkungen auf die menschliche Leistungsfähigkeit
Die meisten Übersichten kommen zu dem Schluss, dass Opioide die menschliche Leistungsfähigkeit bei sensorischen, motorischen oder Aufmerksamkeitstests nur minimal beeinträchtigen. In neueren Studien konnten jedoch einige durch Morphin verursachte Beeinträchtigungen nachgewiesen werden, was angesichts der Tatsache, dass Morphin ein Mittel zur Depression des zentralen Nervensystems ist, nicht überraschend ist. Morphin führte zu einer Beeinträchtigung der kritischen Flimmerfrequenz (ein Maß für die allgemeine Erregung des ZNS) und zu einer Beeinträchtigung der Leistung beim Maddox-Flügeltest (ein Maß für die Abweichung der visuellen Achsen der Augen). Nur wenige Studien haben die Auswirkungen von Morphin auf die motorischen Fähigkeiten untersucht; eine hohe Morphindosis kann das Klopfen mit den Fingern und die Fähigkeit, ein niedriges, konstantes Niveau isometrischer Kraft aufrechtzuerhalten, beeinträchtigen (d. h. die feinmotorische Kontrolle ist beeinträchtigt), obwohl keine Studien eine Korrelation zwischen Morphin und grobmotorischen Fähigkeiten gezeigt haben. ⓘ
Was die kognitiven Fähigkeiten betrifft, so hat eine Studie gezeigt, dass Morphin negative Auswirkungen auf das anterograde und retrograde Gedächtnis haben kann, aber diese Auswirkungen sind minimal und vorübergehend. Insgesamt scheint es, dass akute Dosen von Opioiden bei nicht toleranten Probanden geringfügige Auswirkungen auf einige sensorische und motorische Fähigkeiten und vielleicht auch auf die Aufmerksamkeit und die Kognition haben. Es ist wahrscheinlich, dass die Wirkungen von Morphin bei Opioid-Naiven stärker ausgeprägt sind als bei chronischen Opioidkonsumenten. ⓘ
Bei chronischen Opioidkonsumenten, z. B. solchen, die eine chronische Opioid-Analgetika-Therapie (COAT) zur Behandlung schwerer chronischer Schmerzen erhalten, haben Verhaltenstests gezeigt, dass Wahrnehmung, Kognition, Koordination und Verhalten in den meisten Fällen normal funktionieren. In einer Studie aus dem Jahr 2000 wurden COAT-Patienten daraufhin untersucht, ob sie in der Lage sind, ein Kraftfahrzeug sicher zu führen. Die Ergebnisse dieser Studie deuten darauf hin, dass ein stabiler Opioidkonsum die mit dem Führen eines Kraftfahrzeugs verbundenen Fähigkeiten (einschließlich körperlicher, kognitiver und wahrnehmungsbezogener Fähigkeiten) nicht wesentlich beeinträchtigt. COAT-Patienten erledigten Aufgaben, die eine schnelle Reaktion für eine erfolgreiche Durchführung erfordern (z. B. Rey Complex Figure Test), schnell, machten aber mehr Fehler als Kontrollpersonen. COAT-Patienten zeigten keine Defizite in der visuell-räumlichen Wahrnehmung und Organisation (wie im WAIS-R Block Design Test gezeigt), zeigten aber ein beeinträchtigtes visuelles Sofort- und Kurzzeitgedächtnis (wie im Rey Complex Figure Test - Recall gezeigt). Diese Patienten zeigten keine Beeinträchtigungen bei den kognitiven Fähigkeiten höherer Ordnung (d. h. Planung). COAT-Patienten schienen Schwierigkeiten zu haben, Anweisungen zu befolgen, und zeigten eine Neigung zu impulsivem Verhalten, was jedoch keine statistische Signifikanz erreichte. Es ist wichtig festzuhalten, dass diese Studie zeigt, dass COAT-Patienten keine bereichsspezifischen Defizite aufweisen, was die Annahme stützt, dass chronischer Opioidkonsum nur geringe Auswirkungen auf die psychomotorischen, kognitiven oder neuropsychologischen Funktionen hat. ⓘ
Verstärkungsstörungen
Abhängigkeit

Morphin ist eine stark süchtig machende Substanz. In kontrollierten Studien, in denen die physiologischen und subjektiven Wirkungen von Heroin und Morphin bei ehemals opiatabhängigen Personen verglichen wurden, zeigten die Probanden keine Vorliebe für die eine Droge gegenüber der anderen. Gleiche, injizierte Dosen hatten einen vergleichbaren Wirkungsverlauf, ohne dass sich die Probanden in ihren selbst eingeschätzten Gefühlen von Euphorie, Ehrgeiz, Nervosität, Entspannung, Schläfrigkeit oder Müdigkeit unterschieden. Kurzfristige Suchtstudien derselben Forscher zeigten, dass die Toleranzentwicklung bei Heroin und Morphin ähnlich schnell verläuft. Im Vergleich zu den Opioiden Hydromorphon, Fentanyl, Oxycodon und Pethidin/Meperidin zeigten ehemalige Süchtige eine starke Präferenz für Heroin und Morphin, was darauf schließen lässt, dass Heroin und Morphin besonders anfällig für Missbrauch und Abhängigkeit sind. Morphin und Heroin lösten im Vergleich zu diesen anderen Opioiden auch viel eher Euphorie und andere positive subjektive Wirkungen aus. Dass ehemalige Drogenabhängige Heroin und Morphin anderen Opioiden vorziehen, könnte auch daran liegen, dass Heroin (auch bekannt als Morphindiacetat, Diamorphin oder Diacetylmorphin) ein Morphinester und ein Morphin-Prodrug ist, was bedeutet, dass es sich in vivo um identische Drogen handelt. Heroin wird in Morphin umgewandelt, bevor es sich an die Opioidrezeptoren im Gehirn und im Rückenmark bindet, wo das Morphin die subjektiven Wirkungen hervorruft, die die Süchtigen suchen. ⓘ
Toleranz
Es gibt mehrere Hypothesen darüber, wie sich Toleranz entwickelt, darunter die Phosphorylierung des Opioidrezeptors (die die Konformation des Rezeptors verändern würde), die funktionelle Entkopplung der Rezeptoren von den G-Proteinen (was zu einer Desensibilisierung des Rezeptors führt), die Internalisierung des μ-Opioidrezeptors oder die Herabregulierung des Rezeptors (wodurch sich die Zahl der für die Wirkung des Morphins verfügbaren Rezeptoren verringert) und die Hochregulierung des cAMP-Signalwegs (ein Mechanismus zur Gegenregulierung der Opioidwirkung) (für eine Übersicht über diese Prozesse siehe Koch und Hollt. ) CCK könnte einige gegenregulatorische Wege vermitteln, die für die Opioidtoleranz verantwortlich sind. CCK-Antagonisten, insbesondere Proglumid, verlangsamen nachweislich die Entwicklung einer Toleranz gegenüber Morphin. ⓘ
Abhängigkeit und Entzug
Die Beendigung der Morphineinnahme führt zu dem prototypischen Opioid-Entzugssyndrom, das im Gegensatz zu dem von Barbituraten, Benzodiazepinen, Alkohol oder Sedativa-Hypnotika bei ansonsten gesunden Menschen nicht tödlich ist. ⓘ
Der akute Morphinentzug durchläuft, wie der Entzug jedes anderen Opioids, mehrere Phasen. Andere Opioide unterscheiden sich in der Intensität und Dauer der einzelnen Phasen, und bei schwachen Opioiden und gemischten Agonisten-Antagonisten können akute Entzugssyndrome auftreten, die nicht die höchste Stufe erreichen. Sie werden im Allgemeinen wie folgt beschrieben:
- Stadium I, 6 bis 14 Stunden nach der letzten Dosis: Verlangen nach der Droge, Angst, Reizbarkeit, Schwitzen und leichte bis mittlere Dysphorie
- Stadium II, 14 bis 18 Stunden nach der letzten Dosis: Gähnen, starkes Schwitzen, leichte Depression, Tränenfluss, Weinen, Kopfschmerzen, laufende Nase, Dysphorie, auch Verstärkung der oben genannten Symptome, "Yen-Schlaf" (ein wacher tranceähnlicher Zustand)
- Stadium III, 16 bis 24 Stunden nach der letzten Dosis: Rhinorrhoe (Fließschnupfen) und Zunahme anderer der oben genannten Symptome, erweiterte Pupillen, Piloerektion (Gänsehaut - ein angeblicher Ursprung des Ausdrucks "kalter Entzug", aber in Wirklichkeit entstand der Ausdruck außerhalb der Drogenbehandlung), Muskelzuckungen, Hitzewallungen, Kälteblitze, schmerzende Knochen und Muskeln, Appetitlosigkeit und beginnende Darmkrämpfe
- Stadium IV, 24 bis 36 Stunden nach der letzten Dosis: Zunahme aller oben genannten Symptome, einschließlich schwerer Krämpfe und unwillkürlicher Beinbewegungen ("kicking the habit", auch Restless-Leg-Syndrom genannt), loser Stuhlgang, Schlaflosigkeit, Erhöhung des Blutdrucks, mäßige Erhöhung der Körpertemperatur, Zunahme der Atemfrequenz und des Atemzugvolumens, Tachykardie (erhöhter Puls), Unruhe, Übelkeit
- Stadium V, 36 bis 72 Stunden nach der letzten Dosis: Zunahme der oben genannten Symptome, fetale Position, Erbrechen, freier und häufiger flüssiger Durchfall, der manchmal die Passage der Nahrung vom Mund zum Körper beschleunigen kann, Gewichtsverlust von 2 bis 5 kg pro 24 Stunden, erhöhte Anzahl weißer Blutkörperchen und andere Blutveränderungen
- Stadium VI, nach Abschluss der oben genannten Maßnahmen: Wiedererlangung von Appetit und normaler Darmfunktion, Beginn des Übergangs zu postakuten und chronischen Symptomen, die hauptsächlich psychologischer Natur sind, aber auch erhöhte Schmerzempfindlichkeit, Bluthochdruck, Kolitis oder andere gastrointestinale Beschwerden im Zusammenhang mit der Motilität sowie Probleme mit der Gewichtskontrolle in beide Richtungen umfassen können ⓘ
In fortgeschrittenen Entzugsstadien wurde bei einigen Patienten eine Pankreatitis im Ultraschall nachgewiesen, die vermutlich auf einen Spasmus des Oddi-Schließmuskels der Bauchspeicheldrüse zurückzuführen ist. ⓘ
Die mit der Morphinabhängigkeit verbundenen Entzugssymptome treten in der Regel kurz vor der nächsten geplanten Einnahme auf, manchmal sogar schon wenige Stunden (in der Regel 6 bis 12 Stunden) nach der letzten Einnahme. Zu den frühen Symptomen gehören tränende Augen, Schlaflosigkeit, Durchfall, laufende Nase, Gähnen, Dysphorie, Schwitzen und in einigen Fällen ein starkes Verlangen nach der Droge. Im weiteren Verlauf des Syndroms treten starke Kopfschmerzen, Unruhe, Reizbarkeit, Appetitlosigkeit, Körperschmerzen, starke Bauchschmerzen, Übelkeit und Erbrechen, Zittern und ein noch stärkeres und intensiveres Verlangen nach Drogen auf. Schwere Depressionen und Erbrechen sind sehr häufig. Während der akuten Entzugsphase steigen der systolische und der diastolische Blutdruck, in der Regel über das Niveau der Prämorphine hinaus, und die Herzfrequenz erhöht sich, was zu einem Herzinfarkt, einem Blutgerinnsel oder einem Schlaganfall führen kann. ⓘ
Schüttelfrost oder Kältegefühl mit Gänsehaut ("kalter Truthahn") im Wechsel mit Erröten (Hitzewallungen), kickende Bewegungen der Beine ("kicking the habit") und übermäßiges Schwitzen sind ebenfalls charakteristische Symptome. Es kommt zu starken Schmerzen in den Knochen und Muskeln des Rückens und der Extremitäten sowie zu Muskelkrämpfen. Zu jedem Zeitpunkt dieses Prozesses kann ein geeignetes Narkotikum verabreicht werden, das die Entzugssymptome drastisch umkehrt. Die stärksten Entzugserscheinungen treten zwischen 48 und 96 Stunden nach der letzten Dosis auf und klingen nach etwa 8 bis 12 Tagen ab. Ein plötzlicher Entzug bei stark abhängigen Konsumenten, die sich in einem schlechten Gesundheitszustand befinden, ist sehr selten tödlich. Der Morphinentzug gilt als weniger gefährlich als der Entzug von Alkohol, Barbituraten oder Benzodiazepinen. ⓘ
Die mit der Morphinabhängigkeit verbundene psychische Abhängigkeit ist komplex und langwierig. Lange nachdem das körperliche Bedürfnis nach Morphin abgeklungen ist, wird der Süchtige in der Regel weiterhin über den Konsum von Morphin (oder anderen Drogen) nachdenken und sprechen und sich bei der Bewältigung alltäglicher Aktivitäten ohne den Einfluss von Morphin seltsam oder überfordert fühlen. Der psychologische Entzug von Morphin ist in der Regel ein sehr langer und schmerzhafter Prozess. Süchtige leiden oft unter schweren Depressionen, Angstzuständen, Schlaflosigkeit, Stimmungsschwankungen, Amnesie (Vergesslichkeit), geringem Selbstwertgefühl, Verwirrung, Paranoia und anderen psychischen Störungen. Wenn nicht eingegriffen wird, nimmt das Syndrom seinen Lauf, und die meisten offensichtlichen körperlichen Symptome verschwinden innerhalb von 7 bis 10 Tagen, einschließlich der psychischen Abhängigkeit. Nach dem Morphinentzug besteht eine hohe Rückfallwahrscheinlichkeit, wenn weder das physische Umfeld noch die Verhaltensmotivatoren, die zum Missbrauch beigetragen haben, verändert wurden. Die Rückfallquote ist ein Beleg für die süchtig machende und verstärkende Wirkung von Morphin. Morphin- (und Heroin-)missbraucher haben eine der höchsten Rückfallquoten unter allen Drogenkonsumenten, die nach Einschätzung einiger medizinischer Experten bis zu 98 % beträgt. ⓘ
Toxizität
| Eigenschaften von Morphin ⓘ | |||||
|---|---|---|---|---|---|
| Molekulare Masse | 285,338 g/mol | ||||
| Acidität (pKa) |
| ||||
| Löslichkeit | 0,15 g/L bei 20 °C | ||||
| Schmelzpunkt | 255 °C | ||||
| Siedepunkt | 190 °C sublimiert | ||||
Eine große Überdosis kann zu Erstickung und Tod durch Atemdepression führen, wenn die Person nicht sofort ärztlich behandelt wird. Die Behandlung einer Überdosis umfasst die Verabreichung von Naloxon. Letzteres hebt die Wirkung von Morphin vollständig auf, kann aber bei Opiatabhängigen zu einem sofortigen Entzug führen. Da die Wirkungsdauer von Morphin länger ist als die von Naloxon, können mehrere Dosen erforderlich sein. ⓘ
Die LD50 von Morphinsulfat und anderen Zubereitungen für den Menschen ist nicht mit Sicherheit bekannt. In einer qualitativ schlechten Studie über Morphinüberdosierungen bei Soldaten wurde berichtet, dass die tödliche Dosis bei Männern 0,78 mcg/ml (~71 mg für einen durchschnittlichen 90 kg schweren erwachsenen Mann) und bei Frauen 0,98 mcg/ml (~74 mg für eine durchschnittliche 75 kg schwere Frau) betrug. Es wurde nicht angegeben, ob die Dosis oral, parenteral oder intravenös verabreicht wurde. In der Literatur werden in der Regel Studien an Labortieren zitiert. Bei schwerer Drogenabhängigkeit (hohe Toleranz) können 2000-3000 mg pro Tag toleriert werden. ⓘ
Pharmakologie
Pharmakodynamik
| Verbindung | Affinitäten (Ki) | Verhältnis | Ref | ||
|---|---|---|---|---|---|
| MOR | DOR | KOR | MOR:DOR:KOR | ||
| Morphin | 1,8 nM | 90 nM | 317 nM | 1:50:176 | |
| (-)-Morphin | 1,24 nM | 145 nM | 23,4 nM | 1:117:19 | |
| (+)-Morphin | >10 μM | >100 μM | >300 μM | ND | |
| Verbindung | Weg | Dosis |
|---|---|---|
| Kodein | PO | 200 mg |
| Hydrocodon | PO | 20-30 mg |
| Hydromorphon | PO | 7,5 mg |
| Hydromorphon | IV | 1,5 mg |
| Morphin | PO | 30 mg |
| Morphin | IV | 10 mg |
| Oxycodon | PO | 20 mg |
| Oxycodon | IV | 10 mg |
| Oxymorphon | PO | 10 mg |
| Oxymorphon | IV | 1 mg |
Morphin ist das prototypische Opioid und gilt als Standard, an dem andere Opioide gemessen werden. Es interagiert vorwiegend mit dem μ-δ-Opioid (Mu-Delta)-Rezeptor-Heteromer. Die μ-Bindungsstellen sind diskret im menschlichen Gehirn verteilt, mit hoher Dichte in der hinteren Amygdala, im Hypothalamus, im Thalamus, im Nucleus caudatus, im Putamen und in bestimmten kortikalen Bereichen. Sie finden sich auch auf den Endachsen der primären Afferenzen in den Laminae I und II (Substantia gelatinosa) des Rückenmarks und im spinalen Kern des Trigeminusnervs. ⓘ
Morphin ist ein Phenanthren-Opioidrezeptor-Agonist - seine Hauptwirkung ist die Bindung an den μ-Opioidrezeptor (MOR) im zentralen Nervensystem und dessen Aktivierung. Seine intrinsische Aktivität am MOR hängt stark vom jeweiligen Assay und dem getesteten Gewebe ab; in einigen Situationen ist es ein vollständiger Agonist, während es in anderen ein partieller Agonist oder sogar ein Antagonist sein kann. Im klinischen Bereich übt Morphin seine pharmakologische Hauptwirkung auf das zentrale Nervensystem und den Magen-Darm-Trakt aus. Seine primären Wirkungen von therapeutischem Wert sind Analgesie und Sedierung. Die Aktivierung des MOR ist mit Analgesie, Sedierung, Euphorie, körperlicher Abhängigkeit und Atemdepression verbunden. Morphin ist auch ein κ-Opioidrezeptor (KOR) und δ-Opioidrezeptor (DOR) Agonist. Die Aktivierung des KOR wird mit spinaler Analgesie, Miosis (Pupillenverengung) und psychotomimetischen Wirkungen in Verbindung gebracht. Es wird angenommen, dass der DOR eine Rolle bei der Analgesie spielt. Obwohl Morphin nicht an den σ-Rezeptor bindet, wurde gezeigt, dass σ-Rezeptor-Agonisten wie (+)-Pentazocin die Morphin-Analgesie hemmen und σ-Rezeptor-Antagonisten die Morphin-Analgesie verstärken, was auf eine nachgeschaltete Beteiligung des σ-Rezeptors an den Wirkungen von Morphin schließen lässt. ⓘ
Den Wirkungen von Morphin kann mit Opioidrezeptorantagonisten wie Naloxon und Naltrexon entgegengewirkt werden; die Entwicklung einer Toleranz gegenüber Morphin kann durch NMDA-Rezeptorantagonisten wie Ketamin oder Dextromethorphan gehemmt werden. Der Wechsel von Morphin mit chemisch unähnlichen Opioiden bei der Langzeitbehandlung von Schmerzen wird die Toleranzentwicklung langfristig verlangsamen, insbesondere bei Wirkstoffen, von denen bekannt ist, dass sie eine deutlich unvollständige Kreuztoleranz mit Morphin aufweisen, wie z. B. Levorphanol, Ketobemidon, Piritramid sowie Methadon und seine Derivate; alle diese Arzneimittel haben auch NMDA-Antagonisten-Eigenschaften. Es wird angenommen, dass das starke Opioid mit der unvollständigsten Kreuztoleranz mit Morphin entweder Methadon oder Dextromoramid ist. ⓘ

Genexpression
Studien haben gezeigt, dass Morphin die Expression einer Reihe von Genen verändern kann. Es hat sich gezeigt, dass eine einzige Morphininjektion die Expression von zwei Hauptgruppen von Genen verändert, nämlich für Proteine, die an der mitochondrialen Atmung beteiligt sind, und für Proteine, die mit dem Zytoskelett zusammenhängen. ⓘ
Auswirkungen auf das Immunsystem
Es ist seit langem bekannt, dass Morphin auf Rezeptoren wirkt, die auf Zellen des zentralen Nervensystems exprimiert werden, was zu Schmerzlinderung und Analgesie führt. In den 1970er und 80er Jahren führten Hinweise darauf, dass Opioid-Drogenabhängige ein erhöhtes Infektionsrisiko aufweisen (z. B. vermehrte Lungenentzündung, Tuberkulose und HIV/AIDS), zu der Annahme, dass Morphin auch das Immunsystem beeinflussen könnte. Diese Möglichkeit verstärkte das Interesse an den Auswirkungen des chronischen Morphinkonsums auf das Immunsystem. ⓘ
Der erste Schritt zur Feststellung, dass Morphin das Immunsystem beeinflussen kann, bestand darin, festzustellen, dass die Opiatrezeptoren, von denen bekannt ist, dass sie auf Zellen des zentralen Nervensystems exprimiert werden, auch auf Zellen des Immunsystems exprimiert werden. In einer Studie konnte gezeigt werden, dass dendritische Zellen, die Teil des angeborenen Immunsystems sind, Opiatrezeptoren aufweisen. Dendritische Zellen sind für die Produktion von Zytokinen verantwortlich, die als Kommunikationsmittel des Immunsystems dienen. Dieselbe Studie zeigte, dass dendritische Zellen, die während ihrer Differenzierung chronisch mit Morphin behandelt wurden, mehr Interleukin-12 (IL-12) produzieren, ein Zytokin, das für die Förderung der Proliferation, des Wachstums und der Differenzierung von T-Zellen (eine weitere Zelle des adaptiven Immunsystems) verantwortlich ist, und weniger Interleukin-10 (IL-10), ein Zytokin, das für die Förderung einer B-Zellen-Immunantwort verantwortlich ist (B-Zellen produzieren Antikörper zur Bekämpfung von Infektionen). ⓘ
Diese Regulierung der Zytokine erfolgt offenbar über den p38 MAPKs (mitogen-aktivierte Proteinkinase)-abhängigen Weg. Normalerweise exprimiert die p38 in der dendritischen Zelle den TLR 4 (Toll-like-Rezeptor 4), der durch den Liganden LPS (Lipopolysaccharid) aktiviert wird. Dadurch wird die p38 MAPK phosphoryliert. Durch diese Phosphorylierung wird die p38 MAPK aktiviert und beginnt mit der Produktion von IL-10 und IL-12. Wenn die dendritischen Zellen während ihres Differenzierungsprozesses chronisch Morphin ausgesetzt und dann mit LPS behandelt werden, ist die Produktion von Zytokinen anders. Nach der Behandlung mit Morphin produziert die p38-MAPK kein IL-10 mehr, sondern fördert stattdessen die Produktion von IL-12. Der genaue Mechanismus, durch den die Produktion eines Zytokins zugunsten eines anderen erhöht wird, ist nicht bekannt. Höchstwahrscheinlich bewirkt das Morphin eine erhöhte Phosphorylierung der p38 MAPK. Interaktionen auf Transkriptionsebene zwischen IL-10 und IL-12 können die Produktion von IL-12 weiter erhöhen, wenn IL-10 nicht produziert wird. Diese erhöhte Produktion von IL-12 führt zu einer verstärkten Immunantwort der T-Zellen. ⓘ
Weitere Studien über die Auswirkungen von Morphin auf das Immunsystem haben gezeigt, dass Morphin die Produktion von Neutrophilen und anderen Zytokinen beeinflusst. Da Zytokine als Teil der unmittelbaren immunologischen Reaktion (Entzündung) produziert werden, wurde vermutet, dass sie auch den Schmerz beeinflussen können. Auf diese Weise könnten Zytokine ein logisches Ziel für die Entwicklung von Analgetika sein. Kürzlich wurde in einer Studie ein Tiermodell (Schnitt an der Hinterpfote) verwendet, um die Auswirkungen der Morphinverabreichung auf die akute immunologische Reaktion zu beobachten. Nach der Inzision der Hinterpfoten wurden die Schmerzschwellen und die Zytokinproduktion gemessen. Normalerweise steigt die Zytokinproduktion in und um den verletzten Bereich an, um die Infektion zu bekämpfen und die Heilung zu kontrollieren (und möglicherweise auch, um den Schmerz zu kontrollieren), aber die Verabreichung von Morphin vor dem Schnitt (0,1 mg/kg bis 10,0 mg/kg) reduzierte die Anzahl der Zytokine, die um die Wunde herum gefunden wurden, in einer dosisabhängigen Weise. Die Autoren vermuten, dass die Verabreichung von Morphin in der akuten Phase nach der Verletzung die Infektionsresistenz verringern und die Wundheilung beeinträchtigen könnte. ⓘ
Pharmakokinetik
Absorption und Stoffwechsel
Morphin kann oral, sublingual, bukkal, rektal, subkutan, intranasal, intravenös, intrathekal oder epidural eingenommen und über einen Vernebler inhaliert werden. Als Freizeitdroge wird es immer häufiger inhaliert ("Chasing the Dragon"), aber für medizinische Zwecke ist die intravenöse (IV) Injektion die gängigste Verabreichungsmethode. Morphin unterliegt einem umfangreichen First-Pass-Metabolismus (ein großer Teil wird in der Leber abgebaut), so dass bei oraler Einnahme nur 40 bis 50 % der Dosis das zentrale Nervensystem erreichen. Die resultierenden Plasmaspiegel nach subkutaner (SC), intramuskulärer (IM) und intravenöser Injektion sind alle vergleichbar. Nach IM- oder SC-Injektionen erreichen die Morphin-Plasmaspiegel nach etwa 20 Minuten ihren Höhepunkt, nach oraler Verabreichung nach etwa 30 Minuten. Morphin wird hauptsächlich in der Leber metabolisiert, und etwa 87 % einer Morphindosis werden innerhalb von 72 Stunden nach der Verabreichung mit dem Urin ausgeschieden. Morphin wird hauptsächlich in Morphin-3-Glucuronid (M3G) und Morphin-6-Glucuronid (M6G) über Glucuronidierung durch das Phase-II-Stoffwechselenzym UDP-Glucuronosyltransferase-2B7 (UGT2B7) metabolisiert. Etwa 60 % des Morphins werden in M3G umgewandelt, und 6 bis 10 % werden in M6G umgewandelt. Der Metabolismus findet nicht nur in der Leber statt, sondern kann auch im Gehirn und in den Nieren ablaufen. M3G wird nicht an Opioidrezeptoren gebunden und hat keine analgetische Wirkung. M6G bindet an μ-Rezeptoren und ist ein halb so starkes Analgetikum wie Morphin beim Menschen. Morphin kann auch in geringe Mengen von Normorphin, Codein und Hydromorphon metabolisiert werden. Die Metabolisierungsrate wird durch Geschlecht, Alter, Ernährung, genetische Veranlagung, Krankheitszustand (falls vorhanden) und die Einnahme anderer Medikamente bestimmt. Die Eliminationshalbwertszeit von Morphin beträgt etwa 120 Minuten, wobei es leichte Unterschiede zwischen Männern und Frauen geben kann. Morphin kann in Fett gespeichert werden und ist daher auch nach dem Tod noch nachweisbar. Morphin kann die Blut-Hirn-Schranke überwinden, aber aufgrund der schlechten Lipidlöslichkeit, der Proteinbindung, der schnellen Konjugation mit Glucuronsäure und der Ionisierung passiert es diese Schranke nicht ohne weiteres. Heroin, das von Morphin abgeleitet ist, überwindet die Blut-Hirn-Schranke leichter und ist daher stärker. ⓘ
Verlängerte Wirkstofffreisetzung
Es gibt Formulierungen mit verlängerter Freisetzung von oral verabreichtem Morphin, deren Wirkung länger anhält und die einmal täglich verabreicht werden können. Zu den Markennamen für diese Morphinformulierung gehören Avinza, Kadian, MS Contin und Dolcontin. Bei konstanten Schmerzen ist die schmerzlindernde Wirkung von Morphin mit verlängerter Wirkstofffreisetzung, das einmal (bei Kadian) oder zweimal (bei MS Contin) alle 24 Stunden verabreicht wird, in etwa die gleiche wie die mehrfache Verabreichung von Morphin mit sofortiger Wirkstofffreisetzung (oder "normalem" Morphin). Morphin mit verlängerter Wirkstofffreisetzung kann bei Durchbruchschmerzen zusammen mit "Rettungsdosen" von Morphin mit sofortiger Wirkstofffreisetzung verabreicht werden, die im Allgemeinen jeweils 5 % bis 15 % der 24-Stunden-Dosis mit verlängerter Wirkstofffreisetzung betragen. ⓘ
Nachweis in Körperflüssigkeiten
Morphin und seine wichtigsten Metaboliten, Morphin-3-Glucuronid und Morphin-6-Glucuronid, können in Blut, Plasma, Haaren und Urin mit einem Immunoassay nachgewiesen werden. Mit Hilfe der Chromatographie kann jede dieser Substanzen einzeln getestet werden. Bei einigen Testverfahren werden die Stoffwechselprodukte vor dem Immunoassay zu Morphin hydrolysiert, was beim Vergleich der Morphinwerte in separat veröffentlichten Ergebnissen berücksichtigt werden muss. Morphin kann auch durch Festphasenextraktion (SPE) aus Vollblutproben isoliert und mit Flüssigchromatographie-Massenspektrometrie (LC-MS) nachgewiesen werden. ⓘ
Die Einnahme von Codein oder mohnhaltigen Lebensmitteln kann zu falsch positiven Ergebnissen führen. ⓘ
In einer Überprüfung aus dem Jahr 1999 wurde geschätzt, dass relativ niedrige Dosen von Heroin (das sofort in Morphin umgewandelt wird) in Standard-Urintests 1-1,5 Tage nach dem Konsum nachweisbar sind. In einer Überprüfung aus dem Jahr 2009 wurde festgestellt, dass eine intravenöse Dosis von 20 mg Morphin 12 bis 24 Stunden lang nachweisbar ist, wenn es sich bei dem Analyten um Morphin handelt und die Nachweisgrenze bei 1 ng/ml liegt. Eine Nachweisgrenze von 0,6 ng/ml führte zu ähnlichen Ergebnissen. ⓘ
Natürliches Vorkommen

Morphin ist das am häufigsten vorkommende Opiat in Opium, dem getrockneten Milchsaft, der durch flaches Anritzen der unreifen Samenschoten des Mohns Papaver somniferum gewonnen wird. Der Morphingehalt beträgt im Allgemeinen 8-14 % des Trockengewichts des Opiums, obwohl speziell gezüchtete Sorten 26 % erreichen oder nur wenig Morphin produzieren (unter 1 %, vielleicht sogar nur 0,04 %). Aus den letztgenannten Sorten, zu denen auch die Schlafmohnsorten "Przemko" und "Norman" gehören, werden zwei weitere Alkaloide, Thebain und Oripavin, gewonnen, die zur Herstellung halbsynthetischer und synthetischer Opioide wie Oxycodon und Etorphin sowie einiger anderer Drogenarten verwendet werden. P. bracteatum enthält weder Morphin noch Codein oder andere narkotische Alkaloide vom Phenanthren-Typ. Diese Art ist eher eine Quelle für Thebain. Das Vorkommen von Morphin in anderen Papaverales und Papaveraceae sowie in einigen Arten von Hopfen und Maulbeerbäumen wurde nicht bestätigt. Morphin wird vor allem in den frühen Stadien des Lebenszyklus der Pflanze produziert. Nach dem optimalen Zeitpunkt für die Extraktion entstehen durch verschiedene Prozesse in der Pflanze Codein, Thebain und in einigen Fällen vernachlässigbare Mengen von Hydromorphon, Dihydromorphin, Dihydrocodein, Tetrahydro-Thebain und Hydrocodon (diese Verbindungen werden eher aus Thebain und Oripavin synthetisiert). ⓘ
Im Gehirn von Säugetieren ist Morphin in Spuren in konstanten Konzentrationen nachweisbar. Der menschliche Körper produziert auch Endorphine, chemisch verwandte endogene opioide Peptide, die als Neuropeptide wirken und ähnliche Wirkungen wie Morphin haben. ⓘ
Menschliche Biosynthese
Morphin ist ein endogenes Opioid des Menschen, das von verschiedenen menschlichen Zellen, einschließlich der weißen Blutkörperchen, synthetisiert und freigesetzt werden kann. CYP2D6, ein Cytochrom-P450-Isoenzym, katalysiert die Biosynthese von Morphin aus Codein und Dopamin aus Tyramin entlang des Biosyntheseweges von Morphin beim Menschen. Der Morphin-Biosyntheseweg beim Menschen verläuft wie folgt:
L-Tyrosin → Para-Tyramin oder L-DOPA → Dopamin → (S)-Norlaudanosolin → (S)-Reticulin → 1,2-Dehydroretinulinium → (R)-Reticulin → Salutaridin → Salutaridinol → Thebain → Neopinon → Codeinon → Codein → Morphin
(S)-Norlaudanosolin (auch bekannt als Tetrahydropapaverolin) kann auch aus 3,4-Dihydroxyphenylacetaldehyd (DOPAL), einem Metaboliten von L-DOPA und Dopamin, synthetisiert werden. Es wurde festgestellt, dass die Urinkonzentrationen von endogenem Codein und Morphin bei Personen, die L-DOPA zur Behandlung der Parkinson-Krankheit einnehmen, deutlich ansteigen. ⓘ
Biosynthese im Schlafmohn
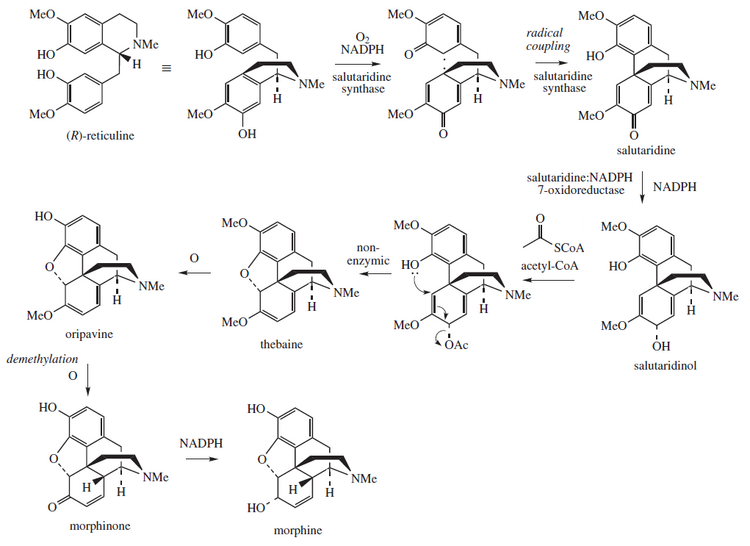
Morphin wird im Schlafmohn aus dem Tetrahydroisochinolin Reticulin biosynthetisiert. Es wird in Salutaridin, Thebain und Oripavin umgewandelt. Die an diesem Prozess beteiligten Enzyme sind die Salutaridin-Synthase, die Salutaridin:NADPH 7-Oxidoreduktase und die Codeinon-Reduktase. Die Forscher versuchen, den Biosyntheseweg, über den Morphin hergestellt wird, in gentechnisch veränderter Hefe zu reproduzieren. Im Juni 2015 konnte das S-Reticulin aus Zucker hergestellt und R-Reticulin in Morphin umgewandelt werden, aber die Zwischenreaktion konnte nicht durchgeführt werden. Im August 2015 wurde die erste vollständige Synthese von Thebain und Hydrocodon in Hefe gemeldet, aber der Prozess müsste 100.000-mal produktiver sein, um für eine kommerzielle Nutzung geeignet zu sein. ⓘ
Chemie
Elemente der Morphinstruktur wurden verwendet, um vollständig synthetische Drogen wie die Morphinan-Familie (Levorphanol, Dextromethorphan und andere) und andere Gruppen zu schaffen, die viele Mitglieder mit morphinähnlichen Eigenschaften haben. Aus der Modifikation von Morphin und den genannten synthetischen Substanzen sind auch nicht-narkotische Drogen mit anderen Verwendungszwecken hervorgegangen, wie Brechmittel, Stimulanzien, Antitussiva, Anticholinergika, Muskelrelaxantien, Lokalanästhetika, Allgemeinanästhetika und andere. Es wurden auch von Morphin abgeleitete Agonisten-Antagonisten entwickelt. ⓘ
Beschreibung der Struktur



Morphin ist ein Benzylisochinolin-Alkaloid mit zwei zusätzlichen Ringschlüssen. Wie Jack DeRuiter vom Department of Drug Discovery and Development (ehemals Pharmacal Sciences) der Harrison School of Pharmacy der Auburn University in seinen Kursunterlagen für den Kurs "Principles of Drug Action 2" (Grundlagen der Arzneimittelwirkung 2) im Herbst 2000 feststellte, "zeigt die Untersuchung des Morphinmoleküls die folgenden strukturellen Merkmale, die für sein pharmakologisches Profil wichtig sind...
- Eine starre pentacyclische Struktur, bestehend aus einem Benzolring (A), zwei teilweise ungesättigten Cyclohexanringen (B und C), einem Piperidinring (D) und einem Tetrahydrofuranring (E). Die Ringe A, B und C bilden das Phenanthren-Ringsystem. Dieses Ringsystem weist eine geringe Konformationsflexibilität auf...
- Zwei funktionelle Hydroxylgruppen: eine C3-phenolische [Hydroxylgruppe] (pKa 9,9) und eine C6-allylische [Hydroxylgruppe],
- Eine Etherverknüpfung zwischen C4 und C5,
- Ungesättigtheit zwischen C7 und C8,
- eine basische, [tertiäre] Aminfunktion an Position 17, [und]
- [Fünf] Chiralitätszentren (C5, C6, C9, C13 und C14), wobei Morphin einen hohen Grad an Stereoselektivität der analgetischen Wirkung aufweist." ⓘ
Morphin und die meisten seiner Derivate weisen keine optische Isomerie auf, obwohl einige entferntere Verwandte wie die Morphinanreihe (Levorphanol, Dextorphan und die racemische Ausgangssubstanz Racemorphan) dies tun, und wie bereits erwähnt, ist die Stereoselektivität in vivo ein wichtiges Thema. ⓘ
Verwendungen und Derivate
Der größte Teil des legal hergestellten Morphins wird zur Herstellung von Codein durch Methylierung verwendet. Es ist auch ein Ausgangsstoff für viele Drogen wie Heroin (3,6-Diacetylmorphin), Hydromorphon (Dihydromorphinon) und Oxymorphon (14-Hydroxydihydromorphinon). Die meisten halbsynthetischen Opioide, sowohl der Morphin- als auch der Codein-Untergruppe, werden durch eine oder mehrere der folgenden Modifikationen hergestellt:
- Halogenierung oder andere Veränderungen an den Positionen 1 oder 2 des Morphin-Kohlenstoffskeletts.
- Die Methylgruppe, die Morphin zu Codein macht, kann entfernt oder wieder hinzugefügt oder durch eine andere funktionelle Gruppe wie Ethyl und andere ersetzt werden, um Codein-Analoga von Morphin-abgeleiteten Arzneimitteln herzustellen und umgekehrt. Codeinanaloga von Morphin-basierten Drogen dienen oft als Prodrugs der stärkeren Droge, wie bei Codein und Morphin, Hydrocodon und Hydromorphon, Oxycodon und Oxymorphon, Nicocodein und Nicomorphin, Dihydrocodein und Dihydromorphin usw.
- Die Sättigung, Öffnung oder sonstige Veränderung der Bindung zwischen den Positionen 7 und 8 sowie das Hinzufügen, Entfernen oder Verändern funktioneller Gruppen an diesen Positionen; die Sättigung, Reduktion, Eliminierung oder sonstige Veränderung der Bindung 7-8 und das Anhängen einer funktionellen Gruppe an 14 ergibt Hydromorphinol; die Oxidation der Hydroxylgruppe zu einem Carbonyl und die Veränderung der Bindung 7-8 von einer Doppelbindung zu einer Einfachbindung verwandelt Codein in Oxycodon.
- Anbringen, Entfernen oder Ändern von funktionellen Gruppen an den Positionen 3 oder 6 (Dihydrocodein und verwandte, Hydrocodon, Nicomorphin); im Falle der Verschiebung der funktionellen Methylgruppe von Position 3 nach 6 wird Codein zu Heterocodein, das 72-mal stärker ist und damit sechsmal stärker als Morphin
- Anbringen von funktionellen Gruppen oder andere Veränderungen an Position 14 (Oxymorphon, Oxycodon, Naloxon)
- Veränderungen an den Positionen 2, 4, 5 oder 17, in der Regel zusammen mit anderen Veränderungen des Moleküls an anderen Stellen des Morphinskeletts. Dies geschieht häufig bei Arzneimitteln, die durch katalytische Reduktion, Hydrierung, Oxidation o. ä. hergestellt werden, wodurch starke Morphin- und Codeinderivate entstehen. ⓘ
Viele Morphinderivate können auch mit Thebain oder Codein als Ausgangsstoff hergestellt werden. Der Ersatz der N-Methylgruppe von Morphin durch eine N-Phenylethylgruppe führt zu einem Produkt, das in seiner opiatagonistischen Potenz 18-mal stärker ist als Morphin. Kombiniert man diese Modifikation mit dem Ersatz der 6-Hydroxyl- durch eine 6-Methylengruppe, so erhält man eine Verbindung, die etwa 1.443-mal stärker ist als Morphin und damit stärker als Bentley-Verbindungen wie Etorphin (M99, der Immobilon-Beruhigungspfeil). Eng verwandt mit Morphin sind die Opioide Morphin-N-Oxid (Genomorphin), ein nicht mehr gebräuchliches Arzneimittel, und Pseudomorphin, ein in Opium vorkommendes Alkaloid, das als Abbauprodukt des Morphins entsteht. ⓘ
Infolge der umfassenden Erforschung und Verwendung dieses Moleküls wurden seit dem letzten Viertel des 19. Jahrhunderts mehr als 250 Morphinderivate (einschließlich Codein und verwandter Medikamente) entwickelt. Jahrhunderts entwickelt. Diese Medikamente reichen von 25 % der analgetischen Stärke von Codein (oder etwas mehr als 2 % der Stärke von Morphin) bis zu mehreren Tausend Mal so stark wie Morphin, bis hin zu starken Opioid-Antagonisten, darunter Naloxon (Narcan), Naltrexon (Trexan), Diprenorphin (M5050, das Umkehrmittel für Immobilon dart) und Nalorphin (Nalline). Einige Opioid-Agonisten-Antagonisten, partielle Agonisten und inverse Agonisten werden ebenfalls von Morphin abgeleitet. Das Rezeptor-Aktivierungsprofil der halbsynthetischen Morphinderivate ist sehr unterschiedlich, und einige, wie Apomorphin, haben keine narkotische Wirkung. ⓘ
Salze
Sowohl Morphin als auch seine hydratisierte Form sind in Wasser nur schwer löslich. Aus diesem Grund stellen pharmazeutische Unternehmen Sulfat- und Hydrochloridsalze der Droge her, die beide mehr als 300-mal wasserlöslicher sind als das Ausgangsmolekül. Während der pH-Wert einer gesättigten Morphinhydratlösung 8,5 beträgt, sind die Salze sauer. Da sie sich von einer starken Säure, aber schwachen Base ableiten, liegen sie beide bei etwa pH = 5; daher werden die Morphinsalze mit geringen Mengen NaOH gemischt, um sie für die Injektion geeignet zu machen. ⓘ
Es wird eine Reihe von Morphinsalzen verwendet, von denen Hydrochlorid, Sulfat, Tartrat und Citrat die gebräuchlichsten sind; seltener sind Methobromid, Hydrobromid, Hydrojodid, Laktat, Chlorid und Bitartrat sowie die anderen unten aufgeführten. Morphin-Diacetat (Heroin) ist kein Salz, sondern ein weiteres Derivat, siehe oben. ⓘ
Morphinmeconat ist eine wichtige Form des Alkaloids im Mohn, ebenso wie Morphinpektinat, -nitrat, -sulfat und einige andere. Wie Codein, Dihydrocodein und andere (vor allem ältere) Opiate wurde Morphin von einigen Anbietern als Salicylat-Salz verwendet und kann leicht zusammengesetzt werden, was den therapeutischen Vorteil sowohl des Opioids als auch des NSAIDs mit sich bringt; in der Vergangenheit wurden auch mehrere Barbiturat-Salze von Morphin verwendet, ebenso wie Morphinvalerat, das Salz der Säure, die den Wirkstoff von Baldrian darstellt. Calciummorphenat ist das Zwischenprodukt bei verschiedenen Methoden der Morphinherstellung aus Latex und Mohnstroh, seltener tritt Natriummorphenat an seine Stelle. Morphinascorbat und andere Salze wie Tannat, Citrat, Acetat, Phosphat, Valerat und andere können je nach Zubereitungsmethode in Mohntee enthalten sein. ⓘ
Die von der United States Drug Enforcement Administration für Meldezwecke aufgelisteten Salze sind neben einigen anderen wie folgt:
| Ausgewählte Morphinsalze mit ihrer CSA-Liste (Controlled Substances Act), der ACSCN (Administrative Controlled Substances Code Number) und dem Umwandlungsverhältnis der freien Basen. ⓘ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
Herstellung

Im Schlafmohn sind die Alkaloide an Meconsäure gebunden. Die Methode besteht darin, die zerkleinerte Pflanze mit verdünnter Schwefelsäure zu extrahieren, die eine stärkere Säure als Meconsäure ist, aber nicht so stark, dass sie mit den Alkaloidmolekülen reagiert. Die Extraktion erfolgt in mehreren Schritten (eine Menge zerkleinerter Pflanzen wird mindestens sechs- bis zehnmal extrahiert, so dass praktisch jedes Alkaloid in die Lösung gelangt). Aus der im letzten Extraktionsschritt erhaltenen Lösung werden die Alkaloide entweder mit Ammoniumhydroxid oder Natriumcarbonat ausgefällt. Der letzte Schritt ist die Reinigung und Abtrennung des Morphins von den anderen Opiumalkaloiden. Das etwas ähnliche Gregory-Verfahren wurde während des Zweiten Weltkriegs im Vereinigten Königreich entwickelt. Es beginnt mit dem Einkochen der gesamten Pflanze, in den meisten Fällen mit Ausnahme der Wurzeln und Blätter, in einfachem oder leicht gesäuertem Wasser und durchläuft dann die Schritte der Konzentration, Extraktion und Reinigung der Alkaloide. Andere Methoden zur Verarbeitung von "Mohnstroh" (d. h. getrocknete Schoten und Stängel) verwenden Dampf, eine oder mehrere Arten von Alkohol oder andere organische Lösungsmittel. ⓘ
Die Mohnstrohmethoden überwiegen in Kontinentaleuropa und im Britischen Commonwealth, während die Latexmethode in Indien am weitesten verbreitet ist. Bei der Latex-Methode werden die unreifen Schoten entweder vertikal oder horizontal mit einem Messer mit zwei bis fünf Klingen und einem speziell für diesen Zweck entwickelten Schutz bis auf den Bruchteil eines Millimeters aufgeschnitten, wobei die Schoten bis zu fünfmal eingeritzt werden können. Eine alternative Latex-Methode, die in China in der Vergangenheit manchmal angewandt wurde, besteht darin, die Mohnköpfe abzuschneiden, mit einer großen Nadel durchzustechen und den getrockneten Milchsaft 24 bis 48 Stunden später aufzufangen. ⓘ
In Indien wird das von lizenzierten Mohnbauern geerntete Opium in staatlichen Verarbeitungszentren auf einen einheitlichen Wassergehalt getrocknet und dann an Pharmaunternehmen verkauft, die daraus Morphin gewinnen. In der Türkei und in Tasmanien hingegen wird Morphin durch Ernte und Verarbeitung der voll ausgereiften trockenen Samenschoten mit den daran befestigten Stängeln, dem so genannten Mohnstroh, gewonnen. In der Türkei wird ein Wasserextraktionsverfahren angewandt, während in Tasmanien ein Lösungsmittelextraktionsverfahren verwendet wird. ⓘ
Schlafmohn enthält mindestens 50 verschiedene Alkaloide, von denen die meisten jedoch nur eine sehr geringe Konzentration aufweisen. Morphin ist das Hauptalkaloid im Rohopium und macht etwa 8-19 % des Trockengewichts des Opiums aus (je nach Anbaubedingungen). Einige eigens entwickelte Mohnsorten produzieren heute Opium mit einem Morphingehalt von bis zu 26 % des Gewichts. Eine grobe Faustregel zur Bestimmung des Morphingehalts von pulverisiertem, getrocknetem Mohnstroh besteht darin, den für den Stamm oder die Pflanze nach der Latex-Methode erwarteten Prozentsatz durch acht oder einen empirisch ermittelten Faktor zu teilen, der häufig im Bereich von 5 bis 15 liegt. Der Norman-Stamm von P. Somniferum, der ebenfalls in Tasmanien entwickelt wurde, produziert bis zu 0,04 % Morphin, jedoch mit viel höheren Mengen an Thebain und Oripavin, die zur Synthese halbsynthetischer Opioide sowie anderer Arzneimittel wie Stimulanzien, Brechmittel, Opioidantagonisten, Anticholinergika und Wirkstoffe für die glatte Muskulatur verwendet werden können. ⓘ
In den 1950er und 1960er Jahren lieferte Ungarn fast 60 % der gesamten Morphinproduktion für medizinische Zwecke in Europa. Bis heute ist der Mohnanbau in Ungarn legal, allerdings ist die Anbaufläche per Gesetz auf 8.100 m2 begrenzt. Auch der Verkauf von getrocknetem Mohn in Blumenläden zur Verwendung in Gestecken ist legal. ⓘ
1973 wurde bekannt gegeben, dass ein Team an den National Institutes of Health in den Vereinigten Staaten eine Methode zur Totalsynthese von Morphin, Codein und Thebain unter Verwendung von Steinkohlenteer als Ausgangsstoff entwickelt hatte. Auslöser für die Forschungen war ein Mangel an Hustenstillern der Codein-Hydrocodon-Klasse (die alle in einem oder mehreren Schritten aus Morphin, aber auch aus Codein oder Thebain hergestellt werden können). ⓘ
Der größte Teil des weltweit für pharmazeutische Zwecke hergestellten Morphins wird in Kodein umgewandelt, da die Konzentration von Kodein sowohl im Rohopium als auch im Mohnstroh viel geringer ist als die von Morphin; in den meisten Ländern ist die Verwendung von Kodein (sowohl als Endprodukt als auch als Vorprodukt) gewichtsmäßig mindestens genauso hoch oder höher als die von Morphin. ⓘ


Morphin wird aus Opium, d. h. aus dem getrockneten Milchsaft des Schlafmohns (Papaver somniferum), gewonnen; der Morphinanteil im Opium liegt bei etwa zwölf Prozent, schwankt aber abhängig von der Herkunft und Vorbehandlung des Milchsafts deutlich. ⓘ
Die Biosynthese von Morphin – und auch aller anderen natürlich vorkommender Opiumalkaloide – erfolgt aus dem Isochinolin-Alkaloid Reticulin. ⓘ
Die Totalsynthese, die 1956 Marshall D. Gates und Gilg Tschudi gelang, ist aufwändig und liefert nur geringe Ausbeuten – bei der Fuchs-Synthese beträgt sie etwa zehn Prozent. Die Ausgangsstoffe dazu sind Phenylalanin und 4-Hydroxyphenyl-acetaldehyd. Dabei ist Norcoclaurin ein wichtiges Zwischenprodukt. Über Reticulin werden dann die Morphinan-Alkaloide gebildet, zu denen das Morphin gehört. ⓘ
Die Rice-Synthese erreicht Ausbeuten von 30 % über 14 Schritte:
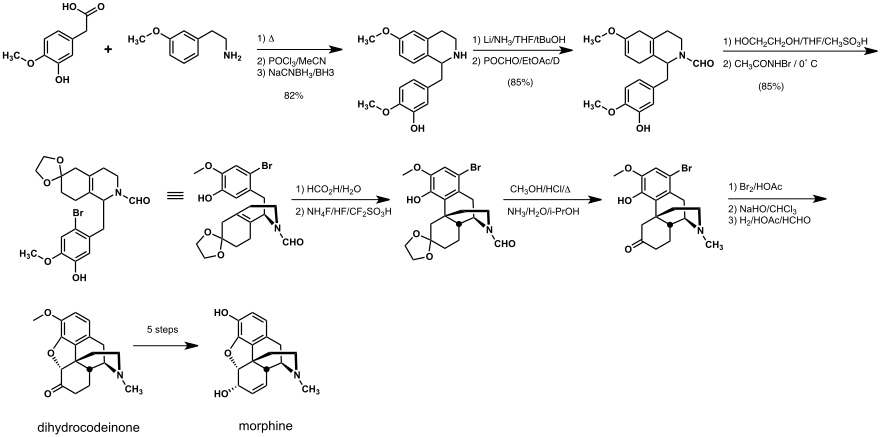
Chemische Synthese
Die erste Morphin-Totalsynthese, die 1952 von Marshall D. Gates, Jr. entwickelt wurde, ist nach wie vor ein weit verbreitetes Beispiel für eine Totalsynthese. Mehrere andere Synthesen wurden berichtet, insbesondere von den Forschungsgruppen von Rice, Evans, Fuchs, Parker, Overman, Mulzer-Trauner, White, Taber, Trost, Fukuyama, Guillou und Stork. Aufgrund der stereochemischen Komplexität und der daraus resultierenden synthetischen Herausforderung, die diese polyzyklische Struktur darstellt, hat Michael Freemantle die Ansicht geäußert, dass es "höchst unwahrscheinlich" ist, dass eine chemische Synthese jemals so kosteneffizient sein wird, dass sie mit den Kosten für die Herstellung von Morphin aus Schlafmohn konkurrieren könnte. ⓘ
Ausgangsstoff für andere Opioide
Pharmazeutische
Morphin ist eine Vorstufe für die Herstellung einer Reihe von Opioiden wie Dihydromorphin, Hydromorphon, Hydrocodon und Oxycodon sowie Codein, das selbst eine große Familie halbsynthetischer Derivate hat. ⓘ
Illegales
Illegales Morphin wird, wenn auch selten, aus Codein hergestellt, das in frei verkäuflichen Husten- und Schmerzmitteln enthalten ist. Eine weitere illegale Quelle ist Morphin, das aus Morphinprodukten mit verlängerter Wirkstofffreisetzung extrahiert wird. Durch chemische Reaktionen können dann Morphin, Dihydromorphin und Hydrocodon in Heroin oder andere Opioide umgewandelt werden [z. B. Diacetyldihydromorphin (Paralaudin) und Thebacon]. Andere illegale Umwandlungen von Morphin in Ketone der Hydromorphonklasse oder andere Derivate wie Dihydromorphin (Paramorfan), Desomorphin (Permonid), Metopon usw. und von Codein in Hydrocodon (Dicodid), Dihydrocodein (Paracodin) usw. erfordern größere Fachkenntnisse sowie Arten und Mengen von Chemikalien und Ausrüstung, die schwieriger zu beschaffen sind, und werden daher seltener illegal verwendet (es wurden jedoch Fälle gemeldet). ⓘ
Geschichte

Ein Elixier auf Opiumbasis wird den Alchemisten der byzantinischen Zeit zugeschrieben, aber die genaue Rezeptur ging bei der osmanischen Eroberung Konstantinopels (Istanbul) verloren. Um 1522 erwähnte Paracelsus ein Elixier auf Opiumbasis, das er Laudanum nannte, abgeleitet von dem lateinischen Wort laudāre, was "loben" bedeutet. Die angegebene Rezeptur unterscheidet sich erheblich von der des heutigen Laudanums. ⓘ
Morphin wurde als erstes aktives Alkaloid, das aus der Schlafmohnpflanze extrahiert wurde, im Dezember 1804 in Paderborn vom deutschen Apotheker Friedrich Sertürner entdeckt. Im Jahr 1817 berichtete Sertürner von Experimenten, bei denen er sich selbst, drei Jungen, drei Hunden und einer Maus Morphin verabreichte; alle vier Personen starben fast. Ursprünglich hatte Sertürner die Substanz Morphium nach dem griechischen Gott der Träume, Morpheus, benannt, da sie dazu neigt, Schlaf zu verursachen. Sertürners Morphium war sechsmal stärker als Opium. Er stellte die Hypothese auf, dass die Droge weniger süchtig machen würde, weil sie in geringerer Dosis verabreicht werden müsste. Sertürner wurde jedoch süchtig nach der Droge und warnte: "Ich halte es für meine Pflicht, auf die schrecklichen Wirkungen dieser neuen Substanz, die ich Morphium nenne, aufmerksam zu machen, damit Unheil abgewendet werden kann." ⓘ
Die Droge wurde 1817 von der Firma Sertürner und Co. als Schmerzmittel sowie als Mittel gegen Opium- und Alkoholsucht auf den Markt gebracht. Als Gift wurde es erstmals 1822 eingesetzt, als der französische Arzt Edme Castaing wegen Mordes an einem Patienten verurteilt wurde. Die kommerzielle Produktion begann 1827 in Darmstadt, Deutschland, durch die Apotheke, aus der das Pharmaunternehmen Merck hervorging, wobei der Verkauf von Morphin einen großen Anteil an ihrem frühen Wachstum hatte. In den 1850er Jahren berichtete Alexander Wood, dass er seiner Frau Rebecca zu Versuchszwecken Morphium injiziert hatte; der Mythos besagt, dass sie daran wegen Atemdepression starb, aber sie überlebte ihren Mann um zehn Jahre. ⓘ
Später stellte man fest, dass Morphium stärker süchtig macht als Alkohol oder Opium, und sein extensiver Gebrauch während des amerikanischen Bürgerkriegs führte angeblich dazu, dass über 400 000 Menschen an der "Soldatenkrankheit" der Morphiumsucht erkrankten. Diese Idee war Gegenstand einer Kontroverse, da es Hinweise darauf gab, dass eine solche Krankheit in Wirklichkeit eine Erfindung war; die erste dokumentierte Verwendung des Begriffs "Soldatenkrankheit" stammt aus dem Jahr 1915. ⓘ
Diacetylmorphin (besser bekannt als Heroin) wurde 1874 aus Morphin synthetisiert und 1898 von Bayer auf den Markt gebracht. Heroin ist im Verhältnis zum Gewicht etwa 1,5 bis 2 Mal stärker als Morphin. Aufgrund der Lipidlöslichkeit von Diacetylmorphin kann es die Blut-Hirn-Schranke schneller überwinden als Morphin, wodurch die verstärkende Komponente der Sucht verstärkt wird. Anhand verschiedener subjektiver und objektiver Messgrößen wurde in einer Studie die relative Potenz von Heroin im Vergleich zu Morphin bei intravenöser Verabreichung an Post-Süchtige auf 1,80-2,66 mg Morphinsulfat zu 1 mg Diamorphinhydrochlorid (Heroin) geschätzt. ⓘ

Mit dem Harrison Narcotics Tax Act von 1914 wurde Morphin in den USA zu einer kontrollierten Substanz, und der Besitz ohne Rezept ist in den USA eine Straftat. Morphin war das weltweit am häufigsten missbrauchte narkotische Analgetikum, bis Heroin synthetisiert wurde und in Gebrauch kam. Im Allgemeinen wurde bis zur Synthese von Dihydromorphin (ca. 1900), der Dihydromorphinon-Klasse der Opioide (1920er Jahre) und Oxycodon (1916) und ähnlicher Drogen gab es keine anderen Drogen in demselben Wirkungsspektrum wie Opium, Morphin und Heroin, Synthetische Drogen waren noch einige Jahre entfernt (Pethidin wurde 1937 in Deutschland erfunden), und zu den halbsynthetischen Opioid-Agonisten gehörten Analoga und Derivate von Codein wie Dihydrocodein (Paracodin), Ethylmorphin (Dionin) und Benzylmorphin (Peronin). Auch heute noch ist Morphin das von Heroinabhängigen am häufigsten nachgefragte verschreibungspflichtige Rauschgift, wenn Heroin knapp ist; unter den örtlichen Gegebenheiten und der Vorliebe der Konsumenten können Hydromorphon, Oxymorphon, hochdosiertes Oxycodon oder Methadon sowie in bestimmten Fällen, z. B. in den 1970er Jahren in Australien, Dextromoramid diese Liste anführen. Die von der größten absoluten Zahl der Heroinsüchtigen konsumierten Drogen sind wahrscheinlich Codein, wobei auch Dihydrocodein, Mohnstrohderivate wie Mohnschoten- und Mohntee, Propoxyphen und Tramadol in erheblichem Umfang verwendet werden. ⓘ
Die Strukturformel von Morphin wurde 1925 von Robert Robinson bestimmt. Mindestens drei Methoden der Totalsynthese von Morphin aus Ausgangsstoffen wie Steinkohlenteer und Erdöldestillaten wurden patentiert, die erste davon wurde 1952 von Dr. Marshall D. Gates, Jr. an der Universität von Rochester angemeldet. Der überwiegende Teil des Morphins wird jedoch aus dem Schlafmohn gewonnen, und zwar entweder durch die traditionelle Methode der Gewinnung von Milchsaft aus den zerkratzten, unreifen Schoten des Mohns oder durch Verfahren, bei denen Mohnstroh, die getrockneten Schoten und Stängel der Pflanze, verwendet werden. Das am weitesten verbreitete Verfahren wurde 1925 in Ungarn erfunden und 1930 von dem ungarischen Pharmakologen János Kabay angekündigt. ⓘ
Im Jahr 2003 wurde entdeckt, dass endogenes Morphin im menschlichen Körper natürlich vorkommt. Dreißig Jahre lang wurde über dieses Thema spekuliert, weil es einen Rezeptor gab, der offenbar nur auf Morphin reagierte: den μ3-Opioidrezeptor im menschlichen Gewebe. Man hat festgestellt, dass menschliche Zellen, die sich als Reaktion auf krebsartige Neuroblastomzellen bilden, Spuren von endogenem Morphin enthalten. ⓘ
Gesellschaft und Kultur
Rechtlicher Status
- In Australien ist Morphin nach den unterschiedlich betitelten Giftgesetzen der Bundesstaaten und Territorien als Droge der Liste 8 eingestuft.
- In Kanada ist Morphin im Rahmen des Controlled Drugs and Substances Act als Droge der Liste I eingestuft.
- In Frankreich steht Morphin auf der Grundlage des französischen Gesetzes über kontrollierte Substanzen vom Dezember 1970 in der strengsten Liste der kontrollierten Substanzen.
- In Deutschland ist Morphin ein verkehrsfähiges und verschreibungsfähiges Betäubungsmittel, das in Anlage III (entspricht CSA Schedule II) des Betäubungsmittelgesetzes aufgeführt ist.
- In der Schweiz ist Morphin ähnlich eingestuft wie in Deutschland.
- In Japan ist Morphin nach dem Gesetz zur Kontrolle von Betäubungsmitteln und Psychopharmaka (麻薬及び向精神薬取締法, mayaku oyobi kōseishinyaku torishimarihō) als Betäubungsmittel eingestuft.
- In den Niederlanden wird Morphin im Rahmen des Opiumgesetzes als Droge der Liste 1 eingestuft.
- In Neuseeland ist Morphin nach dem Misuse of Drugs Act 1975 als Droge der Klasse B eingestuft.
- Im Vereinigten Königreich wird Morphin gemäß dem Misuse of Drugs Act 1971 als Droge der Klasse A und gemäß den Misuse of Drugs Regulations 2001 als kontrollierte Droge der Liste 2 eingestuft.
- In den Vereinigten Staaten ist Morphin gemäß dem Controlled Substances Act unter der Hauptverwaltungsnummer 9300 als kontrollierte Substanz der Liste II eingestuft. Morphin-Arzneimittel unterliegen jährlichen Herstellungsquoten; im Jahr 2017 betrugen diese Quoten 35,0 Tonnen für die Produktion zum Verkauf und 27,3 Tonnen für die Produktion als Zwischenprodukt oder chemischer Vorläufer zur Umwandlung in andere Drogen. Morphin, das zur Verwendung in extrem verdünnten Formulierungen hergestellt wird, ist von der Herstellungsquote ausgenommen.
- Auf internationaler Ebene (UN) wird Morphin im Rahmen des Einheitsübereinkommens über Suchtstoffe als Droge der Liste I eingestuft. ⓘ
Nichtmedizinische Verwendung

Die Euphorie, die umfassende Linderung des Leidens und damit aller Aspekte des Leidens, die Förderung der Geselligkeit und des Einfühlungsvermögens, das "körperliche Hochgefühl" und die Anxiolyse, die von Betäubungsmitteln, einschließlich der Opioide, ausgehen, können dazu führen, dass bei Abwesenheit von Schmerzen über einen längeren Zeitraum hinweg hohe Dosen eingenommen werden, was beim Konsumenten ein krankhaftes Verlangen nach der Droge auslösen kann. Als Prototyp der gesamten Opioidklasse hat Morphin Eigenschaften, die zu seinem Missbrauch führen können. Die Morphinabhängigkeit ist das Modell, auf dem die derzeitige Auffassung von Sucht beruht. ⓘ
Tier- und Humanstudien sowie klinische Erfahrungen bestätigen die Behauptung, dass Morphin eine der euphorischsten Drogen ist, die es gibt, und dass Heroin und Morphin in allen Fällen, mit Ausnahme der intravenösen Einnahme, Studien zufolge nicht zu unterscheiden sind, da Heroin ein Prodrug für die Abgabe von systemischem Morphin ist. Durch chemische Veränderungen des Morphinmoleküls entstehen andere euphorisierende Substanzen wie Dihydromorphin, Hydromorphon (Dilaudid, Hydal) und Oxymorphon (Numorphan, Opana) sowie die methylierten Äquivalente der drei letztgenannten, Dihydrocodein, Hydrocodon und Oxycodon; Neben Heroin gibt es Dipropanoylmorphin, Diacetyldihydromorphin und andere Vertreter der Kategorie der 3,6-Morphin-Diester wie Nicomorphin und andere ähnliche halbsynthetische Opiate wie Desomorphin, Hydromorphinol usw. die in vielen Ländern der Welt klinisch verwendet, aber in seltenen Fällen auch illegal hergestellt werden. ⓘ
Im Allgemeinen umfasst der nichtmedizinische Konsum von Morphin die Einnahme von mehr als der verschriebenen Menge oder außerhalb der ärztlichen Aufsicht, die Injektion oraler Formulierungen, die Mischung mit nicht zugelassenen Potenzmitteln wie Alkohol, Kokain und dergleichen oder die Umgehung des Mechanismus der verlängerten Wirkstofffreisetzung durch Kauen der Tabletten oder Umwandlung in Pulver zum Schnupfen oder zur Herstellung von Injektionspräparaten. Die letztgenannte Methode kann ebenso zeitaufwändig und kompliziert sein wie das traditionelle Rauchen von Opium. Dies und die Tatsache, dass die Leber einen großen Prozentsatz der Droge beim ersten Durchgang zerstört, wirkt sich auf die Nachfrageseite der Gleichung für die illegalen Wiederverkäufer aus, da viele Kunden keine Nadel verwenden und von der oralen Einnahme der Droge enttäuscht waren. Da Morphin in vielen Fällen genauso schwer oder noch schwerer zu beschaffen ist als Oxycodon, ist Morphin in jeglicher Form auf der Straße unüblich, obwohl Ampullen und Ampullen mit Morphininjektionen, reines pharmazeutisches Morphinpulver und lösliche Mehrzwecktabletten sehr beliebt sind, wenn sie verfügbar sind. ⓘ
Morphin ist auch in Form einer Paste erhältlich, die bei der Herstellung von Heroin verwendet wird und entweder geraucht oder in ein lösliches Salz umgewandelt und injiziert werden kann; dasselbe gilt für die vorletzten Produkte des Kompot- (polnisches Heroin) und Schwarzteerverfahrens. Sowohl aus Mohnstroh als auch aus Opium kann Morphin in Reinheitsgraden gewonnen werden, die von Mohntee bis hin zu Morphin in nahezu pharmazeutischer Qualität reichen, und zwar sowohl allein als auch in Verbindung mit mehr als 50 anderen Alkaloiden. Es ist auch der aktive narkotische Wirkstoff in Opium und allen seinen Formen, Derivaten und Analoga und entsteht bei der Zersetzung von Heroin und ist in vielen Chargen von illegalem Heroin als Ergebnis unvollständiger Acetylierung enthalten. ⓘ
Bezeichnungen
Morphin wird unter vielen verschiedenen Markennamen in verschiedenen Teilen der Welt vermarktet. Im britischen Englisch wurde es früher Morphia genannt. ⓘ
Zu den informellen Bezeichnungen für Morphin gehören: Cube Juice, Dope, Dreamer, Emsel, First Line, God's Drug, Hard Stuff, Hocus, Hows, Lydia, Lydic, M, Miss Emma, Mister Blue, Monkey, Morf, Morph, Morphide, Morphie, Morpho, Mother, MS, Ms. Emma, Mud, New Jack Swing (wenn mit Heroin gemischt), Sister, Tab, Unkie, Unkie White und Stuff. ⓘ
MS Contin-Tabletten sind als Misties bekannt, die 100-mg-Tabletten mit verlängerter Wirkstofffreisetzung als Greys und Blockbusters. Der "Speedball" kann Morphin als Opioidkomponente enthalten, das mit Kokain, Amphetaminen, Methylphenidat oder ähnlichen Drogen kombiniert wird. "Blue Velvet" ist eine Kombination von Morphin mit dem Antihistaminikum Tripelennamin (Pyrabenzamin, PBZ, Pelamin), die als Injektion verabreicht wird, oder seltener die Mischung, wenn sie geschluckt oder als Retentionsklistier verwendet wird; der Name bezieht sich auch auf eine Kombination aus Tripelennamin und Dihydrocodein oder Codein-Tabletten oder -Sirup, die oral eingenommen werden. "Morphia" ist eine ältere offizielle Bezeichnung für Morphin, die auch als Slang-Bezeichnung verwendet wird. "Driving Miss Emma" ist die intravenöse Verabreichung von Morphin. Mehrzwecktabletten (leicht lösliche subkutane Tabletten, die auch geschluckt oder unter der Zunge oder zwischen Wange und Kiefer aufgelöst werden können) sind ebenso wie einige Hydromorphonmarken als "Shake & Bake" oder "Shake & Shoot" bekannt. ⓘ
Morphin kann geraucht werden, insbesondere Diacetylmorphin (Heroin), wobei die häufigste Methode die "Chasing The Dragon"-Methode ist. Die Acetylierung, mit der Morphin unmittelbar vor dem Konsum in Heroin und verwandte Drogen umgewandelt wird, wird als AAing (für Acetic Anhydride) oder Home-Bake bezeichnet, und das Ergebnis des Verfahrens ist auch als Home-Bake oder Blue Heroin bekannt (nicht zu verwechseln mit Blue Magic Heroin oder dem als Blue Morphine oder Blue Morphone bekannten Linctus oder der oben beschriebenen Blue Velvet-Mischung). ⓘ
Zugang in Entwicklungsländern
Obwohl Morphin billig ist, haben Menschen in ärmeren Ländern oft keinen Zugang dazu. Nach einer Schätzung des Internationalen Suchtstoffkontrollamtes aus dem Jahr 2005 verbrauchen sechs Länder (Australien, Kanada, Frankreich, Deutschland, das Vereinigte Königreich und die Vereinigten Staaten) 79 % des weltweiten Morphins. Die weniger wohlhabenden Länder, in denen 80 % der Weltbevölkerung leben, verbrauchen nur etwa 6 % des weltweiten Morphinangebots. Einige Länder führen praktisch kein Morphin ein, und in anderen Ländern ist das Medikament selbst zur Linderung starker Schmerzen im Sterben kaum erhältlich. ⓘ
Experten für Schmerztherapie führen die Unterversorgung mit Morphin auf die ungerechtfertigte Angst vor dem Sucht- und Missbrauchspotenzial der Droge zurück. Obwohl Morphin eindeutig süchtig macht, sind westliche Ärzte der Meinung, dass es sich lohnt, das Medikament zu verwenden und den Patienten nach Beendigung der Behandlung wieder abzusetzen. ⓘ
Gewinnung
Dem wässrigen Opiumauszug wird eine Calciumchloridlösung zugesetzt. Nach Abtrennung des mekonsauren Calciums wird die Lösung eingedampft, wobei sich Morphin und Codein als Hydrochloride abscheiden. Die Hydrochloride werden erneut in eine wässrige Lösung gebracht, aus welcher das Morphin durch Zugabe von Ammoniak ausgefällt werden kann. ⓘ
Heroin ist ein Derivat des Morphins: 3,6-Diacetylmorphin. Es wird durch eine chemische Reaktion (Acetylierung) aus Morphin gewonnen. ⓘ
Chemische Eigenschaften
Morphin ist schwer löslich in Wasser (1:5000), etwas leichter löslich in heißem Wasser, löslich in Ethanol (1:250), schwer löslich in Ether (1:7500), in Tetrachlorkohlenstoff (1:6400), leicht löslich in alkalihaltigem Wasser. ⓘ
Morphin ist in stark saurem und in alkalischem Milieu instabil. Starke Säuren lagern es zu Apomorphin um. ⓘ
Auf Grund der schlechten Wasserlöslichkeit von Morphin werden arzneilich vor allem das Sulfat (etwa als Morphinsulfat-Tablette, MST) und das Hydrochlorid des Morphins eingesetzt, deren Wasserlöslichkeit deutlich, d. h. etwa 300-mal, besser ist als das der reinen Base. Nach der Entdeckung der schmerzstillenden Wirkung des Morphins stellte über lange Zeit die schlechte Löslichkeit von Morphin ein ernsthaftes Problem dar, da zu Injektionszwecken eine wässrige Lösung nötig ist. ⓘ
Analytik
Zur zuverlässigen qualitativen und quantitativen Bestimmung von Morphin in unterschiedlichen Untersuchungsgütern wie z. B. Urin, Blut, Blutserum, Blutplasma, Haaren oder pflanzlichem Material sind adäquate Probenvorbereitungsmethoden wie z. B. Extraktionsverfahren oder die SPE erforderlich. Die gewonnenen Extrakte können durch Einsatz der Kopplung chromatographischer Trennverfahren wie z. B. der Gaschromatographie oder HPLC mit der Massenspektrometrie analysiert werden. Die Verfahren eignen sich auch zum Einsatz bei speziellen forensischen Fragestellungen wie z. B. des Einflusses des Genusses von mohnhaltigen Produkten. ⓘ
Therapeutische Verwendung
Anwendungsgebiete
Symptomatische Therapie von Atemnot, Husten und Angst
Da Morphin auch dämpfend auf das Atemzentrum wirkt, wird es insbesondere in der Palliativmedizin zur symptomatischen Behandlung der Luftnot verwendet. Es reduziert den Atemantrieb, senkt damit den Stresspegel des Patienten, die Atmung wird ruhiger und ökonomischer, indem die durch hochfrequente, jedoch flache Atmung entstandene Totraumventilation reduziert wird. Eine Zulassung für diese Therapie hat Morphin nicht, so dass sie im Off-Label-Use durchgeführt wird. Morphin unterdrückt den Hustenreiz (antitussive Wirkung); ein anderes Alkaloid des Opiums, Codein (chemisch gesehen Methylmorphin), wird daher als Wirkstoff gegen Husten eingesetzt. In der Akutmedizin wird Morphin auch zur Symptomlinderung bei akutem Herzinfarkt (siehe dort) eingesetzt, um den Circulus vitiosus aus Schmerzen, Luftnot, Angst, psychischem und körperlichem Stress mit Zunahme des Sauerstoffverbrauchs des Herzens zu unterbinden. Außerdem senkt Morphin durch Dilatation der venösen Kapazitätsgefäße die Vorlast und durch leichte arterielle Dilatation auch die Nachlast des Herzens. Morphin bewirkt zudem eine vermehrte Histaminausschüttung, durch die der Blutdruck sinken kann. ⓘ
Substitutionsbehandlung
Ferner wird Morphin in der Substitutionsbehandlung (Erhaltungstherapie) von Erwachsenen mit Opioidabhängigkeit verwendet. Die Verabreichung erfolgt im Rahmen medizinischer und umfassender psychosozialer Maßnahmen mit einem oral wirksamen Präparat, das den Wirkstoff verzögert abgibt, so dass eine lang anhaltende Wirkung (Retardwirkung) resultiert. ⓘ
In Deutschland wurde Morphin in dieser Indikation im April 2015 im Markt eingeführt (Handelsname Substitol). Die Zulassungsstudie wurde von 2008 bis 2010 an Zentren in der Schweiz und in Deutschland durchgeführt; als Vergleichssubstanz diente DL-Methadon. In Österreich wird retardiertes orales Morphin bereits seit längerem in der Substitutionsbehandlung eingesetzt. In der Schweiz ist orales retardiertes Morphin (Sevre-Long) seit 2013 zugelassen. ⓘ
Nebenwirkungen

Wie bei allen stark wirkenden Opioid-Analgetika können Obstipation (Verstopfung), Übelkeit und Erbrechen auftreten. Ebenso kann es zu Benommenheit, Stimmungsveränderungen sowie zu Veränderungen des Hormonsystems und des autonomen Nervensystems kommen. Bei Überdosierung kann es zu Miosis, Hypoventilation und niedrigem Blutdruck kommen. ⓘ
Zu Beginn der Morphintherapie kann es zu Übelkeit und Erbrechen kommen, da Morphin direkt auf das Brechzentrum im Hirnstamm wirkt. Nach einiger Zeit lässt diese Nebenwirkung meist nach. Einzig die Obstipation unterliegt keiner Gewöhnung. Bei einer Langzeitanwendung sollte daher ein Abführmittel mitverordnet werden. ⓘ
Grundsätzlich gilt die Fahrtüchtigkeit als eingeschränkt. Insbesondere bei einer Neueinstellung oder Therapieumstellung ist ein Fahrverbot auszusprechen, jedoch scheint nach einer angemessenen Einstellung mit retardierten Opioiden die Fahrtüchtigkeit nicht wesentlich beeinträchtigt zu sein. ⓘ
Aufgrund der euphorisierenden Wirkung wird Morphin insbesondere bei Anwendung schnell anflutender Medikamentenformen (Tropfen, nicht retardierte Tabletten, Injektionslösung) ein hohes Suchtpotential zugeschrieben. Eine Schmerzbehandlung mit Opioiden führt nicht grundsätzlich zu einer Suchtentwicklung. Allerdings kann es zu einer Toleranzentwicklung kommen, die bei erneut auftretenden Beschwerden eine weitere Dosisanpassung erfordert. ⓘ
Des Weiteren besteht bei Morphin (im Vergleich etwa zu Fentanyl oder Sufentanil) die Gefahr einer Histaminausschüttung. ⓘ
Überdosierung
Die Hauptgefahr bei der Überdosierung mit Morphin und anderen Opioiden ist die Dämpfung des Atemzentrums (Atemdepression), die zur Bewusstlosigkeit und schließlich zu einem Atemstillstand führen kann. Eine Überdosierung mit Morphin (und anderen Opioiden) zeigt sich u. a. an einer vertieften und von der Frequenz her verminderten Atmung mit nur noch wenigen Atemzügen pro Minute. Bei noch ansprechbaren Patienten mit einer derart verminderten Atmung kann die ständig zu wiederholende Aufforderung, regelmäßig zu atmen, lebensrettend sein (sogenannte Kommandoatmung). Bei Verdacht auf das Vorliegen einer Morphinvergiftung muss ein Notarzt hinzugezogen werden, der als wichtigste Maßnahme für eine Wiederherstellung und Aufrechterhaltung der Atmung sorgt. Eine Morphinintoxikation kann durch die Gabe von Naloxon (oder dem Tartrat von 3-Hydroxy-Nor-Allylmorphin mit dem Präparat Lorfan) behandelt werden. Naloxon wirkt als kompetitiver Antagonist, verdrängt Morphin von den Opioidrezeptoren und hebt dadurch dessen Wirkung auf. Die Halbwertszeit von Naloxon liegt deutlich unter jener von Morphin, so dass der Patient zwar kurzzeitig beschwerdefrei ist, aber nach dem Nachlassen der Wirkung des Naloxons wieder Atemstillstand durch die Opiatüberdosierung droht. Wird zu viel Naloxon verabreicht, kann ein morphinabhängiger Patient von der Überdosis direkt in den Entzug übergehen. ⓘ
Die für einen durchschnittlichen Erwachsenen (ohne vorherige Toleranzentwicklung) tödliche Morphindosis liegt bei oraler Aufnahme (Einnahme) bei 200 mg (bis 1500 mg bei Menschen mit einer herausgebildeten Toleranz), nach parenteraler Applikation (Injektion, Infusion) bei 100 mg. Allerdings können – insbesondere bei intravenöser Gabe (Injektion in die Vene) – auch schon deutlich niedrigere Dosen lebensbedrohlich sein. Für Säuglinge können schon zwei bis drei Tropfen Opiumtinktur tödlich sein. ⓘ
Eine 2013 veröffentlichte Studie zeigte, dass es in der Zeit von 1999 bis 2012 in den USA zu einer Vervierfachung von opioidinduzierten Sterbefällen durch Überdosierung im Rahmen einer Schmerztherapie kam. Parallel dazu fand sich eine Vervierfachung der Opioidverschreibungen in Folge der Bemühungen um eine bessere Schmerztherapie. Als Faktoren eines Opioidmissbrauchs bis hin zur Überdosierung fanden sich u. a. auf Seiten der Patienten eine vorbekannte Neigung zu Medikamenten- oder Alkoholmissbrauch, auf ärztlicher Seite eine zu unkritische Dauerverordnung von Opioiden nach chirurgischen Eingriffen oder bei nicht-tumorbedingten Schmerzen. ⓘ
Bei richtiger Anwendung von Opioiden ist aber kein einziger Todesfall in der Literatur beschrieben; Opioide gelten in der Schmerztherapie als sicherer im Vergleich zu anderen Analgetika wie ASS, Metamizol, COX-Inhibitoren und Paracetamol. ⓘ
Handelsnamen und Darreichungsformen

Arzneilich verwendet wird Morphin in Form des Morphinsulfat-Pentahydrats oder als Morphinhydrochlorid-Trihydrat.
- Fertigarzneimittel
- Capros (D), Compensan (A), Kapanol (D, CH), M-beta (D), M-long (D), Morixon (D), Morphanton (D), MSI (D), MSI Mundipharma Morphin Merck, MSR (D), MSR Mundipharma, MST (D), Mundidol (A), M-retard (CH), M-Stada (D), MST-Continus (D, CH), MST-Mundipharma, MST-Retardgranulat, Painbreak (D), Sevredol (D, CH), Sevre-Long (CH), Substitol (A, D), Vendal (A), und andere. ⓘ
Als Darreichungsformen gibt es schnell- und langsam freisetzende Medikamente in Form von Kapseln, Tabletten, Brausetabletten, Tropfen, Granulaten, Zäpfchen (etwa MSR: Abkürzung für „Morphinsulfat rektal“) sowie Injektionslösungen (MSI = Morphinsulfat per injectionem). Mit der umgangssprachlichen Bezeichnung „Morphinpflaster“ sind transdermale Pflaster mit anderen Opioiden (Fentanyl, Buprenorphin) gemeint. ⓘ


