Gaschromatographie
 Ein Gaschromatograph mit einem Headspace-Sampler | |
| Akronym | GC |
|---|---|
| Klassifizierung | Chromatographie |
| Analyten | Organisch Anorganisch Muss flüchtig sein |
| Andere Techniken | |
| Verwandte | Dünnschichtchromatographie Hochleistungs-Flüssigkeitschromatographie |
| Bindestrich | Gaschromatographie-Massenspektrometrie |
Die Gaschromatographie () ist eine in der analytischen Chemie übliche Art der Chromatographie zur Trennung und Analyse von Verbindungen, die ohne Zersetzung verdampft werden können. Typische Anwendungen der GC sind die Prüfung der Reinheit einer bestimmten Substanz oder die Trennung der verschiedenen Komponenten eines Gemischs. In der präparativen Chromatografie kann die GC zur Herstellung reiner Verbindungen aus einem Gemisch verwendet werden. ⓘ
Die Gaschromatographie wird manchmal auch als Dampfphasenchromatographie (VPC) oder Gas-Flüssigkeits-Verteilungschromatographie (GLPC) bezeichnet. Diese alternativen Bezeichnungen sowie ihre jeweiligen Abkürzungen werden in der wissenschaftlichen Literatur häufig verwendet. ⓘ
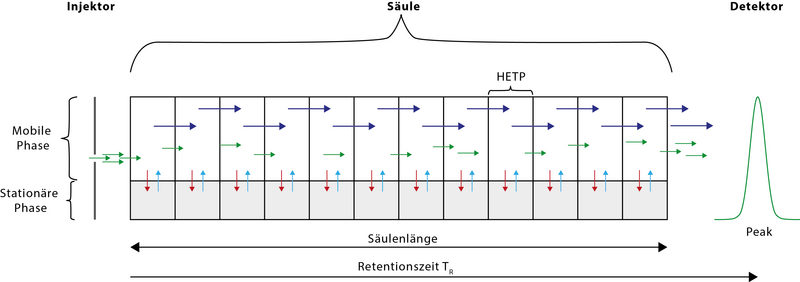
Bei der Gaschromatografie werden Verbindungen in einem Gemisch getrennt, indem eine gasförmige oder flüssige Probe in eine mobile Phase, in der Regel das Trägergas, injiziert und das Gas durch eine stationäre Phase geleitet wird. Bei der mobilen Phase handelt es sich in der Regel um ein Inertgas oder ein nicht reaktives Gas wie Helium, Argon, Stickstoff oder Wasserstoff. Die stationäre Phase ist eine mikroskopisch kleine Schicht einer viskosen Flüssigkeit auf einer Oberfläche von Feststoffpartikeln auf einem inerten festen Träger in einem Glas- oder Metallrohr, das als Säule bezeichnet wird. In einigen Säulen kann auch die Oberfläche der Feststoffteilchen als stationäre Phase dienen. Die Glas- oder Metallsäule, durch die die Gasphase strömt, befindet sich in einem Ofen, in dem die Temperatur des Gases geregelt werden kann, und der aus der Säule austretende Eluent wird von einem computergesteuerten Detektor überwacht. ⓘ

Diese Trennsäule besteht entweder aus Metall (bei älteren Modellen), heute aber überwiegend aus Quarzglas, das zur Erhöhung der Bruchsicherheit beschichtet ist. Sie ist innen mit einer definierten stationären Phase ausgekleidet (häufig mit zähflüssigen Polyorganosiloxanen) und befindet sich in einem temperierbaren Ofen. ⓘ
Nach Eingabe einer Probesubstanz, die nun vom Trägergas transportiert wird, verweilen die Komponenten je nach Polarität und Dampfdruck der einzelnen Gasmoleküle unterschiedlich lange an der stationären Phase der Säule. Ein Detektor misst den Austrittszeitpunkt am Säulenende; mit einem am Detektor angebrachten Schreiber kann dieser Zeitpunkt und die Menge der Substanz grafisch dargestellt und mit Standardsubstanzen verglichen werden. Damit ist eine sehr schnelle und leichte qualitative und quantitative Bestimmung auch sehr komplexer Stoffgemische möglich. Im Unterschied zur Hochleistungsflüssigkeitschromatographie (HPLC) sind nur ausreichend flüchtige Substanzen nachweisbar. ⓘ
Arbeitsprinzip

Ein Gaschromatograph besteht aus einem schmalen Rohr, der so genannten Säule, durch die die verdampfte Probe in einem kontinuierlichen Strom aus inertem oder nicht reaktivem Gas geleitet wird. Die Komponenten der Probe durchlaufen die Säule mit unterschiedlichen Geschwindigkeiten, abhängig von ihren chemischen und physikalischen Eigenschaften und den daraus resultierenden Wechselwirkungen mit der Säulenauskleidung oder -füllung, der so genannten stationären Phase. Die Säule befindet sich normalerweise in einem temperaturgeregelten Ofen. Wenn die Chemikalien am Ende der Säule austreten, werden sie elektronisch nachgewiesen und identifiziert. ⓘ
Geschichte

Hintergrund
Die Chromatographie geht auf die Arbeit des russischen Wissenschaftlers Mikhail Semenovich Tswett im Jahr 1903 zurück, der Pflanzenpigmente mit Hilfe der Flüssigsäulenchromatographie trennte. ⓘ
Erfindung
Die Erfindung der Gaschromatographie wird im Allgemeinen Anthony T. James und Archer J.P. Martin zugeschrieben. Ihr Gaschromatograph verwendete als Trennprinzip die Partitionschromatographie und nicht die Adsorptionschromatographie. Nach der Entwicklung des Flammenionisationsdetektors gewann die Gaschromatographie rasch an Popularität. Martin und ein anderer Kollege, Richard Synge, mit dem er 1952 den Nobelpreis für Chemie teilte, hatten in einer früheren Arbeit darauf hingewiesen, dass die Chromatographie auch zur Trennung von Gasen verwendet werden könnte. Synge widmete sich anderen Arbeiten, während Martin seine Arbeit mit James fortsetzte. ⓘ
Vorläufer der Gasadsorptionschromatographie
Die deutsche Physikalische Chemikerin Erika Cremer entwickelte 1947 zusammen mit dem österreichischen Doktoranden Fritz Prior so etwas wie den ersten Gaschromatographen, der aus einem Trägergas, einer mit Kieselgel gefüllten Säule und einem Wärmeleitfähigkeitsdetektor bestand. Sie stellten den Chromatographen auf der ACHEMA in Frankfurt aus, aber niemand interessierte sich für ihn. N.C. Turner von der Burrell Corporation stellte 1943 ein massives Gerät vor, das eine Aktivkohlesäule und Quecksilberdämpfe verwendete. Stig Claesson von der Universität Uppsala veröffentlichte 1946 seine Arbeit an einer Holzkohlesäule, die ebenfalls mit Quecksilber arbeitete. Gerhard Hesse, Professor an der Universität Marburg/Lahn, beschloss, die unter deutschen Chemikern vorherrschende Meinung zu überprüfen, dass Moleküle in einem sich bewegenden Gasstrom nicht getrennt werden könnten. Er stellte eine einfache, mit Stärke gefüllte Glassäule auf und trennte Brom und Jod erfolgreich mit Stickstoff als Trägergas. Anschließend baute er ein System, bei dem ein Inertgas durch einen mit Kieselgel gefüllten Glaskondensator strömte und die eluierten Fraktionen gesammelt wurden. Courtenay S. G. Phillips von der Universität Oxford untersuchte die Trennung in einer Holzkohlesäule mit Hilfe eines Wärmeleitfähigkeitsdetektors. Er beriet sich mit Claesson und entschied sich für die Verdrängung als Trennprinzip. Nachdem er von den Ergebnissen von James und Martin erfahren hatte, wechselte er zur Partitionschromatographie. ⓘ
Säulentechnologie
In der frühen Gaschromatographie wurden gepackte Säulen verwendet, die aus Schläuchen von typischerweise 1-5 m Länge und 1-5 mm Durchmesser bestanden und mit Partikeln gefüllt waren. Die Auflösung der gepackten Säulen wurde durch die Erfindung der Kapillarsäule verbessert, bei der die stationäre Phase auf die Innenwand der Kapillare aufgetragen wird. ⓘ
Physikalische Komponenten
Autosampler
Der Autosampler bietet die Möglichkeit, eine Probe automatisch in die Einlässe einzuführen. Das manuelle Einführen der Probe ist zwar möglich, aber nicht mehr üblich. Die automatische Zuführung bietet eine bessere Reproduzierbarkeit und Zeitoptimierung.
Es gibt verschiedene Arten von Autosamplern. Autosampler können in Bezug auf die Probenkapazität (Autoinjektoren vs. Autosampler, wobei Autoinjektoren eine geringe Anzahl von Proben verarbeiten können), auf Robotertechnologien (XYZ-Roboter vs. Rotationsroboter - die gängigsten) oder auf die Analyse klassifiziert werden:
- Flüssigkeit
- Statischer Head-Space durch Spritzen-Technologie
- Dynamischer Head-Space durch Transfer-Line-Technologie
- Festphasen-Mikroextraktion (SPME) ⓘ
Einlässe

Der Säuleneinlass (oder Injektor) ermöglicht es, eine Probe in einen kontinuierlichen Trägergasstrom einzuleiten. Der Einlass ist ein am Säulenkopf befestigtes Bauteil. ⓘ
Übliche Einlassarten sind:
- S/SL-Injektor (split/splitless); die Probe wird mit einer Spritze durch ein Septum in eine beheizte kleine Kammer eingeführt - die Wärme erleichtert die Verflüchtigung der Probe und der Probenmatrix. Das Trägergas spült dann entweder die gesamte (splitless mode) oder einen Teil (split mode) der Probe in die Säule. Im Split-Modus wird ein Teil des Proben-/Trägergasgemischs in der Injektionskammer durch die Split-Entlüftung abgeführt. Die Split-Injektion wird bevorzugt bei Proben mit hohen Analytkonzentrationen (>0,1 %) eingesetzt, während die Splitless-Injektion am besten für die Spurenanalyse mit geringen Analytmengen (<0,01 %) geeignet ist. Im Splitless-Modus öffnet sich das Split-Ventil nach einer voreingestellten Zeitspanne, um schwerere Elemente zu spülen, die sonst das System kontaminieren würden. Diese voreingestellte (splitlose) Zeit sollte optimiert werden; je kürzer die Zeit (z. B. 0,2 min), desto geringer das Tailing, aber desto geringer die Reaktion; je länger die Zeit (2 min), desto größer das Tailing, aber desto stärker das Signal.
- On-Column-Inlet; hier wird die Probe direkt und ohne Hitze oder bei einer Temperatur unterhalb des Siedepunkts des Lösungsmittels in die Säule eingeführt. Durch die niedrige Temperatur wird die Probe in einer engen Zone kondensiert. Anschließend können die Säule und der Einlass erhitzt werden, wodurch die Probe in die Gasphase übergeht. Dies gewährleistet die niedrigstmögliche Temperatur für die Chromatographie und verhindert, dass sich die Proben oberhalb ihres Siedepunkts zersetzen.
- PTV-Injektor; Die temperaturprogrammierte Probenzufuhr wurde erstmals 1979 von Vogt beschrieben. Ursprünglich entwickelte Vogt die Technik als Methode für die Einführung großer Probenvolumina (bis zu 250 µL) in die Kapillar-GC. Vogt führte die Probe mit einer kontrollierten Injektionsrate in den Liner ein. Die Temperatur des Liners wurde etwas unterhalb des Siedepunkts des Lösungsmittels gewählt. Das niedrig siedende Lösungsmittel wurde kontinuierlich verdampft und durch die Split-Leitung entlüftet. Auf der Grundlage dieser Technik entwickelte Poy den temperaturprogrammierten Verdampfungsinjektor (PTV). Durch die Einführung der Probe bei einer niedrigen Anfangstemperatur des Liners konnten viele der Nachteile der klassischen Heißinjektionstechniken umgangen werden.
- Gasquelleneinlass oder Gasumschaltventil; gasförmige Proben in Sammelflaschen werden an ein meist sechspoliges Umschaltventil angeschlossen. Der Trägergasstrom wird nicht unterbrochen, während eine Probe in eine zuvor evakuierte Probenschleife expandiert werden kann. Beim Umschalten wird der Inhalt der Probenschleife in den Trägergasstrom eingeleitet.
- P/T (Purge-and-Trap)-System: Ein Inertgas wird durch eine wässrige Probe geblasen, wodurch unlösliche flüchtige Chemikalien aus der Matrix herausgespült werden. Die flüchtigen Stoffe werden auf einer Absorptionssäule (bekannt als Trap oder Konzentrator) bei Umgebungstemperatur "eingefangen". Die Falle wird dann erhitzt und die flüchtigen Stoffe werden in den Trägergasstrom geleitet. Proben, die eine Anreicherung oder Reinigung erfordern, können über ein solches System eingeführt werden, das in der Regel an den S/SL-Anschluss angeschlossen ist. ⓘ
Die Wahl des Trägergases (mobile Phase) ist wichtig. Wasserstoff hat eine Reihe von Durchflussraten, die in ihrer Effizienz mit Helium vergleichbar sind. Helium kann jedoch effizienter sein und die beste Trennung liefern, wenn die Durchflussraten optimiert werden. Helium ist nicht brennbar und funktioniert mit einer größeren Anzahl von Detektoren und älteren Instrumenten. Daher ist Helium das am häufigsten verwendete Trägergas. Allerdings ist der Preis für Helium in den letzten Jahren erheblich gestiegen, so dass immer mehr Chromatographen auf Wasserstoffgas umsteigen. Der Grund für die bevorzugte Verwendung von Helium könnte eher in der Vergangenheit als in rationalen Erwägungen liegen. ⓘ
Detektoren
Die am häufigsten verwendeten Detektoren sind der Flammenionisationsdetektor (FID) und der Wärmeleitfähigkeitsdetektor (TCD). TCDs sind zwar insofern vorteilhaft, als sie zerstörungsfrei arbeiten, aber ihre niedrige Nachweisgrenze für die meisten Analyten verhindert einen breiten Einsatz. FIDs sind in erster Linie für Kohlenwasserstoffe empfindlich, und zwar empfindlicher als TCDs. FIDs können kein Wasser oder Kohlendioxid nachweisen, was sie ideal für die Analyse organischer Umweltanalyten macht. Der FID ist zwei- bis dreimal empfindlicher für den Nachweis von Analyten als der TCD. ⓘ
Der TCD beruht auf der Wärmeleitfähigkeit von Materie, die einen dünnen Wolfram-Rhenium-Draht umspült, durch den ein Strom fließt. Bei diesem Aufbau dienen Helium oder Stickstoff aufgrund ihrer relativ hohen Wärmeleitfähigkeit als Trägergas, das den Draht kühl hält und einen gleichmäßigen Widerstand und elektrischen Wirkungsgrad des Drahtes gewährleistet. Wenn Analytmoleküle aus der mit Trägergas vermischten Säule eluieren, nimmt die Wärmeleitfähigkeit ab, während die Filamenttemperatur und der Widerstand ansteigen, was zu Spannungsschwankungen führt, die schließlich eine Detektorreaktion verursachen. Die Empfindlichkeit des Detektors ist proportional zum Filamentstrom, während sie umgekehrt proportional zur unmittelbaren Umgebungstemperatur des Detektors sowie zur Durchflussrate des Trägergases ist. ⓘ
Bei einem Flammenionisationsdetektor (FID) werden die Elektroden in der Nähe des Säulenausgangs neben einer mit Wasserstoff/Luft betriebenen Flamme platziert, und wenn kohlenstoffhaltige Verbindungen die Säule verlassen, werden sie von der Flamme pyrolysiert. Dieser Detektor funktioniert nur für organische / kohlenwasserstoffhaltige Verbindungen, da die Kohlenstoffe bei der Pyrolyse Kationen und Elektronen bilden, die einen Strom zwischen den Elektroden erzeugen. Der Stromanstieg wird umgesetzt und erscheint als Peak in einem Chromatogramm. FIDs haben niedrige Nachweisgrenzen (einige Pikogramm pro Sekunde), können aber keine Ionen aus carbonylhaltigen Kohlenstoffen erzeugen. Zu den FID-kompatiblen Trägergasen gehören Helium, Wasserstoff, Stickstoff und Argon. ⓘ
Beim FID wird der Gasstrom manchmal modifiziert, bevor er in den Detektor gelangt. Ein Methanizer wandelt Kohlenmonoxid und Kohlendioxid in Methan um, so dass es nachgewiesen werden kann. Eine andere Technologie ist der Polyarc von Activated Research Inc., der alle Verbindungen in Methan umwandelt. ⓘ
Der Alkaliflammendetektor (AFD) oder Alkaliflammenionisationsdetektor (AFID) hat eine hohe Empfindlichkeit für Stickstoff und Phosphor, ähnlich wie der NPD. Allerdings werden die Alkalimetallionen mit dem Wasserstoffgas zugeführt und nicht mit einer Perle über der Flamme. Aus diesem Grund unterliegt der AFID nicht der "Ermüdung" des NPD, sondern bietet eine konstante Empfindlichkeit über einen langen Zeitraum. Wenn der Flamme keine Alkali-Ionen zugesetzt werden, arbeitet der AFD außerdem wie ein Standard-FID. Ein katalytischer Verbrennungsdetektor (CCD) misst brennbare Kohlenwasserstoffe und Wasserstoff. Der Entladungsionisationsdetektor (DID) verwendet eine elektrische Hochspannungsentladung zur Erzeugung von Ionen. ⓘ
Der flammenphotometrische Detektor (FPD) verwendet eine Photomultiplier-Röhre, um die Spektrallinien der Verbindungen zu erfassen, wenn sie in einer Flamme verbrannt werden. Die aus der Säule eluierten Verbindungen werden in eine mit Wasserstoff betriebene Flamme geleitet, die bestimmte Elemente in den Molekülen anregt, und die angeregten Elemente (P, S, Halogene, einige Metalle) emittieren Licht mit bestimmten charakteristischen Wellenlängen. Das emittierte Licht wird gefiltert und von einer Photomultiplier-Röhre erfasst. So liegt die Phosphoremission bei 510-536 nm und die Schwefelemission bei 394 nm. Bei einem Atomemissionsdetektor (AED) gelangt eine aus einer Säule eluierte Probe in eine Kammer, die durch Mikrowellen angeregt wird, die ein Plasma erzeugen. Das Plasma bewirkt, dass sich die Analyseprobe zersetzt und bestimmte Elemente ein Atomemissionsspektrum erzeugen. Die Atomemissionsspektren werden von einem Beugungsgitter gebeugt und von einer Reihe von Photomultipliern oder Photodioden erfasst. ⓘ
Elektroneneinfangdetektoren (ECD) verwenden eine radioaktive Betateilchenquelle (Elektronen), um den Grad des Elektroneneinfangs zu messen. ECD werden für den Nachweis von Molekülen verwendet, die elektronegative/elektronenanziehende Elemente und funktionelle Gruppen wie Halogene, Carbonyl, Nitrile, Nitrogruppen und organometallische Verbindungen enthalten. Bei diesem Detektortyp wird entweder Stickstoff oder 5% Methan in Argon als Trägergas für die mobile Phase verwendet. Das Trägergas strömt zwischen zwei Elektroden, die am Ende der Säule angebracht sind, und neben der Kathode (negative Elektrode) befindet sich eine radioaktive Folie wie 63Ni. Die radioaktive Folie sendet ein Betateilchen (Elektron) aus, das mit dem Trägergas kollidiert und dieses ionisiert, wodurch weitere Ionen erzeugt werden, die einen Strom erzeugen. Wenn Analytmoleküle mit elektronegativen/abziehenden Elementen oder funktionellen Gruppen Elektronen einfangen, führt dies zu einer Abnahme des Stroms und damit zu einer Detektorreaktion. ⓘ
Stickstoff-Phosphor-Detektor (NPD), eine Form des thermionischen Detektors, bei dem Stickstoff und Phosphor die Arbeitsfunktion auf einem speziell beschichteten Kügelchen verändern und ein daraus resultierender Strom gemessen wird. ⓘ
Der trockene elektrolytische Leitfähigkeitsdetektor (DELCD) verwendet eine Luftphase und hohe Temperaturen (v. Coulsen), um chlorierte Verbindungen zu messen. ⓘ
Massenspektrometer (MS), auch GC-MS genannt; hocheffektiv und empfindlich, selbst bei kleinen Probenmengen. Mit diesem Detektor lassen sich die Analyten in Chromatogrammen anhand ihres Massenspektrums identifizieren. Einige GC-MS sind mit einem NMR-Spektrometer verbunden, das als Backup-Detektor dient. Diese Kombination wird als GC-MS-NMR bezeichnet. Einige GC-MS-NMR sind mit einem Infrarot-Spektrophotometer verbunden, das als Backup-Detektor dient. Diese Kombination ist als GC-MS-NMR-IR bekannt. Es muss jedoch betont werden, dass dies sehr selten vorkommt, da die meisten erforderlichen Analysen mit reiner GC-MS durchgeführt werden können. ⓘ
Vakuum-Ultraviolett (VUV) ist die neueste Entwicklung im Bereich der Gaschromatographie-Detektoren. Die meisten chemischen Spezies absorbieren und haben einzigartige Gasphasen-Absorptionsquerschnitte in dem überwachten VUV-Wellenlängenbereich von etwa 120-240 nm. Wenn die Absorptionsquerschnitte der Analyten bekannt sind, kann mit dem VUV-Detektor die Anzahl der in der Durchflusszelle vorhandenen Moleküle absolut (ohne Kalibrierung) bestimmt werden, ohne dass es zu chemischen Interferenzen kommt. ⓘ
Der olfaktometrische Detektor, auch GC-O genannt, verwendet einen menschlichen Prüfer, um die Geruchsaktivität von Verbindungen zu analysieren. Mit einem Geruchsanschluss oder einer Schnüffelöffnung können die Qualität des Geruchs, die Intensität des Geruchs und die Dauer der Geruchsaktivität einer Verbindung bewertet werden. ⓘ
Weitere Detektoren sind der elektrolytische Hall-Leitfähigkeitsdetektor (ElCD), der Helium-Ionisationsdetektor (HID), der Infrarotdetektor (IRD), der Photo-Ionisationsdetektor (PID), der gepulste Entladungsionisationsdetektor (PDD) und der thermionische Ionisationsdetektor (TID). ⓘ


Teilweise werden für spezielle Fragestellungen auch zwei (oder mehrere) Detektoren hintereinander geschaltet (Tandem-Prinzip). Grundvoraussetzung dafür ist aber, dass die vorderen Detektoren die Messung nicht zerstörend durchführen (also z. B. ein ECD/WLD, aber kein FID/NPD). ⓘ
Die elektronischen Signale des Detektors werden in Abhängigkeit von der Zeit seit der Injektion (Retentionszeit) als 2D-Graph, dem sogenannten Chromatogramm, dargestellt. Dies geschieht in der Regel mithilfe von elektronischen Auswerteeinheiten (Computer mit Chromatographiedatensystem), selten nur noch mit Plottern. ⓘ
Methoden

Die Methode ist die Sammlung der Bedingungen, unter denen der GC für eine bestimmte Analyse arbeitet. Bei der Methodenentwicklung wird ermittelt, welche Bedingungen für die erforderliche Analyse angemessen und/oder ideal sind. ⓘ
Zu den Bedingungen, die für eine bestimmte Analyse variiert werden können, gehören die Einlasstemperatur, die Detektortemperatur, die Säulentemperatur und das Temperaturprogramm, das Trägergas und die Durchflussraten des Trägergases, die stationäre Phase der Säule, der Durchmesser und die Länge, der Einlasstyp und die Durchflussraten, die Probengröße und die Injektionstechnik. Je nach Detektor(en) (siehe unten), der/die auf dem GC installiert ist/sind, kann es eine Reihe von Detektorbedingungen geben, die ebenfalls variiert werden können. Einige GCs enthalten auch Ventile, die den Weg des Proben- und Trägerflusses ändern können. Der Zeitpunkt des Öffnens und Schließens dieser Ventile kann für die Methodenentwicklung von Bedeutung sein. ⓘ
Auswahl des Trägergases und Durchflussraten
Typische Trägergase sind Helium, Stickstoff, Argon und Wasserstoff. Welches Gas zu verwenden ist, hängt in der Regel vom verwendeten Detektor ab, z. B. benötigt ein DID Helium als Trägergas. Bei der Analyse von Gasproben wird das Trägergas auch auf der Grundlage der Probenmatrix ausgewählt, z. B. wird bei der Analyse eines Argon-Gemischs ein Argon-Trägergas bevorzugt, da das Argon in der Probe nicht auf dem Chromatogramm erscheint. Auch Sicherheit und Verfügbarkeit können die Wahl des Trägergases beeinflussen. ⓘ
Die Reinheit des Trägergases wird häufig auch durch den Detektor bestimmt, obwohl auch die erforderliche Empfindlichkeit eine wichtige Rolle spielen kann. Üblicherweise werden Reinheiten von 99,995 % oder höher verwendet. Die gebräuchlichsten Reinheitsgrade, die von modernen Geräten für die meisten Empfindlichkeiten verlangt werden, sind 5,0 Grade oder 99,999 % rein, was bedeutet, dass insgesamt 10 ppm Verunreinigungen im Trägergas vorhanden sind, die die Ergebnisse beeinflussen könnten. Die höchsten Reinheitsgrade, die üblicherweise verwendet werden, sind die 6,0-Grade, aber der Bedarf an Nachweisen bei sehr niedrigen Konzentrationen in einigen forensischen und Umweltanwendungen hat den Bedarf an Trägergasen mit einem Reinheitsgrad von 7,0 vorangetrieben, und diese sind jetzt im Handel erhältlich. Zu den Handelsbezeichnungen für typische Reinheitsgrade gehören "Zero Grade", "Ultra-High Purity (UHP) Grade", "4.5 Grade" und "5.0 Grade". ⓘ
Die lineare Geschwindigkeit des Trägergases beeinflusst die Analyse auf die gleiche Weise wie die Temperatur (siehe oben). Je höher die lineare Geschwindigkeit ist, desto schneller ist die Analyse, aber desto geringer ist die Trennung zwischen den Analyten. Die Wahl der linearen Geschwindigkeit ist daher derselbe Kompromiss zwischen dem Grad der Trennung und der Dauer der Analyse wie die Wahl der Säulentemperatur. Die lineare Geschwindigkeit wird durch die Durchflussrate des Trägergases in Bezug auf den Innendurchmesser der Säule bestimmt. ⓘ
Bei GCs, die vor den 1990er Jahren hergestellt wurden, wurde der Trägergasdurchsatz indirekt über den Trägergaseinlassdruck oder den "Säulenkopfdruck" gesteuert. Die tatsächliche Durchflussrate wurde am Ausgang der Säule oder des Detektors mit einem elektronischen Durchflussmesser oder einem Blasendurchflussmesser gemessen, was ein komplizierter, zeitraubender und frustrierender Prozess sein konnte. Es war nicht möglich, die Druckeinstellung während des Laufs zu verändern, so dass der Durchfluss während der Analyse im Wesentlichen konstant war. Das Verhältnis zwischen Durchflussrate und Einlassdruck wird mit der Poiseuille-Gleichung für kompressible Flüssigkeiten berechnet. ⓘ
Viele moderne GCs messen jedoch die Durchflussrate elektronisch und steuern den Trägergasdruck elektronisch, um die Durchflussrate einzustellen. Folglich können Trägergasdruck und Flussrate während des Laufs angepasst werden, wodurch Druck-/Flussprogramme ähnlich wie Temperaturprogramme erstellt werden. ⓘ
Auswahl der stationären Verbindung
Die Polarität des gelösten Stoffes ist entscheidend für die Wahl der stationären Verbindung, die im Idealfall eine ähnliche Polarität wie der gelöste Stoff aufweist. Übliche stationäre Phasen in offenen Röhrensäulen sind Cyanopropylphenyl-Dimethyl-Polysiloxan, Carbowax-Polyethylenglykol, Biscyanopropyl-Cyanopropylphenyl-Polysiloxan und Diphenyl-Dimethyl-Polysiloxan. Für gepackte Säulen sind weitere Optionen verfügbar. ⓘ
Einlasstypen und Durchflussraten
Die Wahl der Einlassart und der Injektionstechnik hängt davon ab, ob die Probe in flüssiger, gasförmiger, adsorbierter oder fester Form vorliegt und ob eine Lösungsmittelmatrix vorhanden ist, die verdampft werden muss. Gelöste Proben können direkt über einen COC-Injektor in die Säule eingebracht werden, wenn die Bedingungen bekannt sind; wenn eine Lösungsmittelmatrix verdampft und teilweise entfernt werden muss, wird ein S/SL-Injektor verwendet (häufigste Injektionstechnik); gasförmige Proben (z. B., Gasförmige Proben (z. B. Luftzylinder) werden in der Regel über ein Gasumschaltventilsystem injiziert; adsorbierte Proben (z. B. auf Adsorptionsröhrchen) werden entweder über ein externes (online oder offline) Desorptionsgerät wie ein Purge-and-Trap-System eingeführt oder im Injektor desorbiert (SPME-Anwendungen). ⓘ
Probengröße und Injektionstechnik
Injektion der Probe
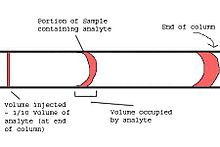
Die eigentliche chromatographische Analyse beginnt mit der Einführung der Probe auf die Säule. Die Entwicklung der Kapillar-Gaschromatographie führte zu vielen praktischen Problemen mit der Injektionstechnik. Die Technik der Injektion auf die Säule, die bei gepackten Säulen häufig verwendet wird, ist bei Kapillarsäulen in der Regel nicht möglich. Im Injektionssystem des Kapillar-Gaschromatographen sollte die injizierte Menge die Säule nicht überlasten und die Breite des injizierten Pfropfens sollte klein sein im Vergleich zur Ausbreitung durch den chromatographischen Prozess. Die Nichteinhaltung der letztgenannten Anforderung führt zu einer Verringerung der Trennleistung der Säule. Als allgemeine Regel gilt, dass das eingespritzte Volumen Vinj und das Volumen der Detektorzelle Vdet etwa 1/10 des Volumens betragen sollten, das der Teil der Probe einnimmt, der die interessierenden Moleküle (Analyten) enthält, wenn sie die Säule verlassen. ⓘ
Einige allgemeine Anforderungen, die eine gute Injektionstechnik erfüllen sollte, sind, dass es möglich sein sollte, die optimale Trenneffizienz der Säule zu erreichen, dass sie genaue und reproduzierbare Injektionen kleiner Mengen repräsentativer Proben ermöglichen sollte, dass sie keine Veränderung der Probenzusammensetzung bewirken sollte, dass sie keine Diskriminierung aufgrund von Unterschieden im Siedepunkt, der Polarität, der Konzentration oder der thermischen/katalytischen Stabilität aufweisen sollte und dass sie sowohl für die Spurenanalyse als auch für unverdünnte Proben geeignet sein sollte. ⓘ
Die Verwendung von Injektionsspritzen ist jedoch mit einer Reihe von Problemen behaftet. Selbst die besten Spritzen haben eine Genauigkeit von nur 3 %, und in ungeübten Händen sind die Fehler viel größer. Die Nadel kann beim Einspritzen der Probe kleine Gummistücke von der Scheidewand abschneiden. Diese können die Nadel blockieren und verhindern, dass sich die Spritze bei der nächsten Verwendung füllt. Dies ist möglicherweise nicht offensichtlich. Ein Teil der Probe kann im Gummi eingeschlossen werden und bei späteren Injektionen wieder freigesetzt werden. Dies kann zu Geisterpeaks im Chromatogramm führen. Es kann zu einem selektiven Verlust der flüchtigeren Bestandteile der Probe durch Verdunstung von der Nadelspitze kommen. ⓘ
Auswahl der Säule
Die Wahl der Säule hängt von der Probe und dem gemessenen Wirkstoff ab. Das wichtigste chemische Merkmal, das bei der Auswahl einer Säule berücksichtigt wird, ist die Polarität des Gemischs, aber auch funktionelle Gruppen können bei der Säulenauswahl eine große Rolle spielen. Die Polarität der Probe muss genau mit der Polarität der stationären Phase der Säule übereinstimmen, um die Auflösung und Trennung zu verbessern und gleichzeitig die Laufzeit zu verkürzen. Die Trennung und Laufzeit hängt auch von der Filmdicke (der stationären Phase), dem Säulendurchmesser und der Säulenlänge ab. ⓘ
Säulentemperatur und Temperaturprogramm

Die Säule(n) in einem GC befinden sich in einem Ofen, dessen Temperatur elektronisch präzise gesteuert wird. (Wenn ein Analytiker von der "Temperatur der Säule" spricht, bezieht er sich technisch gesehen auf die Temperatur des Säulenofens. Die Unterscheidung ist jedoch nicht wichtig und wird in diesem Artikel nicht weiter ausgeführt). ⓘ
Die Geschwindigkeit, mit der eine Probe durch die Säule läuft, ist direkt proportional zur Temperatur der Säule. Je höher die Temperatur der Säule ist, desto schneller bewegt sich die Probe durch die Säule. Je schneller eine Probe jedoch durch die Säule läuft, desto weniger interagiert sie mit der stationären Phase, und desto weniger werden die Analyten getrennt. ⓘ
Im Allgemeinen wird die Säulentemperatur so gewählt, dass ein Kompromiss zwischen der Dauer der Analyse und dem Grad der Trennung gefunden wird. ⓘ
Eine Methode, bei der die Säule während der gesamten Analyse auf der gleichen Temperatur gehalten wird, nennt man isotherm". Bei den meisten Methoden wird die Säulentemperatur jedoch während der Analyse erhöht. Die Anfangstemperatur, die Geschwindigkeit des Temperaturanstiegs (die "Temperaturrampe") und die Endtemperatur werden als Temperaturprogramm bezeichnet. ⓘ
Ein Temperaturprogramm sorgt dafür, dass Analyten, die früh in der Analyse eluieren, angemessen getrennt werden, während die Zeit, die spät eluierende Analyten für den Durchgang durch die Säule benötigen, verkürzt wird. ⓘ
Datenreduktion und Analyse
Qualitative Analyse
Im Allgemeinen werden chromatografische Daten als Diagramm der Detektorreaktion (y-Achse) gegen die Retentionszeit (x-Achse) dargestellt, was als Chromatogramm bezeichnet wird. Dies liefert ein Spektrum von Peaks für eine Probe, die die in einer Probe vorhandenen Analyten darstellen, die zu unterschiedlichen Zeiten aus der Säule eluieren. Die Retentionszeit kann zur Identifizierung von Analyten verwendet werden, wenn die Methodenbedingungen konstant sind. Auch das Muster der Peaks ist für eine Probe unter konstanten Bedingungen konstant und kann komplexe Gemische von Analyten identifizieren. In den meisten modernen Anwendungen ist der GC jedoch an ein Massenspektrometer oder einen ähnlichen Detektor angeschlossen, der in der Lage ist, die durch die Peaks repräsentierten Analyten zu identifizieren. ⓘ
Quantitative Analyse
Die Größe der vom Detektor angezeigten Flächeneinheiten steht in den seltensten Fällen in direktem Verhältnis zu den tatsächlichen Massenanteilen in der zu analysierenden Probe. Das macht eine Kalibrierung mit Referenzmaterialien definierten Gehalts notwendig. Um (zufällige) Fehler des Gaschromatographen (vor allem des Injektionssystems) auszuschließen, werden gerade in der Gaschromatographie gerne interne Standards eingesetzt. Als interner Standard dient hier eine zusätzliche Substanz, deren Retentionszeit in der Nähe der zu bestimmenden Analyten liegt, aber diese nicht überlagert. Sie wird dem Analyt und dem Referenzmaterial bzw. den daraus hergestellten Lösungen zugesetzt. Nach der Messung werden jeweils die Peakflächen von Analyt und Referenzmaterial zu der Peakfläche des internen Standards ins Verhältnis gesetzt und damit die Fehler des Injektionssystems so weit wie möglich herausgerechnet. Nach erfolgter Kalibrierung kann die Konzentration cP einer Probe P mithilfe der folgenden Gleichung ermittelt werden.
cS ist die eingewogene Konzentration an Standard, A bezeichnet die Fläche des Peaks im Chromatogramm und r bezeichnet die Sensitivität einer Substanz (wie viel Signal zeigt der Detektor an pro M). r kann für einen spezifischen Detektor einmalig gemessen und dann tabelliert werden. ⓘ
In den meisten modernen GC-MS-Systemen wird eine Computersoftware verwendet, um Peaks zu zeichnen und zu integrieren und MS-Spektren mit Spektren aus der Bibliothek abzugleichen. ⓘ
Anwendungen
Im Allgemeinen können Stoffe, die unter 300 °C verdampfen (und daher bis zu dieser Temperatur stabil sind), quantitativ gemessen werden. Die Proben müssen außerdem salzfrei sein; sie sollten keine Ionen enthalten. Es können sehr geringe Mengen einer Substanz gemessen werden, aber oft ist es erforderlich, dass die Probe im Vergleich zu einer Probe gemessen wird, die die reine, verdächtige Substanz enthält, die als Referenzstandard bezeichnet wird. ⓘ
Verschiedene Temperaturprogramme können verwendet werden, um die Messwerte aussagekräftiger zu machen, zum Beispiel um zwischen Substanzen zu unterscheiden, die sich während des GC-Prozesses ähnlich verhalten. ⓘ
Fachleute, die mit GC arbeiten, analysieren den Inhalt eines chemischen Produkts, zum Beispiel bei der Qualitätssicherung von Produkten in der chemischen Industrie oder bei der Messung von Chemikalien im Boden, in der Luft oder im Wasser, zum Beispiel von Bodengasen. Die GC ist bei richtiger Anwendung sehr genau und kann Pikomol einer Substanz in einer 1-ml-Flüssigkeitsprobe oder Teile-pro-Milliarde-Konzentrationen in gasförmigen Proben messen. ⓘ
Im Rahmen von Hochschulpraktika machen sich Studenten manchmal mit der GC vertraut, indem sie den Inhalt von Lavendelöl untersuchen oder das Ethylen messen, das von Nicotiana benthamiana-Pflanzen nach künstlicher Verletzung ihrer Blätter abgesondert wird. Diese GC analysieren Kohlenwasserstoffe (C2-C40+). In einem typischen Experiment werden die leichten Gase mit einer gepackten Säule abgetrennt und anschließend mit einem TCD nachgewiesen. Die Kohlenwasserstoffe werden mit einer Kapillarsäule getrennt und mit einem FID nachgewiesen. Eine Komplikation bei der Analyse von leichten Gasen, die H2 enthalten, besteht darin, dass He, der gebräuchlichste und empfindlichste inerte Trägerstoff (die Empfindlichkeit ist proportional zur Molekülmasse), eine fast identische Wärmeleitfähigkeit wie Wasserstoff aufweist (der Unterschied in der Wärmeleitfähigkeit zwischen zwei separaten Filamenten in einer Wheatstone-Bridge-Anordnung zeigt an, wann eine Komponente eluiert wurde). Aus diesem Grund sind Doppel-TCD-Geräte mit einem separaten Kanal für Wasserstoff, der Stickstoff als Träger verwendet, üblich. Argon wird häufig bei der Analyse von Gasphasenreaktionen wie der F-T-Synthese verwendet, so dass ein einziges Trägergas anstelle von zwei separaten Gasen verwendet werden kann. Die Empfindlichkeit ist geringer, aber dies ist ein Kompromiss für die Einfachheit der Gasversorgung. ⓘ
Die Gaschromatographie wird in der forensischen Wissenschaft in großem Umfang eingesetzt. In so unterschiedlichen Bereichen wie der Identifizierung und Quantifizierung fester Arzneimitteldosen (vor dem Konsum), der Untersuchung von Brandstiftung, der Analyse von Farbspänen und toxikologischen Fällen wird die GC zur Identifizierung und Quantifizierung verschiedener biologischer Proben und Tatortspuren eingesetzt. ⓘ
Messprinzip
Die chromatographische Auftrennung eines Stoffgemisches in einem Gaschromatographen erfolgt bei einer unpolaren Trägersäule im einfachsten Falle ausschließlich aufgrund der unterschiedlichen Siedepunkte der Einzelsubstanzen in dem Gemisch, wobei keine spezielle Wechselwirkung mit der stationären Phase erfolgt, sondern „nur“ eine zehntausendfach wiederholte Adsorption- und Desorption. Bei polaren Trennsäulen werden aber Alkohole, Ester, Ketone mit gleichen Siedepunkten wie ähnliche Paraffine stärker festgehalten. Die spezielle Wechselwirkung – genauer das Gleichgewicht zwischen der Gasphase und der stationären Phase – ist als Raoultsches Gesetz bekannt. Je höher der Partialdampfdruck einer Substanz nach dem Raoultschen Gesetz, d. h., je länger sich die Substanz in der Gasphase befindet, desto kürzer wird die Retentionszeit. ⓘ
Die Stärke der Wechselwirkungen, zwischen den Probenkomponenten und der stationären Phase, wird sowohl von deren Struktur als auch von deren funktionellen Gruppen bestimmt. Dabei treten bei unpolaren Substanzen ausschließlich Dispersionswechselwirkungen (Van-der-Waals-Bindungen) auf, während polare Trennphasen auch polare Wechselwirkungen eingehen können, z. B. Wasserstoffbrückenbindungen oder Donator-Akzeptor-Bindungen. Letztere trennen nach dem Prinzip: Gegensätze ziehen sich an. Das bedeutet, dass Trennphasen, die z. B. Wasserstoff zur Wasserstoffbrückenbindung aufzunehmen in der Lage sind, Substanzen trennen, die Wasserstoff zur Brückenbindung bereitstellen können (z. B. Alkohole). Auch können zum Beispiel Enantiomere, welche sich in ihren Siedepunkten nicht unterscheiden und somit gleiche Retentionszeiten aufweisen würden, durch ihre verschieden starken Wechselwirkungen mit speziellen Derivaten von Cyclodextrinen aufgetrennt werden. ⓘ
Eine Grundbedingung für die Gaschromatographie ist, dass sich der Stoff, den man untersuchen möchte, unzersetzt verdampfen lässt – sofern er nicht schon gasförmig vorliegt. Mittels Derivatisierung lassen sich der GC ansonsten schwer zugängliche Analyten wie Alkohole, Amine, Fettsäuren oder Zucker soweit thermisch stabilisieren, dass sie ohne Schwierigkeiten auf handelsüblichen Phasen aufgetrennt werden können. Mögliche Derivate sind bei Carbonsäuren die Methylester (Umwandlung mit BF3 und MeOH), bei Alkoholen die Silylether. ⓘ
Wichtige Geräteteile
Ein Gaschromatograph besteht aus drei wesentlichen Bauteilen: Injektor, Trennsäule im GC-Ofen und Detektor. Im Injektor wird die Probe, gelöst in einem niedrig siedenden Lösemittel, durch eine Durchstichmembran (Septum) eingespritzt. Dieser Injektor wird in der Regel beheizt (bis zu 450 °C), um eine rasche und vollständige Verdampfung der Probe zu erreichen. Möglich ist auch die septumfreie Aufgabe und langsame Verdampfung mittels eines Kaltaufgabesystems (KAS/PTV). Die Substanzen werden durch das Trägergas (Säulenvordruck normalerweise bis zu 6 bar) in die Trennsäule (Kapillare) transportiert, welche in den so genannten GC-Ofen eingebaut ist. Dieser dient dazu, die Trennsäule präzise zu temperieren, um so durch konstante Temperatur (isotherm) oder durch eine kontrollierte Temperaturerhöhung eine ebenso schnelle wie weitgehende Trennung des Stoffgemisches zu erreichen. ⓘ
Am Ende der Säule folgt der Detektor, der ein elektronisches Signal erzeugt, wenn eine Substanz das Trennsystem verlässt. Das elektronische Signal kann als Peak (engl. Gipfel) auf dem Schreiber registriert werden. Die Signale werden dann an einem Integrator oder heute meist an einem Computersystem mit entsprechender Auswertungssoftware verarbeitet. Die Dauer für die Trennung eines Stoffgemisches mit der Darstellung der verschiedenen Peaks zu einem Chromatogramm beträgt häufig zwischen 30 und 60 Minuten. ⓘ
Verwendete Trennsäulen
Wichtige Kenngrößen der Trennsäulen sind:
- der Säulendurchmesser
- die Säulenlänge
- und der Typ der stationären Phase (Belegung). ⓘ
Früher wurden meist gepackte Säulen eingesetzt. Bei ihnen befindet sich im Inneren eines dünnen (< 1 cm) Metall- oder Glasrohres von wenigen Metern Länge, der sogenannten Säule, ein festes, inertes Trägermaterial. Wird das Gas mit der zu analysierenden Substanz direkt über das Trägermaterial geleitet, so spricht man von einer GSC („Gas-Solid-Chromatography“). Ist die Trägersubstanz zudem mit einer dünnen Schicht einer hochmolekularen, zähflüssigen und wenig flüchtigen Flüssigkeit überzogen, so handelt es sich um eine GLC („Gas-Liquid-Chromatography“). Diese Flüssigkeit übernimmt hier die Funktion der eigentlichen stationären Phase. Das bevorzugt verwendete Inertgas ist hier Stickstoff. ⓘ
In den letzten Jahrzehnten wird überwiegend mit der von Marcel J. E. Golay 1958 entwickelten Kapillargaschromatographie gearbeitet. Der Vorteil besteht in der ca. 100–1000 fach besseren Auftrennung, (einer Trennstufenzahl von ca. 300.000) von Stoffen verglichen mit gepackten Säulen, so dass sich auch die Analysezeit verkürzen lässt. Dabei haben die zur Stabilisierung außen mit Polyimid beschichteten Quarzglas-Trennsäulen normalerweise einen Innendurchmesser von 0,1 bis 0,5 mm und eine Länge von 10 bis 60 m. Zur Auftrennung von Fettsäureestern werden sogar kombinierte Säulen bis 100 m verwendet. Die stationäre Phase kleidet die Kapillare dabei nur als dünner Film mit in der Regel 0,1 bis 5 µm aus. Der Vorteil besteht in der drastisch besseren Auftrennung ähnlicher Stoffe, verglichen mit gepackten Säulen. Der Trend in der GC geht momentan zu immer dünneren und kürzeren Säulen, weil dadurch der Zeitaufwand für Analysen deutlich gesenkt werden kann. Das bevorzugt verwendete Inertgas ist Helium, aber auch Wasserstoff oder seltener Stickstoff werden verwendet. ⓘ
Ein wichtiges Kriterium zur Klassifizierung der stationären Phase ist die Polarität ihrer Belegung. Analyten auf unpolaren Säulen (Typ DB-1 o. ä.) eluieren meist nach ihren Siedepunkten. Polare Verbindungen treten bei polaren Säulen dagegen selektiv mit den polaren stationären Phasen in Wechselwirkung und werden entsprechend ihrer Polarität länger zurückgehalten und eluieren später als vergleichbare unpolare Verbindungen wie z. B. Alkane. Bei der Verwendung von Säulen unterschiedlicher Hersteller ist zu beachten, dass identische stationäre Trennphasen mit den unterschiedlichsten Bezeichnungen versehen werden. Der folgenden Liste gängiger stationäre Trennphasen ist zu entnehmen, welche Trennsäulen unterschiedlicher Hersteller hinsichtlich Zusammensetzung der Belegung der Trennsäulen vergleichbar sind. ⓘ
| Zusammensetzung der Belegung der Trennsäule |
Herstellerbezeichnung | Temperaturbereich | Polarität ⓘ |
|---|---|---|---|
| Polydimethylsiloxan 100 % Methyl |
DB-1, SB-1, BP-1, CP-Sil 5 CB, OV–1, OV–101, PB-1, SPB-1, RTX-1, PE-1, Ultra 1, ZB-1, AT-1, SE-30 | −50 °C bis +350 °C | unpolar |
| Polyphenylmethylsiloxan 5 % Phenyl, 95 % Dimethyl |
DB-5, SB-5, BP-5, CP-Sil 8 CB, PVMS-5, PB-2, SPB-5, Rtx-5, PE-2, Ultra 2, ZB-5, AT-5, SE-54, Optima-5, RSL-200 | −20 °C bis +350 °C | leicht polar |
| Polyphenylmethylsiloxan 14 % Phenyl, 86 % Dimethyl |
DB-624, SB-624, CP-Sil 13 CB, VOCOL, Rtx-Volatiles, PE-502, AT-62 | ±0 °C bis +250 °C | mittelpolar |
| Polycyanopropylphenylmethylsiloxan 6 % Cyanopropylphenyl, 94 % Dimethyl |
DB-1301, SB-1301, Rtx-1301, AT-1301 | ±0 °C bis +230 °C | polar |
| Polyphenylmethylcyanosiloxan 6 % Phenyl, 6 % Cyano, 88 % Methyl |
DB-1701, SB-1701, BP-10, CP-Sil 19 CB, PB-1701, SPB-7, Rtx-1701, PE-1701, PAS-1701, AT-1701, RSL-300 | −50 °C bis +225 °C | polar |
| Polyethylenglycol | DB-WAX, SB-Wax, BP-20, CP-Wax 52 CB, Supelcowax-10, Stabilwax, PE-CW, HP-20M, AT-Wax | ±0 °C bis +220 °C | polar |
| Polyethylenglykol-2-nitroterephthalsäureester | OPTIMA FFAP, DB-FFAP, HP-FFAP, CP-Sil 58 CB, 007-FFAP, CP-FFAP, Nukol | ±0 °C bis +250/260 °C | polar |
Seit Beginn der 1990er Jahre wurden von den Säulenherstellern große Anstrengungen unternommen, blutungsarme Säulen zu entwickeln, die vor allem in der GC-MS eingesetzt werden. Diese sind häufig an der Zusatzbezeichnung "-ms" zu erkennen. ⓘ
Trennsäulen, die mit einer chiralen stationären Phase belegt sind, können für die Enantiomerenanalytik benutzt werden. Dies erlaubt die Bestimmung des Enantiomerenverhältnisses in Enantiomerengemischen und die Analyse der Enantiomerenreinheit vermeintlich reiner Enantiomerer. ⓘ
Anwendung in der Analytik

Die Gaschromatographie ist eine sehr empfindliche Methode zur Analyse von Stoffgemischen. Es lassen sich selbst minimale Substanzmengen (10−9 Gramm) nachweisen. Man kann mit ihr komplexe Stoffgemische in die einzelnen Komponenten auftrennen. In vielen Fällen reicht allein die Zeit, die eine Substanz vom Zeitpunkt der Einspritzung bis zum Passieren des Detektors benötigt, die Retentionszeit, um eine Substanz zu identifizieren. Durch Kombination mit einem Massenspektrometer, die sogenannte GC/MS-Kopplung, können sehr geringe Substanzmengen nachgewiesen werden, und gleichzeitig Strukturaufklärung betrieben werden. ⓘ
Anwendung findet die Gaschromatographie in der Analytik von Agrarprodukten auf Herbizide, Fleischprodukte auf Hormone, der Untersuchung von Arzneimittel, von Aromen und ätherischen Ölen, von Kohlenhydraten, von Erdölkomponenten und in der forensischen Chemie, bei Dopingtests, bei Luft- und Meerwasseruntersuchungen in der Umweltanalytik. Auch hochmolekulare Substanzen, wie Triglyceride und Wachse lassen sich auf temperaturstabilen stationären Siliconphasen trennen, identifizieren und quantitativ bestimmen. Schwer flüchtige Analyten müssen vor der Analyse eventuell erst derivatisiert also in leichter flüchtige Substanzen umgewandelt werden. Dieses kann z. B. mit Trimethylsulfoniumhydroxid oder Chlortrimethylsilan geschehen, indem polare Gruppen in unpolare methylierte Gruppen umgewandelt werden. ⓘ