Buprenorphin
 | |
 | |
| Klinische Daten | |
|---|---|
| Handelsnamen | Subutex, Sixmo, andere |
| AHFS/Drogen.de | Monographie |
| MedlinePlus | a605002 |
| Lizenz-Daten |
|
| Schwangerschaft Kategorie |
|
| Abhängigkeit Haftung | Psychisch: Hoch; Körperlich: Mäßig |
| Wege der Verabreichung | Unter die Zunge, durch die Wange, intramuskulär, transdermal, intranasal, rektal, durch den Mund |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | Sublingual: 30% Intranasal: 48% Bukkal: 65% |
| Proteinbindung | 96% |
| Stoffwechsel | Leber (CYP3A4, CYP2C8) |
| Beginn der Wirkung | Innerhalb von 30 min |
| Eliminationshalbwertszeit | 37 Stunden (Bereich 20-70 Stunden) |
| Dauer der Wirkung | bis zu 24 Stunden |
| Ausscheidung | Gallengang und Niere |
| Bezeichner | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Chemische und physikalische Daten | |
| Formel | C29H41NO4 |
| Molare Masse | 467,650 g-mol-1 |
| 3D-Modell (JSmol) | |
SMILES
| |
InChI
| |
| | |
Buprenorphin ist ein Opioid, das zur Behandlung von Opioidkonsumstörungen, akuten Schmerzen und chronischen Schmerzen eingesetzt wird. Es kann unter die Zunge (sublingual), in die Wange (bukkal), durch Injektion (intravenös und subkutan), als Hautpflaster (transdermal) oder als Implantat verabreicht werden. Bei Opioidkonsumstörungen wird es in der Regel zu Beginn der Entzugssymptome und während der ersten beiden Tage der Behandlung unter direkter Beobachtung eines medizinischen Betreuers verabreicht. In den Vereinigten Staaten wird in der Regel die Kombinationsformulierung von Buprenorphin/Naloxon (Suboxone) verschrieben, um einem Missbrauch durch Injektion vorzubeugen. Die maximale Schmerzlinderung tritt in der Regel innerhalb einer Stunde ein, die Wirkung hält bis zu 24 Stunden an. Buprenorphin wirkt auf verschiedene Arten von Opioidrezeptoren auf unterschiedliche Weise. Je nach Art des Rezeptors kann es ein Agonist, ein Teilagonist oder ein Antagonist sein. Bei der Behandlung von Opioidkonsumstörungen ist Buprenorphin ein Agonist/Antagonist, d. h., es lindert die Entzugssymptome anderer Opioide und löst eine gewisse Euphorie aus, blockiert aber auch die Fähigkeit vieler anderer Opioide, einschließlich Heroin, eine Wirkung zu erzielen. Im Gegensatz zu Vollagonisten wie Heroin oder Methadon hat Buprenorphin einen Ceiling-Effekt, d. h. die Wirkung des Medikaments wird durch die Einnahme weiterer Medikamente nicht verstärkt. ⓘ
Zu den Nebenwirkungen können Atemdepression (verminderte Atmung), Schläfrigkeit, Nebenniereninsuffizienz, QT-Verlängerung, niedriger Blutdruck, allergische Reaktionen, Verstopfung und Opioidabhängigkeit gehören. Bei Personen mit Krampfanfällen in der Vorgeschichte besteht das Risiko weiterer Krampfanfälle. Der Opioidentzug nach Absetzen von Buprenorphin ist im Allgemeinen weniger schwerwiegend als bei anderen Opioiden. Ob die Einnahme während der Schwangerschaft sicher ist, ist unklar, aber die Einnahme während der Stillzeit ist wahrscheinlich sicher, da die Dosis, die der Säugling erhält, 1-2 % der mütterlichen Dosis auf Gewichtsbasis beträgt. ⓘ
Buprenorphin wurde 1965 patentiert und 1981 in den Vereinigten Staaten zur medizinischen Verwendung zugelassen. Es steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation. Es wird nicht nur als Schmerzmittel verschrieben, sondern ist auch ein gängiges Medikament zur Behandlung von Opioidkonsumstörungen, wie z. B. Heroinabhängigkeit. Im Jahr 2017 wurden in den Vereinigten Staaten 14,6 Millionen Verschreibungen für das Medikament ausgestellt. In den USA werden sublinguale Formulierungen als Film oder gemischt mit Naloxon vermarktet, um von der Injektion abzuhalten. In den Vereinigten Staaten ist Buprenorphin eine kontrollierte Substanz nach Liste III. ⓘ
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
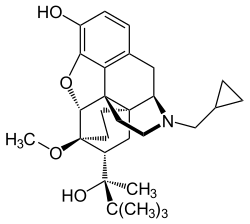
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Buprenorphin | ||||||||||||||||||
| Andere Namen |
(5R,6R,7R,9R,13S,14S)-17-Cyclopropylmethyl-7-[(S)-3,3-dimethyl-2-hydroxybutan-2-yl]-6-methoxy-4,5-epoxy-6,14-ethanomorphinan-3-ol (IUPAC) | ||||||||||||||||||
| Summenformel | C29H41NO4 | ||||||||||||||||||
| Kurzbeschreibung |
Weißes bis fast weißes, kristallines Pulver | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Wirkstoffklasse |
| ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 467,64 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
209 °C | ||||||||||||||||||
| pKS-Wert |
8,5; 10,0 | ||||||||||||||||||
| Löslichkeit |
sehr schwer löslich in Wasser, leicht löslich in Aceton, löslich in Methanol, schwer löslich in Cyclohexan | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
| ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Buprenorphin ist ein stark wirksames Schmerzmittel (Analgetikum) aus der Gruppe der Opioide. Buprenorphin hat eine partialagonistische Wirkung mit hoher Affinität zu µ-Rezeptoren. ⓘ
Es gilt im höheren Alter aufgrund seines guten Sicherheitsprofils als Mittel der ersten Wahl zur Behandlung starker chronischer Schmerzen (etwa bei Schmerzsyndromen). Darüber hinaus wird Buprenorphin hochdosiert seit circa Mitte der 1990er Jahre als Substitutionsmittel in der Therapie einer Abhängigkeit von Opioiden verwendet, 2006 wurde es für diese Anwendung in die Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation aufgenommen. ⓘ
Buprenorphin wird halbsynthetisch aus dem Opium-Alkaloid Thebain gewonnen und vermittelt seine Effekte als Partialagonist über verschiedene Opioid-Rezeptoren. Sein wichtigstes Abbauprodukt ist das pharmakologisch aktive Nor-Buprenorphin. ⓘ
Medizinische Anwendungen
Opioidkonsumstörung

Buprenorphin wird zur Behandlung von Menschen mit Opioidkonsumstörungen eingesetzt. In den USA wird in der Regel die Kombinationsformulierung von Buprenorphin/Naloxon verschrieben, um eine Injektion zu verhindern, da Naloxon, ein Opioid-Antagonist, einen akuten Entzug verursacht, wenn die Formulierung zerdrückt und injiziert wird. Bevor mit der Einnahme von Buprenorphin begonnen wird, wird den Betroffenen in der Regel geraten, nach der letzten Opioiddosis so lange zu warten, bis sie einige Entzugserscheinungen zeigen, damit das Medikament die Rezeptoren binden kann, da Buprenorphin bei zu früher Einnahme andere an die Rezeptoren gebundene Opioide verdrängen und einen akuten Entzug auslösen kann. Die Buprenorphin-Dosis wird dann so lange angepasst, bis sich die Symptome bessern, und die Patienten bleiben bei einer Erhaltungsdosis von 8-16 mg. Da der Entzug für viele Patienten unangenehm und abschreckend ist, haben viele begonnen, andere Methoden für den Beginn der Behandlung zu fordern. Einige Anbieter sind dazu übergegangen, die Berner Methode, auch bekannt als Mikrodosierung, anzuwenden, bei der sehr geringe Buprenorphindosen verabreicht werden, während die Patienten noch Straßenopioide konsumieren, ohne dass es zu einem Entzug kommt, und bei der die Medikamentenspiegel langsam hochtitriert werden. ⓘ
Buprenorphin im Vergleich zu Methadon
Sowohl Buprenorphin als auch Methadon sind Medikamente, die für die Entgiftung und die Opioid-Ersatztherapie eingesetzt werden und nach den vorliegenden begrenzten Daten ähnlich wirksam zu sein scheinen. Beide sind für schwangere Frauen mit Opioidkonsumstörung sicher, obwohl vorläufige Erkenntnisse darauf hindeuten, dass Methadon eher ein neonatales Abstinenzsyndrom verursachen kann. In den USA und in der Europäischen Union dürfen nur zugelassene Kliniken Methadon für Opioidkonsumstörungen verschreiben, so dass die Patienten täglich in die Klinik kommen müssen. Wenn die Patienten eine Zeit lang drogenfrei sind, kann es ihnen gestattet werden, "Dosen zum Mitnehmen" zu erhalten, so dass sie die Klinik nur noch einmal pro Woche aufsuchen müssen. Alternativ kann ein Monatsvorrat an Buprenorphin von Ärzten in den USA oder Europa verschrieben werden, die eine Grundausbildung (8-24 Stunden in den USA) absolviert und eine Ausnahmegenehmigung/Lizenz erhalten haben, die die Verschreibung des Medikaments erlaubt. In Frankreich ist die Verschreibung von Buprenorphin zur Behandlung von Opioidkonsumstörungen seit 1995 ohne besondere Ausbildung oder Einschränkungen erlaubt, was dazu führte, dass in den folgenden zehn Jahren jährlich etwa zehnmal mehr Patienten mit Buprenorphin als mit Methadon behandelt wurden. Um die Rekordzahlen bei den Opioidüberdosierungen anzugehen, haben die Vereinigten Staaten im Jahr 2021 auch die Anforderung einer Sondergenehmigung für verschreibende Ärzte aufgehoben. Ob diese Änderung ausreichen wird, um die Verschreibung zu beeinflussen, ist unklar, da bereits vor der Änderung die Hälfte der Ärzte mit einer Ausnahmegenehmigung, die ihnen die Verschreibung von Buprenorphin erlaubte, dies nicht taten, und ein Drittel der Ärzte, die keine Ausnahmegenehmigung hatten, berichteten, dass sie nichts dazu bewegen würde, Buprenorphin für Opioidkonsumstörungen zu verschreiben. ⓘ
Chronische Schmerzen
Für die Behandlung von chronischen Schmerzen steht ein transdermales Pflaster zur Verfügung. Diese Pflaster sind nicht zur Behandlung von akuten Schmerzen, von Schmerzen, die voraussichtlich nur kurze Zeit anhalten, oder von Schmerzen nach einer Operation geeignet und werden auch nicht zur Behandlung von Opioidabhängigkeit empfohlen. ⓘ
Potenz
Was die äquianalgetische Dosierung betrifft, so ist die Potenz von Buprenorphin bei sublingualer Anwendung etwa 40 bis 70 Mal so hoch wie die von Morphin. Bei der Verwendung als transdermales Pflaster kann die Potenz von Buprenorphin das 100- bis 115-fache von Morphin betragen. ⓘ
Tiermedizinische Anwendungen
Tierärzte verabreichen Buprenorphin häufig zur Behandlung von perioperativen Schmerzen, insbesondere bei Katzen, wo es ähnlich wie Morphin wirkt. Der legale Status des Medikaments und das geringere Missbrauchspotenzial für den Menschen machen es zu einer attraktiven Alternative zu anderen Opioiden. ⓘ
Nebenwirkungen
In der Indikation der analgetischen Therapie hat Buprenorphin unter den Opioiden ein günstigeres Nebenwirkungsprofil – im Vergleich zu z. B. Morphin treten Symptome wie Obstipation und Juckreiz deutlich seltener auf. Initial auftretende Übelkeit bzw. Erbrechen unterliegen schnell einem Toleranzeffekt und können durch prophylaktische Gabe eines Antiemetikums und langsame Dosissteigerung minimiert werden. Da die Ausscheidung überwiegend über die Galle (biliär) erfolgt, besteht keine Notwendigkeit einer Dosisanpassung bei eingeschränkter Nierenfunktion und somit auch kein Risiko einer Substanzkumulation mit Intoxikation bei Patienten mit Nierenfunktionseinschränkung (auch bei älteren Patienten). ⓘ
Die Nebenwirkungen von Buprenorphin in der Substitutionstherapie sind im Vergleich zu den Nebenwirkungen, die eine Substitution mit Methadon mit sich bringt (z. B. starkes Schwitzen, Wasseransammlungen im Körper, Antriebslosigkeit, Schlafstörungen, Konzentrationsschwäche, vermindertes sexuelles Empfinden, Depression, Obstipation) weniger stark ausgeprägt. ⓘ
Am häufigsten treten Störungen des Nervensystems, insbesondere Müdigkeit, Schlafstörungen und Benommenheit mit einer Häufigkeit von über 10 % auf. Ebenso können häufig (1 bis 10 %) Schwindel und Kopfschmerzen sowie gelegentlich (0,1 bis 1 %) Erschöpfung, Mundtrockenheit, verwaschene Sprache, Koma, Tremor, Krämpfe und fehlende Muskelkoordination vorkommen. Ebenso können gelegentlich psychiatrische Störungen, wie Verwirrtheit, Desorientierung, Nervosität, Depression, Psychose, Halluzinationen, Depersonalisation, Euphorie, Dysphorie und Unruhe auftreten. Die charakteristische Opioid-Nebenwirkung der Miosis kann bei etwa 1 bis 10 % der Patienten beobachtet werden, während weitere Störungen des Auges, wie beispielsweise Doppeltsehen, Sehstörungen und Konjunktivitis, oder des Ohrs, wie Tinnitus, nur gelegentlich auftreten. Die häufigste Nebenwirkung auf das Herz-Kreislaufsystem ist ein orthostatischer Blutdruckabfall (1 bis 10 %). Gelegentlich treten auch Tachykardie, Bradykardie, Zyanose, AV-Block und Hypotonie auf. Eine Atemdepression kann häufig beobachtet werden, sie steigert sich jedoch nur gelegentlich in eine Atemnot oder einen Atemstillstand. Ein Bronchospasmus tritt nur sehr selten auf (<0,01 %). Übelkeit und Erbrechen können als charakteristische Opioid-Nebenwirkungen häufig beobachtet werden, während Obstipation, Dyspepsie, Appetitlosigkeit und Durchfall nur gelegentlich auftreten. Gelegentlich können auch Miktionsbeschwerden und Harnretention beobachtet werden. Störungen, welche die Haut betreffen, äußern sich häufig in Schwitzen sowie gelegentlich in Parästhesie, Juckreiz, Hautausschlag, Blässe und Urtikaria. Das Quincke-Ödem tritt nur sehr selten auf. Allgemeine Überempfindlichkeitsreaktionen können gelegentlich auftreten, schwere anaphylaktische Reaktionen sind sehr selten. ⓘ
Da unter der sublingualen hochdosierten Therapie mit Buprenorphin häufig das Auftreten einer Verlängerung des QT-Intervalls beobachtet wurde, sind Vorsichtsmaßnahmen bei Patienten mit bekannter oder vermuteter EKG-Veränderung, einem Elektrolyt-Ungleichgewicht, einer Verlangsamung der Herzfrequenz (Bradykardie) oder bei der gleichzeitigen Behandlung mit Arzneimitteln gegen Herzrhythmusstörungen nötig. Vor und 2 Wochen nach Behandlungsbeginn bzw. Dosiserhöhungen ist daher ein EKG durchzuführen. Verschiedene Studien beschreiben eine sichere Therapie mit Buprenorphin ohne Auswirkungen auf das QT-Intervall. ⓘ

Zu den häufigen unerwünschten Arzneimittelwirkungen im Zusammenhang mit dem Konsum von Buprenorphin, die denen anderer Opioide ähneln, gehören Übelkeit und Erbrechen, Schläfrigkeit, Schwindel, Kopfschmerzen, Gedächtnisverlust, kognitive und neuronale Hemmung, Schwitzen, Juckreiz, Mundtrockenheit, Verengung der Augenpupillen (Miosis), orthostatische Hypotonie, Ejakulationsstörungen beim Mann, verminderte Libido und Harnverhalt. Verstopfung und Wirkungen auf das Zentralnervensystem (ZNS) werden weniger häufig beobachtet als bei Morphin. ⓘ
Auswirkungen auf die Atemwege
Die schwerwiegendste mit Buprenorphin verbundene Nebenwirkung ist die Atemdepression (unzureichende Atmung). Sie tritt häufiger bei Personen auf, die gleichzeitig Benzodiazepine oder Alkohol einnehmen oder eine zugrunde liegende Lungenerkrankung haben. Die üblichen Umkehrmittel für Opioide, wie z. B. Naloxon, sind möglicherweise nur teilweise wirksam, und es können zusätzliche Anstrengungen zur Unterstützung der Atmung erforderlich sein. Die Atemdepression ist möglicherweise geringer als bei anderen Opioiden, insbesondere bei chronischem Gebrauch. Im Rahmen der akuten Schmerzbehandlung scheint Buprenorphin jedoch in gleichem Maße eine Atemdepression zu verursachen wie andere Opioide, z. B. Morphin. ⓘ
Buprenorphin-Abhängigkeit
Die Behandlung mit Buprenorphin birgt das Risiko, eine psychologische oder physiologische (körperliche) Abhängigkeit zu verursachen. Es hat einen langsamen Wirkungseintritt, eine lange Wirkdauer und eine lange Halbwertszeit von 24 bis 60 Stunden. Sobald sich ein Patient auf die (Buprenorphin-)Medikation und das Programm eingestellt hat, bleiben drei Möglichkeiten: die kontinuierliche Einnahme (reine Buprenorphin-Medikation), die Umstellung auf eine Buprenorphin/Naloxon-Kombination oder ein ärztlich überwachter Entzug. ⓘ
Schmerzbehandlung
Bei Personen, die Buprenorphin zur Schmerzbehandlung verwenden, ist es schwierig, eine akute Opioidanalgesie zu erreichen. ⓘ
Pharmakologie
Pharmakodynamik
| Standort | Ki (nM) | Wirkung | Spezies | Ref |
|---|---|---|---|---|
| MOR | 0.21–1.5 0.081 |
Partieller Agonist | Mensch Affe |
|
| DOR | 2.9–6.1 0.82 |
Antagonist | Mensch Affe |
|
| KOR | 0.62–2.5 0.44 |
Antagonist | Mensch Affe |
|
| NOP | 77.4 | Partieller Agonist | Mensch | |
| σ1 | >100,000 | ND | ND | |
| σ2 | ND | ND | ND | ND |
| NMDA | ND | ND | ND | ND |
| TLR4 | >10,000 | Agonist | Mensch | |
| SERT | >100,000 | ND | Ratte | |
| NET | >100,000 | ND | Ratte | |
| DAT | ND | ND | ND | ND |
| VGSC | 33.000 (IC50) | Hemmstoff | Nagetier | |
| Werte sind Ki (nM), sofern nicht anders angegeben. Je kleiner der Wert, desto stärker bindet das Medikament an die Stelle. | ||||
Opioidrezeptor-Modulator
Buprenorphin hat Berichten zufolge die folgenden pharmakologischen Wirkungen:
- μ-Opioidrezeptor (MOR): Partieller Agonist mit sehr hoher Affinität: Bei niedrigen Dosen sind die MOR-vermittelten Wirkungen von Buprenorphin mit denen anderer Narkotika vergleichbar, aber diese Wirkungen erreichen eine "Obergrenze", wenn die Rezeptorpopulation gesättigt ist. Dieses Verhalten ist für mehrere einzigartige Eigenschaften verantwortlich: Buprenorphin schwächt die Wirkung der meisten anderen MOR-Agonisten stark ab, kann bei aktiv Opioidabhängigen zu einem beschleunigten Entzug führen und hat im Vergleich zu vollständigen MOR-Agonisten eine geringere Inzidenz von Atemdepression und tödlicher Überdosierung.
- κ-Opioid-Rezeptor (KOR): Antagonist mit hoher Affinität - es wird vermutet, dass diese Aktivität einigen der Wirkungen von Buprenorphin auf Stimmungsstörungen und Sucht zugrunde liegt.
- δ-Opioid-Rezeptor (DOR): Hochaffiner Antagonist
- Nociceptin-Rezeptor (NOP, ORL-1): Schwache Affinität, sehr schwacher partieller Agonist ⓘ
Vereinfacht ausgedrückt kann Buprenorphin im Wesentlichen als nicht-selektiver, gemischter Agonist-Antagonist-Opioidrezeptor-Modulator betrachtet werden, der als schwacher partieller Agonist des MOR mit ungewöhnlich hoher Affinität, als Antagonist des KOR und des DOR mit hoher Affinität und als sehr schwacher partieller Agonist des ORL-1/NOP mit relativ geringer Affinität wirkt. ⓘ
Obwohl Buprenorphin ein partieller Agonist des MOR ist, wurde in Humanstudien festgestellt, dass es in Bezug auf die Analgesie bei Opioid-intoleranten Personen wie ein vollständiger Agonist wirkt. Umgekehrt verhält sich Buprenorphin in Bezug auf die Atemdepression wie ein partieller Agonist des MOR. ⓘ
Es ist auch bekannt, dass Buprenorphin mit hoher Affinität an den putativen ε-Opioidrezeptor bindet und diesen antagonisiert. ⓘ
Die volle analgetische Wirksamkeit von Buprenorphin erfordert sowohl Exon-11- als auch Exon-1-assoziierte μ-Opioidrezeptor-Splice-Varianten. ⓘ
Man geht davon aus, dass die aktiven Metaboliten von Buprenorphin keine klinische Bedeutung für seine ZNS-Wirkungen haben. ⓘ
In Studien zur Positronen-Emissions-Tomographie (PET) wurde festgestellt, dass Buprenorphin die MOR-Verfügbarkeit im gesamten Gehirn aufgrund der Rezeptorbelegung bei 2 mg um 41 % (d. h. 59 % Verfügbarkeit), bei 16 mg um 80 % (d. h. 20 % Verfügbarkeit) und bei 32 mg um 84 % (d. h. 16 % Verfügbarkeit) verringert. ⓘ
Andere Wirkungen
Im Gegensatz zu einigen anderen Opioiden und Opioidantagonisten bindet Buprenorphin nur schwach an den Sigma-Rezeptor und besitzt dort, wenn überhaupt, nur eine geringe Aktivität. ⓘ
Buprenorphin blockiert über die Bindungsstelle für Lokalanästhetika auch spannungsabhängige Natriumkanäle, was die Grundlage für seine starken lokalanästhetischen Eigenschaften bildet. ⓘ
Ähnlich wie bei verschiedenen anderen Opioiden hat sich gezeigt, dass Buprenorphin auch als Agonist des Toll-like-Rezeptors 4 wirkt, wenn auch mit sehr geringer Affinität. ⓘ
Pharmakokinetik
Buprenorphin wird aufgrund seiner hohen Lipophilie im Körper gespeichert und nur langsam aufgrund seiner trägen Rezeptorkinetik sowie des entero-hepatischen Kreislaufs ausgeschieden. ⓘ
Buprenorphin besitzt nach oraler Gabe eine schlechte Bioverfügbarkeit von nur etwa 6,5 %, bedingt durch einen ausgeprägten First-Pass-Effekt (der unmittelbaren Verstoffwechselung in der Leber nach Aufnahme aus dem Dünndarm). Bei einer Einmalgabe als Sublingualtablette(n) (Einzeldosis: 0,2 bis 0,6 mg bei Erwachsenen) ist die Bioverfügbarkeit durch Umgehung des First-Pass-Effekts etwa doppelt so hoch, bei sublingualer Verabreichung als Flüssigkeit etwa 4- bis 8-mal höher. Bei Einnahme beider Arzneizubereitungen über mehrere Tage erhöht sich allerdings die relative Bioverfügbarkeit der Sublingualtablette. ⓘ
Das wichtigste Stoffwechselprodukt (Metabolit) ist Nor-Buprenorphin, für dessen Bildung das Cytochrom-P450-Enzymsystem verantwortlich ist. Nor-Buprenorphin ist ebenfalls pharmakologisch wirksam, jedoch ist seine analgetische Potenz gegenüber seiner Muttersubstanz um den Faktor 50 reduziert. Die Verstoffwechslung erfolgt zu 75 % über die Isoenzyme CYP3A4 und CYP3A5. Buprenorphin selbst hemmt CYP3A4. Buprenorphin-Wechselwirkungen sind daher mit einer Vielzahl an Medikamenten möglich. Die Ausscheidung von Buprenorphin und Nor-Buprenorphin erfolgt nach einer optionalen Glucuronidierung zum überwiegenden Teil über die Galle und damit über die Faeces und nur zu etwa 10 bis 30 % über die Nieren und damit über den Urin. ⓘ
Die Eliminierungsgeschwindigkeit von Buprenorphin folgt einem komplexen bi- oder triexponentiellen Schema. Als Ursache werden komplexe Verteilungsvorgänge von Buprenorphin im Organismus betrachtet, welche dessen Rückresorption aus dem Magen-Darm-Trakt (enterohepatischer Kreislauf) und eine langsame Diffusion aus dem Fettgewebe einschließen. Zudem hat die Art der Verabreichung Auswirkungen auf das Verteilungsverhalten von Buprenorphin und somit auch auf dessen pharmakokinetische Eigenschaften. Aus diesen Gründen und je nach verwendeter Bestimmungsmethode werden unterschiedliche Plasmahalbwertzeiten für Buprenorphin ermittelt. Diese liegen zwischen 3 und 44 Stunden. Wegen der lang anhaltenden Rezeptorbindung korreliert die Wirkdauer nicht unmittelbar mit Blutkonzentrationen oder der Plasmahalbwertszeit von Buprenorphin. Die Wirkdauer ist mit 24 bis 69 Stunden mindestens ebenso lang wie die von Methadon. ⓘ
Buprenorphin wird in der Leber über die CYP3A4-Isoenzyme (auch CYP2C8 scheint beteiligt zu sein) des Cytochrom-P450-Enzymsystems zu Norbuprenorphin (durch N-Dealkylierung) metabolisiert. Die Glucuronidierung von Buprenorphin wird in erster Linie von UGT1A1 und UGT2B7 durchgeführt, die von Norbuprenorphin von UGT1A1 und UGT1A3. Diese Glucuronide werden dann hauptsächlich durch Ausscheidung in die Galle eliminiert. Die Eliminationshalbwertszeit von Buprenorphin beträgt 20 bis 73 Stunden (Mittelwert 37 Stunden). Da Buprenorphin hauptsächlich über die Leber eliminiert wird, besteht bei Menschen mit Nierenfunktionsstörungen kein Risiko einer Kumulation. ⓘ
Die Glucuronide von Buprenorphin und Norbuprenorphin sind ebenfalls biologisch aktiv und stellen die wichtigsten aktiven Metaboliten von Buprenorphin dar. Buprenorphin-3-glucuronid hat eine Affinität für MOR (Ki = 4,9 pM), DOR (Ki = 270 nM) und ORL-1 (Ki = 36 μM) und keine Affinität für KOR. Es hat eine geringe antinozizeptive Wirkung und keine Wirkung auf die Atmung. Norbuprenorphin-3-glucuronid hat keine Affinität zum MOR oder DOR, bindet aber an den KOR (Ki = 300 nM) und ORL-1 (Ki = 18 μM). Es hat eine sedierende Wirkung, aber keine Auswirkung auf die Atmung. ⓘ
Chemie
Buprenorphin ist ein halbsynthetisches Derivat von Thebain und in Form seines Hydrochloridsalzes gut wasserlöslich. In Gegenwart von Licht wird es abgebaut. ⓘ
Nachweis in Körperflüssigkeiten
Buprenorphin und Norbuprenorphin können in Blut oder Urin quantifiziert werden, um den Konsum oder den nichtmedizinischen Freizeitkonsum zu überwachen, eine Vergiftungsdiagnose zu bestätigen oder bei einer gerichtsmedizinischen Untersuchung zu helfen. Innerhalb des möglichen Spektrums physiologischer Reaktionen, das von asymptomatisch bis komatös reicht, gibt es eine erhebliche Überschneidung der Drogenkonzentrationen in Körperflüssigkeiten. Daher ist die Kenntnis des Verabreichungsweges der Droge und des Toleranzniveaus der Person gegenüber Opioiden für die Interpretation der Ergebnisse von entscheidender Bedeutung. ⓘ
Geschichte
Buprenorphin wurde als starkes Analgetikum 1968 von Reckitt & Colman patentiert. ⓘ
Synthese
Die Ausgangssubstanz für die partialsynthetische Herstellung von Buprenorphin ist das Opium-Nebenalkaloid Thebain. Durch Umsetzung mit Methylvinylketon wird in einem ersten Reaktionsschritt das Cycloadditionsprodukt 7-Acetyl-6,14-endoethenotetrahydrothebain gebildet. Nach Reduktion unter Palladium-Kohle-Katalyse wird das Reaktionsprodukt mit tert-Butylmagnesiumchlorid im Sinne einer Grignard-Reaktion zu 6,14-Endoethano-7-(2-hydroxy-3,3-dimethyl-2-butyl)-tetrahydrothebain umgesetzt. Die tertiäre Aminogruppe dieses Zwischenprodukts wird mit Bromcyan demethyliert und mit Hilfe von Cyclopropylcarbonsäurechlorid unter reduktiven Bedingungen in Gegenwart von Lithiumaluminiumhydrid alkyliert. Nach hydrolytischer Abspaltung der phenolischen Methoxygruppe kann Buprenorphin isoliert werden. ⓘ
Analytik
Das Europäische Arzneibuch verwendet die IR-Spektroskopie zur Identitätsprüfung von Buprenorphin. Die Gehaltsbestimmung sowohl der Base als auch des Hydrochlorids erfolgt als acidimetrische Titration mit Perchlorsäure in Eisessig und potentiometischer Endpunktanzeige. ⓘ
Für den Nachweis von Buprenorphin im Urin steht ein auf einem Immunoassay basierender Schnelltest zur Verfügung. Zusätzlich kann eine Bestätigungsanalyse auf Buprenorphin mit Hilfe chromatographischer Methoden, wie Hochleistungsflüssigkeitschromatographie mit Fotodiodenzeilendetektion, Gaschromatographie mit Massenspektrometrie-Kopplung oder Flüssigchromatographie mit Massenspektrometrie-Kopplung aus biologischen Proben durchgeführt werden. ⓘ
Stereochemie
Buprenorphin weist sieben benachbarte Asymmetriezentren auf, von denen vier durch Syntheseschritte eingeführt werden. ⓘ
Geschichte
1969 versuchten Forscher von Reckitt und Colman (heute Reckitt Benckiser) zehn Jahre lang, eine Opioidverbindung zu synthetisieren, die "eine wesentlich komplexere Struktur als Morphin aufweist [und] die erwünschten Wirkungen beibehält, ohne die unerwünschten Nebenwirkungen zu haben". Die körperliche Abhängigkeit und der Entzug von Buprenorphin selbst sind nach wie vor ein wichtiges Thema, da Buprenorphin ein lang wirkendes Opioid ist. Reckitt hatte Erfolg, als die Forscher RX6029 synthetisierten, das bei Versuchstieren eine erfolgreiche Verringerung der Abhängigkeit gezeigt hatte. RX6029 erhielt den Namen Buprenorphin und wurde ab 1971 an Menschen getestet. Im Jahr 1978 wurde Buprenorphin im Vereinigten Königreich erstmals als Injektion zur Behandlung starker Schmerzen eingeführt, 1982 kam eine sublinguale Formulierung auf den Markt. ⓘ
Gesellschaft und Kultur
Regulierung
Vereinigte Staaten
In den Vereinigten Staaten wurden Buprenorphin und Buprenorphin mit Naloxon im Oktober 2002 von der Food and Drug Administration zur Behandlung von Opioidkonsumstörungen zugelassen. Unmittelbar vor der Zulassung wurde Buprenorphin von der DEA von einem Medikament der Kategorie V in eine Kategorie III umgestuft. Die ACSCN für Buprenorphin lautet 9064, und da es sich um eine Substanz der Liste III handelt, gibt es keine von der DEA festgelegte jährliche Herstellungsquote. Das gebräuchliche Salz ist das Hydrochlorid, das ein Umwandlungsverhältnis von 0,928 zur freien Base aufweist. ⓘ
In den Jahren vor der Zulassung von Buprenorphin/Naloxon hatte sich Reckitt Benckiser im Kongress für die Ausarbeitung des Drug Addiction Treatment Act aus dem Jahr 2000 eingesetzt, der dem Gesundheitsminister die Befugnis erteilte, Ärzten mit einer bestimmten Ausbildung eine Ausnahmegenehmigung für die Verschreibung und Verabreichung von Betäubungsmitteln der Liste III, IV oder V zur Behandlung von Abhängigkeiten oder zur Entgiftung zu erteilen. Vor der Verabschiedung dieses Gesetzes war eine solche Behandlung nur in speziell für Drogenabhängige eingerichteten Kliniken zulässig. ⓘ
Die Ausnahmegenehmigung, die nach Abschluss eines achtstündigen Kurses erteilt werden kann, war von 2000 bis 2021 für die ambulante Behandlung von Opioidabhängigkeit mit Buprenorphin erforderlich. Ursprünglich war die Zahl der Personen, die jeder zugelassene Arzt behandeln durfte, auf 10 begrenzt. Diese Regelung wurde schließlich dahingehend geändert, dass zugelassene Ärzte bis zu 100 Personen ambulant mit Buprenorphin gegen Opioidabhängigkeit behandeln dürfen. Dieser Grenzwert wurde von der Obama-Regierung angehoben, so dass die Zahl der Patienten, denen Ärzte Buprenorphin verschreiben dürfen, auf 275 stieg. Am 14. Januar 2021 gab das US-Gesundheitsministerium bekannt, dass die Ausnahmegenehmigung für die Verschreibung von Buprenorphin zur gleichzeitigen Behandlung von bis zu 30 Personen nicht mehr erforderlich ist. ⓘ
New Jersey hat Sanitäter ermächtigt, Menschen, die sich von einer Überdosis erholt haben, am Unfallort Buprenorphin zu verabreichen. ⓘ
Europa
In der Europäischen Union wurden Subutex und Suboxone, die hochdosierten sublingualen Tablettenpräparate von Buprenorphin, im September 2006 für die Behandlung von Opioidkonsumstörungen zugelassen. In den Niederlanden steht Buprenorphin auf der Liste II des Opiumgesetzes, wobei für seine Verschreibung und Abgabe besondere Vorschriften und Leitlinien gelten. In Frankreich ist die Verschreibung von Buprenorphin durch Allgemeinmediziner und die Abgabe durch Apotheken seit Mitte der 1990er Jahre als Reaktion auf das HIV- und Überdosisrisiko erlaubt. Die Zahl der durch eine Überdosis Heroin verursachten Todesfälle ist zwischen 1994 und 2002 um vier Fünftel zurückgegangen, und die AIDS-Inzidenz bei Menschen, die in Frankreich Drogen injizieren, ist von 25 % Mitte der 1990er Jahre auf 6 % im Jahr 2010 gesunken. ⓘ
Markennamen
Buprenorphin ist unter den Markennamen Cizdol, Brixadi (wöchentliche und monatliche Depotinjektionen, in den USA von der FDA für die Suchtbehandlung im Jahr 2020 zugelassen), Suboxone (mit Naloxon), Subutex (in der Regel zur Behandlung von Opioidkonsumstörungen), Zubsolv, Bunavail, Buvidal (wöchentliche und monatliche Depotinjektionen, im Vereinigten Königreich zugelassen, Europa und Australien für die Suchtbehandlung zugelassen), Sublocade (monatliche Injektion, 2018 in den USA zugelassen), Probuphine, Temgesic (Sublingualtabletten für mäßige bis starke Schmerzen), Buprenex (Lösungen zur Injektion, die häufig bei akuten Schmerzen in der Primärversorgung eingesetzt werden), Norspan und Butrans (transdermale Präparate für chronische Schmerzen). ⓘ
Buprenorphin wurde in den meisten europäischen Ländern als transdermale Formulierung (unter dem Namen Transtec) für die Behandlung chronischer Schmerzen eingeführt, die nicht auf Nichtopioide ansprechen. ⓘ
Veterinärmedizin
In der Veterinärmedizin wird Buprenorphin zur Behandlung von Schmerzen bei Hunden und Katzen eingesetzt. ⓘ
Forschung
Depressionen
Gemäß diverser Studien wurde eine antidepressive Wirkung bei nicht-psychotischen unipolaren Depressionen nachgewiesen. Ein antidepressiver Effekt wurde auch bei jenen Probanden erzielt, welche zuvor weder auf herkömmliche Antidepressiva noch auf eine Elektrokrampftherapie (EKT) angesprochen haben. Aufgrund der unvermeidbaren Entwicklung einer Opioidabhängigkeit ist Buprenorphin in der EU bei Depressionen nicht indiziert. ⓘ
In den USA hingegen ist ein Medikament auf der Basis von Buprenorphin und Samidorphan, einem μ-Rezeptor-Antagonisten, unter dem Namen ALKS-5461 für nicht-psychotische unipolare und therapieresistente Depressionen entwickelt worden. Das Medikament wurde am 31. Januar 2018 durch die Food and Drug Administration (FDA) für den US-Markt zugelassen. ⓘ
Einige Belege sprechen für den Einsatz von Buprenorphin bei Depressionen. Buprenorphin/Samidorphan, ein Kombinationspräparat aus Buprenorphin und Samidorphan (einem bevorzugten μ-Opioidrezeptor-Antagonisten), scheint bei behandlungsresistenten Depressionen nützlich zu sein. ⓘ
Kokainabhängigkeit
In Kombination mit Samidorphan oder Naltrexon (μ-Opioidrezeptor-Antagonisten) wird Buprenorphin für die Behandlung der Kokainabhängigkeit untersucht und hat kürzlich in einer groß angelegten klinischen Studie (n = 302) seine Wirksamkeit für diese Indikation gezeigt (bei einer hohen Buprenorphin-Dosis von 16 mg, aber nicht bei einer niedrigen Dosis von 4 mg). ⓘ
Neonatale Abstinenz
Buprenorphin wurde zur Behandlung des neonatalen Abstinenzsyndroms eingesetzt, einer Erkrankung, bei der Neugeborene, die während der Schwangerschaft Opioiden ausgesetzt waren, Entzugserscheinungen zeigen. In den Vereinigten Staaten ist die Verwendung derzeit auf Säuglinge beschränkt, die an einer klinischen Studie im Rahmen eines von der FDA genehmigten IND-Antrags (Investigational New Drug) teilnehmen. Vorläufige Forschungsergebnisse deuten darauf hin, dass Buprenorphin im Vergleich zu Methadon bei Neugeborenen zu einer kürzeren Verweildauer im Krankenhaus führt. Eine bei Neugeborenen verwendete ethanolische Formulierung ist bei Raumtemperatur mindestens 30 Tage lang stabil. ⓘ
Zwanghafte Störungen
In einer Studie wurde festgestellt, dass Buprenorphin bei einer Untergruppe von Personen mit behandlungsresistenter Zwangsstörung wirksam ist. ⓘ
Klinische Angaben
Gegenanzeigen (Kontraindikationen)
Neben einer bekannten Überempfindlichkeit gelten eine schwere Ateminsuffizienz und eine schwere Leberinsuffizienz als absolute Kontraindikationen. Daher darf Buprenorphin bei diesen Erkrankungen sowie bei gleichzeitiger Verwendung von MAO-Hemmern nicht angewendet werden. Weitere absolute oder relative Kontraindikationen sind Alkoholismus, Delirium tremens, schwere Kopfverletzungen und ein erhöhter Hirndruck. Die Anwendung bei leichten Formen der Atem- und Leberinsuffizienz sowie bei Niereninsuffizienz ist unter Beachtung einer Dosisanpassung und weiterer Vorsichtsmaßnahmen möglich. ⓘ
Wechselwirkungen
Bei gleichzeitiger Anwendung von Buprenorphin mit anderen Opioiden, Alkohol, Anästhetika, Hypnotika, Sedativa, Antidepressiva, Neuroleptika und weiteren Arzneimitteln mit einer dämpfenden Wirkung auf das Zentralnervensystem kann es zur Verstärkung von zentralnervösen Effekten kommen. Insbesondere bei einer gleichzeitigen Einnahme von Alkohol werden die sedierenden Nebenwirkungen von Buprenorphin verstärkt. Benzodiazepine verstärken insbesondere die atemdepressiven Nebenwirkungen von Buprenorphin. Bei gemeinsamer Anwendung von Buprenorphin mit CYP3A4-Inhibitoren, wie beispielsweise Ketoconazol, Gestoden, Triacetyloleandomycin, Ritonavir, Indinavir und Saquinavir, kann die Wirkung von Buprenorphin verstärkt werden. Eine ausgeprägte Erhöhung des Buprenorphinspiegels ist auch bei gleichzeitigem Konsum mit dem ebenfalls CYP3A4-hemmenden Grapefruitsaft beschrieben worden. Eine eventuelle Interaktion mit CYP3A4-Induktoren, wie beispielsweise Phenobarbital, Carbamazepin, Phenytoin und Rifampicin ist zwar nicht hinreichend untersucht, gilt aber auf Grund der pharmakokinetischen Eigenschaften von Buprenorphin als möglich und kann zu einer Verringerung der Buprenorphinwirkung führen. Zusätzlich ist vereinzelt von einer Verstärkung der Nebenwirkungen von Phenprocoumon durch Buprenorphin berichtet worden. ⓘ
Überdosierung
In jedem Fall treten nach einer Überdosis Buprenorphin ähnliche Symptome auf, wie sie auch bei anderen zentralwirksamen Analgetika zu erwarten sind. Sie umfassen Atemdepression, Sedierung, Somnolenz, Übelkeit, Erbrechen, Kreislaufkollaps und ausgeprägte Miosis. Zu beachten ist, dass Buprenorphin wegen der oben genannten hohen Rezeptoraffinität nur sehr langsam vom Rezeptor dissoziiert, es wirkt also vergleichsweise lange, was bei der Behandlung einer Überdosierung zu beachten ist. Es sollte eine kontinuierliche Infusion mit Naloxon erfolgen, da Naloxon eine viel geringere Halbwertzeit (circa 70 Minuten) und damit kürzere Wirkdauer hat. Des Weiteren muss Naloxon deutlich höher dosiert werden als bei der Antagonisierung von etwa Morphin. Eine Atemdepression kann mit Naloxon nicht sicher aufgehoben werden, so dass eine künstliche Beatmung notwendig werden kann. Zur Atemstimulierung kann ein Analeptikum wie Doxapram eingesetzt werden. ⓘ
Handelsnamen
- Monopräparate
- Norspan (D, A), Subutex (D, A, CH, FR, BE), Buvidal (D, UK, DK, NO, SW, SF), Bupensan (A), Temgesic (D, A, CH, FR, BE), Transtec (D, A, CH, FR, BE), Triquisic (A) und Generika
- Buprenovet (Veterinärmedizin, D)
- Kombinationspräparate