Ketone
| Ketone ⓘ |
|---|

|
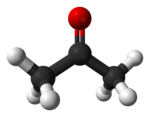
| R1 und R2 sind organische Reste (Alkyl, Aryl o. ä.). Die Carbonylgruppe ist blau markiert. |
Ketone sind chemische Verbindungen, die als funktionelle Gruppe eine nicht endständige Carbonylgruppe (>C=O) enthalten. Eine Ketongruppe [C–C(O)–C] enthält drei Kohlenstoffatome. Alle Ketone enthalten mindestens drei Kohlenstoffatome. Im Gegensatz zu den Aldehyden ist hier der Carbonylkohlenstoff in beide Bindungsrichtungen mit Kohlenstoffatomen verbunden. Ketone kann man als Oxidationsprodukte sekundärer Alkohole auffassen. Die von den Alkanen ableitbaren Ketone nennt man auch Alkanone. Entsprechend bezeichnet man die auf Alkene und Alkine zurückzuführenden Ketone als Alkenone (siehe Enone) bzw. Alkinone. Das einfachste Keton ist Aceton. Ein einfaches aromatisches Keton ist Benzophenon (Diphenylketon). Ein gemischtes Keton ist Acetophenon (Methylphenylketon). Physiologisch entstehen bestimmte Ketone als Stoffwechselprodukt in der Leber. ⓘ
Nomenklatur und Etymologie
Das Wort Keton leitet sich von Aketon ab, einem alten deutschen Wort für "Aceton". ⓘ
Nach den Regeln der IUPAC-Nomenklatur werden Keton-Namen abgeleitet, indem die Endung -ane des Ausgangsalkans in -anone geändert wird. In der Regel wird die Position der Carbonylgruppe durch eine Zahl angegeben, aber für die wichtigsten Ketone, z. B. Aceton und Benzophenon, werden im Allgemeinen noch traditionelle unsystematische Namen verwendet. Diese unsystematischen Namen gelten als beibehaltene IUPAC-Namen, obwohl einige Lehrbücher für Einsteiger in die Chemie systematische Namen wie "2-Propanon" oder "Propan-2-on" für das einfachste Keton (C H3-CO-CH3) anstelle von "Aceton" verwenden. ⓘ
Die abgeleiteten Namen von Ketonen erhält man, indem man die Namen der beiden Alkylgruppen, die an die Carbonylgruppe gebunden sind, getrennt schreibt, gefolgt von "Keton" als separatem Wort. Die Namen der Alkylgruppen werden in der Reihenfolge der zunehmenden Komplexität geschrieben: zum Beispiel Methylethylketon. Nach den Regeln der IUPAC-Nomenklatur werden die Alkylgruppen alphabetisch geschrieben, z. B. Ethylmethylketon. Wenn die beiden Alkylgruppen gleich sind, wird dem Namen der Alkylgruppe die Vorsilbe "di-" vorangestellt. Die Positionen der anderen Gruppen werden mit griechischen Buchstaben angegeben, wobei der α-Kohlenstoff das der Carbonylgruppe benachbarte Atom ist. ⓘ
Obwohl selten verwendet, ist Oxo die IUPAC-Nomenklatur für die Oxo-Gruppe (=O) und wird als Präfix verwendet, wenn das Keton nicht die höchste Priorität hat. Es werden jedoch auch andere Präfixe verwendet. Bei einigen gebräuchlichen Chemikalien (hauptsächlich in der Biochemie) bezieht sich Keto auf die funktionelle Keton-Gruppe. ⓘ
Sehr häufig tragen die Ketone jedoch Namen, welche aus der Bezeichnung der Alkylreste gefolgt von der Endung -keton bestehen (Radikofunktionelle Nomenklatur). So wird Butanon auch Methylethylketon (MEK) genannt. Falls der eine Substituent eine Phenylgruppe ist, ist die Endung -phenon gebräuchlich, wie zum Beispiel bei Acetophenon. ⓘ
Struktur und Eigenschaften

Das Ketonkohlenstoffatom wird häufig als "sp2-hybridisiert" bezeichnet, eine Beschreibung, die sowohl die elektronische als auch die molekulare Struktur umfasst. Ketone sind um das Ketonkohlenstoffatom herum trigonal planar, mit C-C-O- und C-C-C-Bindungswinkeln von etwa 120°. Ketone unterscheiden sich von Aldehyden dadurch, dass die Carbonylgruppe (CO) an zwei Kohlenstoffe innerhalb eines Kohlenstoffskeletts gebunden ist. In Aldehyden ist die Carbonylgruppe an einen Kohlenstoff und einen Wasserstoff gebunden und befindet sich an den Enden der Kohlenstoffketten. Ketone unterscheiden sich auch von anderen carbonylhaltigen funktionellen Gruppen, wie Carbonsäuren, Estern und Amiden. ⓘ
Die Carbonylgruppe ist polar, da die Elektronegativität des Sauerstoffs größer ist als die des Kohlenstoffs. Daher sind Ketone am Sauerstoff nucleophil und am Kohlenstoff elektrophil. Da die Carbonylgruppe mit Wasser durch Wasserstoffbrückenbindungen wechselwirkt, sind Ketone in der Regel besser in Wasser löslich als die verwandten Methylenverbindungen. Ketone sind Wasserstoffbrückenbindungsakzeptoren. Ketone sind in der Regel keine Wasserstoffbrückenbindungsdonatoren und können keine Wasserstoffbrückenbindungen mit sich selbst eingehen. Aufgrund ihrer Unfähigkeit, sowohl als Wasserstoffbrückenbündel-Donatoren als auch als Wasserstoffbrückenbündel-Akzeptoren zu fungieren, neigen Ketone nicht zur "Selbstassoziation" und sind flüchtiger als Alkohole und Carbonsäuren mit vergleichbarem Molekulargewicht. Diese Faktoren sind der Grund für die weite Verbreitung von Ketonen in der Parfümerie und als Lösungsmittel. ⓘ
Klassen von Ketonen
Ketone werden auf der Grundlage ihrer Substituenten klassifiziert. Eine grobe Einteilung unterteilt die Ketone in symmetrische und unsymmetrische Derivate, je nach der Äquivalenz der beiden organischen Substituenten, die an das Carbonylzentrum gebunden sind. Aceton und Benzophenon (C6H5C(O)C6H5) sind symmetrische Ketone. Acetophenon (C6H5C(O)CH3) ist ein unsymmetrisches Keton. ⓘ
Diketone
Es sind viele Arten von Diketonen bekannt, einige mit ungewöhnlichen Eigenschaften. Das einfachste ist Diacetyl (CH3C(O)C(O)CH3), das früher als Butteraroma in Popcorn verwendet wurde. Acetylaceton (Pentan-2,4-dion) ist praktisch eine Fehlbezeichnung, da diese Art hauptsächlich als Monoenol CH3C(O)CH=C(OH)CH3 vorkommt. Sein Enolat ist ein häufiger Ligand in der Koordinationschemie. ⓘ
Ungesättigte Ketone
Ketone, die Alken- und Alkineinheiten enthalten, werden oft als ungesättigte Ketone bezeichnet. Das am häufigsten verwendete Mitglied dieser Verbindungsklasse ist das Methylvinylketon, CH3C(O)CH=CH2, das für die Robinson-Annulationsreaktion verwendet wird. Um Verwirrung zu vermeiden, ist ein Keton selbst eine ungesättigte Stelle, d. h. es kann hydriert werden. ⓘ
Zyklische Ketone
Viele Ketone sind cyclisch. Die einfachste Klasse hat die Formel (CH2)nCO, wobei n von 2 für Cyclopropanon bis in den Zehnerbereich variiert. Es gibt auch größere Derivate. Cyclohexanon, ein symmetrisches cyclisches Keton, ist ein wichtiges Zwischenprodukt bei der Herstellung von Nylon. Isophoron, abgeleitet von Aceton, ist ein ungesättigtes, asymmetrisches Keton, das als Vorläufer für andere Polymere dient. Muscon, 3-Methylpentadecanon, ist ein tierisches Pheromon. Ein weiteres zyklisches Keton ist Cyclobutanon mit der Formel C4H6O. ⓘ
Keto-Enol-Tautomerisierung

Ketone, die mindestens ein Alpha-Wasserstoffatom aufweisen, werden zu Keto-Enol-Tautomeren tautomerisiert; das Tautomer ist ein Enol. Die Tautomerisierung wird sowohl durch Säuren als auch durch Basen katalysiert. Normalerweise ist die Ketoform stabiler als das Enol. Aufgrund dieses Gleichgewichts können Ketone durch Hydratisierung von Alkinen hergestellt werden. ⓘ
Säure/Base-Eigenschaften von Ketonen
Die C-H-Bindungen neben dem Carbonyl in Ketonen sind saurer (pKa ≈ 20) als die C-H-Bindungen in Alkanen (pKa ≈ 50). Dieser Unterschied spiegelt die Resonanzstabilisierung des Enolat-Ions wider, das bei der Deprotonierung gebildet wird. Die relative Acidität des α-Wasserstoffs ist bei den Enolisierungsreaktionen von Ketonen und anderen Carbonylverbindungen von Bedeutung. Der Säuregrad des α-Wasserstoffs ermöglicht es auch, dass Ketone und andere Carbonylverbindungen als Nukleophile an dieser Position mit einer stöchiometrischen und katalytischen Base reagieren. Bei Verwendung sehr starker Basen wie Lithiumdiisopropylamid (LDA, pKa der konjugierten Säure ~36) unter nicht ausgleichenden Bedingungen (-78 °C, 1,1 Äquivalent LDA in THF, Keton zur Base gegeben) wird das weniger substituierte kinetische Enolat selektiv erzeugt, während Bedingungen, die eine Ausbalancierung ermöglichen (höhere Temperatur, Base zum Keton gegeben, Verwendung schwacher oder unlöslicher Basen, z. B., NaOEt in EtOH, oder NaH) das stärker substituierte thermodynamische Enolat liefert. ⓘ
Ketone sind ebenfalls schwache Basen, die in Gegenwart von Brønsted-Säuren eine Protonierung am Carbonylsauerstoff erfahren. Ketonium-Ionen (d. h. protonierte Ketone) sind starke Säuren mit pKa-Werten, die schätzungsweise zwischen -5 und -7 liegen. Obwohl die in der organischen Chemie vorkommenden Säuren selten stark genug sind, um Ketone vollständig zu protonieren, ist die Bildung von Gleichgewichtskonzentrationen protonierter Ketone dennoch ein wichtiger Schritt in den Mechanismen vieler gängiger organischer Reaktionen, wie z. B. der Bildung eines Acetals. Schwache Säuren wie das Pyridiniumkation (wie es in Pyridiniumtosylat vorkommt) mit einem pKa-Wert von 5,2 können in diesem Zusammenhang als Katalysator dienen, trotz der sehr ungünstigen Gleichgewichtskonstante für die Protonierung (Keq < 10-10). ⓘ
Charakterisierung
Ein Aldehyd unterscheidet sich von einem Keton dadurch, dass ein Wasserstoffatom an seine Carbonylgruppe gebunden ist, wodurch Aldehyde leichter zu oxidieren sind. Ketone haben kein Wasserstoffatom, das an die Carbonylgruppe gebunden ist, und sind daher resistenter gegen Oxidation. Sie werden nur durch starke Oxidationsmittel oxidiert, die in der Lage sind, Kohlenstoff-Kohlenstoff-Bindungen zu spalten. ⓘ
Spektroskopie
Ketone und Aldehyde absorbieren stark im Infrarotspektrum bei 1700 cm-1. Die genaue Position des Peaks hängt von den Substituenten ab. ⓘ
Während die 1H-NMR-Spektroskopie im Allgemeinen nicht zum Nachweis eines Ketons geeignet ist, zeigen 13C-NMR-Spektren je nach Struktur Signale, die etwas unterhalb von 200 ppm liegen. Solche Signale sind in der Regel schwach, da es keine Overhauser-Kerneffekte gibt. Da Aldehyde bei ähnlichen chemischen Verschiebungen mitschwingen, werden zur definitiven Unterscheidung von Aldehyden und Ketonen Mehrfachresonanzexperimente durchgeführt. ⓘ
Qualitative organische Tests
Ketone ergeben positive Ergebnisse im Brady-Test, der Reaktion mit 2,4-Dinitrophenylhydrazin zum entsprechenden Hydrazon. Ketone können von Aldehyden unterschieden werden, indem sie mit dem Tollens'schen Reagenz oder mit Fehlingscher Lösung ein negatives Ergebnis liefern. Methylketone führen zu positiven Ergebnissen beim Jodoformtest. Ketone führen auch zu positiven Ergebnissen, wenn sie mit m-Dinitrobenzol in Gegenwart von verdünntem Natriumhydroxid behandelt werden und eine Violettfärbung erhalten. ⓘ
Synthese
Es gibt zahlreiche Methoden zur Herstellung von Ketonen in industriellen und akademischen Laboratorien. Ketone werden auch auf verschiedene Weise von Organismen hergestellt; siehe den Abschnitt über Biochemie weiter unten. ⓘ
In der Industrie ist die wohl wichtigste Methode die Oxidation von Kohlenwasserstoffen, häufig mit Luft. Zum Beispiel werden jährlich eine Milliarde Kilogramm Cyclohexanon durch aerobe Oxidation von Cyclohexan hergestellt. Aceton wird durch Luftoxidation von Cumol hergestellt. ⓘ
Für spezielle oder kleine Anwendungen in der organischen Synthese werden Ketone häufig durch Oxidation sekundärer Alkohole hergestellt:
- R2CH(OH) + O → R2C=O + H2O
Typische starke Oxidationsmittel (Quelle von "O" in der obigen Reaktion) sind Kaliumpermanganat oder eine Cr(VI)-Verbindung. Bei milderen Bedingungen kommen die Dess-Martin-Periodinan- oder die Moffatt-Swern-Methode zum Einsatz. ⓘ
Es wurden zahlreiche weitere Methoden entwickelt, wie z. B.:
- Hydrolyse von Geminalhalogeniden.
- durch Hydratisierung von Alkinen. Diese Prozesse laufen über Enole ab und erfordern die Anwesenheit einer Säure und HgSO4. Die anschließende Enol-Keto-Tautomerisierung ergibt ein Keton. Die einzige Ausnahme ist die Hydratation von Acetylen, bei der Acetaldehyd entsteht.
- Von Weinreb Amide unter Verwendung stöchiometrischer metallorganischer Reagenzien.
- Aromatische Ketone können durch die Friedel-Crafts-Acylierung, die verwandte Houben-Hoesch-Reaktion und die Fries-Umlagerung hergestellt werden.
- Bei der Ozonolyse und den damit verbundenen Dihydroxylierungs-/Oxidationsreaktionen werden Alkene gespalten, wobei je nach Substitutionsmuster des Alkens Aldehyde oder Ketone entstehen.
- Bei der Kornblum-DeLaMare-Umlagerung werden Ketone aus Peroxiden und Basen hergestellt.
- Bei der Ruzicka-Cyclisierung werden cyclische Ketone aus Dicarbonsäuren hergestellt.
- Bei der Nef-Reaktion entstehen Ketone durch Hydrolyse von Salzen sekundärer Nitroverbindungen.
- Bei der Fukuyama-Kupplung bilden sich Ketone aus einem Thioester und einer Organozinkverbindung.
- Durch die Reaktion eines Säurechlorids mit Organocadmiumverbindungen oder Organokupferverbindungen.
- Die Dakin-West-Reaktion ist eine effiziente Methode zur Herstellung bestimmter Methylketone aus Carbonsäuren.
- Ketone können auch durch die Reaktion von Grignard-Reagenzien mit Nitrilen und anschließende Hydrolyse hergestellt werden.
- Durch Decarboxylierung von Carbonsäureanhydriden.
- Ketone können aus Haloketonen durch reduktive Dehalogenierung von Halogenketonen hergestellt werden.
- Bei der ketonischen Decarboxylierung werden symmetrische Ketone aus Carbonsäuren hergestellt.
- Oxidation von Aminen mit Eisen(III)-chlorid.
- Hydrolyse von ungesättigten sekundären Amiden, β-Ketosäureestern oder β-Diketonen.
- Säure-katalysierte Umlagerung von 1,2-Diolen. ⓘ
Reaktionen
Ketone sind an zahlreichen organischen Reaktionen beteiligt. Die wichtigsten Reaktionen ergeben sich aus der Anfälligkeit des Carbonylkohlenstoffs für nukleophile Additionen und der Neigung der Enolate, an Elektrophile zu addieren. Zu den nukleophilen Additionen gehören in ungefährer Reihenfolge ihrer Allgemeinheit:
- mit Wasser (Hydratation) zu geminalen Diolen, die normalerweise nicht in nennenswerten (oder beobachtbaren) Mengen gebildet werden
- mit einem Acetylid zur Bildung des α-Hydroxyalkins
- mit Ammoniak oder einem primären Amin ergibt ein Imin
- mit sekundärem Amin ergibt ein Enamin
- mit Grignard- und Organolithium-Reagenzien ergibt nach wässriger Aufarbeitung einen tertiären Alkohol
- mit Alkoholen oder Alkoxiden zum Hemiketal oder dessen konjugierter Base. Mit einem Diol zum Ketal. Diese Reaktion wird zum Schutz von Ketonen eingesetzt.
- Mit Natriumamid zur Spaltung der C-C-Bindung unter Bildung des Amids RCONH2 und des Alkans oder Arens R'H, eine Reaktion, die Haller-Bauer-Reaktion genannt wird.
- Mit starken Oxidationsmitteln zur Bildung von Carbonsäuren.
- Elektrophile Addition, Reaktion mit einem Elektrophil ergibt ein resonanzstabilisiertes Kation
- mit Phosphoniumyliden in der Wittig-Reaktion zu den Alkenen
- mit Thiolen zum Thioacetal
- mit Hydrazin oder 1-disubstituierten Derivaten von Hydrazin zur Bildung von Hydrazonen.
- Mit einem Metallhydrid erhält man ein Metallalkoxidsalz, dessen Hydrolyse den Alkohol ergibt, ein Beispiel für eine Ketonreduktion
- mit Halogenen zur Bildung eines α-Halogenketons, eine Reaktion, die über ein Enol abläuft (siehe Haloform-Reaktion)
- mit schwerem Wasser unter Bildung eines α-deuterierten Ketons
- Fragmentierung bei der photochemischen Norrish-Reaktion
- Reaktion von 1,4-Aminodiketonen zu Oxazolen durch Dehydratisierung in der Robinson-Gabriel-Synthese
- im Falle von Arylalkylketonen mit Schwefel und einem Amin zu Amiden in der Willgerodt-Reaktion
- mit Hydroxylamin zur Bildung von Oximen
- mit Reduktionsmitteln zur Bildung sekundärer Alkohole
- mit Peroxysäuren zur Bildung von Estern in der Baeyer-Villiger-Oxidation ⓘ
Ketone gehen, ähnlich wie Aldehyde, Additions- und Kondensationsreaktionen ein. ⓘ
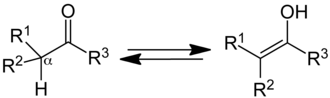
Ketone (R1, R2, R3 = Organyl-Rest) stehen mit ihrer tautomeren Form, den Enolen im Gleichgewicht (Keto-Enol-Tautomerie), wenn an das α-Kohlenstoffatom ein Wasserstoffatom gebunden ist:
Bei der Umsetzung des Vollacetals mit Wasser entsteht säurekatalysiert wieder das Keton, d. h. die Schutzgruppe wird abgespalten. ⓘ
Ketone lassen sich im Gegensatz zu den Aldehyden nur unter drastischen Reaktionsbedingungen oxidativ angreifen. Dabei wird eine Bindung zwischen Carbonylkohlenstoff und einem Nachbarkohlenstoff gespalten. Die entstehenden Molekülbruchstücke sind Carbonsäuren. ⓘ
Biochemie
Ketone sind in der Natur allgegenwärtig. Die Bildung von organischen Verbindungen in der Photosynthese erfolgt über das Keton Ribulose-1,5-bisphosphat. Viele Zucker sind Ketone, die unter der Bezeichnung Ketosen zusammengefasst werden. Die bekannteste Ketose ist die Fruktose; sie liegt meist als zyklisches Hemiketal vor, das die funktionelle Ketongruppe verdeckt. Die Fettsäuresynthese erfolgt über Ketone. Acetoacetat ist ein Zwischenprodukt im Krebszyklus, der Energie aus Zuckern und Kohlenhydraten freisetzt. ⓘ
In der Medizin werden Aceton, Acetoacetat und Beta-Hydroxybutyrat zusammen als Ketonkörper bezeichnet, die bei den meisten Wirbeltieren, einschließlich des Menschen, aus Kohlenhydraten, Fettsäuren und Aminosäuren gebildet werden. Ketonkörper sind im Blut erhöht (Ketose) nach dem Fasten, einschließlich einer Schlafnacht; in Blut und Urin bei Hunger; bei Hypoglykämie, die auf andere Ursachen als Hyperinsulinismus zurückzuführen ist; bei verschiedenen angeborenen Stoffwechselstörungen und absichtlich durch eine ketogene Diät herbeigeführt, sowie bei Ketoazidose (in der Regel aufgrund von Diabetes mellitus). Obwohl die Ketoazidose charakteristisch für dekompensierten oder unbehandelten Typ-1-Diabetes ist, können Ketose oder sogar Ketoazidose unter bestimmten Umständen auch bei Typ-2-Diabetes auftreten. ⓘ
Anwendungen
Ketone werden in großem Maßstab in der Industrie als Lösungsmittel, Polymervorläufer und Arzneimittel hergestellt. Die wichtigsten Ketone in diesem Zusammenhang sind Aceton, Methylethylketon und Cyclohexanon. Sie kommen auch in der Biochemie vor, allerdings in geringerem Maße als in der organischen Chemie im Allgemeinen. Die Verbrennung von Kohlenwasserstoffen ist ein unkontrollierter Oxidationsprozess, bei dem Ketone und viele andere Arten von Verbindungen entstehen. ⓘ
Toxizität
Obwohl es schwierig ist, die Toxizität einer so breiten Klasse von Verbindungen zu verallgemeinern, sind einfache Ketone im Allgemeinen nicht sehr giftig. Diese Eigenschaft ist ein Grund für ihre Beliebtheit als Lösungsmittel. Ausnahmen von dieser Regel sind die ungesättigten Ketone wie Methylvinylketon mit einer LD50 von 7 mg/kg (oral). ⓘ
Eigenschaften
Niedermolekulare Ketone sind farblose, leichtbewegliche Flüssigkeiten und aufgrund der Polarität der Carbonylgruppe in Wasser löslich. Niedermolekulare Ketone zeichnen sich durch einen meist angenehmen, fruchtigen Geruch aus. Höhermolekulare Ketone sind feste Stoffe. ⓘ
Ketone besitzen auf Grund des +I-Effekts der Alkylsubstituenten am Carbonyl-Kohlenstoffatom eine niedrigere Reaktionsfreudigkeit als Aldehyde und neigen nicht zur Polymerisation. Im Unterschied zu den Aldehyden erfolgt mit Ketonen keine Reaktion bei der Fehling-Probe, da die Ketongruppe unter Erhalt des Kohlenstoffgerüsts nicht weiter oxidiert werden kann. ⓘ
Wichtige Vertreter der Ketone
- Aceton, Cyclohexanon
- Himbeerketon, Mycosporin
- Butinon, der einfachste Vertreter der Ketone mit einer zusätzlichen C≡C-Dreifachbindung ⓘ
Verwendung
- Aceton: Lösungsmittel, Reinigungsmittel
- Cyclohexanon: Herstellung von Perlon
- Himbeerketon: Aromatisierung von Lebensmitteln (Geruch nach Himbeeren) ⓘ
Spektroskopie von Ketonen
In IR-Spektren von Ketonen und Aldehyden findet man die charakteristische Bande der C=O-Valenzschwingung im Bereich von 1690 bis 1750 cm−1. ⓘ