Darmflora
Die Darmmikrobiota sind die Mikroorganismen, einschließlich Bakterien und Archaeen, die im Verdauungstrakt von Wirbeltieren, einschließlich Menschen, und von Insekten leben. Alternative Begriffe sind Darmflora (ein veralteter Begriff, der sich technisch gesehen auf Pflanzen bezieht) und Darmmikrobiom. Das gastrointestinale Metagenom (manchmal auch als Mikrobiom bezeichnet) ist die Gesamtheit aller Genome der Darmmikrobiota. Beim Menschen ist der Darm der Hauptort der menschlichen Mikrobiota. Die Darmmikrobiota hat weitreichende Auswirkungen, u. a. auf die Besiedlung, die Resistenz gegen Krankheitserreger, die Aufrechterhaltung des Darmepithels, die Verstoffwechselung von Nahrungsmitteln und Arzneimitteln, die Steuerung der Immunfunktion und sogar das Verhalten über die Darm-Hirn-Achse. ⓘ
Die mikrobielle Zusammensetzung der Darmmikrobiota variiert je nach Region des Verdauungstrakts. Der Dickdarm weist mit 300 bis 1000 verschiedenen Arten die höchste Mikrobendichte auf, die in irgendeinem Lebensraum der Erde festgestellt wurde. Allerdings stammen 99 % der Darmbakterien von etwa 30 bis 40 Arten ab. Bakterien machen auch bis zu 60 % der Trockenmasse des Stuhls aus. Über 99 % der Bakterien im Darm sind Anaerobier, aber im Blinddarm erreichen aerobe Bakterien hohe Dichten. Man schätzt, dass die menschliche Darmmikrobiota etwa hundertmal so viele Gene besitzt wie das menschliche Genom. ⓘ
Die Bezeichnung „Flora“ beruht auf der früher vertretenen Auffassung, Bakterien und viele andere Mikroorganismen gehörten zum Pflanzenreich. Da Bakterien heute eine eigene Domäne bilden, sollte richtigerweise von einer Darmmikroorganismengemeinschaft oder von einer Darmmikrobiota gesprochen werden. Diese Bezeichnungen setzen sich in der Medizin nur langsam durch. ⓘ
Daneben finden sich im menschlichen Darm eine Vielzahl an – überwiegend harmlosen – Viren, etwa Bakteriophagen, die Bakterien abbauen. ⓘ
Überblick
Die Darmmikrobiota des Menschen weist im Vergleich zu anderen Bereichen des Körpers die größte Anzahl von Bakterien und die größte Anzahl von Arten auf. Beim Menschen ist die Darmflora ein bis zwei Jahre nach der Geburt etabliert. Zu diesem Zeitpunkt haben sich das Darmepithel und die von ihm gebildete Darmschleimhautbarriere so entwickelt, dass sie die Darmflora tolerieren und sogar unterstützen und gleichzeitig eine Barriere für pathogene Organismen bilden. ⓘ
Die Beziehung zwischen einigen Darmfloraarten und dem Menschen ist nicht nur eine Kommensale (eine nicht schädliche Koexistenz), sondern vielmehr eine mutualistische Beziehung. Einige Mikroorganismen des menschlichen Darms nützen dem Wirt, indem sie Ballaststoffe in kurzkettige Fettsäuren (SCFAs) wie Essigsäure und Buttersäure fermentieren, die dann vom Wirt aufgenommen werden. Darmbakterien spielen auch eine Rolle bei der Synthese von Vitamin B und Vitamin K sowie bei der Metabolisierung von Gallensäuren, Sterolen und Xenobiotika. Die systemische Bedeutung der SCFAs und anderer Verbindungen, die sie produzieren, sind wie Hormone, und die Darmflora selbst scheint wie ein endokrines Organ zu funktionieren, und eine Dysregulation der Darmflora wurde mit einer Vielzahl von Entzündungs- und Autoimmunerkrankungen in Verbindung gebracht. ⓘ
Die Zusammensetzung der menschlichen Darmmikrobiota ändert sich im Laufe der Zeit, wenn sich die Ernährung ändert und wenn sich der allgemeine Gesundheitszustand ändert. Eine systematische Übersichtsarbeit aus dem Jahr 2016 untersuchte die präklinischen und kleinen Humanstudien, die mit bestimmten im Handel erhältlichen probiotischen Bakterienstämmen durchgeführt wurden, und identifizierte diejenigen, die das größte Potenzial haben, bei bestimmten Erkrankungen des zentralen Nervensystems nützlich zu sein. ⓘ
Klassifizierungen
Die mikrobielle Zusammensetzung der Darmmikrobiota variiert im gesamten Verdauungstrakt. Im Magen und im Dünndarm sind im Allgemeinen nur relativ wenige Bakterienarten vorhanden. Der Dickdarm hingegen weist mit bis zu 1012 Zellen pro Gramm Darminhalt die höchste mikrobielle Dichte auf, die in irgendeinem Lebensraum der Erde festgestellt wurde. Diese Bakterien repräsentieren zwischen 300 und 1000 verschiedene Arten. Allerdings stammen 99 % der Bakterien aus etwa 30 bis 40 Arten. Infolge ihrer Häufigkeit im Darm machen Bakterien auch bis zu 60 % der Trockenmasse des Stuhls aus. Pilze, Protisten, Archaeen und Viren sind ebenfalls in der Darmflora vertreten, doch ist über ihre Aktivitäten weniger bekannt. ⓘ
Über 99 % der Bakterien im Darm sind Anaerobier, aber im Blinddarm erreichen aerobe Bakterien hohe Dichten. Es wird geschätzt, dass diese Darmflora insgesamt etwa hundertmal so viele Gene besitzt wie das menschliche Genom. ⓘ
Viele Arten im Darm sind außerhalb ihrer Wirte nicht untersucht worden, da die meisten nicht kultiviert werden können. Es gibt zwar eine kleine Anzahl von Kernspezies von Mikroben, die von den meisten Menschen geteilt werden, aber die Mikrobenpopulationen können von Mensch zu Mensch stark variieren. Innerhalb eines Individuums bleiben die Mikrobenpopulationen im Laufe der Zeit relativ konstant, auch wenn es bei Änderungen der Lebensweise, der Ernährung und des Alters zu gewissen Veränderungen kommen kann. Das Human Microbiome Project hat sich zum Ziel gesetzt, die Mikrobiota des menschlichen Darms und anderer Körperstellen besser zu beschreiben. ⓘ
Die vier vorherrschenden Bakteriengattungen im menschlichen Darm sind Bacillota, Bacteroidota, Actinomycetota und Pseudomonadota. Die meisten Bakterien gehören zu den Gattungen Bacteroides, Clostridium, Faecalibacterium, Eubacterium, Ruminococcus, Peptococcus, Peptostreptococcus und Bifidobacterium. Andere Gattungen, wie Escherichia und Lactobacillus, sind in geringerem Umfang vertreten. Allein die Arten der Gattung Bacteroides machen etwa 30 % aller Bakterien im Darm aus, was darauf schließen lässt, dass diese Gattung für das Funktionieren des Wirts besonders wichtig ist. ⓘ
Zu den Pilzgattungen, die im Darm nachgewiesen wurden, gehören unter anderem Candida, Saccharomyces, Aspergillus, Penicillium, Rhodotorula, Trametes, Pleospora, Sclerotinia, Bullera und Galactomyces. Rhodotorula wird am häufigsten bei Personen mit entzündlichen Darmerkrankungen gefunden, während Candida am häufigsten bei Personen mit Hepatitis-B-Zirrhose und chronischer Hepatitis B vorkommt. ⓘ
Archaeen bilden eine weitere große Klasse der Darmflora, die für den Stoffwechsel der bakteriellen Gärungsprodukte wichtig sind. ⓘ
Die Industrialisierung geht mit Veränderungen in der Mikrobiota einher, und die Verringerung der Vielfalt könnte bestimmte Arten zum Aussterben bringen. 2018 schlugen Forscher ein Biobank-Repository der menschlichen Mikrobiota vor. ⓘ
Enterotyp
Ein Enterotyp ist eine Klassifizierung von Lebewesen auf der Grundlage ihres bakteriologischen Ökosystems im menschlichen Darmmikrobiom, die nicht durch Alter, Geschlecht, Körpergewicht oder nationale Zugehörigkeit bestimmt ist. Es gibt Hinweise darauf, dass die langfristige Ernährung den Enterotyp beeinflusst. Es wurden drei menschliche Enterotypen vorgeschlagen, deren Wert jedoch in Frage gestellt wird. ⓘ
Zusammensetzung
Bakteriom
Magen
Aufgrund des hohen Säuregehalts des Magens können die meisten Mikroorganismen dort nicht überleben. Zu den wichtigsten bakteriellen Bewohnern des Magens gehören: Streptococcus, Staphylococcus, Lactobacillus, Peptostreptococcus. Helicobacter pylori ist ein gramnegatives, spiralförmiges Bakterium, das sich auf der Magenschleimhaut ansiedelt und chronische Gastritis sowie Magengeschwüre verursacht und ein Karzinogen für Magenkrebs ist. ⓘ
Eingeweide
| Bakterien, die häufig im menschlichen Dickdarm vorkommen ⓘ | |
| Bakterium | Vorkommen (%) |
|---|---|
| Bacteroides fragilis | 100 |
| Bacteroides melaninogenicus | 100 |
| Bacteroides oralis | 100 |
| Enterococcus faecalis | 100 |
| Escherichia coli | 100 |
| Enterobacter sp. | 40–80 |
| Klebsiella sp. | 40–80 |
| Bifidobakterium bifidum | 30–70 |
| Staphylokokkus aureus | 30–50 |
| Lactobacillus | 20–60 |
| Clostridium perfringens | 25–35 |
| Proteus mirabilis | 5–55 |
| Clostridium tetani | 1–35 |
| Clostridium septicum | 5–25 |
| Pseudomonas aeruginosa | 3–11 |
| Salmonella enterica | 3–7 |
| Fäkalienbakterium prausnitzii | ?häufig |
| Peptostreptokokkus sp. | ?häufig |
| Peptococcus sp. | ?häufig |
Der Dünndarm enthält aufgrund der Nähe und des Einflusses des Magens eine geringe Menge an Mikroorganismen. Gram-positive Kokken und stäbchenförmige Bakterien sind die vorherrschenden Mikroorganismen im Dünndarm. Im distalen Teil des Dünndarms begünstigen alkalische Bedingungen jedoch gramnegative Bakterien der Enterobacteriaceae. Die bakterielle Flora des Dünndarms ist an einer Vielzahl von Darmfunktionen beteiligt. Die bakterielle Flora liefert regulatorische Signale, die die Entwicklung und den Nutzen des Darms ermöglichen. Eine Überwucherung der Bakterien im Dünndarm kann zu einem Versagen des Darms führen. Darüber hinaus enthält der Dickdarm das größte bakterielle Ökosystem im menschlichen Körper. Etwa 99 % der Flora des Dickdarms und der Fäkalien bestehen aus obligaten Anaerobiern wie Bacteroides und Bifidobacterium. Zu den Faktoren, die die Mikroorganismenpopulation des Dickdarms stören, gehören Antibiotika, Stress und Parasiten. ⓘ
Bakterien machen den größten Teil der Flora im Dickdarm und 60 % der Trockenmasse des Stuhls aus. Diese Tatsache macht Fäkalien zu einer idealen Quelle der Darmflora für alle Tests und Experimente, bei denen die Nukleinsäure aus Fäkalienproben extrahiert und bakterielle 16S rRNA-Gensequenzen mit bakteriellen Primern erstellt werden. Diese Form der Untersuchung ist auch oft invasiveren Techniken wie Biopsien vorzuziehen. ⓘ
Fünf Phyla dominieren die Darmmikrobiota: Bacteroidota, Bacillota, Actinomycetota, Pseudomonadota und Verrucomicrobiota - wobei Bacteroidota und Bacillota 90% der Zusammensetzung ausmachen. Im Darm leben zwischen 300 und 1000 verschiedene Arten, wobei die meisten Schätzungen bei etwa 500 liegen. Es ist jedoch wahrscheinlich, dass 99 % der Bakterien aus etwa 30 oder 40 Arten stammen, wobei Faecalibacterium prausnitzii (Phylum firmicutes) die häufigste Art bei gesunden Erwachsenen ist. ⓘ
Forschungsergebnisse deuten darauf hin, dass die Beziehung zwischen der Darmflora und dem Menschen nicht nur eine Kommensale (eine nicht schädliche Koexistenz), sondern vielmehr eine wechselseitige, symbiotische Beziehung ist. Obwohl der Mensch auch ohne Darmflora überleben kann, erfüllen die Mikroorganismen eine Vielzahl nützlicher Funktionen, wie z. B. die Fermentierung ungenutzter Energiesubstrate, die Ausbildung des Immunsystems durch Stoffwechselendprodukte wie Propionat und Acetat, die Verhinderung des Wachstums schädlicher Arten, die Regulierung der Entwicklung des Darms, die Produktion von Vitaminen für den Wirt (z. B. Biotin und Vitamin K) und die Produktion von Hormonen, die den Wirt zur Speicherung von Fetten anleiten. Weitreichende Veränderungen und Ungleichgewichte der Darmmikrobiota und ihres Mikrobioms oder ihrer Gensammlung werden mit Fettleibigkeit in Verbindung gebracht. Es wird jedoch angenommen, dass einige Arten unter bestimmten Bedingungen in der Lage sind, Krankheiten zu verursachen, indem sie Infektionen hervorrufen oder das Krebsrisiko für den Wirt erhöhen. ⓘ
Mykobiom
Pilze und Protisten machen ebenfalls einen Teil der Darmflora aus, aber über ihre Aktivitäten ist weniger bekannt. ⓘ
Virom
Das menschliche Virom besteht hauptsächlich aus Bakteriophagen. ⓘ
Darmflora des Hundes
Die Darmflora bei Hunden besteht zu 99 % aus fünf bakteriellen Abteilungen. Neben den Firmicutes, Bacteroidetes, Proteobacteria und Actinobacteria wie beim Menschen kommen beim Hund Fusobacteria vor. Im Magen finden sich bei gesunden Hunden Helicobacter spp., die die Magenschleimhaut einschließlich der Magendrüsen invasiv besiedeln. Im Dünndarm überwiegen Clostridia, Milchsäurebakterien und Proteobacteria, im Dickdarm Clostridiales, Bacteroides, Prevotella und Fusobacteria. Dabei ist zu beachten, dass jedes Tier ein individuelles intestinales Mikrobiom besitzt. ⓘ
Veränderung
Alter
Es hat sich gezeigt, dass sich die Zusammensetzung des Mikrobioms im Laufe des Lebens nach bestimmten Mustern entwickelt. Im Allgemeinen ist die Vielfalt der Zusammensetzung der Mikrobiota in Stuhlproben bei Erwachsenen deutlich höher als bei Kindern, obwohl die interpersonellen Unterschiede bei Kindern größer sind als bei Erwachsenen. Ein Großteil der Reifung der Mikrobiota zu einer erwachsenenähnlichen Konfiguration findet in den ersten drei Lebensjahren statt. ⓘ
In dem Maße, wie sich die Zusammensetzung des Mikrobioms verändert, ändert sich auch die Zusammensetzung der im Darm produzierten bakteriellen Proteine. In Mikrobiomen von Erwachsenen wurde eine hohe Prävalenz von Enzymen festgestellt, die an der Fermentation, Methanogenese und dem Stoffwechsel von Arginin, Glutamat, Aspartat und Lysin beteiligt sind. In Mikrobiomen von Säuglingen hingegen dominieren Enzyme, die am Cystein-Stoffwechsel und an Fermentationswegen beteiligt sind. ⓘ
Geografie
Die Zusammensetzung des Darmmikrobioms hängt von der geografischen Herkunft der Populationen ab. Unterschiede in der Verteilung von Prevotella, der Repräsentation des Urease-Gens und der Repräsentation von Genen, die für die Glutamat-Synthase/den Glutamat-Abbau oder andere Enzyme kodieren, die am Abbau von Aminosäuren oder an der Vitamin-Biosynthese beteiligt sind, zeigen signifikante Unterschiede zwischen Populationen aus den USA, Malawi oder indianischer Herkunft. ⓘ
In der US-Bevölkerung sind Enzyme, die für den Abbau von Glutamin kodieren, und Enzyme, die an der Vitamin- und Liponsäurebiosynthese beteiligt sind, stark vertreten, während in der Bevölkerung Malawis und der indianischen Bevölkerung Enzyme, die für Glutamatsynthase kodieren, stark vertreten sind und auch die α-Amylase in ihren Mikrobiomen überrepräsentiert ist. Da die US-amerikanische Bevölkerung sich fettreicher ernährt als die indianische oder malawische Bevölkerung, deren Ernährung reich an Mais ist, ist die Ernährung wahrscheinlich der Hauptfaktor für die Zusammensetzung der Darmbakterien. ⓘ
Weitere Studien haben gezeigt, dass es große Unterschiede in der Zusammensetzung der Mikrobiota zwischen europäischen und afrikanischen Landkindern gibt. Die Fäkalbakterien von Kindern aus Florenz wurden mit denen von Kindern aus dem kleinen ländlichen Dorf Boulpon in Burkina Faso verglichen. Die Ernährung eines typischen Kindes in diesem Dorf enthält kaum Fette und tierische Proteine und ist reich an Polysacchariden und pflanzlichen Proteinen. Die Fäkalbakterien der europäischen Kinder wurden von Firmicutes dominiert und wiesen eine deutlich geringere Artenvielfalt auf, während die Fäkalbakterien der Kinder aus Boulpon von Bacteroidetes dominiert wurden. Die größere Artenvielfalt und die unterschiedliche Zusammensetzung der Darmflora in afrikanischen Bevölkerungen könnte die Verdauung normalerweise unverdaulicher pflanzlicher Polysaccharide erleichtern und auch zu einem geringeren Auftreten nicht-infektiöser Darmerkrankungen führen. ⓘ
In kleinerem Maßstab hat sich gezeigt, dass zahlreiche gemeinsame Umwelteinflüsse in einer Familie die Zusammensetzung des individuellen Mikrobioms stark beeinflussen. Dieser Effekt hat keinen genetischen Einfluss und wird durchweg in kulturell unterschiedlichen Populationen beobachtet. ⓘ
Unterernährung
Unterernährte Kinder haben eine weniger reife und weniger vielfältige Darmmikrobiota als gesunde Kinder, und Veränderungen im Mikrobiom, die mit Nährstoffmangel einhergehen, können wiederum eine pathophysiologische Ursache für Unterernährung sein. Unterernährte Kinder haben in der Regel auch mehr potenziell pathogene Darmflora und mehr Hefepilze in Mund und Rachen. Eine Änderung der Ernährung kann zu Veränderungen in der Zusammensetzung und Vielfalt der Darmmikrobiota führen. ⓘ
Rasse und ethnische Zugehörigkeit
Forscher des American Gut Project und des Human Microbiome Project fanden heraus, dass zwölf Mikrobenfamilien je nach Rasse oder ethnischer Zugehörigkeit der Person unterschiedlich häufig vorkommen. Die Stärke dieser Assoziationen ist durch die geringe Stichprobengröße begrenzt: Das American Gut Project sammelte Daten von 1 375 Personen, von denen 90 % weiß waren. Die HELIUS-Studie (Healthy Life in an Urban Setting) in Amsterdam ergab, dass Personen niederländischer Abstammung die höchste Diversität der Darmmikrobiota aufwiesen, während Personen südasiatischer und surinamischer Abstammung die geringste Diversität hatten. Die Studienergebnisse deuten darauf hin, dass Personen gleicher Rasse oder ethnischer Zugehörigkeit ein ähnlicheres Mikrobiom haben als Personen mit unterschiedlichem rassischen Hintergrund. ⓘ
Sozioökonomischer Status
Für das Jahr 2020 haben mindestens zwei Studien einen Zusammenhang zwischen dem sozioökonomischen Status (SES) einer Person und ihrer Darmmikrobiota nachgewiesen. In einer Studie in Chicago wurde festgestellt, dass Personen in Stadtvierteln mit höherem sozioökonomischen Status eine größere Vielfalt der Mikrobiota aufwiesen. Menschen aus Stadtvierteln mit höherem Sozialstatus wiesen auch mehr Bacteroides-Bakterien auf. In ähnlicher Weise ergab eine Zwillingsstudie im Vereinigten Königreich, dass ein höherer sozialer Status auch mit einer größeren Vielfalt im Darm verbunden war. ⓘ
Erwerb bei menschlichen Säuglingen
Der Aufbau einer Darmflora ist von entscheidender Bedeutung für die Gesundheit eines Erwachsenen und für das Funktionieren des Magen-Darm-Trakts. Beim Menschen bildet sich eine Darmflora, die der eines Erwachsenen ähnelt, innerhalb von ein bis zwei Jahren nach der Geburt, da die Mikrobiota durch die Übertragung von Eltern auf Kinder sowie durch Nahrung, Wasser und andere Umweltquellen erworben wird. ⓘ
Traditionell wird der Gastrointestinaltrakt eines normalen Fötus als steril angesehen, obwohl diese Ansicht in den letzten Jahren in Frage gestellt wurde. In den letzten Jahren wurde diese Ansicht jedoch in Frage gestellt. Es gibt inzwischen mehrere Hinweise darauf, dass sich in der intrauterinen Umgebung Bakterien befinden können. Beim Menschen haben Forschungen gezeigt, dass eine mikrobielle Besiedlung des Fötus möglich ist. In einer Studie wurden Lactobacillus- und Bifidobacterium-Arten in Plazenta-Biopsien nachgewiesen. Mehrere Studien an Nagetieren haben das Vorhandensein von Bakterien im Fruchtwasser und in der Plazenta sowie im Mekonium von Säuglingen, die durch einen sterilen Kaiserschnitt geboren wurden, nachgewiesen. In einer anderen Studie verabreichten Forscher einer schwangeren Mutter eine Bakterienkultur oral und wiesen die Bakterien in den Nachkommen nach, was wahrscheinlich auf eine Übertragung zwischen Verdauungstrakt und Fruchtwasser über den Blutkreislauf zurückzuführen ist. Die Forscher geben jedoch zu bedenken, dass die Quelle dieser intrauterinen Bakterien, ob sie lebendig sind und welche Rolle sie spielen, noch nicht bekannt ist. ⓘ
Während der Geburt und kurz danach besiedeln Bakterien von der Mutter und aus der Umgebung den Darm des Säuglings. Die genauen Quellen der Bakterien sind noch nicht vollständig geklärt, aber es könnte sich um den Geburtskanal, andere Personen (Eltern, Geschwister, Krankenhauspersonal), Muttermilch, Nahrungsmittel und die allgemeine Umgebung handeln, mit der der Säugling in Kontakt kommt. Die Forschung hat gezeigt, dass sich das Mikrobiom von vaginal geborenen Säuglingen deutlich von dem von Säuglingen unterscheidet, die per Kaiserschnitt entbunden wurden, und dass vaginal geborene Säuglinge die meisten ihrer Darmbakterien von der Mutter erhalten, während die Mikrobiota von Kaiserschnitt-Säuglingen mehr Bakterien aufweist, die mit der Krankenhausumgebung in Verbindung stehen. ⓘ
Im ersten Lebensjahr ist die Zusammensetzung der Darmflora in der Regel einfach und ändert sich im Laufe der Zeit sehr stark, und sie ist nicht bei allen Menschen gleich. Bei der ersten Bakterienpopulation handelt es sich in der Regel um fakultativ anaerobe Organismen; die Forscher glauben, dass diese Erstbesiedler die Sauerstoffkonzentration im Darm verringern, was wiederum obligat anaeroben Bakterien wie Bacteroidota, Actinomycetota und Bacillota ermöglicht, sich zu etablieren und zu gedeihen. Gestillte Säuglinge werden von Bifidobakterien dominiert, was möglicherweise auf den Gehalt an bifidobakteriellen Wachstumsfaktoren in der Muttermilch und auf die Tatsache zurückzuführen ist, dass die Muttermilch präbiotische Komponenten enthält, die ein gesundes Bakterienwachstum ermöglichen. Im Gegensatz dazu ist die Mikrobiota von Säuglingen, die mit künstlicher Säuglingsnahrung ernährt werden, vielfältiger und weist eine hohe Anzahl von Enterobacteriaceae, Enterokokken, Bifidobakterien, Bacteroides und Clostridien auf. ⓘ
Kaiserschnitt, Antibiotika und Säuglingsnahrung können die Zusammensetzung des Darmmikrobioms verändern. Kinder, die mit Antibiotika behandelt werden, haben weniger stabile und weniger vielfältige Blütengemeinschaften. Es hat sich gezeigt, dass Kaiserschnitte die Übertragung von Bakterien zwischen Mutter und Kind stören, was sich auf die allgemeine Gesundheit der Nachkommen auswirkt, indem es das Risiko für Krankheiten wie Zöliakie, Asthma und Typ-1-Diabetes erhöht. Dies ist ein weiterer Beweis dafür, wie wichtig ein gesundes Darmmikrobiom ist. Es werden verschiedene Methoden zur Wiederherstellung des Mikrobioms erforscht, wobei der Säugling in der Regel dem mütterlichen Vaginalinhalt ausgesetzt wird und Probiotika oral eingenommen werden. ⓘ
Funktionen
Als man 1995 mit der Erforschung der Darmflora begann, ging man davon aus, dass sie drei Hauptaufgaben hat: direkte Abwehr von Krankheitserregern, Stärkung der Wirtsabwehr durch ihre Rolle bei der Entwicklung und Aufrechterhaltung des Darmepithels und bei der Induzierung der Antikörperproduktion dort, und Metabolisierung von ansonsten unverdaulichen Verbindungen in der Nahrung; spätere Arbeiten entdeckten ihre Rolle bei der Ausbildung des sich entwickelnden Immunsystems, und weitere Arbeiten konzentrierten sich auf ihre Rolle in der Darm-Hirn-Achse. ⓘ
Direkte Hemmung von Krankheitserregern
Die Gemeinschaft der Darmflora spielt eine direkte Rolle bei der Abwehr von Krankheitserregern, indem sie den Raum vollständig besiedelt, alle verfügbaren Nährstoffe nutzt und Verbindungen absondert, die unerwünschte Organismen, die mit ihr um Nährstoffe konkurrieren würden, abtöten oder hemmen. Verschiedene Darmbakterienstämme verursachen die Produktion unterschiedlicher Zytokine. Zytokine sind chemische Verbindungen, die von unserem Immunsystem produziert werden, um die Entzündungsreaktion gegen Infektionen einzuleiten. Eine Störung der Darmflora ermöglicht es konkurrierenden Organismen wie Clostridium difficile, sich zu etablieren, die sonst in Schach gehalten werden. ⓘ
Entwicklung des Darmschutzes und des Immunsystems
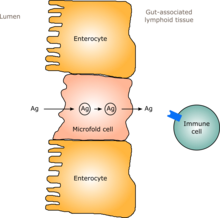
Beim Menschen bildet sich innerhalb von ein bis zwei Jahren nach der Geburt eine Darmflora, die der eines Erwachsenen ähnelt. Mit der Etablierung der Darmflora entwickelt sich auch die Darmschleimhaut - das Darmepithel und die von ihm gebildete Darmschleimhautbarriere - in einer Weise, die in gewissem Maße tolerant und sogar förderlich für kommensalistische Mikroorganismen ist und gleichzeitig eine Barriere für pathogene Mikroorganismen darstellt. Insbesondere vermehren sich die Becherzellen, die die Schleimhaut produzieren, und die Schleimhautschicht verdickt sich, so dass eine äußere Schleimhautschicht entsteht, in der sich "freundliche" Mikroorganismen verankern und ernähren können, und eine innere Schicht, die selbst diese Organismen nicht durchdringen können. Außerdem entwickelt sich in der Zeit, in der sich die Darmflora entwickelt und etabliert, das darmassoziierte lymphatische Gewebe (GALT), das Teil des Darmepithels ist und Krankheitserreger erkennt und auf sie reagiert. Die sich entwickelnde GALT ist tolerant gegenüber Arten der Darmflora, aber nicht gegenüber anderen Mikroorganismen. GALT wird normalerweise auch tolerant gegenüber Nahrungsmitteln, denen der Säugling ausgesetzt ist, sowie gegenüber Verdauungsprodukten aus der Nahrung und den Metaboliten der Darmflora (Moleküle, die aus dem Stoffwechsel entstehen), die aus der Nahrung gewonnen werden. ⓘ
Das menschliche Immunsystem bildet Zytokine, die das Immunsystem zur Produktion von Entzündungen anregen können, um sich selbst zu schützen, und die die Immunreaktion dämpfen können, um die Homöostase aufrechtzuerhalten und die Heilung nach einer Beeinträchtigung oder Verletzung zu ermöglichen. Es hat sich gezeigt, dass verschiedene Bakterienarten, die in der Darmflora vorkommen, das Immunsystem selektiv zur Bildung von Zytokinen anregen können; so scheinen beispielsweise Bacteroides fragilis und einige Clostridienarten eine entzündungshemmende Reaktion hervorzurufen, während einige segmentierte filamentöse Bakterien die Produktion von Entzündungszytokinen fördern. Die Darmflora kann auch die Produktion von Antikörpern durch das Immunsystem regulieren. Eine Funktion dieser Regulierung besteht darin, die B-Zellen zu einem Klassenwechsel zu IgA zu veranlassen. In den meisten Fällen müssen die B-Zellen durch T-Helferzellen aktiviert werden, um den Klassenwechsel zu bewirken. Auf einem anderen Weg bewirkt die Darmflora jedoch eine NF-kB-Signalisierung durch Darmepithelzellen, die zur Ausschüttung weiterer Signalmoleküle führt. Diese Signalmoleküle interagieren mit B-Zellen, um den Klassenwechsel zu IgA einzuleiten. IgA ist eine wichtige Art von Antikörpern, die in Schleimhautumgebungen wie dem Darm verwendet wird. Es hat sich gezeigt, dass IgA zur Diversifizierung der Darmgemeinschaft beiträgt und dabei hilft, Bakterien loszuwerden, die Entzündungsreaktionen verursachen. Letztendlich sorgt IgA für ein gesundes Milieu zwischen dem Wirt und den Darmbakterien. Diese Zytokine und Antikörper können auch außerhalb des Darms, in der Lunge und in anderen Geweben Wirkung zeigen. ⓘ
Das Immunsystem kann auch durch die Fähigkeit der Darmbakterien verändert werden, Stoffwechselprodukte zu produzieren, die Zellen des Immunsystems beeinflussen können. So können beispielsweise kurzkettige Fettsäuren (SCFA) von einigen Darmbakterien durch Fermentation produziert werden. SCFAs stimulieren einen raschen Anstieg der Produktion von angeborenen Immunzellen wie Neutrophilen, Basophilen und Eosinophilen. Diese Zellen sind Teil des angeborenen Immunsystems, das versucht, die Ausbreitung von Infektionen zu begrenzen. ⓘ
Stoffwechsel
Der Stoffwechsel von Tryptophan durch die menschliche gastrointestinale Mikrobiota ()
|
Ohne die Darmflora wäre der menschliche Körper nicht in der Lage, einen Teil der unverdauten Kohlenhydrate, die er zu sich nimmt, zu verwerten, da einige Arten der Darmflora über Enzyme verfügen, die den menschlichen Zellen fehlen, um bestimmte Polysaccharide abzubauen. Nagetiere, die in einer sterilen Umgebung aufgezogen werden und denen die Darmflora fehlt, müssen 30 % mehr Kalorien zu sich nehmen, um das gleiche Gewicht wie ihre normalen Artgenossen zu halten. Zu den Kohlenhydraten, die der Mensch ohne bakterielle Hilfe nicht verdauen kann, gehören bestimmte Stärken, Ballaststoffe, Oligosaccharide und Zucker, die der Körper nicht verdauen und aufnehmen kann, wie Laktose bei Laktoseintoleranz und Zuckeralkohole, vom Darm produzierter Schleim und Proteine. ⓘ
Bakterien verwandeln die von ihnen fermentierten Kohlenhydrate in kurzkettige Fettsäuren durch eine Form der Fermentation, die als saccharolytische Fermentation bezeichnet wird. Zu den Produkten gehören Essigsäure, Propionsäure und Buttersäure. Diese Stoffe können von den Wirtszellen genutzt werden und stellen eine wichtige Energie- und Nährstoffquelle dar. Auch Gase (die an der Signalübertragung beteiligt sind und Blähungen verursachen können) und organische Säuren wie Milchsäure werden durch die Gärung erzeugt. Essigsäure wird von den Muskeln verwendet, Propionsäure erleichtert die ATP-Produktion in der Leber, und Buttersäure liefert Energie für die Darmzellen. ⓘ
Die Darmflora synthetisiert auch Vitamine wie Biotin und Folat und erleichtert die Aufnahme von Mineralien aus der Nahrung, darunter Magnesium, Kalzium und Eisen. Methanobrevibacter smithii ist einzigartig, denn es ist keine Bakterienart, sondern gehört zur Domäne der Archaea und ist die häufigste Methan produzierende Archaeenart in der menschlichen gastrointestinalen Mikrobiota. ⓘ
Die Darmmikrobiota dient auch als Quelle für die Vitamine K und B12, die vom Körper nicht oder nur in geringen Mengen produziert werden. ⓘ
Pharmakomische Mikrobiomik
Das menschliche Metagenom (d. h. die genetische Zusammensetzung eines Individuums und aller Mikroorganismen, die sich auf oder im Körper des Individuums befinden) variiert von Person zu Person erheblich. Da die Gesamtzahl der mikrobiellen und viralen Zellen im menschlichen Körper (mehr als 100 Billionen) die Zahl der Zellen des Homo sapiens (einige Billionen) bei weitem übersteigt, besteht ein beträchtliches Potenzial für Wechselwirkungen zwischen Arzneimitteln und dem Mikrobiom eines Menschen: Arzneimittel verändern die Zusammensetzung des menschlichen Mikrobioms, der Arzneimittelstoffwechsel durch mikrobielle Enzyme verändert das pharmakokinetische Profil des Arzneimittels, und der mikrobielle Arzneimittelstoffwechsel beeinflusst die klinische Wirksamkeit und das Toxizitätsprofil eines Arzneimittels. ⓘ
Abgesehen von Kohlenhydraten kann die Darmmikrobiota auch andere Xenobiotika wie Arzneimittel, sekundäre Pflanzenstoffe und Lebensmittelgifte verstoffwechseln. Es wurde nachgewiesen, dass mehr als 30 Arzneimittel von der Darmmikrobiota verstoffwechselt werden können. Der mikrobielle Stoffwechsel von Arzneimitteln kann manchmal das Arzneimittel inaktivieren. ⓘ
Darm-Gehirn-Achse
Die Darm-Hirn-Achse ist die biochemische Signalübertragung zwischen dem Magen-Darm-Trakt und dem zentralen Nervensystem. Dieser Begriff wurde erweitert, um die Rolle der Darmflora in diesem Wechselspiel einzubeziehen; der Begriff "Mikrobiom-Darm-Hirn-Achse" wird manchmal verwendet, um Paradigmen zu beschreiben, die ausdrücklich die Darmflora einbeziehen. Im weitesten Sinne umfasst die Darm-Hirn-Achse das zentrale Nervensystem, die neuroendokrinen und neuroimmunen Systeme einschließlich der Hypothalamus-Hypophysen-Nebennieren-Achse (HPA-Achse), die sympathischen und parasympathischen Arme des autonomen Nervensystems einschließlich des enterischen Nervensystems, den Vagusnerv und die Darmmikrobiota. ⓘ
Eine systematische Übersichtsarbeit aus dem Jahr 2016 untersuchte die präklinischen und kleinen Humanstudien, die mit bestimmten handelsüblichen probiotischen Bakterienstämmen durchgeführt wurden, und kam zu dem Ergebnis, dass von den getesteten Gattungen Bifidobacterium und Lactobacillus (B. longum, B. breve, B. infantis, L. helveticus, L. rhamnosus, L. plantarum und L. casei) das größte Potenzial für die Behandlung bestimmter Störungen des zentralen Nervensystems haben. ⓘ
Veränderungen im Gleichgewicht der Mikrobiota
Auswirkungen der Einnahme von Antibiotika
Eine Veränderung der Anzahl der Darmbakterien, beispielsweise durch die Einnahme von Breitbandantibiotika, kann sich auf die Gesundheit des Wirts und seine Fähigkeit, Nahrung zu verdauen, auswirken. Antibiotika können antibiotika-assoziierte Diarrhöe verursachen, indem sie den Darm direkt reizen, die Menge der Mikrobiota verändern oder das Wachstum pathogener Bakterien ermöglichen. Eine weitere schädliche Auswirkung von Antibiotika ist die Zunahme von antibiotikaresistenten Bakterien, die nach ihrer Verwendung gefunden werden und die, wenn sie in den Wirt eindringen, Krankheiten verursachen, die mit Antibiotika schwer zu behandeln sind. ⓘ
Eine Veränderung der Anzahl und der Arten der Darmmikrobiota kann die Fähigkeit des Körpers, Kohlenhydrate zu fermentieren und Gallensäuren zu verstoffwechseln, verringern und Durchfall verursachen. Kohlenhydrate, die nicht aufgespalten werden, können zu viel Wasser absorbieren und flüssigen Stuhl verursachen, oder ein Mangel an SCFAs, die von der Darmmikrobiota produziert werden, kann Durchfall verursachen. ⓘ
Eine Verringerung des Gehalts an einheimischen Bakterienarten beeinträchtigt auch deren Fähigkeit, das Wachstum schädlicher Arten wie C. difficile und Salmonella kedougou zu hemmen, und diese Arten können außer Kontrolle geraten, auch wenn ihr übermäßiges Wachstum möglicherweise nur zufällig auftritt und nicht die eigentliche Ursache für Durchfall ist. Neuere Behandlungsprotokolle für C.-difficile-Infektionen beinhalten die fäkale Mikrobiota-Transplantation von Spenderfäkalien (siehe Fäkaltransplantation). In ersten Berichten über die Behandlung werden Erfolgsquoten von 90 % mit wenigen Nebenwirkungen beschrieben. Es wird vermutet, dass die Wirksamkeit auf die Wiederherstellung des Gleichgewichts zwischen den Bakterienklassen Bacteroides und Firmicutes zurückzuführen ist. ⓘ
Die Zusammensetzung des Darmmikrobioms verändert sich auch bei schweren Erkrankungen, nicht nur aufgrund der Einnahme von Antibiotika, sondern auch aufgrund von Faktoren wie Ischämie des Darms, Nahrungsmangel und Immunschwäche. Diese negativen Auswirkungen haben dazu geführt, dass man sich für eine selektive Dekontamination des Verdauungstrakts interessiert, eine Behandlung, die nur pathogene Bakterien abtötet und die Wiederansiedlung gesunder Bakterien ermöglicht. ⓘ
Antibiotika verändern die Population der Mikrobiota im Gastrointestinaltrakt, was zu einer Veränderung der metabolischen Interaktionen innerhalb der Gemeinschaft, zu einer veränderten Kalorienaufnahme durch die Verwendung von Kohlenhydraten und zu globalen Auswirkungen auf die metabolische, hormonelle und immunologische Homöostase des Wirtes führen kann. ⓘ
Es gibt hinreichende Hinweise darauf, dass die Einnahme von Probiotika, die Lactobacillus-Spezies enthalten, dazu beitragen kann, Antibiotika-assoziierte Durchfälle zu verhindern, und dass die Einnahme von Probiotika mit Saccharomyces (z. B. Saccharomyces boulardii ) dazu beitragen kann, Clostridium-difficile-Infektionen nach einer systemischen Antibiotikabehandlung zu verhindern. ⓘ
Schwangerschaft
Die Darmmikrobiota einer Frau verändert sich mit fortschreitender Schwangerschaft, wobei die Veränderungen denen ähneln, die bei metabolischen Syndromen wie Diabetes zu beobachten sind. Die Veränderung der Darmmikrobiota hat keine negativen Auswirkungen. Die Darmmikrobiota des Neugeborenen ähnelt den Proben der Mutter aus dem ersten Trimester. Die Vielfalt des Mikrobioms nimmt vom ersten bis zum dritten Trimester ab, während die Anzahl bestimmter Arten zunimmt. ⓘ
Probiotika, Präbiotika, Synbiotika und Pharmabiotika
Probiotika sind Mikroorganismen, von denen angenommen wird, dass sie bei Verzehr einen gesundheitlichen Nutzen haben. In Bezug auf die Darmmikrobiota sind Präbiotika in der Regel unverdauliche Ballaststoffe, die den oberen Teil des Magen-Darm-Trakts unverdaut passieren und das Wachstum oder die Aktivität der vorteilhaften Darmflora stimulieren, indem sie als Substrat für sie dienen. ⓘ
Der Begriff Synbiotika bezieht sich auf Lebensmittelzutaten oder Nahrungsergänzungsmittel, die Probiotika und Präbiotika in Form von Synergieeffekten kombinieren. ⓘ
Der Begriff "Pharmabiotika" wird auf unterschiedliche Weise verwendet: pharmazeutische Formulierungen (standardisierte Herstellung, die als Arzneimittel zugelassen werden kann) von Probiotika, Präbiotika oder Synbiotika; Probiotika, die gentechnisch verändert oder auf andere Weise für beste Leistungen (Haltbarkeit, Überleben im Verdauungstrakt usw.) optimiert wurden; und die natürlichen Produkte des Stoffwechsels der Darmflora (Vitamine usw.). ⓘ
Es gibt einige Hinweise darauf, dass eine Behandlung mit bestimmten probiotischen Bakterienstämmen bei Reizdarmsyndrom und chronischer idiopathischer Verstopfung wirksam sein kann. Zu den Organismen, die am ehesten zu einer Linderung der Symptome führen, gehören:
- Enterococcus faecium
- Laktobazillus plantarum
- Laktobazillus rhamnosus
- Propionibacterium freudenreichii
- Bifidobacterium breve
- Laktobazillus reuteri
- Laktobazillus salivarius
- Bifidobakterium infantis
- Streptokokkus thermophilus ⓘ
Forschung
Um herauszufinden, ob nicht-antibiotische Medikamente Auswirkungen auf die menschlichen Darmbakterien haben, wurden In-vitro-Analysen von mehr als 1000 vermarkteten Medikamenten gegen 40 Darmbakterienstämme durchgeführt. Dabei zeigte sich, dass 24 % der Medikamente das Wachstum von mindestens einem der Bakterienstämme hemmten. ⓘ
Auswirkungen von Bewegung
Kürzlich wurde nachgewiesen, dass die Darmmikrobiota und körperliche Betätigung miteinander zusammenhängen. Sowohl mäßige als auch intensive sportliche Betätigung sind typischerweise Teil des Trainingsprogramms von Ausdauersportlern, haben jedoch unterschiedliche Auswirkungen auf die Gesundheit. Der Zusammenhang zwischen der Darmmikrobiota und Ausdauersport hängt von der Trainingsintensität und dem Trainingszustand ab. ⓘ
Rolle bei Krankheiten
Die Bakterien im Verdauungstrakt können auf verschiedene Weise zu Krankheiten beitragen und von ihnen beeinflusst werden. Das Vorhandensein oder ein Übermaß einiger Bakterienarten kann zu entzündlichen Erkrankungen wie entzündlichen Darmerkrankungen beitragen. Darüber hinaus können die Stoffwechselprodukte bestimmter Mitglieder der Darmflora die Signalwege des Wirts beeinflussen und so zu Erkrankungen wie Fettleibigkeit und Darmkrebs beitragen. Im Falle eines Zusammenbruchs des Darmepithels kann das Eindringen von Bestandteilen der Darmflora in andere Wirtskompartimente zu einer Sepsis führen. ⓘ
Geschwüre
Eine Infektion mit Helicobacter pylori kann die Bildung von Magengeschwüren auslösen, wenn die Bakterien in die Magenepithelschleimhaut eindringen und dann eine entzündliche phagozytotische Reaktion hervorrufen. Die Entzündung schädigt wiederum die Parietalzellen, die übermäßig viel Salzsäure in den Magen abgeben und weniger schützenden Schleim produzieren. Eine Verletzung der Magenschleimhaut, die zu Geschwüren führt, entsteht, wenn die Magensäure die Abwehrkräfte der Zellen überwältigt und die endogene Prostaglandinsynthese hemmt, die Schleim- und Bikarbonatsekretion verringert, die Durchblutung der Schleimhaut reduziert und die Widerstandsfähigkeit gegen Verletzungen verringert. Die verminderten Schutzeigenschaften der Magenschleimhaut erhöhen die Anfälligkeit für weitere Verletzungen und die Bildung von Geschwüren durch Magensäure, Pepsin und Gallensalze. ⓘ
Perforation des Darms
Normalerweise friedliche Bakterien können den Wirt schädigen, wenn sie aus dem Darmtrakt austreten. Eine Translokation, bei der Bakterien den Darm durch die Schleimhaut verlassen, kann bei verschiedenen Krankheiten auftreten. Wird der Darm perforiert, dringen die Bakterien in das Interstitium ein und verursachen eine potenziell tödliche Infektion. ⓘ
Entzündliche Darmerkrankungen
Die beiden wichtigsten Arten von entzündlichen Darmerkrankungen, Morbus Crohn und Colitis ulcerosa, sind chronisch entzündliche Erkrankungen des Darms; die Ursachen dieser Krankheiten sind nicht bekannt, und es werden Probleme mit der Darmflora und ihrer Beziehung zum Wirt für diese Erkrankungen verantwortlich gemacht. Darüber hinaus scheinen Wechselwirkungen zwischen der Darmflora und der Darm-Hirn-Achse bei CED eine Rolle zu spielen, wobei physiologischer Stress, der über die Hypothalamus-Hypophysen-Nebennieren-Achse vermittelt wird, zu Veränderungen des Darmepithels führt und die Darmflora ihrerseits Faktoren und Metaboliten freisetzt, die Signale im enterischen Nervensystem und im Vagusnerv auslösen. ⓘ
Die Vielfalt der Darmflora scheint bei Menschen mit entzündlichen Darmerkrankungen im Vergleich zu gesunden Menschen deutlich verringert zu sein; außerdem scheinen bei Menschen mit Colitis ulcerosa Proteobakterien und Actinobakterien zu dominieren; bei Menschen mit Morbus Crohn scheinen Enterococcus faecium und verschiedene Proteobakterien überrepräsentiert zu sein. ⓘ
Es gibt hinreichende Belege dafür, dass die Korrektur eines Ungleichgewichts der Darmflora durch die Einnahme von Probiotika mit Laktobazillen und Bifidobakterien die viszeralen Schmerzen und die Darmentzündung bei CED verringern kann. ⓘ
Reizdarmsyndrom
Das Reizdarmsyndrom ist eine Folge von Stress und chronischer Aktivierung der HPA-Achse; zu seinen Symptomen gehören Bauchschmerzen, Veränderungen des Stuhlgangs und ein Anstieg proinflammatorischer Zytokine. Insgesamt haben Studien ergeben, dass die luminale und mukosale Mikrobiota bei Personen mit Reizdarmsyndrom verändert ist, und diese Veränderungen können mit der Art der Reizung wie Durchfall oder Verstopfung zusammenhängen. Außerdem nimmt die Diversität des Mikrobioms ab, mit einem geringen Anteil an fäkalen Laktobazillen und Bifidobakterien, einem hohen Anteil an fakultativ anaeroben Bakterien wie Escherichia coli und einem erhöhten Anteil an Firmicutes: Bacteroidetes. ⓘ
Andere entzündliche oder Autoimmunerkrankungen
Allergie, Asthma und Diabetes mellitus sind Autoimmun- und Entzündungserkrankungen unbekannter Ursache, die jedoch mit einem Ungleichgewicht in der Darmflora und ihrer Beziehung zum Wirt in Verbindung gebracht werden. Im Jahr 2016 war noch nicht klar, ob Veränderungen der Darmflora diese Autoimmun- und Entzündungserkrankungen verursachen oder ein Produkt oder eine Anpassung an diese Erkrankungen sind. ⓘ
Asthma
Für Asthma wurden zwei Hypothesen aufgestellt, um die steigende Prävalenz in den Industrieländern zu erklären. Die Hygienehypothese besagt, dass Kinder in den Industrieländern nicht genügend Mikroben ausgesetzt sind und daher eine geringere Prävalenz bestimmter Bakterientaxa aufweisen, die eine schützende Rolle spielen. Die zweite Hypothese konzentriert sich auf die westliche Ernährungsweise, der es an Vollkornprodukten und Ballaststoffen mangelt und die einen Überschuss an einfachen Zuckern aufweist. Beide Hypothesen gehen davon aus, dass kurzkettige Fettsäuren (SCFAs) eine Rolle bei der Immunmodulation spielen. Diese bakteriellen Fermentationsmetaboliten sind an der Immunsignalisierung beteiligt, die die Auslösung von Asthma verhindert, und niedrigere SCFA-Spiegel werden mit der Krankheit in Verbindung gebracht. Ein Mangel an schützenden Gattungen wie Lachnospira, Veillonella, Rothia und Faecalibacterium wird mit einem reduzierten SCFA-Spiegel in Verbindung gebracht. Außerdem sind SCFAs das Produkt der bakteriellen Fermentierung von Ballaststoffen, die in der westlichen Ernährungsweise kaum vorkommen. SCFAs stellen eine Verbindung zwischen der Darmflora und Immunstörungen her, und 2016 war dies ein aktiver Forschungsbereich. Ähnliche Hypothesen wurden auch für die Zunahme von Lebensmittel- und anderen Allergien aufgestellt. ⓘ
Diabetes mellitus Typ 1
Der Zusammenhang zwischen der Darmmikrobiota und Diabetes mellitus Typ 1 wurde auch mit SCFAs, wie Butyrat und Acetat, in Verbindung gebracht. Diäten, die Butyrat und Acetat aus bakterieller Fermentation liefern, zeigen eine erhöhte Treg-Expression. Treg-Zellen regulieren Effektor-T-Zellen herunter, was wiederum die Entzündungsreaktion im Darm reduziert. Butyrat ist eine Energiequelle für Dickdarmzellen. Butyrathaltige Diäten verringern daher die Durchlässigkeit des Darms, indem sie ausreichend Energie für die Bildung von Tight Junctions bereitstellen. Darüber hinaus hat sich gezeigt, dass Butyrat die Insulinresistenz verringert, was darauf hindeutet, dass Darmgemeinschaften mit wenig Butyrat-produzierenden Mikroben die Wahrscheinlichkeit erhöhen, an Diabetes mellitus Typ 2 zu erkranken. Eine Butyrat-reiche Ernährung könnte auch potenziell kolorektalen Krebs unterdrücken. ⓘ
Fettleibigkeit und metabolisches Syndrom
Die Darmflora wird auch mit Fettleibigkeit und dem metabolischen Syndrom in Verbindung gebracht, da sie eine Schlüsselrolle im Verdauungsprozess spielt. Die Ernährung nach westlichem Muster scheint Veränderungen in der Darmflora hervorzurufen und aufrechtzuerhalten, die sich wiederum darauf auswirken, wie viel Energie aus der Nahrung gewonnen wird und wie diese Energie genutzt wird. Ein Aspekt einer gesunden Ernährung, der in der westlichen Musterdiät oft fehlt, sind Ballaststoffe und andere komplexe Kohlenhydrate, die eine gesunde Darmflora zum Gedeihen benötigt; Veränderungen der Darmflora als Reaktion auf eine westliche Musterdiät scheinen die von der Darmflora erzeugte Energiemenge zu erhöhen, was zu Fettleibigkeit und metabolischem Syndrom beitragen kann. Es gibt auch Hinweise darauf, dass die Mikrobiota das Essverhalten auf der Grundlage der Präferenzen der Mikrobiota beeinflusst, was dazu führen kann, dass der Wirt mehr Nahrung zu sich nimmt, was schließlich zu Fettleibigkeit führt. Es wurde allgemein beobachtet, dass die Mikrobiota bei einer größeren Vielfalt des Darmmikrobioms Energie und Ressourcen für den Wettbewerb mit anderen Mikrobiota und weniger für die Beeinflussung des Wirts aufwenden. Bei einer geringeren Vielfalt des Darmmikrobioms ist das Gegenteil der Fall, und diese Mikrobiota können zusammenarbeiten, um beim Wirt Heißhunger auf Nahrung zu erzeugen. ⓘ
Darüber hinaus spielt die Leber eine wichtige Rolle bei der Blutzuckerhomöostase, indem sie das Gleichgewicht zwischen der Aufnahme und Speicherung von Glukose über die Stoffwechselwege der Glykogenese und Glukoneogenese aufrechterhält. Intestinale Lipide regulieren die Glukosehomöostase über eine Darm-Hirn-Leber-Achse. Die direkte Verabreichung von Lipiden in den oberen Darm erhöht den Gehalt an langkettigem Fettacyl-Coenzym A (LCFA-CoA) im oberen Darm und unterdrückt die Glukoseproduktion selbst bei subdiaphragmatischer Vagotomie oder vagaler Deafferenzierung des Darms. Dadurch wird die neuronale Verbindung zwischen dem Gehirn und dem Darm unterbrochen und die Fähigkeit der oberen Darmlipide, die Glukoseproduktion zu hemmen, blockiert. Die Darm-Hirn-Leber-Achse und die Zusammensetzung der Darmmikrobiota können die Glukosehomöostase in der Leber regulieren und bieten potenzielle therapeutische Methoden zur Behandlung von Fettleibigkeit und Diabetes. ⓘ
Ebenso wie die Darmflora in einer Rückkopplungsschleife funktionieren kann, die die Entwicklung von Fettleibigkeit fördern kann, gibt es Hinweise darauf, dass eine Einschränkung der Kalorienzufuhr (d. h. eine Diät) Veränderungen in der Zusammensetzung der Darmflora bewirken kann. ⓘ
Lebererkrankung
Da die Leber direkt von der Pfortader gespeist wird, gelangt alles, was das Darmepithel und die Darmschleimhautbarriere passiert, in die Leber, ebenso wie die dort gebildeten Zytokine. Eine Dysbiose der Darmflora wird mit der Entwicklung von Leberzirrhose und nichtalkoholischer Fettleber in Verbindung gebracht. ⓘ
Krebs
Einige Bakteriengattungen, wie z. B. Bacteroides und Clostridium, wurden mit einer erhöhten Tumorwachstumsrate in Verbindung gebracht, während andere Gattungen, wie z. B. Lactobacillus und Bifidobakterien, bekanntermaßen die Tumorbildung verhindern. Im Dezember 2017 gab es vorläufige und indirekte Hinweise darauf, dass die Darmmikrobiota die Reaktion auf PD-1-Inhibitoren vermitteln könnte; der Mechanismus war jedoch unbekannt. ⓘ
Übergewichtige Menschen haben ein höheres Risiko für verschiedene Krebsarten, darunter auch für das Leberzellkarzinom. Dieses erhöhte Risiko könnte mit der vermehrten Produktion krebserregender Gallensäuren durch Darmmikroorganismen bei diesen Menschen zusammenhängen. Ernährungsbedingte oder genetisch bedingte Fettleibigkeit wird mit Veränderungen der Darmmikrobiota in Verbindung gebracht, die den Gehalt an der Gallensäure Desoxycholsäure erhöhen, einem Metaboliten, der DNA-Schäden verursacht. ⓘ
Neuropsychiatrische
Das Interesse an der Beziehung zwischen der Darmflora und neuropsychiatrischen Problemen wurde durch eine Studie aus dem Jahr 2014 geweckt, die zeigte, dass keimfreie Mäuse im Vergleich zu nicht keimfreien Labormäusen eine übertriebene Reaktion der HPA-Achse auf Stress zeigten. Bis Januar 2016 wurden die meisten Arbeiten zur Rolle der Darmflora in der Darm-Hirn-Achse an Tieren durchgeführt oder charakterisierten die verschiedenen neuroaktiven Verbindungen, die die Darmflora produzieren kann, und Studien mit Menschen, in denen Unterschiede zwischen Menschen mit verschiedenen psychiatrischen und neurologischen Störungen oder Veränderungen der Darmflora als Reaktion auf Stress gemessen wurden oder die Auswirkungen verschiedener Probiotika (in diesem Zusammenhang als "Psychobiotika" bezeichnet) gemessen wurden, waren im Allgemeinen klein und konnten nicht verallgemeinert werden; ob Veränderungen der Darmflora eine Folge von Krankheiten, eine Ursache von Krankheiten oder beides in einer Reihe von möglichen Rückkopplungsschleifen in der Darm-Hirn-Achse sind, blieb unklar. ⓘ
Eine systematische Übersichtsarbeit aus dem Jahr 2016 untersuchte die präklinischen und kleinen Humanstudien, die mit bestimmten handelsüblichen probiotischen Bakterienstämmen durchgeführt wurden, und stellte fest, dass von den getesteten Gattungen die Gattungen Bifidobacterium und Lactobacillus (B. longum, B. breve, B. infantis, L. helveticus, L. rhamnosus, L. plantarum und L. casei) das größte Potenzial haben, bei bestimmten Störungen des zentralen Nervensystems nützlich zu sein. ⓘ
Andere Tiere
Die Zusammensetzung des menschlichen Darmmikrobioms ähnelt derjenigen der anderen Menschenaffen. Allerdings hat die menschliche Darmbiota seit unserer evolutionären Abspaltung von Pan an Vielfalt verloren und sich in ihrer Zusammensetzung verändert. Der Mensch weist eine Zunahme der Bacteroidetes auf, einer Bakteriengruppe, die mit einer Ernährung mit hohem Anteil an tierischem Eiweiß und Fett in Verbindung gebracht wird, und eine Abnahme von Methanobrevibacter und Fibrobacter, Gruppen, die komplexe pflanzliche Polysaccharide vergären. Diese Veränderungen sind das Ergebnis der kombinierten diätetischen, genetischen und kulturellen Veränderungen, die der Mensch seit seiner evolutionären Abspaltung von Pan durchlaufen hat. ⓘ
Neben Menschen und Wirbeltieren besitzen auch einige Insekten eine komplexe und vielfältige Darmmikrobiota, die eine wichtige Rolle bei der Ernährung spielt. Die mit Termiten assoziierten mikrobiellen Gemeinschaften können einen Großteil des Gewichts der Individuen ausmachen und spielen eine wichtige Rolle bei der Verdauung von Lignozellulose und der Stickstofffixierung. Diese Gemeinschaften sind wirtsspezifisch, und eng verwandte Insektenarten weisen vergleichbare Ähnlichkeiten in der Zusammensetzung der Darmmikrobiota auf. Bei Schaben hat sich gezeigt, dass sich die Darmmikrobiota unabhängig vom Inokulum auf deterministische Weise zusammensetzt; der Grund für diese wirtsspezifische Zusammensetzung bleibt unklar. Bakteriengemeinschaften, die mit Insekten wie Termiten und Schaben assoziiert sind, werden durch eine Kombination von Kräften bestimmt, in erster Linie durch die Ernährung, aber es gibt auch Hinweise darauf, dass die Phylogenie des Wirts bei der Auswahl der Linien eine Rolle spielen könnte. ⓘ
Seit mehr als 51 Jahren ist bekannt, dass die Verabreichung niedriger Dosen antibakterieller Wirkstoffe das Wachstum von Nutztieren fördert, um die Gewichtszunahme zu erhöhen. ⓘ
In einer an Mäusen durchgeführten Studie war das Verhältnis von Firmicutes und Lachnospiraceae bei Tieren, die mit subtherapeutischen Dosen verschiedener Antibiotika behandelt wurden, deutlich erhöht. Die Analyse des Kaloriengehalts der Fäkalien und der Konzentration der kleinkettigen Fettsäuren im Magen-Darm-Trakt führte zu dem Schluss, dass die Veränderungen in der Zusammensetzung der Mikrobiota zu einer erhöhten Fähigkeit führen, Kalorien aus ansonsten unverdaulichen Bestandteilen zu extrahieren, und zu einer erhöhten Produktion von kleinkettigen Fettsäuren. Diese Ergebnisse belegen, dass Antibiotika nicht nur die Zusammensetzung des Mikrobioms des Magen-Darm-Trakts stören, sondern auch dessen metabolische Fähigkeiten, insbesondere im Hinblick auf SCFAs. ⓘ
Nutzen, Funktion, Bedeutung
Im Darm befinden sich rund 1,3-mal so viel Mikroorganismen, wie der Organismus des Menschen Zellen enthält. Im Dickdarm befinden sich sehr viel mehr Mikroorganismen als im Dünndarm. Die Intestinalmikroflora ist an der Abwehr von Krankheitserregern (Kolonisationsresistenz) beteiligt und beeinflusst das Immunsystem, wobei nicht ganz klar ist, ob sich für den Wirt insgesamt ein Vorteil ergibt. Experimente mit von Mikroorganismen freien und normalen Mäusen haben gezeigt, dass verschiedene Bakterien und Amöben durch die Anwesenheit der Darmflora erst pathogen werden, hingegen werden die negativen Auswirkungen von einigen anderen eukaryotischen Einzellern und Saugwürmern verringert. Die Konstanz der Milieubedingungen im Darm und die Vielseitigkeit der in Form der Nahrung zugeführten Substrate begünstigen die Entwicklung einer an Individuen- und Arten-Zahl und Aktivitäten äußerst komplexen Mikroorganismengesellschaft. Nahrungsbestandteile und vom menschlichen Organismus gebildete Stoffe dienen den Mikroorganismen als Nährstoff- und Energiequelle. Die Mikroorganismen haben verschiedene Wirkungen auf den Menschen wie ⓘ
- Immunmodulation
- Abwehr und Bekämpfung von pathogenen Erregern,
- Versorgung mit Vitaminen (Thiamin, Riboflavin, Pyridoxin, B12, K)
- Unterstützung der Verdauung von Nahrungsbestandteilen
- Versorgung der Darmepithelschicht mit Energie (Butyrat)
- Anregung der Darmperistaltik
- Produktion von kurzkettigen Fettsäuren (Butyrat, Essigsäure, Propionsäure)
- Detoxifizierung von Xenobiotika
- Verbesserung der Hitzeresistenz
- Verbesserung der Ausdauer-Leistungsfähigkeit ⓘ
Während des mikrobiellen Abbaus unverdaulicher Kohlenhydrate (Ballaststoffe) werden im menschlichen Darm kurzkettige Fettsäuren (hauptsächlich Essig-, Propion- und Buttersäure) und Gase gebildet, wie Wasserstoff (H2), Kohlenstoffdioxid (CO2) und Methan (CH4). Darmepithelzellen nehmen die Fettsäuren auf und verstoffwechseln sie; die Gase werden ausgeschieden (Flatulenz). Unter den kurzkettigen Fettsäuren wird besonders der Buttersäure auf Grund ihrer physiologischen Effekte eine besondere Bedeutung zugesprochen. Beispielsweise wurde bei Darmkrebs eine verminderte intestinale Buttersäurekonzentration beobachtet. Eine weitere Funktion der kurzkettigen Fettsäuren ist die Anregung der Darmperistaltik, der kontraktiven Bewegung des Darms zur Beförderung von Nahrungsbrei in Richtung Enddarm. ⓘ

Bei der anaeroben Verstoffwechselung von Proteinen werden kurzkettige, aber auch verzweigtkettige Fettsäuren gebildet (iso-Valeriansäure, iso-Buttersäure). Daneben können noch Produkte wie Thiole (Mercaptane), Indole, Amine und Schwefelwasserstoff (H2S) gebildet werden. Im geringen Maße wird auch Stickstoff (N2) gebildet. Fette werden unter anoxischen Bedingungen im Darm nicht verstoffwechselt. ⓘ
Die Darmflora beeinflusst das Körpergewicht und spielt eine Rolle bei der Fettsucht (Adipositas). Aus Experimenten an „dicken“ (englisch obese) Mäusemutanten (ob/ob), denen der Fettsäureregulator Leptin fehlt, ist bekannt, dass sich die Darmflora von dicken und schlanken Mäusen hinsichtlich der Zusammensetzung des Verhältnisses von Bakterien der Gattung Bacteroides und des Stamms (Abteilung) der Firmicutes unterscheidet, wobei dicke Mäuse einen größeren Anteil an Firmicutes aufweisen. Auch die Darmflora des Menschen hat Einfluss auf das Körpergewicht. Im Darm von gesunden Menschen finden sich Firmicuten- und Bacteroideten-Stämme in einem Verhältnis von 1:1 bis 3:1. Bei übergewichtigen Patienten finden sich häufig verschobene Verhältnisse zu Gunsten der Firmicutes von 3:1 auf bis 25:1 (in Extremfällen bis 200:1). Eine Dominanz der Firmicutes führt zu einem besseren Abbau von Ballaststoffen und der Gewinnung von zusätzlicher Energie. Übergewichtigkeit ist deshalb auch ein Resultat einer verbesserten Energieversorgung durch übermäßig stark ausgeprägte Firmicutes. Bei einer Gewichtsreduktion verschiebt sich das Verhältnis von Firmicutes zu Bacteroides hin. Die gegenseitige Beeinflussung der Zusammensetzung der Darmflora und des Körpergewichtes wird mit der Energieaufnahme in Zusammenhang gebracht, weil durch die Zusammensetzung der Darmflora die Verdauung von Fettsäuren und Polysacchariden beeinflusst wird. Dies geht aus Experimenten hervor, in denen die Darmflora (aus dem Caecum) von dicken Mäusen in Mikroorganismen-freie Mäuse transplantiert wurde, und diese anschließend, trotz Verringerung der Nahrungszufuhr, an Gewicht zunahmen. ⓘ
Es wird diskutiert, inwiefern die Zusammensetzung der Darmflora bei Mäusen, wie bei Menschen, einen Einfluss auf das emotionale Verhalten und den Umgang mit Stress hat. ⓘ
In ihrer Funktion als Kommensalen verhindern die Mikroorganismen durch ihre bloße Menge ein Überwuchern von pathogenen Mikroorganismen, wie dies durch Clostridium difficile bei der pseudomembranösen Kolitis geschieht. Umgekehrt kann durch die Verabreichung von Stuhl eines gesunden Spenders durch einen Einlauf (über das Rektum oder eine liegende Nasoduodenalsonde) eine therapieresistente pseudomembranöse Kolitis in der Mehrzahl der Fälle ausgeheilt werden, wie Studien zeigten. Über Erfolge bei anderen chronisch-entzündlichen Darmerkrankungen wurde ebenfalls berichtet. ⓘ
Mit etwa 30 % der Trockenmasse ist die Darmflora ein wesentlicher Bestandteil der Fäzes. ⓘ
Fehlbesiedelung des Darms
Veränderungen der Darmflora können in einer Unter- oder Überbesiedelung und in einer Veränderung ihrer Zusammensetzung bestehen. Es können Fehlbesiedelungen entweder im Dick- oder im Dünndarm oder bei beiden gleichzeitig auftreten. Die optimale Zusammensetzung der Darmflora ist wirtsabhängig. Mäuse, die mit einer typischen Darmflora vom Menschen oder von der Ratte ausgestattet werden, weisen gegenüber Mäusen, welche die typische Darmflora für Mäuse besitzen, Schwachstellen in ihrem Immunsystem auf. ⓘ
Symptome
Diese umfassen allgemein Bauchschmerzen, Blähungen, eine erhöhte Infektanfälligkeit sowie Anfälligkeit für Nahrungsmittelunverträglichkeiten. Bei einer gestörten Dünndarmflora tritt ein Blähbauch ohne abgehende Darmgase auf, der Bauch verflacht über Nacht wieder. Bei einer Fehlbesiedelung des Dickdarms dagegen tritt der Blähbauch mit abgehenden Darmgasen auf. Es sind ebenso Rückwirkungen auf das Immunsystem und Zusammenhänge der gestörten Darmbesiedelung mit dem Nervensystem zu beobachten. ⓘ
Diagnose
Um auf eine Fehlbesiedelung zu prüfen, wird zuerst zum Ausschluss einer Dünndarmfehlbesiedlung ein Lactulose-H2-Atemtest durchgeführt. Zusätzlich empfiehlt sich ein ausführlicher H2-Atemtest mit Laktose oder Fruktose, da diese Unverträglichkeiten einer bakteriellen Überbesiedelung aufgelagert sein können. Wenn eine Fehlbesiedelung des Dünndarms ausgeschlossen wurde, kann zusätzlich mit Hilfe einer Stuhlprobe der Darmflorastatus ermittelt werden, um auf eine Fehlbesiedelung des Dickdarms zu prüfen. ⓘ
Forschungsgeschichte
Da entdeckt wurde, dass Bakterien Krankheiten verursachen können, wurde die Existenz der Darmflora nach ihrer Entdeckung für eine Krankheit gehalten, die den Namen „intestinale Toxämie“ erhielt: Sir Arbuthnot Lane, der Chirurg des britischen Königshauses, empfahl seinen Patienten, sich wegen der gefährlichen Eingeweidebewohner den Dickdarm entfernen zu lassen. Darmreinigungen kamen bei Ärzten in Mode. In der weiteren Folge wurde das Thema von der Forschung weitgehend ignoriert. Die anaeroben Mikroorganismen konnten im Labor nicht untersucht werden. ⓘ
Erst das Aufkommen der Antibiotika, deren bakterientötende Eigenschaft die Darmflora beschädigte, und die Folgen dieser Schädigung brachten das Thema zurück auf die Agenda der Forschung. Letztlich blieben wegen der praktischen Schwierigkeiten zunächst große Fortschritte aus. Dies lag daran, dass mit den klassischen Kulturverfahren nur ein Bruchteil der Darmmikrobiota nachgewiesen werden konnte. Das Bild der Zusammensetzung der Darmflora hat sich seit Einführung molekularer Techniken teilweise grundlegend geändert. ⓘ
Beeinflussung der Darmflora
Zunächst wird bei einer Vaginalgeburt sofort der Darm des Säuglings besiedelt. Anfänglich sind Enterobakterien und Streptokokken im Stuhl nachweisbar, und bei Muttermilch-Ernährung sind bald Bifidobakterien und Ruminococcus-Arten vorherrschend. Es besteht ein Zusammenhang zwischen mütterlicher Vaginalflora und fetaler Darmflora bei Vaginalgeburten. ⓘ
Medizinische Eingriffe
Die Schädigung der Darmflora durch Antibiotika ist eine Nebenwirkung dieser Medikamentengruppe und kann zu einer antibiotika-assoziierten Diarrhoe führen. Normalerweise stellt sich jedoch das ursprüngliche Gleichgewicht innerhalb weniger Wochen wieder ein. Durch intensive und beständige Antibiotikabehandlung kann die Besiedlung mit Mikroorganismen im Darm bleibend gestört werden, insbesondere bei Kindern. Jedes vierte Medikament aus der Humanmedizin beeinflusst die Darmbakterien negativ und kann zu einer Antibiotikaresistenz beitragen. ⓘ
Inwieweit die Darmflora durch die Zuführung von Mikroorganismen, beispielsweise durch Probiotika, beeinflusst werden kann („Symbioselenkung“), ist wissenschaftlich umstritten. ⓘ
In der Behandlung von Clostridium-difficile-Darminfektionen (antibiotikaassoziierte Kolitis) sowie anderen bakteriell bedingten Darmentzündungen wird seit einigen Jahren mit großem Erfolg die fäkale Bakterien-Therapie in Form der Stuhltransplantation angewendet. Dabei wird Stuhl eines gesunden Spenders in physiologischer Kochsalzlösung aufgelöst, gereinigt und entweder über ein Klistier in den Dickdarm oder über eine nasogastrische Sonde in den Magen des Empfängers gebracht. ⓘ
Nach den Ergebnissen jüngster Forschungen wird BLIS als mögliche Sanierung empfohlen. In einer Studie wird zudem der positive Einfluss auf den Darmzustand durch Probiotika-Gabe bestätigt. ⓘ
Da die zugeführten Bakterien nur bei intakter Darmbarriere ihre optimale Wirkung entfalten können, ist es sinnvoll, diese zuvor oder gleichzeitig z. B. durch ein Arzneimittel mit Myrrhe zu stabilisieren. Untersuchungen an der Charité Berlin belegen, dass die Arzneipflanze Myrrhe die Darmbarriere stabilisiert und sie vor schädlichen Einflüssen schützt. Forschungen an der Universität Leipzig konnten darüber hinaus zeigen, dass Myrrhe und Kaffeekohle dabei vergleichbar gut wirken wie das häufig verordnete Kortisonpräparat Budesonid. ⓘ
Siehe auch
- Bakterienflora
- Hautflora
- Scheidenflora ⓘ
Literatur
- Jörg Blech: Leben auf dem Menschen – Die Geschichte unserer Besiedler. Rowohlt-Verlag, 2010, ISBN 978-3-499-62494-0.
- Peter Brookesmith, Karin Prager: Kleine Ungeheuer. Die geheime Welt der winzigen Lebewesen. Gondrom-Verlag, 1999, ISBN 3-8112-1735-6, S. 55–59.
- J. Müller, R. Ottenjann, J. Seifert (Hrsg.): Ökosystem Darm – Morphologie. Mikrobiologie. Immunologie. Springer-Verlag, Berlin 1989, ISBN 3-540-51707-3.
- Rosemarie Blatz: Medizinische Mikrobiologie und Immunologie – systematisch. Uni-Med, Bremen 1999, ISBN 3-89599-139-2.
- Jürgen Schulze u. a.: Probiotika; Mikroökologie, Mikrobiologie, Qualität, Sicherheit und gesundheitliche Effekte. Hippokrates-Verlag, 2008, ISBN 978-3-8304-5356-7.
- B. D. Muegge, J. Kuczynski: Diet drives convergence in gut microbiome functions across mammalian phylogeny and within humans. In: Science. Band 332, Nummer 6032, Mai 2011, S. 970–974, ISSN 1095-9203. doi:10.1126/science.1198719. PMID 21596990. PMC 3303602 (freier Volltext). ⓘ
Dokumentarfilme
- Unser Bauch - Die wunderbare Welt des Mikrobioms, Regie: Thierry de Lestrade und Sylvie Gilman, ARTE F, 2019. ⓘ

