Liponsäure

| |
| |

| |
| Bezeichnungen | |
|---|---|
| IUPAC-Bezeichnung
(R)-5-(1,2-Dithiolan-3-yl)-pentansäure
| |
| Andere Namen
α-Liponsäure; Alpha-Liponsäure; Thioctsäure; 6,8-Dithiooctansäure
| |
| Bezeichner | |
3D-Modell (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Arzneimittelbank | |
IUPHAR/BPS
|
|
| KEGG | |
| MeSH | Lipoic+Säure |
PubChem CID
|
|
| UNII |
|
InChI
| |
SMILES
| |
| Eigenschaften | |
Chemische Formel
|
C8H14O2S2 |
| Molekulare Masse | 206,32 g-mol-1 |
| Erscheinungsbild | Gelbe nadelartige Kristalle |
| Schmelzpunkt | 60-62 °C (140-144 °F; 333-335 K) |
Löslichkeit in Wasser
|
Sehr schwach löslich (0,24 g/L) |
| Löslichkeit in Ethanol 50 mg/ml | Löslich |
| Pharmakologie | |
ATC-Code
|
A16AX01 (WHO) |
| Pharmakokinetik: | |
Bioverfügbarkeit
|
30% (oral) |
| Verwandte Verbindungen | |
Verwandte Verbindungen
|
Lipoamid Asparagusinsäure |
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien in ihrem Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |
Liponsäure (LA), auch bekannt als α-Liponsäure, Alpha-Liponsäure (ALA) und Thioctsäure, ist eine schwefelorganische Verbindung, die sich von Caprylsäure (Octansäure) ableitet. ALA wird normalerweise in Tieren gebildet und ist für den aeroben Stoffwechsel unerlässlich. Sie wird auch hergestellt und ist in einigen Ländern, in denen sie als Antioxidans vermarktet wird, als Nahrungsergänzungsmittel erhältlich, während sie in anderen Ländern als Arzneimittel erhältlich ist. Lipoat ist die konjugierte Base der Liponsäure und die unter physiologischen Bedingungen am häufigsten vorkommende Form der LA. In der Natur kommt nur das (R)-(+)-Enantiomer (RLA) vor, das für den aeroben Stoffwechsel unerlässlich ist, da RLA ein wesentlicher Cofaktor vieler Enzymkomplexe ist. ⓘ
| Strukturformel ⓘ | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||
| Vereinfachte Strukturformel (ohne Stereochemie) | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Liponsäure | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C8H14O2S2 | |||||||||||||||
| Kurzbeschreibung |
gelbliche Nadeln [(RS)-Liponsäure] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code | ||||||||||||||||
| Wirkstoffklasse |
Neuropathiemittel | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 206,33 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt |
| |||||||||||||||
| Siedepunkt |
160–165 °C [(R)-Liponsäure] | |||||||||||||||
| pKS-Wert |
5,4 | |||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten |
502 mg·kg−1 (LD50, Maus, oral) | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
α-Liponsäure (abgekürzt LA vom englischen lipoic acid oder ALA vom englischen alpha lipoic acid; anderer Name Thioctsäure) ist eine schwefelhaltige Fettsäure. In ihrer natürlichen (R)-Form kommt sie als Coenzym in den Mitochondrien fast aller Eukaryoten vor und spielt eine wichtige Rolle im Energiestoffwechsel. Die Salze der Liponsäure heißen Lipoate. ⓘ
Physikalische und chemische Eigenschaften
Liponsäure (LA), auch bekannt als α-Liponsäure, Alpha-Liponsäure (ALA) und Thioctsäure, ist eine schwefelorganische Verbindung, die sich von Octansäure ableitet. LA enthält zwei Schwefelatome (an C6 und C8), die durch eine Disulfidbindung verbunden sind, und gilt daher als oxidiert, obwohl beide Schwefelatome in höheren Oxidationsstufen vorliegen können. ⓘ
Das Kohlenstoffatom an C6 ist chiral, und das Molekül liegt als zwei Enantiomere (R)-(+)-Liponsäure (RLA) und (S)-(-)-Liponsäure (SLA) sowie als racemisches Gemisch (R/S)-Liponsäure (R/S-LA) vor. ⓘ
LA erscheint physikalisch als gelber Feststoff und enthält strukturell eine endständige Carbonsäure und einen endständigen Dithiolanring. ⓘ
Für die Verwendung in Nahrungsergänzungsmitteln und Compounding-Apotheken hat die USP eine offizielle Monographie für R/S-LA erstellt. ⓘ
Biologische Funktion
Liponsäure ist ein Cofaktor für fünf Enzyme oder Enzymklassen: Pyruvatdehydrogenase, a-Ketoglutaratdehydrogenase, das Glycinspaltsystem, verzweigtkettig und die alpha-Oxo(keto)adipatdehydrogenase. Die ersten beiden sind entscheidend für den Zitronensäurezyklus. Das GCS reguliert die Glycinkonzentration. ⓘ
Biosynthese und Bindung
Die meisten endogen produzierten RLA sind nicht "frei", da Oktansäure, die Vorstufe zu RLA, vor dem enzymatischen Einbau der Schwefelatome an die Enzymkomplexe gebunden wird. Als Cofaktor ist RLA kovalent durch eine Amidbindung an einen terminalen Lysinrest der Lipoyl-Domänen des Enzyms gebunden. Der Vorläufer der Liponsäure, die Octansäure, wird über die Fettsäurebiosynthese in Form des Octanoyl-Acylträgerproteins hergestellt. Bei Eukaryoten wird dazu ein zweiter Fettsäurebiosyntheseweg in den Mitochondrien genutzt. Das Octanoat wird als Thioester des Acylträgerproteins aus der Fettsäurebiosynthese durch ein Enzym namens Octanoyltransferase auf ein Amid des Lipoyldomänenproteins übertragen. Zwei Wasserstoffatome des Octanoats werden von der Lipoylsynthase über einen radikalen SAM-Mechanismus durch Schwefelgruppen ersetzt. Infolgedessen wird Liponsäure an Proteine gebunden synthetisiert und es wird keine freie Liponsäure gebildet. Liponsäure kann beim Abbau von Proteinen und durch die Wirkung des Enzyms Lipoamidase entfernt werden. Freies Lipoat kann von einigen Organismen durch ein Enzym namens Lipoat-Protein-Ligase genutzt werden, das es kovalent an das richtige Protein bindet. Die Ligaseaktivität dieses Enzyms erfordert ATP. ⓘ
Zellulärer Transport
Zusammen mit Natrium und den Vitaminen Biotin (B7) und Pantothensäure (B5) gelangt die Liponsäure über den SMVT (Natrium-abhängiger Multivitamin-Transporter) in die Zellen. Jede der durch den SMVT transportierten Verbindungen steht in Konkurrenz zu den anderen. So haben Untersuchungen gezeigt, dass eine erhöhte Zufuhr von Liponsäure oder Pantothensäure die Aufnahme von Biotin und/oder die Aktivitäten von biotinabhängigen Enzymen verringert. ⓘ
Enzymatische Aktivität
Liponsäure ist ein Kofaktor für mindestens fünf Enzymsysteme. Zwei davon sind am Zitronensäurezyklus beteiligt, durch den viele Organismen Nährstoffe in Energie umwandeln. Bei lipoylierten Enzymen ist die Liponsäure kovalent an sie gebunden. Die Lipoylgruppe überträgt Acylgruppen in 2-Oxosäure-Dehydrogenasekomplexen und Methylamingruppen im Glycinspaltungskomplex oder in der Glycindehydrogenase. ⓘ
2-Oxosäure-Dehydrogenase-Übertragungsreaktionen laufen nach einem ähnlichen Mechanismus ab in:
- dem Pyruvat-Dehydrogenase-Komplex
- dem α-Ketoglutarat-Dehydrogenase- oder 2-Oxoglutarat-Dehydrogenase-Komplex
- dem Komplex der verzweigtkettigen Oxosäure-Dehydrogenase (BCDH)
- der Acetoin-Dehydrogenase-Komplex. ⓘ
Der am besten untersuchte Komplex ist der Pyruvat-Dehydrogenase-Komplex. Diese Komplexe bestehen aus drei zentralen Untereinheiten: E1-3, die die Decarboxylase, die Lipoyltransferase bzw. die Dihydrolipoamid-Dehydrogenase darstellen. Diese Komplexe haben einen zentralen E2-Kern, und die anderen Untereinheiten umgeben diesen Kern, um den Komplex zu bilden. In der Lücke zwischen diesen beiden Untereinheiten transportiert die Lipoyl-Domäne Zwischenprodukte zwischen den aktiven Stellen. Die Lipoyl-Domäne selbst ist über einen flexiblen Linker mit dem E2-Kern verbunden, und die Anzahl der Lipoyl-Domänen variiert bei einem bestimmten Organismus zwischen einer und drei. Die Anzahl der Domänen wurde experimentell variiert und scheint nur geringe Auswirkungen auf das Wachstum zu haben, bis mehr als neun Domänen hinzugefügt werden, obwohl mehr als drei die Aktivität des Komplexes verringern. ⓘ
Liponsäure dient als Co-Faktor für den Acetoin-Dehydrogenase-Komplex, der die Umwandlung von Acetoin (3-Hydroxy-2-Butanon) in Acetaldehyd und Acetyl-Coenzym A katalysiert. ⓘ
Das Glycin-Spaltungssystem unterscheidet sich von den anderen Komplexen und hat eine andere Nomenklatur. In diesem System ist das H-Protein eine freie Lipoyl-Domäne mit zusätzlichen Helices, das L-Protein ist eine Dihydrolipoamid-Dehydrogenase, das P-Protein ist die Decarboxylase, und das T-Protein überträgt das Methylamin von Lipoat auf Tetrahydrofolat (THF), wodurch Methylen-THF und Ammoniak entstehen. Methylen-THF wird dann von der Serin-Hydroxymethyltransferase zur Synthese von Serin aus Glycin verwendet. Dieses System ist Teil der pflanzlichen Photorespiration. ⓘ
Biologische Quellen und Abbau
Liponsäure ist in vielen Lebensmitteln enthalten, in denen sie an Lysin in Proteinen gebunden ist, etwas stärker jedoch in Niere, Herz, Leber, Spinat, Brokkoli und Hefeextrakt. Natürlich vorkommende Liponsäure ist immer kovalent gebunden und nicht ohne weiteres aus Nahrungsmitteln verfügbar. Außerdem ist die Menge an Liponsäure, die in Nahrungsmitteln enthalten ist, gering. So wurden beispielsweise für die Reinigung von Liponsäure zur Bestimmung ihrer Struktur schätzungsweise 10 Tonnen Leberrückstände verwendet, die 30 mg Liponsäure ergaben. Folglich ist die gesamte als Nahrungsergänzungsmittel erhältliche Liponsäure chemisch synthetisiert. ⓘ
Die Ausgangswerte (vor der Supplementierung) von RLA und R-DHLA wurden im menschlichen Plasma nicht nachgewiesen. RLA wurde in einer Konzentration von 12,3-43,1 ng/ml nach saurer Hydrolyse nachgewiesen, bei der proteingebundene Liponsäure freigesetzt wird. Die enzymatische Hydrolyse von proteingebundener Liponsäure setzte 1,4-11,6 ng/mL bzw. <1-38,2 ng/mL unter Verwendung von Subtilisin und Alcalase frei. ⓘ
Verdauungsproteolytische Enzyme spalten den R-Lipoyllysin-Rest von den aus der Nahrung stammenden mitochondrialen Enzymkomplexen ab, sind aber nicht in der Lage, die Liponsäure-L-Lysin-Amidbindung zu spalten. Sowohl synthetisches Lipoamid als auch (R)-Lipoyl-L-Lysin werden rasch von Serum-Lipoamidasen gespalten, die freie (R)-Liponsäure und entweder L-Lysin oder Ammoniak freisetzen. Über den Abbau und die Verwertung von aliphatischen Sulfiden wie Liponsäure ist wenig bekannt, mit Ausnahme von Cystein. ⓘ
Liponsäure wird auf verschiedene Weise verstoffwechselt, wenn sie Säugetieren als Nahrungsergänzungsmittel verabreicht wird. Es wurden der Abbau zu Tetranorliponsäure, die Oxidation eines oder beider Schwefelatome zum Sulfoxid und die S-Methylierung des Sulfids beobachtet. Die Konjugation von unmodifizierter Liponsäure an Glycin wurde insbesondere bei Mäusen festgestellt. Der Abbau von Liponsäure ist beim Menschen ähnlich, obwohl nicht klar ist, ob die Schwefelatome signifikant oxidiert werden. Offenbar sind Säugetiere nicht in der Lage, Liponsäure als Schwefelquelle zu nutzen. ⓘ
Chemische Synthese

SLA gab es vor der chemischen Synthese im Jahr 1952 nicht. SLA wird in gleichen Mengen wie RLA in achiralen Herstellungsverfahren produziert. Die racemische Form wurde in den 1950er bis 1960er Jahren in Europa und Japan in größerem Umfang klinisch eingesetzt, obwohl man schon früh erkannt hatte, dass die verschiedenen LA-Formen nicht bioäquivalent sind. Die ersten synthetischen Verfahren für RLA und SLA erschienen Mitte der 1950er Jahre. Fortschritte in der chiralen Chemie führten zu effizienteren Technologien für die Herstellung der einzelnen Enantiomere sowohl durch klassische Auflösung als auch durch asymmetrische Synthese, und die Nachfrage nach RLA stieg zu dieser Zeit ebenfalls an. Im 21. Jahrhundert sind R/S-LA, RLA und SLA mit hoher chemischer und/oder optischer Reinheit in industriellen Mengen verfügbar. Gegenwärtig wird der größte Teil des weltweiten Angebots an R/S-LA und RLA in China hergestellt, kleinere Mengen in Italien, Deutschland und Japan. RLA wird durch Modifikationen eines Verfahrens hergestellt, das erstmals von Georg Lang in einer Doktorarbeit beschrieben und später von DeGussa patentiert wurde. Obwohl RLA aufgrund seiner "vitaminähnlichen" Rolle im Stoffwechsel ernährungsphysiologisch bevorzugt wird, sind sowohl RLA als auch R/S-LA in großem Umfang als Nahrungsergänzungsmittel erhältlich. Es ist bekannt, dass in vivo sowohl stereospezifische als auch nicht stereospezifische Reaktionen stattfinden und zu den Wirkmechanismen beitragen, aber die bisherigen Erkenntnisse deuten darauf hin, dass RLA das Eutomer (die ernährungsphysiologisch und therapeutisch bevorzugte Form) sein könnte. ⓘ
Pharmakologie
Pharmakokinetik
Eine pharmakokinetische Studie mit Natrium-RLA aus dem Jahr 2007 hat gezeigt, dass die maximale Plasmakonzentration und die Bioverfügbarkeit deutlich höher sind als bei der freien Säureform und dass durch die intravenöse Verabreichung der freien Säureform höhere Plasmaspiegel erreicht werden. Darüber hinaus wurden hohe Plasmaspiegel erreicht, die mit denen in Tiermodellen vergleichbar sind, bei denen Nrf2 aktiviert wurde. ⓘ
Die verschiedenen Formen von LA sind nicht bioäquivalent. Nur sehr wenige Studien vergleichen einzelne Enantiomere mit racemischer Liponsäure. Es ist unklar, ob die doppelte Menge an racemischer Liponsäure die RLA ersetzen kann. ⓘ
Die toxische Dosis von LA bei Katzen ist viel niedriger als bei Menschen oder Hunden und führt zu hepatozellulärer Toxizität. ⓘ
Pharmakodynamik
Der Mechanismus und die Wirkung von Liponsäure, wenn sie einem Organismus äußerlich zugeführt wird, sind umstritten. Liponsäure scheint in einer Zelle in erster Linie die oxidative Stressreaktion zu induzieren und nicht direkt freie Radikale abzufangen. Diese Wirkung ist spezifisch für RLA. Trotz des stark reduzierenden Milieus wurde LA intrazellulär sowohl in oxidierter als auch in reduzierter Form nachgewiesen. LA ist in der Lage, reaktive Sauerstoff- und Stickstoffspezies in einem biochemischen Test aufgrund langer Inkubationszeiten abzufangen, aber es gibt kaum Hinweise darauf, dass dies innerhalb einer Zelle geschieht oder dass der Radikalfänger zu den primären Wirkmechanismen von LA beiträgt. Die relativ gute Radikalfängeraktivität von LA gegenüber hypochloriger Säure (ein von Neutrophilen produziertes Bakterizid, das Entzündungen und Gewebeschäden verursachen kann) ist auf die gespannte Konformation des 5-gliedrigen Dithiolanrings zurückzuführen, die bei der Reduktion zu DHLA verloren geht. In den Zellen wird LA zu Dihydroliponsäure reduziert, die allgemein als die bioaktivere Form von LA angesehen wird und die für die meisten antioxidativen Wirkungen und die Verringerung der Redoxaktivitäten von ungebundenem Eisen und Kupfer verantwortlich ist. Diese Theorie wurde aufgrund der hohen Reaktivität der beiden freien Sulfhydride, der niedrigen intrazellulären Konzentrationen von DHLA sowie der schnellen Methylierung eines oder beider Sulfhydride, der schnellen Oxidation der Seitenkette zu kürzeren Metaboliten und des schnellen Ausflusses aus der Zelle in Frage gestellt. Obwohl sowohl DHLA als auch LA nach Verabreichung in den Zellen gefunden wurden, liegt das meiste intrazelluläre DHLA wahrscheinlich als gemischte Disulfide mit verschiedenen Cysteinresten aus zytosolischen und mitochondrialen Proteinen vor. Jüngste Erkenntnisse deuten darauf hin, dass therapeutische und Anti-Aging-Effekte auf eine Modulation der Signaltransduktion und der Gentranskription zurückzuführen sind, die den antioxidativen Status der Zelle verbessern. Dies geschieht jedoch wahrscheinlich über pro-oxidative Mechanismen und nicht durch Radikalfänger oder reduzierende Effekte. ⓘ
Alle Disulfidformen von LA (R/S-LA, RLA und SLA) können zu DHLA reduziert werden, obwohl in Modellsystemen sowohl gewebespezifische als auch stereoselektive (Bevorzugung eines Enantiomers gegenüber dem anderen) Reduktionen berichtet wurden. Mindestens zwei zytosolische Enzyme, Glutathion-Reduktase (GR) und Thioredoxin-Reduktase (Trx1), und zwei mitochondriale Enzyme, Lipoamid-Dehydrogenase und Thioredoxin-Reduktase (Trx2), reduzieren LA. SLA wird stereoselektiv durch zytosolisches GR reduziert, während Trx1, Trx2 und Lipoamid-Dehydrogenase stereoselektiv RLA reduzieren. (R)-(+)-Liponsäure wird enzymatisch oder chemisch zu (R)-(-)-Dihydroliponsäure reduziert, während (S)-(-)-Liponsäure zu (S)-(+)-Dihydroliponsäure reduziert wird. Dihydroliponsäure (DHLA) kann auch intra- und extrazellulär über nicht-enzymatische Thiol-Disulfid-Austauschreaktionen gebildet werden. ⓘ
RLA kann in vivo wie ein B-Vitamin und in höheren Dosen wie pflanzliche Nährstoffe wie Curcumin, Sulforaphan, Resveratrol und andere Nährstoffe wirken, die Phase-II-Entgiftungsenzyme induzieren und somit als zytoprotektive Mittel wirken. Diese Stressreaktion verbessert indirekt die antioxidative Kapazität der Zelle. ⓘ
Das (S)-Enantiomer von LA erwies sich bei Verabreichung an Ratten mit Thiaminmangel als toxisch. ⓘ
Mehrere Studien haben gezeigt, dass SLA entweder eine geringere Aktivität als RLA hat oder die spezifischen Wirkungen von RLA durch kompetitive Hemmung beeinträchtigt. ⓘ
Verwendungen
R/S-LA und RLA sind in den Vereinigten Staaten als Nahrungsergänzungsmittel in Form von Kapseln, Tabletten und wässrigen Flüssigkeiten erhältlich und werden als Antioxidantien vermarktet. ⓘ
Obwohl der Körper LA synthetisieren kann, kann es auch über die Nahrung aufgenommen werden. Eine Nahrungsergänzung in Dosen von 200-600 mg liefert wahrscheinlich das bis zu 1000-fache der Menge, die über die normale Ernährung aufgenommen wird. Die gastrointestinale Absorption ist variabel und nimmt mit der Aufnahme von Nahrung ab. Es wird daher empfohlen, LA 30-60 Minuten vor oder mindestens 120 Minuten nach einer Mahlzeit einzunehmen. Maximale LA-Blutspiegel werden 30-60 Minuten nach der Nahrungsergänzung erreicht, und man nimmt an, dass LA größtenteils in der Leber metabolisiert wird. ⓘ
In Deutschland ist LA seit 1966 als Medikament zur Behandlung der diabetischen Neuropathie zugelassen und als rezeptfreies Arzneimittel erhältlich. ⓘ
Klinische Forschung
Laut der American Cancer Society (Stand 2013) gibt es derzeit keine verlässlichen wissenschaftlichen Beweise dafür, dass Liponsäure die Entstehung oder Ausbreitung von Krebs verhindert". Mit Stand von 2015 ist intravenös verabreichte ALA weltweit außer in Deutschland nicht für diabetische Neuropathie zugelassen, hat sich aber in vier klinischen Studien als einigermaßen sicher und wirksam erwiesen; eine weitere große Studie über vier Jahre ergab jedoch keinen Unterschied zu Placebo. Im Jahr 2012 gab es keine guten Beweise dafür, dass Alpha-Liponsäure Menschen mit mitochondrialen Störungen hilft. In einer Übersichtsarbeit aus dem Jahr 2018 wird ALA als Nahrungsergänzungsmittel gegen Fettleibigkeit in niedriger Dosierung (< 600 mg/Tag) für einen kurzen Zeitraum (< 10 Wochen) empfohlen; es ist jedoch zu teuer, um als ergänzende Therapie bei Fettleibigkeit sinnvoll zu sein. ⓘ
Andere Liponsäuren
- β-Liponsäure ist ein Thiosulfinat der α-Liponsäure ⓘ
Struktur und Isomerie
α-Liponsäure ist eine schwefelhaltige Fettsäure, wobei die beiden Schwefelatome in einer Ringstruktur miteinander verbunden sind. Die natürliche α-Liponsäure ist am (einzigen) stereogenen Zentrum (R)-konfiguriert; ihr Enantiomer ist (S)-konfiguriert. ⓘ
| Isomere von Liponsäure ⓘ | ||
| Name | (R)-Liponsäure | (S)-Liponsäure |
| Andere Namen | L-Liponsäure (+)-Liponsäure |
D-Liponsäure (−)-Liponsäure |
| Strukturformel | 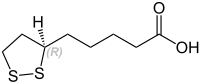
|

|
| CAS-Nummer | 1200-22-2 | 1077-27-6 |
| 1077-28-7 (RS) | ||
| EG-Nummer | 638-752-2 | 664-251-3 |
| 214-071-2 (unspez.) | ||
| ECHA-Infocard | 100.166.365 | 100.190.488 |
| 100.012.793 (unspez.) | ||
| PubChem | 6112 | 445125 |
| 864 (unspez.) | ||
| DrugBank | DB00166 | − |
| Wikidata | Q27887203 | Q21097956 |
| Q312229 (unspez.) | ||
In der Natur sind nur die (R)-Liponsäure (Synonym L-Liponsäure) und ihre reduzierte Form, die Dihydroliponsäure (6,8-Dimercaptooctansäure), biologisch aktiv. Strukturanaloga mit sechs- oder mehrgliedrigen Ringen sind biologisch unwirksam. ⓘ
Als Arzneistoff wird außer der (R)-Liponsäure auch das Racemat (RS)-Liponsäure [Synonyme: DL-Liponsäure, (±)-Liponsäure] verwendet. ⓘ
Verwendung
α-Liponsäure wird seit 1966 in Deutschland als Arzneistoff zur Behandlung von Lebererkrankungen und bei peripheren Polyneuropathien eingesetzt. ⓘ
In der Chelat-Therapie kann α-Liponsäure bei Vergiftung mit anorganischen Quecksilberverbindungen eingesetzt werden. Im Gegensatz zu anderen Chelatbildnern wie DMSA oder DMPS kann Liponsäure in alle Bereiche des zentralen und peripheren Nervensystems eindringen, kann insbesondere die Blut-Hirn-Schranke passieren. Ihre Wirksamkeit zu diesem Zweck beruht vor allem auf ihrer reduzierten Form Dihydroliponsäure, einem Dithiol, das starke antioxidative Eigenschaften besitzt und Chelatbindungen eingehen kann. Die Ausscheidung dieser Komplexe erfolgt fast ausschließlich über die Gallenwege. ⓘ
α-Liponsäure wirkt als Antidot bei Vergiftungen mit Amanita-Pilzen. ⓘ
Wegen ihrer antioxidativen Wirkung wird α-Liponsäure auch als Nahrungsergänzungsmittel (NEM) angeboten. Eine Warnung zur Höchstmenge diesbezüglicher NEMs gibt es nicht, die tägliche Einnahme von 0,6 mg pro Kilogramm Körpergewicht betrachtet die Bayerische Kontrollbehörde für Lebensmittelsicherheit und Veterinärwesen als unbedenklich. Eine Überdosierung (z. B. bei 50 bis 100 mg pro kg KW) kann zu Toxizitäten führen: zunächst psychomotorische Unruhe oder Bewusstseinstrübung, später treten generalisierte Krampfanfälle und Hypoglykämien auf, bei massiven Überdosierungen besteht die Gefahr für Schock. ⓘ
Für eine behauptete Wirkung gegen das Fortschreiten von Demenz des Alzheimer-Typus fehlen aussagekräftige Belege, es ist daher nicht bekannt, ob α-Liponsäure die Krankheit abmildern oder sogar davor schützen vermag. ⓘ
Handelsnamen
- Monopräparate
Alpha-Lipogamma (D), Alpha-Lipon STADA (D), Alpha-Vibolex (D), Biomo-Lipon (D), espa-lipon (D), Liponsäure-ratiopharm (D), Neurium (D), Pleomix-Alpha (D), Sana Alpha-Liponsäure (D), Thioctacid (D, A), Thiogamma (D), Tromlipon (D), Vitatrans (D), Alpha-Lipon AL (D), Alpan (D), Unilipon (D). ⓘ