Budesonid
 | |
 | |
| Klinische Daten | |
|---|---|
| Handelsnamen | Pulmicort, Rhinocort, Entocort, andere |
| Andere Namen | BUD |
| AHFS/Drugs.com | Monographie |
| MedlinePlus | a608007 |
| Lizenz-Daten |
|
| Schwangerschaft Kategorie |
|
| Wege der Verabreichung | Durch den Mund, nasal, tracheal, rektal, Inhalation |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | 10-20% (First-Pass-Effekt) |
| Proteinbindung | 85-90% |
| Verstoffwechselung | CYP3A4 in der Leber |
| Eliminationshalbwertszeit | 2,0-3,6 Stunden |
| Ausscheidung | Urin, Fäkalien |
| Bezeichner | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| PDB-Ligand |
|
| Chemische und physikalische Daten | |
| Formel | C25H34O6 |
| Molare Masse | 430,541 g-mol-1 |
| 3D-Modell (JSmol) | |
SMILES
| |
InChI
| |
| | |
Budesonid, das unter anderem unter dem Markennamen Pulmicort verkauft wird, ist ein Medikament vom Typ der Kortikosteroide. Es ist als Inhalator, Vernebelungslösung, Pille, Nasenspray und rektale Form erhältlich. Die inhalative Form wird zur Langzeitbehandlung von Asthma und chronisch obstruktiver Lungenerkrankung (COPD) eingesetzt. Das Nasenspray wird bei allergischer Rhinitis und Nasenpolypen eingesetzt. Die Tabletten mit verzögerter Wirkstofffreisetzung und die rektalen Formen können bei entzündlichen Darmerkrankungen wie Morbus Crohn, Colitis ulcerosa und mikroskopischer Colitis eingesetzt werden. ⓘ
Häufige Nebenwirkungen der inhalativen Form sind Infektionen der Atemwege, Husten und Kopfschmerzen. Zu den häufigen Nebenwirkungen der Tabletten gehören Müdigkeit, Erbrechen und Gelenkschmerzen. Zu den schwerwiegenden Nebenwirkungen gehören ein erhöhtes Infektionsrisiko, Verlust der Knochenstärke und Katarakte. Die langfristige Einnahme der Pillenform kann zu einer Nebenniereninsuffizienz führen. Ein plötzliches Absetzen der Tabletten nach langfristiger Einnahme kann daher gefährlich sein. Die inhalative Form ist im Allgemeinen in der Schwangerschaft sicher. Budesonid wirkt vor allem als Glukokortikoid. ⓘ
Budesonid wurde erstmals 1973 patentiert. Die kommerzielle Verwendung als Asthma-Medikament begann 1981. Es steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation. Einige Formen sind als Generika erhältlich. Im Jahr 2019 wurde das Generikum Budesonid als an der Preisabsprache von Teva in den Vereinigten Staaten beteiligt aufgeführt. Im Jahr 2019 war es das 201. am häufigsten verschriebene Medikament in den Vereinigten Staaten, mit mehr als 2 Millionen Verschreibungen. ⓘ
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Grundstrukturformel (Stereozentrum in Position 22 ist mit einem * markiert) | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Budesonid | ||||||||||||||||||
| Andere Namen |
16α,17-[(RS)-Butan-1,1-diyldioxy]-11β,21-dihydroxypregna-1,4-dien-3,20-dion (IUPAC) | ||||||||||||||||||
| Summenformel | C25H34O6 | ||||||||||||||||||
| Kurzbeschreibung |
weißes bis fast weißes, kristallines Pulver | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Wirkstoffklasse | |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 430,53 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
226 °C | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
| ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Das Team um Mona Bafadhel an der University of Oxford in Großbritannien stellte im Februar 2021 fest, dass Patienten, die infolge Atemwegserkrankungen Budesonid als trockenes Aerosol via Luftröhre inhalieren, wesentlich weniger von schweren Symptomen von COVID-19 betroffen waren als eine Vergleichsgruppe. Die Daten dieser Studie reichen für eine breite Anwendung jedoch noch nicht aus. ⓘ
Medizinische Anwendungen
Asthma
Budesonid wird per Dosierinhalator oder Vernebler zur Erhaltungstherapie und prophylaktischen Behandlung von Asthma verabreicht, einschließlich Patienten, die orale Kortikosteroide benötigen, und Patienten, die von einer systemischen Dosisreduktion profitieren können. ⓘ
Entzündliche Darmerkrankungen
Formulierungen von Budesonid mit verzögerter Wirkstofffreisetzung sind eine wirksame Behandlung bei leichtem bis mittelschwerem Morbus Crohn, der das Ileum und/oder den aufsteigenden Dickdarm betrifft. Eine Cochrane-Überprüfung ergab, dass die Remission bei Morbus Crohn bis zu drei Monate (aber nicht länger) aufrechterhalten werden kann. ⓘ
Budesonid unterstützt die Induktion einer Remission bei Menschen mit aktiver Colitis ulcerosa. ⓘ
Budesonid ist hochwirksam und wird als Mittel der Wahl bei mikroskopischer Kolitis, zur Induktion und Aufrechterhaltung der Remission und sowohl bei der lymphozytären Kolitis als auch bei der kollagenen Kolitis empfohlen. ⓘ
Allergischer Schnupfen
Budesonid in Form von Nasensprays ist ein Mittel zur Behandlung der allergischen Rhinitis. ⓘ
Eosinophile Ösophagitis
Topisches Budesonid hat erhebliche Auswirkungen auf die eosinophile Ösophagitis. Zu diesem Zweck wird es als Tablette formuliert, die sich im Mund verteilt, und unter dem Handelsnamen Jorveza verkauft. ⓘ
Bergersche Krankheit
Budesonid (Tarpeyo) ist angezeigt zur Verringerung der Proteinurie (erhöhter Eiweißgehalt im Urin) bei Erwachsenen mit primärer Immunglobulin A (IgA)-Nephropathie (Berger-Krankheit), bei denen das Risiko eines raschen Fortschreitens der Krankheit besteht. ⓘ
Nebenwirkungen
Nasale Budesonid-Inhalatoren wurden mit einer Reihe von Nebenwirkungen in Verbindung gebracht. Dazu gehören Nasenreizung oder -brennen, Nasenbluten oder -wunden, Benommenheit, Magenverstimmung, Husten, Heiserkeit, Mundtrockenheit, Hautausschlag, Halsschmerzen, schlechter Geschmack im Mund, Veränderung des Schleims und verschwommenes Sehen. Andere Symptome, die sofort gemeldet werden sollten, sind Atembeschwerden, Schwellungen im Gesicht, weiße Flecken im Hals, Mund oder Nase, unregelmäßige Menstruation, schwere Akne und in seltenen Fällen, Verhaltensänderungen (meist bei Kindern) ⓘ
Häufige Nebenwirkungen bei der Einnahme von Budesonid sind:
Kontraindikationen
Budesonid ist kontraindiziert als Erstbehandlung des Status asthmaticus oder anderer akuter Asthmaanfälle, die intensive Maßnahmen erfordern. Es ist auch kontraindiziert für Patienten, die überempfindlich auf Budesonid reagieren. ⓘ
Wechselwirkungen
Wer Tabletten oder Kapseln oral einnimmt, sollte Grapefruit und Grapefruitsaft sowie Echinacea vermeiden. ⓘ
- Grapefruitsaft kann die Bioverfügbarkeit von oralem Budesonid verdoppeln.
- Echinacea vermindert die Bioverfügbarkeit. ⓘ
Auch fettreiche Mahlzeiten verzögern die Absorption, beeinträchtigen sie aber nicht. ⓘ
Pharmakologie
Budesonid ist ein Agonist der Glucocorticoid-Rezeptoren. Zu seinen Wirkungen gehören:
- Steuert die Geschwindigkeit der Proteinsynthese.
- Es hemmt die Migration von polymorphkernigen Leukozyten und Fibroblasten.
- hebt die Kapillarpermeabilität und die lysosomale Stabilisierung auf zellulärer Ebene auf, um Entzündungen zu verhindern oder zu kontrollieren.
- Hat eine starke Glukokortikoid-Aktivität und eine schwache Mineralokortikoid-Aktivität. ⓘ
Wirkung
Budesonid wirkt am Ort seiner Zufuhr oder Freisetzung (als Tropfen oder Spray in der Nase, als Inhalation im Bronchialsystem, als Kapseln oder Klysma im Darm). Wenn die Substanz in die Blutbahn gelangt – beispielsweise durch Verschlucken und Resorption –, ist die Wirksamkeit auf den Gesamtorganismus („systemische Wirkung“) aufgrund des starken Abbaus bei der ersten Leberpassage (First-Pass-Effekt) nur gering. Daher sind die typischen Nebenwirkungen der Glucocorticoide weniger ausgeprägt vorhanden. ⓘ
Bei Inhalation von Budesonid kann es zu einer Pilzinfektion in der Mundhöhle oder zu Heiserkeit kommen. Deshalb sollte diese Anwendung immer vor einer Mahlzeit erfolgen oder der Mund anschließend gut ausgespült werden. Bei Inhalation ist auch zu beachten, dass der Wirkstoff seine Wirkung erst nach 1–4 Wochen entfaltet, da er für die Langzeitbehandlung vorgesehen ist. ⓘ
Budesonid kann auch im akuten Schub bei Morbus Crohn eingesetzt werden, wenn der aufsteigende Teil des Dickdarms betroffen ist. Die Therapie ist zwar weniger effektiv als mit anderen Glukokortikoiden, aber es treten weniger unerwünschte Wirkungen auf. Ebenso gibt es bereits Präparate zur Behandlung von Colitis ulcerosa. Insbesondere wenn sich die Entzündung auf den Enddarm beschränkt, ist die lokale Behandlung durch Klysmen relativ wirksam und gleichzeitig nebenwirkungsarm. Auch hierbei setzt die volle Wirkung erst nach 2–4 Wochen ein. ⓘ
- Beginn der Wirkung: Vernebelung: 2-8 Tage; Inhalation: 24 Stunden; Nasal: 10 Stunden
- Spitzenwert der Wirkung: Vernebelung: 4-6 Wochen; Inhalation: 1-2 Wochen
- Verteilung: 2,2-3,9 L/kg
- Proteinbindung: 85% bis 90%
- Metabolismus: hepatisch über CYP3A4 zu zwei Metaboliten: 16 alpha-Hydroxyprednisolon und 6 beta-Hydroxybudesonid; geringe Aktivität
- Budesonid wird im ersten Durchgang extensiv metabolisiert, was zu einer geringen Bioverfügbarkeit und systemischen Wirkungen führt
- Bioverfügbarkeit: Kapsel: 9% bis 21%; Vernebelung: 6%; Inhalation: 6% bis 13%
- Eliminationshalbwertszeit: 2-3,6 Stunden
- Zeit bis zum Höhepunkt: Kapsel: 0,5-10 Stunden (variabel bei Morbus Crohn); Vernebelung: 10-30 Minuten; Inhalation: 1-2 Stunden; Tablette: 7,4-19,2 Stunden
- Ausscheidung: Urin (60%) und Fäkalien als Metaboliten. ⓘ
Chemie
Budesonid, auch bekannt als 11β,21-Dihydroxy-16α,17α-(Butylidenbis(oxy))pregna-1,4-dien-3,20-dion, ist ein synthetisches Pregnan-Steroid und nicht-halogeniertes zyklisches Ketal-Kortikosteroid. Es ist das C16α-Hydroxyl, C16α,17α-zyklische Ketal mit Butyraldehyd-Derivat von Prednisolon (11β,17α,21-Trihydroxypregna-1,4-dien-3,20-dion). ⓘ
Stereoisomerie
Budesonid ist ein Diastereomerengemisch, bei dem die Konfiguration aller Stereozentren identisch ist, mit einer Ausnahme am C-22; daher stehen die beiden Diastereomere mit der (22R)- bzw. (22S)-Konfiguration in einem Verhältnis von 1:1. ⓘ
Das (22R)-Isomer ist auch unter der Bezeichnung Dexbudesonid bekannt. ⓘ
| Isomere von Budesonid ⓘ | ||
| Name | (22R)-Budesonid | (22S)-Budesonid |
| Andere Namen | Dexbudesonid | |
| Strukturformel | 
|
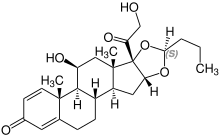
|
| CAS-Nummer | 51372-29-3 | 51372-28-2 |
| 51333-22-3 (Gemisch) | ||
| EG-Nummer | 257-161-7 | 257-160-1 |
| 257-139-7 (Gemisch) | ||
| ECHA-Infocard | 100.051.947 | 100.051.946 |
| 100.007.162 (Gemisch) | ||
| PubChem | 40000 | 63006 |
| 5281004 (Gemisch) | ||
| Wikidata | Q27254753 | Q27251792 |
| Q422212 (Gemisch) | ||
Gesellschaft und Kultur
Rechtlicher Status
Am 19. Mai 2022 gab der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittel-Agentur (EMA) ein positives Gutachten ab, in dem er die Erteilung einer bedingten Zulassung für das Arzneimittel Kinpeygo zur Behandlung der primären Immunglobulin-A-Nephropathie empfiehlt. Der Antragsteller für dieses Arzneimittel ist Calliditas Therapeutics AB. Kinpeygo ist ein Hybridpräparat von Entocort, das seit dem 2. April 1992 in der EU zugelassen ist. Kinpeygo enthält den gleichen Wirkstoff wie Entocort, hat aber eine andere Formulierung und ein anderes Anwendungsgebiet. ⓘ
Markennamen

Aeronide (TH); Aquacort (DE); B Cort (CO); Bronex (PH); Budair (MY); Budecort DP (MY); Budenofalk (DE, GB, HK, KP, PH, SG); Budeson (AR); Budeson Aqua (AR); BudeSpray (TH); Budiair (KP); Budicort Respules (IL); Budinide (KSA); Bunase (TH); Clebudan (CN); Cortiment (CA, GB, AU); Cycortide (HK); Denecort (PH); Duasma (TW); Eltair (MY); Entocort (AR, AT, BE, BR, CH, CZ, DK, FI, FR, GB, HK, IE, IL, IT, KP, NL, NO, PL, PT, SE, TR); Giona Easyhaler (MY, SG, TH); Inflammide (PE); Miflonid (CZ); Miflonide (BE, DE, IL, IT, NZ, PT); Neumocort (PY); Novopulmon (DE, FR); Pulmicon Susp für Vernebler (KP); Pulmicort (AT, BE, BG, BR, CH, CL, CN, CO, CR, CZ, DE, DK, DO, EE, FI, FR, GB, GR, GT, HN, ID, IN, NI, NL, NO, PA, PK, PL, PT, RU, SE, SV, TR, TW, UY, VE, ZA); Pulmicort Nasal Turbohaler (CL, KE, MU, NG); Pulmicort Turbuhaler (KE, MU, NG); Rafton (FR); Rhinocort (AU); Rhinocort Aqua (HK); Rhinoside (GR); Symbicort (FR, US, ZA) Uceris (US). ⓘ
Forschung
COVID-19
Budesonid wurde im April 2021 vom britischen Nationalen Gesundheitsdienst (NHS) zur Behandlung von COVID-19 auf Einzelfallbasis für Menschen ab 50 Jahren empfohlen. Nachdem ein Forschungsteam der Universität Oxford in einer Studie mit 1 700 Patienten festgestellt hatte, dass Budesonid vielen Menschen über 50 mit COVID-19-Symptomen zugute kommen könnte, wurde es ab dem 12. April 2021 vom Nationalen Gesundheitsdienst im Vereinigten Königreich für Allgemeinmediziner (GPs) zur Behandlung von COVID-19 auf Einzelfallbasis empfohlen. Die im August 2021 veröffentlichten Ergebnisse einer groß angelegten Studie deuten darauf hin, dass inhalatives Budesonid die Genesungszeit und das Wohlbefinden der Betroffenen während des Genesungsprozesses verbessert. Die Empfehlung wurde im Dezember 2021 mit der Begründung zurückgezogen, dass weitere Forschungsarbeiten erforderlich seien. ⓘ
In Indien wurde inhalatives Budesonid im April 2021 in die empfohlene Behandlung von COVID-19-Fällen aufgenommen. ⓘ
Kontraindikation/Gegenanzeigen
Bei der Einnahme der Antibabypille ist Vorsicht geboten, da das Hormon Ethinylestradiol von dem gleichen Enzym wie der Asthma-Wirkstoff abgebaut wird. Dadurch kann sich die Konzentration von Budesonid im Blut erhöhen und die Wirkung verstärken. ⓘ
Bei einer Milchproteinempfindlichkeit darf der Wirkstoff nicht angewendet werden. ⓘ
Schwangere und stillende Frauen sollten vor der Einnahme einen Arzt konsultieren und Budesonid erst nach einer Abwägung aller Risiken anwenden. Der Wirkstoff kann durch die Plazenta auf das ungeborene Kind und die Muttermilch übertragen werden. Bei einer Studie von 6000 Schwangerschaftsverläufen gab es allerdings keinen Hinweis auf eine Gefährdung des Kindes. ⓘ
Handelsnamen
Monopräparate ⓘ
Aquacort (D), Budapp (D), Budecort (D), Budenobronch (D, A), Budenofalk (D, CH), Budes (D), Budiair (D, A), Budo-San (A), Cortiment (D), Cortinasal (CH), Cyclocaps Budesonid (D), Entocort (D, A, CH), Entocort rektal (D), Jorveza (D), Giona (A), Miflonide (D, A, CH), Novolizer Budesonid (A), Novopulmon (D), Pulmax (D), Pulmicort (D, A, CH), Rhinocort (A, CH), diverse Generika (D, A, CH) ⓘ
Kombinationspräparate ⓘ
Kombinationspräparate mit Formoterol: Bufori (D), Symbicort (D, A, CH), Vannair (CH) ⓘ