Chinin
 | |
 | |
| Klinische Daten | |
|---|---|
| Aussprache | US: /ˈkwaɪnaɪn/, /kwɪˈniːn/ oder UK: /ˈkwɪniːn/ KWIN-een |
| Handelsnamen | Qualaquin, Quinbisul, andere |
| AHFS/Drugs.com | Monographie |
| MedlinePlus | a682322 |
| Lizenz-Daten |
|
| Schwangerschaft Kategorie |
|
| Wege der Verabreichung | Durch den Mund, intramuskulär, intravenös, rektal |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Proteinbindung | 70–95% |
| Verstoffwechselung | Leber (hauptsächlich CYP3A4 und CYP2C19-vermittelt) |
| Eliminationshalbwertszeit | 8-14 Stunden (Erwachsene), 6-12 Stunden (Kinder) |
| Ausscheidung | Niere (20%) |
| Bezeichner | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Chemische und physikalische Daten | |
| Formel | C20H24N2O2 |
| Molare Masse | 324,424 g-mol-1 |
| 3D-Modell (JSmol) | |
| Schmelzpunkt | 177 °C (351 °F) |
SMILES
| |
InChI
| |
| | |
Chinin ist ein Medikament, das zur Behandlung von Malaria und Babesiose eingesetzt wird. Dazu gehört auch die Behandlung von Malaria durch Plasmodium falciparum, die gegen Chloroquin resistent ist, wenn Artesunat nicht verfügbar ist. Obwohl Chinin manchmal bei nächtlichen Wadenkrämpfen eingesetzt wird, wird es wegen des Risikos schwerer Nebenwirkungen nicht für diesen Zweck empfohlen. Es kann durch den Mund oder intravenös eingenommen werden. In bestimmten Gebieten der Welt gibt es Resistenzen gegen Chinin. Chinin ist auch der Inhaltsstoff von Tonic Water, der ihm seinen bitteren Geschmack verleiht. ⓘ
Häufige Nebenwirkungen sind Kopfschmerzen, Ohrensausen, Sehstörungen und Schweißausbrüche. Zu den schwereren Nebenwirkungen gehören Taubheit, niedrige Blutplättchen und ein unregelmäßiger Herzschlag. Die Einnahme kann die Anfälligkeit für Sonnenbrände erhöhen. Es ist zwar unklar, ob die Einnahme während der Schwangerschaft dem Baby schadet, dennoch wird empfohlen, Malaria während der Schwangerschaft mit Chinin zu behandeln, wenn dies angebracht ist. Chinin ist ein Alkaloid, eine natürlich vorkommende chemische Verbindung. Wie es als Medikament wirkt, ist nicht ganz klar. ⓘ
Chinin wurde erstmals 1820 aus der Rinde des in Peru beheimateten Chinarindenbaums isoliert, und seine Summenformel wurde 1854 von Strecker bestimmt. Die Klasse der chemischen Verbindungen, zu der es gehört, wird daher als Chininalkaloide bezeichnet. Extrakte aus der Rinde werden seit mindestens 1632 zur Behandlung von Malaria verwendet und wurden bereits 1636 von Jesuitenmissionaren, die aus der Neuen Welt zurückkehrten, in Spanien eingeführt. Sie steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation. Die Behandlung von Malaria mit Chinin ist die erste bekannte Verwendung einer chemischen Verbindung zur Behandlung einer Infektionskrankheit. ⓘ
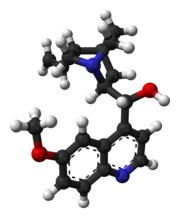
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Chinin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C20H24N2O2 | ||||||||||||||||||
| Kurzbeschreibung |
weißer, geruchloser kristalliner Feststoff | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Wirkstoffklasse |
Muskelrelaxans, Malariamittel | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 324,42 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
| ||||||||||||||||||
| pKS-Wert |
| ||||||||||||||||||
| Löslichkeit |
sehr schwer löslich in Wasser (0,5 g·l−1 bei 20 °C) | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Verwendungen
Medizinisch
Seit 2006 wird Chinin von der Weltgesundheitsorganisation (WHO) nicht mehr als Mittel der ersten Wahl zur Behandlung von Malaria empfohlen, da es andere Substanzen gibt, die ebenso wirksam sind und weniger Nebenwirkungen haben. Die WHO empfiehlt, Chinin nur dann einzusetzen, wenn Artemisinine nicht verfügbar sind. Chinin wird auch zur Behandlung von Lupus und Arthritis eingesetzt. ⓘ
Chinin wurde häufig als Off-Label-Behandlung für nächtliche Wadenkrämpfe verschrieben, was jedoch aufgrund einer Warnung der US Food and Drug Administration (FDA), dass eine solche Praxis mit lebensbedrohlichen Nebenwirkungen verbunden ist, seltener geworden ist. Chinin kann auch als kompetitiver Hemmer der Monoaminoxidase (MAO) wirken, eines Enzyms, das Neurotransmitter aus dem Gehirn entfernt. Als MAO-Hemmer hat es das Potenzial, zur Behandlung von Personen mit psychischen Störungen, die auf Neurotransmitterdefizite zurückzuführen sind, eingesetzt zu werden. ⓘ
Verfügbare Formen
Chinin ist ein basisches Amin und wird in der Regel in Form eines Salzes angeboten. Zu den verschiedenen vorhandenen Zubereitungen gehören Hydrochlorid, Dihydrochlorid, Sulfat, Bisulfat und Gluconat. In den Vereinigten Staaten ist Chininsulfat in 324-mg-Tabletten unter dem Markennamen Qualaquin im Handel erhältlich. ⓘ
Alle Chininsalze können oral oder intravenös (IV) verabreicht werden; Chiningluconat kann auch intramuskulär (IM) oder rektal (PR) gegeben werden. Das Hauptproblem bei der rektalen Verabreichung besteht darin, dass die Dosis ausgeschieden werden kann, bevor sie vollständig resorbiert ist; in der Praxis wird dies durch die Gabe einer weiteren halben Dosis korrigiert. In den USA ist kein injizierbares Chininpräparat zugelassen; stattdessen wird Chinidin verwendet. ⓘ
| Bezeichnung | Äquivalenz Chininbase ⓘ |
|---|---|
| Chininbase | 100 mg |
| Chinin-Bisulfat | 169 mg |
| Chinindihydrochlorid | 122 mg |
| Chinin-Gluconat | 160 mg |
| Chinin-Hydrochlorid | 111 mg |
| Chinin-Sulfat-Dihydrat [(Chinin)2H2SO4∙2H2O] | 121 mg |
Getränke

Chinin ist ein geschmacksgebender Bestandteil von Tonic Water und Bitter Lemon Mixgetränken. Auf der Limonadenpistole hinter vielen Bars ist Tonic Water mit dem Buchstaben "Q" gekennzeichnet, der für Chinin steht. ⓘ
Ursprünglich wurde Tonic Water als Mittel vermarktet, das den Verbrauchern Chinin zuführte, um einen Schutz vor Malaria zu bieten. Der Überlieferung zufolge mischten die britischen Kolonialherren in Indien das Chinin-Tonic wegen seines bitteren Geschmacks mit Gin, um es schmackhafter zu machen, und schufen so den Gin-Tonic-Cocktail, der auch heute noch beliebt ist. Es ist zwar möglich, durch das Trinken von Tonic Water vorübergehend einen Chininspiegel zu erreichen, der einen Schutz vor Malaria bietet, doch ist dies kein dauerhafter Schutz. ⓘ
In Frankreich ist Chinin ein Bestandteil des Aperitifs Chinquina oder Cap Corse" und des Wein-Aperitifs Dubonnet. In Spanien wird Chinin (wegen seiner Herkunft aus dem einheimischen Chinarindenbaum auch "peruanische Rinde" genannt) manchmal mit süßem Malaga-Wein vermischt, der dann "Malaga Quina" genannt wird. In Italien wird der traditionelle aromatisierte Wein Barolo Chinato mit Chinin und lokalen Kräutern versetzt und als Digestif serviert. In Schottland verwendet das Unternehmen A.G. Barr Chinin als Bestandteil des kohlensäurehaltigen und koffeinhaltigen Getränks Irn-Bru. In Uruguay und Argentinien ist Chinin ein Bestandteil des Tonic Water von PepsiCo namens Paso de los Toros. In Dänemark wird es als Zutat in dem kohlensäurehaltigen Sportgetränk Faxe Kondi von Royal Unibrew verwendet. ⓘ
Als Aromastoff in Getränken ist Chinin in den Vereinigten Staaten auf weniger als 83 Teile pro Million und in der Europäischen Union auf 100 mg⁄l beschränkt. ⓘ
Wissenschaftlich
Chinin (und Chinidin) werden als chirale Komponente für die Liganden der asymmetrischen Sharpless-Dihydroxylierung sowie für zahlreiche andere chirale Katalysatorgrundgerüste verwendet. Aufgrund seiner relativ konstanten und bekannten Fluoreszenzquantenausbeute wird Chinin in der Photochemie als gängiger Fluoreszenzstandard verwendet. ⓘ
Kontraindikationen
Wegen des geringen Unterschieds zwischen seinen therapeutischen und toxischen Wirkungen ist Chinin eine häufige Ursache für arzneimittelinduzierte Störungen, einschließlich Thrombozytopenie und thrombotischer Mikroangiopathie. Selbst bei geringen Mengen, die in gewöhnlichen Getränken vorkommen, kann Chinin schwerwiegende unerwünschte Wirkungen haben, die mehrere Organsysteme betreffen, darunter Auswirkungen auf das Immunsystem und Fieber, Hypotonie, hämolytische Anämie, akute Nierenschäden, Lebertoxizität und Erblindung. Bei Menschen mit Vorhofflimmern, Erregungsleitungsstörungen oder Herzblock kann Chinin Herzrhythmusstörungen verursachen und sollte daher vermieden werden. ⓘ
Chinin kann bei G6PD-Mangel (einem vererbten Mangel) eine Hämolyse verursachen, aber dieses Risiko ist gering und der Arzt sollte nicht zögern, Chinin bei Menschen mit G6PD-Mangel einzusetzen, wenn es keine Alternative gibt. ⓘ
Unerwünschte Wirkungen
Chinin kann unvorhersehbare schwerwiegende und lebensbedrohliche Blut- und kardiovaskuläre Reaktionen hervorrufen, darunter niedrige Thrombozytenzahlen und hämolytisch-urämisches Syndrom/thrombotische thrombozytopenische Purpura (HUS/TTP), Long-QT-Syndrom und andere schwerwiegende Herzrhythmusstörungen einschließlich Torsades de pointes, Schwarzwasserfieber, disseminierte intravasale Gerinnung, Leukopenie und Neutropenie. Bei einigen Personen, die aufgrund von Chinin eine TTP entwickelt haben, ist es zu einem Nierenversagen gekommen. Es kann auch zu schweren Überempfindlichkeitsreaktionen wie anaphylaktischem Schock, Urtikaria, schweren Hautausschlägen, einschließlich Stevens-Johnson-Syndrom und toxischer epidermaler Nekrolyse, Angioödemen, Gesichtsödemen, Bronchospasmus, granulomatöser Hepatitis und Juckreiz führen. ⓘ
Zu den häufigsten unerwünschten Wirkungen gehört eine Gruppe von Symptomen, die als Cinchonismus bezeichnet werden und zu denen Kopfschmerzen, Gefäßerweiterung und Schwitzen, Übelkeit, Tinnitus, Hörstörungen, Schwindel oder Benommenheit, verschwommenes Sehen und Störungen der Farbwahrnehmung gehören können. Zu den schwereren Formen des Cinchonismus gehören Erbrechen, Durchfall, Bauchschmerzen, Taubheit, Blindheit und Herzrhythmusstörungen. Cinchonismus tritt viel seltener auf, wenn Chinin oral verabreicht wird, aber orales Chinin wird nicht gut vertragen (Chinin ist äußerst bitter und viele Menschen erbrechen nach der Einnahme von Chinintabletten). Andere Medikamente wie Fansidar (Sulfadoxin mit Pyrimethamin) oder Malarone (Proguanil mit Atovaquon) werden häufig eingesetzt, wenn eine orale Therapie erforderlich ist. Chinin-Ethylcarbonat ist geschmacks- und geruchsneutral, aber nur in Japan im Handel erhältlich. Bei der oralen Verabreichung von Chinin ist keine Blutzucker-, Elektrolyt- und Herzüberwachung erforderlich. ⓘ
Chinin hat verschiedene unerwünschte Wechselwirkungen mit zahlreichen verschreibungspflichtigen Arzneimitteln, wie z. B. die Verstärkung der gerinnungshemmenden Wirkung von Warfarin. ⓘ
Mechanismus der Wirkung
Chinin wird wegen seiner Toxizität für den Malariaerreger Plasmodium falciparum eingesetzt, indem es dessen Fähigkeit, Hämoglobin aufzulösen und zu metabolisieren, beeinträchtigt. Wie bei anderen Chinolin-Malariamitteln ist der genaue Wirkmechanismus von Chinin noch nicht vollständig geklärt, obwohl In-vitro-Studien darauf hindeuten, dass es die Nukleinsäure- und Proteinsynthese hemmt und die Glykolyse in P. falciparum hemmt. Die am weitesten akzeptierte Hypothese über die Wirkung von Chloroquin basiert auf dem gut untersuchten und eng verwandten Chinolin-Wirkstoff Chloroquin. Dieses Modell beinhaltet die Hemmung der Biokristallisation von Hämozoin im Häm-Entgiftungsweg, wodurch die Aggregation von zytotoxischem Häm erleichtert wird. Das freie zytotoxische Häm reichert sich in den Parasiten an und führt zu deren Tod. Chinin kann auf das Enzym Purin-Nukleosid-Phosphorylase der Malaria abzielen. ⓘ
Chemie
Die UV-Absorption von Chinin erreicht ihren Höhepunkt bei 350 nm (im UVA-Bereich). Die Fluoreszenzemission erreicht ihren Höhepunkt bei etwa 460 nm (hellblauer/cyanfarbener Farbton). Chinin ist stark fluoreszierend (Quantenausbeute ~0,58) in 0,1 M Schwefelsäurelösung. ⓘ
Synthese
Cinchona-Bäume sind nach wie vor die einzige wirtschaftlich nutzbare Chininquelle. Unter dem Druck des Zweiten Weltkriegs wurden jedoch Forschungsarbeiten zur synthetischen Herstellung von Chinin durchgeführt. Eine formale chemische Synthese wurde 1944 von den amerikanischen Chemikern R.B. Woodward und W.E. Doering durchgeführt. Seitdem wurden mehrere effizientere Totalsynthesen von Chinin durchgeführt, aber keine von ihnen kann in wirtschaftlicher Hinsicht mit der Isolierung des Alkaloids aus natürlichen Quellen konkurrieren. Der erste synthetische organische Farbstoff, Mauvein, wurde 1856 von William Henry Perkin entdeckt, als er versuchte, Chinin zu synthetisieren. ⓘ
Biosynthese

Im ersten Schritt der Chinin-Biosynthese katalysiert das Enzym Strictosidin-Synthase eine stereoselektive Pictet-Spengler-Reaktion zwischen Tryptamin und Secologanin zur Bildung von Strictosidin. Eine geeignete Modifikation von Strictosidin führt zu einem Aldehyd. Durch Hydrolyse und Decarboxylierung würde zunächst ein Kohlenstoff aus dem Iridoidteil entfernt und Corynantheal erzeugt. Dann wird die Tryptamin-Seitenkette in der Nähe des Stickstoffs gespalten, und dieser Stickstoff wird dann an die Acetaldehyd-Funktion gebunden, um Cinchonaminal zu erhalten. Durch Ringöffnung im Indol-Heterocyclus konnten neue Amin- und Ketofunktionen erzeugt werden. Der neue Chinolin-Heterocyclus würde dann durch Kombination dieses Amins mit dem bei der Tryptamin-Seitenkettenspaltung entstandenen Aldehyd gebildet, wodurch Cinchonidinon entsteht. In der letzten Stufe wird durch Hydroxylierung und Methylierung Chinin gebildet. ⓘ
Katalyse
Chinin und andere Cinchona-Alkaloide können als Katalysatoren für stereoselektive Reaktionen in der organischen Synthese verwendet werden. So bietet beispielsweise die durch Chinin katalysierte Michael-Addition eines Malononitrils an α,β-Enone ein hohes Maß an stereochemischer Kontrolle. ⓘ
Geschichte

Chinin wurde vom Volk der Quechua, das in Peru, Bolivien und Ecuador beheimatet ist, als Muskelrelaxans verwendet, um das Frösteln zu stoppen. Die Quechua mischten die gemahlene Rinde des Chinarindenbaums mit gesüßtem Wasser, um den bitteren Geschmack der Rinde auszugleichen, und stellten so etwas Ähnliches wie Tonic Water her. ⓘ
Spanische Jesuitenmissionare waren die ersten, die Chinarinde nach Europa brachten. Die Spanier hatten die Verwendung von Chinarinde durch die Quechua beobachtet und waren sich der medizinischen Eigenschaften der Chinarinde bereits in den 1570er Jahren oder früher bewusst: Nicolás Monardes (1571) und Juan Fragoso (1572) beschrieben beide einen Baum, der später als Chinarinde identifiziert wurde und aus dessen Rinde ein Getränk gegen Durchfall hergestellt wurde. Chinin wurde von den Europäern mindestens seit dem frühen 17. Jahrhundert in nicht extrahierter Form verwendet. ⓘ
Eine populäre Geschichte, wonach es von der Gräfin von Chinchon nach Europa gebracht wurde, wurde von dem Medizinhistoriker Alec Haggis um 1941 widerlegt. Im 17. Jahrhundert war die Malaria in den Sümpfen und Marschen um Rom endemisch. Sie hatte den Tod mehrerer Päpste, vieler Kardinäle und unzähliger römischer Bürger verursacht. Die meisten der in Rom ausgebildeten katholischen Priester hatten Malariakranke gesehen und waren mit dem Schüttelfrost vertraut, der durch die fieberhafte Phase der Krankheit ausgelöst wurde. ⓘ
Der Jesuit Agostino Salumbrino (1564-1642), ein ausgebildeter Apotheker, der in Lima (im heutigen Peru) lebte, beobachtete, wie die Quechua die Rinde des Chinarindenbaums zur Behandlung dieses Schüttelfrosts verwendeten. Die Wirkung bei der Behandlung von Malaria (und malariabedingtem Frösteln) stand zwar in keinem Zusammenhang mit der Wirkung bei der Bekämpfung von Frösteln aufgrund von Starre, doch war es ein erfolgreiches Mittel gegen Malaria. Bei der ersten Gelegenheit schickte Salumbrino eine kleine Menge nach Rom, um sie als Malariamittel zu testen. In den folgenden Jahren wurde die Chinarinde, die auch als Jesuitenrinde oder peruanische Rinde bekannt war, zu einer der wertvollsten Waren, die aus Peru nach Europa verschifft wurden. Als König Karl II. Ende des 17. Jahrhunderts mit Chinin von Malaria geheilt wurde, wurde es in London populär. Es blieb bis in die 1940er Jahre das bevorzugte Malariamittel, bis es von anderen Medikamenten abgelöst wurde. ⓘ
Die wirksamste Form von Chinin zur Behandlung von Malaria wurde 1737 von Charles Marie de La Condamine entdeckt. Im Jahr 1820 isolierten die französischen Forscher Pierre Joseph Pelletier und Joseph Bienaimé Caventou erstmals Chinin aus der Rinde eines Baumes der Gattung Cinchona - wahrscheinlich Cinchona pubescens - und gaben der Substanz anschließend ihren Namen. Der Name leitet sich von dem ursprünglichen Quechua-Wort für die Rinde des Cinchona-Baums ab, quina oder quina-quina, was so viel wie "Rinde der Rinde" oder "heilige Rinde" bedeutet. Vor 1820 wurde die Rinde getrocknet, zu einem feinen Pulver gemahlen und mit einer Flüssigkeit (in der Regel Wein) vermischt, um getrunken zu werden. Die großflächige Verwendung von Chinin als Malariaprophylaxe begann um 1850. Im Jahr 1853 veröffentlichte Paul Briquet eine kurze Geschichte und Diskussion der Literatur über "Chinin". ⓘ
Chinin spielte bei der Kolonisierung Afrikas durch die Europäer eine wichtige Rolle. Die Verfügbarkeit von Chinin für die Behandlung von Krankheiten soll der Hauptgrund dafür gewesen sein, dass Afrika nicht mehr als "Grab des weißen Mannes" bezeichnet wurde. Ein Historiker sagte: "Es war die Wirksamkeit von Chinin, die den Kolonisten neue Möglichkeiten bot, in die Goldküste, Nigeria und andere Teile Westafrikas einzudringen". ⓘ
Um ihr Monopol auf Chinarinde aufrechtzuerhalten, begannen Peru und die umliegenden Länder Anfang des 19. Jahrhunderts, die Ausfuhr von Chinarindensamen und -schösslingen zu verbieten. Im Jahr 1865 sammelte Manuel Incra Mamani Samen einer besonders chininhaltigen Pflanze und übergab sie Charles Ledger. Ledger schickte sie an seinen Bruder, der sie an die niederländische Regierung verkaufte. Mamani wurde 1871 auf einer Saatgutsammelreise verhaftet und so schwer verprügelt, wahrscheinlich weil er die Samen an Ausländer geliefert hatte, dass er bald darauf starb. ⓘ
Im späten 19. Jahrhundert bauten die Niederländer die Pflanzen in indonesischen Plantagen an. Bald wurden sie die Hauptlieferanten des Baumes. Im Jahr 1913 gründeten sie das Kina Bureau, ein Kartell von Cinchona-Produzenten, das die Preise und die Produktion kontrollieren sollte. In den 1930er Jahren produzierten die niederländischen Plantagen auf Java 22 Millionen Pfund Chinarinde, was 97 % der weltweiten Chininproduktion entsprach. Die Versuche der USA, das Kina-Büro strafrechtlich zu verfolgen, blieben erfolglos. ⓘ
Während des Zweiten Weltkriegs waren die alliierten Mächte von ihrer Chininversorgung abgeschnitten, als Deutschland die Niederlande eroberte und Japan die Philippinen und Indonesien kontrollierte. Die USA hatten vier Millionen Chinarindensamen von den Philippinen erhalten und begannen, Chinarindenplantagen in Costa Rica anzulegen. Außerdem begannen sie, während der Cinchona-Missionen wilde Chinarinde zu ernten. Diese Lieferungen kamen zu spät. Zehntausende von US-Soldaten in Afrika und im Südpazifik starben an Malaria, weil es an Chinin mangelte. Obwohl die Japaner die Versorgung kontrollierten, setzten sie das Chinin nicht wirksam ein, so dass Tausende von japanischen Truppen im Südwestpazifik daran starben. ⓘ
Chinin blieb bis nach dem Zweiten Weltkrieg das Mittel der Wahl zur Bekämpfung der Malaria. Seitdem wurde es weitgehend durch andere Medikamente mit weniger Nebenwirkungen, wie z. B. Chloroquin, ersetzt. ⓘ
Bromo Chinine waren chininhaltige Erkältungstabletten, die von Grove Laboratories hergestellt wurden. Sie wurden erstmals 1889 auf den Markt gebracht und waren mindestens bis in die 1960er Jahre erhältlich. ⓘ
Dr. John S. Sappington, der in Zentral-Missouri forschte, entwickelte unabhängig eine Anti-Malaria-Pille aus Chinin. Sappington begann 1820 mit dem Import von Chinarinde aus Peru. Mit dem aus der Chinarinde gewonnenen Chinin entwickelte Sappington 1832 eine Pille, mit der sich neben Malaria auch eine Reihe von Fiebererkrankungen wie Scharlach, Gelbfieber und Grippe behandeln ließen. Diese Krankheiten waren in den Tälern von Missouri und Mississippi weit verbreitet. Er stellte "Dr. Sappington's Anti-Fieber-Pillen" her und verkaufte sie in ganz Missouri. Die Nachfrage war so groß, dass Dr. Sappington innerhalb von drei Jahren ein Unternehmen namens Sappington and Sons gründete, um seine Pillen landesweit zu verkaufen. ⓘ
Um 1630 verwendeten südamerikanische Indianer Pflanzen der Cinchona-Gattung aus dem Bereich der Anden innerhalb Kolumbiens und Boliviens erstmals gegen Kälte-Zittern. Außerdem wendeten sie es erfolgreich gegen durch Malariafieber bedingtes Zittern an. ⓘ
Die Legende besagt, dass es im 17. Jahrhundert dem Leibarzt des damaligen spanischen Vizekönigs von Peru gelang, dessen an Malaria erkrankte Frau, Condesa de Chinchon (1599–1640), zu heilen. Dadurch soll der Chinarindenbaum zu seinem Namen gekommen sein. Wenige Jahre später brachte der Jesuit Barnabas Cobo (1582–1657) die Chinarinde nach Madrid. Dort erreichte sie den jesuitischen Kardinal Juan de Lugo (1583–1660), der das Chinarindenpulver in Rom einführte. Er gilt als der eigentliche Propagandist der Chinarinde. Aus diesem Grund waren die Jesuiten allein zuständig für den Vertrieb. Dadurch kam es zu einem religiös geprägten Streit, denn viele Ärzte protestierten gegen die Monopolstellung der Jesuiten beim Handel der Chinarinde. ⓘ
Die Wirkung der Chinarinde war umstritten. Es gab Zweifler wie zum Beispiel den französischen Arzt Jean-Jacques Chifflet oder den Pariser Dekan Guy Patin. Krankengeschichten von zwei berühmten Patienten der Frühzeit bestätigen die Kontroversen zur Wirkung des Chinins:
- Zum einen starb der Vizekönig der Niederlande Ferdinand von Habsburg 1641 an Tertianfieber (Malaria). Dadurch kam es zu Streitereien, nachdem 1645 die Chinarinde in den Niederlanden eingeführt wurde.
- Zum anderen erhielt der Erzherzog Leopold Wilhelm von Österreich, der 1652 ebenfalls an dem Fieber erkrankte, von seinem Leibarzt Chifflet Auszüge aus der Chinarinde und erholte sich darauf. Chifflet verfasste nach der Genesung des Erzherzogs ein Buch über die Wirkung von Chinin (Jean-Jacques Chifflet: Pulvis febrifugus orbis Americani Iussu Serenissimi Principis Leopoldi Guilielmi, Archiducis Austriae, Belgii ac Burgundiae proregis, ventilatus ratione, experienta, auctoritate, a Ioanne Iacobo Chifletio... MDCIII). Leopold Wilhelm starb erst 1662 in Wien, nicht am Fieber.
Obwohl sich die protestantischen Länder nicht von der Wirkung der Chinarinde überzeugen ließen, braute der englische Arzt Robert Talbor einen Chinarindenwein und verkaufte diesen 1679 teuer an Ludwig XIV. 1663 hatte sich das Arzneimittel in Deutschland durchgesetzt, obgleich Georg Ernst Stahl die Verwendung der Chinarinde ablehnte. Erst 1709 untersuchte Francesco Torti verstärkt die Wirkung der Chinarinde gegen Malaria und konnte diese belegen. Im späten 18. Jahrhundert manifestierte sich die Chinarinde als Therapeutikum gegen Malaria. Ein Faktor hierfür war insbesondere die Kolonisation Indiens, Amerikas und Südostasiens. Das Problem zu dieser Zeit allerdings war, dass die Rinde weiterhin aus Südamerika importiert werden musste, was zum einen sehr teuer und zum anderen sehr umständlich war. Außerdem lösten sich die Andenrepubliken allmählich von der spanischen Herrschaft. Dies hatte zur Folge, dass man neue Anbaugebiete erschließen musste. ⓘ
1944 wurde Chinin von Robert B. Woodward formal totalsynthetisiert, die tatsächliche Totalsynthese gelang Milan R. Uskokovic erst 1970. ⓘ
Der Franzose François Magendie analysierte um 1840 erstmals die physiologische Wirkung von Chinin. ⓘ
Mit Chinin wurden 1916 zum ersten Mal experimentell ausgelöste neuromuskuläre Krämpfe gehemmt. Anhand weiterer Forschungsergebnisse um 1930 kristallisierten sich zwei Haupteffekte des Chinins heraus: eine neurotrope (nervenbezogene) und eine myotrope (muskelbezogene) Wirkung. ⓘ
Größere wirtschaftskriminelle Ausmaße erreichte im 20. Jahrhundert das Chininkartell. ⓘ
Gesellschaft und Kultur
Natürliches Vorkommen
Die Rinde der Remijia enthält 0,5-2% Chinin. Die Rinde ist billiger als die Rinde von Cinchona. Da sie einen intensiven Geschmack hat, wird sie zur Herstellung von Tonic Water verwendet. ⓘ
Regulierung in den USA
Von 1969 bis 1992 gingen bei der US-amerikanischen Food and Drug Administration (FDA) 157 Berichte über Gesundheitsprobleme im Zusammenhang mit der Einnahme von Chinin ein, darunter 23 mit Todesfolge. Im Jahr 1994 verbot die FDA die Vermarktung von rezeptfreiem Chinin zur Behandlung von nächtlichen Wadenkrämpfen. Pfizer Pharmaceuticals hatte zu diesem Zweck den Markennamen Legatrin vertrieben. Es wird auch als Softgel (von SmithKlineBeecham) unter dem Namen Q-vel verkauft. Ärzte dürfen Chinin weiterhin verschreiben, aber die FDA hat die Unternehmen angewiesen, keine nicht zugelassenen chininhaltigen Arzneimittel mehr zu vermarkten. Die FDA warnt die Verbraucher auch vor der Off-Label-Verwendung von Chinin zur Behandlung von Beinkrämpfen. Chinin ist für die Behandlung von Malaria zugelassen, wurde aber auch häufig zur Behandlung von Wadenkrämpfen und ähnlichen Beschwerden verschrieben. Da Malaria lebensbedrohlich ist, werden die mit der Verwendung von Chinin verbundenen Risiken als akzeptabel angesehen, wenn es zur Behandlung dieser Krankheit eingesetzt wird. ⓘ
Obwohl Legatrin von der FDA für die Behandlung von Wadenkrämpfen verboten wurde, hat der Arzneimittelhersteller URL Mutual ein chininhaltiges Medikament namens Qualaquin auf den Markt gebracht. Es wird als Mittel zur Behandlung von Malaria vermarktet und ist in den Vereinigten Staaten nur auf Rezept erhältlich. Im Jahr 2004 meldete das CDC nur 1.347 bestätigte Malariafälle in den Vereinigten Staaten. ⓘ
Schneidendes Mittel
Chinin wird manchmal als Streckmittel in Straßendrogen wie Kokain und Heroin nachgewiesen. ⓘ
Andere Tiere
Chinin wird zur Behandlung von Infektionen mit Cryptocaryon irritans (allgemein als Weißpünktchen-, Krypto- oder Seefischkrankheit bezeichnet) bei Fischen im Meeresaquarium eingesetzt. ⓘ
Der Weg zur Totalsynthese
Chinin war ein sehr wichtiger Wirkstoff. Daher war die Aufklärung seiner Struktur und später die Totalsynthese ein interessantes Forschungsprojekt, das mit großer Anerkennung verbunden war. Vor allem im Zweiten Weltkrieg wurde die Forschung an der Synthese stark vorangetrieben, da viele Seewege blockiert wurden, sodass nicht genug Lieferungen mit dem Medikament die Truppen der Alliierten erreichen konnten. ⓘ
Als 1944 Woodward und Doering die Totalsynthese gelang, wurden sie deshalb auch in der Bevölkerung gefeiert. Obwohl die Synthese nie Anwendung fand, trug sie maßgeblich zur Weiterentwicklung der Naturstoff-Synthese bei. Woodward erkannte den Nutzen der Spektroskopie als Mittel zur Aufklärung von Strukturen an Stelle von chemischen Reaktionen. Dieser deutlich elegantere Weg war die Grundlage für die Synthesen von beispielsweise Cholesterin, Chlorophyll oder Vitamin B12. 1965 erhielt Woodward für seine Arbeiten an den Synthesen von Naturstoffen den Nobelpreis in Chemie. ⓘ
Strukturaufklärung
Schon die Strukturaufklärung war ein langer Prozess. Es dauerte 147 Jahre, bis nach der ersten Isolierung die Struktur komplett geklärt werden konnte. Dabei wurde die Summenformel, die Konstitution sowie relative und absolute Konfiguration untersucht. Die große Herausforderung bestand darin, das richtige der 16 Stereoisomeren des Chinins zu identifizieren. ⓘ
Den Anfang machte 1879 Skraup, der die Summenformel (C20H24N2O2) herausfand. 1907 bestimmte Rabe die Konstitution des Chinin-Moleküls. Auf Basis der Verknüpfung der Moleküle (ohne räumliche Orientierung) bestimmten 1950 Prelog und Häflinger die relative Konfiguration. Dies gelang ihnen durch chemische Abbaureaktionen. Dadurch bestimmten sie schrittweise jede Konfiguration an den stereogenen Zentren. Die absolute Konfiguration (es handelt sich um ein (−)-Isomer) konnte schließlich von Carter 1967 festgelegt werden. ⓘ
Totalsynthese
Nachdem die Struktur des Chinins geklärt war, begann die Forschung an der Totalsynthese von Chinin. Bis diese erstmals 1944 Robert B. Woodward und William von Eggers Doering gelang, vergingen fast 100 Jahre. Woodward und Doering brauchten 14 Monate, bis ihnen die Synthese gelang. ⓘ
Bei den Syntheseversuchen entstand unter anderem der Phenazinium-Farbstoff Mauvein (von William Perkin, der ausgehend von der Summenformel N-Allyltoluidin zu Chinin oxidieren wollte), der am Anfang der Teerfarben-Synthese steht, welche als die Wurzel der chemischen Industrie gilt. ⓘ
Die Totalsynthese, die Woodward 1944 präsentierte, bestand aus der Synthese von 7-Hydroxyisochinolin zu racemischem Chinotoxin und der Synthese von Rabe und Kindler, die bereits 1918 Chinin aus (+)-Chinotoxin gewonnen hatten. ⓘ
Den Beginn der Totalsynthese machte Louis Pasteur bereits 1853, indem er Chinin durch Erwärmen in verdünnter Säure in das isomere Chinotoxin umlagerte, und das, obwohl damals noch nichts über den Aufbau des Moleküls bekannt war. Darauf aufbauend gelang es Kindler und Rabe 65 Jahre später, 1918, Chinotoxin in einer dreistufigen Synthese in Chinin zurückzuwandeln. 1943 gelang M. Proštenik und V. Prelog die Synthese von Chinotoxin. Dafür bauten sie Cinchonin zu (+)-Homomerochinen ab. Dieses setzten sie mit Chininsäure zu (+)-Chinotoxin um. ⓘ
Die Synthese des Homomerochinens gelang schließlich Woodward und Doering 1944. Dieses stellten sie racemisch aus 7-Hydroxyisochinolin her. Das Racemat setzten sie auf dem Weg von Proštenik und Prelog zu racemischem Chinotoxin um. Mithilfe von einem D-Weinsäurederivat trennten sie die beiden Enantiomere. Den letzten Schritt, die Synthese von (+)-Chinotoxin zu Chinin, führten sie nicht mehr durch, sondern beriefen sich auf die Arbeiten von Kindler und Rabe. ⓘ
Dies führte im Nachhinein zu einigen Diskussionen. So argumentierte Gilber Stork über 50 Jahre später, dass Woodward und Doering die Arbeit von Kindler und Rabe überprüfen hätten müssen und es sich somit nicht um die erste Totalsynthese handeln könne. Gilbert Stork war auch derjenige, dem die erste stereokontrollierte Synthese von Chinin gelang, nachdem sie zuvor bereits immer weiter verfeinert wurde. Er schaffte es, in knapp 20 eleganten Reaktionsschritten die Konfiguration des chiralen Bausteins zu erhalten, weshalb nur stereoselektive Reaktionen angewandt werden konnten. ⓘ
Extraktionsverfahren
Heute können mit einem industriellen Verfahren aus einer Tonne Rinde 30–40 kg Chinin gewonnen werden. Davon werden ca. 75 % in die Pharmaindustrie, 20 % in die Getränkeindustrie und der Rest an die chemische Industrie verkauft. ⓘ
Das erste industrielle Verfahren zur Gewinnung von Chinin aus Chinarinde wurde 1823 von Friedrich Koch vorgestellt. Dieses wurde stetig weiterentwickelt, bis zum heutigen Extraktionsverfahren. Dieses wird am Beispiel des Verfahrens der Firma Buchler & Co. aus Braunschweig gezeigt. Sie sind einer von 7 Chinin-Produzenten, der einzige in Europa und mit einem Anteil von 20–30 % Weltmarktführer. ⓘ
Im ersten Schritt wird die Rinde fein zermahlen. Das Mahlgut wird dann mit gebranntem Kalk und verdünnter Natronlauge aufgeschlossen. Das Rindenpulver ist nun aufgequollen und wird dann für mehrere Stunden mit Toluol extrahiert. Toluol als organisches Lösungsmittel löst sich nicht in Wasser, sodass die Chinaalkaloide, die Fette und Harze sich in die organische Phase extrahieren. Dieses Gemisch wird im Anschluss filtriert. Um das restliche Toluol zu entfernen, wird der Filterrückstand (Chinarinde) mit Wasserdampf behandelt. Die Toluol-Phase wird währenddessen in Flüssig-Flüssig-Extraktoren mit verdünnter Schwefelsäure versetzt. Da die Chinaalkaloide als basische Amine mit der Säure Salze bilden, gehen sie aus der organischen in die wässrige Phase über. Die Fette und Harze verbleiben in der organischen Phase. Diese wird im Anschluss abgetrennt und das Toluol über Destillation zurückgewonnen. In der wässrigen Phase (die die gesamten Chinaalkaloide enthält) wird der pH-Wert exakt eingestellt, sodass durch Kristallisation bereits 70 % des Chinins ausfällt. In der restlichen Lösung befinden sich neben dem restlichen Chinin Chinidin, Chinchoin, Chinchonidin und Chininsäure. Diese können in weiteren Kristallisationsschritten gewonnen werden. Die Kristallisationsprodukte werden auf Reinheit und Lösemittelrestgehalt untersucht und dann weiterverarbeitet. ⓘ
Eigenschaften

Chinin schmeckt bitter. Es fluoresziert in saurer Lösung bei Bestrahlung mit Ultraviolettstrahlung (315–380 nm) intensiv hellblau. Dieser Effekt liegt an der auxochromen Wirkung der Methoxy-Gruppe am 10 π-Elektronensystem des Chinolins. Die Fluoreszenz verschwindet bei Zugabe von Salzsäure, da die darin enthaltenen Chloridionen die Fluoreszenz löschen. ⓘ
Mit Chrom(VI)-oxid (CrO3) kann Chinin in saurer wässriger Lösung zu Chininsäure und Merochinen oxidiert werden:
Wirkung und Verwendung
Medizinische Verwendung
Als Anti-Malaria-Mittel
Chinin gehört zu den ältesten Malariamitteln der Welt und ist auch als fiebersenkendes Heilmittel bekannt. Bis 1940 war Chinin das einzige wirksame Medikament gegen Malaria. Heute gibt es deutlich mehr und auch wirksamere Mittel zur Behandlung, sowie eine Impfung mit eingeschränktem Schutz. ⓘ
Ist der Mensch durch den Stich einer weiblichen Anopheles-Mücke infiziert worden, entwickelt sich der parasitäre Erreger im Körper weiter. Er gelangt über das Blut in die Leberzellen, wo er sich fortpflanzt und eine Überdauerungsform hervorbringt, die Monate oder sogar Jahre schlummern und danach wieder aktiv werden kann. Nach wenigen Tagen strömen viele Einzeller in die Blutbahn und befallen die roten Blutkörperchen. Ein Teil der Erreger geht in die Geschlechtsform der Gametozyten über, sodass eine Mücke, die den infizierten Menschen sticht, die Gametozyten aufnimmt und diese sich in ihr vermehren können. Sticht diese Mücke wiederum einen Menschen, wird dieser infiziert und der Infektionskreislauf schließt sich. ⓘ
In den infizierten roten Blutkörperchen zerlegt der Einzeller das Hämoglobin, um an die Aminosäuren des Komplexes zu kommen. Dabei bleibt als Spaltprodukt der eisenhaltige Farbstoff des Blutes, das Häm (Ferriprotoporphyrin IX), zurück. Dieses ist in freier Form für den Erreger giftig, weswegen er es in einem einmaligen Schutzmechanismus in Schichten übereinanderstapelt und so über Wasserstoffbrücken verknüpfte Häm-Dimere erhält, die in dieser gebundenen Form als nicht toxische Hämozoin-Kristalle (β-Hämatin) ausfallen. Die Kristallisation von β-Hämatin verläuft entgegen früheren Annahmen nicht enzymatisch. ⓘ
Chinin setzt an der Stelle gegen den Malariaerreger an, wo dieser die roten Blutkörperchen befällt und das Protein Globin des Hämoglobins abbaut, das für ihn giftige Häm jedoch über Biomineralisierung unschädlich macht. Hier liegt auch die Lebensbedrohung für den infizierten Menschen, da auf diese Weise bis zu 80 % der roten Blutkörperchen zerstört werden können, was zu einer Anämie führt. Außerdem verändert sich die Oberfläche von befallenen Blutkörperchen, sodass sie dazu neigen, die Kapillaren, besonders im Gehirn, zu verstopfen. ⓘ
Die pharmakologische Wirkung des Chinins besteht darin, die Biomineralisierung des Häms in das kristalline Hämozoin zu verhindern. Der exakte Mechanismus ist noch unbekannt. Es wurde noch nicht geklärt, ob Chinin beispielsweise die dimeren Häm-Komplexe bindet und eine weitere Zusammenlagerung aufhält oder ob es an den Kristallflächen eine Schutzschicht bildet. Klar ist jedoch, dass der Erreger sich durch den weiteren Abbau des Hämoglobins selbst tötet. ⓘ
Chinin wird heute kaum noch als Malariamedikament eingesetzt (meist zur Behandlung der komplizierten Malaria tropica), weil sich mittlerweile bei den Erregern Resistenzen entwickelt haben. Meist werden heutzutage Kombinationspräparate zur Prophylaxe und Therapie verwendet. Helfen diese bei schweren Krankheitsverläufen allerdings nicht, wird auch heute noch Chinin, manchmal in Kombination mit anderen Wirkstoffen gegeben., ⓘ
Die Malariabehandlung erfolgt über eineinhalb bis zwei Wochen mit oralen Gaben von Chininsalzen in Dosierungen, die mindestens 0,8 bis 1,0 Gramm freier Chininbase pro Tag entsprechen (z. B. Tagesgabe von 1,95 Gramm Chininsulfatdihydrat). ⓘ
Chinin wirkt außerdem schmerzstillend, in unmittelbarer Umgebung betäubend und fiebersenkend. In China wird es aufgrund der fiebersenkenden und schmerzstillenden Wirkung in geringen Dosen Mitteln zur Behandlung von grippalen Infekten beigemischt. ⓘ
Als wehenförderndes Mittel
Chinin wirkt anregend auf die Gebärmuttermuskulatur und wurde früher als wehenförderndes Mittel eingesetzt. In diesem Zusammenhang wurde Chinin als Abortivum (Abtreibungsmittel) missbraucht, was auf Grund der Aufnahme sehr hoher Dosen oftmals zum Tod der Mutter führte. Das Bundesinstitut für Risikobewertung (BfR) warnt wegen der Wirkung auf die Gebärmuttermuskulatur in einer Publikation Schwangere vor dem Verzehr. ⓘ
Gegenanzeigen
Chinin kann bei empfindlichen Personen allergische Reaktionen auslösen. Zudem sollte das Medikament bei Personen mit Überempfindlichkeiten gegen China-Alkaloide oder Xanthine vorsichtig eingesetzt werden. Personen mit Glukose-6-Phosphat-Dehydrogenase-Mangel, Tinnitus, Optikusneuritis, Myasthenia gravis, peptischem Ulcus oder Gastritis sollten auf das Präparat verzichten. Kinder, ältere Patienten oder Patienten mit ernsthaften Herzkrankheiten, Leberkrankheiten und Nierenkrankheiten sollten kein Chininsulfat einnehmen. Da Chinin fruchtschädigend wirkt, darf es nicht von Schwangeren eingenommen werden. In der Stillzeit ist es kein geeignetes Medikament, da Chinin über die Muttermilch an den Säugling abgegeben wird. ⓘ
Nebenwirkungen
Eine mögliche Oxidation des Hämoglobins durch aufgenommenes Chinin kann eine Methämoglobinämie verursachen. ⓘ
Bei Chininsulfat können vor allem bei längerer Einnahme und hohen Dosen Tinnitus, Übelkeit und Sehstörungen auftreten. Weitere Nebenwirkungen betreffen den Gastrointestinaltrakt, das Nervensystem, das kardiovaskuläre System und die Haut. Überempfindlichkeiten manifestieren sich meist durch Hautrötungen, Juckreiz, Fieber, Hautausschlag, Magenbeschwerden, Ohrensausen oder Sehstörungen. Seltene Nebenwirkungen sind Hämoglobinurie, Asthma und thrombopenische Purpura. ⓘ
Chinin ist wie jedes Präparat in Abhängigkeit von der Dosierung giftig. (siehe auch: Cinchonismus) Eine Überdosis führt unter anderem zu Schwindelgefühl, Kopfschmerz, Tinnitus, Taubheit, vorübergehender Erblindung und Herzlähmung. Die Nebenwirkungen beruhen auf einer Hemmung von Enzymen der Gewebsatmung sowie einer Blockierung der Synthese der Desoxyribonukleinsäure. Die tödliche Dosis liegt für einen erwachsenen Menschen bei etwa fünf bis zehn Gramm Chinin. Der Tod tritt durch zentrale Atemlähmung ein. ⓘ
Wechselwirkungen
Da Chinin das QT-Intervall im EKG verlängert, muss darauf geachtet werden, es nicht mit anderen Medikamenten einzunehmen, die ebenfalls eine verlängernde Wirkung auf die QT-Zeit haben. Dies könnte zu Torsade de pointes und zum Herzstillstand führen. ⓘ
In der Leber hemmt Chinin den Abbau anderer Wirkstoffe und erhöht so den Wirkstoffspiegel. Vor allem bei Präparaten wie Digitalis, Muskelrelaxantien und Antikoagulantien müssen Wechselwirkungen berücksichtigt werden. ⓘ
Nichtmedizinische Verwendung
Das bitter schmeckende Chinin wird in geringen Mengen Getränken wie Bitter Lemon oder Tonic Water zugesetzt. Als Höchstmenge ist in Deutschland 85 mg/kg in alkoholfreien Getränken, 300 mg/kg in Spirituosen zugelassen. Generell ist es ein beliebter Bittermacher der Lebensmittelindustrie und beispielsweise in Magenbitter zu finden. ⓘ
Da es sich jedoch um eine pharmakologisch wirksame Substanz handelt, muss die Verwendung in Deutschland in alkoholfreien Getränken stets kenntlich gemacht werden. ⓘ
Gelegentlich wird Chinin als Streckmittel für Heroin benutzt. ⓘ
In der chemischen Reaktionsführung kann Chinin bzw. dessen Derivate in asymmetrischen Synthesen eingesetzt werden. Aufgrund der Tatsache, dass Chinin enantiomerenrein aus der Natur gewonnen werden kann, wird es besonders dazu genutzt, mit Enantiomeren diastereomere Paare zu bilden, welche sich in chemischen und physikalischen Eigenschaften unterscheiden. Damit ist eine Trennung der zuvor chemisch und physikalisch identischen Enantiomere möglich. Chinin dient zudem oft als Katalysatorbestandteil für die Induktion einer spezifischen stereochemischen Information, damit bei einer Synthese ein höherer Anteil eines Enantiomers erhalten wird (hoher ee-Wert). Beispiele sind Epoxidierungen, Dihydroxylierungen und Aminohydroxylierungen an Doppelbindungen. ⓘ
Handelsnamen
Monopräparate
Limptar N (D, Chininsulfat) ⓘ
