Atropin
 | |
 | |
| Klinische Daten | |
|---|---|
| Handelsnamen | Atropen, andere |
| Andere Namen | Daturin |
| AHFS/Drugs.com | Monographie |
| MedlinePlus | a682487 |
| Lizenz-Daten |
|
| Schwangerschaft Kategorie |
|
| Wege der Verabreichung | Durch den Mund, intravenös, intramuskulär, rektal, ophthalmisch |
| Wirkstoffklasse | Antimuskarinikum (Anticholinergikum) |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | 25% |
| Verstoffwechselung | ≥50% hydrolysiert zu Tropin und Tropinsäure |
| Beginn der Wirkung | c. 1 Minute |
| Halbwertszeit der Eliminierung | 2 Stunden |
| Dauer der Wirkung | 30 bis 60 Minuten |
| Ausscheidung | 15-50% werden unverändert mit dem Urin ausgeschieden |
| Bezeichner | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Chemische und physikalische Daten | |
| Formel | C17H23NO3 |
| Molare Masse | 289,375 g-mol-1 |
| 3D-Modell (JSmol) | |
SMILES
| |
InChI
| |
| | |
Atropin ist ein Tropanalkaloid und ein anticholinerges Medikament, das zur Behandlung bestimmter Arten von Vergiftungen durch Nervenkampfstoffe und Pestizide sowie einiger Arten von verlangsamtem Herzschlag und zur Verringerung der Speichelproduktion bei Operationen eingesetzt wird. Es wird in der Regel intravenös oder durch Injektion in einen Muskel verabreicht. Es sind auch Augentropfen erhältlich, die zur Behandlung von Uveitis und früher Amblyopie eingesetzt werden. Die intravenöse Lösung beginnt in der Regel innerhalb einer Minute zu wirken und hält eine halbe bis eine Stunde an. Zur Behandlung einiger Vergiftungen können hohe Dosen erforderlich sein. ⓘ
Häufige Nebenwirkungen sind ein trockener Mund, große Pupillen, Harnverhalt, Verstopfung und ein schneller Herzschlag. Es sollte im Allgemeinen nicht bei Menschen mit einem Winkelverschlussglaukom verwendet werden. Es gibt zwar keine Hinweise darauf, dass die Einnahme während der Schwangerschaft zu Geburtsschäden führt, doch ist dies nicht ausreichend untersucht worden. Während der Stillzeit ist es wahrscheinlich sicher. Es ist ein Antimuskarinikum (eine Art Anticholinergikum), das durch Hemmung des parasympathischen Nervensystems wirkt. ⓘ
Atropin kommt natürlich in einer Reihe von Pflanzen aus der Familie der Nachtschattengewächse vor, darunter die Tollkirsche (Belladonna), der Stechapfel und die Alraune. Es wurde erstmals 1833 isoliert und steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation. Es ist als Generikum erhältlich. ⓘ
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
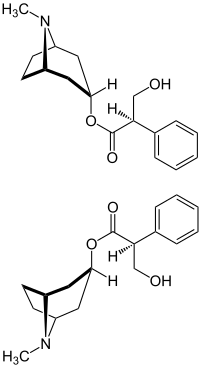
| |||||||||||||||||||
| (R)-Form (oben) und (S)-Form (unten) | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Atropin; (±)-Hyoscyamin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C17H23NO3 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Prismen | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Wirkstoffklasse |
Parasympatholytikum | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 289,38 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
118 °C | ||||||||||||||||||
| pKS-Wert |
9,43 | ||||||||||||||||||
| Löslichkeit |
wenig in Wasser (2,2 g·l−1 bei 25 °C) | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Medizinische Anwendungen
Seltener findet Atropin Anwendung bei der glatten Muskulatur im Bereich des Magen-Darm-Trakts. Auch kann Atropin bei Harninkontinenz und zur Behandlung einer Reizblase gegeben werden. Selten wurde Atropin in der Frauenheilkunde bei Dysmenorrhoe (schmerzhafte Regelblutung) eingesetzt. Den gleichen Effekt erzielt man heute mit Butylscopolamin, einem chemisch weiterentwickelten Derivat des Scopolamins, das entspannend auf die verkrampfte glatte Muskulatur wirkt und aufgrund der geringeren Nebenwirkungen rezeptfrei erhältlich ist. Als Asthmamittel wird Atropin nicht mehr verwendet, stattdessen werden besser verträgliche Arzneistoffe eingesetzt. Der Atropintest kann zur kardiologischen Diagnostik und als Hilfestellung bei der Feststellung des Hirntodes verwendet werden. ⓘ
Atropin vermindert die Speichel- und Schleimsekretion, daher kann es zum Verhindern einer übermäßigen Speichelproduktion als Nebenwirkung bei Einsatz von Ketamin sowie zur Reduktion der Speichel- und Schleimsekretion vor Operationen im Mund und Rachenbereich sowie bei fiberoptischen Intubationen und Bronchoskopien genutzt werden ⓘ
Außerdem wird Atropin auch gegen übermäßiges Schwitzen (Hyperhidrose) eingesetzt (Off-Label-Use). ⓘ

Augen
Topisches Atropin wird als Zykloplegikum zur vorübergehenden Lähmung des Akkommodationsreflexes und als Mydriatikum zur Erweiterung der Pupillen verwendet. Atropin wird nur langsam abgebaut und lässt in der Regel nach 7 bis 14 Tagen nach, so dass es im Allgemeinen als therapeutisches Mydriatikum verwendet wird, während Tropicamid (ein kürzer wirkender cholinerger Antagonist) oder Phenylephrin (ein α-adrenerger Agonist) als Hilfsmittel für die augenärztliche Untersuchung bevorzugt werden. ⓘ
Bei refraktiver und akkommodativer Amblyopie wird, wenn eine Okklusion nicht angebracht ist, manchmal Atropin verabreicht, um eine Unschärfe im guten Auge hervorzurufen. Es gibt Hinweise darauf, dass die Atropin-Bestrafung bei der Verbesserung der Sehschärfe ebenso wirksam ist wie die Okklusion. Topische Antimuskarinika sind wirksam bei der Verlangsamung des Fortschreitens der Myopie bei Kindern; Akkommodationsschwierigkeiten sowie Papillen und Follikel sind mögliche Nebenwirkungen. Alle Dosen von Atropin scheinen ähnlich wirksam zu sein, während höhere Dosen stärkere Nebenwirkungen haben. Die niedrigere Dosis von 0,01 % wird daher in der Regel empfohlen, da sie weniger Nebenwirkungen hat und sich nach dem Absetzen des Atropins nicht so schnell wieder verschlimmert. ⓘ
Herz
Atropin-Injektionen werden zur Behandlung einer symptomatischen oder instabilen Bradykardie eingesetzt. ⓘ
Atropin war früher in den internationalen Wiederbelebungsrichtlinien für den Einsatz bei Herzstillstand in Verbindung mit Asystolie und PEA enthalten, wurde aber 2010 aus diesen Richtlinien gestrichen, da es keine Belege für seine Wirksamkeit gab. Bei symptomatischer Bradykardie beträgt die übliche Dosis 0,5 bis 1 mg intravenös, die alle 3 bis 5 Minuten bis zu einer Gesamtdosis von 3 mg (maximal 0,04 mg/kg) wiederholt werden kann. ⓘ
Atropin eignet sich auch zur Behandlung eines Herzblocks zweiten Grades nach Mobitz Typ 1 (Wenckebach-Block) sowie eines Herzblocks dritten Grades mit einem hohen Purkinje- oder AV-Knoten-Escape-Rhythmus. Bei einem Mobitz-Block zweiten Grades (Typ 2) und bei einem Herzblock dritten Grades mit geringem Purkinje- oder ventrikulärem Escape-Rhythmus ist es in der Regel nicht wirksam. ⓘ
Atropin wurde auch eingesetzt, um eine niedrige Herzfrequenz während der Intubation von Kindern zu verhindern; allerdings gibt es keine Belege für diese Verwendung. ⓘ
Sekrete
Die Wirkung von Atropin auf das parasympathische Nervensystem hemmt die Speichel- und Schleimdrüsen. Das Medikament kann auch das Schwitzen über das sympathische Nervensystem hemmen. Dies kann bei der Behandlung von Hyperhidrosis nützlich sein und das Todesröcheln sterbender Patienten verhindern. Obwohl Atropin von der FDA für diese beiden Zwecke nicht offiziell zugelassen ist, wird es von Ärzten für diese Zwecke verwendet. ⓘ
Vergiftungen
Atropin ist kein wirkliches Gegenmittel für Organophosphatvergiftungen. Da Atropin jedoch die Wirkung von Acetylcholin an Muskarinrezeptoren blockiert, dient es auch zur Behandlung von Vergiftungen durch Organophosphat-Insektizide und Nervenkampfstoffe wie Tabun (GA), Sarin (GB), Soman (GD) und VX. Truppen, die Gefahr laufen, mit chemischen Waffen angegriffen zu werden, tragen häufig Autoinjektoren mit Atropin und einem Oxim zur schnellen Injektion in die Oberschenkelmuskulatur bei sich. Im Falle einer fortgeschrittenen Nervengasvergiftung ist eine maximale Atropinisierung wünschenswert. Atropin wird häufig in Verbindung mit dem Oxim Pralidoximchlorid verwendet. ⓘ
Einige Nervenkampfstoffe greifen die Acetylcholinesterase an und zerstören sie durch Phosphorylierung, so dass die Wirkung von Acetylcholin übermäßig wird und sich verlängert. Pralidoxim (2-PAM) kann gegen Organophosphatvergiftungen wirksam sein, da es diese Phosphorylierung wieder aufheben kann. Atropin kann eingesetzt werden, um die Wirkung der Vergiftung zu verringern, indem es die muskarinischen Acetylcholinrezeptoren blockiert, die andernfalls durch eine übermäßige Acetylcholinanreicherung überstimuliert würden. ⓘ
Atropin oder Diphenhydramin können zur Behandlung einer Muscarin-Intoxikation eingesetzt werden. ⓘ
Irinotecan-induzierte Diarrhöe
Es wurde beobachtet, dass Atropin eine durch Irinotecan induzierte akute Diarrhöe verhindert oder behandelt. ⓘ
Nebenwirkungen
Zu den Nebenwirkungen von Atropin gehören Kammerflimmern, supraventrikuläre oder ventrikuläre Tachykardie, Schwindel, Übelkeit, verschwommenes Sehen, Gleichgewichtsverlust, erweiterte Pupillen, Photophobie, Mundtrockenheit und möglicherweise extreme Verwirrung, delirante Halluzinationen und Erregung, insbesondere bei älteren Menschen. Die letztgenannten Wirkungen sind darauf zurückzuführen, dass Atropin in der Lage ist, die Blut-Hirn-Schranke zu überwinden. Aufgrund der halluzinogenen Eigenschaften wird Atropin von einigen Menschen als Freizeitdroge verwendet, was jedoch potenziell gefährlich und oft unangenehm ist. ⓘ
In Überdosen ist Atropin giftig. Atropin wird manchmal zu potenziell süchtig machenden Medikamenten hinzugefügt, insbesondere zu Opioid-Medikamenten gegen Durchfall wie Diphenoxylat oder Difenoxin, wobei die sekretionsreduzierende Wirkung des Atropins auch die durchfallhemmende Wirkung unterstützen kann. ⓘ
Obwohl Atropin in Notfallsituationen die Bradykardie (langsame Herzfrequenz) behandelt, kann es bei sehr niedrigen Dosen (d. h. <0,5 mg) zu einer paradoxen Verlangsamung der Herzfrequenz führen, vermutlich als Folge einer zentralen Wirkung im ZNS. Ein vorgeschlagener Mechanismus für die paradoxe bradykarde Wirkung von Atropin bei niedrigen Dosen besteht in der Blockade hemmender präsynaptischer Muscarin-Autorezeptoren, wodurch ein System blockiert wird, das die parasympathische Reaktion hemmt. ⓘ
Atropin wirkt bei Dosen von 10 bis 20 mg pro Person handlungsunfähig. Seine LD50 wird auf 453 mg pro Person (durch den Mund) mit einer Probit-Steigung von 1,8 geschätzt. Das Antidot für Atropin ist Physostigmin oder Pilocarpin. ⓘ
Eine gängige Eselsbrücke zur Beschreibung der physiologischen Erscheinungen einer Atropin-Überdosierung lautet: "heiß wie ein Hase, blind wie eine Fledermaus, trocken wie ein Knochen, rot wie eine Rübe und verrückt wie ein Hutmacher". Diese Assoziationen spiegeln die spezifischen Veränderungen der warmen, trockenen Haut durch vermindertes Schwitzen, verschwommenes Sehen, verminderten Tränenfluss, Vasodilatation und die Auswirkungen auf das zentrale Nervensystem an den Muscarinrezeptoren Typ 4 und 5 wider. Diese Reihe von Symptomen wird als anticholinerges Oxidrom bezeichnet und kann auch durch andere Arzneimittel mit anticholinerger Wirkung wie Hyoscinhydrobromid (Scopolamin), Diphenhydramin, Phenothiazin-Antipsychotika und Benztropin verursacht werden. ⓘ
Die Wirkungen auf Herz und Kreislauf stehen schon bei geringen Dosen im Vordergrund (z. B. zur Narkoseeinleitung). Psychische („berauschende“) Wirkungen sind erst bei hohen Dosen zu erwarten, bei denen unangenehme und gefährliche körperliche Nebenwirkungen auftreten. ⓘ
Neben Vergiftungen durch freiwilligen oder unfreiwilligen Verzehr von Pflanzenteilen (zum Beispiel Tollkirsche) kommen medizinale Vergiftungen infolge Überdosierung, Verwechslung oder falscher Anwendung vor. Z. B. hat die Food and Drug Administration (FDA) im Jahre 2016 Globuli im Zusammenhang mit zehn Todesfällen in den USA von Kleinkindern untersucht, die nach der Verabreichung dieses Mittels, das Atropin enthielt, starben. Das Atropin war offenbar in zu hoher Konzentration in den Globuli enthalten. Die Behörde wies die Hersteller an, die Tabletten zurückzurufen. ⓘ
Die Erste Hilfe bei Atropinvergiftung besteht in sofortiger Entleerung des Magen-Darm-Traktes (Erbrechen, Magenspülung) sowie erforderlichenfalls künstlicher Beatmung bzw. Atemspende. Die erweiterten Maßnahmen zielen auf die medikamentöse Hemmung der Acetylcholinesterase, durch Physostigmin als Antidot, wodurch der Abbau des Acetylcholins verzögert wird. Folglich erhöht sich die Konzentration im synaptischen Spalt. Am Rezeptor selbst wird somit indirekt eine parasympathische Wirkung erzielt. Das Atropin wird aus dem Bereich der Rezeptoren verdrängt und die Reizleitung ist wiederhergestellt. ⓘ
Atropin gehört zu den Parasympatholytika (auch Anticholinergika genannt). Atropin wirkt demnach antagonistisch und konkurriert somit an den muskarinischen Rezeptoren des Parasympathikus mit dem Neurotransmitter Acetylcholin. Atropin blockiert teilweise die Rezeptoren und hemmt somit den Parasympathikus. Die Wirkung des Acetylcholins sinkt. Der Einfluss des Parasympathikus sinkt, wodurch der Einfluss des Sympathikus überwiegt. ⓘ
Atropin hat folgende körperliche Wirkungen:
- Beschleunigung der Herzfrequenz (positive Chronotropie)
- Beschleunigung der Erregungsweiterleitung am Herz (positive Dromotropie)
- Weitstellung der Bronchien (Bronchodilatation)
- Weitstellung der Pupillen (= Mydriasis, vgl. Atropa belladonna, Schwarze Tollkirsche)
- stark verminderte Schweißbildung
- verminderte Speichelbildung
- Hemmung der Magen-Darm-Tätigkeit (verminderte Sekretion und Peristaltik)
- Erschlaffung der glatten Muskulatur (Spasmolyse)
- verminderte Sehfähigkeit, insbesondere in der Nähe (Hemmung der Akkommodation)
- starke Lichtempfindlichkeit (Photophobie)
- blockiert Rezeptoren der Nervenzellen (kein Erreichen der Rezeptoren durch Transmitter; Rezeptoren bleiben inaktiv) ⓘ
Kontraindikationen
Es ist generell kontraindiziert bei Menschen mit Glaukom, Pylorusstenose oder Prostatahypertrophie, außer in den für die Präanästhesie üblichen Dosen. ⓘ
Chemie
Atropin, ein Tropanalkaloid, ist ein enantiomeres Gemisch aus d-Hyoscyamin und l-Hyoscyamin, wobei die meisten physiologischen Wirkungen auf das l-Hyoscyamin zurückzuführen sind. Seine pharmakologischen Wirkungen sind auf die Bindung an muskarinische Acetylcholinrezeptoren zurückzuführen. Es ist ein Antimuskarinikum. Signifikante Konzentrationen werden im ZNS innerhalb von 30 Minuten bis 1 Stunde erreicht und verschwinden rasch aus dem Blut mit einer Halbwertszeit von 2 Stunden. Etwa 60% werden unverändert mit dem Urin ausgeschieden, der Rest erscheint im Urin als Hydrolyse- und Konjugationsprodukte. Noratropin (24 %), Atropin-N-oxid (15 %), Tropin (2 %) und Tropinsäure (3 %) scheinen die wichtigsten Metaboliten zu sein, während 50 % der verabreichten Dosis als offenbar unverändertes Atropin ausgeschieden werden. Es waren keine Konjugate nachweisbar. Es wurden Hinweise darauf gefunden, dass Atropin als (+)-Hyoscyamin vorliegt, was darauf hindeutet, dass wahrscheinlich ein stereoselektiver Metabolismus von Atropin stattfindet. Die Wirkungen auf die Iris und den Ziliarmuskel können länger als 72 Stunden anhalten. ⓘ
Die am häufigsten in der Medizin verwendete Atropinverbindung ist Atropinsulfat (Monohydrat) (C
17H
23NO
3)2-H2SO4-H2O, die vollständige chemische Bezeichnung lautet 1α H, 5α H-Tropan-3-α ol (±)-tropat(ester), Sulfatmonohydrat. ⓘ
Pharmakologie
Im Allgemeinen wirkt Atropin der "Ruhe- und Verdauungstätigkeit" von Drüsen entgegen, die vom parasympathischen Nervensystem gesteuert werden. Dies geschieht, weil Atropin ein kompetitiver, reversibler Antagonist der muskarinischen Acetylcholinrezeptoren ist (Acetylcholin ist der wichtigste Neurotransmitter des parasympathischen Nervensystems). ⓘ
Atropin ist ein kompetitiver Antagonist der muskarinischen Acetylcholinrezeptoren der Typen M1, M2, M3, M4 und M5. Es wird als Anticholinergikum (Parasympatholytikum) eingestuft. ⓘ
Im Herzbereich wirkt es als nichtselektiver muskarinischer Acetylcholin-Antagonist, der die Erregung des Sinusknotens (SA) und die Erregungsleitung durch den Atrioventrikularknoten (AV) des Herzens erhöht, den Aktionen des Vagusnervs entgegenwirkt, Acetylcholin-Rezeptoren blockiert und die Bronchialsekretion verringert. ⓘ
Im Auge bewirkt Atropin eine Mydriasis, indem es die Kontraktion des zirkulären Pupillenschließmuskels hemmt, der normalerweise durch die Freisetzung von Acetylcholin stimuliert wird, wodurch sich der radiale Irisdilatatormuskel zusammenziehen und die Pupille weiten kann. Atropin bewirkt eine Zykloplegie durch Lähmung der Ziliarmuskeln, deren Wirkung die Akkommodation hemmt, um eine genaue Refraktion bei Kindern zu ermöglichen, und hilft bei der Linderung von Schmerzen im Zusammenhang mit Iridozyklitis sowie bei der Behandlung des Ziliarblocks (malignes Glaukom). ⓘ
Die Vagusnerven (Parasympathikus), die das Herz innervieren, setzen Acetylcholin (ACh) als primären Neurotransmitter frei. ACh bindet an Muscarinrezeptoren (M2), die sich hauptsächlich auf Zellen befinden, die den sinoatrialen (SA) und atrioventrikulären (AV) Knoten bilden. Muscarinrezeptoren sind an die Gi-Untereinheit gekoppelt; daher führt eine vagale Aktivierung zu einer Verringerung von cAMP. Die Aktivierung des Gi-Proteins führt auch zur Aktivierung von KACh-Kanälen, die den Kalium-Efflux erhöhen und die Zellen hyperpolarisieren. ⓘ
Eine Zunahme der vagalen Aktivitäten am SA-Knoten verringert die Feuerungsrate der Schrittmacherzellen, indem die Steigung des Schrittmacherpotenzials (Phase 4 des Aktionspotenzials) verringert wird; dadurch sinkt die Herzfrequenz (negative Chronotropie). Die Veränderung der Steigung der Phase 4 resultiert aus Veränderungen der Kalium- und Kalziumströme sowie des langsam einwärts fließenden Natriumstroms, der vermutlich für den Schrittmacherstrom verantwortlich ist (If). Durch die Hyperpolarisierung der Zellen erhöht die vagale Aktivierung den Schwellenwert der Zelle für das Feuern, was zur Verringerung der Feuerrate beiträgt. Ähnliche elektrophysiologische Effekte treten auch am AV-Knoten auf; in diesem Gewebe äußern sich diese Veränderungen jedoch in einer Verringerung der Impulsleitungsgeschwindigkeit durch den AV-Knoten (negative Dromotropie). Im Ruhezustand besteht ein hoher vagaler Tonus am Herzen, der für die niedrigen Ruheherzfrequenzen verantwortlich ist. ⓘ
Auch der Vorhofmuskel wird in gewissem Umfang vagal innerviert, und in viel geringerem Maße auch der Kammermuskel. Eine Vagusaktivierung führt daher zu einer bescheidenen Verringerung der Vorhofkontraktilität (Inotropie) und einer noch geringeren Verringerung der Ventrikelkontraktilität. ⓘ
Muskarinrezeptor-Antagonisten binden an Muskarinrezeptoren und verhindern so, dass ACh an den Rezeptor bindet und ihn aktiviert. Indem sie die Wirkung von ACh blockieren, blockieren Muskarinrezeptorantagonisten sehr wirksam die Auswirkungen der vagalen Nervenaktivität auf das Herz. Auf diese Weise erhöhen sie die Herzfrequenz und die Erregungsleitung. ⓘ
Geschichte

Der Name Atropin wurde im 19. Jahrhundert geprägt, als erstmals reine Extrakte aus der Belladonna-Pflanze Atropa belladonna hergestellt wurden. Die medizinische Verwendung von Zubereitungen aus Pflanzen der Nachtschattengewächse ist jedoch viel älter. Mandragora (Alraune) wurde von Theophrastus im vierten Jahrhundert v. Chr. zur Behandlung von Wunden, Gicht und Schlaflosigkeit sowie als Liebestrank beschrieben. Im ersten Jahrhundert n. Chr. erkannte Dioskurides den Alraunenwein als Anästhetikum zur Behandlung von Schmerzen oder Schlaflosigkeit an, das vor Operationen oder Kauterisationen verabreicht werden sollte. Die Verwendung von Nachtschattenpräparaten zur Anästhesie, oft in Kombination mit Opium, setzte sich während des Römischen und Islamischen Reiches fort und wurde in Europa fortgesetzt, bis sie im 19. ⓘ
Atropinreiche Extrakte aus dem ägyptischen Bilsenkraut (einem weiteren Nachtschattengewächs) wurden von Kleopatra im letzten Jahrhundert v. Chr. verwendet, um die Pupillen ihrer Augen zu erweitern, in der Hoffnung, sie würde dadurch attraktiver erscheinen. Auch in der Renaissance verwendeten Frauen den Saft der Beeren der Tollkirsche (Atropa belladonna), um ihre Pupillen aus kosmetischen Gründen zu erweitern. Diese Praxis wurde im späten neunzehnten und frühen zwanzigsten Jahrhundert in Paris kurzzeitig wieder aufgenommen. ⓘ
Die pharmakologische Untersuchung von Belladonna-Extrakten wurde von dem deutschen Chemiker Friedlieb Ferdinand Runge (1795-1867) begonnen. Im Jahr 1831 gelang es dem deutschen Apotheker Heinrich F. G. Mein (1799-1864), eine reine kristalline Form des Wirkstoffs herzustellen, der den Namen Atropin erhielt.
Die Substanz wurde erstmals 1901 von dem deutschen Chemiker Richard Willstätter synthetisiert. ⓘ
Natürliche Quellen
Atropin kommt in vielen Nachtschattengewächsen (Solanaceae) vor. Die am häufigsten vorkommenden Quellen sind Atropa belladonna (Tollkirsche), Datura innoxia, D. wrightii, D. metel und D. stramonium. Andere Quellen sind Mitglieder der Gattungen Brugmansia (Engelstrompeten) und Hyoscyamus. ⓘ
Synthese
Atropin kann durch die Reaktion von Tropin mit Tropinsäure in Gegenwart von Salzsäure synthetisiert werden. ⓘ
Biosynthese
Bei der Biosynthese von Atropin wird ausgehend von L-Phenylalanin zunächst eine Transaminierung zu Phenylbrenztraubensäure durchgeführt, die dann zu Phenylmilchsäure reduziert wird. Coenzym A koppelt dann Phenylmilchsäure mit Tropin und bildet Littorin, das dann eine radikalische Umlagerung durchläuft, die durch ein P450-Enzym eingeleitet wird und Hyoscyamin-Aldehyd bildet. Eine Dehydrogenase reduziert dann den Aldehyd zu einem primären Alkohol, wodurch (-)-Hyoscyamin entsteht, das nach Racemisierung Atropin bildet. ⓘ
Name
Der Gattungsname "Belladonna" (italienisch für "schöne Frau") geht auf die ursprüngliche Verwendung der Tollkirsche zur Erweiterung der Pupillen der Augen zu kosmetischen Zwecken zurück. Sowohl Atropin als auch der Gattungsname der Tollkirsche leiten sich von Atropos ab, einem der drei Schicksale, die in der griechischen Mythologie über den Tod eines Menschen entschieden. ⓘ
Chemische Struktur
Das (S)-Hyoscyamin ist ein Ester der Tropasäure mit α-Tropin und zählt somit zu den Tropan-Alkaloiden. Atropin ist die racemisierte Form des natürlich vorkommenden (S)-Hyoscyamins. Allein das 1:1-Gemisch von (R)- und (S)-Hyoscyamin wird Atropin genannt (vgl. Cahn-Ingold-Prelog-Konvention zur Benennung). Die Racemisierung findet bereits bei der Isolierung statt, wenn Laugen zum Einsatz kommen; hierbei bildet sich intermediär ein Enolat. Durch eine Aufarbeitung unter neutralen Bedingungen (pH-Wert 7) kann die Racemisierung von (S)-Hyoscyamin unterdrückt werden. Der Bedeutung der Enantiomerenreinheit von Arzneistoffen wird zunehmend Beachtung geschenkt, denn die beiden Enantiomere eines chiralen Arzneistoffes zeigen fast immer eine unterschiedliche Pharmakodynamik und Pharmakokinetik. Dies wurde früher aus Unkenntnis über stereochemische Zusammenhänge oft ignoriert. Arzneimittel enthalten den Arzneistoff Atropin als Racemat (1:1-Gemisch der Enantiomere); aus grundsätzlichen Überlegungen wäre die Verwendung des besser bzw. nebenwirkungsärmer wirksamen Enantiomers zu bevorzugen. ⓘ
Ein dem Hyoscyamin strukturell nah verwandtes Alkaloid ist das Scopolamin (Hyoscin). ⓘ
Medizinische Verwendung
Kreislaufstillstand
Atropin wurde in der kardio-pulmonalen Reanimation bei Asystolie und pulsloser elektrischer Aktivität (PEA) eingesetzt, Dosen von 0,5 bis maximal 3 mg wurden intravenös verabreicht. Wegen mangelnder Evidenz ist die Gabe von Atropin bei einer Reanimation nach den Richtlinien des European Resuscitation Council nicht mehr empfohlen. ⓘ
Einsatz bei Bradykardien
Atropin wird in der Anästhesie, Intensiv- und Notfallmedizin bei der symptomatischen Behandlung einer zu niedrigen Herzfrequenz (Bradykardie) verwendet. Insbesondere durch den N. Vagus ausgelöste Bradykardien (z. B. Okulokardialer-Reflex, Bradykardie im Rahmen der Intubation, Bradykardien als Nebenwirkung anderer Medikamente) können mit Atropin therapiert werden. Häufig findet sich die Angabe einer Mindestdosis insbesondere bei der Therapie von Säuglingen und Kleinkindern, da es ansonsten zu paradoxen Bradykardien kommen könne. Diese Behauptung ist wissenschaftlich nicht begründet und wurde in einigen Studien sogar widerlegt und sollte nicht weiter verbreitet werden, da es aufgrund dieser Mindestdosis bereits bei Frühgeborenen zu gefährlichen Überdosierungen mit Atropin kam. ⓘ
Augenheilkunde
Atropin wird in der Augenheilkunde zur diagnostischen und therapeutischen Akkommodationslähmung eingesetzt. Als Mydriatikum wird Atropin aufgrund seiner langen Wirkdauer zur therapeutischen, jedoch nicht zur kurzzeitigen diagnostischen Erweiterung der Pupillen verwendet. ⓘ
Weite Pupillen galten besonders während der Renaissance bei Frauen als schön (ital. bella donna „schöne Frau“). Das Einträufeln der (S)-Hyoscyamin enthaltenden Tollkirschen-Extrakte in die Augen bewirkte eine bis zu mehreren Tagen anhaltende Pupillenerweiterung („feuriger Blick“). ⓘ
Außerdem zeigen durchgeführte Studien die Wirksamkeit von Atropin zur Bremsung einer fortschreitenden Kurzsichtigkeit im Kindesalter. ⓘ
Verwendung als Gegengift
Atropin hemmt die muscarinerge Wirkung des Acetylcholins durch kompetitive Inhibition der Acetylcholinrezeptoren an der postsynaptischen Membran und unterbricht die Signalübertragung in der Nervenleitung. In sehr hohen Dosen hemmt Atropin vermutlich auch einige Subtypen des nikotinischen Acetylcholinrezeptors. ⓘ
Auf Grund dieses Wirkungsmechanismus wird Atropin als Gegengift (Antidot) bei Vergiftungen mit bestimmten Pflanzenschutzmitteln (Insektiziden) und Nervenkampfstoffen eingesetzt, deren Giftwirkung auf einer irreversiblen Hemmung der Acetylcholinesterase beruht (z. B. organische Phosphorsäureester und Phosphonsäureester wie Parathion, Tabun oder Paraoxon). Patienten (z. B. mit Sarin kontaminierte Soldaten) werden per Autoinjektor Gaben von 2 mg Atropinsulfat bzw. 2 mg Atropinsulfat plus 220 mg Obidoximchlorid verabreicht. ⓘ
Prämedikation
Atropin hemmt vor allem die M1-, M2- und M3-Rezeptoren und verursacht so eine Steigerung der Herzfrequenz (M2), eine Reduktion der Magensäureproduktion (M1) sowie eine Speichelreduktion (M3). Zusammen mit einer dezenten Bronchodilatation (M3) sind diese Wirkungen auch von Vorteil für eine Narkoseeinleitung. Ein genereller Einsatz in der Prämedikation (medikamentöse Vorbereitung) von Narkosepatienten wird jedoch heute nicht mehr empfohlen, da das Nutzen-Nebenwirkungs-Verhältnis von Atropin-Sulfat schlecht ist. ⓘ
Handelsnamen
- Monopräparate: Bellafit (CH), Dysurgal (D), Generika (D, A, CH)
- in ehemaligen Kombinationspräparaten: Eucard (D) ⓘ