Edelgase
| Edelgase ⓘ | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||
| ↓ Zeitraum | |||||||||||
| 1 | Helium (He) 2 | ||||||||||
| 2 | Neon (Ne) 10 | ||||||||||
| 3 | Argon (Ar) 18 | ||||||||||
| 4 | Krypton (Kr) 36 | ||||||||||
| 5 | Xenon (Xe) 54 | ||||||||||
| 6 | Radon (Rn) 86 | ||||||||||
| 7 | Oganesson (Og) 118 | ||||||||||
|
Legende
| |||||||||||
Die Edelgase (historisch auch Inertgase; manchmal auch als Aerogene bezeichnet) bilden eine Klasse von chemischen Elementen mit ähnlichen Eigenschaften; unter Standardbedingungen sind sie alle geruchlose, farblose, einatomige Gase mit sehr geringer chemischer Reaktivität. Die sechs natürlich vorkommenden Edelgase sind Helium (He), Neon (Ne), Argon (Ar), Krypton (Kr), Xenon (Xe) und das radioaktive Radon (Rn). ⓘ
Oganesson (Og) ist ein synthetisch hergestelltes, hochradioaktives Element, von dem man annimmt, dass es ein weiteres Edelgas ist, oder dass es aufgrund relativistischer Effekte reaktiv ist. Unter anderem wegen der extrem kurzen Halbwertszeit von 0,7 ms seines einzigen bekannten Isotops ist seine Chemie noch nicht untersucht worden. ⓘ
In den ersten sechs Perioden des Periodensystems sind die Edelgase genau die Mitglieder der Gruppe 18. Edelgase sind in der Regel sehr reaktionsträge, es sei denn, sie werden unter besonders extremen Bedingungen eingesetzt. Aufgrund ihrer Reaktionsträgheit eignen sich Edelgase sehr gut für Anwendungen, bei denen Reaktionen nicht erwünscht sind. So wird beispielsweise Argon in Glühlampen verwendet, um zu verhindern, dass der heiße Wolframdraht oxidiert; außerdem wird Helium als Atemgas von Tiefseetauchern verwendet, um eine Vergiftung durch Sauerstoff, Stickstoff und Kohlendioxid zu verhindern. ⓘ
Die Eigenschaften der Edelgase lassen sich durch moderne Theorien der Atomstruktur gut erklären: Ihre äußere Schale mit Valenzelektronen gilt als "voll", so dass sie kaum an chemischen Reaktionen teilnehmen, und es konnten nur einige hundert Edelgasverbindungen hergestellt werden. Der Schmelz- und der Siedepunkt eines bestimmten Edelgases liegen nahe beieinander und unterscheiden sich um weniger als 10 °C (18 °F); das heißt, sie sind nur in einem kleinen Temperaturbereich flüssig. ⓘ
Neon, Argon, Krypton und Xenon werden aus Luft in einer Luftzerlegungsanlage durch Verflüssigung von Gasen und fraktionierte Destillation gewonnen. Helium wird aus Erdgasfeldern gewonnen, die hohe Heliumkonzentrationen im Erdgas aufweisen, wobei kryogene Gastrennungstechniken zum Einsatz kommen, und Radon wird in der Regel aus dem radioaktiven Zerfall von gelösten Radium-, Thorium- oder Uranverbindungen isoliert. Edelgase haben mehrere wichtige Anwendungen in der Industrie, z. B. in der Beleuchtung, beim Schweißen und in der Weltraumforschung. Ein Helium-Sauerstoff-Atemgas wird häufig von Tiefseetauchern in Meerwassertiefen über 55 m (180 ft) verwendet. Nachdem die Risiken der Entflammbarkeit von Wasserstoff bei der Hindenburg-Katastrophe deutlich geworden waren, wurde er in Luftschiffen und Ballons durch Helium ersetzt. ⓘ
|
Lage im Periodensystem ⓘ
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe | 18 ⓘ |
| Hauptgruppe | 8 |
| Periode | |
| 1 | 2 He |
| 2 | 10 Ne |
| 3 | 18 Ar |
| 4 | 36 Kr |
| 5 | 54 Xe |
| 6 | 86 Rn |
| 7 | 118 Og |
Das einheitliche Hauptmerkmal sämtlicher Edelgasatome ist, dass sie für die energetisch höchsten Atomorbitale die Elektronenkonfiguration s2 (Helium) bzw. s2p6 aufweisen (Edelgaskonfiguration). Es gibt nur vollständig gefüllte Atomorbitale, die dazu führen, dass Edelgase nur unter extremen Bedingungen chemische Reaktionen eingehen; sie bilden auch miteinander keine Moleküle, sondern sind einatomig und bei Raumtemperatur Gase. Dieser geringen Reaktivität verdanken sie ihren Gruppennamen, der sich an die ebenfalls nur wenig reaktiven Edelmetalle anlehnt. ⓘ
Helium ist das mit Abstand häufigste Edelgas. Auf der Erde kommt Argon am häufigsten vor; alle anderen zählen zu den seltenen Bestandteilen der Erde. Als Gase sind sie Bestandteile der Luft; in der Erdkruste findet man sie mit Ausnahme des Heliums, das in Erdgas enthalten ist, nur in sehr geringen Mengen. Entdeckt wurden sie – mit Ausnahme des erst 2006 hergestellten Oganessons – kurz nacheinander in den Jahren 1868 (Helium) bis 1900 (Radon). Die meisten Edelgase wurden erstmals vom britischen Chemiker William Ramsay isoliert. ⓘ
Verwendung finden Edelgase vor allem als Schutzgas, z. B. in Glühlampen, wichtig sind sie als Füllgas von Gasentladungslampen, in denen sie in der für jedes Gas charakteristischen Farbe leuchten. Trotz der geringen Reaktivität sind von den schwereren Edelgasen, insbesondere Xenon, chemische Verbindungen bekannt. Deren wichtigste ist das starke Oxidationsmittel Xenon(II)-fluorid. ⓘ
Geschichte
Die Bezeichnung Edelgas stammt aus dem Deutschen und wurde erstmals 1898 von Hugo Erdmann verwendet, um auf die extrem geringe Reaktivität der Gase hinzuweisen. Der Name ist eine Analogie zum Begriff "Edelmetalle", die ebenfalls eine geringe Reaktivität aufweisen. Die Edelgase wurden auch als Inertgase bezeichnet, aber diese Bezeichnung ist veraltet, da inzwischen viele Edelgasverbindungen bekannt sind. Auch die Bezeichnung "seltene Gase" wurde verwendet, ist aber ebenfalls ungenau, da Argon durch den Zerfall von radioaktivem Kalium-40 einen beträchtlichen Anteil (0,94 % des Volumens, 1,3 % der Masse) der Erdatmosphäre ausmacht. ⓘ
Pierre Janssen und Joseph Norman Lockyer hatten am 18. August 1868 bei der Beobachtung der Chromosphäre der Sonne ein neues Element entdeckt und es nach dem griechischen Wort für Sonne, ἥλιος (hḗlios), Helium genannt. Eine chemische Analyse war damals noch nicht möglich, aber später stellte sich heraus, dass Helium ein Edelgas ist. Vor ihnen, im Jahr 1784, hatte der englische Chemiker und Physiker Henry Cavendish entdeckt, dass Luft einen geringen Anteil einer Substanz enthält, die weniger reaktiv ist als Stickstoff. Ein Jahrhundert später, im Jahr 1895, entdeckte Lord Rayleigh, dass Stickstoffproben aus der Luft eine andere Dichte aufwiesen als Stickstoff aus chemischen Reaktionen. Zusammen mit dem schottischen Wissenschaftler William Ramsay am University College in London stellte Lord Rayleigh die Theorie auf, dass der aus der Luft gewonnene Stickstoff mit einem anderen Gas vermischt war, was zu einem Experiment führte, bei dem erfolgreich ein neues Element isoliert wurde, nämlich Argon, vom griechischen Wort ἀργός (argós, "müßig" oder "faul"). Mit dieser Entdeckung erkannten sie, dass eine ganze Klasse von Gasen im Periodensystem fehlte. Auf der Suche nach Argon gelang es Ramsay auch, beim Erhitzen von Cleveit, einem Mineral, erstmals Helium zu isolieren. Nachdem Dmitri Mendelejew 1902 den Nachweis der Elemente Helium und Argon akzeptiert hatte, nahm er diese Edelgase als Gruppe 0 in seine Anordnung der Elemente auf, aus der später das Periodensystem werden sollte. ⓘ
Ramsay setzte seine Suche nach diesen Gasen fort und nutzte die Methode der fraktionierten Destillation, um flüssige Luft in mehrere Komponenten zu trennen. Im Jahr 1898 entdeckte er die Elemente Krypton, Neon und Xenon und benannte sie nach den griechischen Wörtern κρυπτός (kryptós, "verborgen"), νέος (néos, "neu") bzw. ξένος (ksénos, "fremd"). Radon wurde erstmals 1898 von Friedrich Ernst Dorn identifiziert und als Radium-Emanation bezeichnet, wurde aber erst 1904 als Edelgas betrachtet, als festgestellt wurde, dass seine Eigenschaften denen anderer Edelgase ähneln. Rayleigh und Ramsay erhielten 1904 den Nobelpreis für Physik bzw. Chemie für ihre Entdeckung der Edelgase. In den Worten von J. E. Cederblom, dem damaligen Präsidenten der Königlich Schwedischen Akademie der Wissenschaften, "ist die Entdeckung einer völlig neuen Gruppe von Elementen, von denen kein einziger Vertreter mit Sicherheit bekannt war, etwas völlig Einzigartiges in der Geschichte der Chemie und an sich ein Fortschritt in der Wissenschaft von besonderer Bedeutung". ⓘ
Die Entdeckung der Edelgase trug zur Entwicklung eines allgemeinen Verständnisses der atomaren Struktur bei. Im Jahr 1895 versuchte der französische Chemiker Henri Moissan, eine Reaktion zwischen Fluor, dem elektronegativsten Element, und Argon, einem der Edelgase, herzustellen, was jedoch misslang. Bis zum Ende des 20. Jahrhunderts gelang es den Wissenschaftlern nicht, Argonverbindungen herzustellen, aber diese Versuche trugen zur Entwicklung neuer Theorien über die atomare Struktur bei. Auf der Grundlage dieser Experimente schlug der dänische Physiker Niels Bohr 1913 vor, dass die Elektronen in den Atomen in Schalen angeordnet sind, die den Kern umgeben, und dass bei allen Edelgasen außer Helium die äußerste Schale immer acht Elektronen enthält. Im Jahr 1916 formulierte Gilbert N. Lewis die Oktett-Regel, die besagt, dass ein Oktett von Elektronen in der äußeren Schale die stabilste Anordnung für jedes Atom ist; diese Anordnung bewirkt, dass sie mit anderen Elementen nicht reagieren, da sie keine weiteren Elektronen benötigen, um ihre äußere Schale zu vervollständigen. ⓘ
Im Jahr 1962 entdeckte Neil Bartlett die erste chemische Verbindung eines Edelgases, Xenonhexafluoroplatinat. Bald darauf wurden Verbindungen anderer Edelgase entdeckt: 1962 für Radon das Radondifluorid (RnF
2), das mit Hilfe von Radiotracer-Techniken identifiziert wurde, und 1963 für Krypton, Kryptondifluorid (KrF
2). Die erste stabile Argonverbindung wurde im Jahr 2000 gemeldet, als Argonfluorhydrid (HArF) bei einer Temperatur von 40 K (-233,2 °C; -387,7 °F) gebildet wurde. ⓘ
Im Oktober 2006 gelang es Wissenschaftlern des Joint Institute for Nuclear Research und des Lawrence Livermore National Laboratory, Oganesson, das siebte Element der Gruppe 18, synthetisch herzustellen, indem sie Kalifornium mit Kalzium beschossen. ⓘ

Nachdem die wichtigsten Eigenschaften von Helium und Argon bestimmt worden waren, konnte festgestellt werden, dass diese Gase im Gegensatz zu den anderen atmosphärischen Gasen einatomig sind. Dies wurde dadurch erkannt, dass das Verhältnis der molaren Wärmekapazität Cp bei konstantem Druck im Verhältnis zur Wärmekapazität CV bei konstantem Volumen bei Edelgasen einen sehr hohen Wert von 1,67 (= Cp/CV) aufweist, während zwei- und mehratomige Gase deutlich kleinere Werte aufweisen. Daraufhin vermutete William Ramsay, dass es eine ganze Gruppe derartiger Gase geben müsse, die eine eigene Gruppe im Periodensystem bilden und er begann nach diesen zu suchen. 1898 gelang es ihm und Morris William Travers, durch fraktionierte Destillation von Luft, Neon, Krypton und Xenon zu isolieren. ⓘ
Als letztes der natürlich vorkommenden Edelgase wurde 1900 von Friedrich Ernst Dorn als Radium-Emanation (Ausdünstung von Radium) das Radon entdeckt und mit dem Symbol Em bezeichnet. Dabei handelte es sich um das Isotop 222Rn. Weitere Radon-Isotope wurden von Ernest Rutherford und André-Louis Debierne gefunden und zunächst für eigene Elemente gehalten. Erst nachdem William Ramsay 1910 das Spektrum und weitere Eigenschaften bestimmte, erkannte er, dass es sich um ein einziges Element handelt. Er nannte dies zunächst Niton (Nt), seit 1934 wird der Name Radon verwendet. Oganesson, das letzte Element der Gruppe, konnte nach mehreren nicht erfolgreichen Versuchen erstmals 2002–2005 am Vereinigten Institut für Kernforschung in Dubna erzeugt werden. ⓘ
Es wurden schon bald nach der Entdeckung Versuche unternommen, Verbindungen der Edelgase zu synthetisieren. 1894 versuchte Henri Moissan, eine Reaktion von Argon mit Fluor zu erreichen, scheiterte jedoch. Im Jahr 1924 behauptete A. von Antropoff, eine erste Kryptonverbindung in Form eines roten stabilen Feststoffes aus Krypton und Chlor synthetisiert zu haben. Später stellte sich jedoch heraus, dass in dieser Verbindung kein Krypton, sondern Stickstoffmonoxid und Chlorwasserstoff enthalten waren. ⓘ
Vorkommen und Herstellung
Die Häufigkeit der Edelgase im Universum nimmt mit steigender Ordnungszahl ab. Helium ist nach Wasserstoff das häufigste Element im Universum, mit einem Massenanteil von etwa 24 %. Der größte Teil des Heliums im Universum entstand während der Nukleosynthese des Urknalls, aber die Menge an Helium nimmt durch die Fusion von Wasserstoff in der stellaren Nukleosynthese (und, in sehr geringem Maße, durch den Alphazerfall schwerer Elemente) stetig zu. Die Häufigkeiten auf der Erde folgen anderen Trends; so ist Helium beispielsweise nur das dritthäufigste Edelgas in der Atmosphäre. Der Grund dafür ist, dass es in der Atmosphäre kein primordiales Helium gibt; aufgrund der geringen Masse des Atoms kann Helium nicht vom Gravitationsfeld der Erde zurückgehalten werden. Das Helium auf der Erde stammt aus dem Alphazerfall schwerer Elemente wie Uran und Thorium, die in der Erdkruste vorkommen, und sammelt sich in der Regel in Erdgaslagerstätten an. Die Häufigkeit von Argon hingegen wird durch den Betazerfall von Kalium-40 erhöht, das ebenfalls in der Erdkruste vorkommt. Dabei entsteht Argon-40, das auf der Erde am häufigsten vorkommende Isotop von Argon, obwohl es im Sonnensystem relativ selten ist. Dieser Prozess ist die Grundlage für die Kalium-Argon-Datierungsmethode. Xenon kommt in der Atmosphäre unerwartet wenig vor, was als Problem des fehlenden Xenons bezeichnet wird; eine Theorie besagt, dass das fehlende Xenon in Mineralien in der Erdkruste eingeschlossen sein könnte. Nach der Entdeckung von Xenon-Dioxid haben Forschungen gezeigt, dass Xe Si in Quarz ersetzen kann. Radon wird in der Lithosphäre durch den Alphazerfall von Radium gebildet. Es kann durch Risse im Fundament in Gebäude eindringen und sich in schlecht belüfteten Räumen ansammeln. Aufgrund seiner hohen Radioaktivität stellt Radon ein erhebliches Gesundheitsrisiko dar; es wird allein in den Vereinigten Staaten für schätzungsweise 21.000 Todesfälle durch Lungenkrebs pro Jahr verantwortlich gemacht. Oganesson kommt in der Natur nicht vor und wird stattdessen von Wissenschaftlern manuell erzeugt. ⓘ
| Abundanz | Helium | Neon | Argon | Krypton | Xenon | Radon ⓘ |
|---|---|---|---|---|---|---|
| Sonnensystem (für jedes Siliziumatom) | 2343 | 2.148 | 0.1025 | 5.515 × 10−5 | 5.391 × 10−6 | – |
| Erdatmosphäre (Volumenanteil in ppm) | 5.20 | 18.20 | 9340.00 | 1.10 | 0.09 | (0.06–18) × 10−19 |
| Igneous rock (Massenanteil in ppm) | 3 × 10−3 | 7 × 10−5 | 4 × 10−2 | – | – | 1.7 × 10−10 |
| Gas | Preis 2004 (USD/m3) |
|---|---|
| Helium (Industriequalität) | 4.20–4.90 |
| Helium (Laborqualität) | 22.30–44.90 |
| Argon | 2.70–8.50 |
| Neon | 60–120 |
| Krypton | 400–500 |
| Xenon | 4000–5000 |
Für die großtechnische Verwendung wird Helium durch fraktionierte Destillation aus Erdgas gewonnen, das bis zu 7 % Helium enthalten kann. ⓘ
Neon, Argon, Krypton und Xenon werden aus Luft durch Verflüssigung von Gasen und durch fraktionierte Destillation, bei der Gemische in ihre Bestandteile getrennt werden, gewonnen. Helium wird in der Regel durch Abtrennung aus Erdgas gewonnen, und Radon wird durch den radioaktiven Zerfall von Radiumverbindungen isoliert. Die Preise der Edelgase hängen von ihrem natürlichen Vorkommen ab, wobei Argon am billigsten und Xenon am teuersten ist. In der nebenstehenden Tabelle sind als Beispiel die Preise für Labormengen der einzelnen Gase in den Vereinigten Staaten für das Jahr 2004 aufgeführt. ⓘ
Edelgase finden sich vorwiegend in der Erdatmosphäre, in geringem Maße aber auch in der Erdkruste; ihre Häufigkeiten sind jedoch sehr unterschiedlich. Das mit Abstand häufigste ist Argon, das mit einem Volumenanteil von 0,934 % (9340 ppm) einen nennenswerten Anteil der gesamten Atmosphäre ausmacht. Alle anderen sind mit Anteilen unter 20 ppm sehr viel seltener, sie zählen daher zu den Spurengasen. Krypton, Xenon und Radon zählen zu den seltensten Elementen auf der Erde überhaupt. Helium ist außerdem Bestandteil von Erdgas, an dem es einen Anteil von bis zu 16 % am Volumen haben kann. ⓘ
Gewinnung
Mit Ausnahme eines Großteils des Heliums und der radioaktiven Elemente erfolgt die Gewinnung der Edelgase ausschließlich aus der Luft. Sie fallen als Nebenprodukte bei der Gewinnung von Stickstoff und Sauerstoff im Linde-Verfahren an. In der Haupt-Rektifikationskolonne, in der Sauerstoff und Stickstoff getrennt werden, reichern sich die verschiedenen Edelgase an unterschiedlichen Stellen an. Sie können aber in eine eigene Kolonne überführt und dort von allen anderen Gasen getrennt werden. Während Argon leicht abgetrennt werden kann und nur von Stickstoff und Sauerstoff befreit werden muss, besteht bei Helium und Neon, aber auch bei Krypton und Xenon das Problem, dass diese sich zunächst zusammen anreichern und anschließend getrennt werden müssen. Dies kann über eine weitere Rektifikationskolonne oder auch durch unterschiedliche Adsorption der Gase an geeigneten Adsorptionsmedien erfolgen. ⓘ
Helium wird zumindest seit 1980 überwiegend aus Erdgas gewonnen. Diese Heliumquelle wurde zuerst in den Vereinigten Staaten entdeckt, später auch in der Sowjetunion genutzt, heute in wenigen weiteren Ländern und Werken, so etwa in Algerien, dessen Ausbeute tiefkalt verflüssigt im 40-Fuß-Container nach Marseille und damit Europa verschifft wird. Von den anderen Bestandteilen des Erdgases kann es als Rohhelium entweder durch Ausfrieren aller anderen Gase oder durch Permeation an geeigneten Membranen getrennt werden. Anschließend muss das Helium noch durch Druckwechsel-Adsorption, chemische oder kryotechnische Verfahren von restlichen störenden Gasen wie Stickstoff oder Wasserstoff befreit werden. ⓘ
Radon lässt sich auf Grund der kurzen Halbwertszeit nicht in größeren Mengen gewinnen. In kleinerem Maßstab dient Radium als Quelle, Radon entsteht beim Zerfall dieses Elements und gast aus einem entsprechenden Präparat aus. Oganesson konnte als künstliches Element in wenigen Atomen durch Beschuss von Californium mit Calcium-Atomen erzeugt werden. ⓘ
Eigenschaften
| Eigenschaft | Helium | Neon | Argon | Krypton | Xenon | Radon | Oganesson ⓘ |
|---|---|---|---|---|---|---|---|
| Dichte (g/dm3) | 0.1786 | 0.9002 | 1.7818 | 3.708 | 5.851 | 9.97 | 7200 (vorhergesagt) |
| Siedepunkt (K) | 4.4 | 27.3 | 87.4 | 121.5 | 166.6 | 211.5 | 450±10 (vorhergesagt) |
| Schmelzpunkt (K) | – | 24.7 | 83.6 | 115.8 | 161.7 | 202.2 | 325±15 (vorhergesagt) |
| Verdampfungsenthalpie (kJ/mol) | 0.08 | 1.74 | 6.52 | 9.05 | 12.65 | 18.1 | – |
| Löslichkeit in Wasser bei 20 °C (cm3/kg) | 8.61 | 10.5 | 33.6 | 59.4 | 108.1 | 230 | – |
| Ordnungszahl | 2 | 10 | 18 | 36 | 54 | 86 | 118 |
| Atomradius (berechnet) (pm) | 31 | 38 | 71 | 88 | 108 | 120 | – |
| Ionisierungsenergie (kJ/mol) | 2372 | 2080 | 1520 | 1351 | 1170 | 1037 | 839 (vorhergesagt) |
| Elektronegativität | 4.16 | 4.79 | 3.24 | 2.97 | 2.58 | 2.60 | – |
Die Edelgase haben eine schwache interatomare Kraft und folglich sehr niedrige Schmelz- und Siedepunkte. Unter Standardbedingungen sind sie alle einatomige Gase, einschließlich der Elemente mit größeren Atommassen als viele normalerweise feste Elemente. Helium hat im Vergleich zu anderen Elementen mehrere einzigartige Eigenschaften: Sein Siedepunkt bei 1 atm ist niedriger als der jedes anderen bekannten Stoffes; es ist das einzige bekannte Element, das Suprafluidität aufweist; und es ist das einzige Element, das bei Atmosphärendruck nicht durch Abkühlung verfestigt werden kann (ein Effekt, der durch die Quantenmechanik erklärt wird, da seine Nullpunktenergie zu hoch ist, um ein Einfrieren zu ermöglichen) - ein Druck von 25 Standardatmosphären (2.500 kPa; 370 psi) muss bei einer Temperatur von 0. 95 K (-272.200 °C; -457.960 °F) ein Druck von 25 Standardatmosphären (2.500 kPa; 370 psi) aufgebracht werden, um es in einen Festkörper zu verwandeln, während bei Raumtemperatur ein Druck von etwa 115 kbar erforderlich ist. Die Edelgase bis hin zu Xenon haben mehrere stabile Isotope. Radon hat keine stabilen Isotope; sein langlebigstes Isotop, 222Rn, hat eine Halbwertszeit von 3,8 Tagen und zerfällt zu Helium und Polonium, das schließlich zu Blei zerfällt. Die Schmelz- und Siedepunkte steigen in der Gruppe nach unten hin an. ⓘ

Die Edelgasatome nehmen, wie die Atome der meisten Gruppen, von einer Periode zur nächsten aufgrund der zunehmenden Anzahl von Elektronen stetig an Atomradius zu. Die Größe des Atoms hängt mit mehreren Eigenschaften zusammen. So nimmt beispielsweise das Ionisierungspotenzial mit zunehmendem Radius ab, weil die Valenzelektronen in den größeren Edelgasen weiter vom Kern entfernt sind und daher nicht so fest vom Atom zusammengehalten werden. Edelgase haben das größte Ionisierungspotenzial unter den Elementen jeder Periode, was die Stabilität ihrer Elektronenkonfiguration widerspiegelt und mit ihrer relativ geringen chemischen Reaktivität zusammenhängt. Einige der schwereren Edelgase haben jedoch so geringe Ionisierungspotenziale, dass sie mit denen anderer Elemente und Moleküle vergleichbar sind. Die Erkenntnis, dass Xenon ein ähnliches Ionisierungspotenzial wie ein Sauerstoffmolekül hat, veranlasste Bartlett zu dem Versuch, Xenon mit Platinhexafluorid zu oxidieren, einem Oxidationsmittel, das bekanntermaßen stark genug ist, um mit Sauerstoff zu reagieren. Edelgase können kein Elektron aufnehmen, um stabile Anionen zu bilden, d. h. sie haben eine negative Elektronenaffinität. ⓘ
Die makroskopischen physikalischen Eigenschaften der Edelgase werden von den schwachen van-der-Waals-Kräften zwischen den Atomen bestimmt. Die Anziehungskraft nimmt mit der Größe des Atoms zu, was auf die Zunahme der Polarisierbarkeit und die Abnahme des Ionisierungspotenzials zurückzuführen ist. Daraus ergeben sich systematische Gruppentrends: Je weiter man in der Gruppe 18 nach unten geht, desto größer wird der Atomradius und damit die zwischenatomaren Kräfte, was zu einem Anstieg von Schmelzpunkt, Siedepunkt, Verdampfungsenthalpie und Löslichkeit führt. Die Zunahme der Dichte ist auf die Zunahme der Atommasse zurückzuführen. ⓘ
Die Edelgase sind unter Standardbedingungen nahezu ideale Gase, aber ihre Abweichungen vom idealen Gasgesetz lieferten wichtige Hinweise für die Untersuchung der zwischenmolekularen Wechselwirkungen. Das Lennard-Jones-Potenzial, das häufig zur Modellierung intermolekularer Wechselwirkungen verwendet wird, wurde 1924 von John Lennard-Jones aus experimentellen Daten über Argon abgeleitet, bevor die Entwicklung der Quantenmechanik die Instrumente zum Verständnis intermolekularer Kräfte nach den ersten Prinzipien lieferte. Die theoretische Analyse dieser Wechselwirkungen wurde möglich, weil die Edelgase einatomig und die Atome kugelförmig sind, was bedeutet, dass die Wechselwirkung zwischen den Atomen richtungsunabhängig bzw. isotrop ist. ⓘ

Physikalische Eigenschaften
Alle Edelgase sind unter Normalbedingungen einatomige, farb- und geruchlose Gase. Sie kondensieren und erstarren erst bei sehr niedrigen Temperaturen, wobei die Schmelz- und Siedepunkte umso höher liegen, je größer die Atommasse ist. Der Siedepunkt des Heliums liegt mit 4,224 K (−268,926 °C) nur knapp über dem absoluten Nullpunkt, das schwerste Edelgas Radon siedet bei 211,9 K (−61,25 °C). ⓘ
Helium besitzt die Besonderheit, dass es als einziges Element unter Atmosphärendruck und auch deutlich darüber nicht erstarrt. Stattdessen geht es bei 2,17 K in einen speziellen Aggregatzustand, die Suprafluidität, über. In diesem verliert die Flüssigkeit die innere Reibung und kann so beispielsweise über höhere Gefäßwände kriechen (Onnes-Effekt). Erst bei Drücken über 25,316 bar erstarrt Helium bei 0,775 K. Diese Temperaturen und Drücke gelten nur für das häufige Isotop 4He, das seltene zweite, leichtere stabile Isotop 3He hat dagegen deutlich andere Eigenschaften. Es wird erst bei Temperaturen unter 2,6 · 10−3 K suprafluid. Auch Schmelz-, Siede- und kritischer Punkt liegen bei anderen Temperaturen und Drücken. ⓘ
Mit Ausnahme des Heliums, das im hexagonalen Kristallsystem kristallisiert, besitzen alle Edelgase eine kubisch-flächenzentrierte Kristallstruktur. Wie durch die steigenden Atomradien zu erwarten, wird der Gitterparameter a von Neon zu Radon immer größer. ⓘ
Auch die Dichten der Edelgase korrelieren wie zu erwarten mit der Atommasse. Helium ist nach Wasserstoff das Gas mit der geringsten Dichte. Als einziges weiteres Edelgas hat Neon eine geringere Dichte als Luft, während Argon, Krypton, Xenon und Radon dichter sind. Radon ist mit einer Dichte von 9,73 kg/m3 eines der dichtesten Gase überhaupt. ⓘ
| Element | Helium (3He und 4He) | Neon | Argon | Krypton | Xenon | Radon ⓘ | |
|---|---|---|---|---|---|---|---|
| Farbe Gasentladung |  |
 |
 |
 |
 |
Rot | |
| Schmelzpunkt (1013 hPa) | 0,319 K (−272,831 °C) (29,315 bar) |
0,775 K (−272,375 °C) (25,316 bar) |
24,57 K (−248,58 °C) |
84,0 K (−189,2 °C) |
116,2 K (−157,0 °C) |
161,4 K (−111,8 °C) |
ca. 202 K (ca. −71 °C) |
| Siedepunkt (1013 hPa) | 3,1905 K (−269,9595 °C) |
4,224 K (−268,926 °C) |
27,09 K (−246,06 °C) |
87,295 K (−185,855 °C) |
119,79 K (−153,36 °C) |
165,03 K (−108,12 °C) |
211,9 K (−61,3 °C) |
| Kritischer Punkt |
|
|
|
|
|
|
|
| Tripelpunkt | nicht vorhanden |
|
|
|
|
| |
| Dichte (0 °C, 1013 hPa) | 0,13448 kg/m3 | 0,17847 kg/m3 | 0,9000 kg/m3 | 1,7839 kg/m3 | 3,7493 kg/m3 | 5,8971 kg/m3 | 9,73 kg/m3 |
| Struktur |  |
 |
 |
 |
 |

| |
| Kristallsystem | hexagonal | kubisch | kubisch | kubisch | kubisch | kubisch | |
| Gitterparameter |
|
a = 4,43 Å |
a = 5,26 Å |
a = 5,72 Å |
a = 6,20 Å |
a = 6,55 Å (berechnet) | |
Die Eigenschaften von Oganesson sind auf Grund der kurzen Halbwertszeit nicht experimentell ermittelbar. Nach theoretischen Überlegungen ist durch relativistische Effekte und die hohe Polarisierbarkeit des Oganesson-Atoms anzunehmen, dass Oganesson deutlich reaktiver ist als Radon. Auch ist es unwahrscheinlich, dass es bei Standardbedingungen gasförmig ist, durch Extrapolation kann ein Siedepunkt zwischen 320 und 380 K angenommen werden. ⓘ
- Edelgase in Gasentladungslampen
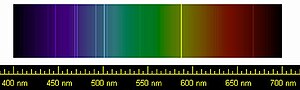
Xenon ⓘ
Atomare Eigenschaften

Bei Edelgasen sind alle Elektronenschalen entweder vollständig mit Elektronen besetzt oder leer. Deshalb wird dieser Zustand auch Edelgaskonfiguration genannt. Helium ist dabei das einzige Edelgas, bei dem lediglich ein s-Orbital vollständig besetzt ist (da es kein 1p-Orbital gibt), bei allen anderen ist das äußerste besetzte Orbital ein p-Orbital. Nach den Gesetzen der Quantenmechanik ist dieser Zustand der Orbitale energetisch besonders günstig. Darum tendieren auch Atome anderer Elemente dazu, Edelgaskonfiguration zu erreichen, indem sie Elektronen abgeben oder aufnehmen (Edelgasregel). ⓘ
Die Eigenschaften der Edelgase sind deutlich davon bestimmt, dass sie Edelgaskonfiguration nicht durch Abgabe oder Aufnahme von Elektronen, sondern bereits im neutralen, nicht-ionisierten Zustand erreichen. Edelgase liegen daher einatomig vor, besitzen eine hohe Ionisierungsenergie und reagieren fast nicht mit anderen Elementen oder Verbindungen. ⓘ
Chemische Eigenschaften
Trotz des Aufbaus der Edelgasatome sind die schweren Edelgase nicht völlig unreaktiv und können einige Verbindungen bilden. Verantwortlich hierfür sind der größere Abstand der Valenzelektronen vom Kern, wodurch die Ionisierungsenergie sinkt, sowie relativistische Effekte. Die größte Vielfalt an Verbindungen ist vom Xenon und nicht wie zu erwarten vom Radon bekannt, da bei diesem die starke Radioaktivität und kurze Halbwertszeit die Bildung von Verbindungen und deren Untersuchung erschwert. ⓘ
Das einzige Element, das in der Lage ist, direkt mit Xenon, Radon und unter bestimmten Bedingungen auch Krypton zu reagieren, ist Fluor. Während das bei der Reaktion von Krypton und Fluor gebildete Krypton(II)-fluorid thermodynamisch instabil und daher nur bei tiefen Temperaturen synthetisierbar ist, sind die Xenon- und auch Radonfluoride auch bei Raumtemperatur stabil. Andere Elemente reagieren nicht mit Edelgasen, dennoch sind verschiedene weitere Verbindungen bekannt, die durch Reaktionen der Fluoride zugänglich sind. ⓘ
Die Reaktivität und Stabilität von Verbindungen der leichten Edelgase Helium, Neon und Argon konnte mit Ausnahme einer bekannten Argonverbindung, HArF, nur theoretisch untersucht werden. Demnach gilt Neon als das am wenigsten reaktive Edelgas. So zeigte sich in Rechnungen, dass das Neonanalogon der einzigen in der Theorie stabilen Heliumverbindung HHeF nicht stabil sein sollte. ⓘ
Aufgrund des Fehlens chemischer Verbindungen der Edelgase gab es lange Zeit auch keine Zahlenwerte ihrer Elektronegativitäten – bestimmt werden konnten davon bis jetzt nur die Werte der Pauling-Skala für die beiden Elemente Xenon (2,6) und Krypton (3,0), die damit in etwa denen der Halogene entsprechen. In den neueren Elektronegativitätsskalen nach Mulliken, Allred und Rochow dagegen lassen sich auch Zahlenwerte für die übrigen Edelgase berechnen, die in diesem Fall über die der Halogene hinausreichen. Bei Helium betragen sie beispielsweise 5,50 nach Allred-Rochow und 4,86 nach Mullikan. ⓘ
Anwendungen

Edelgase haben sehr niedrige Siede- und Schmelzpunkte, was sie zu nützlichen Tiefkühlmitteln macht. Insbesondere flüssiges Helium, das bei 4,2 K (-268,95 °C; -452,11 °F) siedet, wird für supraleitende Magnete verwendet, wie sie in der Kernspintomographie und der magnetischen Kernresonanz benötigt werden. Flüssiges Neon erreicht zwar nicht so tiefe Temperaturen wie flüssiges Helium, wird aber ebenfalls in der Kryotechnik verwendet, da es eine über 40-mal höhere Kühlkapazität als flüssiges Helium und eine über dreimal höhere als flüssiger Wasserstoff hat. ⓘ
Helium wird als Bestandteil von Atemgasen verwendet, um Stickstoff zu ersetzen, da es in Flüssigkeiten, insbesondere in Fetten, schwer löslich ist. Gase werden vom Blut und Körpergewebe absorbiert, wenn sie unter Druck stehen, wie beim Tauchen, was eine narkotisierende Wirkung verursacht, die als Stickstoffnarkose bekannt ist. Aufgrund seiner geringeren Löslichkeit wird nur wenig Helium in die Zellmembranen aufgenommen, und wenn Helium als Ersatz für einen Teil der Atemgasmischungen verwendet wird, wie z. B. in Trimix oder Heliox, wird eine Verringerung der narkotischen Wirkung des Gases in der Tiefe erreicht. Die geringere Löslichkeit von Helium bietet weitere Vorteile bei der so genannten Dekompressionskrankheit oder der Taucherkrankheit. Die geringere Menge an gelöstem Gas im Körper bedeutet, dass sich beim Druckabfall während des Aufstiegs weniger Gasblasen bilden. Ein weiteres Edelgas, Argon, gilt als beste Option für die Verwendung als Füllgas für Trockenanzüge beim Tauchen. Helium wird auch als Füllgas in Kernbrennstäben für Kernreaktoren verwendet. ⓘ

Seit der Hindenburg-Katastrophe im Jahr 1937 hat Helium aufgrund seiner Leichtigkeit und Unbrennbarkeit Wasserstoff als Auftriebsgas in Luftschiffen und Ballons ersetzt, obwohl es den Auftrieb um 8,6 % verringert. ⓘ
In vielen Anwendungen werden die Edelgase verwendet, um eine inerte Atmosphäre zu schaffen. Argon wird bei der Synthese von luftempfindlichen Verbindungen verwendet, die empfindlich auf Stickstoff reagieren. Festes Argon wird auch für die Untersuchung sehr instabiler Verbindungen, wie z. B. reaktiver Zwischenprodukte, verwendet, indem diese bei sehr niedrigen Temperaturen in einer inerten Matrix eingeschlossen werden. Helium wird als Trägermedium in der Gaschromatographie, als Füllgas für Thermometer und in Geräten zur Strahlungsmessung, wie dem Geigerzähler und der Blasenkammer, verwendet. Helium und Argon werden häufig verwendet, um Schweißbögen und das umgebende Grundmetall beim Schweißen und Schneiden von der Atmosphäre abzuschirmen, aber auch bei anderen metallurgischen Prozessen und bei der Herstellung von Silizium für die Halbleiterindustrie. ⓘ
Edelgase werden wegen ihrer fehlenden chemischen Reaktivität häufig in der Beleuchtung eingesetzt. Argon, gemischt mit Stickstoff, wird als Füllgas für Glühbirnen verwendet. Krypton wird in Hochleistungsglühbirnen verwendet, die höhere Farbtemperaturen und einen höheren Wirkungsgrad haben, da es die Verdampfungsrate des Glühfadens stärker reduziert als Argon; insbesondere bei Halogenlampen wird Krypton in Verbindung mit geringen Mengen von Jod- oder Bromverbindungen verwendet. Die Edelgase leuchten in unverwechselbaren Farben, wenn sie in Gasentladungslampen, z. B. "Neonlampen", verwendet werden. Diese Lampen sind nach Neon benannt, enthalten aber oft auch andere Gase und Leuchtstoffe, die der orange-roten Farbe des Neons verschiedene Nuancen hinzufügen. Xenon wird häufig in Xenon-Bogenlampen verwendet, die aufgrund ihres nahezu kontinuierlichen Spektrums, das dem Tageslicht ähnelt, in Filmprojektoren und Autoscheinwerfern zum Einsatz kommen. ⓘ
Die Edelgase werden in Excimer-Lasern verwendet, die auf kurzlebigen, elektronisch angeregten Molekülen, so genannten Excimern, basieren. Bei den für die Laser verwendeten Excimern kann es sich um Edelgasdimere wie Ar2, Kr2 oder Xe2 handeln. Häufiger wird das Edelgas mit einem Halogen in Excimern wie ArF, KrF, XeF oder XeCl kombiniert. Diese Laser erzeugen ultraviolettes Licht, das aufgrund seiner kurzen Wellenlänge (193 nm für ArF und 248 nm für KrF) eine hochpräzise Bildgebung ermöglicht. Excimerlaser haben viele industrielle, medizinische und wissenschaftliche Anwendungen. Sie werden für die Mikrolithografie und Mikrofabrikation eingesetzt, die für die Herstellung integrierter Schaltkreise unerlässlich sind, sowie für die Laserchirurgie, einschließlich Laserangioplastie und Augenchirurgie. ⓘ
Einige Edelgase finden direkte Anwendung in der Medizin. Helium wird manchmal verwendet, um Asthmatikern das Atmen zu erleichtern. Xenon wird als Narkosemittel verwendet, weil es sich gut in Lipiden löst und dadurch wirksamer ist als das übliche Distickstoffmonoxid und weil es leicht vom Körper ausgeschieden wird, was zu einer schnelleren Erholung führt. Xenon findet Anwendung in der medizinischen Bildgebung der Lunge durch hyperpolarisierte MRT. Radon, das hochradioaktiv ist und nur in geringen Mengen zur Verfügung steht, wird in der Strahlentherapie eingesetzt. ⓘ
Edelgase, insbesondere Xenon, werden aufgrund ihrer Trägheit vor allem in Ionentriebwerken verwendet. Da Ionentriebwerke nicht durch chemische Reaktionen angetrieben werden, sind chemisch inerte Brennstoffe erwünscht, um unerwünschte Reaktionen zwischen dem Brennstoff und anderen Teilen des Triebwerks zu vermeiden. ⓘ
Oganesson ist zu instabil, um damit zu arbeiten, und hat außer in der Forschung keine bekannte Anwendung. ⓘ

Edelgase werden auf Grund ihrer geringen Reaktivität, der niedrigen Schmelzpunkte und der charakteristischen Farben bei Gasentladungen genutzt. Vor allem Argon und Helium werden in größerem Maßstab verwendet, die anderen Edelgase können nur in geringeren Mengen produziert werden und sind daher teuer. Die geringe Reaktivität wird in der Verwendung als Inert- bzw. Schutzgas beispielsweise beim Schutzgasschweißen und in der Produktion von bestimmten Metallen wie Titan oder Tantal ausgenutzt. Dafür wird vorwiegend das Argon immer dann eingesetzt, wenn der billigere, aber reaktivere Stickstoff nicht verwendet werden kann. ⓘ
Helium ist Füll- und Traggas für Gasballone und Zeppeline. Neben Helium kann auch Wasserstoff verwendet werden. Dieser ist zwar leichter und ermöglicht mehr Nutzlast, jedoch kann er mit dem Sauerstoff der Luft reagieren und brennen. Beim unreaktiven Helium besteht diese Gefahr nicht. ⓘ
Entsprechend ihrer Häufigkeit und Verfügbarkeit werden Edelgase in unterschiedlichen Mengen produziert. So betrug 1998 die Menge des hergestellten Argons etwa 2 Milliarden m3, Helium wurde in einer Menge von rund 130 Millionen m3 isoliert. Die Weltjahresproduktion an Xenon wird dagegen für 1998 auf nur 5.000–7.000 m3 geschätzt (jeweils Normkubikmeter). Entsprechend unterschiedlich sind die Preise der Gase: Argon kostet etwa 15 Euro pro Kubikmeter (unter Standardbedingungen, Laborqualität), Xenon 10.000 Euro pro Kubikmeter (Stand 1999). ⓘ
Verbindungen
Xenonverbindungen

Die größte Vielfalt an Edelgasverbindungen gibt es mit dem Xenon. Die wichtigsten und stabilsten sind dabei die Xenonfluoride Xenon(II)-fluorid, Xenon(IV)-fluorid und Xenon(VI)-fluorid, die durch Reaktion von Xenon und Fluor in unterschiedlichen Verhältnissen synthetisiert werden. Xenon(II)-fluorid ist die einzige Edelgasverbindung, die in geringen Mengen technisch genutzt wird, sie dient als starkes Oxidations- und Fluorierungsmittel in der organischen Chemie. ⓘ
Mit Sauerstoff erreicht Xenon die höchste mögliche Oxidationsstufe +8. Diese wird in Xenon(VIII)-oxid und dem Oxifluorid Xenondifluoridtrioxid XeO3F2 sowie in Perxenaten der Form XeO4− erreicht. Weiterhin sind Xenon(VI)-oxid und die Oxifluoride XeO2F2 und XeOF4 in der Oxidationsstufe +6 sowie das Oxifluorid XeOF2 mit vierwertigem Xenon bekannt. Alle Xenonoxide und -oxifluoride sind instabil und vielfach explosiv. Auch Verbindungen des Xenons mit Stickstoff, Chlor und Kohlenstoff sind bekannt. Unter supersauren Bedingungen konnten auch Komplexe mit Metallen wie Gold oder Quecksilber synthetisiert werden. ⓘ
Verbindungen anderer Edelgase
Von den anderen Edelgasen sind Verbindungen nur in geringer Zahl bekannt. So sollten Radonverbindungen zwar thermodynamisch ähnlich stabil wie Xenonverbindungen sein, aufgrund der starken Radioaktivität und kurzen Halbwertszeit der Radon-Isotope ist ihre Synthese und exakte Charakterisierung aber außerordentlich schwierig. Vermutet wird die Existenz eines stabilen Radon(II)-fluorids, da Radon nach dem Durchleiten durch flüssiges Chlortrifluorid nicht mehr nachweisbar ist, somit reagiert haben muss. Löst man die Rückstände dieser Lösung in Wasser oder Säuren, bilden sich als Zersetzungsprodukte Sauerstoff und Fluorwasserstoff im gleichen Verhältnis wie bei Krypton- oder Xenondifluorid. ⓘ
Alle bekannten Verbindungen leichterer Edelgase sind thermodynamisch instabil, zersetzen sich leicht und lassen sich deshalb, wenn überhaupt, nur bei tiefen Temperaturen synthetisieren. Die wichtigste und stabilste Kryptonverbindung ist Krypton(II)-fluorid, das zu den stärksten bekannten Oxidations- und Fluorierungsmitteln zählt. Krypton(II)-fluorid ist direkt aus den Elementen herstellbar und Ausgangsprodukt einer Reihe weiterer Kryptonverbindungen. ⓘ
Während Helium- und Neonverbindungen weiterhin allein Gegenstand theoretischer Untersuchungen sind und Rechnungen ergaben, dass allenfalls eine Heliumverbindung (HHeF), dagegen keine einzige Neonverbindung stabil sein sollte, konnte eine erste Argonverbindung inzwischen tatsächlich synthetisiert werden: Durch Photolyse von Fluorwasserstoff in einer auf 7,5 K heruntergekühlten Argonmatrix konnte das sehr instabile Argonfluorohydrid gebildet werden, das schon bei Berührung zweier Moleküle oder Erwärmung über 27 K wieder in seine Bestandteile zerfällt. ⓘ
Clathrate
Argon, Krypton und Xenon bilden Clathrate, Einschlussverbindungen, bei denen das Edelgas physikalisch in einen umgebenden Feststoff eingeschlossen ist. Typische Beispiele hierfür sind Edelgas-Hydrate, bei denen die Gase in Eis eingeschlossen sind. Ein Argon-Hydrat bildet sich langsam erst bei −183 °C, Hydrate des Kryptons und Xenons schon bei −78 °C. Auch mit anderen Stoffen wie Hydrochinon sind Edelgas-Clathrate bekannt. ⓘ
Entladungsfarbe

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|
| Helium | Neon | Argon | Krypton | Xenon |
Die Farbe der Gasentladungsemission hängt von mehreren Faktoren ab, unter anderem von den folgenden
- Entladungsparameter (lokaler Wert der Stromdichte und des elektrischen Feldes, Temperatur usw.) - Beachten Sie die Farbvariation entlang der Entladung in der oberen Reihe);
- Gasreinheit (selbst kleine Anteile bestimmter Gase können die Farbe beeinflussen);
- Material der Entladungsröhrenhülle - beachten Sie die Unterdrückung der UV- und Blauanteile in den Röhren der unteren Reihe, die aus dickem Haushaltsglas bestehen. ⓘ










