Dekompressionskrankheit
| Dekompressionskrankheit ⓘ | |
|---|---|
| Andere Bezeichnungen | Taucherkrankheit, Taucherkrankheit, Aerobullose, Caisson-Krankheit |
 | |
| Zwei Matrosen der United States Navy demonstrieren die Behandlung der Dekompressionskrankheit in einer Dekompressionskammer | |
| Fachgebiet | Notfallmedizin |
Die Dekompressionskrankheit (abgekürzt DCS; auch Taucherkrankheit, Taucherkrankheit, Aerobullose und Caissonkrankheit genannt) ist ein medizinischer Zustand, der durch gelöste Gase verursacht wird, die während der Dekompression in Form von Blasen im Körpergewebe aufsteigen. DCS tritt am häufigsten während oder kurz nach einem Dekompressionsaufstieg beim Tauchen auf, kann aber auch durch andere Ursachen von Druckabfall verursacht werden, z. B. beim Ausstieg aus einem Caisson, bei Dekompression aus Sättigung, beim Flug in einem Flugzeug ohne Druckausgleich in großer Höhe und bei Außenbordeinsätzen in Raumfahrzeugen. DCS und arterielle Gasembolie werden zusammen als Dekompressionskrankheit bezeichnet. ⓘ
Da sich Blasen in jedem Teil des Körpers bilden oder dorthin wandern können, kann die DCS viele Symptome hervorrufen, und ihre Auswirkungen können von Gelenkschmerzen und Hautausschlägen bis hin zu Lähmungen und Tod reichen. Die individuelle Anfälligkeit kann von Tag zu Tag variieren, und verschiedene Personen können unter den gleichen Bedingungen unterschiedlich oder gar nicht betroffen sein. Die Klassifizierung der DCS-Typen nach Symptomen hat sich seit der ursprünglichen Beschreibung im 19. Jahrhundert weiterentwickelt. Der Schweregrad der Symptome reicht von kaum spürbar bis hin zu schnell tödlich. ⓘ
Das Risiko einer durch das Tauchen verursachten DCS kann durch geeignete Dekompressionsverfahren beherrscht werden, und es ist selten geworden, an dieser Krankheit zu erkranken. Aufgrund des potenziellen Schweregrads wurde viel Forschung betrieben, um sie zu verhindern, und Taucher verwenden fast durchgängig Tauchtabellen oder Tauchcomputer, um ihre Exposition zu begrenzen und ihre Aufstiegsgeschwindigkeit zu überwachen. Besteht der Verdacht auf DCS, wird sie durch eine hyperbare Sauerstofftherapie in einer Rekompressionskammer behandelt. Die Diagnose wird durch eine positive Reaktion auf die Behandlung bestätigt. Eine frühzeitige Behandlung erhöht die Chance auf eine erfolgreiche Genesung erheblich. ⓘ
| Klassifikation nach ICD-10 | |
|---|---|
| T70.3 | Caissonkrankheit [Dekompressionskrankheit] Druckluftkrankheit Taucherkrankheit |
| ICD-10 online (WHO-Version 2019) | |
Als Dekompressionskrankheit oder Druckfallkrankheit werden verschiedene Störungen durch Verletzungen in Folge zu schneller Druckentlastung nach Einwirkung von Überdruck bezeichnet. Die Verletzungen treten vor allem bei Tauchunfällen auf (Dekompressionsunfall), weswegen die Krankheit auch als Taucherkrankheit oder Caissonkrankheit (vom französischen Wort für Senkkasten) bezeichnet wird. Die gemeinsame Ursache aller Dekompressionsunfälle ist die Bildung von Gasblasen im Körperinneren (Ebullismus). ⓘ
Klassifizierung
DCS wird anhand der Symptome klassifiziert. In den frühesten Beschreibungen der DCS wurden die Begriffe: "Beugen" für Gelenk- oder Skelettschmerzen, "Würgen" für Atemprobleme und "Taumeln" für neurologische Probleme. Im Jahr 1960 führten Golding et al. eine einfachere Klassifizierung ein, die den Begriff "Typ I ('einfach')" für Symptome verwendet, die nur die Haut, den Bewegungsapparat oder das Lymphsystem betreffen, und "Typ II ('ernst')" für Symptome, bei denen andere Organe (wie das zentrale Nervensystem) betroffen sind. Die DCS vom Typ II gilt als schwerwiegender und hat in der Regel einen schlechteren Ausgang. Dieses System wird, mit geringfügigen Änderungen, auch heute noch verwendet. Infolge der veränderten Behandlungsmethoden ist diese Klassifizierung für die Diagnose heute weit weniger nützlich, da sich die neurologischen Symptome erst nach der Erstvorstellung entwickeln können und sowohl für die Typ-I- als auch für die Typ-II-DKS die gleiche Erstbehandlung gilt. ⓘ
Dekompressionskrankheit und Dysbarismus
Der Begriff Dysbarismus umfasst die Dekompressionskrankheit, die arterielle Gasembolie und das Barotrauma, während die Dekompressionskrankheit und die arterielle Gasembolie in der Regel gemeinsam als Dekompressionskrankheit bezeichnet werden, wenn eine genaue Diagnose nicht gestellt werden kann. Dekompressionskrankheit und arterielle Gasembolie werden sehr ähnlich behandelt, da sie beide durch Gasblasen im Körper verursacht werden. Die US-Marine schreibt für DCS Typ II und arterielle Gasembolie die gleiche Behandlung vor. Auch das Spektrum der Symptome überschneidet sich, obwohl die Symptome der arteriellen Gasembolie im Allgemeinen schwerwiegender sind, da sie häufig auf einen Infarkt (Unterbrechung der Blutversorgung und Absterben von Gewebe) zurückzuführen sind. ⓘ
Anzeichen und Symptome
Obwohl sich Blasen überall im Körper bilden können, wird DCS am häufigsten in den Schultern, Ellenbogen, Knien und Knöcheln beobachtet. Gelenkschmerzen ("die Beulen") machen etwa 60 % bis 70 % aller DCS-Fälle in der Höhe aus, wobei die Schulter die häufigste Stelle beim Höhen- und Prelltauchen ist und die Knie und Hüftgelenke bei Sättigungs- und Pressluftarbeiten. Neurologische Symptome treten in 10 bis 15 % der DCS-Fälle auf, wobei Kopfschmerzen und Sehstörungen die häufigsten Symptome sind. Hauterscheinungen treten in etwa 10 bis 15 % der Fälle auf. Pulmonale DCS ("Erstickungsanfälle") sind bei Tauchern sehr selten und werden bei Fliegern seit der Einführung von Protokollen zur Sauerstoffvorbeatmung viel seltener beobachtet. In der nachstehenden Tabelle sind die Symptome für die verschiedenen DCS-Typen aufgeführt. ⓘ
| DCS-Typ | Lage der Blase | Anzeichen und Symptome (klinische Manifestationen) |
|---|---|---|
| Muskel-Skelett-System | Meistens große Gelenke der Gliedmaßen
(Ellenbogen, Schultern, Hüfte, Handgelenke, Knie, Knöchel) |
|
| Kutane | Haut |
|
| Neurologisch | Gehirn |
|
| Neurologisch | Rückenmark |
|
| Konstitutionelle | Ganzer Körper |
|
| Audiovestibulär | Innenohr |
|
| Lunge | Lunge |
|
Häufigkeit
Die relative Häufigkeit der verschiedenen DCS-Symptome, die von der U.S. Navy beobachtet wurden, ist wie folgt:
| Symptome | Häufigkeit |
|---|---|
| lokale Gelenkschmerzen | 89% |
| Armsymptome | 70% |
| Bein-Symptome | 30% |
| Schwindel | 5.3% |
| Lähmungen | 2.3% |
| Kurzatmigkeit | 1.6% |
| extreme Müdigkeit | 1.3% |
| Kollaps/Bewusstlosigkeit | 0.5% |
Beginn
Obwohl die DCS schnell nach einem Tauchgang einsetzen kann, treten die Symptome in mehr als der Hälfte aller Fälle frühestens nach einer Stunde auf. In extremen Fällen können die Symptome auftreten, bevor der Tauchgang beendet ist. Die U.S. Navy und Technical Diving International, eine führende Ausbildungsorganisation für technische Taucher, haben eine Tabelle veröffentlicht, die die Zeit bis zum Auftreten der ersten Symptome dokumentiert. In der Tabelle wird nicht zwischen den verschiedenen Arten von DCS oder den verschiedenen Symptomen unterschieden. ⓘ
| Zeit bis zum Auftreten | Prozentsatz der Fälle |
|---|---|
| innerhalb von 1 Stunde | 42% |
| innerhalb von 3 Stunden | 60% |
| innerhalb von 8 Stunden | 83% |
| innerhalb von 24 Stunden | 98% |
| innerhalb von 48 Stunden | 100% |
Verursacht
DCS wird durch eine Verringerung des Umgebungsdrucks verursacht, die zur Bildung von Blasen aus inerten Gasen in den Geweben des Körpers führt. Sie kann beim Verlassen einer Hochdruckumgebung, beim Aufstieg aus der Tiefe oder beim Aufstieg in die Höhe auftreten. ⓘ
Auftauchen aus der Tiefe
DCS ist am besten bekannt als eine Taucherkrankheit, die Taucher betrifft, die ein Gas eingeatmet haben, das aufgrund des Drucks des umgebenden Wassers unter einem höheren Druck als dem Oberflächendruck steht. Das DCS-Risiko steigt, wenn über längere Zeit oder in größerer Tiefe getaucht wird, ohne allmählich aufzusteigen und die erforderlichen Dekompressionsstopps einzulegen, um den Überdruck der im Körper gelösten Inertgase langsam abzubauen. Die spezifischen Risikofaktoren sind nicht gut erforscht, und einige Taucher können unter gleichen Bedingungen anfälliger sein als andere. DCS wurde in seltenen Fällen bei Tauchern mit angehaltenem Atem bestätigt, die eine Reihe von Tieftauchgängen mit kurzen Oberflächenpausen durchgeführt haben, und könnte die Ursache für die Krankheit sein, die von den Ureinwohnern südpazifischer Inseln, die seit Jahrhunderten mit angehaltenem Atem nach Nahrung und Perlen tauchen, Taravana genannt wird. ⓘ
Das Risiko, dass ein Taucher an DCS erkrankt, hängt im Wesentlichen von zwei Faktoren ab:
- die Geschwindigkeit und Dauer der Gasaufnahme unter Druck - je tiefer oder länger der Tauchgang, desto mehr Gas wird in höheren Konzentrationen als normal in das Körpergewebe aufgenommen (Henry's Law);
- Geschwindigkeit und Dauer der Ausgasung bei Druckabfall - je schneller der Aufstieg und je kürzer die Abstände zwischen den Tauchgängen, desto weniger Zeit bleibt für den sicheren Abtransport des absorbierten Gases durch die Lungen, was dazu führt, dass diese Gase aus der Lösung kommen und "Mikroblasen" im Blut bilden. ⓘ
Selbst wenn die Druckveränderung keine unmittelbaren Symptome verursacht, kann die schnelle Druckveränderung zu dauerhaften Knochenschäden führen, die als dysbare Osteonekrose (DON) bezeichnet werden. DON kann sich aus einer einzigen Exposition gegenüber einer schnellen Dekompression entwickeln. ⓘ
Verlassen einer Hochdruckumgebung
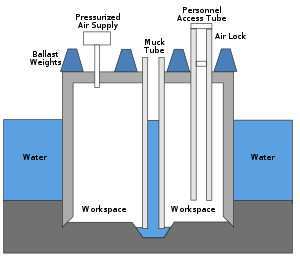
Wenn Arbeiter einen unter Druck stehenden Senkkasten oder ein Bergwerk verlassen, das unter Druck gesetzt wurde, um Wasser fernzuhalten, erfahren sie eine erhebliche Verringerung des Umgebungsdrucks. Ein ähnlicher Druckabfall tritt auf, wenn Astronauten ein Raumfahrzeug verlassen, um einen Weltraumspaziergang oder eine Außenbordaktivität durchzuführen, wobei der Druck in ihrem Raumanzug niedriger ist als der Druck im Fahrzeug. ⓘ
Der ursprüngliche Name für DCS war "Caisson-Krankheit". Dieser Begriff wurde im 19. Jahrhundert eingeführt, als unter Druck stehende Senkkästen verwendet wurden, um zu verhindern, dass Wasser große Baugruben unterhalb des Grundwasserspiegels überflutet, z. B. Brückenpfeiler und Tunnel. Arbeiter, die sich unter hohem Umgebungsdruck aufhalten, sind gefährdet, wenn sie zum niedrigeren Druck außerhalb des Senkkastens zurückkehren, wenn der Druck nicht langsam reduziert wird. DCS war ein wichtiger Faktor beim Bau der Eads-Brücke, als 15 Arbeiter an einer damals mysteriösen Krankheit starben, und später beim Bau der Brooklyn-Brücke, wo es den Projektleiter Washington Roebling außer Gefecht setzte. Auf der anderen Seite der Insel Manhattan stellte der Bauunternehmer Ernest William Moir 1889 beim Bau des Hudson River Tunnels fest, dass die Arbeiter an der Dekompressionskrankheit starben, und leistete Pionierarbeit bei der Verwendung einer Schleusenkammer zur Behandlung. ⓘ
Aufstieg in die Höhe
Das häufigste Gesundheitsrisiko beim Aufstieg in die Höhe ist nicht die Dekompressionskrankheit, sondern die Höhenkrankheit oder akute Höhenkrankheit (AMS), deren Ursachen und Symptome völlig anders gelagert sind und in keinem Zusammenhang stehen. AMS entsteht nicht durch die Bildung von Blasen aus gelösten Gasen im Körper, sondern durch die Exposition gegenüber einem niedrigen Sauerstoffpartialdruck und Alkalose. Allerdings können auch Passagiere in Flugzeugen ohne Druckausgleich in großer Höhe einem gewissen Risiko für DCS ausgesetzt sein. ⓘ
Höhen-DCS wurde in den 1930er Jahren mit der Entwicklung von Höhenballon- und Flugzeugflügen zu einem Problem, das jedoch nicht so groß war wie das AMS, das die Entwicklung von Druckkabinen vorantrieb, die zufälligerweise DCS kontrollierten. In Verkehrsflugzeugen muss der Kabinendruck auch bei Flügen über 12.000 m (39.000 ft) auf oder unter 2.400 m (7.900 ft) gehalten werden. DCS-Symptome bei gesunden Personen sind in der Folge sehr selten, es sei denn, es kommt zu einem Druckabfall oder die Person hat kürzlich getaucht. Taucher, die kurz nach dem Tauchen auf einen Berg fahren oder fliegen, sind selbst in einem Flugzeug mit Druckausgleich besonders gefährdet, da die vorgeschriebene Kabinenhöhe von 2.400 m (7.900 ft) nur 73 % des Drucks auf Meereshöhe entspricht. ⓘ
Generell gilt: Je höher die Flughöhe, desto größer das Risiko einer Höhen-DCS, aber es gibt keine spezifische, maximale und sichere Flughöhe, unterhalb der sie niemals auftritt. Auf oder unter 5.500 m (18.000 ft) treten nur sehr wenige Symptome auf, es sei denn, die Patienten hatten prädisponierende medizinische Bedingungen oder waren erst kürzlich getaucht. Es besteht ein Zusammenhang zwischen der zunehmenden Höhe über 5.500 m (18.000 ft) und der Häufigkeit von DCS in der Höhe, aber es besteht kein direkter Zusammenhang mit dem Schweregrad der verschiedenen Arten von DCS. Eine Studie der US Air Force berichtet, dass es nur wenige Vorfälle zwischen 5.500 m (18.000 ft) und 7.500 m (24.600 ft) gibt und 87 % der Vorfälle auf oder über 7.500 m (24.600 ft) stattfanden. Fallschirmspringer, die in großen Höhen abspringen, können das Risiko einer Höhen-DCS verringern, wenn sie den Stickstoff aus dem Körper spülen, indem sie vorher reinen Sauerstoff einatmen. ⓘ
Prädisponierende Faktoren
Obwohl das Auftreten von DCS nicht leicht vorhersehbar ist, sind viele prädisponierende Faktoren bekannt. Sie können entweder umweltbedingt oder individuell sein. Die Dekompressionskrankheit und die arterielle Gasembolie beim Sporttauchen werden mit bestimmten demografischen, umweltbedingten und tauchstilistischen Faktoren in Verbindung gebracht. In einer 2005 veröffentlichten statistischen Studie wurden potenzielle Risikofaktoren untersucht: Alter, Geschlecht, Body-Mass-Index, Rauchen, Asthma, Diabetes, Herz-Kreislauf-Erkrankungen, frühere Dekompressionskrankheiten, Jahre seit der Zertifizierung, Tauchgänge im letzten Jahr, Anzahl der Tauchtage, Anzahl der Tauchgänge in einer Wiederholungsserie, letzte Tauchtiefe, Verwendung von Nitrox und Trockenanzug. Für Asthma, Diabetes, kardiovaskuläre Erkrankungen, Rauchen oder den Body-Mass-Index wurde kein signifikanter Zusammenhang mit dem Risiko einer Dekompressionskrankheit oder einer arteriellen Gasembolie festgestellt. Eine größere Tiefe, eine frühere DCI, eine größere Anzahl aufeinander folgender Tauchtage und die Tatsache, dass es sich um einen Mann handelte, waren mit einem höheren Risiko für Dekompressionskrankheit und Arteriengasembolie verbunden. Die Verwendung von Nitrox und Trockentauchanzügen, die Häufigkeit des Tauchens im letzten Jahr, das zunehmende Alter und die Jahre seit der Zertifizierung wurden mit einem geringeren Risiko in Verbindung gebracht, möglicherweise als Indikatoren für eine umfangreichere Ausbildung und Erfahrung. ⓘ
Umwelt
Die folgenden Umweltfaktoren erhöhen nachweislich das Risiko einer DCS:
- die Größe des Druckabfallverhältnisses - ein großes Druckabfallverhältnis verursacht mit größerer Wahrscheinlichkeit eine DCS als ein kleines Verhältnis.
- sich wiederholende Expositionen - wiederholte Tauchgänge innerhalb eines kurzen Zeitraums (einige Stunden) erhöhen das Risiko der Entwicklung einer DCS. Wiederholte Aufstiege in Höhen von mehr als 5.500 Metern (18.000 Fuß) innerhalb ähnlich kurzer Zeiträume erhöhen das Risiko der Entwicklung einer Höhen-DCS.
- die Aufstiegsgeschwindigkeit - je schneller der Aufstieg, desto größer das Risiko der Entwicklung von DCS. Das U.S. Navy Diving Manual weist darauf hin, dass Aufstiegsgeschwindigkeiten von mehr als 20 m/min (66 ft/min) beim Tauchen das Risiko einer DCS erhöhen, während Sporttauchtabellen wie die Bühlmann-Tabellen eine Aufstiegsgeschwindigkeit von 10 m/min (33 ft/min) vorschreiben, wobei die letzten 6 m (20 ft) mindestens eine Minute dauern sollten. Eine Person, die einer schnellen Dekompression (hohe Aufstiegsgeschwindigkeit) in einer Höhe von mehr als 5.500 Metern ausgesetzt ist, hat ein größeres Risiko für eine Höhen-DCS als eine Person, die in der gleichen Höhe, aber mit einer geringeren Aufstiegsgeschwindigkeit ausgesetzt ist.
- Dauer der Exposition - je länger die Dauer des Tauchgangs, desto größer ist das Risiko einer DCS. Längere Flüge, insbesondere in Höhen von 5.500 m (18.000 ft) und darüber, bergen ein größeres Risiko für Höhen-DCS.
- Unterwassertauchen vor dem Fliegen - Taucher, die kurz nach einem Tauchgang in die Höhe aufsteigen, erhöhen ihr Risiko, eine DCS zu entwickeln, auch wenn der Tauchgang selbst innerhalb der sicheren Grenzen der Tauchtabelle lag. In den Tauchtabellen ist vorgesehen, dass nach dem Tauchgang vor dem Flug eine gewisse Zeit an der Oberfläche verbracht werden muss, damit überschüssiger Stickstoff entweichen kann. Der Druck, der selbst in einem Flugzeug mit Druckausgleich aufrechterhalten wird, kann jedoch so niedrig sein wie der Druck, der einer Höhe von 2.400 m über dem Meeresspiegel entspricht. Daher wird die Annahme, dass die Oberflächenpause in der Tauchtabelle bei normalem Atmosphärendruck stattfindet, durch das Fliegen während der Oberflächenpause außer Kraft gesetzt, und ein ansonsten sicherer Tauchgang kann dann die Grenzen der Tauchtabelle überschreiten.
- Tauchen vor einer Reise in die Höhe - DCS kann auch ohne Flug auftreten, wenn sich die Person unmittelbar nach dem Tauchgang an einen hochgelegenen Ort an Land begibt. So erhöhen z. B. Taucher in Eritrea, die von der Küste zum Asmara-Plateau auf 2.400 m fahren, ihr DCS-Risiko.
- Tauchen in der Höhe - Tauchen in Gewässern, deren Oberflächendruck deutlich unter dem des Meeresspiegels liegt, z. B. der Titicacasee auf 3.800 m. Versionen von Dekompressionstabellen für Höhen über 300 m (980 ft) oder Tauchcomputer mit Höheneinstellungen oder Oberflächendrucksensoren können verwendet werden, um dieses Risiko zu verringern. ⓘ
Einzelne

Die folgenden individuellen Faktoren wurden als mögliche Ursache für ein erhöhtes DCS-Risiko identifiziert:
- Dehydrierung - Studien von Walder kamen zu dem Schluss, dass die Dekompressionskrankheit bei Fliegern reduziert werden konnte, wenn die Oberflächenspannung des Serums durch die Einnahme von isotonischer Kochsalzlösung erhöht wurde, und die hohe Oberflächenspannung von Wasser wird allgemein als hilfreich für die Kontrolle der Blasengröße angesehen. Es wird empfohlen, auf eine angemessene Flüssigkeitszufuhr zu achten. Es gibt keine überzeugenden Beweise dafür, dass eine Überwässerung irgendwelche Vorteile hat, und sie wird mit dem Lungenödem beim Tauchen in Verbindung gebracht.
- Offenes Foramen ovale - ein Loch zwischen den Vorhofkammern des Herzens beim Fötus wird normalerweise mit den ersten Atemzügen bei der Geburt durch eine Klappe verschlossen. Bei etwa 20 % der Erwachsenen verschließt sich die Klappe jedoch nicht vollständig, so dass beim Husten oder bei Aktivitäten, die den Druck im Brustkorb erhöhen, Blut durch das Loch fließen kann. Beim Tauchen kann dies dazu führen, dass venöses Blut mit Mikrobläschen aus Inertgas die Lunge umgeht, wo die Bläschen andernfalls durch das Lungenkapillarsystem herausgefiltert würden, und direkt in das arterielle System (einschließlich der Arterien zum Gehirn, Rückenmark und Herz) zurückkehrt. Im arteriellen System sind die Blasen (arterielle Gasembolie) weitaus gefährlicher, da sie den Blutkreislauf blockieren und einen Infarkt (Absterben des Gewebes durch lokalen Blutflussverlust) verursachen. Im Gehirn führt der Infarkt zu einem Schlaganfall, im Rückenmark kann er zu Lähmungen führen.
- das Alter einer Person - es gibt einige Berichte, die auf ein höheres Risiko für Höhen-DCS mit zunehmendem Alter hinweisen.
- Frühere Verletzungen - es gibt Hinweise darauf, dass kürzlich erlittene Verletzungen der Gelenke oder Gliedmaßen das Risiko für die Entwicklung dekompressionsbedingter Blasen erhöhen.
- Umgebungstemperatur - Es gibt einige Hinweise darauf, dass die individuelle Exposition gegenüber sehr kalten Umgebungstemperaturen das Risiko einer Höhen-DCS erhöhen kann. Das Risiko der Dekompressionskrankheit kann durch eine höhere Umgebungstemperatur während der Dekompression nach Tauchgängen in kaltem Wasser verringert werden.
- Körpertyp - Personen mit einem hohen Körperfettanteil haben in der Regel ein höheres Risiko für DCS. Dies ist darauf zurückzuführen, dass Stickstoff in Fett fünfmal leichter löslich ist als in Wasser, was dazu führt, dass während der Zeit unter Druck größere Mengen an gelöstem Stickstoff im Körper vorhanden sind. Fett macht etwa 15-25 Prozent des Körpers eines gesunden Erwachsenen aus, speichert aber bei normalem Druck etwa die Hälfte der Gesamtstickstoffmenge (etwa 1 Liter).
- Alkoholkonsum - obwohl Alkoholkonsum die Dehydrierung erhöht und daher die Anfälligkeit für DCS steigern kann, fand eine Studie aus dem Jahr 2005 keine Hinweise darauf, dass Alkoholkonsum die Häufigkeit von DCS erhöht. ⓘ
Mechanismus

Der Druckabfall bewirkt, dass inerte Gase, die unter höherem Druck gelöst wurden, aus der physikalischen Lösung austreten und Gasblasen im Körper bilden. Diese Blasen verursachen die Symptome der Dekompressionskrankheit. Blasen können sich immer dann bilden, wenn der Körper einem Druckabfall ausgesetzt ist, aber nicht alle Blasen führen zu DCS. Die Menge des in einer Flüssigkeit gelösten Gases wird durch das Henry'sche Gesetz beschrieben, das besagt, dass bei einer Verringerung des Drucks eines Gases, das mit einer Flüssigkeit in Berührung kommt, auch die Menge des in der Flüssigkeit gelösten Gases proportional abnimmt. ⓘ
Beim Auftauchen aus einem Tauchgang tritt inertes Gas in einem Prozess aus, der "Ausgasen" oder "Offgassing" genannt wird. Unter normalen Bedingungen erfolgt der größte Teil der Ausgasung durch den Gasaustausch in der Lunge. Wenn das Inertgas zu schnell aus der Lösung austritt, um in der Lunge ausgasen zu können, können sich Blasen im Blut oder in den festen Geweben des Körpers bilden. Die Bildung von Blasen in der Haut oder den Gelenken führt zu milderen Symptomen, während eine große Anzahl von Blasen im venösen Blut Lungenschäden verursachen kann. Bei den schwersten Formen von DCS wird die Funktion des Rückenmarks unterbrochen und letztlich geschädigt, was zu Lähmungen, sensorischen Störungen oder zum Tod führt. Bei einem Rechts-Links-Shunt des Herzens, wie z. B. einem offenen Foramen ovale, können venöse Blasen in das arterielle System gelangen und zu einer arteriellen Gasembolie führen. Ein ähnlicher Effekt, der als Ebullismus bezeichnet wird, kann bei einer explosiven Dekompression auftreten, wenn Wasserdampf aufgrund eines drastischen Druckabfalls in der Umgebung Blasen in den Körperflüssigkeiten bildet. ⓘ
Inerte Gase
Das wichtigste Inertgas in der Luft ist Stickstoff, aber Stickstoff ist nicht das einzige Gas, das DCS verursachen kann. Atemgasgemische wie Trimix und Heliox enthalten Helium, das ebenfalls die Dekompressionskrankheit auslösen kann. Helium tritt schneller in den Körper ein als Stickstoff und verlässt ihn auch schneller wieder. Daher sind andere Dekompressionspläne erforderlich, aber da Helium keine Narkose verursacht, wird es in Gasgemischen für das Tieftauchen gegenüber Stickstoff bevorzugt. Es gibt eine Debatte über die Dekompressionsanforderungen für Helium bei Kurzzeittauchgängen. Die meisten Taucher führen längere Dekompressionen durch; einige Gruppen wie die WKPP haben jedoch mit kürzeren Dekompressionszeiten experimentiert, indem sie tiefe Stopps einlegten. ⓘ
Jedes inerte Gas, das unter Druck eingeatmet wird, kann Blasen bilden, wenn der Umgebungsdruck sinkt. Sehr tiefe Tauchgänge wurden mit Wasserstoff-Sauerstoff-Gemischen (Hydrox) durchgeführt, aber eine kontrollierte Dekompression ist immer noch erforderlich, um DCS zu vermeiden. ⓘ
Isobare Gegendiffusion
DCS kann auch bei konstantem Umgebungsdruck entstehen, wenn zwischen Gasgemischen mit unterschiedlichen Anteilen an Inertgas gewechselt wird. Dies wird als isobare Gegendiffusion bezeichnet und stellt ein Problem bei sehr tiefen Tauchgängen dar. So wechselt ein Taucher nach der Verwendung eines sehr heliumreichen Trimix in der tiefsten Phase des Tauchgangs während des Aufstiegs zu Gemischen, die immer weniger Helium und immer mehr Sauerstoff und Stickstoff enthalten. Stickstoff diffundiert 2,65 Mal langsamer in das Gewebe als Helium, ist aber etwa 4,5 Mal besser löslich. Der Wechsel zwischen Gasgemischen mit sehr unterschiedlichen Anteilen von Stickstoff und Helium kann dazu führen, dass "schnelles" Gewebe (d. h. gut durchblutetes Gewebe) seine Gesamtbelastung mit Inertgas erhöht. Dies führt häufig zur Dekompressionskrankheit des Innenohrs, da das Ohr besonders empfindlich auf diesen Effekt zu reagieren scheint. ⓘ
Blasenbildung
Es ist nicht bekannt, wo sich die Mikrokerne befinden oder wo sich die Blasen ursprünglich bilden. Die wahrscheinlichsten Mechanismen für die Blasenbildung sind die Tribonukleation, bei der sich zwei Oberflächen berühren und wieder trennen (z. B. in Fugen), und die heterogene Nukleation, bei der die Blasen an einer Stelle entstehen, die auf einer mit der Flüssigkeit in Kontakt stehenden Oberfläche liegt. Die homogene Keimbildung, bei der sich die Blasen in der Flüssigkeit selbst bilden, ist weniger wahrscheinlich, da sie sehr viel größere Druckunterschiede erfordert, als sie bei der Dekompression auftreten. Die spontane Bildung von Nanoblasen auf hydrophoben Oberflächen ist eine mögliche Quelle für Mikrokerne, aber es ist noch nicht klar, ob diese groß genug werden können, um Symptome zu verursachen, da sie sehr stabil sind. ⓘ
Sobald sich Mikrobläschen gebildet haben, können sie entweder durch eine Druckverringerung oder durch Diffusion von Gas aus der Umgebung in das Gas wachsen. Im Körper können sich die Bläschen in den Geweben befinden oder mit dem Blutstrom mitgeführt werden. Die Geschwindigkeit des Blutflusses innerhalb eines Blutgefäßes und die Geschwindigkeit der Zufuhr von Blut in die Kapillaren (Perfusion) sind die wichtigsten Faktoren, die bestimmen, ob gelöstes Gas von den Gewebeblasen oder von den Blasen im Blutkreislauf aufgenommen wird, um das Blasenwachstum zu fördern. ⓘ
Pathophysiologie
Der primäre Auslöser der Dekompressionskrankheit ist die Blasenbildung durch überschüssige gelöste Gase. Für die Entstehung und das Wachstum von Blasen in Geweben sowie für den Grad der Übersättigung, der das Blasenwachstum begünstigt, wurden verschiedene Hypothesen aufgestellt. Die früheste Blasenbildung sind subklinische intravaskuläre Blasen, die mit Doppler-Ultraschall im venösen Kreislauf nachgewiesen werden können. Das Vorhandensein dieser "stillen" Blasen ist keine Garantie dafür, dass sie bestehen bleiben und sich zu Symptomen entwickeln. ⓘ
In den systemischen Kapillaren gebildete Gefäßblasen können sich in den Lungenkapillaren festsetzen und diese vorübergehend verstopfen. Wenn dies schwerwiegend ist, kann das Symptom "Würgen" auftreten. Wenn der Taucher ein offenes Foramen ovale (oder einen Shunt im Lungenkreislauf) hat, können die Blasen dieses passieren und unter Umgehung des Lungenkreislaufs in das arterielle Blut gelangen. Wenn diese Blasen nicht im arteriellen Plasma absorbiert werden und sich in den systemischen Kapillaren festsetzen, blockieren sie den Fluss des sauerstoffhaltigen Blutes zu den Geweben, die von diesen Kapillaren versorgt werden, und diese Gewebe werden mit Sauerstoff unterversorgt. Moon und Kisslo (1988) kamen zu dem Schluss, dass "es Hinweise darauf gibt, dass das Risiko einer schweren neurologischen DCI oder einer früh einsetzenden DCI bei Tauchern mit einem ruhenden Rechts-Links-Shunt durch ein PFO erhöht ist. Es gibt derzeit keine Hinweise darauf, dass ein PFO mit leichten oder spät auftretenden Beugungen zusammenhängt. Blasen bilden sich nicht nur in den Blutgefäßen, sondern auch in anderen Geweben. Inertes Gas kann in die Blasenkerne zwischen den Geweben diffundieren. In diesem Fall können sich die Blasen verformen und das Gewebe dauerhaft schädigen. Wenn sie wachsen, können die Blasen auch auf Nerven drücken und Schmerzen verursachen. Extravaskuläre oder autochthone Blasen bilden sich in der Regel in langsamen Geweben wie Gelenken, Sehnen und Muskelummantelungen. Die direkte Ausdehnung führt zu Gewebeschäden mit der Freisetzung von Histaminen und den damit verbundenen Auswirkungen. Biochemische Schäden können ebenso wichtig oder wichtiger sein als mechanische Auswirkungen. ⓘ
Die Größe und das Wachstum von Blasen können durch verschiedene Faktoren beeinflusst werden: Gasaustausch mit angrenzendem Gewebe, Vorhandensein von Tensiden, Koaleszenz und Zerfall durch Kollision. Gefäßblasen können eine direkte Verstopfung verursachen, Thrombozyten und rote Blutkörperchen aggregieren und den Gerinnungsprozess auslösen, was zu einer lokalen und stromabwärts gerichteten Gerinnung führt. ⓘ
Arterien können durch intravaskuläre Fettaggregation blockiert werden. Thrombozyten sammeln sich in der Nähe von Blasen an. Die Endothelschädigung kann eine mechanische Wirkung des Blasendrucks auf die Gefäßwände, eine toxische Wirkung der stabilisierten Thrombozytenaggregate und möglicherweise toxische Wirkungen aufgrund der Assoziation von Lipiden mit den Luftblasen sein. Proteinmoleküle können durch eine Neuausrichtung der Sekundär- und Tertiärstruktur denaturiert werden, wenn unpolare Gruppen in das Blasengas eindringen und hydrophile Gruppen im umgebenden Blut verbleiben, was eine Kaskade pathophysiologischer Ereignisse auslösen kann, die zu den klinischen Anzeichen der Dekompressionskrankheit führen. ⓘ
Die physiologischen Auswirkungen einer Verringerung des Umgebungsdrucks hängen von der Geschwindigkeit des Blasenwachstums, dem Ort und der Oberflächenaktivität ab. Ein plötzlicher Druckabfall in gesättigtem Gewebe führt zu einer vollständigen Zerstörung der Zellorganellen, während ein allmählicherer Druckabfall die Ansammlung einer geringeren Anzahl größerer Blasen ermöglichen kann, von denen einige zwar keine klinischen Anzeichen hervorrufen, aber dennoch physiologische Wirkungen verursachen, die typisch für eine Blut-Gas-Grenzfläche und mechanische Effekte sind. Gas wird in allen Geweben gelöst, aber die Dekompressionskrankheit wird klinisch nur im zentralen Nervensystem, in den Knochen, Ohren, Zähnen, der Haut und der Lunge erkannt. ⓘ
Nekrosen wurden häufig im unteren Hals-, Brust- und oberen Lendenbereich des Rückenmarks festgestellt. Ein katastrophaler Druckabfall aus der Sättigung führt zu einer explosiven mechanischen Zerstörung der Zellen durch lokales Aufbrausen, während ein allmählicherer Druckabfall eher zu diskreten Blasen führt, die sich in der weißen Substanz ansammeln und von einer Proteinschicht umgeben sind. Typische akute Dekompressionsverletzungen der Wirbelsäule treten in den Säulen der weißen Substanz auf. Infarkte sind durch Ödeme, Blutungen und eine frühe Myelin-Degeneration gekennzeichnet und befinden sich in der Regel in der Nähe kleiner Blutgefäße. Die Läsionen sind im Allgemeinen diskret. Die Ödeme erstrecken sich in der Regel auf die angrenzende graue Substanz. In den mit den Infarkten verbundenen Blutgefäßen finden sich Mikrothromben. ⓘ
Nach den akuten Veränderungen kommt es zu einer Invasion von Lipidphagozyten und einer Degeneration der angrenzenden Nervenfasern mit Gefäßhyperplasie an den Rändern der Infarkte. Die Lipidphagozyten werden später durch eine zelluläre Reaktion von Astrozyten ersetzt. Die Gefäße in den umliegenden Gebieten bleiben durchlässig, sind aber kollagenisiert. Die Verteilung der Rückenmarksläsionen hängt möglicherweise mit der Gefäßversorgung zusammen. Über die Ätiologie der Dekompressionserkrankung am Rückenmark herrscht noch Unklarheit. ⓘ
Dysbarische Osteonekrosen sind in der Regel bilateral und treten in der Regel an beiden Enden des Oberschenkels und am proximalen Ende des Oberarmknochens auf. Die anfängliche Schädigung wird auf die Bildung von Blasen zurückgeführt, und ein einziger Vorfall kann ausreichen. Die Inzidenz ist jedoch sporadisch und steht im Allgemeinen in Zusammenhang mit relativ langen Zeiträumen der Hyperbar-Exposition, und die Ätiologie ist ungewiss. Eine frühzeitige Identifizierung der Läsionen durch Röntgenaufnahmen ist nicht möglich, aber im Laufe der Zeit entwickeln sich Bereiche mit Röntgentrübungen in Verbindung mit dem geschädigten Knochen. ⓘ
Diagnose
Die Diagnose der Dekompressionskrankheit beruht fast ausschließlich auf dem klinischen Bild, da es keine Labortests gibt, die die Diagnose zweifelsfrei bestätigen oder widerlegen können. Es wurden verschiedene Bluttests vorgeschlagen, die jedoch nicht spezifisch für die Dekompressionskrankheit sind, einen ungewissen Nutzen haben und nicht allgemein verwendet werden. ⓘ
Der Verdacht auf Dekompressionskrankheit sollte geäußert werden, wenn eines der mit dieser Krankheit verbundenen Symptome nach einem Druckabfall, insbesondere innerhalb von 24 Stunden nach dem Tauchen, auftritt. Im Jahr 1995 traten bei 95 % aller dem Divers Alert Network gemeldeten Fälle innerhalb von 24 Stunden Symptome auf. Dieses Zeitfenster kann auf 36 Stunden beim Aufstieg in die Höhe und 48 Stunden bei längerer Höhenexposition nach dem Tauchen verlängert werden. Eine andere Diagnose sollte vermutet werden, wenn schwere Symptome mehr als sechs Stunden nach einer Dekompression ohne Höhenexposition beginnen oder wenn ein Symptom mehr als 24 Stunden nach dem Auftauchen auftritt. Die Diagnose wird bestätigt, wenn die Symptome durch Rekompression gelindert werden. Obwohl MRT oder CT bei DCS häufig Blasen erkennen können, sind sie für die Diagnose nicht so gut geeignet wie eine genaue Anamnese des Ereignisses und eine Beschreibung der Symptome. ⓘ
Drucktest
Es gibt keinen Goldstandard für die Diagnose, und DCI-Experten sind selten. Die meisten Kammern, die für die Behandlung von Sporttauchern offen sind und dem Diver's Alert Network Bericht erstatten, behandeln weniger als 10 Fälle pro Jahr, so dass es für die behandelnden Ärzte schwierig ist, Erfahrung in der Diagnose zu entwickeln. Eine Methode, die von kommerziellen Tauchbetreuern angewandt wird, wenn sie überlegen, ob eine Rekompression als Erste-Hilfe-Maßnahme durchgeführt werden soll, wenn sie eine Kammer vor Ort haben, ist der so genannte Drucktest. Der Taucher wird auf Kontraindikationen für die Rekompression untersucht, und wenn keine vorliegen, wird rekomprimiert. Wenn die Symptome während der Rekompression abklingen oder sich verringern, kann davon ausgegangen werden, dass ein Behandlungsplan wirksam ist. Der Test ist nicht völlig zuverlässig, und es sind sowohl falsch positive als auch falsch negative Ergebnisse möglich, aber im kommerziellen Tauchumfeld wird er im Zweifelsfall oft als behandlungswürdig angesehen. ⓘ
Differentialdiagnose
Die Symptome einer DCS und einer arteriellen Gasembolie können praktisch nicht voneinander zu unterscheiden sein. Am zuverlässigsten lässt sich der Unterschied anhand des Tauchprofils feststellen, da die Wahrscheinlichkeit einer DCS von der Dauer der Exposition und der Höhe des Drucks abhängt, während eine AGE ausschließlich von der Durchführung des Aufstiegs abhängig ist. In vielen Fällen ist es nicht möglich, zwischen den beiden zu unterscheiden, aber da die Behandlung in solchen Fällen dieselbe ist, spielt dies normalerweise keine Rolle. ⓘ
Zu den anderen Erkrankungen, die mit DCS verwechselt werden können, gehören die Hautsymptome Cutis marmorata aufgrund von DCS und das Barotrauma der Haut aufgrund von Druck auf den Trockenanzug, für das keine Behandlung erforderlich ist. Die Quetschung des Trockenanzugs führt zu Rötungen und möglicherweise zu Blutergüssen an den Stellen, an denen die Haut zwischen den Falten des Anzugs eingeklemmt wurde, während die marmorierte Cutis marmorata in der Regel auf der Haut auftritt, wo sich subkutanes Fett befindet, und kein lineares Muster aufweist. ⓘ
Vorübergehende Episoden schwerer neurologischer Ausfälle mit schneller Spontanerholung kurz nach einem Tauchgang können auf Unterkühlung zurückgeführt werden, können aber auch symptomatisch für eine kurzfristige ZNS-Beteiligung sein, die Restprobleme oder Rückfälle haben kann. Man geht davon aus, dass diese Fälle unterdiagnostiziert sind. ⓘ
Innenohr-DCS kann mit alternobarem Schwindel und Reverse Squeeze verwechselt werden. Die Anamnese von Ausgleichsschwierigkeiten während des Tauchgangs macht ein Barotrauma des Ohrs wahrscheinlicher, schließt aber nicht immer die Möglichkeit einer Innenohr-DCS aus, die mit tiefen Mischgastauchgängen mit Dekompressionsstopps einhergeht. ⓘ
Taubheitsgefühle und Kribbeln werden mit DCS der Wirbelsäule in Verbindung gebracht, können aber auch durch Druck auf Nerven (Kompressionsneurapraxie) verursacht werden. Bei DCS ist das Taubheitsgefühl oder Kribbeln in der Regel auf ein oder eine Reihe von Dermatomen beschränkt, während Druck auf einen Nerv in der Regel charakteristische Taubheitsbereiche hervorruft, die mit dem spezifischen Nerv auf nur einer Seite des Körpers distal zum Druckpunkt verbunden sind. Ein Verlust von Kraft oder Funktion ist wahrscheinlich ein medizinischer Notfall. Ein Gefühlsverlust, der länger als ein oder zwei Minuten anhält, weist darauf hin, dass eine sofortige ärztliche Behandlung erforderlich ist. Nur bei partiellen Gefühlsveränderungen oder Parästhesien gilt diese Unterscheidung zwischen leichten und schweren Verletzungen. ⓘ
Großflächige Taubheitsgefühle mit einhergehender Schwäche oder Lähmung, insbesondere wenn eine ganze Gliedmaße betroffen ist, deuten auf eine wahrscheinliche Beteiligung des Gehirns hin und erfordern dringend ärztliche Hilfe. Parästhesien oder Schwäche, die ein Dermatom betreffen, deuten auf eine wahrscheinliche Beteiligung des Rückenmarks oder der Spinalnervenwurzel hin. Obwohl es möglich ist, dass dies auch andere Ursachen haben kann, wie z. B. eine verletzte Bandscheibe, weisen diese Symptome auf die dringende Notwendigkeit einer medizinischen Untersuchung hin. In Kombination mit Schwäche, Lähmung oder Verlust der Darm- oder Blasenkontrolle weisen sie auf einen medizinischen Notfall hin. ⓘ
Vorbeugung
Tauchen unter Wasser

Um eine übermäßige Blasenbildung zu vermeiden, die zur Dekompressionskrankheit führen kann, begrenzen Taucher ihre Aufstiegsgeschwindigkeit - die von den gängigen Dekompressionsmodellen empfohlene Aufstiegsgeschwindigkeit liegt bei etwa 10 Metern pro Minute - und befolgen bei Bedarf einen Dekompressionsplan. Dieser Plan kann vorsehen, dass der Taucher bis zu einer bestimmten Tiefe aufsteigt und in dieser Tiefe bleibt, bis genügend Inertgas aus dem Körper ausgeschieden ist, um einen weiteren Aufstieg zu ermöglichen. Jeder dieser Schritte wird als "Dekompressionsstopp" bezeichnet, und ein Tauchplan für eine bestimmte Grundzeit und Tiefe kann einen oder mehrere Stopps oder auch gar keinen enthalten. Tauchgänge, die keine Dekompressionsstopps enthalten, werden als "Nullzeittauchgänge" bezeichnet, aber Taucher planen in der Regel einen kurzen "Sicherheitsstopp" auf 3 bis 6 m (10 bis 20 ft) ein, je nach Ausbildungsorganisation oder Tauchcomputer. ⓘ
Der Dekompressionsplan kann aus Dekompressionstabellen, Dekompressionssoftware oder von Tauchcomputern abgeleitet werden. Diese basieren im Allgemeinen auf einem mathematischen Modell der Aufnahme und Abgabe von Inertgas durch den Körper bei Druckänderungen. Diese Modelle, wie z. B. der Bühlmann-Dekompressionsalgorithmus, werden an empirische Daten angepasst und liefern einen Dekompressionsplan für eine bestimmte Tiefe und Tauchdauer unter Verwendung eines bestimmten Atemgasgemisches. ⓘ
Da Taucher nach einem Tauchgang an der Oberfläche immer noch einen Überschuss an Inertgas im Körper haben können, muss der Dekompressionsplan bei jedem weiteren Tauchgang, bevor dieser Überschuss beseitigt ist, modifiziert werden, um die Restgasbelastung des vorherigen Tauchgangs zu berücksichtigen. Dies führt zu einer kürzeren zulässigen Zeit unter Wasser ohne obligatorische Dekompressionsstopps oder zu einer längeren Dekompressionszeit während des nachfolgenden Tauchgangs. Der vollständige Abbau des überschüssigen Gases kann viele Stunden dauern, und in den Tabellen ist die erforderliche Zeit bei normalen Drücken angegeben, die bis zu 18 Stunden betragen kann. ⓘ
Die Dekompressionszeit kann erheblich verkürzt werden, wenn während der Dekompressionsphase des Tauchgangs Gemische mit einem wesentlich geringeren Inertgasanteil geatmet werden (oder reiner Sauerstoff bei Stopps in 6 m Wassertiefe oder weniger). Der Grund dafür ist, dass das Inertgas proportional zur Differenz zwischen dem Partialdruck des Inertgases im Körper des Tauchers und dem Partialdruck im Atemgas ausgast, während die Wahrscheinlichkeit der Blasenbildung von der Differenz zwischen dem Partialdruck des Inertgases im Körper des Tauchers und dem Umgebungsdruck abhängt. Eine Verringerung der Dekompressionsanforderungen kann auch durch das Atmen eines Nitroxgemisches während des Tauchgangs erreicht werden, da weniger Stickstoff in den Körper aufgenommen wird als bei demselben Tauchgang mit Luft. ⓘ
Die Einhaltung eines Dekompressionsplans bietet keinen vollständigen Schutz vor DCS. Die verwendeten Algorithmen sind so konzipiert, dass sie die Wahrscheinlichkeit einer DCS auf ein sehr niedriges Niveau reduzieren, sie aber nicht auf Null reduzieren. Die mathematischen Implikationen aller aktuellen Dekompressionsmodelle besagen, dass längere Dekompressionsstopps das Dekompressionsrisiko verringern oder schlimmstenfalls nicht erhöhen, vorausgesetzt, dass kein Gewebe ingasiert wird. Eine effiziente Dekompression setzt voraus, dass der Taucher schnell genug aufsteigt, um in möglichst vielen Geweben einen möglichst hohen Dekompressionsgradienten zu erzeugen, ohne die Entwicklung symptomatischer Blasen zu provozieren. Dies wird durch den höchsten akzeptabel sicheren Sauerstoffpartialdruck im Atemgas und die Vermeidung von Gaswechseln, die zur Bildung oder zum Wachstum von Gegendiffusionsblasen führen könnten, erleichtert. Die Entwicklung von Plänen, die sowohl sicher als auch effizient sind, wird durch eine große Anzahl von Variablen und Ungewissheiten erschwert, einschließlich der individuellen Schwankungen in der Reaktion auf unterschiedliche Umgebungsbedingungen und Arbeitsbelastungen, die auf unterschiedliche Körpertypen, Fitness und andere Risikofaktoren zurückzuführen sind. ⓘ
Exposition in der Höhe
Einer der bedeutendsten Durchbrüche bei der Prävention von DCS in der Höhe ist die Sauerstoffvorbeatmung. Das Einatmen von reinem Sauerstoff verringert die Stickstoffbelastung in den Körpergeweben erheblich, indem der Stickstoffpartialdruck in der Lunge gesenkt wird, was zur Diffusion von Stickstoff aus dem Blut in das Atemgas führt, und dieser Effekt senkt schließlich die Stickstoffkonzentration in den anderen Körpergeweben. Wenn dies lange genug und ohne Unterbrechung fortgesetzt wird, bietet dies einen wirksamen Schutz, wenn man einer Umgebung mit niedrigem barometrischen Druck ausgesetzt ist. Das Atmen von reinem Sauerstoff allein während des Fluges (Aufstieg, Flugstrecke, Abstieg) verringert jedoch nicht das Risiko einer Höhen-DCS, da die für den Aufstieg benötigte Zeit im Allgemeinen nicht ausreicht, um die langsameren Gewebe deutlich zu entsättigen. ⓘ
Reiner Fliegersauerstoff, dem die Feuchtigkeit entzogen wurde, um ein Einfrieren der Ventile in der Höhe zu verhindern, ist leicht erhältlich und wird in der allgemeinen Luftfahrt bei Bergflügen und in großen Höhen routinemäßig verwendet. Die meisten kleinen Flugzeuge der allgemeinen Luftfahrt sind nicht druckbeaufschlagt, daher ist die Verwendung von Sauerstoff in größeren Höhen eine FAA-Vorschrift. ⓘ
Obwohl die Vorbeatmung mit reinem Sauerstoff eine wirksame Methode zum Schutz vor DCS in der Höhe ist, ist sie für den Schutz von Fluggästen der zivilen Luftfahrt, ob gewerblich oder privat, logistisch kompliziert und teuer. Daher wird sie derzeit nur von militärischen Flugbesatzungen und Astronauten zum Schutz in großen Höhen und bei Weltraumeinsätzen verwendet. Er wird auch von Flugtestteams verwendet, die an der Zulassung von Flugzeugen beteiligt sind, und kann auch für Fallschirmsprünge in großer Höhe eingesetzt werden. ⓘ
Astronauten an Bord der Internationalen Raumstation, die sich auf eine Außenbordaktivität (EVA) vorbereiten, verbringen vor ihrem Weltraumspaziergang acht Schlafstunden in der Quest-Luftschleuse bei niedrigem Atmosphärendruck, d. h. bei 0,70 bar (10,2 psi). Während der EVA atmen sie 100 % Sauerstoff in ihren Raumanzügen, die mit einem Druck von 0,30 bar (4,3 psi) arbeiten. Allerdings wurde in der Forschung die Möglichkeit untersucht, 100 % O2 bei 0,66 bar (9,5 psi) in den Anzügen zu verwenden, um den Druckabfall und damit das Risiko von DCS zu verringern. ⓘ
Behandlung


Alle Fälle von Dekompressionskrankheit sollten zunächst mit der höchsten verfügbaren Sauerstoffkonzentration behandelt werden, bis eine hyperbare Sauerstofftherapie (100 % Sauerstoff in einer Überdruckkammer) durchgeführt werden kann. Leichte Fälle von Dekompressionskrankheit und einige Hautsymptome können beim Abstieg aus großer Höhe verschwinden; es wird jedoch empfohlen, diese Fälle dennoch zu untersuchen. Neurologische Symptome, Lungensymptome und fleckige oder marmorierte Hautläsionen sollten mit hyperbarer Sauerstofftherapie behandelt werden, wenn sie innerhalb von 10 bis 14 Tagen nach ihrer Entstehung auftreten. ⓘ
Die Rekompression an Luft wurde 1909 von Keays als wirksame Behandlung für leichte DCS-Symptome nachgewiesen. Der Beweis für die Wirksamkeit der Rekompressionstherapie mit Sauerstoff wurde erstmals von Yarbrough und Behnke erbracht und ist seitdem zum Standard für die Behandlung von DCS geworden. Die Rekompression wird normalerweise in einer Rekompressionskammer durchgeführt. An einem Tauchplatz ist die Rekompression im Wasser eine riskantere Alternative. ⓘ
Die Erste Hilfe mit Sauerstoff wird seit Jahren als Notfallbehandlung für Tauchverletzungen eingesetzt. Wird sie innerhalb der ersten vier Stunden nach dem Auftauchen verabreicht, erhöht sie den Erfolg der Rekompressionstherapie und verringert die Anzahl der erforderlichen Rekompressionsbehandlungen. Die meisten Kreislauftauchgeräte können dauerhaft hohe Konzentrationen von sauerstoffreichem Atemgas abgeben und könnten als Mittel zur Sauerstoffversorgung eingesetzt werden, wenn keine spezielle Ausrüstung zur Verfügung steht. ⓘ
Die Verabreichung von Flüssigkeit ist von Vorteil, da sie dazu beiträgt, die Dehydrierung zu verringern. Es wird nicht mehr empfohlen, Aspirin zu verabreichen, es sei denn, das medizinische Personal rät dazu, da Analgetika die Symptome überdecken können. Die Betroffenen sollten es sich bequem machen und in die Rückenlage (waagerecht) oder in die Aufstehposition gebracht werden, wenn Erbrechen auftritt. In der Vergangenheit wurden sowohl die Trendelenburg-Lage als auch die linksseitige Dekubitus-Lage (Durant-Manöver) bei Verdacht auf eine Luftembolie als vorteilhaft vorgeschlagen, werden aber aufgrund von Bedenken hinsichtlich eines Hirnödems nicht mehr für längere Zeit empfohlen. ⓘ
Die Dauer der Rekompressionsbehandlung hängt von der Schwere der Symptome, der Tauchvorgeschichte, der Art der angewandten Rekompressionstherapie und dem Ansprechen des Patienten auf die Behandlung ab. Eines der am häufigsten verwendeten Behandlungsschemata ist die Tabelle 6 der US Navy, die eine hyperbare Sauerstofftherapie mit einem maximalen Druck, der 18 m (60 Fuß) Meerwasser (2,8 bar PO2) entspricht, für eine Gesamtzeit unter Druck von 288 Minuten vorsieht, von denen 240 Minuten mit Sauerstoff und die restliche Zeit mit Luftpausen verbracht werden, um die Möglichkeit einer Sauerstofftoxizität zu minimieren. ⓘ
Eine Mehrplatzkammer ist die bevorzugte Einrichtung für die Behandlung der Dekompressionskrankheit, da sie dem medizinischen Personal einen direkten physischen Zugang zum Patienten ermöglicht. Einplatzkammern sind jedoch in größerem Umfang verfügbar und sollten für die Behandlung verwendet werden, wenn keine Mehrplatzkammer verfügbar ist oder der Transport zu einer erheblichen Verzögerung der Behandlung führen würde, da die Zeitspanne zwischen dem Auftreten der Symptome und der Rekompression für die Qualität der Erholung wichtig ist. Es kann notwendig sein, den optimalen Behandlungsplan zu ändern, um die Verwendung einer Einplatzkammer zu ermöglichen, aber dies ist in der Regel besser als eine Verzögerung der Behandlung. Der US-Navy-Behandlungstisch 5 kann sicher ohne Luftpausen durchgeführt werden, wenn kein eingebautes Atmungssystem zur Verfügung steht. In den meisten Fällen kann der Patient im aufnehmenden Krankenhaus in einer Monoplace-Kammer angemessen behandelt werden. ⓘ
Prognose
Eine sofortige Behandlung mit 100 % Sauerstoff, gefolgt von einer Rekompression in einer Überdruckkammer, hat in den meisten Fällen keine langfristigen Auswirkungen. Dauerhafte Langzeitschäden durch DCS sind jedoch möglich. Eine dreimonatige Nachuntersuchung von Tauchunfällen, die der DAN 1987 gemeldet wurden, ergab, dass 14,3 % der 268 befragten Taucher anhaltende Symptome einer DCS vom Typ II und 7 % eine DCS vom Typ I aufwiesen. Langfristige Nachuntersuchungen ergaben ähnliche Ergebnisse, wobei 16 % bleibende neurologische Folgen aufwiesen. ⓘ
Langfristige Auswirkungen hängen sowohl von der ursprünglichen Verletzung als auch von der Behandlung ab. Während fast alle Fälle mit einer Behandlung schneller abklingen, können sich leichtere Fälle mit der Zeit ohne Rekompression adäquat zurückbilden, wenn die Schädigung geringfügig ist und sich der Schaden durch eine fehlende Behandlung nicht wesentlich verschlimmert. In einigen Fällen kann es aufgrund der Kosten, der Unannehmlichkeiten und des Risikos für den Patienten sinnvoll sein, sich nicht in eine hyperbare Behandlungseinrichtung zu begeben. Diese Fälle sollten von einem Spezialisten für Tauchmedizin beurteilt werden, was im Allgemeinen per Telefon oder Internet möglich ist. ⓘ
Bei Gelenkschmerzen hängt es von den Symptomen ab, welche Gewebe wahrscheinlich betroffen sind, und die Dringlichkeit einer hyperbaren Behandlung hängt weitgehend von den betroffenen Geweben ab.
- Scharfe, örtlich begrenzte Schmerzen, die durch Bewegung beeinträchtigt werden, lassen auf eine Sehnen- oder Muskelverletzung schließen, die in der Regel mit Sauerstoff und entzündungshemmenden Medikamenten vollständig verschwinden.
- Scharfe, örtlich begrenzte Schmerzen, die durch Bewegung nicht beeinträchtigt werden, deuten auf eine lokale Entzündung hin, die in der Regel ebenfalls mit Sauerstoff und entzündungshemmenden Medikamenten vollständig abklingt.
- Tiefe, nicht lokalisierte Schmerzen, die durch Bewegung beeinträchtigt werden, deuten auf eine Verspannung der Gelenkkapsel hin, die wahrscheinlich mit Sauerstoff und entzündungshemmenden Medikamenten vollständig verschwindet, obwohl eine Rekompression zu einer schnelleren Besserung beiträgt.
- Tiefe, nicht lokalisierte Schmerzen, die durch Bewegung nicht beeinträchtigt werden, deuten auf eine Beteiligung des Knochenmarks hin, mit Ischämie aufgrund von Blutgefäßverstopfung und Schwellungen im Knochen, die mechanistisch mit Osteonekrose in Verbindung stehen. ⓘ
Epidemiologie
Die Inzidenz der Dekompressionskrankheit ist selten und wird auf 2,8 bis 4 Fälle pro 10.000 Tauchgänge geschätzt, wobei das Risiko für Männer 2,6 Mal höher ist als für Frauen. Die Dekompressionskrankheit betrifft etwa 1.000 Taucher in den USA pro Jahr. Im Jahr 1999 rief das Divers Alert Network (DAN) das "Project Dive Exploration" ins Leben, um Daten über Tauchprofile und Zwischenfälle zu sammeln. Von 1998 bis 2002 wurden 50.150 Tauchgänge aufgezeichnet, bei denen 28 Rekompressionen erforderlich waren - obwohl diese mit ziemlicher Sicherheit Vorfälle von arteriellen Gasembolien (AGE) enthalten - eine Rate von etwa 0,05 %. ⓘ
Um das Jahr 2013 verzeichnete Honduras die höchste Zahl an dekompressionsbedingten Todesfällen und Behinderungen weltweit, verursacht durch unsichere Praktiken beim Hummer-Tauchen unter dem indigenen Volk der Miskito, das unter großem wirtschaftlichen Druck steht. Damals wurde geschätzt, dass in dem Land seit den 1970er Jahren über 2000 Taucher verletzt wurden und 300 weitere starben. ⓘ
Zeitleiste
- 1670: Robert Boyle wies nach, dass eine Verringerung des Umgebungsdrucks zur Blasenbildung in lebendem Gewebe führen kann. Diese Beschreibung einer Blasenbildung im Auge einer Viper, die einem Beinahe-Vakuum ausgesetzt war, war die erste aufgezeichnete Beschreibung der Dekompressionskrankheit.
- 1769: Giovanni Morgagni beschrieb den postmortalen Befund von Luft im Hirnkreislauf und vermutete, dass dies die Todesursache war.
- 1840: Charles Pasley, der an der Bergung des gesunkenen Kriegsschiffs HMS Royal George beteiligt war, bemerkte, dass von denjenigen, die häufig getaucht waren, "kein Mann den wiederholten Anfällen von Rheuma und Kälte entging".
- 1841: Der erste dokumentierte Fall von Dekompressionskrankheit wird von einem Bergbauingenieur gemeldet, der Schmerzen und Muskelkrämpfe bei Bergleuten beobachtete, die in Schächten arbeiteten, die unter Luftdruck standen, um Wasser fernzuhalten.
- 1854: Dekompressionskrankheit und ein Todesfall bei Caisson-Arbeitern auf der Royal Albert Bridge.
- 1867: Perlentaucher aus Panama, die das revolutionäre Tauchboot Sub Marine Explorer benutzten, erkrankten wiederholt an "Fieber" aufgrund des schnellen Aufstiegs. Die anhaltende Krankheit führte dazu, dass das Schiff 1869 aufgegeben wurde.
- 1870: Bauer veröffentlicht die Ergebnisse von 25 gelähmten Caisson-Arbeitern.
- Von 1870 bis 1910 wurden alle auffälligen Merkmale festgestellt. Zu den damaligen Erklärungen gehörten: Kälte oder Erschöpfung, die eine reflexartige Schädigung des Rückenmarks verursachten; Elektrizität durch Reibung bei der Kompression; oder Organstauung; und Gefäßstauung durch Dekompression.
- 1871: Die Eads-Brücke in St. Louis beschäftigte 352 Druckluftarbeiter, darunter Alphonse Jaminet als leitender Arzt. Es gab 30 Schwerverletzte und 12 Todesopfer. Jaminet erkrankte selbst an der Dekompressionskrankheit, und seine persönliche Beschreibung war die erste, über die berichtet wurde. Nach Angaben von Divers Alert Network in seinem Kurs Inertgasaustausch, Luftblasen und Dekompressionstheorie wurde der Begriff Dekompressionskrankheit (DCS) hier erstmals verwendet.
- 1872: Die Ähnlichkeit zwischen Dekompressionskrankheit und iatrogener Luftembolie sowie der Zusammenhang zwischen unzureichender Dekompression und Dekompressionskrankheit wurde von Friedburg festgestellt. Er vermutete, dass intravaskuläres Gas durch schnelle Dekompression freigesetzt wurde, und empfahl: langsame Kompression und Dekompression, vierstündige Arbeitsschichten, Begrenzung auf einen Maximaldruck von 44,1 psig (4 atm), Einsatz nur gesunder Arbeiter und Rekompressionsbehandlung bei schweren Fällen.
- 1873: Andrew Smith verwendet zum ersten Mal den Begriff "Caisson-Krankheit" und beschreibt damit 110 Fälle von Dekompressionskrankheit, die er als verantwortlicher Arzt während des Baus der Brooklyn Bridge beobachtete. Bei dem Projekt waren 600 Druckluftarbeiter beschäftigt. Eine Rekompressionsbehandlung wurde nicht durchgeführt. Der Chefingenieur des Projekts, Washington Roebling, erkrankte an der Caisson-Krankheit und litt für den Rest seines Lebens an den Nachwirkungen der Krankheit. Während dieses Projekts wurde die Dekompressionskrankheit unter dem Namen "The Grecian Bends" oder einfach "the bends" bekannt, weil sich die Betroffenen typischerweise in der Hüfte nach vorne beugten: Dies erinnert möglicherweise an eine damals beliebte Damenmode und Tanzbewegung, die als Grecian Bend bekannt war.
- 1890: Während des Baus des Hudson River Tunnels leistet der Bauunternehmer Ernest William Moir Pionierarbeit bei der Verwendung einer Schleusenkammer für die Behandlung.
- 1900: Leonard Hill wies anhand eines Froschmodells nach, dass Dekompression Blasen verursacht und dass Rekompression diese auflöst. Hill sprach sich für lineare oder gleichmäßige Dekompressionsprofile aus. Diese Art der Dekompression wird heute von Sättigungstauchern angewendet. Seine Arbeit wurde von Augustus Siebe und der Siebe Gorman Company finanziert.
- 1904: Der Tunnelbau zur und von der Insel Manhattan verursachte über 3.000 Verletzungen und über 30 Todesfälle, was zu Gesetzen führte, die PSI-Grenzwerte und Dekompressionsregeln für "Sandhogs" in den Vereinigten Staaten vorschrieben.
- 1904: Siebe und Gorman entwickelten und produzierten in Zusammenarbeit mit Leonard Hill eine geschlossene Glocke, in der ein Taucher an der Oberfläche dekomprimiert werden kann.
- 1908: "The Prevention of Compressed Air Illness" wird von JS Haldane, Boycott und Damant veröffentlicht, die eine gestaffelte Dekompression empfehlen. Diese Tabellen wurden von der Royal Navy übernommen.
- 1914-16: Experimentelle Dekompressionskammern werden an Land und an Bord von Schiffen eingesetzt.
- 1924: Die US Navy veröffentlicht das erste standardisierte Rekompressionsverfahren.
- 1930s: Albert R. Behnke unterscheidet die Symptome der Arteriellen Gasembolie (AGE) von denen der DCS.
- 1935: Behnke et al. experimentieren mit Sauerstoff für die Rekompressionstherapie.
- 1937: Behnke führt die "No-Stop"-Dekompressionstabellen ein.
- 1941: Höhen-DCS wird zum ersten Mal mit hyperbarem Sauerstoff behandelt.
- 1944: Die US Navy veröffentlicht die hyperbaren Behandlungstabellen "Long Air Recompression Table with Oxygen" und "Short Oxygen Recompression Table", die beide 100 % Sauerstoff unterhalb von 60 fsw (18 msw) verwenden.
- 1945: Die Ergebnisse aus der Praxis zeigen, dass die Sauerstoff-Behandlungstische von 1944 noch nicht zufriedenstellend sind. Daher führen Mitarbeiter des Navy Medical Research Institute und der Navy Experimental Diving Unit eine Reihe von Tests mit menschlichen Probanden durch, um die Behandlungstische zu überprüfen und zu modifizieren. Es wurden Tests mit der 100-Fuß-Luft-Sauerstoff-Behandlungstabelle und der 100-Fuß-Luft-Behandlungstabelle durchgeführt, die sich als zufriedenstellend erwiesen. Andere Tabellen wurden erweitert, bis sie zufriedenstellende Ergebnisse lieferten. Die daraus resultierenden Tabellen wurden für die nächsten 20 Jahre als Standardbehandlung verwendet, und diese Tabellen und leichte Abänderungen wurden von anderen Marinen und der Industrie übernommen. Im Laufe der Zeit häuften sich die Hinweise, dass der Erfolg dieser Tabellen bei schwerer Dekompressionskrankheit nicht sehr gut war.
- 1957: Robert Workman entwickelte eine neue Methode zur Berechnung der Dekompressionsanforderungen (M-Werte).
- 1959: Das "SOS Decompression Meter", ein mechanisches Tauchgerät, das die Aufnahme und Abgabe von Stickstoff simuliert, wird eingeführt.
- 1960: FC Golding et al. teilen die Klassifizierung von DCS in Typ 1 und 2 ein.
- 1965: Die geringen Erfolgsquoten der bestehenden Behandlungstabellen der US Navy führten 1965 zur Entwicklung der Sauerstoffbehandlungstabelle durch Goodman und Workman, die in verschiedenen Varianten immer noch als endgültige Behandlung für die meisten Fälle der Dekompressionskrankheit verwendet wird.
- 1965: LeMessurier und Hills veröffentlichen eine Abhandlung über einen thermodynamischen Ansatz, der sich aus einer Studie über Torres-Strait-Tauchtechniken ergibt und der nahelegt, dass die Dekompression nach herkömmlichen Modellen zu einer Blasenbildung führt, die dann durch die Wiederauflösung an den Dekompressionsstopps beseitigt wird.
- 1976 - M.P. Spencer zeigte, dass die Empfindlichkeit der Dekompressionstests durch den Einsatz von Ultraschallmethoden erhöht wird, die mobile venöse Blasen aufspüren können, bevor Symptome von DCS auftreten.
- 1982: Paul K. Weathersby, Louis D. Homer und Edward T. Flynn führen die Überlebensanalyse in die Untersuchung der Dekompressionskrankheit ein.
- 1983: Orca stellt den "EDGE" her, einen persönlichen Tauchcomputer, der mit einem Mikroprozessor die Stickstoffabsorption für zwölf Gewebekompartimente berechnet.
- 1984: Albert A. Bühlmann veröffentlicht sein Buch "Decompression-Decompression Sickness" (Dekompressionskrankheit), in dem er sein deterministisches Modell für die Berechnung von Dekompressionsplänen beschreibt. ⓘ
Gesellschaft und Kultur
Wirtschaft
In den Vereinigten Staaten ist es üblich, dass Krankenversicherungen die Behandlung von Taucherkrankheiten, die durch Sporttauchen verursacht werden, nicht übernehmen. Dies liegt daran, dass das Tauchen als freiwillige und "risikoreiche" Aktivität gilt und die Behandlung der Dekompressionskrankheit teuer ist. Ein typischer Aufenthalt in einer Rekompressionskammer kostet leicht mehrere Tausend Dollar, selbst wenn man den Notfalltransport mit einrechnet. Aus diesem Grund bieten Gruppen wie Divers Alert Network (DAN) Krankenversicherungen an, die speziell alle Aspekte der Behandlung der Dekompressionskrankheit zu Preisen von weniger als 100 Dollar pro Jahr abdecken. ⓘ
Im Vereinigten Königreich wird die Behandlung der Dekompressionskrankheit vom National Health Service übernommen. Sie kann entweder in einer spezialisierten Einrichtung oder in einem Hyperbariezentrum eines allgemeinen Krankenhauses erfolgen. ⓘ
Andere Tiere
Auch Tiere können an DCS erkranken, insbesondere solche, die in Netzen gefangen und schnell an die Oberfläche gebracht werden. Sie ist bei Unechten Karettschildkröten und wahrscheinlich auch bei prähistorischen Meerestieren nachgewiesen worden. Moderne Reptilien sind anfällig für DCS, und es gibt Hinweise darauf, dass auch Meeressäugetiere wie Wale und Robben betroffen sein können. AW Carlsen hat vorgeschlagen, dass das Vorhandensein eines Rechts-Links-Shunts im Herzen von Reptilien für die Veranlagung verantwortlich sein könnte, ähnlich wie ein offenes Foramen ovale beim Menschen. ⓘ
Begriffsbestimmung
Die Unterscheidung zwischen Dekompressionskrankheit (decompression illness, DCI) und Caissonkrankheit (decompression sickness, DCS) kommt in der deutschen Übersetzung der Begriffe „Illness“ und „Sickness“ kaum zum Ausdruck und wird auch nicht von allen Tauchmedizinern akzeptiert. Daneben wird in der Literatur DCI auch als Abkürzung für den Dekompressionsunfall (decompression incident, DCI) verwendet, der dann anhand der Entwicklung der Symptome weiter typisiert wird. ⓘ
Im Englischen wird die häufigste Form der Dekompressionskrankheit als decompression sickness (DCS) oder als decompression illness (DCI) bezeichnet. In großen Höhen (Bergseetauchen) ist die Gefahr durch den geringeren Atmosphärendruck größer. ⓘ
Um bei Astronauten die Gefahr einer Dekompressionskrankheit bei Weltraumausstiegen zu vermeiden, werden Astronauten vor dem Ausstieg durch eine Übernachtung bei vermindertem Druck an die Druckbedingungen angepasst. ⓘ
Der Überbegriff Dekompressionskrankheit umfasst die Schäden durch
- Gasblasenbildung durch überschüssiges Inertgas (meist Stickstoff, bei Spezialatemgasen auch Helium und Wasserstoff) = Caissonkrankheit oder Dekompressionskrankheit (DCS)
- Druckbedingter Einriss zentraler Lungengefäße mit darauf folgenden gasembolischen Verschlüssen (arterielle Gasblasenembolie, AGE) ⓘ
Die Bezeichnung Caissonkrankheit (Kastenkrankheit) kommt von den Senkkästen, die ab 1870 vermehrt zur Herstellung von Gründungen für Brückenpfeiler eingesetzt wurden. Im Gegensatz zu den bis dahin üblichen Taucherglocken ermöglichten diese eine wesentlich längere Arbeitszeit, die in der Folge zu einem sprunghaften Ansteigen der Fälle von Dekompressionskrankheit führte. ⓘ
Erste Hilfe, lebensrettende Sofortmaßnahmen und Therapie
- Alarmierung geeigneter Rettungsmittel (Taucharzt, Rettungsdienst)
- Wenn möglich, Gabe von reinem Sauerstoff
- Bei Bewusstlosigkeit: Stabile Seitenlage und ständige Kontrolle der Atmungs- und Kreislaufparameter
- Bei Atemstillstand und/oder Kreislaufstillstand: Herz-Lungen-Wiederbelebung
- Wärmeerhaltung (Rettungsdecke)
- Wenn Patient bewusstseinsklar:
- Rückenlage, ggf. Seitenlage (keine Schocklage, da dies die intrakranielle Druckerhöhung (Hirndruck) begünstigt)
- 500 bis 1000 ml Flüssigkeitszufuhr (ggf. Infusionstherapie mit kristallinen und kolloidalen Lösungen)
- Sicherstellung des Tauchcomputers und der restlichen Tauchausrüstung
- Druckkammerbehandlung mit hyperbarem Sauerstoff (Hyperbare Oxygenierung) (schnellstmögliche „Rekompression“ in einer Überdruckkrankenkammer) ⓘ
Eine Zusammenfassung über die initiale Notfallversorgung zeigt die Österreichische Wasserrettung in ihrem Tauchunfallmerkblatt. ⓘ
Vorbeugung und Risikofaktoren
Bei allen Tauchgängen sind die Aufstiegsgeschwindigkeiten sowie die Dekompressionsregeln zu beachten. In den Fällen, in denen es trotz Einhaltung dieser Regeln zu akuten DCI-Symptomen kam, lag meist ein oder mehrere der folgenden Risikofaktoren vor:
- Akute Infekte der oberen Luftwege (Erkältung oder allergisches Asthma)
- Tabakgenuss
- Dehydratation (z. B. durch akute Durchfallerkrankungen oder unzureichende Flüssigkeitsaufnahme)
- Fieber
- Alkoholgenuss
- Persistierendes Foramen ovale (PFO) – eine häufig vorkommende, aber oft unbemerkte Herzkrankheit (Vorkommen bei ca. 10–20 % der Menschen).
- Zuckerkrankheit
- höheres Alter
- Fettleibigkeit
- Stress
- Müdigkeit
- Muskelkater
- Bluthochdruck (Hypertonie)
- Unterkühlung (Hypothermie, z. B. wegen einer unzureichenden Wärmedämmung durch den Tauchanzug). ⓘ
Typisierung
Dekompressionskrankheit Typ II
Bei einer Dekompressionskrankheit vom Typ II manifestieren sich Blasen im Innenohr, dem Gehirn oder dem Rückenmark. Verschlüsse der Blutgefäße durch Gasblasen (Aeroembolismus) werden ebenfalls hier eingeordnet. ⓘ
Zentrale Gasembolien verursachen unmittelbar eine Bewusstseinstrübung, bisweilen auch Bewusstlosigkeit und Atemlähmung, wenn wichtige Gehirnbezirke ausfallen. Manchmal hat der Taucher zunächst eine Bewusstseinseintrübung, die erst später in eine vollständige Bewusstlosigkeit übergeht. Ebenso können Halbseitenlähmungen und isolierte Ausfälle der Extremitäten auftreten. ⓘ
Embolische Verschlüsse von Rückenmarksgefäßen können beidseitige Lähmungen und Empfindungsstörungen sowie, bei sakralen Segmenten, auch Harn- bzw. Mastdarmstörungen verursachen. Die nach zentralen Embolien auftretenden Symptome steigern sich oft von Missempfindungen bis hin zur vollständigen Lähmung zwei Stunden später. ⓘ
Innenohrembolien verursachen Brechreiz, Übelkeit, Ohrgeräusche und Schwindel bis hin zum Verlust des Lagesinnes. ⓘ
Eine Differenzierung zwischen DCS II und AGE (arterielle Gasembolie) ist dem Ersthelfer kaum möglich (AGE tritt unmittelbar auf). Die fehlende Unterscheidbarkeit ist aber aufgrund gleicher Erste-Hilfe-Maßnahmen zunächst nicht wesentlich. ⓘ
Dekompressionskrankheit Typ III
Langzeitschäden bei Tauchern werden unter Typ III zusammengefasst. Als Berufskrankheit anerkannt sind bisher die aseptische Knochennekrose (AON), Hörschädigungen, Netzhautschäden sowie neurologische Folgeschäden nicht behobener DCS Typ II. ⓘ
Ursache der Skeletterkrankungen und Gelenkveränderungen sind durch die langfristige Aufsättigung dieser Gewebe begründet. Hier reichen die Tauchpausen nicht aus, um diese langsamen Gewebe vollständig entsättigen zu können. Ebenfalls stehen Mikroblasen in Verdacht, die bei Berufstauchern in der Zeit zwischen Auftauchen und Aufsuchen der Dekompressionskammer entstehen. Diese Blasen bleiben durch die Rekompression „stumm“, führen aber möglicherweise zu Langzeitschäden. ⓘ
Es sind aber auch Schäden dieser Art bei einmaliger, aber sehr langer Druckexposition berichtet worden (U-Boot-Fahrer eines 1931 gesunkenen U-Bootes, die vor ihrer Rettung sehr lange unter Druck (36,5 m) standen und bei denen 12 Jahre später AON festgestellt wurde). ⓘ
Lungenüberdruckunfall AGE (arterielle Gasembolie)
Bei einem zentralen Lungenriss gewinnt die Alveolarluft durch die Verletzung des blutreichen Gewebes der Lunge Zugang zum Gefäßsystem. Es kommt zum Übertritt der Atmungsluft in die Lungenvenen. Die Luftblasen rufen dann nach Passage durch die linke Herzkammer embolische Verschlüsse in den Endarterien des Rückenmarks, des Gehirns oder auch der Herzkranzgefäße hervor. Symptome ansonsten wie bei DCS II. ⓘ

