Kolloid
| Physik der kondensierten Materie ⓘ |
|---|
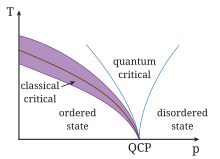 |
| Phasen - Phasenübergang - QCP |
|
Ein Kolloid ist ein Gemisch, in dem ein Stoff, der aus mikroskopisch dispergierten unlöslichen Teilchen besteht, in einem anderen Stoff suspendiert ist. Einige Definitionen legen fest, dass die Teilchen in einer Flüssigkeit dispergiert sein müssen, während andere die Definition auf Stoffe wie Aerosole und Gele ausweiten. Der Begriff kolloidale Suspension bezieht sich eindeutig auf das Gesamtgemisch (obwohl sich eine engere Bedeutung des Wortes Suspension von Kolloiden durch eine größere Teilchengröße unterscheidet). Ein Kolloid hat eine dispergierte Phase (die suspendierten Teilchen) und eine kontinuierliche Phase (das Medium der Suspension). Die Teilchen der dispergierten Phase haben einen Durchmesser von etwa 1 Nanometer bis 1 Mikrometer. ⓘ
Einige Kolloide sind aufgrund des Tyndall-Effekts, d. h. der Streuung des Lichts an den Teilchen im Kolloid, durchscheinend. Andere Kolloide können undurchsichtig sein oder eine leichte Färbung aufweisen. ⓘ
Kolloidale Suspensionen sind das Thema der Grenzflächen- und Kolloidwissenschaften. Dieses Forschungsgebiet wurde 1845 vom italienischen Chemiker Francesco Selmi eingeführt und seit 1861 vom schottischen Wissenschaftler Thomas Graham weiter erforscht.
Kolloid: Kurzes Synonym für kolloidales System.
Kolloidal: Zustand der Unterteilung, bei dem die in einem Medium dispergierten Moleküle oder polymolekularen Teilchen mindestens eine Dimension zwischen etwa 1 nm und 1 μm aufweisen, oder bei dem in einem System Diskontinuitäten in Abständen dieser Größenordnung auftreten. ⓘ
Als Kolloide (von altgriechisch κόλλα kólla „Leim“ und εἶδος eidos „Form, Aussehen“) oder Kolloiddispersion werden Teilchen oder Tröpfchen bezeichnet, die im Dispersionsmedium (Feststoff, Gas oder Flüssigkeit) fein verteilt sind. Die Größe der einzelnen Teilchen liegt im Bereich von einem Nanometer bis zu einem Mikrometer. ⓘ
In diesem Größenbereich liegen viele Moleküle sowie die meisten Viren. ⓘ
Neben der Größe der Teilchen ist auch ihre gleichmäßige Verteilung für ein kolloidales System kennzeichnend, die sich nicht oder nur langsam ändert. Sind die Teilchen beweglich (etwa in einem flüssigen Dispersionsmedium), so zeigen sie Brownsche Bewegung. ⓘ
Je nach Bindungsart zwischen den Atomen der Kolloide können unterschieden werden:
- Dispersionskolloide enthalten Teilchen, die durch Zerkleinerung, Kondensation oder Peptisation von beliebigen (lyophoben) Stoffen entstanden sind, die sich nicht im Dispersionsmedium lösen, z. B. Tonkolloid in Wasser. Eine elektrostatische oder sterische Stabilisierung mit Schutzkolloiden ist notwendig, um eine Auflösung oder Aggregation zu verhindern. Ein thermodynamisches Gleichgewicht liegt nicht vor.
- Molekülkolloide enthalten Teilchen die typischerweise aus etwa 100 Atomen bestehen, die über Hauptvalenzen gebunden sind. Beispiele sind Heteropolysäuren, Polysaccharide und Polyphosphate. Der Aufbau entspricht niedermolekularen Substanzen.
- Assoziationskolloide/ Mizellkolloide enthalten Mizellen, die sich ab einer bestimmten Massenkonzentration selbsttätig, d. h. ohne Mitwirkung von Schutzkolloiden oder Peptisatoren, bilden. Beispiele sind Seifen, Tenside und manche Farbstoffe. ⓘ
Kolloidale Suspensionen haben große Bedeutung in der Nahrungsmittel- und Kosmetikindustrie und in der Grundlagenforschung, insbesondere in der statistischen Physik. Die Kolloidchemie ist der Bereich der Chemie, der sich mit ihren stofflichen Eigenschaften befasst. ⓘ
Einteilung
Kolloide können wie folgt klassifiziert werden:
| Medium/Phase | Dispergierte Phase ⓘ | |||
|---|---|---|---|---|
| Gas | Flüssigkeit | Fest | ||
| Dispersion Medium |
Gas | Es sind keine solchen Kolloide bekannt. Es ist bekannt, dass Helium und Xenon unter bestimmten Bedingungen nicht mischbar sind. |
Flüssiges Aerosol Beispiele: Nebel, Wolken, Kondensation, Dunst, Dampf, Haarspray |
Festes Aerosol Beispiele: Rauch, Eiswolke, atmosphärischer Feinstaub |
| Flüssigkeit | Schaum Beispiel: Schlagsahne, Rasierschaum |
Emulsion oder Flüssigkristall Beispiele: Milch, Mayonnaise, Handcreme, Latex, biologische Membranen, flüssiges biomolekulares Kondensat |
Sol Beispiele: pigmentierte Tinte, Sediment, Präzipitate, festes biomolekulares Kondensat | |
| Fest | Fester Schaum Beispiele: Aerogel, Styropor, Bimsstein |
Gel Beispiele: Agar, Gelatine, Gelee, gelartiges biomolekulares Kondensat |
Festes Sol Beispiel: Cranberry-Glas | |
Homogene Gemische mit einer dispergierten Phase in diesem Größenbereich können als kolloidale Aerosole, kolloidale Emulsionen, kolloidale Suspensionen, kolloidale Schäume, kolloidale Dispersionen oder Hydrosole bezeichnet werden. ⓘ
Hydrokolloide
Als Hydrokolloide werden bestimmte Chemikalien (meist Polysaccharide und Proteine) bezeichnet, die in Wasser kolloidal dispergierbar sind. Dadurch werden sie effektiv "löslich" und verändern die Rheologie des Wassers, indem sie die Viskosität erhöhen und/oder eine Gelierung bewirken. Sie können auch mit anderen Chemikalien interagieren, in einigen Fällen synergistisch, in anderen antagonistisch. Mit diesen Eigenschaften sind Hydrokolloide sehr nützliche Chemikalien, da sie in vielen Bereichen der Technik - von Lebensmitteln über Arzneimittel und Körperpflegemittel bis hin zu industriellen Anwendungen - für Stabilisierung, Destabilisierung und Trennung, Gelierung, Fließkontrolle, Kristallisationskontrolle und zahlreiche andere Effekte sorgen können. Neben der Verwendung der löslichen Formen haben einige Hydrokolloide zusätzliche nützliche Funktionen in trockener Form, wenn ihnen nach der Solubilisierung das Wasser entzogen wird - wie bei der Bildung von Filmen für Atemstreifen oder Wursthüllen oder auch Wundverbandfasern, von denen einige besser mit der Haut verträglich sind als andere. Es gibt viele verschiedene Arten von Hydrokolloiden, die sich in ihrer Struktur, ihrer Funktion und ihrem Nutzen unterscheiden und sich im Allgemeinen am besten für bestimmte Anwendungsbereiche zur Steuerung der Rheologie und zur physikalischen Veränderung von Form und Textur eignen. Einige Hydrokolloide wie Stärke und Kasein sind sowohl als Lebensmittel als auch als Rheologiemodifikatoren nützlich, andere haben nur einen begrenzten Nährwert und dienen gewöhnlich als Ballaststoffquelle. ⓘ
Der Begriff Hydrokolloide bezieht sich auch auf eine Art von Verband, der die Feuchtigkeit in der Haut speichern und den natürlichen Heilungsprozess der Haut unterstützen soll, um Narbenbildung, Juckreiz und Wundsein zu verringern. ⓘ
Bestandteile
Hydrokolloide enthalten eine Art von Gelbildner, z. B. Natriumcarboxymethylcellulose (NaCMC) und Gelatine. Sie werden in der Regel mit einer Art Versiegelung, z. B. Polyurethan, kombiniert, um auf der Haut zu "haften". ⓘ
Kolloid im Vergleich zur Lösung
Ein Kolloid hat eine dispergierte Phase und eine kontinuierliche Phase, während in einer Lösung der gelöste Stoff und das Lösungsmittel nur eine Phase bilden. Bei einem gelösten Stoff in einer Lösung handelt es sich um einzelne Moleküle oder Ionen, während kolloidale Partikel größer sind. In einer Salzlösung in Wasser zum Beispiel löst sich der Natriumchlorid (NaCl)-Kristall auf, und die Na+- und Cl- Ionen sind von Wassermolekülen umgeben. In einem Kolloid wie Milch bestehen die kolloidalen Teilchen jedoch aus Fettkügelchen und nicht aus einzelnen Fettmolekülen. Da ein Kolloid aus mehreren Phasen besteht, hat es ganz andere Eigenschaften als eine vollständig gemischte, kontinuierliche Lösung. ⓘ
Wechselwirkung zwischen den Teilchen
Die folgenden Kräfte spielen bei der Wechselwirkung von Kolloidteilchen eine wichtige Rolle:
- Ausgeschlossene Volumenabstoßung: Dies bezieht sich auf die Unmöglichkeit einer Überlappung zwischen harten Teilchen.
- Elektrostatische Wechselwirkung: Kolloidale Teilchen tragen oft eine elektrische Ladung und ziehen sich daher gegenseitig an oder stoßen sich ab. Die Ladung sowohl der kontinuierlichen als auch der dispergierten Phase sowie die Mobilität der Phasen sind Faktoren, die diese Wechselwirkung beeinflussen.
- Van-der-Waals-Kräfte: Dies ist auf die Wechselwirkung zwischen zwei Dipolen zurückzuführen, die entweder permanent oder induziert sind. Selbst wenn die Teilchen keinen permanenten Dipol haben, führen Fluktuationen der Elektronendichte zu einem temporären Dipol in einem Teilchen. Dieser temporäre Dipol induziert einen Dipol in benachbarten Teilchen. Der temporäre Dipol und die induzierten Dipole ziehen sich dann gegenseitig an. Diese als van-der-Waals-Kraft bezeichnete Kraft ist immer vorhanden (es sei denn, die Brechungsindizes der dispergierten und der kontinuierlichen Phase stimmen überein), hat eine kurze Reichweite und ist attraktiv.
- Sterische Kräfte zwischen polymerbedeckten Oberflächen oder in Lösungen, die nicht adsorbierende Polymere enthalten, können die Kräfte zwischen den Partikeln modulieren und eine zusätzliche sterische Abstoßungskraft (die überwiegend entropischen Ursprungs ist) oder eine anziehende Verarmungskraft zwischen ihnen erzeugen. ⓘ
Sedimentationsgeschwindigkeit

Das Gravitationsfeld der Erde wirkt auf die kolloidalen Teilchen ein. Wenn die kolloidalen Teilchen dichter sind als das Suspensionsmedium, sedimentieren sie (fallen auf den Boden), wenn sie weniger dicht sind, cremen sie (schwimmen nach oben). Größere Partikel neigen auch eher zur Sedimentation, weil sie eine geringere Brownsche Bewegung haben, die dieser Bewegung entgegenwirkt. ⓘ
Die Sedimentations- oder Rahmungsgeschwindigkeit wird durch Gleichsetzung der Stokes'schen Widerstandskraft mit der Gravitationskraft ermittelt: ⓘ
wobei ⓘ
das archimedische Gewicht der kolloidalen Teilchen ist, ⓘ
die Viskosität des Suspensionsmediums ist, ⓘ
der Radius der kolloidalen Teilchen ist, ⓘ
und die Sedimentations- oder Aufrahmungsgeschwindigkeit ist. ⓘ
Die Masse des kolloidalen Partikels wird ermittelt durch: ⓘ
wobei ⓘ
ist das Volumen des kolloidalen Teilchens, berechnet anhand des Volumens einer Kugel , ⓘ
und ist der Unterschied in der Massendichte zwischen dem kolloidalen Teilchen und dem Suspensionsmedium. ⓘ
Durch Umstellen ergibt sich die Sedimentations- oder Aufrahmgeschwindigkeit: ⓘ
Es gibt eine obere Größengrenze für den Durchmesser der kolloidalen Teilchen, da Teilchen, die größer als 1 μm sind, zur Sedimentation neigen, so dass die Substanz nicht mehr als kolloidale Suspension betrachtet werden kann. ⓘ
Die kolloidalen Teilchen befinden sich im Sedimentationsgleichgewicht, wenn die Sedimentationsrate gleich der Bewegungsrate der Brownschen Bewegung ist. ⓘ
Herstellung
Es gibt zwei Hauptmethoden zur Herstellung von Kolloiden:
- Dispersion großer Partikel oder Tröpfchen auf die kolloidale Größe durch Mahlen, Sprühen oder Anwendung von Scherkräften (z. B. Schütteln, Mischen oder Mischen unter hoher Scherung).
- Kondensation kleiner gelöster Moleküle zu größeren kolloidalen Partikeln durch Ausfällung, Kondensation oder Redoxreaktionen. Solche Verfahren werden bei der Herstellung von kolloidalem Siliziumdioxid oder Gold eingesetzt. ⓘ
Stabilisierung
Die Stabilität eines kolloidalen Systems wird dadurch definiert, dass die Teilchen in der Lösung suspendiert bleiben, und hängt von den Wechselwirkungskräften zwischen den Teilchen ab. Dazu gehören elektrostatische Wechselwirkungen und van-der-Waals-Kräfte, da beide zur gesamten freien Energie des Systems beitragen. ⓘ
Ein Kolloid ist stabil, wenn die Wechselwirkungsenergie aufgrund von Anziehungskräften zwischen den kolloidalen Teilchen kleiner als kT ist, wobei k die Boltzmann-Konstante und T die absolute Temperatur ist. Ist dies der Fall, stoßen sich die Kolloidteilchen ab oder ziehen sich nur schwach an, und die Substanz bleibt eine Suspension. ⓘ
Ist die Wechselwirkungsenergie größer als kT, überwiegen die Anziehungskräfte, und die kolloidalen Teilchen beginnen zu verklumpen. Dieser Vorgang wird allgemein als Aggregation bezeichnet, aber auch als Flockung, Koagulation oder Ausfällung. Diese Begriffe werden zwar häufig synonym verwendet, haben aber für einige Definitionen eine leicht unterschiedliche Bedeutung. Mit Koagulation kann beispielsweise eine irreversible, dauerhafte Aggregation bezeichnet werden, bei der die Kräfte, die die Teilchen zusammenhalten, stärker sind als die durch Rühren oder Mischen verursachten äußeren Kräfte. Mit Flockung kann eine reversible Aggregation beschrieben werden, bei der schwächere Anziehungskräfte wirken, und das Aggregat wird gewöhnlich als Flocken bezeichnet. Der Begriff Fällung ist in der Regel für die Beschreibung eines Phasenwechsels von einer kolloidalen Dispersion zu einem Feststoff (Präzipitat) reserviert, wenn dieser einer Störung unterworfen wird. Die Aggregation führt zu Sedimentation oder Aufrahmung, daher ist das Kolloid instabil: Wenn einer dieser Prozesse eintritt, ist das Kolloid keine Suspension mehr.

Elektrostatische Stabilisierung und sterische Stabilisierung sind die beiden wichtigsten Mechanismen zur Stabilisierung gegen Aggregation.
- Die elektrostatische Stabilisierung beruht auf der gegenseitigen Abstoßung gleicher elektrischer Ladungen. Die Ladung der kolloidalen Teilchen ist in einer elektrischen Doppelschicht strukturiert, wobei die Teilchen an der Oberfläche geladen sind, dann aber Gegenionen (Ionen mit entgegengesetzter Ladung) anziehen, die das Teilchen umgeben. Die elektrostatische Abstoßung zwischen suspendierten kolloidalen Teilchen lässt sich am einfachsten anhand des Zetapotenzials quantifizieren. Die kombinierte Wirkung von Van-der-Waals-Anziehung und elektrostatischer Abstoßung auf die Aggregation wird durch die DLVO-Theorie quantitativ beschrieben. Eine gängige Methode zur Stabilisierung eines Kolloids (d. h. zur Umwandlung in einen Niederschlag) ist die Peptisierung, ein Verfahren, bei dem das Kolloid mit einem Elektrolyten geschüttelt wird.
- Die sterische Stabilisierung besteht darin, eine Schicht eines Polymers oder eines Tensids auf den Partikeln zu absorbieren, um zu verhindern, dass sie sich im Bereich der Anziehungskräfte annähern. Das Polymer besteht aus Ketten, die an der Partikeloberfläche befestigt sind, und der Teil der Kette, der sich nach außen erstreckt, ist im Suspensionsmedium löslich. Diese Technik wird zur Stabilisierung von kolloidalen Partikeln in allen Arten von Lösungsmitteln, einschließlich organischer Lösungsmittel, eingesetzt.
Auch eine Kombination der beiden Mechanismen ist möglich (elektrosterische Stabilisierung). ⓘ
Eine Methode, die als Gel-Netzwerk-Stabilisierung bezeichnet wird, ist die wichtigste Methode zur Herstellung von Kolloiden, die sowohl gegen Aggregation als auch gegen Sedimentation stabil sind. Bei dieser Methode wird der kolloidalen Suspension ein Polymer zugesetzt, das ein Gelnetzwerk bilden kann. Das Absetzen der Partikel wird durch die Steifigkeit der Polymermatrix behindert, in der die Partikel eingeschlossen sind, und die langen Polymerketten können eine sterische oder elektrosterische Stabilisierung der dispergierten Partikel bewirken. Beispiele für solche Stoffe sind Xanthan und Guarkernmehl. ⓘ
Destabilisierung
Die Destabilisierung kann durch verschiedene Methoden erreicht werden:
- Beseitigung der elektrostatischen Barriere, die die Aggregation der Teilchen verhindert. Dies kann durch die Zugabe von Salz zu einer Suspension erreicht werden, um die Debye-Sieblänge (die Breite der elektrischen Doppelschicht) der Teilchen zu verringern. Außerdem kann der pH-Wert einer Suspension verändert werden, um die Oberflächenladung der Partikel in der Suspension effektiv zu neutralisieren. Dadurch werden die abstoßenden Kräfte, die die kolloidalen Teilchen voneinander trennen, aufgehoben und die Aggregation aufgrund von van der Waals-Kräften ermöglicht. Geringfügige Änderungen des pH-Werts können sich in einer erheblichen Veränderung des Zetapotenzials niederschlagen. Wenn die Größe des Zetapotenzials unter einem bestimmten Schwellenwert liegt, in der Regel bei ± 5 mV, kommt es zu einer schnellen Koagulation oder Aggregation.
- Zugabe eines geladenen Polymerflockungsmittels. Polymerflockungsmittel können einzelne kolloidale Teilchen durch attraktive elektrostatische Wechselwirkungen verbinden. So können z. B. negativ geladene kolloidale Kieselsäure- oder Tonpartikel durch die Zugabe eines positiv geladenen Polymers ausgeflockt werden.
- Zugabe von nicht adsorbierten Polymeren, so genannten Verarmungsmitteln, die aufgrund entropischer Effekte zur Aggregation führen. ⓘ
Instabile kolloidale Suspensionen mit geringem Volumenanteil bilden geclusterte flüssige Suspensionen, in denen einzelne Teilchencluster sedimentieren, wenn sie eine höhere Dichte als das Suspensionsmedium aufweisen, oder cremen, wenn sie eine geringere Dichte haben. Kolloidale Suspensionen mit höherem Volumenanteil hingegen bilden kolloidale Gele mit viskoelastischen Eigenschaften. Viskoelastische kolloidale Gele, wie Bentonit und Zahnpasta, fließen unter Scherung wie Flüssigkeiten, behalten aber ihre Form, wenn die Scherung aufgehoben wird. Aus diesem Grund lässt sich Zahnpasta aus einer Zahnpastatube herausdrücken, bleibt aber nach dem Auftragen auf der Zahnbürste. ⓘ
Überwachung der Stabilität

Die am weitesten verbreitete Technik zur Überwachung des Dispersionszustands eines Produkts und zur Identifizierung und Quantifizierung von Destabilisierungsphänomenen ist die Mehrfachlichtstreuung in Verbindung mit der vertikalen Abtastung. Diese als Turbidimetrie bezeichnete Methode basiert auf der Messung des Anteils des Lichts, der nach dem Durchgang durch die Probe von den kolloidalen Partikeln zurückgestreut wird. Die Rückstreuungsintensität ist direkt proportional zur durchschnittlichen Partikelgröße und zum Volumenanteil der dispergierten Phase. Daher werden lokale Konzentrationsänderungen, die durch Sedimentation oder Aufrahmung verursacht werden, und die Verklumpung von Partikeln durch Aggregation erkannt und überwacht. Diese Phänomene werden mit instabilen Kolloiden in Verbindung gebracht. ⓘ
Mit Hilfe der dynamischen Lichtstreuung kann die Größe eines kolloidalen Partikels ermittelt werden, indem man misst, wie schnell es diffundiert. Bei dieser Methode wird Laserlicht auf ein Kolloid gerichtet. Das gestreute Licht bildet ein Interferenzmuster, und die Schwankung der Lichtintensität in diesem Muster wird durch die Brownsche Bewegung der Teilchen verursacht. Nimmt die scheinbare Größe der Teilchen zu, weil sie durch Aggregation zusammenklumpen, führt dies zu einer langsameren Brownschen Bewegung. Diese Technik kann bestätigen, dass eine Aggregation stattgefunden hat, wenn die scheinbare Partikelgröße außerhalb des typischen Größenbereichs für kolloidale Partikel liegt. ⓘ
Beschleunigende Methoden für die Vorhersage der Lagerfähigkeit
Der kinetische Prozess der Destabilisierung kann recht langwierig sein (bis zu mehreren Monaten oder sogar Jahren bei einigen Produkten), und der Formulierer muss oft weitere beschleunigende Methoden anwenden, um eine angemessene Entwicklungszeit für das Design neuer Produkte zu erreichen. Thermische Methoden werden am häufigsten eingesetzt und bestehen in der Erhöhung der Temperatur, um die Destabilisierung zu beschleunigen (unterhalb der kritischen Temperaturen für Phaseninversion oder chemischen Abbau). Die Temperatur wirkt sich nicht nur auf die Viskosität aus, sondern auch auf die Grenzflächenspannung bei nichtionischen Tensiden oder allgemeiner auf die Wechselwirkungskräfte innerhalb des Systems. Die Lagerung einer Dispersion bei hohen Temperaturen ermöglicht es, die realen Bedingungen für ein Produkt zu simulieren (z. B. eine Tube Sonnenschutzcreme im Auto im Sommer), aber auch Destabilisierungsprozesse bis zum 200-fachen zu beschleunigen. Manchmal werden auch mechanische Beschleunigungsverfahren wie Vibration, Zentrifugation und Schütteln eingesetzt. Sie setzen das Produkt verschiedenen Kräften aus, die die Partikel/Tröpfchen gegeneinander drücken und so zur Entwässerung des Films beitragen. Einige Emulsionen würden jedoch bei normaler Schwerkraft nie zusammenfließen, während sie es bei künstlicher Schwerkraft tun. Darüber hinaus wurde die Entmischung verschiedener Partikelpopulationen bei der Verwendung von Zentrifugation und Vibration hervorgehoben. ⓘ
Als Modellsystem für Atome
In der Physik sind Kolloide ein interessantes Modellsystem für Atome. Kolloidale Partikel im Mikrometermaßstab sind groß genug, um mit optischen Techniken wie der konfokalen Mikroskopie beobachtet werden zu können. Viele der Kräfte, die die Struktur und das Verhalten von Materie bestimmen, wie z. B. die Wechselwirkungen zwischen ausgeschlossenen Volumina oder elektrostatische Kräfte, bestimmen auch die Struktur und das Verhalten von kolloidalen Suspensionen. So können beispielsweise dieselben Techniken, die zur Modellierung idealer Gase verwendet werden, auch zur Modellierung des Verhaltens einer kolloidalen Hartkugelsuspension eingesetzt werden. Darüber hinaus können Phasenübergänge in kolloidalen Suspensionen mit Hilfe optischer Techniken in Echtzeit untersucht werden und sind mit Phasenübergängen in Flüssigkeiten vergleichbar. In vielen interessanten Fällen wird die optische Fluidität zur Kontrolle kolloidaler Suspensionen eingesetzt. ⓘ
Kristalle
Ein kolloidaler Kristall ist eine hochgradig geordnete Anordnung von Teilchen, die über einen sehr großen Bereich (typischerweise in der Größenordnung von einigen Millimetern bis zu einem Zentimeter) gebildet werden kann und die analog zu ihren atomaren oder molekularen Gegenstücken erscheint. Eines der schönsten natürlichen Beispiele für dieses Ordnungsphänomen findet sich in kostbarem Opal, in dem brillante Bereiche reiner Spektralfarben aus dicht gepackten Domänen amorpher kolloidaler Kugeln aus Siliziumdioxid (oder Siliziumdioxid, SiO2) entstehen. Diese kugelförmigen Partikel fallen in stark kieselsäurehaltigen Becken in Australien und anderswo aus und bilden nach jahrelanger Sedimentation und Kompression unter hydrostatischen und gravitativen Kräften diese hoch geordneten Anordnungen. Die periodischen Anordnungen kugelförmiger Teilchen im Submikrometerbereich bilden ähnliche Anordnungen von Zwischenräumen, die als natürliches Beugungsgitter für sichtbare Lichtwellen wirken, insbesondere wenn der Abstand zwischen den Zwischenräumen in der gleichen Größenordnung liegt wie die einfallende Lichtwelle. ⓘ
So ist seit vielen Jahren bekannt, dass elektrisch geladene Makromoleküle in wässriger Umgebung aufgrund abstoßender Coulomb-Wechselwirkungen kristallähnliche Korrelationen mit großen Abständen zwischen den Teilchen aufweisen können, die oft erheblich größer sind als der Durchmesser der einzelnen Teilchen. In all diesen Fällen in der Natur kann das gleiche brillante Schillern (oder Farbenspiel) auf die Beugung und konstruktive Interferenz von sichtbaren Lichtwellen zurückgeführt werden, die dem Bragg'schen Gesetz entsprechen, analog zur Streuung von Röntgenstrahlen in kristallinen Festkörpern. ⓘ
Die zahlreichen Experimente zur Erforschung der Physik und Chemie dieser so genannten "kolloidalen Kristalle" sind das Ergebnis der relativ einfachen Methoden, die in den letzten 20 Jahren entwickelt wurden, um synthetische monodisperse Kolloide (sowohl Polymere als auch Mineralien) herzustellen und durch verschiedene Mechanismen die Bildung einer langreichweitigen Ordnung zu erreichen und zu erhalten. ⓘ
In der Biologie
Die kolloidale Phasentrennung ist ein wichtiges Organisationsprinzip für die Kompartimentierung sowohl des Zytoplasmas als auch des Zellkerns in biomolekulare Kondensate - ähnlich wichtig wie die Kompartimentierung über Lipid-Doppelschichtmembranen, eine Art Flüssigkristall. Der Begriff biomolekulare Kondensate wird für Makromolekülcluster verwendet, die durch Phasentrennung zwischen Flüssigkeit und Flüssigkeit oder Flüssigkeit und Festkörper in Zellen entstehen. Makromolekulares Gedränge verstärkt die kolloidale Phasentrennung und die Bildung biomolekularer Kondensate stark. ⓘ
In der Umwelt
Kolloidale Partikel können auch als Transportvektor dienen diverser Schadstoffe im Oberflächenwasser (Meerwasser, Seen, Flüsse, Süßwasser) und in unterirdischem Wasser, das in zerklüftetem Gestein zirkuliert (z. B. Kalkstein, Sandstein, Granit). Radionuklide und Schwermetalle sorbieren leicht an im Wasser suspendierte Kolloide. Es werden verschiedene Arten von Kolloiden unterschieden: anorganische Kolloide (z. B. Tonpartikel, Silikate, Eisenoxydhydroxide) und organische Kolloide (Huminstoffe und Fulvosubstanzen). Wenn Schwermetalle oder Radionuklide ihre eigenen reinen Kolloide bilden, wird der Begriff "Eigenkolloid" verwendet, um reine Phasen zu bezeichnen, d. h. reines Tc(OH)4, U(OH)4 oder Am(OH)3. Kolloide stehen im Verdacht, für den weiträumigen Transport von Plutonium auf dem Atomtestgelände in Nevada verantwortlich zu sein. Sie sind seit vielen Jahren Gegenstand eingehender Studien. Die Mobilität der anorganischen Kolloide ist jedoch in verdichteten Bentoniten und in tiefen Tonformationen sehr gering aufgrund des Prozesses der Ultrafiltration in dichten Tonmembranen. Bei kleinen organischen Kolloiden, die im Porenwasser oft mit tatsächlich gelösten organischen Molekülen vermischt sind, ist die Frage weniger klar. ⓘ
In der Bodenkunde besteht die kolloidale Fraktion in Böden aus winzigen Ton- und Humuspartikeln mit einem Durchmesser von weniger als 1 μm, die entweder positive und/oder negative elektrostatische Ladungen tragen, die je nach den chemischen Bedingungen der Bodenprobe, d. h. dem pH-Wert des Bodens, variieren. ⓘ
Intravenöse Therapie
Kolloidlösungen, die in der intravenösen Therapie verwendet werden, gehören zu einer großen Gruppe von Volumenexpandern und können für den intravenösen Flüssigkeitsersatz verwendet werden. Kolloide erhalten einen hohen kolloidosmotischen Druck im Blut aufrecht und sollten daher theoretisch vorzugsweise das intravaskuläre Volumen erhöhen, während andere Arten von Volumenexpandern, die so genannten Kristalloide, auch das interstitielle Volumen und das intrazelluläre Volumen erhöhen. Der tatsächliche Unterschied in der Wirksamkeit ist jedoch nach wie vor umstritten, und ein Großteil der Forschung zu dieser Verwendung von Kolloiden beruht auf den betrügerischen Untersuchungen von Joachim Boldt. Ein weiterer Unterschied ist, dass Kristalloide im Allgemeinen viel billiger sind als Kolloide. ⓘ
Geschichte und Herkunft des Begriffs
Kolloide wurden schon genutzt, als noch keinerlei Kenntnis über ihre Systematik bestand. Die wissenschaftliche Auseinandersetzung mit Kolloiden ist erst in jüngerer Zeit zu verzeichnen, als sich die früher begrenzten technischen Möglichkeiten für eine gezielte, reproduzierbare Herstellung wohldefinierter Kolloide verbesserte. ⓘ
Bereits den Alchimisten waren Formen des kolloidalen Goldes bekannt und Pierre Joseph Macquer vermutete 1744, dass es sich hierbei um eine feine Verteilung des Goldes in einer Dispersion handeln könnte. Erste empirische Untersuchungen führte Selmi 1845 durch, 1856 folgten die Versuche Michael Faradays mit kolloidalem Gold. ⓘ
Der britische Physiker Thomas Graham führte 1861 den englischen Begriff „colloid“ ein, den er von dem griechischen Wort für Leim ableitete. Er benutzte ihn, um Stoffe aufgrund ihres Diffusionsverhaltens durch poröse Membranen in „kristalloide“ und „kolloidale“ Substanzen zu unterteilen. Grahams Kriterien waren jedoch nicht zielführend. Was er als kolloidal bezeichnete, war nicht eine chemische Eigenschaft, sondern ein Zustand der feinen physikalischen Unterteilung bestimmter Proben. Seit Beginn des zwanzigsten Jahrhunderts wird der Begriff im Sinne der modernen Definition verwendet. Im Jahr 1922 gründete Wolfgang Ostwald in Leipzig die Kolloid-Gesellschaft zur Pflege und Förderung der Kolloidwissenschaft, die bis heute noch besteht. ⓘ
Eine kinetische Theorie für kolloidale Systeme wurde erstmals von Marian Smoluchowski geschaffen. Die Chemie der Kolloide und deren Eigenschaften wurden besonders von Richard Zsigmondy (Nobelpreis 1925) und seinen Mitarbeitern untersucht. ⓘ
Eigenschaften
Makroskopisch

Aufgrund ihrer im Verhältnis zum Volumen vergleichsweise großen Grenzflächen spielen Effekte der Oberflächenchemie für Kolloide eine besondere Rolle. Kolloide weisen zudem in der Regel den Tyndall-Effekt auf. Durch Lichtstreuung an den Grenzflächen erscheinen selbst Dispersionen aus transparenten Phasen milchig oder trüb (es kann auch Opaleszenz auftreten), solange die Brechungsindizes nicht genau gleich sind. ⓘ
Bedeutung und Anwendungen
Chemie
Die Kolloidchemie untersucht die Eigenschaften kolloiddisperser Systeme und ist ein selbständiges Gebiet der physikalischen Chemie. ⓘ
Physik
Kolloidsuspensionen sind wichtige Modellsysteme um Vorhersagen der statistischen Thermodynamik zu überprüfen oder atomare Festkörperprozesse zu simulieren.
- Die Wechselwirkungen zwischen einzelnen Kolloidteilchen lassen sich durch Auswahl der Teilchen, Behandlung ihrer Oberfläche und Zusammensetzung der Flüssigkeit einstellen. Man kann Stärke und Reichweite der Wechselwirkung separat einstellen und damit verschiedenartige Potentialverläufe modellieren. Die Teilchen verhalten sich wie Atome eines Metalls oder wie die eines ionischen Systems und bilden entsprechende Kristalle. Bei hinreichender Konzentration tritt die Kristallisation sogar bei nicht wechselwirkenden Partikeln („Harte Kugeln“) ein, was paradoxerweise entropische Ursachen hat.
- Kolloide sind etwa um den Faktor 1000 bis 10.000 größer als Atome. Daher sind sie wesentlich einfacher und mit deutlich weniger experimentellem Aufwand (dynamischer Lichtstreuung oder Konfokalmikroskopie) zu beobachten.
- Ihre Bewegung ist deutlich langsamer als die von Atomen. Das erlaubt die Beobachtung von Prozessen wie Kristallisation, die in atomaren Systemen zu schnell ablaufen. ⓘ
Verfahrenstechnik
Kolloiddisperse Systeme haben durch die feine Verteilung der einen Phase in der anderen im Verhältnis zu ihrem Volumen eine enorm große Grenzfläche. Dies wird überall ausgenutzt, wo Grenzflächeneffekte wichtig sind, wie in der Trocknungstechnik oder bei der Reaktion zweier nichtmischbarer Flüssigkeiten. ⓘ
Bodenkunde
In der Bodenkunde wird das Größenspektrum der Kolloide bis zwei Mikrometer erweitert. Diese Einteilung schließt die bodenkundlich relevante Tonfraktion ein, da Bodenteilchen mit einem Durchmesser bis etwa 2 μm kolloidale Eigenschaften aufweisen. Dies ist unter anderem Folge des blattförmigen Habitus von Tonteilchen. Dabei treten Eigenschaften, die auf Grund der Masse der Teilchen auftreten, gegenüber den Eigenschaften aus der großen spezifischen Oberfläche, zurück. ⓘ
Medizin
In der Infusionstherapie werden kolloidale Infusionslösungen eingesetzt, die eine Stabilisierung oder Zunahme des Volumens in den Blutgefäßen bewirken. Sie enthalten kolloidale Makromoleküle wie Kohlenhydrate (Hydroxyethylstärke, Dextrane) oder Proteine (Gelatine oder humanes Albumin). ⓘ


















