Corticosteroide
Corticosteroide oder Kortikosteroide (von lateinisch cortex = ‚Rinde‘; gr. stereos, στερεος = ‚fest‘), kurz auch Corticoide, Kortikoide oder Cortine geschrieben, sind eine Gruppe von ca. 50 in der Nebennierenrinde (dem Kortex der Nebenniere) gebildeten Steroidhormonen sowie chemisch vergleichbarer synthetischer Stoffe. Alle Corticoide entstehen dabei aus dem Ausgangsstoff Cholesterin. Gemeinsames Grundgerüst der Hormone ist das Progesteron (Δ4-Pregnen-3,20-dion). ⓘ

Die Corticosteroide lassen sich nach ihrer biologischen Wirkung bzw. ihrem Bildungsort in drei Gruppen einteilen:
- Mineralocorticoide (Hauptvertreter Aldosteron) werden in der Zona glomerulosa der Nebennierenrinde gebildet und beeinflussen vorwiegend den Kalium-Natrium-Haushalt und damit den Wassergehalt des Körpers.
- Glucocorticoide (Hauptvertreter Cortisol) werden in der Zona fasciculata der Nebennierenrinde gebildet. Sie vermitteln wichtige Wirkungen im Glucose-, Lipid- und Proteinstoffwechsel.
- Androgene (Hauptvertreter Dehydroepiandrosteron (DHEA)) und Estrogene werden in der Zona reticularis der Nebennierenrinde gebildet. ⓘ
Zu den natürlichen Glucocorticoiden gehören Cortison, Corticosteron und Cortisol; zu den Mineralocorticoiden das Aldosteron und das bereits 1935 von Reichstein isolierte Desoxycorticosteron. Synthetische Corticoide sind z. B. Prednison und Prednisolon, Methylprednisolon, Triamcinolon, Dexamethason, Betamethason und Paramethason. ⓘ
| Kortikosteroid ⓘ | |
|---|---|
| Wirkstoffklasse | |
| Identifikatoren der Klasse | |
| Synonyme | Kortikoid |
| Verwendung | Verschiedene |
| ATC-Code | H02 |
| Biologisches Ziel | Glucocorticoid-Rezeptor, Mineralocorticoid-Rezeptor |
| Chemische Klasse | Steroide |
Kortikosteroide sind eine Klasse von Steroidhormonen, die in der Nebennierenrinde von Wirbeltieren produziert werden, sowie die synthetischen Analoga dieser Hormone. Zwei Hauptklassen von Kortikosteroiden, die Glukokortikoide und die Mineralokortikoide, sind an einer Vielzahl physiologischer Prozesse beteiligt, u. a. an der Stressreaktion, der Immunreaktion und der Regulierung von Entzündungen, des Kohlenhydratstoffwechsels, des Eiweißabbaus, des Blutelektrolytspiegels und des Verhaltens. ⓘ
Einige häufige natürlich vorkommende Steroidhormone sind Cortisol (C
21H
30O
5), Kortikosteron (C
21H
30O
4), Kortison (C
21H
28O
5) und Aldosteron (C
21H
28O
5). (Beachten Sie, dass Kortison und Aldosteron Isomere sind.) Die wichtigsten von der Nebennierenrinde produzierten Kortikosteroide sind Kortisol und Aldosteron. ⓘ
Klassen
thumb|200px|Cortisol thumb|200px|Cortison thumb|200px|Corticosteron thumb|200px|Aldosteron
- Glucocorticoide wie Cortisol beeinflussen den Kohlenhydrat-, Fett- und Eiweißstoffwechsel und haben entzündungshemmende, immunsuppressive, antiproliferative und gefäßverengende Wirkungen. Die entzündungshemmenden Wirkungen werden durch die Blockierung der Wirkung von Entzündungsmediatoren (Transrepression) und die Induktion von entzündungshemmenden Mediatoren (Transaktivierung) vermittelt. Immunsuppressive Wirkungen werden durch die Unterdrückung verzögerter Überempfindlichkeitsreaktionen durch direkte Wirkung auf T-Lymphozyten vermittelt. Proliferationshemmende Wirkungen werden durch die Hemmung der DNA-Synthese und des epidermalen Zellumsatzes vermittelt. Vasokonstriktorische Wirkungen werden durch die Hemmung der Wirkung von Entzündungsmediatoren wie Histamin vermittelt.
- Mineralokortikoide wie Aldosteron sind in erster Linie an der Regulierung des Elektrolyt- und Wasserhaushalts beteiligt, indem sie den Ionentransport in den Epithelzellen der Nierentubuli der Niere modulieren. ⓘ
Medizinische Anwendungen
Synthetische Arzneimittel mit kortikosteroidähnlichen Wirkungen werden bei einer Vielzahl von Erkrankungen eingesetzt, die von Hirntumoren bis zu Hautkrankheiten reichen. Dexamethason und seine Derivate sind fast reine Glukokortikoide, während Prednison und seine Derivate neben der Glukokortikoidwirkung auch eine gewisse Mineralokortikoidwirkung aufweisen. Fludrocortison (Florinef) ist ein synthetisches Mineralocorticoid. Hydrocortison (Cortisol) wird in der Regel als Ersatztherapie eingesetzt, z. B. bei Nebenniereninsuffizienz und kongenitaler Nebennierenhyperplasie. ⓘ
Krankheiten, die mit systemischen Kortikosteroiden behandelt werden:
- Allergie- und Atemwegsmedizin
- Asthma (schwere Exazerbationen)
- Chronisch obstruktive Lungenerkrankung (COPD)
- Allergischer Schnupfen
- Atopische Dermatitis
- Nesselsucht
- Angioödem
- Anaphylaxie
- Nahrungsmittelallergien
- Medikamentenallergien
- Nasenpolypen
- Hypersensitivitäts-Pneumonitis
- Sarkoidose
- Eosinophile Lungenentzündung
- Einige andere Arten von Lungenentzündung (zusätzlich zu den herkömmlichen Antibiotikabehandlungsprotokollen)
- Interstitielle Lungenerkrankung
- Dermatologie
- Pemphigus vulgaris
- Kontaktdermatitis
- Endokrinologie (normalerweise in physiologischen Dosen)
- Addisonsche Krankheit
- Nebennieren-Insuffizienz
- Kongenitale Nebennierenhyperplasie
- Gastroenterologie
- Colitis ulcerosa
- Morbus Crohn
- Autoimmun-Hepatitis
- Hämatologie
- Lymphome
- Leukämie
- Hämolytische Anämie
- Idiopathische thrombozytopenische Purpura
- Multiples Myelom
- Rheumatologie/Immunologie
- Rheumatoide Arthritiseen
- Systemischer Lupus erythematodes
- Polymyalgia rheumatica
- Polymyositis
- Dermatomyositis
- Polyarteriitis
- Vaskulitis
- Ophthalmologie
- Uveitis
- Sehnervenentzündung
- Keratoconjunctivitis
- Andere Erkrankungen
- Multiple Sklerose-Schübe
- Organtransplantation
- Nephrotisches Syndrom
- Chronische Hepatitis (Krankheitsschübe)
- Zerebrale Ödeme
- IgG4-bedingte Krankheit
- Prostata-Krebs
- Tendinose
- Lichen planus ⓘ
Topische Formulierungen sind auch für die Haut, die Augen (Uveitis), die Lunge (Asthma), die Nase (Rhinitis) und den Darm erhältlich. Kortikosteroide werden auch unterstützend zur Vorbeugung von Übelkeit eingesetzt, oft in Kombination mit 5-HT3-Antagonisten (z. B. Ondansetron). ⓘ
Typische unerwünschte Wirkungen von Glukokortikoiden treten recht einheitlich als medikamenteninduziertes Cushing-Syndrom auf. Typische Mineralokortikoid-Nebenwirkungen sind Hypertonie (abnorm hoher Blutdruck), steroidbedingter Diabetes mellitus, Psychosen, Schlafstörungen, Hypokaliämie (niedriger Kaliumspiegel im Blut), Hypernatriämie (hoher Natriumspiegel im Blut), ohne dass es zu peripheren Ödemen, metabolischer Alkalose und Bindegewebsschwäche kommt. Die Wundheilung oder die Bildung von Geschwüren kann durch die immunsuppressive Wirkung gehemmt werden. ⓘ
Klinische und experimentelle Hinweise deuten darauf hin, dass Kortikosteroide dauerhafte Augenschäden verursachen können, indem sie eine zentrale seröse Retinopathie (CSR, auch bekannt als zentrale seröse Chorioretinopathie, CSC) hervorrufen. Dies sollte bei der Behandlung von Patienten mit Optikusneuritis berücksichtigt werden. Es gibt experimentelle und klinische Belege dafür, dass zumindest bei der Optikusneuritis ein schneller Behandlungsbeginn wichtig ist. ⓘ
Eine Vielzahl von Steroidmedikamenten, von Anti-Allergie-Nasensprays (Nasonex, Flonase) über topische Hautcremes bis hin zu Augentropfen (Tobradex) und Prednison, wurde mit der Entwicklung von CSR in Verbindung gebracht. ⓘ
Kortikosteroide werden bei der Behandlung von Menschen mit traumatischen Hirnverletzungen häufig eingesetzt. In einer systematischen Übersichtsarbeit wurden 20 randomisierte kontrollierte Studien mit 12 303 Teilnehmern ermittelt und anschließend Patienten, die Kortikosteroide erhielten, mit Patienten verglichen, die keine Behandlung erhielten. Die Autoren empfehlen, dass Menschen mit traumatischen Kopfverletzungen nicht routinemäßig mit Kortikosteroiden behandelt werden sollten. ⓘ
Pharmakologie
Kortikosteroide wirken als Agonisten des Glukokortikoidrezeptors und/oder des Mineralokortikoidrezeptors. ⓘ
Zusätzlich zu ihrer kortikosteroidalen Wirkung können einige Kortikosteroide eine gewisse progestogene Wirkung haben und geschlechtsbezogene Nebenwirkungen hervorrufen. ⓘ
Pharmakogenetik
Asthma
Das Ansprechen der Patienten auf inhalative Kortikosteroide ist zum Teil auf genetische Variationen zurückzuführen. Zwei Gene von Interesse sind CHRH1 (Corticotropin-Releasing-Hormon-Rezeptor 1) und TBX21 (Transkriptionsfaktor T-bet). Beide Gene weisen beim Menschen ein gewisses Maß an polymorpher Variation auf, was erklären könnte, warum manche Patienten besser auf eine inhalative Kortikosteroidtherapie ansprechen als andere. Allerdings sprechen nicht alle Asthma-Patienten auf Kortikosteroide an, und große Untergruppen von Asthma-Patienten sind kortikosteroidresistent. ⓘ
Eine vom Patient-Centered Outcomes Research Institute finanzierte Studie mit Kindern und Jugendlichen mit leichtem persistierendem Asthma ergab, dass die bedarfsgerechte Anwendung des Kontrollinhalators die gleiche Wirkung hat wie die tägliche Anwendung, wenn es um die Verbesserung der Asthmakontrolle, die Anzahl der Asthmaanfälle, die Funktionsfähigkeit der Lunge und die Lebensqualität geht. Kinder und Jugendliche, die den Inhalator bei Bedarf verwendeten, brauchten nur etwa ein Viertel der Menge an Kortikosteroid-Medikamenten im Vergleich zu Kindern und Jugendlichen, die ihn täglich verwendeten. ⓘ
Unerwünschte Wirkungen
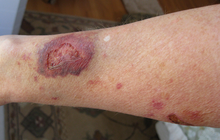
Die Anwendung von Kortikosteroiden hat zahlreiche Nebenwirkungen, von denen einige schwerwiegend sein können:
- Schwere Amöbenkolitis: Fulminante Amöbenkolitis ist mit einer hohen Sterblichkeitsrate verbunden und kann bei Patienten auftreten, die mit dem Parasiten Entamoeba histolytica infiziert sind, nachdem sie Kortikosteroid-Medikamenten ausgesetzt waren.
- Neuropsychiatrie: Steroidpsychose, Angstzustände und Depressionen. Therapeutische Dosen können ein Gefühl des künstlichen Wohlbefindens ("Steroideuphorie") hervorrufen. Die neuropsychiatrischen Wirkungen werden teilweise durch eine Sensibilisierung des Körpers für die Wirkung von Adrenalin vermittelt. Therapeutisch wird der Großteil der Kortikosteroiddosis morgens verabreicht, um den Tagesrhythmus des Körpers zu imitieren; bei nächtlicher Verabreichung stört das Gefühl der Energiezufuhr den Schlaf. Eine ausführliche Übersicht findet sich bei Flores und Gumina.
- Kardiovaskulär: Kortikosteroide können durch eine direkte Wirkung auf die Niere eine Natriumretention verursachen, und zwar in ähnlicher Weise wie das Mineralokortikoid Aldosteron. Dies kann zu Flüssigkeitsretention und Bluthochdruck führen.
- Metabolisch: Kortikosteroide bewirken eine Verlagerung von Körperfett in das Gesicht und den Rumpf, was zu "Mondgesicht", "Büffelbuckel" und "Topfbauch" oder "Bierbauch" führt, und bewirken eine Verlagerung von Körperfett weg von den Gliedmaßen. Dies wird als Kortikosteroid-induzierte Lipodystrophie bezeichnet. Da Aminosäuren in Glukose umgewandelt werden, gelten sie als antianabolisch, und eine Langzeittherapie kann zu Muskelschwund führen.
- Endokrin: Da sie die Produktion von Glukose aus dem Abbau von Aminosäuren erhöhen und der Wirkung von Insulin entgegenwirken, können Kortikosteroide Hyperglykämie, Insulinresistenz und Diabetes mellitus verursachen.
- Skelett: Steroid-induzierte Osteoporose kann eine Nebenwirkung der langfristigen Kortikosteroideinnahme sein. Die Anwendung von inhalativen Kortikosteroiden bei Kindern mit Asthma kann zu einer verminderten Körpergröße führen.
- Gastrointestinales: Obwohl Fälle von Kolitis berichtet wurden, werden Kortikosteroide häufig verschrieben, wenn die Kolitis zwar auf eine Unterdrückung der Immunantwort auf Krankheitserreger zurückzuführen ist, aber erst nach Ausschluss einer Infektion oder einer Mikroben-/Pilzüberwucherung im Magen-Darm-Trakt in Betracht gezogen werden sollte. Obwohl die Beweise dafür, dass Kortikosteroide peptische Ulzerationen verursachen, relativ dürftig sind, außer bei hohen Dosen, die über einen Monat eingenommen werden, ist die Mehrheit der Ärzte (Stand 2010) immer noch der Meinung, dass dies der Fall ist, und würde prophylaktische Schutzmaßnahmen in Betracht ziehen.
- Augen: Chronischer Konsum kann Katarakt und Glaukom begünstigen.
- Anfälligkeit für Infektionen: Durch die Unterdrückung von Immunreaktionen (einer der Hauptgründe für ihren Einsatz bei Allergien) können Steroide das Aufflammen von Infektionen, insbesondere von Candidose, verursachen.
- Schwangerschaft: Kortikosteroide haben eine geringe, aber signifikante teratogene Wirkung und verursachen einige Geburtsfehler pro 1.000 behandelte Schwangere. Kortikosteroide sind daher in der Schwangerschaft kontraindiziert.
- Gewöhnung: Bei Langzeitanwendern topischer Steroide (Anwender, die über einen Zeitraum von Wochen, Monaten oder Jahren topische Steroide auf ihre Haut aufgetragen haben) wurde über eine Abhängigkeit von topischen Steroiden (TSA) oder rot brennende Haut berichtet. TSA ist gekennzeichnet durch eine unkontrollierbare, sich ausbreitende Dermatitis und eine sich verschlimmernde Hautentzündung, die ein stärkeres topisches Steroid erfordert, um das gleiche Ergebnis wie bei der ersten Verschreibung zu erzielen. Wenn die topische Steroidmedikation abgesetzt wird, kommt es zu Rötungen, Brennen, Juckreiz, heißer Haut, Schwellungen und/oder Nässen der Haut über einen längeren Zeitraum. Dies wird auch als "Syndrom der roten Haut" oder "topischer Steroidentzug" (TSW) bezeichnet. Nach Ablauf der Entzugszeit kann die atopische Dermatitis abklingen oder ist weniger schwerwiegend als zuvor.
- Bei Kindern erhöht die kurzfristige Einnahme von Steroiden über den Mund das Risiko von Erbrechen, Verhaltensänderungen und Schlafproblemen. ⓘ
Da Corticosteroide eine Magensäureüberproduktion induzieren, sollte bei dauerhafter Gabe zusätzlich ein Protonenpumpenhemmer genommen werden, um die Entstehung eines Magenulkus zu verhindern. Allgemein kann, insbesondere bei langfristiger und/oder hochdosierter Anwendung, eine große Zahl von Nebenwirkungen auftreten, insbesondere Störungen in der Hypothalamus-Hypophysen-Nebennieren-Achse mit der Folge einer sekundären Nebennierenrinden-Insuffizienz (z. B. Cushing-Syndrom, siehe auch Absatz Überproduktion), die eine sorgfältige Abwägung bei der Anwendung erforderlich machen. Bei einer Stoßtherapie im Bereich der Behandlung von Epilepsie oder eines Multiple-Sklerose-Schubes muss etwa eine Stunde nach der Einnahme einer Dosis ein Magenschutzmittel verabreicht werden. ⓘ
Durch die immunsuppressive Wirkung von Glucocorticoiden treten bei Patienten aufgrund der geschwächten Immunabwehr gehäuft Infektionen mit Viren, Bakterien oder Pilzen auf. ⓘ
Biosynthese

Die Kortikosteroide werden in der Nebennierenrinde aus Cholesterin synthetisiert. Die meisten steroidogenen Reaktionen werden durch Enzyme der Cytochrom-P450-Familie katalysiert. Sie befinden sich in den Mitochondrien und benötigen Adrenodoxin als Kofaktor (außer 21-Hydroxylase und 17α-Hydroxylase). ⓘ
Aldosteron und Corticosteron haben den ersten Teil ihres Biosyntheseweges gemeinsam. Der letzte Teil wird entweder durch die Aldosteronsynthase (für Aldosteron) oder durch die 11β-Hydroxylase (für Kortikosteron) vermittelt. Diese Enzyme sind fast identisch (sie teilen sich die Funktionen der 11β-Hydroxylierung und der 18-Hydroxylierung), aber die Aldosteron-Synthase ist auch in der Lage, eine 18-Oxidation durchzuführen. Außerdem befindet sich die Aldosteronsynthase in der Zona glomerulosa am äußeren Rand der Nebennierenrinde; die 11β-Hydroxylase ist in der Zona fasciculata und der Zona glomerulosa zu finden. ⓘ
Klassifizierung der Kortikosteroide
Nach chemischer Struktur
Im Allgemeinen werden Kortikosteroide auf der Grundlage ihrer chemischen Struktur in vier Klassen eingeteilt. Allergische Reaktionen auf ein Mitglied einer Klasse deuten in der Regel auf eine Unverträglichkeit gegenüber allen Mitgliedern der Klasse hin. Dies wird als "Coopman-Klassifikation" bezeichnet. ⓘ
Die hervorgehobenen Steroide werden häufig für das Screening von Allergien gegen topische Steroide verwendet. ⓘ
Gruppe A - Hydrocortison-Typ
Hydrocortison, Hydrocortisonacetat, Cortisonacetat, Tixocortolpivalat, Prednisolon, Methylprednisolon und Prednison. ⓘ
Gruppe B - Acetonide (und verwandte Stoffe)
Amcinonid, Budesonid, Desonid, Fluocinolonacetonid, Fluocinonid, Halcinonid und Triamcinolonacetonid. ⓘ
Gruppe C - Betamethason-Typ
Beclometason, Betamethason, Dexamethason, Fluocortolon, Halometason und Mometason. ⓘ
Gruppe D - Ester
Gruppe D1 - Halogenierte (weniger labil)
Alclometasondipropionat, Betamethasondipropionat, Betamethasonvalerat, Clobetasolpropionat, Clobetasonbutyrat, Fluprednidenacetat und Mometasonfuroat. ⓘ
Gruppe D2 - Labile Prodrug-Ester
Ciclesonid, Cortisonacetat, Hydrocortison-Aceponat, Hydrocortisonacetat, Hydrocortisonbuteprat, Hydrocortisonbutyrat, Hydrocortisonvalerat, Prednicarbat und Tixocortolpivalat. ⓘ
Nach Art der Verabreichung
Topische Steroide
Zur topischen Anwendung auf der Haut, den Augen und den Schleimhäuten. ⓘ
Topische Kortikosteroide werden in den meisten Ländern in die Potenzklassen I bis IV eingeteilt (A bis D in Japan). In den Vereinigten Staaten werden sieben Kategorien verwendet, um den Grad der Wirksamkeit eines bestimmten topischen Kortikosteroids zu bestimmen. ⓘ
Inhalative Steroide
Für Nasenschleimhaut, Nasennebenhöhlen, Bronchien und Lunge. Zu dieser Gruppe gehören:
- Flunisolid
- Fluticasonfuroat
- Fluticasonpropionat
- Triamcinolonacetonid
- Beclomethasondipropionat
- Budesonid
- Mometasonfuroat
- Ciclesonid ⓘ
Es gibt auch bestimmte Kombinationspräparate wie Advair Diskus in den Vereinigten Staaten, das Fluticasonpropionat und Salmeterol (einen lang wirkenden Bronchodilatator) enthält, und Symbicort, das Budesonid und Formoterolfumarat-Dihydrat (einen weiteren lang wirkenden Bronchodilatator) enthält. Beide sind für die Anwendung bei Kindern über 12 Jahren zugelassen. ⓘ
Orale Formen
Wie z. B. Prednison, Prednisolon, Methylprednisolon oder Dexamethason. ⓘ
Systemische Formen
Erhältlich in Form von Injektionspräparaten zur intravenösen und parenteralen Verabreichung. ⓘ
Geschichte
| Kortikosteroid | Eingeführt |
|---|---|
| Kortison | 1948 |
| Hydrocortison | 1951 |
| Fludrocortisonacetat | 1954 |
| Prednisolon | 1955 |
| Prednison | 1955 |
| Methylprednisolon | 1956 |
| Triamcinolon | 1956 |
| Dexamethason | 1958 |
| Betamethason | 1958 |
| Triamcinolonacetonid | 1958 |
| Fluorometholon | 1959 |
Tadeusz Reichstein, Edward Calvin Kendall und Philip Showalter Hench erhielten 1950 den Nobelpreis für Physiologie und Medizin für ihre Arbeiten über Hormone der Nebennierenrinde, die in der Isolierung von Kortison gipfelten. ⓘ
Anfänglich als Wundermittel gepriesen und in den 1950er Jahren reichlich verschrieben, führte die Behandlung mit Steroiden zu so starken Nebenwirkungen, dass die nächste große Kategorie entzündungshemmender Medikamente, die nichtsteroidalen Antirheumatika (NSAIDs), so genannt wurde, um sich von der Schmach abzugrenzen. Kortikosteroide wurden 2005 von der amerikanischen Gesellschaft für Kontaktdermatitis zum Allergen des Jahres gewählt. ⓘ
Lewis Sarett von Merck & Co. war der erste, der Kortison in einem 36-stufigen Prozess synthetisierte, der mit Desoxycholsäure begann, die aus Rindergalle gewonnen wurde. Die geringe Effizienz der Umwandlung von Desoxycholsäure in Kortison führte zu Kosten von 200 US-Dollar pro Gramm. Russell Marker von Syntex entdeckte einen viel billigeren und bequemeren Ausgangsstoff, Diosgenin aus wilden mexikanischen Yamswurzeln. Seine Umwandlung von Diosgenin in Progesteron durch einen vierstufigen Prozess, der heute als Marker-Abbau bekannt ist, war ein wichtiger Schritt in der Massenproduktion aller Steroidhormone, einschließlich Cortison und Chemikalien, die in der hormonellen Empfängnisverhütung verwendet werden. ⓘ
1952 entwickelten D.H. Peterson und H.C. Murray von Upjohn ein Verfahren, bei dem ein Rhizopus-Schimmelpilz verwendet wurde, um Progesteron in eine Verbindung zu oxidieren, die sich leicht in Kortison umwandeln ließ. Die Möglichkeit, große Mengen an Cortison aus dem Diosgenin der Yamswurzel kostengünstig zu synthetisieren, führte zu einem raschen Preisverfall auf 6 US-Dollar pro Gramm, der bis 1980 auf 0,46 US-Dollar pro Gramm fiel. Auch die Forschungen von Percy Julian trugen zum Fortschritt in diesem Bereich bei. Die genaue Art der entzündungshemmenden Wirkung von Kortison blieb jedoch noch jahrelang ein Rätsel, bis die Leukozytenadhäsionskaskade und die Rolle der Phospholipase A2 bei der Produktion von Prostaglandinen und Leukotrienen Anfang der 1980er Jahre vollständig geklärt waren. ⓘ
Etymologie
Der Cortico-Teil des Namens bezieht sich auf die Nebennierenrinde, die diese Steroidhormone herstellt. Ein Kortikosteroid ist also ein "Rindensteroid". ⓘ
Synthese
Die unterschiedlichen Hormone werden aus Progesteron durch Hydroxylierung (Einbau von OH-Gruppen) und Oxidation dieser Gruppen zu Keto- oder Aldehydgruppen an verschiedenen Positionen gebildet. Die Synthese und Sekretion der Androgene und Glucocorticoide wird durch ACTH (Kortikotropin) aus der Adenohypophyse (Hypophysenvorderlappen der Hirnanhangdrüse) stimuliert. Die Synthese und Sekretion der Mineralocorticoide wird über Angiotensin II und Kalium stimuliert. ⓘ
Wirkung
Als lipophile Hormone wirken Corticosteroide auf Rezeptoren im Zytosol und Zellkern, zu denen sie frei durch die Zellmembran diffundieren können. Inzwischen wird aber auch die Existenz von membranständigen Rezeptoren für Kortikoide angenommen und erforscht. Die Rezeptoren im Zellinneren kann man in zwei Typen aufteilen. Typ I ist spezifisch für Mineralcorticoide und Typ II für Glucocorticoide. Die Spezifität der Rezeptoren scheint von der Aktivität der 11β-Hydroxysteroid-Dehydrogenase 1 abhängig zu sein, die durch eine Dehydrierung der β-OH-Gruppe am C11Atom erfolgt. Dadurch werden die Corticoide (mit Ausnahme des Aldosterons) unwirksam. Exzessiver Genuss von Lakritze kann die 11-Hydroxysteroid-Dehydrogenase hemmen und so zu stärkeren Wirkungen der Mineralcorticoide führen. ⓘ
Überproduktion, Mangel
Krankhafte Überproduktion, etwa bei Stress, oder langdauernde Einnahme von Glucocorticoiden erzeugen ein charakteristisches Krankheitsbild (Cushing-Syndrom) mit Osteoporose, Diabetes mellitus, Fettsucht (v. a. Stammfettsucht) und Muskelschwund. Zu hohe Mineralocorticoid-Konzentrationen stören den Wasser-Elektrolythaushalt und schädigen die Nieren (Conn-Syndrom). ⓘ
Ein Mangel an Nebennierenrindenhormonen erzeugt den Morbus Addison, eine lebensbedrohliche Erkrankung mit Kreislaufschwäche, Austrocknung und Kachexie. Ein bestimmter Gendefekt, bei dem zu viel Androgene und zu wenig Aldosteron produziert werden, verursacht Virilismus und Wassereinlagerung; das Vollbild der Krankheit wird als adrenogenitales Syndrom bezeichnet. ⓘ
Abbau
Corticoide werden in der Leber durch Reduktion zu inaktiven Derivaten (17-Hydroxysteroide, 17-Ketosteroide) umgewandelt und über Urin und Gallenflüssigkeit ausgeschieden. ⓘ
Therapie
Außer bei den o. g. Mangelzuständen werden vor allem Glucocorticoide in zahlreichen Immunerkrankungen und Notfallsituationen als Medikament eingesetzt. Die natürlichen Corticoide sind gegenüber den künstlichen Corticoiden schwächer wirksam. Medikamente mit einer höheren Affinität binden sich leichter an die Rezeptoren und haben bei gleicher Arzneimittelkonzentration eine größere Wirkung. ⓘ
Für die orale und intravenöse Therapie werden Äquivalenzdosen (die gleichwirksame Dosis Cortison) angegeben. Prednison (17α,21-Dihydroxy-1,4-pregnadien-3,20-dion) ist ein künstliches Corticoid, welches einer dehydrierten Variante des Cortisons entspricht. Seine Wirkung liegt etwa bei der vier- bis fünffachen des Cortisons. ⓘ
Corticoide werden zur Behandlung von u. a. Autoimmunerkrankungen wie Asthma, Cluster-Kopfschmerz, Ekzemen, Epilepsie, Hörsturz sowie akutem Tinnitus, Nephritis, Neurodermitis und bei bestimmten Chemotherapien (Morbus Hodgkin, NHL) eingesetzt. ⓘ