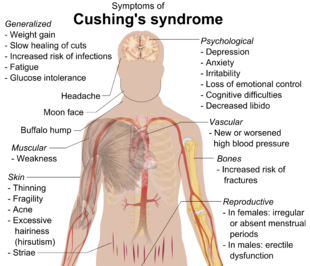
Cushing-Syndrom
| Cushing-Syndrom ⓘ | |
|---|---|
| Andere Bezeichnungen | Hyperkortisolismus, Itsenko-Cushing-Syndrom, Hyperadrenokortizismus |
 | |
| Gesichtsausdruck der Person 3 Monate nach der Behandlung mit inhaliertem Fluticason | |
| Fachgebiet | Endokrinologie |
| Symptome | Hoher Blutdruck, abdominale Adipositas mit dünnen Armen und Beinen, rötliche Dehnungsstreifen, rundes rotes Gesicht, Fettklumpen zwischen den Schultern, schwache Muskeln, Akne, brüchige Haut |
| Komplikationen | Hoher Blutdruck (Hypertonie), Typ-2-Diabetes, häufige oder ungewöhnliche Infektionen, Verlust von Muskelmasse und -kraft, Knochenschwund (Osteoporose). |
| Übliches Auftreten | 20-50 Jahre |
| Ursachen | Längerer Kontakt mit Cortisol |
| Diagnostische Methode | Erfordert eine Reihe von Schritten |
| Behandlung | Abhängig von der zugrunde liegenden Ursache |
| Prognose | Im Allgemeinen gut mit Behandlung |
| Häufigkeit | 2-3 pro Million Menschen pro Jahr (von 1/333.333 bis 1/500.000 Menschen) |
Beim Cushing-Syndrom handelt es sich um eine Reihe von Anzeichen und Symptomen, die auf eine anhaltende Exposition gegenüber Glukokortikoiden wie Cortisol zurückzuführen sind. Zu den Anzeichen und Symptomen gehören Bluthochdruck, abdominale Fettleibigkeit mit dünnen Armen und Beinen, rötliche Dehnungsstreifen, ein rundes rotes Gesicht, ein Fettklumpen zwischen den Schultern, schwache Muskeln, schwache Knochen, Akne und brüchige Haut, die schlecht heilt. Frauen haben möglicherweise mehr Haare und eine unregelmäßige Menstruation. Gelegentlich können Stimmungsschwankungen, Kopfschmerzen und ein chronisches Müdigkeitsgefühl auftreten. ⓘ
Das Cushing-Syndrom wird entweder durch eine übermäßige Einnahme von cortisolähnlichen Medikamenten wie Prednison oder durch einen Tumor verursacht, der entweder eine übermäßige Cortisolproduktion in den Nebennieren hervorruft oder zur Folge hat. Fälle, die auf ein Hypophysenadenom zurückzuführen sind, werden als Morbus Cushing bezeichnet, der nach Medikamenten die zweithäufigste Ursache für das Cushing-Syndrom ist. Eine Reihe anderer Tumoren, die aufgrund ihrer Lage außerhalb der Hypophyse oft als ektopisch bezeichnet werden, können ebenfalls das Cushing-Syndrom verursachen. Einige dieser Tumoren stehen im Zusammenhang mit Erbkrankheiten wie der multiplen endokrinen Neoplasie Typ 1 und dem Carney-Komplex. Die Diagnose erfordert eine Reihe von Schritten. Der erste Schritt ist die Überprüfung der Medikamente, die eine Person einnimmt. Der zweite Schritt ist die Messung des Cortisolspiegels im Urin, im Speichel oder im Blut nach der Einnahme von Dexamethason. Fällt dieser Test abnormal aus, kann das Cortisol spät in der Nacht gemessen werden. Bleibt der Cortisolwert hoch, kann ein Bluttest auf ACTH durchgeführt werden. ⓘ
Die meisten Fälle können behandelt und geheilt werden. Wenn die Ursache in der Einnahme von Medikamenten liegt, können diese oft langsam reduziert oder abgesetzt werden, wenn sie noch erforderlich sind. Wird die Krankheit durch einen Tumor verursacht, kann sie durch eine Kombination aus Operation, Chemotherapie und/oder Bestrahlung behandelt werden. Wenn die Hypophyse betroffen war, können andere Medikamente erforderlich sein, um die verlorene Funktion zu ersetzen. Mit der Behandlung ist die Lebenserwartung in der Regel normal. Bei einigen Patienten, bei denen die Operation den Tumor nicht vollständig entfernen kann, besteht ein erhöhtes Sterberisiko. ⓘ
Jährlich sind etwa zwei bis drei Menschen pro Million betroffen. Am häufigsten sind Menschen im Alter von 20 bis 50 Jahren betroffen. Frauen sind dreimal so häufig betroffen wie Männer. Ein leichter Grad der Überproduktion von Cortisol ohne offensichtliche Symptome ist jedoch häufiger. Das Cushing-Syndrom wurde erstmals von dem amerikanischen Neurochirurgen Harvey Cushing im Jahr 1932 beschrieben. Das Cushing-Syndrom kann auch bei anderen Tieren wie Katzen, Hunden und Pferden auftreten. ⓘ
| Klassifikation nach ICD-10 ⓘ | |
|---|---|
| E24 | Cushing-Syndrom |
| ICD-10 online (WHO-Version 2019) | |
Anzeichen und Symptome

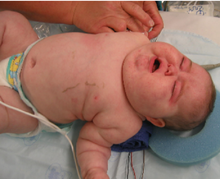
Zu den Symptomen gehört eine rasche Gewichtszunahme, insbesondere am Rumpf und im Gesicht, wobei die Gliedmaßen verschont bleiben (zentrale Fettleibigkeit). Häufige Anzeichen sind das Wachstum von Fettpolstern entlang des Schlüsselbeins, auf der Rückseite des Halses ("Büffelbuckel" oder Lipodystrophie) und im Gesicht ("Mondgesicht"). Weitere Symptome sind übermäßiges Schwitzen, Erweiterung der Kapillaren, Ausdünnung der Haut (was zu leichten Blutergüssen und Trockenheit führt, vor allem an den Händen) und der Schleimhäute, violette oder rote Striemen (die Gewichtszunahme beim Cushing-Syndrom dehnt die Haut aus, (die Gewichtszunahme beim Cushing-Syndrom dehnt die Haut, die dünn und geschwächt ist, was zu Blutungen führt) an Rumpf, Gesäß, Armen, Beinen oder Brüsten, proximale Muskelschwäche (Hüften, Schultern) und Hirsutismus (männlicher Haarwuchs im Gesicht), Kahlheit und/oder extrem trockenes und brüchiges Haar. In seltenen Fällen kann das Cushing-Syndrom eine Hypokalzämie verursachen. Das überschüssige Cortisol kann sich auch auf andere endokrine Systeme auswirken und z. B. Schlaflosigkeit, gehemmte Aromatase, verminderte Libido und Impotenz bei Männern sowie Amenorrhoe, Oligomenorrhoe und Unfruchtbarkeit bei Frauen aufgrund erhöhter Androgene verursachen. Studien haben auch gezeigt, dass die daraus resultierende Amenorrhoe auf Hypercortisolismus zurückzuführen ist, der auf den Hypothalamus zurückwirkt und zu einer verminderten GnRH-Freisetzung führt. ⓘ
Viele der Merkmale des Cushing-Syndroms entsprechen denen des metabolischen Syndroms, einschließlich Insulinresistenz, Bluthochdruck, Fettleibigkeit und erhöhter Triglyceridwerte im Blut. ⓘ
Kognitive Störungen, einschließlich Gedächtnis- und Aufmerksamkeitsstörungen sowie Depressionen, werden häufig mit einem erhöhten Cortisolspiegel in Verbindung gebracht und können Frühindikatoren für ein exogenes oder endogenes Cushing sein. Auch Depressionen und Angstzustände sind häufig. ⓘ
Weitere auffällige und beunruhigende Hautveränderungen, die beim Cushing-Syndrom auftreten können, sind Akne im Gesicht, Anfälligkeit für oberflächliche Pilzinfektionen (Dermatophyten und Malassezien) und die charakteristischen violetten, atrophischen Striemen auf dem Bauch. ⓘ
Weitere Anzeichen sind vermehrtes Wasserlassen (und damit einhergehender erhöhter Durst), anhaltender Bluthochdruck (aufgrund der Verstärkung der gefäßverengenden Wirkung von Adrenalin durch Cortisol) und Insulinresistenz (besonders häufig bei ACTH-Produktion außerhalb der Hypophyse), was zu hohem Blutzucker und Insulinresistenz führt, die zu Diabetes mellitus führen kann. Die Insulinresistenz geht mit Hautveränderungen wie Acanthosis nigricans in der Achselhöhle und im Nackenbereich sowie mit Hautmarkierungen in der Achselhöhle einher. Unbehandelt kann das Cushing-Syndrom zu Herzkrankheiten und einer erhöhten Sterblichkeit führen. Cortisol kann in hohen Konzentrationen auch eine mineralokortikoide Aktivität aufweisen, was die Hypertonie verschlimmert und zu Hypokaliämie (häufig bei ektopischer ACTH-Sekretion) und Hypernatriämie (erhöhte Na+-Ionen-Konzentration im Plasma) führt. Darüber hinaus kann übermäßiges Cortisol zu gastrointestinalen Störungen, opportunistischen Infektionen und einer gestörten Wundheilung führen, die auf die Unterdrückung der Immun- und Entzündungsreaktionen durch Cortisol zurückzuführen ist. Auch Osteoporose ist beim Cushing-Syndrom ein Thema, da die Aktivität der Osteoblasten gehemmt ist. Außerdem kann das Cushing-Syndrom zu schmerzenden Gelenken führen, insbesondere in der Hüfte, den Schultern und im unteren Rücken. ⓘ
Gehirnveränderungen wie z. B. eine Hirnatrophie können auftreten. Diese Atrophie ist mit Bereichen hoher Glukokortikoidrezeptorkonzentrationen wie dem Hippocampus verbunden und korreliert in hohem Maße mit psychopathologischen Persönlichkeitsveränderungen.
- Schnelle Gewichtszunahme
- Stimmungsschwankungen, Reizbarkeit oder Depression
- Muskel- und Knochenschwäche
- Gedächtnis- und Aufmerksamkeitsstörungen
- Osteoporose
- Diabetes mellitus
- Bluthochdruck
- Unterdrückung des Immunsystems
- Schlafstörungen
- Menstruationsstörungen wie Amenorrhoe bei Frauen
- Unfruchtbarkeit bei Frauen
- Impotenz bei Männern
- Hirsutismus
- Kahlheit
- Hypercholesterinämie ⓘ
- (mäßige) Adipositas mit Bevorzugung des Stammes (Stammfettsucht)
- rundes, pausbackiges, gerötetes Gesicht (Vollmondgesicht)
- pralles Doppelkinn
- „Stiernacken“, auch „Büffelnacken“ und „Büffelhöcker“ genannt, bedingt durch Fettansammlung zwischen den Schultern
- Stoffwechsellage wie bei Diabetes mellitus mit Durst und häufigem Wasserlassen
- (geringe) Arterielle Hypertonie
- oft Hirsutismus (übermäßige Behaarung) und Akne
- Gynäkomastie oder Pseudogynäkomastie
- Hypogonadismus, Libido- und Potenzminderung bei Männern
- Menstruationsstörungen (Oligo- und Amenorrhoe)
- Osteoporose
- Hautatrophie
- dünner werdende Haut und Bildung von rotviolettfarbenen breiten Gewebsstreifen (sogenannte Striae rubrae)
- leichte Ermüdbarkeit
- Verminderung der Muskelmasse (Muskelatrophie) mit schlankwirkenden Extremitäten (dünne Beine) mit proximaler Muskelschwäche der Extremitäten, auch Herzschwäche
- Suffusionen, vor allem an den Streckseiten der Vorderarme, durch erhöhte Kapillarfragilität
- positives Rumpel-Leede-Zeichen
- Plethora
- vermehrte Pigmentierung der Haut
- Wasseransammlungen im Gewebe (Ödeme)
- Bildung von Nierensteinen
- Rückenschmerzen
- erhöhte Infektanfälligkeit und langsames Heilen von Wunden, Pyodermien, Nagelmykosen
- Plötzlich auftretende Gelenksschmerzen, die kommen und gehen
- endokrines Psychosyndrom (mit psychischen Wesensveränderungen) ⓘ
Eine spezielle Form des Cushing-Syndroms mit ähnlicher Symptomatik ist das Achard-Thiers-Syndrom. ⓘ
Hyperpigmentierung
Das Cushing-Syndrom aufgrund eines ACTH-Überschusses kann auch zu einer Hyperpigmentierung führen. Dies ist auf die Produktion von melanozytenstimulierendem Hormon als Nebenprodukt der ACTH-Synthese aus Pro-Opiomelanocortin (POMC) zurückzuführen. Alternativ wird vorgeschlagen, dass die hohen Spiegel von ACTH, β-Lipotropin und γ-Lipotropin, die eine schwache MSH-Funktion aufweisen, auf den Melanocortin-1-Rezeptor wirken können. Eine Variante des Cushing-Syndroms kann durch eine ektopische, d. h. zusätzliche hypophysäre ACTH-Produktion verursacht werden, z. B. durch ein kleinzelliges Lungenkarzinom. ⓘ
Wenn das Cushing-Syndrom durch einen Anstieg des Cortisols auf der Ebene der Nebennieren (über ein Adenom oder eine Hyperplasie) verursacht wird, reduziert die negative Rückkopplung schließlich die ACTH-Produktion in der Hypophyse. In diesen Fällen bleibt der ACTH-Spiegel niedrig und es entwickelt sich keine Hyperpigmentierung. ⓘ
Ursachen
Das Cushing-Syndrom kann aus jeder Ursache für erhöhte Glukokortikoidspiegel resultieren, sei es aufgrund von Medikamenten oder internen Prozessen. Einige Quellen betrachten den durch Glukokortikoid-Medikamente hervorgerufenen Zustand jedoch nicht als "Cushing-Syndrom" im eigentlichen Sinne, sondern verwenden stattdessen den Begriff "Cushingoid", um die Nebenwirkungen der Medikamente zu beschreiben, die den endogenen Zustand nachahmen. ⓘ
Das Cushing-Syndrom ist eine spezifische Form des Cushing-Syndroms, die durch einen Hypophysentumor verursacht wird, der zu einer übermäßigen Produktion von ACTH (adrenocorticotropes Hormon) führt. Das überschüssige ACTH regt die Nebennierenrinde zur Produktion hoher Cortisolspiegel an, wodurch der Krankheitszustand entsteht. Zwar führt jedes Cushing-Syndrom zu einem Cushing-Syndrom, aber nicht jedes Cushing-Syndrom ist auf das Cushing-Syndrom zurückzuführen. Es sind mehrere mögliche Ursachen des Cushing-Syndroms bekannt. ⓘ
Exogenes
Die häufigste Ursache des Cushing-Syndroms ist die Verabreichung von Glukokortikoiden zur Behandlung anderer Krankheiten (iatrogenes Cushing-Syndrom). Glukokortikoide werden bei der Behandlung einer Vielzahl von Erkrankungen eingesetzt, darunter Asthma und rheumatoide Arthritis, und auch zur Immunsuppression nach Organtransplantationen verwendet. Auch die Verabreichung von synthetischem ACTH ist möglich, doch wird ACTH aufgrund der Kosten und des geringeren Nutzens seltener verschrieben. In seltenen Fällen kann das Cushing-Syndrom auch auf die Verwendung von Medroxyprogesteronacetat zurückzuführen sein. Beim exogenen Cushing-Syndrom können die Nebennieren oft allmählich verkümmern, weil die Stimulation durch ACTH fehlt, dessen Produktion durch Glukokortikoid-Medikamente unterdrückt wird. Ein abruptes Absetzen des Medikaments kann daher zu einer akuten und potenziell lebensbedrohlichen Nebenniereninsuffizienz führen, so dass die Dosis langsam und vorsichtig reduziert werden muss, damit die interne Cortisolproduktion wieder anlaufen kann. In einigen Fällen erreichen die Patienten nie wieder ein ausreichendes Niveau der körpereigenen Produktion und müssen lebenslang Glukokortikoide in physiologischer Dosierung einnehmen. ⓘ
Das Cushing-Syndrom im Kindesalter ist besonders selten und meist eine Folge der Einnahme von Glukokortikoid-Medikamenten. ⓘ
Endogenes
Das endogene Cushing-Syndrom entsteht durch eine Störung des körpereigenen Systems der Cortisolsekretion. Normalerweise wird ACTH von der Hypophyse bei Bedarf freigesetzt, um die Freisetzung von Cortisol aus den Nebennieren zu stimulieren.
- Beim hypophysären Cushing-Syndrom sezerniert ein gutartiges Hypophysenadenom ACTH. Dies wird auch als Cushing-Syndrom bezeichnet und ist für 70 % des endogenen Cushing-Syndroms verantwortlich.
- Beim adrenalen Cushing-Syndrom wird überschüssiges Cortisol von Nebennierentumoren, hyperplastischen Nebennieren oder Nebennieren mit knotiger Nebennierenhyperplasie produziert.
- Tumore außerhalb des normalen Hypophysen-Nebennieren-Systems können ACTH (gelegentlich zusammen mit CRH) produzieren, das die Nebennieren beeinflusst. Diese Ätiologie wird als ektopes oder paraneoplastisches Cushing-Syndrom bezeichnet und tritt bei Krankheiten wie kleinzelligem Lungenkrebs auf.
- Schließlich wurden seltene Fälle von CRH-sezernierenden Tumoren (ohne ACTH-Sekretion) berichtet, die die ACTH-Produktion der Hypophyse anregen. ⓘ
Pseudo-Cushing-Syndrom
Erhöhte Gesamtkortisolwerte können auch auf Östrogen zurückzuführen sein, das in oralen Verhütungspillen enthalten ist, die eine Mischung aus Östrogen und Progesteron enthalten, was zum Pseudo-Cushing-Syndrom führt. Östrogen kann zu einem Anstieg des kortisolbindenden Globulins und damit zu einer Erhöhung des Gesamtkortisolspiegels führen. Das gesamte freie Cortisol, das aktive Hormon im Körper, das durch eine 24-Stunden-Urinsammlung für freies Cortisol im Urin gemessen wird, ist jedoch normal. ⓘ
Pathophysiologie
Der Hypothalamus befindet sich im Gehirn und die Hypophyse sitzt direkt darunter. Der paraventrikuläre Kern (PVN) des Hypothalamus setzt Corticotropin-Releasing-Hormon (CRH) frei, das die Hypophyse zur Ausschüttung von Adrenocorticotropin (ACTH) anregt. ACTH gelangt über das Blut in die Nebenniere, wo es die Ausschüttung von Cortisol anregt. Cortisol wird von der Nebennierenrinde aus einer Region namens Zona fasciculata als Reaktion auf ACTH ausgeschüttet. Erhöhte Cortisolspiegel üben eine negative Rückkopplung auf CRH im Hypothalamus aus, wodurch die ACTH-Ausschüttung des Hypophysenvorderlappens verringert wird. ⓘ
Streng genommen bezieht sich das Cushing-Syndrom auf einen Cortisolüberschuss jeglicher Ätiologie (denn Syndrom bedeutet eine Gruppe von Symptomen). Eine der Ursachen des Cushing-Syndroms ist ein cortisolproduzierendes Adenom in der Nebennierenrinde (primärer Hypercortisolismus/Hypercortizismus). Das Adenom verursacht einen sehr hohen Cortisolspiegel im Blut, und die negative Rückkopplung der hohen Cortisolspiegel auf die Hypophyse führt zu einem sehr niedrigen ACTH-Spiegel. ⓘ
Das Cushing-Syndrom bezieht sich nur auf Hyperkortisolismus, der sekundär auf eine übermäßige Produktion von ACTH durch ein kortikotropes Hypophysenadenom (sekundärer Hyperkortisolismus/Hyperkortizismus) oder auf eine übermäßige Produktion von CRH (Corticotropin-Releasing-Hormon) im Hypothalamus (tertiärer Hyperkortisolismus/Hyperkortizismus) zurückzuführen ist. Dies führt dazu, dass der ACTH-Spiegel im Blut zusammen mit dem Cortisol aus der Nebenniere erhöht ist. Die ACTH-Spiegel bleiben hoch, weil der Tumor nicht auf die negative Rückkopplung der hohen Cortisolspiegel reagiert. ⓘ
Wenn das Cushing-Syndrom auf zusätzliches ACTH zurückzuführen ist, wird es als ektopisches Cushing-Syndrom bezeichnet. Dies kann im Rahmen eines paraneoplastischen Syndroms vorkommen. ⓘ
Bei Verdacht auf das Cushing-Syndrom bieten entweder ein Dexamethason-Suppressionstest (Verabreichung von Dexamethason und häufige Bestimmung des Cortisol- und ACTH-Spiegels) oder eine 24-Stunden-Urinmessung des Cortisols gleiche Nachweisraten. Dexamethason ist ein Glucocorticoid und simuliert die Wirkungen von Cortisol, einschließlich der negativen Rückkopplung auf die Hypophyse. Wenn Dexamethason verabreicht und eine Blutprobe untersucht wird, sind Cortisolwerte von mehr als 50 nmol/l (1,81 μg/dl) ein Hinweis auf das Cushing-Syndrom, weil eine ektopische Cortisol- oder ACTH-Quelle (z. B. ein Nebennierenadenom) vorhanden ist, die durch das Dexamethason nicht gehemmt wird. Ein neuartiger Ansatz, der vor kurzem von der US-amerikanischen FDA genehmigt wurde, ist die Messung des Cortisolspiegels im Speichel über 24 Stunden, die möglicherweise ebenso empfindlich ist, da die Speichelcortisolwerte in der Nacht bei cushingoiden Patienten hoch sind. Möglicherweise müssen auch andere Hypophysenhormonspiegel bestimmt werden. Bei Verdacht auf eine Hypophysenläsion, die das Chiasma opticum zusammendrücken und eine typische bitemporale Hemianopie verursachen kann, kann eine körperliche Untersuchung zur Feststellung von Gesichtsfeldausfällen erforderlich sein. ⓘ
Fällt einer dieser Tests positiv aus, werden eine CT-Untersuchung der Nebenniere und eine MRT-Untersuchung der Hypophyse durchgeführt, um das Vorhandensein von Nebennieren- oder Hypophysenadenomen oder Inzidentalomen (zufällige Entdeckung harmloser Läsionen) festzustellen. Gelegentlich ist eine Szintigraphie der Nebenniere mit Jodocholesterin-Scan erforderlich. Gelegentlich ist die Bestimmung des ACTH-Spiegels in verschiedenen Venen des Körpers durch Venenkatheterisierung in Richtung Hypophyse (Sinus petrosus sampling) erforderlich. In vielen Fällen sind die Tumoren, die das Cushing-Syndrom verursachen, weniger als 2 mm groß und mit MRT- oder CT-Bildgebung schwer zu erkennen. In einer Studie an 261 Patienten mit bestätigtem hypophysären Cushing-Syndrom wurden nur 48 % der Hypophysenläsionen vor der Operation mittels MRT erkannt. ⓘ
Der CRH-Plasmaspiegel ist aufgrund der peripheren Verdünnung und der Bindung an CRHBP für die Diagnose unzureichend (mit der möglichen Ausnahme von Tumoren, die CRH sezernieren). ⓘ
Diagnose
Das Cushing-Syndrom kann durch eine Reihe von Tests festgestellt werden, zu denen die folgenden gehören:
- Freies Cortisol im 24-Stunden-Urin
- Dexamethason-Suppressionstest
- Cortisolspiegel im Speichel ⓘ
Behandlung
Die meisten Fälle von Cushingoid-Symptomen werden durch Kortikosteroid-Medikamente verursacht, wie sie bei Asthma, Arthritis, Ekzemen und anderen entzündlichen Erkrankungen eingesetzt werden. Daher können die meisten Patienten wirksam behandelt werden, indem die Medikamente, die die Symptome verursachen, vorsichtig reduziert (und schließlich abgesetzt) werden. ⓘ
Wenn ein Nebennierenadenom festgestellt wird, kann es durch einen chirurgischen Eingriff entfernt werden. Ein ACTH-sezernierendes kortikotropes Hypophysenadenom sollte nach der Diagnose entfernt werden. Unabhängig von der Lage des Adenoms benötigen die meisten Patienten zumindest in der Übergangszeit nach der Operation einen Steroidersatz, da sich die langfristige Unterdrückung des hypophysären ACTH und des normalen Nebennierengewebes nicht sofort erholt. Wenn beide Nebennieren entfernt werden, ist eine Substitution mit Hydrocortison oder Prednisolon unumgänglich. ⓘ
Bei Patienten, die nicht für einen chirurgischen Eingriff geeignet sind oder sich diesem nicht unterziehen wollen, wurden mehrere Medikamente zur Hemmung der Cortisol-Synthese gefunden (z. B. Ketoconazol, Metyrapon), die jedoch nur begrenzt wirksam sind. Mifepriston ist ein starker Glukokortikoid-Rezeptor-Antagonist vom Typ II und kann, da es die normale Cortisol-Homöostase vom Typ I nicht beeinträchtigt, besonders nützlich für die Behandlung der kognitiven Auswirkungen des Cushing-Syndroms sein. Allerdings ist das Medikament wegen seiner Verwendung als Abtreibungsmittel sehr umstritten. Im Februar 2012 genehmigte die FDA Mifepriston zur Kontrolle hoher Blutzuckerwerte (Hyperglykämie) bei erwachsenen Patienten, die nicht für eine Operation in Frage kommen oder die auf eine vorherige Operation nicht angesprochen haben, mit der Warnung, dass Mifepriston niemals von schwangeren Frauen verwendet werden sollte - obwohl eine Schwangerschaft im Verlauf des Cushing-Syndroms extrem selten ist, Isturisa (Osilodrostat) orale Tabletten, ein 11-beta-Hydroxylase-Enzymhemmer, wurde von der FDA für die Behandlung von Patienten zugelassen, die nicht an der Hypophyse operiert werden können, oder für Patienten, die bereits operiert wurden, aber weiterhin an der Krankheit leiden. ⓘ
Die Entfernung der Nebennieren ohne bekannten Tumor wird gelegentlich durchgeführt, um die Produktion von überschüssigem Cortisol zu unterbinden. In einigen Fällen wird dadurch die negative Rückkopplung von einem zuvor verborgenen Hypophysenadenom beseitigt, das schnell zu wachsen beginnt und extreme Mengen an ACTH produziert, was zu einer Hyperpigmentierung führt. Diese klinische Situation wird als Nelson-Syndrom bezeichnet. ⓘ
Epidemiologie
Das Cushing-Syndrom, das durch die Behandlung mit Kortikosteroiden verursacht wird, ist die häufigste Form. Das Cushing-Syndrom ist selten; eine dänische Studie ergab eine Inzidenz von weniger als einem Fall pro Million Menschen pro Jahr. Asymptomatische Mikroadenome (weniger als 10 mm groß) der Hypophyse werden jedoch bei etwa einem von sechs Menschen gefunden. ⓘ
Menschen mit Cushing-Syndrom haben im Vergleich zur Allgemeinbevölkerung eine erhöhte Morbidität und Mortalität. Die häufigste Todesursache beim Cushing-Syndrom sind kardiovaskuläre Ereignisse. Menschen mit Cushing-Syndrom haben eine fast viermal höhere kardiovaskuläre Sterblichkeit als die Allgemeinbevölkerung. ⓘ
Etwa 0,9 bis 1 % der Menschen mit Cushing-Syndrom neigen zur Entwicklung einer Venenthrombose. Andere Faktoren wie chirurgische Eingriffe und Fettleibigkeit erhöhen ebenfalls das Thromboserisiko. ⓘ
Andere Tiere
Weitere Informationen über die Form bei Pferden finden Sie unter Dysfunktion der Hypophyse pars intermedia. ⓘ
Cushing-Syndrom I
Cushing-Schwellendosis
In der Fachliteratur wird die Cushing-Schwellendosis mit der Wirkungsstärke von 7,5 mg Prednison oder 30–40 mg (bei Männern), 15–30 mg (bei Frauen) Cortisol pro Tag angegeben. ⓘ
Bei Kindern beträgt die Cushing-Schwellendosis 6 mg / m² Körperoberfläche / Tag Prednisonäquivalent (Prednison ist ca. viermal so wirksam wie Cortisol). Dies beschreibt die tägliche Erhaltungsdosis, die gerade noch kein Cushing-Syndrom auslösen soll. Allerdings ist diese Angabe als grobe Richtlinie zu verstehen, da erhebliche inter-individuelle Unterschiede bestehen. Eine absolute Untergrenze, unter der die Glukokortikoidtherapie als sicher anzusehen ist, besteht nicht. Topisch (auf der Haut) angewandte Glukokortikoidpräparate verursachen mit höchster Wahrscheinlichkeit kein Cushing-Syndrom, da sie nur zu sehr geringem Teil die Hautbarriere durchdringen. Dennoch wird empfohlen, die Therapie auf maximal 20 % der Körperoberfläche zu beschränken und zurückhaltend bei der Anwendung im Gesicht oder am Auge zu sein. ⓘ
Therapie
Die Therapie richtet sich nach der Ursache des Cushing-Syndroms: Adenome der Hypophyse oder der Nebennieren werden operativ entfernt; die Therapie der Wahl bei einer Nebennierenrinden-Hyperplasie ist die Adrenalektomie und eine sich anschließende lebenslange Hormonsubstitution zur Vermeidung der Ausbildung eines Morbus Addison. Als Komplikation kann sich danach ein Nelson-Tumor entwickeln. ⓘ
Die EU-Kommission hat im Januar 2020 Osilodrostat (Handelsname: Isturisa, Hersteller: Novartis) als orale Behandlung von erwachsenen Patienten mit endogenem Cushing-Syndrom zugelassen. Osilodrostat ist Hemmstoff der körpereigenen Cortisol-Biosynthese. ⓘ
Cushing-Syndrom II
Das Cushing-Syndrom II ist eine seltene Erkrankung, bei der ein Tumor im Bereich von Pons oder Cerebellum gleichseitige Schädigungen der Hirnnerven VI, VII und VIII hervorruft. Ausfallerscheinungen des Kleinhirns und Hirndruckzeichen sind im Rahmen dieser Erkrankung ebenfalls beschrieben. Die aktuelle Bezeichnung lautet Kleinhirnbrücken-Symptomatik. ⓘ
Der Erstbeschrieb erfolgte 1917 durch Harvey Williams Cushing. ⓘ
Diagnostische Kriterien sind: