Nebennierenrindeninsuffizienz
| Addisonsche Krankheit ⓘ | |
|---|---|
| Andere Bezeichnungen | Addison-Krankheit, primäre Nebenniereninsuffizienz, primäre Nebennierenrindeninsuffizienz, chronische Nebenniereninsuffizienz, chronische Nebennierenrindeninsuffizienz, primärer Hypokortikalismus, primärer Hypokortisolismus, primärer Hypoadrenokortizismus, primärer Hypokortizismus, primärer Hypoadrenalismus |
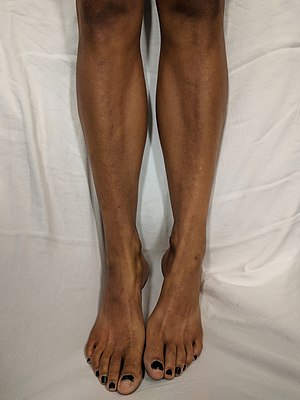 | |
| Dunkle Hautverfärbung an den Beinen eines Patienten mit einem Überschuss an Melanin. | |
| Fachgebiet | Endokrinologie |
| Symptome | Unterleibsschmerzen, Schwäche, Gewichtsverlust, Hautverdunkelung |
| Komplikationen | Nebennierenkrise |
| Übliches Auftreten | Frauen mittleren Alters |
| Ursachen | Probleme mit der Nebennierenrinde |
| Diagnostische Methode | Blutuntersuchungen, Urintests, medizinische Bildgebung |
| Behandlung | Synthetisches Kortikosteroid wie Hydrocortison und Fludrocortison |
| Häufigkeit | 0,9-1,4 pro 10.000 Menschen (entwickelte Welt) |
| Todesfälle | Verdoppelt das Sterberisiko |
Die Addison-Krankheit, auch bekannt als primäre Nebenniereninsuffizienz, ist eine seltene, langwierige endokrine Störung, die durch eine unzureichende Produktion der Steroidhormone Cortisol und Aldosteron durch die beiden äußeren Zellschichten der Nebennieren (Nebennierenrinde) gekennzeichnet ist und eine Nebenniereninsuffizienz verursacht. Die Symptome treten im Allgemeinen langsam und schleichend auf und können Bauchschmerzen und Magen-Darm-Anomalien, Schwäche und Gewichtsverlust umfassen. Auch eine Verdunkelung der Haut an bestimmten Stellen kann auftreten. Unter bestimmten Umständen kann es zu einer Nebennierenkrise mit niedrigem Blutdruck, Erbrechen, Schmerzen im unteren Rücken und Bewusstlosigkeit kommen. Auch Stimmungsschwankungen können auftreten. Ein schnelles Auftreten der Symptome deutet auf ein akutes Nebennierenversagen hin, das einen ernsten und dringenden Zustand darstellt. Eine Nebennierenkrise kann durch Stress ausgelöst werden, z. B. durch eine Verletzung, eine Operation oder eine Infektion. ⓘ
Die Addison-Krankheit entsteht durch Probleme mit der Nebenniere, so dass nicht genügend des Steroidhormons Cortisol und möglicherweise Aldosteron produziert werden. In den Industrieländern wird die Ätiologie der Addison-Krankheit häufig auf eine idiopathische Schädigung durch das körpereigene Immunsystem zurückgeführt, in den Entwicklungsländern am häufigsten auf Tuberkulose. Andere Ursachen sind bestimmte Medikamente, Sepsis und Blutungen in beide Nebennieren. Die sekundäre Nebenniereninsuffizienz wird durch einen Mangel an adrenocorticotropem Hormon (ACTH) (das von der Hypophyse produziert wird) oder an Corticotropin-releasing-Hormon (CRH) (das vom Hypothalamus produziert wird) verursacht. Trotz dieser Unterscheidung können Nebennierenkrisen bei allen Formen der Nebenniereninsuffizienz auftreten. Die Addison-Krankheit wird in der Regel durch Blut- und Urinuntersuchungen sowie durch medizinische Bildgebung diagnostiziert. ⓘ
Der Morbus Addison kann in Verbindung mit chronischer mukokutaner Candidiasis, erworbenem Hypoparathyreoidismus, Diabetes mellitus, perniziöser Anämie, Hypogonadismus, chronischer und aktiver Hepatitis, Malabsorption, Immunglobulinanomalien, Alopezie, Vitiligo, spontanem Myxödem, Morbus Basedow und chronischer lymphozytärer Thyreoiditis beschrieben werden. ⓘ
Die Behandlung besteht darin, die fehlenden Hormone zu ersetzen. Dazu gehört die Einnahme eines synthetischen Kortikosteroids wie Hydrocortison oder Fludrocortison. Diese Medikamente werden in der Regel über den Mund eingenommen. Eine lebenslange, kontinuierliche Steroidersatztherapie ist erforderlich, mit regelmäßiger Nachbehandlung und Überwachung auf andere Gesundheitsprobleme. Bei manchen Menschen kann auch eine salzreiche Diät sinnvoll sein. Wenn sich die Symptome verschlimmern, wird eine Kortikosteroid-Injektion empfohlen, und die Betroffenen sollten eine Dosis bei sich tragen. Häufig sind auch große Mengen an intravenöser Flüssigkeit mit dem Zucker Dextrose erforderlich. Unbehandelt kann eine Nebennierenkrise zum Tod führen. ⓘ
Die Addison-Krankheit betrifft etwa 9 bis 14 von 100.000 Menschen in den Industrieländern. Sie tritt am häufigsten bei Frauen im mittleren Alter auf. Die sekundäre Nebenniereninsuffizienz ist weiter verbreitet. Die Langzeitergebnisse der Behandlung sind in der Regel günstig. Sie ist nach Thomas Addison benannt, einem Absolventen der medizinischen Fakultät der Universität Edinburgh, der die Krankheit 1855 erstmals beschrieb. Das Adjektiv "addisonisch" wird verwendet, um die Merkmale der Krankheit sowie die Menschen mit Morbus Addison zu beschreiben. ⓘ
Die Nebennierenrindeninsuffizienz, kurz auch Nebenniereninsuffizienz, ist eine durch unzureichende Hormonproduktion gekennzeichnete Unterfunktion der Nebennierenrinde (NNR), die gut zu behandeln ist. ⓘ
| Klassifikation nach ICD-10 ⓘ | |
|---|---|
| E27.1 | Primäre Nebennierenrindeninsuffizienz Addison-Krankheit |
| E85 | Amyloidose |
| E35.1* | Krankheiten der Nebennieren bei anderenorts klassifizierten Krankheiten |
| A39.1+ | Waterhouse-Friderichsen-Syndrom |
| A18.7+ | Tuberkulose der Nebennieren |
| E23.0 | Hypopituitarismus |
| ICD-10 online (WHO-Version 2019) | |
Anzeichen und Symptome
Die Symptome der Addison-Krankheit entwickeln sich im Allgemeinen allmählich. Zu den Symptomen gehören Müdigkeit, Muskelschwäche, Gewichtsverlust, Übelkeit, Erbrechen, Appetitlosigkeit, Schwindelgefühl beim Aufstehen, Reizbarkeit, Depression und Durchfall. Manche Menschen haben aufgrund des Natriumverlusts über den Urin Heißhunger auf salzige Lebensmittel. Es kann zu einer Hyperpigmentierung der Haut kommen, insbesondere wenn die Betroffenen in einem sonnigen Gebiet leben, sowie zu einer Verdunkelung der Handwurzelfalte, von Reibungsstellen, frischen Narben, dem Zinnoberrand der Lippen und der Genitalhaut. Diese Hautveränderungen sind bei sekundärem und tertiärem Hypoadrenalismus nicht zu beobachten.
- Hautveränderungen
- Hyperpigmentierung der Haut
- Vitiligo
- Gastrointestinale Veränderungen
- Übelkeit und Erbrechen
- Gewichtsverlust
- Unterleibsschmerzen
- Seltener, aber dennoch vorkommend: Unterernährung und Muskelschwund
- Verhaltensauffälligkeiten
- Angstzustände
- Depressionen
- Reizbarkeit
- Schlechte Konzentration
- Veränderungen bei Frauen
- Ausfall oder Unregelmäßigkeit des Menstruationszyklus
- Verlust der Körperbehaarung
- Verminderter Sexualtrieb ⓘ
Bei der körperlichen Untersuchung können diese klinischen Anzeichen festgestellt werden:
- Niedriger Blutdruck mit oder ohne orthostatische Hypotonie (Blutdruck, der beim Stehen abfällt)
- Verdunkelung (Hyperpigmentierung) der Haut, auch an Stellen, die nicht der Sonne ausgesetzt sind - charakteristische Stellen der Verdunkelung sind Hautfalten (z. B. an den Händen), die Brustwarze und die Innenseite der Wange (Wangenschleimhaut); auch alte Narben können sich verdunkeln. Dies ist darauf zurückzuführen, dass das Melanozyten-stimulierende Hormon (MSH) und ACTH das gleiche Vorläufermolekül, das Pro-Opiomelanocortin (POMC), enthalten. Nach der Produktion im Hypophysenvorderlappen wird das POMC in gamma-MSH, ACTH und beta-Lipotropin gespalten. Die Untereinheit ACTH wird weiter gespalten, um alpha-MSH zu produzieren, das wichtigste MSH für die Hautpigmentierung. Bei sekundären und tertiären Formen der Nebenniereninsuffizienz kommt es nicht zur Hautverdunkelung, da kein ACTH überproduziert wird. ⓘ
Die Addison-Krankheit wird mit der Entwicklung anderer Autoimmunkrankheiten in Verbindung gebracht, z. B. Typ-I-Diabetes, Schilddrüsenerkrankungen (Hashimoto-Thyreoiditis), Zöliakie oder Vitiligo. Die Addison-Krankheit kann die einzige Manifestation einer undiagnostizierten Zöliakie sein. Beide Krankheiten haben die gleichen genetischen Risikofaktoren (HLA-DQ2- und HLA-DQ8-Haplotypen). ⓘ
Das Vorhandensein von Addison zusätzlich zu mukokutaner Candidose, Hypoparathyreoidismus oder beidem wird als autoimmunes polyendokrines Syndrom Typ 1 bezeichnet. Das Vorhandensein einer Addison-Krankheit zusätzlich zu einer autoimmunen Schilddrüsenerkrankung, einem Typ-1-Diabetes oder beidem wird als autoimmunes polyendokrines Syndrom Typ 2 bezeichnet. ⓘ
Nebennierenkrise
Eine "Nebennierenkrise" oder "addisonsche Krise" ist eine Konstellation von Symptomen, die auf eine schwere Nebenniereninsuffizienz hinweist. Sie kann die Folge einer zuvor nicht diagnostizierten Addison-Krankheit, eines plötzlich auftretenden Krankheitsprozesses, der die Nebennierenfunktion beeinträchtigt (z. B. eine Nebennierenblutung), oder eines interkurrenten Problems (z. B. Infektion, Trauma) bei einer Person mit bekannter Addison-Krankheit sein. Es handelt sich um einen medizinischen Notfall und eine potenziell lebensbedrohliche Situation, die eine sofortige Notfallbehandlung erfordert. ⓘ
Charakteristische Symptome sind:
- Plötzlich auftretende durchdringende Schmerzen in den Beinen, im unteren Rücken oder im Unterleib
- Starkes Erbrechen und Durchfall, was zu Dehydrierung führt
- Niedriger Blutdruck
- Synkope (Verlust des Bewusstseins und der Fähigkeit zu stehen)
- Hypoglykämie (verminderter Blutzuckerspiegel)
- Verwirrung, Psychose, undeutliche Sprache
- Schwere Lethargie
- Hyponatriämie (niedriger Natriumspiegel im Blut)
- Hyperkaliämie (erhöhter Kaliumspiegel im Blut)
- Hyperkalzämie (erhöhter Kalziumspiegel im Blut)
- Konvulsionen
- Fieber ⓘ
Ursachen

Die Ursachen der Nebenniereninsuffizienz lassen sich nach dem Mechanismus einteilen, durch den sie dazu führen, dass die Nebennieren zu wenig Cortisol produzieren. Dies kann auf eine Schädigung oder Zerstörung der Nebennierenrinde zurückzuführen sein. Zu diesen Mängeln gehören auch Glukokortikoid- und Mineralokortikoid-Hormone. Dabei handelt es sich um eine Nebennieren-Dysgenese (die Drüse hat sich während der Entwicklung nicht ausreichend gebildet), eine gestörte Steroidogenese (die Drüse ist vorhanden, aber biochemisch nicht in der Lage, Cortisol zu produzieren) oder eine Nebennieren-Zerstörung (Krankheitsprozesse, die zu einer Schädigung der Drüse führen). ⓘ
Zerstörung der Nebenniere
Autoimmunbedingte Nebennierenentzündung ist die häufigste Ursache der Addison-Krankheit in den Industrieländern. Die autoimmune Zerstörung der Nebennierenrinde wird durch eine Immunreaktion gegen das Enzym 21-Hydroxylase verursacht (ein Phänomen, das erstmals 1992 beschrieben wurde). Dies kann isoliert oder im Rahmen eines autoimmunen polyendokrinen Syndroms (APS Typ 1 oder 2) geschehen, bei dem auch andere hormonproduzierende Organe wie die Schilddrüse und die Bauchspeicheldrüse betroffen sein können. ⓘ
Die Zerstörung der Nebenniere ist auch ein Merkmal der Adrenoleukodystrophie und wenn die Nebennieren an der Metastasierung (Aussaat von Krebszellen aus anderen Körperregionen, insbesondere der Lunge), an Blutungen (z. B. beim Waterhouse-Friderichsen-Syndrom oder beim Antiphospholipid-Syndrom), an bestimmten Infektionen (Tuberkulose, Histoplasmose, Kokzidioidomykose) oder an der Ablagerung abnormaler Proteine bei Amyloidose beteiligt sind. ⓘ
Dysgenesie der Nebenniere
Alle Ursachen in dieser Kategorie sind genetisch bedingt und im Allgemeinen sehr selten. Dazu gehören Mutationen des Transkriptionsfaktors SF1, kongenitale Nebennierenhypoplasie aufgrund von Mutationen des DAX-1-Gens und Mutationen des ACTH-Rezeptor-Gens (oder verwandter Gene, wie beim Triple-A- oder Allgrove-Syndrom). DAX-1-Mutationen können in einem Syndrom mit Glycerinkinase-Mangel mit einer Reihe anderer Symptome gehäuft auftreten, wenn DAX-1 zusammen mit einer Reihe anderer Gene deletiert ist. ⓘ
Gestörte Steroidogenese
Zur Bildung von Cortisol benötigt die Nebenniere Cholesterin, das dann biochemisch in Steroidhormone umgewandelt wird. Zu den Störungen der Cholesterinzufuhr gehören das Smith-Lemli-Opitz-Syndrom und die Abetalipoproteinämie. Von den Synthesestörungen sind die kongenitale Nebennierenhyperplasie (in verschiedenen Formen: 21-Hydroxylase, 17α-Hydroxylase, 11β-Hydroxylase und 3β-Hydroxysteroid-Dehydrogenase), das lipoide CAH aufgrund eines Mangels an StAR und mitochondriale DNA-Mutationen am häufigsten. Einige Medikamente greifen in die Enzyme der Steroidsynthese ein (z. B. Ketoconazol), während andere den normalen Abbau der Hormone durch die Leber beschleunigen (z. B. Rifampicin, Phenytoin). ⓘ
Diagnose
Suggestive Merkmale
Routinemäßige Laboruntersuchungen können zeigen:
- Niedriger Blutzucker (bei Kindern schlimmer, da die glukogenen Wirkungen des Glukokortikoids wegfallen)
- Natriummangel im Blut, bedingt durch den Verlust der Produktion des Hormons Aldosteron, durch die Unfähigkeit der Niere, freies Wasser auszuscheiden, wenn nicht genügend Cortisol vorhanden ist, und durch die Wirkung des Corticotropin-Releasing-Hormons, das die Sekretion von ADH stimuliert.
- Erhöhter Kaliumspiegel im Blut aufgrund des Ausfalls der Produktion des Hormons Aldosteron.
- Eosinophilie und Lymphozytose (erhöhte Anzahl von Eosinophilen oder Lymphozyten, zwei Arten von weißen Blutkörperchen)
- Metabolische Azidose (erhöhter Säuregehalt des Blutes) ist ebenfalls auf den Verlust des Hormons Aldosteron zurückzuführen, da die Natriumrückresorption im distalen Tubulus mit der Sekretion von Säure/Wasserstoffionen (H+) verbunden ist. Eine fehlende oder unzureichende Stimulation des distalen Nierentubulus durch Aldosteron führt zu Natriumverlusten im Urin und H+-Retention im Serum. ⓘ
Testen

Bei Verdacht auf Morbus Addison ist für die Diagnose der Nachweis niedriger Nebennierenhormonspiegel auch nach entsprechender Stimulation (ACTH-Stimulationstest oder Synacthen-Test genannt) mit dem synthetischen Hypophysen-ACTH-Hormon Tetracosactid erforderlich. Es werden zwei Tests durchgeführt, der kurze und der lange Test. Dexamethason zeigt keine Kreuzreaktion mit dem Test und kann während des Tests verabreicht werden. ⓘ
Beim Kurztest werden die Cortisolwerte im Blut vor und nach der Verabreichung von 250 Mikrogramm Tetracosactid (intramuskulär oder intravenös) verglichen. Wenn eine Stunde später das Plasmacortisol über 170 nmol/l liegt und um mindestens 330 nmol/l auf mindestens 690 nmol/l angestiegen ist, wird eine Nebenniereninsuffizienz ausgeschlossen. Fällt der Kurztest abnormal aus, wird der Langtest verwendet, um zwischen einer primären Nebenniereninsuffizienz und einer sekundären Nebennierenrindeninsuffizienz zu unterscheiden. ⓘ
Für den langen Test wird 1 mg Tetracosactid (intramuskulär) verwendet. Die Blutentnahme erfolgt 1, 4, 8 und 24 Stunden später. Der normale Plasmakortisolspiegel sollte innerhalb von 4 Stunden 1.000 nmol/l erreichen. Bei der primären Addison-Krankheit ist der Cortisolspiegel in allen Stadien reduziert, während bei der sekundären Nebenniereninsuffizienz eine verzögerte, aber normale Reaktion zu beobachten ist. Zur Unterscheidung zwischen den verschiedenen Ursachen des Hypoadrenalismus können weitere Tests durchgeführt werden, darunter die Bestimmung des Renin- und des adrenokortikotropen Hormonspiegels sowie bildgebende Untersuchungen - in der Regel in Form von Ultraschall, Computertomographie oder Magnetresonanztomographie. ⓘ
Die Adrenoleukodystrophie und die mildere Form, die Adrenomyeloneuropathie, verursachen eine Nebenniereninsuffizienz in Kombination mit neurologischen Symptomen. Diese Erkrankungen sind schätzungsweise bei etwa 35 % der diagnostizierten Männer mit idiopathischer Addison-Krankheit die Ursache der Nebenniereninsuffizienz und sollten bei der Differenzialdiagnose aller Männer mit Nebenniereninsuffizienz in Betracht gezogen werden. Die Diagnose wird durch einen Bluttest zum Nachweis sehr langkettiger Fettsäuren gestellt. ⓘ
Behandlung
Wartung
Die Behandlung der Addison-Krankheit besteht darin, das fehlende Cortisol zu ersetzen, manchmal in Form von Hydrocortison-Tabletten oder Prednison-Tabletten in einem Dosierungsschema, das die physiologischen Cortisol-Konzentrationen nachahmt. Alternativ kann bei gleicher Glukokortikoidwirkung wie Hydrocortison ein Viertel der Prednisolonmenge verwendet werden. Die Behandlung ist in der Regel lebenslang. Darüber hinaus benötigen viele Menschen Fludrocortison als Ersatz für das fehlende Aldosteron. ⓘ
Menschen mit Morbus Addison wird oft geraten, Informationen bei sich zu tragen (z. B. in Form eines MedicAlert-Armbands oder einer Informationskarte), damit sie von medizinischen Notdiensten, die sich um sie kümmern müssen, benachrichtigt werden können. Es wird auch empfohlen, eine Nadel, eine Spritze und eine injizierbare Form von Cortisol für Notfälle bei sich zu tragen. Menschen mit Morbus Addison wird empfohlen, ihre Medikation in Krankheitszeiten oder bei Operationen oder Zahnbehandlungen zu erhöhen. Bei schweren Infektionen, Erbrechen oder Durchfall ist sofortige ärztliche Hilfe erforderlich, da diese Zustände eine Addisonsche Krise auslösen können. Eine Person, die erbricht, benötigt möglicherweise stattdessen Hydrocortison-Injektionen. ⓘ
Personen mit niedrigem Aldosteronspiegel können auch von einer natriumreichen Diät profitieren. Für Menschen mit Morbus Addison kann es auch von Vorteil sein, ihre Kalzium- und Vitamin-D-Zufuhr zu erhöhen. Hohe Kortikosteroiddosen werden mit Osteoporose in Verbindung gebracht, so dass sie für die Knochengesundheit notwendig sein können. Zu den Kalziumquellen gehören unter anderem Milchprodukte, Blattgemüse und angereichertes Mehl. Vitamin D kann unter anderem über die Sonne, fetten Fisch, rotes Fleisch und Eigelb aufgenommen werden. Obwohl es viele Quellen gibt, um Vitamin D über die Ernährung zu erhalten, entscheiden sich viele Menschen für ein Nahrungsergänzungsmittel. ⓘ
Krisensituation
Die Standardtherapie umfasst intravenöse Injektionen von Glukokortikoiden und große Mengen intravenöser Kochsalzlösung mit Traubenzucker (Glukose). Diese Behandlung führt in der Regel zu einer raschen Besserung. Wenn ein intravenöser Zugang nicht sofort möglich ist, können Glukokortikoide auch intramuskulär injiziert werden. Wenn der Betroffene Flüssigkeit und Medikamente über den Mund einnehmen kann, wird die Menge der Glukokortikoide verringert, bis eine Erhaltungsdosis erreicht ist. Bei Aldosteronmangel umfasst die Erhaltungstherapie auch orale Dosen von Fludrocortisonacetat. ⓘ
Prognose
Die Ergebnisse der Behandlung sind in der Regel gut. Die meisten können ein relativ normales Leben führen. Betroffene sollten auf die Symptome einer "Addison-Krise" achten, wenn der Körper stark beansprucht wird, z. B. bei anstrengender körperlicher Betätigung oder bei Krankheit, wobei in letzterem Fall häufig eine Notfallbehandlung mit intravenösen Injektionen zur Behandlung der Krise erforderlich ist. ⓘ
Die Sterblichkeitsrate von Menschen mit Addison-Krankheit ist mehr als doppelt so hoch. Außerdem ist die Sterblichkeitsrate bei Personen mit Morbus Addison und Diabetes mellitus im Vergleich zu Personen, die nur an Diabetes erkrankt sind, fast um das Vierfache erhöht. Das Risikoverhältnis für die ursächliche Sterblichkeit beträgt bei Männern 2,19 und bei Frauen 2,86. ⓘ
Der Tod von Personen mit Morbus Addison ist unter anderem auf Herz-Kreislauf-Erkrankungen, Infektionskrankheiten und bösartige Tumore zurückzuführen. ⓘ
Epidemiologie
Die Häufigkeit der Addison-Krankheit in der menschlichen Bevölkerung wird manchmal auf einen von 100.000 geschätzt. Manche schätzen die Zahl auf 40-144 Fälle pro Million Einwohner (1/25.000-1/7.000). Die Addison-Krankheit kann Personen jeden Alters, Geschlechts oder jeder ethnischen Zugehörigkeit betreffen, tritt aber typischerweise bei Erwachsenen zwischen 30 und 50 Jahren auf. Die Forschung hat keine signifikanten Prädispositionen aufgrund der ethnischen Zugehörigkeit gezeigt. Etwa 70 % der Diagnosen der Addison-Krankheit sind auf Autoimmunreaktionen zurückzuführen, die eine Schädigung der Nebennierenrinde verursachen. ⓘ
Geschichte
Die Addison-Krankheit ist nach dem britischen Arzt Thomas Addison benannt, der die Krankheit erstmals in seinem Buch On the Constitutional and Local Effects of Disease of the Suprarenal Capsules (1855) beschrieb. Ursprünglich bezeichnete er sie als "melasma suprarenale", aber spätere Ärzte gaben ihr in Anerkennung von Addisons Entdeckung den medizinischen Beinamen "Addisonsche Krankheit". ⓘ
Obwohl die sechs Personen, die 1855 unter Addison behandelt wurden, alle an einer Nebennierentuberkulose litten, impliziert der Begriff "Addison-Krankheit" keinen zugrunde liegenden Krankheitsprozess. ⓘ
Die Krankheit wurde zunächst als eine Form der Anämie angesehen, die mit den Nebennieren in Verbindung gebracht wurde. Da zu dieser Zeit nur wenig über die Nebennieren (damals "Supra-Renal-Kapseln" genannt) bekannt war, stellte Addisons Monographie, in der er die Krankheit beschrieb, eine isolierte Erkenntnis dar. Als die Funktion der Nebennieren besser bekannt wurde, wurde Addisons Monographie als ein wichtiger medizinischer Beitrag und ein klassisches Beispiel für sorgfältige medizinische Beobachtung bekannt. Sie ist auch heute noch eine der Hauptursachen in den Entwicklungsländern. ⓘ
Nebennierenrindeninsuffizienz bei Tieren
Eine Nebenniereninsuffizienz oder ein Hypoadrenokortizismus wird gelegentlich bei Haushunden beobachtet. In 95 % der Fälle handelt es sich um eine immunvermittelte primäre Nebenniereninsuffizienz (Morbus Addison), gelegentlich kann sie auch bei Überdosierung von Mitotan oder Trilostan bei Behandlung eines Cushing-Syndroms auftreten. Dabei kommt es zu einem Mangel an den in der Nebennierenrinde gebildeten Hormonen Cortisol (Glukokortikoid) und meist auch Aldosteron (Mineralokortikoid). Die Krankheit entwickelt sich oft schleichend und zeigt sich anfänglich häufig nur in wechselndem Allgemeinbefinden und Verschlechterung bei erhöhtem Stress. Abgeschlagenheit, Appetitlosigkeit, Schwäche, verminderte Leistungsfähigkeit, Gewichtsverlust und Erbrechen treten am häufigsten auf. Auch chronischer Durchfall, vermehrtes Trinken und Harnabsetzen sowie Bauchschmerzen können auftreten. Eine Addison-Krise verläuft dagegen dramatisch mit hochgradiger Schwäche, Austrocknung, Zusammenbrechen und plötzlichen Todesfällen. Eine rassespezifische Häufung tritt bei Pudel, Labradoodle und West Highland White Terrier auf. ⓘ
Typische Laborbefunde sind Hyponatriämie und Hyperkaliämie (bei etwa 80 bis 90 % der Hunde), (prärenale) Azotämie, nicht regenerative Anämie und Lymphozytose. Die basale Cortisolkonzentration liegt meist unter 2 µg/dl und bleibt beim ACTH-Stimulationstest unter dieser Schwelle. Stimulationswerte von 2,1 bis 5 µg/dl Cortisol gelten als Graubereich. Die Akutbehandlung eines Hundes in Addison-Krise basiert primär auf der intravenösen Verabreichung von physiologischer Kochsalzlösung und der Gabe eines Glukokortikoids. Zur Langzeitbehandlung ist seit 2016 in der EU Desoxycortonpivalat (Handelsname Zycortal) zugelassen. Es hat nur eine mineralokortikoide Wirkung und muss mit Prednisolon ergänzt werden. Zuvor wurden Hunde meist mit Fludrocortison mit oder ohne Zusatz von Prednisolon behandelt, allerdings ließ sich die Erkrankung bei einem Teil der Hunde damit nicht kontrollieren. ⓘ
Hypoadrenokortizismus ist bei Hunden unüblich und bei Katzen selten. Seit der ersten Dokumentation im Jahr 1983 sind weltweit weniger als 40 Fälle bei Katzen bekannt. Einzelne Fälle wurden bei einer Kegelrobbe, einem Roten Panda, einem Flughund und einem Faultier gemeldet. ⓘ
Bei Hunden ist Hypoadrenokortizismus bei vielen Rassen diagnostiziert worden. Vage Symptome, die zu- und abnehmen, können dazu führen, dass die Krankheit erst spät erkannt wird. Weibliche Hunde scheinen häufiger betroffen zu sein als männliche, obwohl dies nicht bei allen Rassen der Fall ist. Am häufigsten wird die Krankheit bei Hunden im jungen bis mittleren Alter diagnostiziert, sie kann jedoch in jedem Alter zwischen 4 Monaten und 14 Jahren auftreten. Bei der Behandlung des Hypoadrenokortizismus müssen die Hormone (Cortisol und Aldosteron) ersetzt werden, die der Hund nicht selbst produzieren kann. Dies wird entweder durch eine tägliche Behandlung mit Fludrocortison oder durch monatliche Injektionen mit Desoxycorticosteronpivalat (DOCP) und eine tägliche Behandlung mit einem Glucocorticoid wie Prednison erreicht. Es sind mehrere Nachuntersuchungen des Blutes erforderlich, damit die Dosis angepasst werden kann, bis der Hund die richtige Menge an Behandlung erhält, da die zur Therapie des Hypoadrenokortizismus verwendeten Medikamente übermäßigen Durst und Harndrang verursachen können, wenn sie nicht in der niedrigsten wirksamen Dosis verschrieben werden. In Erwartung von Stresssituationen, wie z. B. einem Aufenthalt in einer Hundepension, benötigen die Hunde eine erhöhte Prednisondosis. Eine lebenslange Behandlung ist erforderlich, aber die Prognose für Hunde mit Hypoadrenokortizismus ist sehr gut. ⓘ
Verbreitung
Eine Nebenniereninsuffizienz findet sich bei etwa 40 von 100.000 Menschen. ⓘ
Einteilung
Es werden nach der Entstehung drei Formen der Unterfunktion der Nebennierenrinde unterschieden. ⓘ
Sekundäre Nebennierenrindeninsuffizienz
Die sekundäre Form wird durch eine Unterfunktion der Hirnanhangdrüse (Hypophyseninsuffizienz) verursacht. Durch den Mangel an ACTH wird die Nebennierenrinde nicht ausreichend zur Bildung von Cortisol angeregt. Man vermutete früher eine „relative Nebennierenrindeninsuffizienz“ und nannte diese auch Hypadrenie und Addisonismus. Ursachen können sein:
- Tumoren
- Verletzungen (Schädel-Hirn-Trauma, Geburtstraumen)
- Durchblutungsstörungen, Sonderform: Sheehan-Syndrom
- Entzündungen
- Autoimmunreaktionen ⓘ
Tertiäre Nebennierenrindeninsuffizienz
Eine Unterfunktion des Hypothalamus verursacht die tertiäre Form. Hierbei wird zu wenig CRH gebildet, wodurch die Hirnanhangsdrüse nicht ausreichend zur Bildung von ACTH angeregt wird und es wie bei der sekundären Form zu einem relativen Mangel an ACTH kommt. Erkrankungen des Hypothalamus sind selten. Häufiger ist eine länger andauernde höher dosierte Behandlung mit Corticosteroiden. Hierdurch wird die CRH-Bildung längerfristig unterdrückt, abruptes Absetzen kann zu einer Addisonkrise führen. ⓘ
Patienten, die länger als fünf Tage Cortisonpräparate oberhalb der Cushing-Schwellendosis einnehmen, muss bei Operationen zusätzliches Cortisol verabreicht werden, da der Körper den bei Operationen notwendigen Cortisolstoß nicht selber erzeugen kann. Bei kleinen Operationen reicht dabei eine einmalige Cortisoldosis. Bei größeren Operationen sollte über die ersten 24 Stunden zusätzliches Cortisol kontinuierlich verabreicht werden, um danach wieder auf die Dauerdosis vor der OP zurückzukehren. ⓘ
Klinische Erscheinungen
Führende Beschwerde ist die anfangs vorwiegend stressabhängige Schwäche und Kraftlosigkeit (Asthenie). Die ebenfalls sehr häufige Hyperpigmentierung (eine bereits von Addison neben der Schwäche, der Muskelermüdbarkeit und Verdauungsstörungen beschriebene zunehmende Braunfärbung lichtausgesetzter Partien) der Haut kann komplett fehlen, eine normale Pigmentierung schließt die Diagnose also nicht aus. ⓘ
| Symptome | Patienten [%] |
|---|---|
| Schwäche | 99 |
| Hyperpigmentierung | 98 |
| Gewichtsverlust | 97 |
| Anorexie, Übelkeit, Erbrechen | 90 |
| Lageabhängig niedriger Blutdruck (< 110/70 mmHg) | 87 |
| Pigmentierung der Schleimhäute | 82 |
| Bauchschmerzen | 34 |
| Verlangen nach salzigen Nahrungsmitteln („Salzhunger“) | 22 |
| Durchfall | 20 |
| Verstopfung | 19 |
| Ohnmacht | 16 |
| Schwindel | 9 |
- Addisonkrise
Durch besondere Belastungssituationen, wie z. B. Operationen und Krankheiten, kann sich vor allem eine noch nicht behandelte NNR-Insuffizienz plötzlich innerhalb weniger Stunden verschlechtern. Dieser potenziell lebensbedrohliche Zustand, genannt Addisonkrise, ist durch Bewusstseinstrübung bis hin zu Koma, Blutdruckabfall, Fieber, massiver Austrocknung des Organismus, Unterzuckerung und Bauchbeschwerden (Pseudoperitonitis) gekennzeichnet. Prodrome sind Unruhe, Angstgefühl und Blässe. ⓘ
Untersuchungsmethoden
Bei Verdacht auf eine NNR-Insuffizienz wird zunächst Labordiagnostik durchgeführt. Mit bildgebenden Verfahren (Ultraschall, Computer-, Magnetresonanztomographie) können dann ggf. Veränderungen der Nebennieren, der Hypophyse oder des Hypothalamus dargestellt werden. ⓘ
| Form | Natrium | Kalium | Cortisol | ACTH | Aldosteron | ACTH-Test | CRH-Test | NNR-Antikörper |
|---|---|---|---|---|---|---|---|---|
| primär | vermindert | erhöht | vermindert | erhöht | vermindert | Cortisol steigt nicht | Cortisol steigt nicht ACTH steigt |
häufig positiv |
| sekundär | normal | normal | vermindert | vermindert | normal | Cortisol steigt | Cortisol steigt nicht ACTH steigt nicht |
negativ |
| tertiär | normal | normal | vermindert | vermindert | normal | Cortisol steigt | Cortisol steigt ACTH steigt |
negativ |
