Progesteron

| |

| |
| Bezeichnungen | |
|---|---|
| Bevorzugter IUPAC-Name
(1S,3aS,3bS,9aR,9bS,11aS)-1-Acetyl-9a,11a-dimethyl-1,2,3,3a,3b,4,5,8,9,9a,9b,10,11,11a-tetradecahydro-7H-cyclopenta[a]phenanthren-7-one | |
| Andere Bezeichnungen
P4; Pregnenedion; Pregn-4-en-3,20-dion
| |
| Kennungen | |
3D-Modell (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Arzneimittelbank | |
| KEGG | |
PubChem CID
|
|
| UNII | |
InChI
| |
SMILES
| |
| Eigenschaften | |
Chemische Formel
|
C21H30O2 |
| Molekulare Masse | 314.469 g/mol |
| Schmelzpunkt | 126 |
| log P | 4.04 |
| Pharmakologie | |
ATC-Code
|
G03DA04 (WHO) |
Wege der
Verabreichung |
Durch den Mund, topisch/transdermal, vaginal, intramuskuläre Injektion, subkutane Injektion, subkutanes Implantat |
| Pharmakokinetik: | |
Bioverfügbarkeit
|
OMP: <10% |
Proteinbindung
|
- Albumin: 80% - CBG: 18% - SHBG: <1% - Frei: 1-2% |
| Hepatisch (CYP2C19, CYP3A4, CYP2C9, 5α-Reduktase, 3α-HSD, 17α-Hydroxylase, 21-Hydroxylase, 20α-HSD) | |
Biologische Halbwertszeit
|
OMP: 16-18 Stunden IM: 22-26 Stunden SC: 13-18 Stunden |
Ausscheidung
|
Nieren |
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien in ihrem Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |
Progesteron (P4) ist ein körpereigenes Steroid und ein gestagenes Sexualhormon, das am Menstruationszyklus, der Schwangerschaft und der Embryogenese des Menschen und anderer Spezies beteiligt ist. Es gehört zu einer Gruppe von Steroidhormonen, den Gestagenen, und ist das wichtigste Gestagen im Körper. Progesteron hat eine Vielzahl von wichtigen Funktionen im Körper. Es ist auch ein entscheidendes metabolisches Zwischenprodukt bei der Produktion anderer körpereigener Steroide, einschließlich der Sexualhormone und der Kortikosteroide, und spielt als Neurosteroid eine wichtige Rolle bei der Gehirnfunktion. ⓘ
Neben seiner Rolle als natürliches Hormon wird Progesteron auch als Medikament verwendet, z. B. in Kombination mit Östrogen zur Empfängnisverhütung, zur Verringerung des Risikos von Gebärmutter- oder Gebärmutterhalskrebs, in der Hormonersatztherapie und in der feminisierenden Hormontherapie. Es wurde erstmals 1934 verschrieben. ⓘ
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Progesteron | ||||||||||||||||||
| Andere Namen |
Pregn-4-en-3,20-dion | ||||||||||||||||||
| Summenformel | C21H30O2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Kristalle | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code |
G03DA04 | ||||||||||||||||||
| Wirkstoffklasse |
Gestagen | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 314,47 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
127–131 °C (α-Form) oder 121 °C (β-Form) | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
327 mg·kg−1 (LD50, Maus, i.p.) | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Bei Frauen wird Progesteron hauptsächlich vom Corpus luteum (Gelbkörper) in der zweiten Phase des Menstruationszyklus und in wesentlich höheren Mengen während der Schwangerschaft von der Plazenta gebildet. Bei Männern bilden die Leydig-Zwischenzellen in den Hoden den Hauptanteil. Geringe Progesteronmengen werden bei Frauen und Männern auch von der Nebennierenrinde synthetisiert. Im menschlichen Organismus wird Progesteron aus Cholesterin synthetisiert. ⓘ
Progesteron regt das Wachstum der Gebärmutterschleimhaut an und bereitet diese auf die Einbettung einer befruchteten Eizelle vor. Kommt es zu einer Befruchtung der Eizelle, verhindert Progesteron eine weitere Follikelreifung; kommt es hingegen zu keiner Empfängnis, vermindert sich die Progesteronproduktion wieder und die Gebärmutterschleimhaut wird abgestoßen und ausgeschieden. ⓘ
Biologische Aktivität
Progesteron ist das wichtigste Progestogen im Körper. Als potenter Agonist des nuklearen Progesteronrezeptors (nPR) (mit einer Affinität von KD = 1 nM) spielt die daraus resultierende Wirkung auf die ribosomale Transkription eine wichtige Rolle bei der Regulierung der weiblichen Fortpflanzung. Darüber hinaus ist Progesteron ein Agonist der erst kürzlich entdeckten Membran-Progesteron-Rezeptoren (mPR), deren Expression sich regulierend auf die Fortpflanzungsfunktion (Eizellreifung, Wehen und Spermienmotilität) und auf Krebs auswirkt, wobei allerdings noch weitere Forschungsarbeiten erforderlich sind, um die Rollen genauer zu definieren. Es fungiert auch als Ligand des PGRMC1 (Progesteronrezeptor-Membrankomponente 1), der die Tumorprogression, die Stoffwechselregulation und die Kontrolle der Lebensfähigkeit von Nervenzellen beeinflusst. Darüber hinaus ist Progesteron auch als Antagonist des Sigma-σ1-Rezeptors, als negativer allosterischer Modulator von nikotinischen Acetylcholinrezeptoren und als potenter Antagonist des Mineralocorticoidrezeptors (MR) bekannt. Progesteron verhindert die Aktivierung des MR, indem es an diesen Rezeptor mit einer Affinität bindet, die sogar die von Aldosteron und Glukokortikoiden wie Cortisol und Corticosteron übertrifft, und bewirkt bei physiologischen Konzentrationen antimineralokortikoide Wirkungen, wie z. B. die Natriurese. Darüber hinaus bindet Progesteron an den Glukokortikoidrezeptor (GR) und verhält sich wie ein partieller Agonist, wenn auch mit sehr geringer Potenz (EC50 >100-fach geringer als bei Cortisol). ⓘ
Progesteron wirkt über seine neurosteroidaktiven Metaboliten wie 5α-Dihydroprogesteron und Allopregnanolon indirekt als positiver allosterischer Modulator des GABAA-Rezeptors. ⓘ
Progesteron und einige seiner Metaboliten, wie 5β-Dihydroprogesteron, sind Agonisten des Pregnan-X-Rezeptors (PXR), wenn auch nur schwach (EC50 >10 μM). Entsprechend induziert Progesteron mehrere hepatische Cytochrom-P450-Enzyme, wie CYP3A4, insbesondere während der Schwangerschaft, wenn die Konzentrationen viel höher als gewöhnlich sind. Bei Frauen in der Perimenopause wurde eine höhere CYP3A4-Aktivität festgestellt als bei Männern und Frauen nach der Menopause, und es wurde vermutet, dass dies auf die höheren Progesteronspiegel bei Frauen in der Perimenopause zurückzuführen sein könnte. ⓘ
Progesteron moduliert die Aktivität der spannungsgesteuerten Ca2+-Kanäle von CatSper (Kationenkanäle von Spermien). Da die Eizellen Progesteron freisetzen, können die Spermien Progesteron als Zielsignal verwenden, um zu den Eizellen zu schwimmen (Chemotaxis). Daher wurde vorgeschlagen, dass Substanzen, die die Progesteron-Bindungsstelle an den CatSper-Kanälen blockieren, möglicherweise zur männlichen Empfängnisverhütung eingesetzt werden könnten. ⓘ
Biologische Funktion

Hormonelle Wechselwirkungen
Progesteron hat eine Reihe von physiologischen Wirkungen, die in Gegenwart von Östrogenen verstärkt werden. Östrogene induzieren über Östrogenrezeptoren (ERs) die Expression der PR oder regulieren sie hoch. Ein Beispiel hierfür ist das Brustgewebe, wo Östrogene es Progesteron ermöglichen, die lobuloalveoläre Entwicklung zu vermitteln. ⓘ
Erhöhte Progesteronspiegel verringern die natriumrückhaltende Wirkung von Aldosteron, was zu einer Natriurese und einer Verringerung des extrazellulären Flüssigkeitsvolumens führt. Der Entzug von Progesteron geht dagegen mit einer vorübergehenden Zunahme der Natriumretention einher (verringerte Natriurese, mit einer Zunahme des extrazellulären Flüssigkeitsvolumens), was auf die kompensatorische Zunahme der Aldosteronproduktion zurückzuführen ist, die die Blockade des Mineralocorticoidrezeptors durch den zuvor erhöhten Progesteronspiegel bekämpft. ⓘ
Fortpflanzungsorgane

Progesteron hat über nicht-genomische Signale entscheidende Auswirkungen auf die menschlichen Spermien, wenn sie vor der Befruchtung durch den weiblichen Trakt wandern, obwohl der/die Rezeptor(en) noch nicht identifiziert sind. Eine detaillierte Charakterisierung der Ereignisse, die in den Spermien als Reaktion auf Progesteron ablaufen, hat bestimmte Ereignisse aufgezeigt, darunter intrazelluläre Kalziumtransienten und anhaltende Veränderungen, langsame Kalziumoszillationen, von denen man heute annimmt, dass sie möglicherweise die Beweglichkeit regulieren. Es wird von den Eierstöcken produziert. Progesteron hat auch Auswirkungen auf die Spermatozoen von Tintenfischen gezeigt. ⓘ
Progesteron wird manchmal als "Schwangerschaftshormon" bezeichnet und spielt bei der Entwicklung des Fötus eine wichtige Rolle:
- Progesteron wandelt die Gebärmutterschleimhaut in ihr sekretorisches Stadium um, um die Gebärmutter auf die Einnistung vorzubereiten. Gleichzeitig wirkt Progesteron auf das Vaginalepithel und den Gebärmutterhalsschleim ein und macht ihn dick und undurchdringlich für Spermien. Progesteron wirkt in den Epithelzellen der Gebärmutterschleimhaut antimikrobiell und mildert so die tropischen Wirkungen von Östrogen. Wenn keine Schwangerschaft eintritt, sinkt der Progesteronspiegel, was beim Menschen zur Menstruation führt. Die normale Menstruationsblutung ist eine Progesteron-Entzugsblutung. Wenn der Eisprung ausbleibt und sich der Gelbkörper nicht entwickelt, kann der Progesteronspiegel niedrig sein, was zu anovulatorischen dysfunktionalen Uterusblutungen führt.
- Während der Einnistung und der Schwangerschaft scheint Progesteron die mütterliche Immunreaktion zu verringern, um die Annahme der Schwangerschaft zu ermöglichen.
- Progesteron verringert die Kontraktilität der glatten Muskulatur der Gebärmutter. Dieser Effekt trägt zur Vorbeugung von vorzeitigen Wehen bei.
- Ein Absinken des Progesteronspiegels ist möglicherweise ein Schritt, der das Einsetzen der Wehen erleichtert.
- Außerdem hemmt Progesteron die Laktation während der Schwangerschaft. Der Abfall des Progesteronspiegels nach der Entbindung ist einer der Auslöser für die Milchproduktion. ⓘ
Der Fötus verstoffwechselt das plazentare Progesteron bei der Produktion von Nebennierensteroiden. ⓘ
Brüste
Lobuloalveoläre Entwicklung
Progesteron spielt eine wichtige Rolle bei der Brustentwicklung der Frau. In Verbindung mit Prolaktin vermittelt es die lobuloalveoläre Reifung der Brustdrüsen während der Schwangerschaft, um die Milchproduktion und damit das Stillen des Nachwuchses nach der Geburt zu ermöglichen. Östrogen induziert die Expression von PR im Brustgewebe, so dass Progesteron zur Vermittlung der lobuloalveolären Entwicklung von Östrogen abhängig ist. Es wurde festgestellt, dass RANKL ein entscheidender nachgeschalteter Mediator der Progesteron-induzierten lobuloalveolären Reifung ist. RANKL-Knockout-Mäuse zeigen einen nahezu identischen Mammaphänotyp wie PR-Knockout-Mäuse, einschließlich einer normalen Entwicklung der Brustdrüsengänge, aber eines völligen Ausfalls der lobuloalveolären Strukturen. ⓘ
Duktale Entwicklung
Wenn auch in weitaus geringerem Maße als Östrogen, das (über ERα) der Hauptvermittler der Entwicklung der Milchgänge ist, könnte auch Progesteron in gewissem Maße an der Entwicklung der Milchgänge beteiligt sein. PR-Knockout-Mäuse oder Mäuse, die mit dem PR-Antagonisten Mifepriston behandelt wurden, zeigen eine verzögerte, aber ansonsten normale Entwicklung der Brustdrüsengänge in der Pubertät. Darüber hinaus zeigen Mäuse, die so verändert wurden, dass sie eine Überexpression von PRA aufweisen, eine duktale Hyperplasie, und Progesteron induziert ein duktales Wachstum in der Brustdrüse der Maus. Progesteron vermittelt die Entwicklung der Gänge vor allem über die Induktion der Expression von Ampiregulin, dem gleichen Wachstumsfaktor, dessen Expression durch Östrogen primär induziert wird, um die Entwicklung der Gänge zu vermitteln. Diese Ergebnisse deuten darauf hin, dass Progesteron zwar für die vollständige Entwicklung der Brustdrüsengänge nicht unerlässlich ist, aber offenbar eine verstärkende oder beschleunigende Rolle bei der Östrogen-vermittelten Entwicklung der Brustdrüsengänge spielt. ⓘ
Brustkrebsrisiko
Progesteron scheint auch an der Pathophysiologie von Brustkrebs beteiligt zu sein, obwohl seine Rolle und die Frage, ob es das Brustkrebsrisiko fördert oder hemmt, noch nicht vollständig geklärt ist. Die meisten Gestagene oder synthetischen Gestagene wie Medroxyprogesteronacetat erhöhen nachweislich das Brustkrebsrisiko bei postmenopausalen Frauen in Kombination mit Östrogen als Bestandteil der Hormontherapie in den Wechseljahren. Die Kombination von natürlichem oralen Progesteron oder dem atypischen Gestagen Dydrogesteron mit Östrogen wurde mit einem geringeren Brustkrebsrisiko in Verbindung gebracht als Gestagene plus Östrogen. Dies könnte jedoch einfach ein Artefakt der niedrigen Progesteronspiegel sein, die bei oralem Progesteron entstehen. Die Rolle von Progesteron bei Brustkrebs muss weiter erforscht werden. ⓘ
Gesundheit der Haut
Sowohl der Östrogenrezeptor als auch der Progesteronrezeptor wurden in der Haut nachgewiesen, auch in Keratinozyten und Fibroblasten. In der Menopause und danach führt der Rückgang der weiblichen Geschlechtshormone zu Atrophie, Ausdünnung und verstärkter Faltenbildung der Haut sowie zu einer Abnahme der Elastizität, Festigkeit und Stärke der Haut. Diese Hautveränderungen stellen eine Beschleunigung der Hautalterung dar und sind das Ergebnis eines verringerten Kollagengehalts, von Unregelmäßigkeiten in der Morphologie der epidermalen Hautzellen, einer verringerten Grundsubstanz zwischen den Hautfasern sowie einer verminderten Kapillarität und Durchblutung. In den Wechseljahren wird die Haut außerdem trockener, was auf eine verringerte Hautfeuchtigkeit und Oberflächenlipide (Talgproduktion) zurückzuführen ist. Neben der chronologischen Alterung und der Lichtalterung ist der Östrogenmangel in den Wechseljahren einer der drei Hauptfaktoren, die die Hautalterung am stärksten beeinflussen. ⓘ
Die Hormonersatztherapie, die aus einer systemischen Behandlung mit Östrogen allein oder in Kombination mit einem Gestagen besteht, hat gut dokumentierte und beträchtliche positive Auswirkungen auf die Haut postmenopausaler Frauen. Zu diesen Vorteilen gehören ein höherer Kollagengehalt der Haut, eine größere Hautdicke und -elastizität sowie eine höhere Hautfeuchtigkeit und mehr Oberflächenlipide. Topisches Östrogen hat nachweislich ähnliche positive Auswirkungen auf die Haut. Darüber hinaus wurde in einer Studie festgestellt, dass topische 2%ige Progesteroncreme bei Frauen in der Peri- und Postmenopause die Elastizität und Festigkeit der Haut signifikant erhöht und die Faltenbildung deutlich verringert. Der Feuchtigkeitsgehalt der Haut und die Oberflächenlipide hingegen veränderten sich durch topisches Progesteron nicht signifikant. Diese Ergebnisse deuten darauf hin, dass Progesteron wie Östrogen auch positive Auswirkungen auf die Haut hat und möglicherweise unabhängig davon vor Hautalterung schützt. ⓘ
Sexualität
Libido
Progesteron und sein aktiver Neurosteroid-Metabolit Allopregnanolon scheinen eine wichtige Rolle bei der Libido der Frau zu spielen. ⓘ
Homosexualität
Dr. Diana Fleischman von der Universität Portsmouth und Kollegen untersuchten bei 92 Frauen einen Zusammenhang zwischen Progesteron und sexuellen Einstellungen. Ihre in den Archives of Sexual Behavior veröffentlichte Studie ergab, dass Frauen mit einem höheren Progesteronspiegel in einem Fragebogen zur Messung der homoerotischen Motivation besser abschnitten. Sie fanden auch heraus, dass Männer mit einem hohen Progesteronspiegel im Vergleich zu Männern mit einem niedrigen Progesteronspiegel nach einem affiliativen Priming mit größerer Wahrscheinlichkeit höhere Werte bei der homoerotischen Motivation erzielten. ⓘ
Nervensystem
Progesteron gehört wie Pregnenolon und Dehydroepiandrosteron (DHEA) zu einer wichtigen Gruppe körpereigener Steroide, den Neurosteroiden. Es kann in allen Teilen des zentralen Nervensystems verstoffwechselt werden. ⓘ
Neurosteroide sind Neuromodulatoren, die neuroprotektiv und neurogen wirken und die Neurotransmission und Myelinisierung regulieren. Die Wirkungen von Progesteron als Neurosteroid werden vor allem durch seine Wechselwirkungen mit nicht-nukleären PRs, nämlich den mPRs und PGRMC1, sowie mit bestimmten anderen Rezeptoren, wie den σ1- und nACh-Rezeptoren, vermittelt. ⓘ
Schädigung des Gehirns
Frühere Studien haben gezeigt, dass Progesteron die normale Entwicklung von Neuronen im Gehirn unterstützt und dass das Hormon eine schützende Wirkung auf geschädigtes Hirngewebe hat. In Tiermodellen wurde beobachtet, dass weibliche Tiere weniger anfällig für traumatische Hirnverletzungen sind, und es wurde die Hypothese aufgestellt, dass diese schützende Wirkung durch erhöhte zirkulierende Östrogen- und Progesteronspiegel bei weiblichen Tieren verursacht wird. ⓘ
Vorgeschlagener Mechanismus
Der Mechanismus der schützenden Wirkung von Progesteron könnte in der Verringerung der Entzündung nach einem Hirntrauma und einer Hirnblutung liegen. ⓘ
Es wird vermutet, dass die Schäden durch traumatische Hirnverletzungen zum Teil durch Massendepolarisationen verursacht werden, die zu Exzitotoxizität führen. Progesteron trägt dazu bei, einen Teil dieser Exzitotoxizität zu mildern, indem es die spannungsabhängigen Kalziumkanäle blockiert, die die Freisetzung von Neurotransmittern auslösen. Dies geschieht durch die Beeinflussung der Signalwege von Transkriptionsfaktoren, die an dieser Freisetzung beteiligt sind. Eine weitere Methode zur Verringerung der Exzitotoxizität ist die Hochregulierung des GABAA, eines weit verbreiteten hemmenden Neurotransmitter-Rezeptors. ⓘ
Progesteron verhindert nachweislich auch die Apoptose in Neuronen, eine häufige Folge von Hirnverletzungen. Dies geschieht durch die Hemmung von Enzymen, die am Apoptoseweg beteiligt sind und speziell die Mitochondrien betreffen, wie z. B. die aktivierte Caspase 3 und Cytochrom c. ⓘ
Progesteron trägt nicht nur dazu bei, weitere Schäden zu verhindern, sondern hilft auch nachweislich bei der Neuroregeneration. Eine der schwerwiegenden Folgen von traumatischen Hirnverletzungen sind Ödeme. Tierstudien zeigen, dass die Behandlung mit Progesteron zu einer Verringerung des Ödems führt, indem die Konzentration von Makrophagen und Mikroglia, die zum verletzten Gewebe geschickt werden, erhöht wird. Dies wurde in Form einer verringerten Leckage aus der Blut-Hirn-Schranke bei der sekundären Genesung von mit Progesteron behandelten Ratten beobachtet. Darüber hinaus wurde beobachtet, dass Progesteron antioxidative Eigenschaften hat und die Konzentration freier Sauerstoffradikale schneller reduziert als ohne Progesteron. Es gibt auch Hinweise darauf, dass Progesteron dazu beitragen kann, die durch ein Trauma geschädigten Axone zu remyelinisieren und so einen Teil der verlorenen neuronalen Signalleitung wiederherzustellen. Eine weitere Möglichkeit, wie Progesteron zur Regeneration beiträgt, besteht darin, die Zirkulation endothelialer Vorläuferzellen im Gehirn zu erhöhen. Dies trägt dazu bei, dass neue Blutgefäße um Narbengewebe herum wachsen, was die Reparatur des verletzten Bereichs unterstützt. ⓘ
Sucht
Progesteron fördert die Funktion der Serotoninrezeptoren im Gehirn, so dass ein Überschuss oder ein Mangel an Progesteron zu erheblichen neurochemischen Problemen führen kann. Dies erklärt, warum manche Menschen zu Substanzen greifen, die die Serotoninaktivität steigern, wie Nikotin, Alkohol und Cannabis, wenn ihr Progesteronspiegel unter ein optimales Niveau fällt. ⓘ
- Geschlechtsspezifische Unterschiede im Hormonspiegel können dazu führen, dass Frauen anders als Männer auf Nikotin reagieren. Wenn Frauen zyklische Veränderungen oder verschiedene hormonelle Übergangsphasen durchlaufen (Wechseljahre, Schwangerschaft, Pubertät), verändert sich ihr Progesteronspiegel. Daher sind Frauen im Vergleich zu Männern biologisch anfälliger für die verstärkende Wirkung von Nikotin, und Progesteron kann eingesetzt werden, um dieser erhöhten Anfälligkeit entgegenzuwirken. Diese Informationen unterstützen die Idee, dass Progesteron das Verhalten beeinflussen kann.
- Ähnlich wie Nikotin steigert auch Kokain die Freisetzung von Dopamin im Gehirn. Dieser Neurotransmitter ist am Belohnungszentrum beteiligt und einer der wichtigsten Neurotransmitter, die mit Drogenmissbrauch und Abhängigkeit in Verbindung gebracht werden. In einer Studie mit Kokainkonsumenten wurde berichtet, dass Progesteron das Verlangen und das Gefühl der Stimulation durch Kokain verringert. Somit wurde Progesteron als ein Mittel vorgeschlagen, das das Verlangen nach Kokain verringert, indem es die dopaminergen Eigenschaften der Droge reduziert. ⓘ
Gesellschaftliche
In einer 2012 an der Universität Amsterdam durchgeführten Studie mit 120 Frauen wurde festgestellt, dass die Lutealphase der Frauen (höhere Progesteronspiegel und steigende Östrogenspiegel) mit einem geringeren Wettbewerbsverhalten bei Glücksspielen und Mathematikwettbewerben korreliert, während die prämenstruelle Phase der Frauen (stark abnehmende Progesteronspiegel und sinkende Östrogenspiegel) mit einem höheren Wettbewerbsverhalten korreliert war. ⓘ
Andere Auswirkungen
- Progesteron spielt auch eine Rolle bei der Elastizität der Haut und der Festigkeit der Knochen, bei der Atmung, im Nervengewebe und bei der weiblichen Sexualität, und das Vorhandensein von Progesteronrezeptoren in bestimmten Muskel- und Fettgeweben könnte auf eine Rolle bei den geschlechtsdimorphen Proportionen dieser Gewebe hinweisen.
- Während der Schwangerschaft soll Progesteron die Reizbarkeit der Gebärmutter verringern.
- Während der Schwangerschaft trägt Progesteron zur Unterdrückung von Immunreaktionen der Mutter auf fötale Antigene bei, was eine Abstoßung des Fötus verhindert.
- Progesteron erhöht den Spiegel des epidermalen Wachstumsfaktors 1 (EGF-1), eines Faktors, der häufig zur Anregung der Proliferation von Stammzellen und zur Aufrechterhaltung von Kulturen verwendet wird.
- Progesteron erhöht die Kerntemperatur (thermogene Funktion) während des Eisprungs.
- Progesteron reduziert Spasmen und entspannt die glatte Muskulatur. Die Bronchien werden geweitet und der Schleim reguliert. (PRs sind im submukösen Gewebe weit verbreitet.)
- Progesteron wirkt entzündungshemmend und reguliert die Immunreaktion.
- Progesteron reduziert die Aktivität der Gallenblase.
- Progesteron normalisiert die Blutgerinnung und den Gefäßtonus, den Zink- und Kupferspiegel, den Sauerstoffgehalt der Zellen und die Nutzung der Fettspeicher zur Energiegewinnung.
- Progesteron kann die Gesundheit des Zahnfleisches beeinträchtigen und das Risiko einer Zahnfleischentzündung (Gingivitis) erhöhen.
- Progesteron scheint Endometriumkrebs (der die Gebärmutterschleimhaut betrifft) zu verhindern, indem es die Wirkung von Östrogen reguliert.
- Progesteron spielt eine wichtige Rolle bei der Signalisierung der Insulinausschüttung und der Funktion der Bauchspeicheldrüse und kann die Anfälligkeit für Diabetes oder Schwangerschaftsdiabetes beeinflussen. ⓘ
Biochemie
Biosynthese

Bei Säugetieren wird Progesteron, wie alle anderen Steroidhormone, aus Pregnenolon synthetisiert, das wiederum aus Cholesterin gewonnen wird. ⓘ
Cholesterin wird einer doppelten Oxidation unterzogen, um 22R-Hydroxycholesterin und dann 20α,22R-Dihydroxycholesterin zu bilden. Dieses vicinale Diol wird dann unter Verlust der Seitenkette, beginnend an Position C22, weiter oxidiert, um Pregnenolon zu bilden. Diese Reaktion wird durch Cytochrom P450scc katalysiert. ⓘ
Die Umwandlung von Pregnenolon in Progesteron findet in zwei Schritten statt. Erstens wird die 3β-Hydroxylgruppe zu einer Ketogruppe oxidiert und zweitens wird die Doppelbindung durch eine Keto/Enol-Tautomerisierungsreaktion von C5 nach C4 verschoben. Diese Reaktion wird durch die 3β-Hydroxysteroiddehydrogenase/δ5-4-Isomerase katalysiert. ⓘ
Progesteron wiederum ist die Vorstufe des Mineralocorticoids Aldosteron und nach Umwandlung in 17α-Hydroxyprogesteron von Cortisol und Androstendion. Androstendion kann in Testosteron, Estron und Östradiol umgewandelt werden, was die entscheidende Rolle von Progesteron bei der Testosteronsynthese unterstreicht. ⓘ
Pregnenolon und Progesteron können auch von Hefen synthetisiert werden. ⓘ
Bei Frauen werden pro Tag etwa 25 mg Progesteron von den Eierstöcken ausgeschieden, während die Nebennieren etwa 2 mg Progesteron pro Tag produzieren. ⓘ
| Geschlecht | Sexualhormon | Fortpflanzung Phase |
Blut Produktionsrate |
Keimdrüsen Sekretionsrate |
Stoffwechsel Clearance-Rate |
Referenzbereich (Serumspiegel) | |
|---|---|---|---|---|---|---|---|
| SI-Einheiten | Nicht-SI-Einheiten | ||||||
| Männer | Androstendion | –
|
2,8 mg/Tag | 1,6 mg/Tag | 2200 L/Tag | 2,8-7,3 nmol/L | 80-210 ng/dL |
| Testosteron | –
|
6,5 mg/Tag | 6,2 mg/Tag | 950 L/Tag | 6,9-34,7 nmol/L | 200-1000 ng/dL | |
| Estron | –
|
150 μg/Tag | 110 μg/Tag | 2050 L/Tag | 37-250 pmol/L | 10-70 pg/ml | |
| Estradiol | –
|
60 μg/Tag | 50 μg/Tag | 1600 L/Tag | <37-210 pmol/L | 10-57 pg/ml | |
| Estron-Sulfat | –
|
80 μg/Tag | Unbedeutend | 167 L/Tag | 600-2500 pmol/L | 200-900 pg/ml | |
| Frauen | Androstendion | –
|
3,2 mg/Tag | 2,8 mg/Tag | 2000 L/Tag | 3,1-12,2 nmol/L | 89-350 ng/dL |
| Testosteron | –
|
190 μg/Tag | 60 μg/Tag | 500 L/Tag | 0,7-2,8 nmol/L | 20-81 ng/dL | |
| Estron | Follikuläre Phase | 110 μg/Tag | 80 μg/Tag | 2200 L/Tag | 110-400 pmol/L | 30-110 pg/ml | |
| Lutealphase | 260 μg/Tag | 150 μg/Tag | 2200 L/Tag | 310-660 pmol/L | 80-180 pg/ml | ||
| Postmenopause | 40 μg/Tag | Unbedeutend | 1610 L/Tag | 22-230 pmol/L | 6-60 pg/ml | ||
| Estradiol | Follikuläre Phase | 90 μg/Tag | 80 μg/Tag | 1200 L/Tag | <37-360 pmol/L | 10-98 pg/ml | |
| Lutealphase | 250 μg/Tag | 240 μg/Tag | 1200 L/Tag | 699-1250 pmol/L | 190-341 pg/ml | ||
| Postmenopause | 6 μg/Tag | Unbedeutend | 910 L/Tag | <37-140 pmol/L | 10-38 pg/ml | ||
| Estron-Sulfat | Follikuläre Phase | 100 μg/Tag | Unbedeutend | 146 L/Tag | 700-3600 pmol/L | 250-1300 pg/ml | |
| Lutealphase | 180 μg/Tag | Unbedeutend | 146 L/Tag | 1100-7300 pmol/L | 400-2600 pg/ml | ||
| Progesteron | Follikuläre Phase | 2 mg/Tag | 1,7 mg/Tag | 2100 L/Tag | 0,3-3 nmol/L | 0,1-0,9 ng/ml | |
| Lutealphase | 25 mg/Tag | 24 mg/Tag | 2100 L/Tag | 19-45 nmol/L | 6-14 ng/ml | ||
Anmerkungen und Quellen
Anmerkungen: "Die Konzentration eines Steroids im Blutkreislauf wird durch die Geschwindigkeit bestimmt, mit der es aus den Drüsen ausgeschieden wird, durch die Geschwindigkeit, mit der Vorläufer- oder Prähormone in das Steroid umgewandelt werden, und durch die Geschwindigkeit, mit der es von den Geweben extrahiert und metabolisiert wird. Die Sekretionsrate eines Steroids bezieht sich auf die Gesamtausscheidung der Verbindung aus einer Drüse pro Zeiteinheit. Die Sekretionsraten wurden durch die Entnahme von Proben aus dem venösen Ausfluss einer Drüse über einen bestimmten Zeitraum und durch Subtraktion der arteriellen und peripheren venösen Hormonkonzentration ermittelt. Die metabolische Clearance-Rate eines Steroids ist definiert als das Blutvolumen, das pro Zeiteinheit vollständig von dem Hormon abgebaut wurde. Die Produktionsrate eines Steroidhormons bezieht sich auf den Eintritt der Verbindung in das Blut aus allen möglichen Quellen, einschließlich der Sekretion aus Drüsen und der Umwandlung von Prohormonen in das Steroid von Interesse. Im Fließgleichgewicht ist die Menge des Hormons, die aus allen Quellen ins Blut gelangt, gleich der Rate, mit der es abgebaut wird (metabolische Clearance-Rate), multipliziert mit der Blutkonzentration (Produktionsrate = metabolische Clearance-Rate × Konzentration). Wenn der Prohormonstoffwechsel nur wenig zum zirkulierenden Steroidpool beiträgt, entspricht die Produktionsrate ungefähr der Sekretionsrate." Quellen: Siehe Vorlage. | |||||||
Verteilung
Progesteron bindet in hohem Maße an Plasmaproteine, darunter Albumin (50-54%) und Transcortin (43-48%). Es hat eine ähnliche Affinität zu Albumin wie das PR. ⓘ
Stoffwechsel
Der Metabolismus von Progesteron ist schnell und umfassend und findet hauptsächlich in der Leber statt, obwohl Enzyme, die Progesteron metabolisieren, auch im Gehirn, in der Haut und in verschiedenen anderen extrahepatischen Geweben weit verbreitet sind. Progesteron hat im Blutkreislauf eine Eliminationshalbwertszeit von nur etwa 5 Minuten. Der Stoffwechsel von Progesteron ist komplex, und bei oraler Einnahme können bis zu 35 verschiedene nicht konjugierte Metaboliten entstehen. Progesteron ist aufgrund seiner Doppelbindung (zwischen den Positionen C4 und C5) und seiner beiden Ketone (an den Positionen C3 und C20) sehr anfällig für enzymatische Reduktion durch Reduktasen und Hydroxysteroid-Dehydrogenasen. ⓘ
Der wichtigste Stoffwechselweg von Progesteron ist die Reduktion durch 5α-Reduktase und 5β-Reduktase in das dihydrierte 5α-Dihydroprogesteron bzw. 5β-Dihydroprogesteron. Anschließend werden diese Metaboliten durch 3α-Hydroxysteroid-Dehydrogenase und 3β-Hydroxysteroid-Dehydrogenase weiter zu tetrahydriertem Allopregnanolon, Pregnanolon, Isopregnanolon und Epipregnanolon reduziert. Anschließend reduzieren 20α-Hydroxysteroid-Dehydrogenase und 20β-Hydroxysteroid-Dehydrogenase diese Metaboliten zu den entsprechenden hexahydrierten Pregnandiolen (insgesamt acht verschiedene Isomere), die dann über Glucuronidierung und/oder Sulfatierung konjugiert, von der Leber in den Blutkreislauf abgegeben und über die Nieren in den Urin ausgeschieden werden. Der Hauptmetabolit von Progesteron im Urin ist das 3α,5β,20α-Isomer von Pregnandiol-Glucuronid, das nachweislich 15 bis 30 % einer Progesteron-Injektion ausmacht. Zu den anderen Metaboliten von Progesteron, die von den Enzymen in diesem Stoffwechselweg gebildet werden, gehören 3α-Dihydroprogesteron, 3β-Dihydroprogesteron, 20α-Dihydroprogesteron und 20β-Dihydroprogesteron sowie verschiedene Kombinationsprodukte der Enzyme neben den bereits genannten. Progesteron kann auch zunächst hydroxyliert (siehe unten) und dann reduziert werden. Endogenes Progesteron wird im Gelbkörper zu etwa 50% in 5α-Dihydroprogesteron, in der Leber zu 35% in 3β-Dihydroprogesteron und zu 10% in 20α-Dihydroprogesteron umgewandelt. ⓘ
Relativ kleine Anteile des Progesterons werden durch 17α-Hydroxylase (CYP17A1) und 21-Hydroxylase (CYP21A2) zu 17α-Hydroxyprogesteron bzw. 11-Desoxycorticosteron (21-Hydroxyprogesteron) hydroxyliert, und sekundär zur 17α-Hydroxylierung werden Pregnantriole gebildet. Noch geringere Mengen Progesteron können auch über 11β-Hydroxylase (CYP11B1) und in geringerem Maße über Aldosteron-Synthase (CYP11B2) zu 11β-Hydroxyprogesteron hydroxyliert werden. Darüber hinaus kann Progesteron in der Leber durch andere Cytochrom-P450-Enzyme hydroxyliert werden, die nicht steroidspezifisch sind. Die 6β-Hydroxylierung, die hauptsächlich durch CYP3A4 katalysiert wird, ist die wichtigste Umwandlung und für etwa 70 % des Cytochrom-P450-vermittelten Progesteron-Metabolismus verantwortlich. Andere Wege sind die 6α-, 16α- und 16β-Hydroxylierung. Die Behandlung von Frauen mit Ketoconazol, einem starken CYP3A4-Inhibitor, hatte jedoch nur minimale Auswirkungen auf den Progesteronspiegel und führte nur zu einem leichten und nicht signifikanten Anstieg, was darauf hindeutet, dass Cytochrom-P450-Enzyme nur eine geringe Rolle beim Progesteronstoffwechsel spielen. ⓘ
Metabolismus von Progesteron beim Menschen
|
Werte

Bei Frauen ist der Progesteronspiegel während der präovulatorischen Phase des Menstruationszyklus relativ niedrig, steigt nach dem Eisprung an und ist während der Lutealphase erhöht, wie im obigen Diagramm dargestellt. Der Progesteronspiegel liegt in der Regel unter 2 ng/ml vor dem Eisprung und über 5 ng/ml nach dem Eisprung. Kommt es zu einer Schwangerschaft, wird humanes Choriongonadotropin freigesetzt, das den Gelbkörper aufrechterhält und es ihm ermöglicht, den Progesteronspiegel aufrechtzuerhalten. Zwischen der 7. und 9. Woche beginnt die Plazenta, anstelle des Gelbkörpers Progesteron zu produzieren. ⓘ
Nach der luteal-plazentaren Verschiebung beginnt der Progesteronspiegel weiter anzusteigen und kann bei der Geburt 100 bis 200 ng/ml erreichen. Es ist umstritten, ob ein Rückgang des Progesteronspiegels für die Einleitung der Wehen entscheidend ist; möglicherweise ist er artspezifisch. Nach der Geburt der Plazenta und während der Stillzeit ist der Progesteronspiegel sehr niedrig. ⓘ
Auch bei Kindern und Frauen nach der Menopause sind die Progesteronspiegel niedrig. Bei erwachsenen Männern sind die Werte ähnlich hoch wie bei Frauen während der Follikelphase des Menstruationszyklus. ⓘ
| Gruppe | P4-Produktion | P4-Spiegel | ||
|---|---|---|---|---|
| Vorpubertäre Kinder | ND | 0,06-0,5 ng/ml | ||
| Pubertierende Mädchen Tanner-Stadium I (Kindheit) Tanner-Stadium II (Alter 8-12) Tanner-Stadium III (Alter 10-13) Tanner-Stadium IV (Alter 11-14) Tanner-Stadium V (12-15 Jahre) Follikelphase (Tage 1-14) Lutealphase (Tage 15-28) |
ND ND ND ND ND ND |
0,22 (<0,10-0,32) ng/ml 0,30 (0,10-0,51) ng/ml 0,36 (0,10-0,75) ng/ml 1,75 (<0,10-25,0) ng/mL 0,35 (0,13-0,75) ng/mL 2,0-25,0 ng/mL | ||
| Prämenopausale Frauen Follikelphase (Tage 1-14) Lutealphase (Tage 15-28) Orale Verhütungsmittel (anovulatorisch) |
0,75-5,4 mg/Tag 15-50 mg/Tag ND |
0,02-1,2 ng/ml 4-30 ng/ml 0,1-0,3 ng/ml | ||
| Postmenopausale Frauen Oophorektomierte Frauen Oophorektomierte und nebennierenresektomierte Frauen |
ND 1,2 mg/Tag <0,3 mg/Tag |
0,03-0,3 ng/ml 0,39 ng/ml ND | ||
| Schwangere Frauen Erstes Trimester (Wochen 1-12) Zweites Trimenon (13-26 Wochen) Drittes Trimenon (Wochen 27-40) Postpartum (innerhalb von 24 Stunden) |
55 mg/Tag 92-100 mg/Tag 190-563 mg/Tag ND |
9-75 ng/ml 17-146 ng/ml 55-255 ng/ml 19 ng/ml | ||
| Männer | 0,75-3 mg/Tag | 0,1-0,3 ng/ml | ||
| Anmerkungen: Der Mittelwert wird als Einzelwert angegeben, die Spannen werden in Klammern angegeben. Quellen: Siehe Vorlage. | ||||
Wertebereiche
Die Ergebnisse von Bluttests sollten immer anhand der Referenzbereiche interpretiert werden, die von dem Labor, das die Ergebnisse ermittelt hat, angegeben wurden. Beispiele für Referenzbereiche sind unten aufgeführt. ⓘ
| Personentyp | Referenzbereich für Bluttest ⓘ | ||
|---|---|---|---|
| Untere Grenze | Oberer Grenzwert | Einheit | |
| Weiblich - Menstruationszyklus | (siehe Diagramm unten) | ||
| Weiblich - postmenopausal | <0.2 | 1 | ng/ml |
| <0.6 | 3 | nmol/L | |
| Frauen, die orale Verhütungsmittel einnehmen | 0.34 | 0.92 | ng/ml |
| 1.1 | 2.9 | nmol/L | |
| Männer ≥16 Jahre | 0.27 | 0.9 | ng/ml |
| 0.86 | 2.9 | nmol/L | |
| Weiblich oder männlich 1-9 Jahre | 0.1 | 4,1 oder 4,5 | ng/ml |
| 0.3 | 13 | nmol/L | |
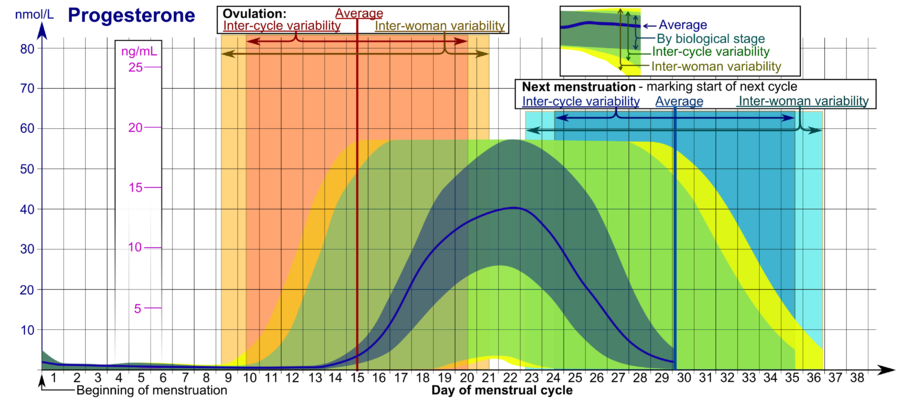
- Die mit Nach biologischem Stadium bezeichneten Bereiche können bei engmaschig überwachten Menstruationszyklen im Hinblick auf andere Marker des biologischen Verlaufs verwendet werden, wobei die Zeitskala komprimiert oder gedehnt wird, um festzustellen, wie viel schneller bzw. langsamer der Zyklus im Vergleich zu einem durchschnittlichen Zyklus voranschreitet.
- Die mit "Inter-Zyklus-Variabilität" bezeichneten Bereiche eignen sich besser für nicht überwachte Zyklen, bei denen nur der Beginn der Menstruation bekannt ist, die Frau aber ihre durchschnittlichen Zykluslängen und den Zeitpunkt des Eisprungs genau kennt und diese einigermaßen durchschnittlich regelmäßig sind, wobei die Zeitskala dahingehend gestaucht oder gedehnt wird, um wie viel die durchschnittliche Zykluslänge der Frau kürzer bzw. länger ist als der Durchschnitt der Bevölkerung.
- Die mit Inter-woman variability bezeichneten Bereiche sind besser geeignet, wenn die durchschnittlichen Zykluslängen und der Zeitpunkt des Eisprungs nicht bekannt sind, sondern nur der Beginn der Menstruation angegeben wird. ⓘ
Quellen
Tiere
Progesteron wird vom Beginn der Pubertät bis zur Menopause in großen Mengen in den Eierstöcken (durch den Gelbkörper) und in kleineren Mengen nach Beginn der Adrenarche sowohl bei Männern als auch bei Frauen in den Nebennieren produziert. In geringerem Umfang wird Progesteron auch im Nervengewebe, insbesondere im Gehirn, und im Fettgewebe produziert. ⓘ
Während der Schwangerschaft wird Progesteron in immer größeren Mengen von den Eierstöcken und der Plazenta produziert. Zunächst ist die Quelle der Gelbkörper, der durch das Vorhandensein von menschlichem Choriongonadotropin (hCG) aus dem Konzeptus "gerettet" wurde. Nach der 8. Woche verlagert sich die Produktion von Progesteron jedoch auf die Plazenta. Die Plazenta verwendet mütterliches Cholesterin als Ausgangssubstrat, und der größte Teil des produzierten Progesterons gelangt in den mütterlichen Kreislauf, ein Teil wird jedoch vom fetalen Kreislauf aufgenommen und als Substrat für fetale Kortikosteroide verwendet. Zum Zeitpunkt der Geburt produziert die Plazenta etwa 250 mg Progesteron pro Tag. ⓘ
Eine weitere tierische Quelle für Progesteron sind Milchprodukte. Nach dem Verzehr von Milchprodukten steigt der Gehalt an bioverfügbarem Progesteron an. ⓘ
Pflanzen
In mindestens einer Pflanze, Juglans regia, ist Progesteron nachgewiesen worden. Außerdem werden progesteronähnliche Steroide in Dioscorea mexicana gefunden. Dioscorea mexicana ist eine in Mexiko beheimatete Pflanze aus der Familie der Yamswurzelgewächse. Sie enthält ein Steroid namens Diosgenin, das aus der Pflanze gewonnen und in Progesteron umgewandelt wird. Diosgenin und Progesteron kommen auch in anderen Dioscorea-Arten sowie in anderen, nicht eng verwandten Pflanzen wie dem Bockshornklee vor. ⓘ
Eine weitere Pflanze, die leicht in Progesteron umwandelbare Substanzen enthält, ist die in Taiwan beheimatete Dioscorea pseudojaponica. Untersuchungen haben gezeigt, dass die taiwanesische Yamswurzel Saponine enthält - Steroide, die in Diosgenin und damit in Progesteron umgewandelt werden können. ⓘ
Viele andere Dioscorea-Arten aus der Familie der Yamswurzelgewächse enthalten steroidale Substanzen, aus denen Progesteron hergestellt werden kann. Zu den bekanntesten gehören Dioscorea villosa und Dioscorea polygonoides. Eine Studie ergab, dass Dioscorea villosa 3,5 % Diosgenin enthält. Dioscorea polygonoides enthält 2,64 % Diosgenin, wie durch Gaschromatographie-Massenspektrometrie nachgewiesen wurde. Viele der Dioscorea-Arten, die aus der Familie der Yamswurzelgewächse stammen, wachsen in Ländern mit tropischem und subtropischem Klima. ⓘ
Medizinische Verwendung
Progesteron wird als Medikament verwendet. Es wird in Kombination mit Östrogenen hauptsächlich in der Hormontherapie bei Wechseljahrsbeschwerden und niedrigem Sexualhormonspiegel bei Frauen eingesetzt. Außerdem wird es bei Frauen zur Unterstützung von Schwangerschaft und Fruchtbarkeit sowie zur Behandlung gynäkologischer Erkrankungen eingesetzt. Progesteron verhindert nachweislich Fehlgeburten bei Frauen mit 1) vaginalen Blutungen zu Beginn der aktuellen Schwangerschaft und 2) einer Fehlgeburt in der Vorgeschichte. Progesteron kann unter anderem durch den Mund, durch die Vagina und durch Injektion in Muskeln oder Fett eingenommen werden. ⓘ
Chemie

Progesteron ist ein natürlich vorkommendes Pregnan-Steroid und wird auch als Pregn-4-en-3,20-dion bezeichnet. Es hat eine Doppelbindung (4-En) zwischen den Positionen C4 und C5 und zwei Ketongruppen (3,20-Dion), eine an der Position C3 und die andere an der Position C20. ⓘ
Synthese
Progesteron wird im Wege der Semisynthese kommerziell hergestellt. Dabei werden im Wesentlichen zwei Wege beschritten: einer aus Yamswurzeldiosgenin, der 1940 von Marker entwickelt wurde, und ein anderer, der auf Sojaphytosterolen basiert und in den 1970er Jahren weiterentwickelt wurde. Weitere (nicht notwendigerweise kostengünstige) Semisynthesen von Progesteron sind ebenfalls berichtet worden, ausgehend von einer Vielzahl von Steroiden. So kann z. B. Kortison durch Behandlung mit Iodtrimethylsilan in Chloroform gleichzeitig an den Positionen C-17 und C-21 desoxidiert werden, um 11-Keto-Progesteron (Ketogestin) zu erzeugen, das wiederum an Position 11 reduziert werden kann, um Progesteron zu erhalten. ⓘ
Marker-Semisynthese
Eine kostengünstige Semisynthese von Progesteron aus dem aus Süßkartoffeln isolierten Pflanzensteroid Diosgenin wurde 1940 von Russell Marker für das Pharmaunternehmen Parke-Davis entwickelt. Diese Synthese ist als Marker-Degradation bekannt. ⓘ

Das 16-DPA-Zwischenprodukt ist wichtig für die Synthese vieler anderer medizinisch wichtiger Steroide. Mit einem sehr ähnlichen Ansatz kann 16-DPA aus Solanin hergestellt werden. ⓘ
Herstellung
Progesteron wird technisch in großen Mengen durch oxidativen Abbau von Stigmasterol (im Sojabohnenöl enthalten), Solanum-Alkaloiden oder aus dem Sapogenin Diosgenin gewonnen, das aus plantagenmäßig angebauten Yamswurzelgewächsen (Dioscoreaceae) isoliert wird. ⓘ

Totalsynthese
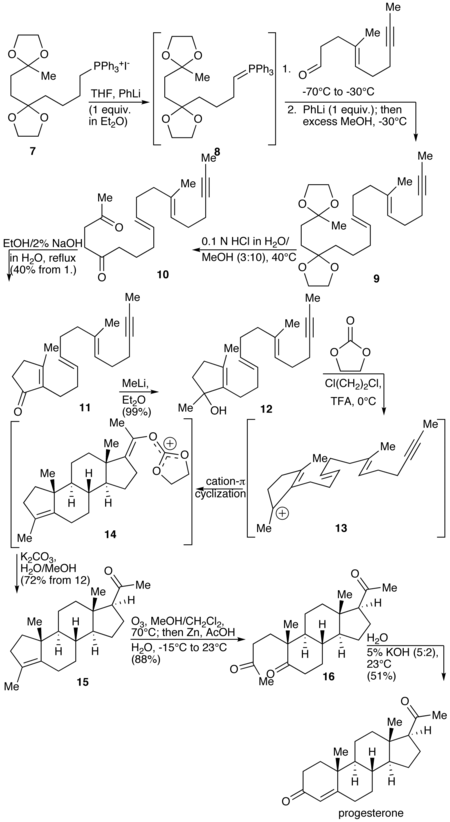
Eine Totalsynthese von Progesteron wurde 1971 von W.S. Johnson beschrieben. Die Synthese beginnt mit der Reaktion des Phosphoniumsalzes 7 mit Phenyllithium zur Herstellung des Phosphoniumylids 8. Das Ylid 8 wird mit einem Aldehyd umgesetzt, um das Alken 9 zu erzeugen. Die Ketalschutzgruppen von 9 werden hydrolysiert, um das Diketon 10 zu erzeugen, das seinerseits zum Cyclopentenon 11 cyclisiert wird. Das Keton von 11 wird mit Methyllithium umgesetzt, um den tertiären Alkohol 12 zu erhalten, der wiederum mit Säure behandelt wird, um das tertiäre Kation 13 zu bilden. Der Schlüsselschritt der Synthese ist die π-Kationenzyklisierung von 13, bei der die B-, C- und D-Ringe des Steroids gleichzeitig gebildet werden, um 14 zu erzeugen. Dieser Schritt ähnelt der kationischen Zyklisierungsreaktion, die in der Biosynthese von Steroiden verwendet wird, und wird daher als biomimetisch bezeichnet. Im nächsten Schritt wird der Enolorthoester hydrolysiert, um das Keton 15 zu bilden. Der Cyclopenten-A-Ring wird dann durch Oxidation mit Ozon geöffnet, wobei 16 entsteht. Schließlich wird das Diketon 17 durch Behandlung mit wässrigem Kaliumhydroxid einer intramolekularen Aldolkondensation unterzogen, um Progesteron herzustellen. ⓘ
Geschichte
George W. Corner und Willard M. Allen entdeckten die hormonelle Wirkung von Progesteron im Jahr 1929. In den Jahren 1931-1932 wurde nahezu reines kristallines Material mit hoher Progesteronaktivität aus dem Gelbkörper von Tieren isoliert, und 1934 wurde reines kristallines Progesteron raffiniert und gewonnen und die chemische Struktur von Progesteron bestimmt. Dies gelang Adolf Butenandt am Chemischen Institut der Technischen Hochschule in Danzig, der diese neue Verbindung aus mehreren tausend Litern Urin extrahierte. ⓘ
Die chemische Synthese von Progesteron aus Stigmasterin und Pregnandiol wurde später im selben Jahr abgeschlossen. Bis zu diesem Zeitpunkt war Progesteron, das allgemein als Gelbkörperhormon bekannt ist, von verschiedenen Gruppen unter verschiedenen Namen bezeichnet worden, darunter Corporin, Lutein, Luteosteron und Progestin. Im Jahr 1935 wurde auf der Zweiten Internationalen Konferenz über die Standardisierung von Sexualhormonen in London, England, ein Kompromiss zwischen den Gruppen geschlossen und der Name Progesteron (progestationales steroidales Keton) eingeführt. ⓘ
Progesteron wurde unabhängig von vier Arbeitsgruppen entdeckt. ⓘ
Willard Myron Allen entdeckte Progesteron zusammen mit seinem Anatomieprofessor George Washington Corner an der University of Rochester Medical School im Jahr 1933 und bestimmte als erster Schmelzpunkt, Molekülmasse und Partialstruktur. Er gab der Verbindung den Namen Progesteron, abgeleitet von Progestational Steroidal Keton. Corner und Allen entwickelten 1928 am Kaninchenendometrium einen Test zur Bestimmung der Progesteron-Aktivität. ⓘ
Tierärztliche Verwendung
Die Verwendung von Progesteron bei Tests in der Hundezucht zur Bestimmung des Eisprungs wird immer häufiger eingesetzt. Es stehen mehrere Tests zur Verfügung, aber der zuverlässigste Test ist ein Bluttest, bei dem ein Tierarzt Blut abnimmt und es zur Verarbeitung an ein Labor schickt. Die Ergebnisse liegen in der Regel innerhalb von 24 bis 72 Stunden vor. Der Grund für die Verwendung von Progesterontests ist, dass erhöhte Werte in unmittelbarer Nähe des präovulatorischen Anstiegs der Gonadotropine beginnen und während des Eisprungs und des Östrus anhalten. Wenn die Progesteronspiegel bestimmte Werte erreichen, können sie das Östrus-Stadium der Frau anzeigen. Wenn der Zeitpunkt des Eisprungs bekannt ist, lässt sich das Geburtsdatum des anstehenden Wurfs sehr genau vorhersagen. Welpen kommen in den meisten Fällen ein oder zwei Tage nach der 9-wöchigen Trächtigkeit zur Welt. Es ist jedoch nicht möglich, die Trächtigkeit mit Hilfe von Progesterontests festzustellen, wenn eine Zucht stattgefunden hat. Das liegt daran, dass der Progesteronspiegel bei Hunden während der gesamten Östrusperiode erhöht bleibt. ⓘ
Eigenschaften

Progesteron ist ein kristalliner Feststoff. Die Verbindung tritt in drei polymorphen Kristallformen auf, die sich anhand ihres Schmelzpunktes unterscheiden lassen. Die thermodynamisch stabile Form I (α-Form) schmilzt bei 129 °C (ΔfH = 26,17 kJ/mol). Die beiden anderen Formen – Form II oder β-Form (Smp. 122 °C, ΔfH = 21,42 kJ/mol) und Form III (Smp. 104 °C, ΔfH = 16,13 kJ/mol) – sind metastabil und stehen monotrop zur Form I. ⓘ
Physiologie

Progesteron wird vor allem im Corpus luteum von den Granulosazellen und in der Plazenta synthetisiert und ausgeschüttet, in geringeren Mengen auch von anderen Geweben. Die Synthese geht vom Pregnenolon aus und benötigt das Enzym 3β-Hydroxysteroid-Dehydrogenase. ⓘ
Die Ausschüttung des Hormons wird durch LH stimuliert. Die Freisetzung bewirkt die Dezidualisierung, eine für die Nidation benötigte Modifikation des proliferierten Endometriums, besonders deren Lamina functionalis, die dadurch drüsenreich und stark durchblutet wird (dann als Dezidua bezeichnet) sowie eine Anpassung der Uterusmuskulatur an den wachsenden Embryo. ⓘ
In manchen steroidproduzierenden Zellen der Gonaden fungiert das Progesteron als Ausgangsstoff für die Synthese von Androgenen und Estrogenen. ⓘ
Progesteron wird zu Pregnandiol metabolisiert und nach Glucuronidierung über den Urin ausgeschieden. ⓘ
Pathophysiologie
Erhöhte Progesteronwerte ergeben sich neben der Schwangerschaft vor allem bei Eierstocktumoren und beim adrenogenitalen Syndrom (AGS). Bei Zyklusstörungen und beim sogenannten Hypogonadismus, einer Unterentwicklung der Eierstöcke, ist die Progesteronkonzentration verringert. ⓘ
Verwendung
Progesteron wird zur Therapie der Endometriose verwendet. ⓘ
Handelsnamen
Monopräparate
