Ibuprofen
 | |
 | |
| Klinische Daten | |
|---|---|
| Aussprache | /ˈaɪbjuːproʊfɛn/, /aɪbjuːˈproʊfən/, EYE-bew-PROH-fən |
| Handelsnamen | Advil, Motrin, Nurofen, andere |
| Andere Namen | Isobutylphenylpropionsäure |
| AHFS/Drugs.com | Monographie |
| MedlinePlus | a682159 |
| Lizenz-Daten | |
| Schwangerschaft Kategorie |
|
| Wege der Verabreichung | oral, rektal, topisch, intravenös |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | 80-100% (durch den Mund), 87% (rektal) |
| Proteinbindung | 98% |
| Verstoffwechselung | Leber (CYP2C9) |
| Metaboliten | Ibuprofen-Glucuronid, 2-Hydroxyibuprofen, 3-Hydroxyibuprofen, Carboxy-Ibuprofen, 1-Hydroxyibuprofen |
| Beginn der Wirkung | 30 Minuten |
| Eliminationshalbwertszeit | 2-4 h |
| Ausscheidung | Urin (95%) |
| Bezeichner | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| PDB-Ligand |
|
| Chemische und physikalische Daten | |
| Formel | C13H18O2 |
| Molare Masse | 206,285 g-mol-1 |
| 3D-Modell (JSmol) | |
| Chiralität | Racemisches Gemisch |
| Dichte | 1,03 g/cm3 |
| Schmelzpunkt | 75 bis 78 °C (167 bis 172 °F) |
| Siedepunkt | 157 °C (315 °F) bei 4 mmHg |
| Löslichkeit in Wasser | 0,021 mg/ml (20 °C) |
SMILES
| |
InChI
| |
| (Überprüfen) | |
Ibuprofen ist ein Medikament aus der Klasse der nichtsteroidalen Antirheumatika (NSAID), das zur Behandlung von Schmerzen, Fieber und Entzündungen eingesetzt wird. Dazu gehören schmerzhafte Menstruationsblutungen, Migräne und rheumatoide Arthritis. Es kann auch verwendet werden, um einen offenen Ductus arteriosus bei Frühgeborenen zu schließen. Es kann durch den Mund oder intravenös verabreicht werden. Die Wirkung setzt in der Regel innerhalb einer Stunde ein. ⓘ
Häufige Nebenwirkungen sind Sodbrennen und Hautausschlag. Im Vergleich zu anderen NSAIDs kann es andere Nebenwirkungen wie Magen-Darm-Blutungen haben. Es erhöht das Risiko von Herzversagen, Nierenversagen und Leberversagen. Bei niedrigen Dosen scheint es das Risiko eines Herzinfarkts nicht zu erhöhen, bei höheren Dosen jedoch schon. Ibuprofen kann auch Asthma verschlimmern. Während unklar ist, ob es in der frühen Schwangerschaft sicher ist, scheint es in der späteren Schwangerschaft schädlich zu sein und wird daher nicht empfohlen. Wie andere NSAIDs hemmt Ibuprofen die Produktion von Prostaglandinen, indem es die Aktivität des Enzyms Cyclooxygenase (COX) vermindert. Ibuprofen ist ein schwächeres entzündungshemmendes Mittel als andere NSAIDs. ⓘ
Ibuprofen wurde 1961 von Stewart Adams und John Nicholson entdeckt, als sie bei Boots UK Limited arbeiteten, und zunächst als Brufen vermarktet. Es ist unter einer Reihe von Handelsnamen erhältlich, darunter Nurofen, Advil und Motrin. Ibuprofen wurde erstmals 1969 im Vereinigten Königreich und 1974 in den Vereinigten Staaten auf den Markt gebracht. Es steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation. Es ist als Generikum erhältlich. Im Jahr 2019 war es mit mehr als 21 Millionen Verschreibungen das 29. am häufigsten verschriebene Medikament in den Vereinigten Staaten. ⓘ
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Stereoisomerengemisch – Strukturformel ohne Stereochemie | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Ibuprofen | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C13H18O2 | ||||||||||||||||||
| Kurzbeschreibung |
weißer, fast geruchloser Feststoff | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Wirkstoffklasse |
nichtsteroidales Antirheumatikum | ||||||||||||||||||
| Wirkmechanismus |
hemmt nichtselektiv die Cyclooxygenasen I und II | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 206,28 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,175 g·cm−3 | ||||||||||||||||||
| Schmelzpunkt |
| ||||||||||||||||||
| Siedepunkt |
154–157 °C (5 hPa) | ||||||||||||||||||
| Dampfdruck |
1,2 mPa (25 °C) | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
| ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Medizinische Anwendungen

Ibuprofen wird hauptsächlich zur Behandlung von Fieber (einschließlich Fieber nach einer Impfung), leichten bis mäßigen Schmerzen (einschließlich Schmerzlinderung nach einer Operation), schmerzhafter Menstruation, Arthrose, Zahnschmerzen, Kopfschmerzen und Schmerzen durch Nierensteine eingesetzt. Etwa 60 % der Menschen sprechen auf jedes nichtsteroidale entzündungshemmende Medikament an; wer auf ein bestimmtes Medikament nicht gut anspricht, kann auch auf ein anderes reagieren. ⓘ
Es wird bei entzündlichen Erkrankungen wie der juvenilen idiopathischen Arthritis und der rheumatoiden Arthritis eingesetzt. Es wird auch bei Herzbeutelentzündung und offenem Ductus arteriosus eingesetzt. ⓘ
Wenn ein Patient sich selbst mit rezeptfreiem Ibuprofen behandelt, sollte es nicht länger als 10 Tage eingenommen werden, es sei denn, der Patient hat mit seinem Arzt gesprochen. ⓘ
Lysin
In einigen Ländern ist Ibuprofen-Lysin (das Lysin-Salz von Ibuprofen, manchmal auch "Ibuprofen-Lysinat" genannt) für die Behandlung der gleichen Erkrankungen wie Ibuprofen zugelassen; das Lysin-Salz wird verwendet, weil es besser wasserlöslich ist. ⓘ
Ibuprofen-Lysin wird zur raschen Schmerzlinderung verkauft; wird es in Form eines Lysinsalzes verabreicht, ist die Absorption viel schneller (35 Minuten im Vergleich zu 90-120 Minuten). In einer von Sanofi finanzierten klinischen Studie mit 351 Teilnehmern im Jahr 2020 wurde jedoch kein signifikanter Unterschied zwischen Ibuprofen und Ibuprofen-Lysin hinsichtlich des möglichen Wirkungseintritts oder der analgetischen Wirksamkeit festgestellt. ⓘ
Im Jahr 2006 wurde Ibuprofen-Lysin in den USA von der Food and Drug Administration (FDA) für den Verschluss des Ductus arteriosus bei Frühgeborenen mit einem Gewicht von 500 bis 1.500 g zugelassen, die nicht älter als 32 Wochen sind, wenn die übliche medizinische Behandlung (wie Flüssigkeitsrestriktion, Diuretika und Atemunterstützung) nicht wirksam ist. ⓘ
Unerwünschte Wirkungen
Häufig (1 bis 10 %) bis sehr häufig (> 10 %) können gastrointestinale Beschwerden wie Sodbrennen, Übelkeit oder Durchfall auftreten. Das Auftreten von Magen-Darm-Blutungen, Magengeschwüren oder Magenschleimhautentzündungen (Gastritis) sowie Magendurchbrüchen, auch mit tödlichem Ausgang, wird gelegentlich beobachtet und hängt von der Dosis und der Anwendungsdauer ab. Bei älteren Patienten treten diese unerwünschten Nebenwirkungen häufiger auf. ⓘ
Bei chronisch entzündlichen Darmerkrankungen (Morbus Crohn, Colitis ulcerosa) kann Ibuprofen schubauslösend wirken. Überempfindlichkeitsreaktionen wie Hautausschlag oder Hautjucken (Pruritus) sind möglich. ⓘ
Der Einfluss von Ibuprofen auf die Blutgerinnung ist vergleichsweise gering, es hemmt die Thrombozytenfunktion lediglich reversibel und damit die Blutgerinnung nur kurzfristig, im Gegensatz zu Acetylsalicylsäure als einziger irreversibler COX-Hemmer auf dem Markt. Dennoch kann nach Operationen das Risiko von Nachblutungen steigen. In Fällen, bei denen Ibuprofen die Magenschleimhaut entzündlich verändert, kann die durch das Medikament bewirkte Gerinnungshemmung dazu führen, dass aus der Magenwand unkontrolliert über einen längeren Zeitraum Blut sickert. ⓘ
Ödeme (z. B. auch Knochenmarködeme) sind eine bekannte Nebenwirkung vieler Schmerzmittel, welche auf einer Hemmung der Prostaglandinsynthese beruhen, wie dies auch bei Ibuprofen bekannt ist. ⓘ
Im Übrigen wird vereinzelt vom Auftreten einer Agranulozytose (starke lebensbedrohliche Verminderung der Granulozyten) berichtet. ⓘ
Gerade bei längerer Verabreichung kann es bei Ibuprofen zu stärkeren Nebenwirkungen kommen. Nach langfristiger Gabe erhöht sich das Risiko für gastrointestinale Blutungen um den Faktor vier. Außerdem steigt bei hoch dosierter Gabe das Risiko auf kardiovaskuläre Ereignisse um den Faktor 2,2. ⓘ
Zu den unerwünschten Wirkungen gehören Übelkeit, Dyspepsie, Durchfall, Verstopfung, gastrointestinale Ulzerationen/Blutungen, Kopfschmerzen, Schwindel, Hautausschlag, Salz- und Flüssigkeitsretention und hoher Blutdruck. ⓘ
Seltene unerwünschte Wirkungen sind Speiseröhrengeschwüre, Herzversagen, hohe Kaliumwerte im Blut, Nierenfunktionsstörungen, Verwirrtheit und Bronchospasmus. Ibuprofen kann Asthma verschlimmern, manchmal mit tödlichem Ausgang. ⓘ
Allergische Reaktionen, einschließlich Anaphylaxie und anaphylaktischer Schock, können auftreten. Ibuprofen kann in Blut, Plasma oder Serum quantifiziert werden, um das Vorhandensein des Arzneimittels bei einer Person nachzuweisen, bei der eine anaphylaktische Reaktion aufgetreten ist, um eine Vergiftungsdiagnose bei Personen zu bestätigen, die ins Krankenhaus eingeliefert wurden, oder um bei einer gerichtsmedizinischen Todesfalluntersuchung zu helfen. Eine Monographie über die Plasmakonzentration von Ibuprofen, die Zeit seit der Einnahme und das Risiko der Entwicklung einer Nierentoxizität bei Personen, die eine Überdosis eingenommen haben, wurde veröffentlicht. ⓘ
Im Oktober 2020 verlangte die US-Arzneimittelbehörde (FDA) eine Aktualisierung der Arzneimittelbeschreibung für alle nichtsteroidalen entzündungshemmenden Medikamente, um das Risiko von Nierenproblemen bei ungeborenen Babys zu beschreiben, die zu niedrigem Fruchtwasser führen. Es wird empfohlen, NSAIDs bei Schwangeren ab der 20. Schwangerschaftswoche zu vermeiden. ⓘ
Kardiovaskuläres Risiko
Zusammen mit mehreren anderen NSAIDs wurde festgestellt, dass die chronische Einnahme von Ibuprofen bei Frauen mit dem Risiko der Entwicklung von Bluthochdruck (wenn auch in geringerem Maße als bei Paracetamol) und Herzinfarkt korreliert, insbesondere bei chronischer Einnahme höherer Dosen. Am 9. Juli 2015 verschärfte die US-Arzneimittelbehörde (FDA) die Warnungen vor einem erhöhten Herzinfarkt- und Schlaganfallrisiko im Zusammenhang mit Ibuprofen und verwandten NSAIDs; das NSAID Aspirin ist von dieser Warnung nicht betroffen. Die Europäische Arzneimittel-Agentur (EMA) hat 2015 ähnliche Warnhinweise herausgegeben. ⓘ
Haut
Zusammen mit anderen NSAIDs wurde Ibuprofen mit dem Auftreten von bullösem Pemphigoid oder pemphigoidähnlicher Blasenbildung in Verbindung gebracht. Wie andere NSAIDs wurde auch Ibuprofen als photosensibilisierendes Mittel gemeldet, das jedoch im Vergleich zu anderen Vertretern der 2-Arylpropionsäureklasse als schwach photosensibilisierend gilt. Wie andere NSAR ist Ibuprofen eine äußerst seltene Ursache für die Autoimmunerkrankung Stevens-Johnson-Syndrom (SJS). Ibuprofen ist auch eine extrem seltene Ursache der toxischen epidermalen Nekrolyse. ⓘ
Wechselwirkungen
Alkohol
Der Genuss von Alkohol während der Einnahme von Ibuprofen kann das Risiko von Magenblutungen erhöhen. ⓘ
Aspirin
Nach Angaben der Food and Drug Administration (FDA) kann Ibuprofen die thrombozytenaggregationshemmende Wirkung von niedrig dosiertem Aspirin beeinträchtigen, wodurch Aspirin bei der Anwendung zum Schutz des Herzens und zur Vorbeugung von Schlaganfällen möglicherweise weniger wirksam ist. Durch einen ausreichenden zeitlichen Abstand zwischen der Einnahme von Ibuprofen und Aspirin mit sofortiger Wirkstofffreisetzung (IR) kann dieses Problem vermieden werden. Die empfohlene Zeitspanne zwischen einer Ibuprofen- und einer Aspirindosis hängt davon ab, was zuerst eingenommen wird. Bei Ibuprofen, das nach IR-Aspirin eingenommen wird, sind es 30 Minuten oder mehr, bei Ibuprofen, das vor IR-Aspirin eingenommen wird, 8 Stunden oder mehr. Für magensaftresistentes Aspirin kann dieses Timing jedoch nicht empfohlen werden. Wird Ibuprofen jedoch nur gelegentlich eingenommen, ohne dass der empfohlene Zeitpunkt eingehalten wird, ist die Verringerung der kardioprotektiven Wirkung und der Schlaganfallprävention eines täglichen Aspirinschemas minimal. ⓘ
Paracetamol
Ibuprofen in Kombination mit Paracetamol gilt bei kurzfristiger Anwendung bei Kindern als allgemein sicher. ⓘ
Überdosierung
Seit der Zulassung von Ibuprofen als rezeptfreies Arzneimittel sind Überdosierungen keine Seltenheit mehr. In der medizinischen Fachliteratur wird über zahlreiche Überdosierungserfahrungen berichtet, obwohl die Häufigkeit lebensbedrohlicher Komplikationen bei einer Ibuprofen-Überdosierung gering ist. Die menschliche Reaktion auf eine Überdosierung reicht vom Fehlen von Symptomen bis hin zu einem tödlichen Ausgang trotz intensivmedizinischer Behandlung. Die meisten Symptome sind eine Übersteigerung der pharmakologischen Wirkung von Ibuprofen und umfassen Bauchschmerzen, Übelkeit, Erbrechen, Schläfrigkeit, Schwindel, Kopfschmerzen, Ohrensausen und Nystagmus. In seltenen Fällen wurden schwerwiegendere Symptome wie gastrointestinale Blutungen, Krampfanfälle, metabolische Azidose, hohe Kaliumwerte im Blut, niedriger Blutdruck, langsame Herzfrequenz, schnelle Herzfrequenz, Vorhofflimmern, Koma, Leberfunktionsstörungen, akutes Nierenversagen, Zyanose, Atemdepression und Herzstillstand berichtet. Der Schweregrad der Symptome hängt von der eingenommenen Dosis und der verstrichenen Zeit ab; allerdings spielt auch die individuelle Empfindlichkeit eine wichtige Rolle. Im Allgemeinen ähneln die bei einer Überdosierung von Ibuprofen beobachteten Symptome den Symptomen, die bei einer Überdosierung anderer NSAIDs auftreten. ⓘ
Die Korrelation zwischen dem Schweregrad der Symptome und den gemessenen Ibuprofen-Plasmaspiegeln ist schwach. Toxische Wirkungen sind bei Dosen unter 100 mg/kg unwahrscheinlich, können aber bei Dosen über 400 mg/kg (etwa 150 Tabletten à 200 mg für einen durchschnittlichen Mann) schwerwiegend sein; hohe Dosen bedeuten jedoch nicht, dass der klinische Verlauf wahrscheinlich tödlich ist. Eine genaue tödliche Dosis ist schwer zu bestimmen, da sie von Alter, Gewicht und Begleitumständen der einzelnen Person abhängen kann. ⓘ
Die Behandlung einer Ibuprofen-Überdosierung richtet sich danach, wie die Symptome auftreten. In Fällen, die früh auftreten, wird eine Dekontamination des Magens empfohlen. Dazu wird Aktivkohle verwendet, die das Medikament adsorbiert, bevor es in den Blutkreislauf gelangen kann. Eine Magenspülung wird heute nur noch selten durchgeführt, kann aber in Betracht gezogen werden, wenn die aufgenommene Menge potenziell lebensbedrohlich ist und sie innerhalb von 60 Minuten nach der Einnahme durchgeführt werden kann. Gezieltes Erbrechen wird nicht empfohlen. Die Mehrzahl der eingenommenen Ibuprofen-Mengen hat nur leichte Wirkungen, und die Behandlung einer Überdosierung ist unkompliziert. Es sollten Standardmaßnahmen zur Aufrechterhaltung einer normalen Urinausscheidung ergriffen und die Nierenfunktion überwacht werden. Da Ibuprofen saure Eigenschaften hat und auch über den Urin ausgeschieden wird, ist eine forcierte alkalische Diurese theoretisch von Vorteil. Da Ibuprofen jedoch stark proteingebunden im Blut vorliegt, ist die Ausscheidung des unveränderten Arzneimittels über die Nieren minimal. Eine forcierte alkalische Diurese ist daher von begrenztem Nutzen. ⓘ
Fehlgeburten
Eine Studie an schwangeren Frauen legt nahe, dass die Wahrscheinlichkeit einer Fehlgeburt bei Frauen, die NSAR jeglicher Art oder Menge (einschließlich Ibuprofen, Diclofenac und Naproxen) einnehmen, 2,4-mal höher ist als bei Frauen, die diese Medikamente nicht einnehmen. In einer israelischen Studie wurde jedoch kein erhöhtes Risiko für eine Fehlgeburt in der Gruppe der Mütter festgestellt, die NSAIDs einnahmen. ⓘ
Pharmakologie
NSAIDs wie Ibuprofen wirken durch Hemmung der Cyclooxygenase-Enzyme (COX), die Arachidonsäure in Prostaglandin H2 (PGH2) umwandeln. PGH2 wiederum wird von anderen Enzymen in verschiedene andere Prostaglandine (die als Vermittler von Schmerzen, Entzündungen und Fieber wirken) und in Thromboxan A2 (das die Thrombozytenaggregation anregt und zur Bildung von Blutgerinnseln führt) umgewandelt. ⓘ
Wie Aspirin und Indomethacin ist Ibuprofen ein nichtselektiver COX-Hemmer, da es zwei Isoformen der Cyclooxygenase, COX-1 und COX-2, hemmt. Die analgetische, fiebersenkende und entzündungshemmende Wirkung von NSAIDs scheint hauptsächlich durch die Hemmung von COX-2 zu wirken, wodurch die Synthese von Prostaglandinen, die an der Vermittlung von Entzündungen, Schmerzen, Fieber und Schwellungen beteiligt sind, verringert wird. Die fiebersenkenden Wirkungen sind möglicherweise auf eine Wirkung auf den Hypothalamus zurückzuführen, die zu einer erhöhten peripheren Durchblutung, einer Vasodilatation und einer anschließenden Wärmeableitung führt. Die Hemmung von COX-1 wäre hingegen für die unerwünschten Wirkungen auf den Magen-Darm-Trakt verantwortlich. Die Rolle der einzelnen COX-Isoformen bei den analgetischen, entzündungshemmenden und magenschädigenden Wirkungen von NSAIDs ist jedoch ungewiss, und verschiedene Wirkstoffe verursachen unterschiedliche Grade von Analgesie und Magenschädigung. ⓘ
Ibuprofen wird als racemisches Gemisch verabreicht. Das R-Enantiomer unterliegt in vivo einer umfangreichen Umwandlung in das S-Enantiomer. Es wird angenommen, dass das S-Enantiomer das pharmakologisch aktivere Enantiomer ist. Die Umwandlung des R-Enantiomers erfolgt durch eine Reihe von drei wichtigen Enzymen. Zu diesen Enzymen gehören die Acyl-CoA-Synthetase, die das R-Enantiomer in (-)-R-Ibuprofen I-CoA umwandelt, die 2-Arylpropionyl-CoA-Epimerase, die (-)-R-Ibuprofen I-CoA in (+)-S-Ibuprofen I-CoA umwandelt, und die Hydrolase, die (+)-S-Ibuprofen I-CoA in das S-Enantiomer umwandelt. Neben der Umwandlung von Ibuprofen in das S-Enantiomer kann der Körper Ibuprofen in verschiedene andere Verbindungen umwandeln, darunter zahlreiche Hydroxyl-, Carboxyl- und Glucuronyl-Metaboliten. Praktisch alle von ihnen haben keine pharmakologischen Wirkungen. ⓘ
Im Gegensatz zu den meisten anderen NSAIDs wirkt Ibuprofen auch als Hemmstoff der Rho-Kinase und kann bei der Genesung nach Rückenmarksverletzungen nützlich sein. ⓘ
Pharmakokinetik
Nach oraler Verabreichung wird die maximale Serumkonzentration nach 1 bis 2 Stunden erreicht, und bis zu 99 % des Wirkstoffs sind an Plasmaproteine gebunden. Der größte Teil des Ibuprofens wird metabolisiert und innerhalb von 24 Stunden mit dem Urin ausgeschieden. 1 % des unveränderten Arzneimittels wird jedoch über die Galle ausgeschieden. ⓘ
Chemie
Ibuprofen ist praktisch unlöslich in Wasser, aber sehr gut löslich in den meisten organischen Lösungsmitteln wie Ethanol (66,18 g/100 mL bei 40 °C für 90 % EtOH), Methanol, Aceton und Dichlormethan. ⓘ
Die ursprüngliche Synthese von Ibuprofen durch die Boots-Gruppe begann mit der Verbindung 2-Methylpropylbenzol. Die Synthese erfolgte in sechs Schritten. Eine moderne, umweltfreundlichere Technik für die Synthese umfasst nur drei Schritte. ⓘ
Stereochemie
 |

|
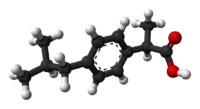 |
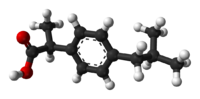
|
| (R)-Ibuprofen | (S)-Ibuprofen |
Ibuprofen enthält, wie andere 2-Arylpropionat-Derivate wie Ketoprofen, Flurbiprofen und Naproxen, ein Stereocenter in der α-Position des Propionat-Anteils. Das in Apotheken verkaufte Produkt ist ein racemisches Gemisch der S- und R-Isomere. Das S-Isomer (rechtsdrehend) ist das biologisch aktivere; dieses Isomer wurde isoliert und medizinisch verwendet (Einzelheiten siehe Dexibuprofen). ⓘ
Das Isomerase-Enzym alpha-Methylacyl-CoA-Racemase wandelt (R)-Ibuprofen in das (S)-Enantiomer um. ⓘ
Geschichte
Die Entdeckung von Ibuprofen war das Ergebnis eines Forschungsprojekts bei The Boots Pure Drug Company Ltd. unter Stewart Adams in den 1950er und 1960er Jahren. Das Ziel des Projekts war die Entwicklung neuer Arzneistoffe zur Behandlung rheumatischer Erkrankungen. Als Vorbild wurde die Acetylsalicylsäure gewählt, da sie als die nebenwirkungsärmste Substanz unter den damals gebräuchlichen Standardtherapeutika wie Glucocorticoide und Phenylbutazon galt. Erste Versuche mit Salicyl- und den ihr verwandten Phthalsäureabkömmlingen führten zwar zu wirksamen, aber deutlich toxischeren Substanzen. Dafür wurden Erkenntnisse zur Struktur-Wirkungsbeziehung, wie beispielsweise die Wichtigkeit der Carbonsäuregruppe, gefunden. Ausgehend von dieser Erkenntnis wurde die Suche nach neuen antientzündlichen Substanzen auf andere Gruppen von Carbonsäureverbindungen erweitert. Als besonders vielversprechend erwiesen sich 1958 in präklinischen Tests eine Gruppe von Phenoxyalkansäuren, die ursprünglich von Boots als Herbizide entwickelt wurden. Trotz positiver Resultate im Tierversuch stellten sie sich als klinisch unwirksam heraus. Der Durchbruch gelang mit den von John Nicholson bei Boots synthetisierten Phenylalkansäuren. Diese Substanzen, einschließlich Ibuprofen, wurden 1961 als antiinflammatorische Substanzen zum Patent angemeldet. Drei Substanzen mit einer Phenylessigsäurepartialstruktur wurden zunächst klinisch getestet. Zwei der getesteten Substanzen führten zu Ausschlag, die dritte, Ibufenac, erwies sich nach längerer Nutzung nach Markteinführung als lebertoxisch. Ibuprofen, das auf Grund von Sicherheitsbedenken zunächst nicht klinisch getestet wurde, erwies sich bei ersten Versuchen im Jahr 1966 an Patienten mit rheumatoider Arthritis mit einer Tagesdosis von 300 bis 600 mg als wirksam und sicher. ⓘ
1969 wurde Ibuprofen in Großbritannien unter dem Markennamen Brufen mit einer empfohlenen Tagesdosis von 600 bis 800 mg in den Markt eingeführt. In der Anfangszeit stellten sich die Behandlungsergebnisse als enttäuschend heraus, woraufhin nach weiteren klinischen Studien die Tagesdosis auf zunächst 1200 mg und später auf die heute gebräuchliche Tagesdosis von 1200 bis 2400 mg erhöht wurde. In den USA wurde Ibuprofen 1974 von Upjohn unter dem Markennamen Motrin mit einer Tagesdosis von 1200 bis 3200 mg eingeführt. ⓘ
Nach einem 1979 zunächst gescheiterten Antrag wurde Ibuprofen zuerst 1983 in Großbritannien mit einer Einzeldosis von bis zu 200 mg und einer Tagesdosis bis 1200 mg aus der ärztlichen Verschreibungspflicht entlassen. Ein Jahr später wurde es auch in den USA mit einer Tagesdosis bis zu 1600 mg verschreibungsfrei. In Deutschland ist Ibuprofen seit 1989 in einer Einzeldosis von bis zu 200 mg und seit 1998 auch in bis zu 400 mg zur oralen Behandlung von Schmerzen und Fieber bis zu einer maximalen Tagesdosis von 1200 mg ohne ärztliche Verordnung in Apotheken erhältlich. ⓘ

Das Medikament wurde 1969 im Vereinigten Königreich und 1974 in den Vereinigten Staaten zur Behandlung von rheumatoider Arthritis eingeführt. Später, in den Jahren 1983 und 1984, war es das erste NSAID (neben Aspirin), das in diesen beiden Ländern rezeptfrei erhältlich war. Boots wurde 1985 für die Entwicklung des Medikaments mit dem Queen's Award for Technical Achievement ausgezeichnet. Dr. Adams wurde daraufhin 1987 mit dem Order of the British Empire (OBE) ausgezeichnet. ⓘ
Im November 2013 wurde die Arbeit an Ibuprofen durch die Anbringung einer blauen Plakette der Royal Society of Chemistry am Boots-Standort Beeston Factory in Nottingham gewürdigt, auf der zu lesen ist:
In Anerkennung der in den 1980er Jahren von The Boots Company PLC geleisteten Arbeit an der Entwicklung von Ibuprofen, die dazu führte, dass es nicht mehr verschreibungspflichtig, sondern frei verkäuflich ist und somit von Millionen von Menschen weltweit verwendet wird ⓘ
und eine weitere in der BioCity Nottingham, dem Standort des ursprünglichen Labors, mit der Aufschrift:
In Anerkennung der bahnbrechenden Forschungsarbeit von Dr. Stewart Adams und Dr. John Nicholson in der Forschungsabteilung von Boots hier in der Pennyfoot Street, die zur Entdeckung des Ibuprofens führte, das von Millionen Menschen weltweit zur Schmerzlinderung verwendet wird. ⓘ
Gesellschaft und Kultur
Verfügbarkeit

Ibuprofen ist seit 1969 im Vereinigten Königreich und seit 1974 in den Vereinigten Staaten auf Rezept erhältlich. In den folgenden Jahren haben das gute Verträglichkeitsprofil und die umfangreichen Erfahrungen in der Bevölkerung sowie in den so genannten Phase-IV-Studien (Studien nach der Zulassung) dazu geführt, dass Ibuprofen weltweit in Apotheken sowie in Supermärkten und anderen Einzelhandelsgeschäften rezeptfrei erhältlich ist. ⓘ
Ibuprofen ist sein Internationaler Freiname (INN), sein British Approved Name (BAN), sein Australian Approved Name (AAN) und sein United States Adopted Name (USAN). In den USA ist Motrin seit 1974 und Advil seit 1984 auf dem Markt. Ibuprofen ist in den Vereinigten Staaten bis zu der von der FDA 1984 festgelegten Höchstdosis rezeptfrei erhältlich, höhere Dosen werden nur selten verschrieben. ⓘ
Im Jahr 2009 wurde in den Vereinigten Staaten die erste injizierbare Formulierung von Ibuprofen unter dem Handelsnamen Caldolor zugelassen. ⓘ
Art der Anwendung und Dosierung
Ibuprofen kann oral, rektal, dermal, topisch oder intravenös verabreicht werden. Es wird in Abhängigkeit von Indikation, Alter, Körpergewicht und Applikationsweg dosiert. Nach oraler Gabe bleibt Ibuprofen etwa zweieinhalb Stunden lang in gleicher Konzentration im Blut, danach nimmt die Wirkung ab. Eine Dosisanpassung wird unter anderem bei Kindern vorgenommen. ⓘ
Bei schweren Nieren- oder Leberfunktionsstörungen ist die Anwendung von Ibuprofen kontraindiziert. ⓘ
Forschung
Ibuprofen wird aufgrund seiner entzündungshemmenden Eigenschaften manchmal zur Behandlung von Akne eingesetzt und wurde in Japan in topischer Form für Akne bei Erwachsenen verkauft. Wie andere NSAIDs kann Ibuprofen bei der Behandlung von schwerer orthostatischer Hypotonie (niedriger Blutdruck beim Aufstehen) nützlich sein. Der Nutzen von NSAIDs bei der Prävention und Behandlung der Alzheimer-Krankheit ist unklar. ⓘ
Ibuprofen wird mit einem geringeren Risiko für die Parkinson-Krankheit in Verbindung gebracht und kann diese verzögern oder verhindern. Aspirin, andere NSAIDs und Paracetamol (Paracetamol) hatten keinen Einfluss auf das Parkinson-Risiko. Im März 2011 gaben Forscher der Harvard Medical School in der Fachzeitschrift Neurology bekannt, dass Ibuprofen einen neuroprotektiven Effekt auf das Risiko der Entwicklung der Parkinson-Krankheit hat. Menschen, die regelmäßig Ibuprofen einnahmen, hatten ein um 38 % geringeres Risiko, an Parkinson zu erkranken, während für andere Schmerzmittel wie Aspirin und Paracetamol keine derartige Wirkung festgestellt wurde. Die Einnahme von Ibuprofen zur Senkung des Parkinson-Risikos in der Allgemeinbevölkerung wäre nicht unproblematisch, da es zu unerwünschten Wirkungen auf das Harn- und Verdauungssystem kommen kann. ⓘ
Einige Nahrungsergänzungsmittel könnten gefährlich sein, wenn sie zusammen mit Ibuprofen und anderen NSAIDs eingenommen werden, aber bis 2016 müssen noch weitere Untersuchungen durchgeführt werden, um sicher zu sein. Zu diesen Nahrungsergänzungsmitteln gehören solche, die die Thrombozytenaggregation verhindern können, wie Ginkgo, Knoblauch, Ingwer, Heidelbeere, Dong Quai, Mutterkraut, Ginseng, Kurkuma, Mädesüß (Filipendula ulmaria) und Weide (Salix spp.); solche, die Cumarin enthalten, wie Kamille, Rosskastanie, Bockshornklee und Rotklee; und solche, die das Risiko von Blutungen erhöhen, wie Tamarinde. ⓘ
COVID-19
In Córdoba, Argentinien, wird Ibuprofen zur Behandlung von COVID-19 erforscht, wobei es in einer hypertonen Lösung verwendet und inhaliert wird. Die klinischen Versuche begannen im Juni 2020. Es gibt keine validierte (von Fachleuten überprüfte) Veröffentlichung, die die Wirksamkeit von Ibuprofen bei der Behandlung von COVID-19 belegt, und es gibt auch keine Belege dafür, dass es die SARS-CoV-2-Infektiosität in irgendeinem Test blockiert, weder bei kultivierten Zellen noch bei Tieren. Die einzige Veröffentlichung der argentinischen Gruppe ist in der umstrittenen Zeitschrift "Medical Hypotheses" erschienen und enthält keinerlei Daten über die Wirksamkeit von Ibuprofen. Sie enthält lediglich einen hypothetischen Vorschlag, der sich in erster Linie auf Daten von anderen Viren stützt, die sich von SARS-CoV-2 stark unterscheiden. ⓘ
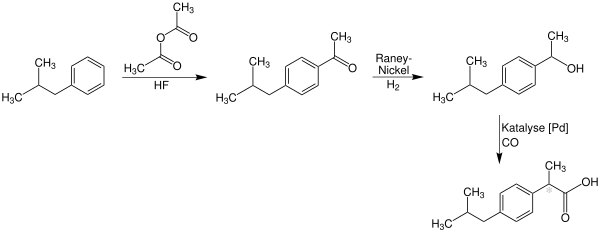
Darstellung
Die bei Boots entwickelte Syntheseroute verläuft über insgesamt sechs Stufen und geht von Isobutylbenzol aus. Dieses wird zunächst in einer Friedel-Crafts-Acylierung mit Essigsäureanhydrid zum Keton umgesetzt, anschließend folgt eine Darzens-Glycidester-Kondensation mit Chloressigsäureethylester zum Epoxid. Hydrolyse und Decarboxylierung führen zum Aldehyd, der mit Hydroxylamin zunächst zum Oxim, anschließend zum Nitril umgesetzt und schließlich zur freien Säure hydrolysiert wird. ⓘ
Ein neuerer Syntheseweg geht ebenfalls von Isobutylbenzol aus, das im ersten Schritt acyliert wird, das Keton wird hier jedoch mit Raney-Nickel und Wasserstoff zum Alkohol reduziert und anschließend unter Palladium-Katalyse direkt zum Produkt carbonyliert. ⓘ
Dieser Syntheseweg wurde 1997 mit dem Greener Synthetic Pathways Award für Grüne Chemie ausgezeichnet. ⓘ
In beiden technischen Synthesen wird ein racemisches Gemisch der beiden Enantiomere erhalten. ⓘ
Pharmakokinetik
Die Plasmahalbwertszeit beträgt etwa zwei bis drei Stunden. In geringeren Dosen (200 bis 400 mg für Erwachsene) wirkt Ibuprofen schmerzlindernd und fiebersenkend, in höheren Dosen (bis 800 mg für Erwachsene) zusätzlich entzündungshemmend. Die Resorption erfolgt hauptsächlich im Dünndarm, aber auch teilweise im Magen. Bei oraler Gabe werden nach ein bis zwei Stunden maximale Plasmaspiegel gemessen. Nach Metabolisierung in der Leber (Hydroxylierung, Carboxylierung) werden die pharmakologisch unwirksamen Metabolite vollständig, hauptsächlich (90 %) über die Nieren (renal), aber auch über die Gallenflüssigkeit (biliär), eliminiert. In einer Tierstudie mit Mäusen konnte die Bioverfügbarkeit und Wirksamkeit von Ibuprofen mit Piperin, einem Inhaltsstoff des Pfeffers, erhöht werden. ⓘ
Analytik
Die zuverlässige qualitative und quantitative Bestimmung von Ibuprofen und seinen Metaboliten in den unterschiedlichsten Untersuchungsgütern gelingt nach angemessener Probenvorbereitung durch Kopplung chromatographischer Verfahren mit der Massenspektrometrie. Unter dem Einsatz enantioselektiver Verfahren lassen sich auch die Enantiomeren des Ibuprofens trennen und quantifizieren. Auch bei ökotoxikologischen Fragen so z. B. der Untersuchung benthischer Organismen lassen sich diese Verfahren einsetzen. ⓘ
Anwendung
Anwendungsgebiete
Die Anwendungsgebiete sind allgemein zur Schmerztherapie wie bei der rheumatoiden Arthritis, bei Schmerzen der Muskeln und des Bewegungsapparates, bei der akuten Gicht, bei Kopf- und Zahnschmerzen, akute Menstruationsbeschwerden, zur Fiebersenkung und speziell bei Kindern zur Behandlung eines hämodynamisch wirksamen offenen Ductus arteriosus Botalli bei Frühgeborenen vor der 34. Schwangerschaftswoche. Bei der Mukoviszidose bessert eine Hochdosisbehandlung die Symptome bei Kindern mit leichter Mukoviszidose deutlich. Die potenziellen Nebenwirkungen verhindern jedoch einen breiten Einsatz. ⓘ
Schwangerschaft und Stillzeit
In den ersten zwei Dritteln der Schwangerschaft gehört Ibuprofen, wie Paracetamol, zu den Schmerzmitteln der Wahl. Ab der 28. Schwangerschaftswoche dürfen Ibuprofen und andere NSAR nicht mehr eingenommen werden, da es durch den vorzeitigen Verschluss des Ductus arteriosus Botalli zu Schädigungen des Fetus kommen kann. ⓘ
In der Stillzeit gehört Ibuprofen neben Paracetamol zu den bevorzugten Schmerzmitteln. ⓘ
Tiermedizin
In Deutschland und der Schweiz sind derzeit keine Tierarzneimittel auf Ibuprofenbasis zugelassen. Die Anwendung von Ibuprofen bei lebensmittelliefernden Tieren ist nicht erlaubt, da es in keinem Anhang zur Verordnung (EWG) Nr. 2377/90 über Höchstmengen für Tierarzneimittelrückstände in Nahrungsmitteln aufgeführt ist. Eine Anwendung bei Pferden kann nur erfolgen, wenn sie im Equidenpass eingetragen wird und eine Wartezeit von sechs Monaten bis zu einer Schlachtung eingehalten wird. Gegenüber den für Hunde zugelassenen NSAID treten bei Gabe von Ibuprofen vermehrt gastrointestinale Nebenwirkungen auf. ⓘ