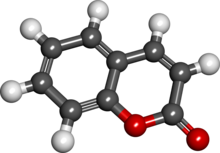
Cumarin

| |
| |

| |
| Bezeichnungen | |
|---|---|
| IUPAC-Bezeichnung
2H-Chromen-2-one
| |
| Bevorzugte IUPAC-Bezeichnung
2H-1-Benzopyran-2-one | |
| Andere Bezeichnungen
1-Benzopyran-2-on
| |
| Bezeichner | |
3D-Modell (JSmol)
|
|
Beilstein-Referenz
|
383644 |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Arzneimittelbank | |
| EC-Nummer |
|
Gmelin Referenz
|
165222 |
| KEGG | |
PubChem CID
|
|
| RTECS-Nummer |
|
| UNII | |
InChI
| |
SMILES
| |
| Eigenschaften | |
Chemische Formel
|
C9H6O2 |
| Molekulare Masse | 146,145 g-mol-1 |
| Erscheinungsbild | farblose bis weiße Kristalle |
| Geruch | angenehm, nach Vanilleschoten |
| Dichte | 0,935 g/cm3 (20 °C (68 °F)) |
| Schmelzpunkt | 71 °C (160 °F; 344 K) |
| Siedepunkt | 301,71 °C (575,08 °F; 574,86 K) |
Löslichkeit in Wasser
|
0,17 g / 100 mL |
| Löslichkeit | sehr löslich in Ether, Diethylether, Chloroform, Öl, Pyridin löslich in Ethanol |
| log P | 1.39 |
| Dampfdruck | 1,3 hPa (106 °C (223 °F)) |
Magnetische Suszeptibilität (χ)
|
-82,5×10-6 cm3/mol |
| Struktur | |
Kristallstruktur
|
orthorhombisch |
| Gefahren | |
| GHS-Kennzeichnung: | |
Piktogramme
|
 
|
Signalwort
|
Warnhinweis |
Gefahrenhinweise
|
H302, H317, H373 |
Sicherheitshinweise
|
P260, P261, P264, P270, P272, P280, P301+P312, P302+P352, P314, P321, P330, P333+P313, P363, P501 |
| NFPA 704 (Feuerdiamant) | |
| Flammpunkt | 150 °C (302 °F; 423 K) |
| Letale Dosis oder Konzentration (LD, LC): | |
LD50 (Mittlere Dosis)
|
293 mg/kg (Ratte, oral) |
| Sicherheitsdatenblatt (SDS) | Sigma-Aldrich |
| Verwandte Verbindungen | |
Verwandte Verbindungen
|
Chromon |
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |
Cumarin (/ˈkuːmərɪn/) oder 2H-Chromen-2-on ist eine aromatische organische chemische Verbindung mit der Formel C9H6O2. Sein Molekül lässt sich als Benzolmolekül beschreiben, bei dem zwei benachbarte Wasserstoffatome durch eine lactonartige Kette -(CH)=(CH)-(C=O)-O- ersetzt sind, wodurch ein zweiter sechsgliedriger Heterocyclus gebildet wird, der sich zwei Kohlenstoffe mit dem Benzolring teilt. Es kann in die chemische Klasse der Benzopyrone eingeordnet und als Lacton betrachtet werden. ⓘ
Cumarin ist ein farbloser kristalliner Feststoff mit einem süßen Geruch, der an Vanille erinnert, und einem bitteren Geschmack. Es kommt in vielen Pflanzen vor, wo es als chemischer Schutz gegen Fressfeinde dienen kann. Eine verwandte Verbindung hemmt die Synthese von Vitamin K und wird als verschreibungspflichtiges Medikament Warfarin - ein Antikoagulans - verwendet, um die Bildung von Blutgerinnseln, tiefen Venenthrombosen und Lungenembolien zu verhindern. ⓘ
Cumarin oder Kumarin ist ein natürlich vorkommender, aromatischer sekundärer Pflanzenstoff aus der Gruppe der Benzopyrone mit eigentümlichem, angenehm würzigem Geruch. Wird es in größeren Mengen eingenommen, ist es gesundheitsschädlich. Verbindungen, die das Strukturgerüst des Cumarins enthalten, werden auch unter der Sammelbezeichnung Cumarine geführt; die Derivate des 4-Hydroxycumarins besitzen als 4-Hydroxycumarine Bedeutung als blutgerinnungshemmende Arzneistoffe und Schädlingsbekämpfungsmittel. Der Name leitet sich vom ins Spanische übernommenen Tupí-Wort cumarú ‚Tonkabohnenbaum‘ ab. ⓘ
Etymologie
Cumarin leitet sich von coumarou, dem französischen Wort für die Tonkabohne, ab. Das Wort Tonka für die Tonkabohne stammt aus der Sprache der Galibi (Kariben), die von den Eingeborenen in Französisch-Guayana gesprochen wird (eine Quelle für die Pflanze); es erscheint auch im alten Tupi, einer anderen Sprache derselben Region, als Name des Baums. Der alte Gattungsname Coumarouna wurde aus einem anderen Tupi-Namen für Baum, kumarú, gebildet. ⓘ
Geschichte
Cumarin wurde erstmals 1820 von A. Vogel aus München aus der Tonkabohne isoliert, der es zunächst mit Benzoesäure verwechselte. ⓘ
Ebenfalls 1820 isolierte der Franzose Nicholas Jean Baptiste Gaston Guibourt (1790-1867) unabhängig voneinander Cumarin, erkannte aber, dass es sich nicht um Benzoesäure handelte. In einem Aufsatz, den er der pharmazeutischen Sektion der Académie Royale de Médecine vorlegte, nannte Guibourt die neue Substanz Cumarin. ⓘ
1835 wies der französische Pharmazeut A. Guillemette nach, dass Vogel und Guibourt dieselbe Substanz isoliert hatten. Cumarin wurde erstmals 1868 von dem englischen Chemiker William Henry Perkin synthetisiert. ⓘ
Cumarin ist seit seiner ersten Verwendung in Houbigants Fougère Royale im Jahr 1882 ein fester Bestandteil der Parfümgattung Fougère. ⓘ
Synthese
Ausgangsstoff für Cumarin in der Pflanze ist die Zimtsäure, aus der es durch Hydroxylierung, Glycosidierung und Cyclisierung gebildet wird. Der Stoff seinerseits ist Grundkörper zahlreicher Naturstoffe, unter anderem des Aesculins, der Furocumarine und des Umbelliferons. ⓘ
Synthetisch wird Cumarin nach Perkin (Perkinsche Synthese) aus Salicylaldehyd und Essigsäureanhydrid hergestellt:
Ein alternatives Herstellungsverfahren ist der Raschig-Prozess aus o-Kresol. ⓘ
Biosynthese
Aus der Lactonisierung von ortho-hydroxylierter cis-Hydroxyzimtsäure. ⓘ
Natürliches Vorkommen
Cumarin kommt in der Natur in vielen Pflanzen vor. Frisch gemahlene Pflanzenteile enthalten einen höheren Anteil an erwünschten und unerwünschten sekundären Pflanzenstoffen als Pulver. Außerdem sind ganze Pflanzenteile schwerer zu fälschen; so zeigte eine Studie, dass echte Ceylon-Zimtrinde 0,012 bis 0,143 mg/g Cumarin enthielt, während auf Märkten gekaufte Proben bis zu 3,462 mg/g enthielten, möglicherweise weil sie mit anderen Zimtsorten vermischt waren. ⓘ
- Vanillegras (Anthoxanthum odoratum)
- Süßer Waldmeister (Galium odoratum)
- Süßgras (Hierochloe odorata)
- Süßklee (Gattung Melilotus)
- Tonkabohne (Dipteryx odorata)
- Zimt; eine Studie aus dem Jahr 2013 ergab, dass die verschiedenen Sorten unterschiedliche Mengen an Cumarin enthalten:
- Ceylon-Zimt oder echter Zimt (Cinnamomum verum): 0,005 bis 0,090 mg/g
- Chinesischer Zimt oder chinesische Kassia (C. cassia): 0,085 bis 0,310 mg/g
- Indonesischer Zimt oder Padang-Kassie (C. burmannii): 2,14 bis 9,30 mg/g
- Saigon-Zimt oder vietnamesische Kassia (C. loureiroi): 1,06 bis 6,97 mg/g
- Deertzunge (Carphephorus odoratissimus),
- Tilo (Justicia pectoralis),
- Königskerze (Gattung Verbascum)
- Viele Kirschblütenbaumsorten (der Gattung Prunus).
- Ähnliche Verbindungen finden sich in einigen, aber nicht allen Exemplaren der Gattung Glycyrrhiza, von der sich die Wurzel und das Aroma Lakritz ableiten. ⓘ
Cumarin kommt natürlich auch in vielen essbaren Pflanzen wie Erdbeeren, schwarzen Johannisbeeren, Aprikosen und Kirschen vor. ⓘ
Santos-Buelga und Gonzalez-Paramas (2017) stellten fest, dass Cumarine seltene, aber gelegentliche Bestandteile von Propolis sind. ⓘ
Tonkabohne als Gewürz ⓘ
Cumarin und nah verwandte Stoffe sind die wesentlichen Komponenten des typischen Geruchs von Waldmeister und dem beim Trocknen von Gras entstehenden Heugeruch. In der Pflanze ist Cumarin häufig glycosidisch gebunden und wird erst bei Verletzung der Pflanze beziehungsweise beim Welken durch Abspaltung des Zuckers freigesetzt. Kommen das Glycosid und die zugehörige Glycosidase zusammen, zum Beispiel durch Zerstörung von Pflanzenzellen oder bei Verwesung, wird das Glycosid hydrolytisch abgespalten und das Aglykon, hier das Cumarin, frei und in diesem Fall zum Geruchsstoff. ⓘ
Biologische Funktion
Cumarin hat appetithemmende Eigenschaften, die Tiere davon abhalten können, Pflanzen zu fressen, die es enthalten. Obwohl die Verbindung einen angenehmen süßen Geruch hat, schmeckt sie bitter und wird daher von Tieren eher gemieden. ⓘ
Stoffwechsel
Die Biosynthese von Cumarin in Pflanzen erfolgt durch Hydroxylierung, Glykolyse und Zyklisierung von Zimtsäure. Beim Menschen hat das vom Gen UGT1A8 kodierte Enzym Glucuronidase-Aktivität mit vielen Substraten, einschließlich Cumarinen. ⓘ
Verwandte Verbindungen und Derivate
Cumarin und seine Derivate werden alle zu den Phenylpropanoiden gezählt. ⓘ
Zu den natürlich vorkommenden Cumarinderivaten gehören Umbelliferon (7-Hydroxycumarin), Aesculetin (6,7-Dihydroxycumarin), Herniarin (7-Methoxycumarin), Psoralen und Imperatorin. ⓘ
4-Phenylcumarin ist das Grundgerüst der Neoflavone, einer Art von Neoflavonoiden. ⓘ
Cumarin-Pyrazol-Hybride wurden aus Hydrazonen, Carbazonen und Thiocarbazonen über die Vilsmeier-Hack-Formylierungsreaktion synthetisiert. ⓘ
Von Cumarin abgeleitete Verbindungen werden auch als Cumarine oder Cumarinoide bezeichnet; zu dieser Familie gehören:
- Brodifacoum
- Bromadiolon
- Difenacoum
- Auraptene
- Enzaculin
- Phenprocoumon (Marcoumar)
- PSB-SB-487
- PSB-SB-1202
- Scopoletin kann aus der Rinde von Shorea pinanga isoliert werden
- Warfarin (Coumadin) ⓘ
Cumarin wird von einer Reihe von Pilzarten in das natürliche Antikoagulans Dicoumarol umgewandelt. Dies geschieht durch die Bildung von 4-Hydroxycumarin und dann weiter (in Gegenwart von natürlich vorkommendem Formaldehyd) in das eigentliche Antikoagulans Dicoumarol, ein Fermentationsprodukt und Mykotoxin. Dicoumarol war für die historisch als "Süßkleekrankheit" bekannte Bluterkrankheit bei Rindern verantwortlich, die verschimmelte Süßkleesilage gefressen hatten. In der Grundlagenforschung gibt es erste Hinweise darauf, dass Cumarin verschiedene biologische Aktivitäten hat, darunter entzündungshemmende, antitumorale, antibakterielle und antimykotische Eigenschaften. ⓘ
Verwendungen
Arzneimittel
Warfarin - ein Cumarin - mit dem Markennamen Coumadin ist ein verschreibungspflichtiges Medikament, das als Gerinnungshemmer eingesetzt wird, um die Bildung von Blutgerinnseln zu verhindern, und somit eine Therapie für tiefe Venenthrombosen und Lungenembolien darstellt. Es kann auch zur Vorbeugung von wiederkehrenden Blutgerinnseln bei Vorhofflimmern, thrombotischen Schlaganfällen und transitorischen ischämischen Attacken eingesetzt werden. ⓘ
Cumarine haben einige Hinweise auf biologische Aktivität erbracht und sind in begrenztem Umfang für einige wenige medizinische Anwendungen als Arzneimittel zugelassen, z. B. für die Behandlung von Lymphödemen. Sowohl Cumarin- als auch 1,3-Indandion-Derivate haben eine urikosurische Wirkung, vermutlich durch Beeinträchtigung der renalen tubulären Rückresorption von Urat. ⓘ
Vorläufer von Rodentiziden
Cumarin wird in der pharmazeutischen Industrie als Vorläuferreagenz bei der Synthese einer Reihe von synthetischen gerinnungshemmenden Arzneimitteln ähnlich dem Dicoumarol verwendet. 4-Hydroxycumarine sind eine Art von Vitamin-K-Antagonisten. Sie blockieren die Regeneration und das Recycling von Vitamin K. Diese Chemikalien werden manchmal auch fälschlicherweise als "Cumadine" und nicht als 4-Hydroxycumarine bezeichnet. Einige Chemikalien aus der Klasse der 4-Hydroxycumarine, die die Blutgerinnung hemmen, sind auf hohe Wirksamkeit und lange Verweildauer im Körper ausgelegt und werden speziell als Nagetiergifte ("Rattengift") eingesetzt. Der Tod tritt nach einem Zeitraum von mehreren Tagen bis zu zwei Wochen ein, in der Regel durch innere Blutungen. ⓘ
Laser-Farbstoffe
Cumarinfarbstoffe werden in großem Umfang als Verstärkungsmedien in blau-grün abstimmbaren organischen Farbstofflasern verwendet. Zu den verschiedenen Cumarin-Laserfarbstoffen gehören die Cumarine 480, 490, 504, 521, 504T und 521T. Cumarin-Tetramethyl-Laserfarbstoffe bieten eine breite Abstimmbarkeit und eine hohe Laserverstärkung und werden auch als aktives Medium in kohärenten OLED-Emittern und als Sensibilisator in älteren Fotovoltaik-Technologien verwendet. ⓘ
Parfüm und Aromastoffe
Cumarin ist häufig in künstlichen Vanilleersatzstoffen zu finden, obwohl es seit Mitte des 20. Jahrhunderts in zahlreichen Ländern als Lebensmittelzusatzstoff verboten ist. Jahrhunderts als Lebensmittelzusatzstoff verboten ist. Es wird immer noch als legaler Aromastoff in Seifen, Gummiprodukten und in der Tabakindustrie verwendet, insbesondere für süßen Pfeifentabak und bestimmte alkoholische Getränke. ⓘ
Toxizität
Cumarin ist mäßig toxisch für Leber und Nieren von Nagetieren, mit einer mittleren letalen Dosis (LD50) von 293 mg/kg bei der Ratte, einer geringen Toxizität im Vergleich zu verwandten Verbindungen. Cumarin ist bei Ratten hepatotoxisch, bei Mäusen jedoch weniger. Nagetiere verstoffwechseln es hauptsächlich zu 3,4-Cumarinepoxid, einer toxischen, instabilen Verbindung, die bei weiterem differenzierten Stoffwechsel Leberkrebs bei Ratten und Lungentumore bei Mäusen verursachen kann. Beim Menschen wird es hauptsächlich zu 7-Hydroxycumarin verstoffwechselt, einer Verbindung mit geringerer Toxizität, und es wurden keine schädlichen Auswirkungen beim Menschen direkt gemessen. Das deutsche Bundesinstitut für Risikobewertung hat eine tolerierbare tägliche Aufnahmemenge (TDI) von 0,1 mg Cumarin pro kg Körpergewicht festgelegt, weist aber auch darauf hin, dass eine höhere Aufnahme für kurze Zeit nicht gefährlich ist. Die Occupational Safety and Health Administration (OSHA) der Vereinigten Staaten stuft Cumarin nicht als krebserregend für den Menschen ein. ⓘ
Europäische Gesundheitsbehörden warnen vor dem Verzehr großer Mengen von Cassiarinde, einer der vier Hauptarten von Zimt, wegen ihres Cumaringehalts. Nach Angaben des deutschen Bundesinstituts für Risikobewertung (BFR) enthält 1 kg (Cassia-)Zimtpulver etwa 2,1 bis 4,4 g Cumarin. Cassia-Zimtpulver hat ein Gewicht von 0,56 g/cm3, so dass ein Kilogramm Cassia-Zimtpulver 362,29 Teelöffel entspricht. Ein Teelöffel Cassia-Zimtpulver enthält somit 5,8 bis 12,1 mg Cumarin, was bei kleineren Personen über dem tolerierbaren Tagesbedarf liegen kann. Der BFR warnt jedoch nur vor einer hohen täglichen Aufnahme von kumarinhaltigen Lebensmitteln. In seinem Bericht heißt es ausdrücklich, dass Ceylon-Zimt (Cinnamomum verum) "kaum" Cumarin enthält. ⓘ
In der europäischen Verordnung (EG) Nr. 1334/2008 sind folgende Höchstwerte für Cumarin festgelegt: 50 mg/kg in traditionellen und/oder saisonalen Backwaren, die einen Hinweis auf Zimt in der Etikettierung enthalten, 20 mg/kg in Frühstücksflocken einschließlich Müsli, 15 mg/kg in feinen Backwaren, mit Ausnahme von traditionellen und/oder saisonalen Backwaren, die einen Hinweis auf Zimt in der Etikettierung enthalten, und 5 mg/kg in Desserts. ⓘ
Eine Untersuchung der dänischen Veterinär- und Lebensmittelbehörde aus dem Jahr 2013 zeigt, dass Backwaren, die als Feine Backwaren bezeichnet werden, in fast 50 % der Fälle den europäischen Grenzwert (15 mg/kg) überschreiten. In dem Papier wird auch erwähnt, dass Tee ein weiterer wichtiger Faktor für die Gesamtaufnahme von Cumarin ist, insbesondere bei Kindern, die zu Süßigkeiten neigen. ⓘ
Cumarin wurde 1954 in den Vereinigten Staaten als Lebensmittelzusatzstoff verboten, vor allem wegen der Ergebnisse der Hepatotoxizität bei Nagetieren. Cumarin wird derzeit von der Food and Drug Administration (FDA) der Vereinigten Staaten unter "Substances Generally Prohibited From Direct Addition or Use as Human Food" (Stoffe, die generell für den direkten Zusatz oder die Verwendung in Lebensmitteln verboten sind) gemäß 21 CFR 189.130 aufgeführt, aber einige natürliche Zusatzstoffe, die Cumarin enthalten, wie z. B. der Aromastoff Waldmeister, sind gemäß 21 CFR 172.510 "nur in alkoholischen Getränken" erlaubt. In Europa beliebte Beispiele für solche Getränke sind Maiwein, Weißwein mit Waldmeister, und Żubrówka, mit Bisongras aromatisierter Wodka. ⓘ
Die Verwendung von Cumarin in der Parfümerie unterliegt Beschränkungen, da manche Menschen darauf sensibilisiert werden können; der Nachweis, dass Cumarin beim Menschen eine allergische Reaktion hervorrufen kann, wird jedoch bestritten. ⓘ
Bei Kindern, die während der Schwangerschaft den Gerinnungshemmern Acenocoumarol oder Phenprocoumon ausgesetzt waren, wurden leichte neurologische Funktionsstörungen festgestellt. Eine Gruppe von 306 Kindern wurde im Alter von 7 bis 15 Jahren getestet, um subtile neurologische Auswirkungen der Exposition gegenüber Antikoagulanzien zu ermitteln. Die Ergebnisse zeigten eine Dosis-Wirkungs-Beziehung zwischen der Exposition gegenüber Gerinnungshemmern und leichten neurologischen Störungen. Insgesamt wurde bei Kindern, die diesen Antikoagulanzien, die zusammenfassend als "Cumarine" bezeichnet werden, ausgesetzt waren, ein 1,9-facher (90 %) Anstieg leichter neurologischer Funktionsstörungen beobachtet. Abschließend erklärten die Forscher: "Die Ergebnisse deuten darauf hin, dass Cumarine einen Einfluss auf die Entwicklung des Gehirns haben, der zu leichten neurologischen Störungen bei Kindern im Schulalter führen kann." ⓘ
Das Vorhandensein von Cumarin in Zigarettentabak veranlasste den Geschäftsführer von Brown & Williamson, Dr. Jeffrey Wigand, 1995 dazu, sich an die CBS-Nachrichtensendung 60 Minutes zu wenden und zu behaupten, der Tabak enthalte eine "Form von Rattengift". Er behauptete, dass Cumarin aus chemischer Sicht ein "unmittelbarer Vorläufer" des Rodentizids Cumadin sei. Dr. Wigand erklärte später, dass Cumarin selbst gefährlich sei, und wies darauf hin, dass die FDA 1954 den Zusatz von Cumarin zu Lebensmitteln verboten habe. In seinen späteren Aussagen stufte er Cumarin wiederholt als "lungenspezifisches Karzinogen" ein. In Deutschland ist Cumarin als Zusatzstoff in Tabak verboten. ⓘ
Für alkoholische Getränke, die in der Europäischen Union verkauft werden, ist ein Höchstgehalt von 10 mg/l Cumarin gesetzlich festgelegt. Bei Zimtaroma handelt es sich im Allgemeinen um dampfdestillierte Kassiarinde, um den Zimtaldehyd auf etwa 93 % zu konzentrieren. Klare alkoholische Getränke mit Zimtgeschmack werden in der Regel negativ auf Cumarin getestet, aber wenn ganze Cassiarinde zur Herstellung von Glühwein verwendet wird, taucht Cumarin in erheblichen Mengen auf. ⓘ
Analytik
Die zuverlässige qualitative und quantitative Bestimmung von Cumarin gelingt nach angemessener Probenvorbereitung durch Kopplung der HPLC bzw. Gaschromatographie mit der Massenspektrometrie. ⓘ
Derivate
Die blutgerinnungshemmenden Cumarin-Derivate Phenprocoumon, Warfarin und Ethylbiscoumacetat werden in der Medizin bei entsprechend risikobehafteten Personen eingesetzt, um beispielsweise ischämische Schlaganfälle zu verhindern. Außerdem werden sie als Rodentizide vor allem zur Bekämpfung von Ratten eingesetzt, da sie in entsprechend hoher Dosierung zu tödlichen inneren Blutungen führen. In der Naturheilkunde werden Extrakte aus Eschenrinde verwendet, deren Wirkung möglicherweise dem Cumarinderivat Fraxin zugeschrieben werden kann. ⓘ
Stark fluoreszierende Cumarin-Derivate finden darüber hinaus Anwendung als effektive Farbstoffe in Farbstofflasern und optischen Aufhellern. Als Farbstofflaser emittieren sie im blauen bis in den grünen Spektralbereich des Lichtspektrums. ⓘ

Das Isocumarin ist ein Stellungisomer des Cumarins, bei dem die Carbonylgruppe und das Sauerstoffatom vertauscht sind. Einige Dihydro-Isocumarin-Derivate, wie z. B. das Phyllodulcin, das in den Blättern der Gartenhortensie vorkommt, haben einen süßen Geschmack. Die Süßkraft von Phyllodulcin im Vergleich zu Saccharose beträgt 250. ⓘ
Als Ersatzstoff in der Industrie werden Dihydrocumarin und 6-Methylcumarin verwendet. ⓘ
Insektenschutz
Cumarin, etwa in Form von Duftendem Mariengras, wirkt moskitoabweisend. Bei Steinklee, einigen Gräsern und Waldmeister gelten aus der Vakuole freigesetzte Cumarine als Fraßschutz. ⓘ






