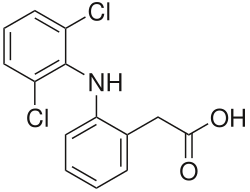
Diclofenac
 | |
 | |
| Klinische Daten | |
|---|---|
| Handelsnamen | Cataflam, Voltaren, Zipsor, andere |
| AHFS/Drugs.com | Monographie |
| MedlinePlus | a689002 |
| Lizenz-Daten |
|
| Schwangerschaft Kategorie |
|
| Wege der Verabreichung | Durch den Mund, rektal, intramuskulär, intravenös, äußerlich |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Proteinbindung | Mehr als 99% |
| Verstoffwechselung | Leber, oxidativ, hauptsächlich durch CYP2C9, auch durch CYP2C8, CYP3A4, sowie konjugativ durch Glucuronidierung (UGT2B7) und Sulfatierung; es gibt keine aktiven Metaboliten |
| Beginn der Wirkung | Innerhalb von 4 Stunden (Gel), 30 Minuten (Nicht-Gel) |
| Eliminationshalbwertszeit | 1,2-2 Stunden (35% des Wirkstoffs gelangen in den enterohepatischen Kreislauf) |
| Ausscheidung | 40% über die Gallenwege 60% über den Urin |
| Bezeichner | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| PDB-Ligand |
|
| Chemische und physikalische Daten | |
| Formel | C14H11Cl2NO2 |
| Molare Masse | 296,15 g-mol-1 |
| 3D-Modell (JSmol) | |
SMILES
| |
InChI
| |
| | |
Diclofenac, das unter anderem unter dem Markennamen Voltaren verkauft wird, ist ein nichtsteroidales entzündungshemmendes Arzneimittel (NSAID), das zur Behandlung von Schmerzen und entzündlichen Erkrankungen wie Gicht eingesetzt wird. Es wird oral oder rektal als Zäpfchen eingenommen, als Injektion verabreicht oder auf die Haut aufgetragen. Die Besserung der Schmerzen hält bis zu acht Stunden an. Es ist auch in Kombination mit Misoprostol erhältlich, um Magenprobleme zu verringern. Es ist dafür bekannt, dass es zur Verringerung der Geierpopulationen beiträgt. ⓘ
Häufige Nebenwirkungen sind Bauchschmerzen, Magen-Darm-Blutungen, Übelkeit, Schwindel, Kopfschmerzen und Schwellungen. Zu den schwerwiegenden Nebenwirkungen können Herzerkrankungen, Schlaganfälle, Nierenprobleme und Magengeschwüre gehören. Die Einnahme wird im dritten Trimester der Schwangerschaft nicht empfohlen. Während der Stillzeit ist es wahrscheinlich sicher. Es wird angenommen, dass es durch die Verringerung der Produktion von Prostaglandin wirkt. Es blockiert sowohl COX-1 (wie Aspirin) als auch COX-2 (wie Celecoxib), ist also ein COX-2-Inhibitor. ⓘ
Diclofenac wurde 1965 von Ciba-Geigy patentiert und kam 1988 in den Vereinigten Staaten zur medizinischen Anwendung. Es ist als Generikum erhältlich. Im Jahr 2019 war es das 74. am häufigsten verschriebene Medikament in den Vereinigten Staaten, mit mehr als 10 Millionen Verschreibungen. Es ist als Natrium- oder Kaliumsalz erhältlich. ⓘ
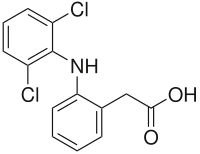
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Diclofenac | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel |
| ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Wirkstoffklasse |
Nichtsteroidales Antirheumatikum | ||||||||||||||||||
| Wirkmechanismus |
Cyclooxygenase-Inhibitor | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | |||||||||||||||||||
| Schmelzpunkt |
ca. 280 °C (Diclofenac-Natriumsalz/Zersetzung) | ||||||||||||||||||
| pKS-Wert |
4,15 | ||||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (2,37 mg·l−1 bei 25 °C) | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
62,5 mg·kg−1 (LD50, Ratte, oral) | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Diclofenac (Name abgeleitet von der englischen chemischen Bezeichnung 2-[2-(2,6-Dichlorophenylamino)phenyl]acetic acid) ist ein Arzneistoff aus der Gruppe der Nichtopioid-Analgetika, der bei leichten bis mittleren Schmerzen und Entzündungen eingesetzt wird, beispielsweise bei Rheuma, Prellungen, Zerrungen, Hexenschuss, Arthrose, Arthritis und Schweißdrüsenabszessen. Seine Wirkung beruht auf einer nichtselektiven Hemmung der Cyclooxygenasen (COX), die im Körper die Entzündungsmediatoren, die Prostaglandine, bilden. Chemisch gehört es zu den Phenylessigsäuren. In Arzneimitteln wird Diclofenac in Form verschiedener Salze verwendet, z. B. als Natriumsalz oder Diethylammoniumsalz. ⓘ
Medizinische Anwendungen
Diclofenac wird zur Behandlung von Schmerzen, entzündlichen Erkrankungen und Dysmenorrhö eingesetzt. ⓘ
Schmerzen
Zu den entzündlichen Erkrankungen gehören Beschwerden des Bewegungsapparates, insbesondere Arthritis, rheumatoide Arthritis, Polymyositis, Dermatomyositis, Osteoarthritis, Zahnschmerzen, Kiefergelenkschmerzen, Spondylarthritis, Morbus Bechterew, Gichtanfälle und Schmerzbehandlung bei Nieren- und Gallensteinen. Eine weitere Indikation ist die Behandlung von akuter Migräne. Diclofenac wird häufig zur Behandlung leichter bis mäßiger postoperativer oder posttraumatischer Schmerzen eingesetzt, insbesondere wenn gleichzeitig eine Entzündung vorliegt, und ist wirksam bei Menstruationsschmerzen und Endometriose. ⓘ
Diclofenac ist auch in topischen Darreichungsformen erhältlich und hat sich als nützlich bei Osteoarthritis erwiesen, nicht jedoch bei anderen Arten von langfristigen Schmerzen des Bewegungsapparats. ⓘ
Es kann auch bei aktinischer Keratose und akuten Schmerzen aufgrund kleinerer Zerrungen, Verstauchungen und Prellungen helfen. ⓘ
In vielen Ländern werden Augentropfen zur Behandlung akuter und chronischer nichtbakterieller Entzündungen des vorderen Augenabschnitts (z. B. nach Operationen) verkauft. Diclofenac-Augentropfen wurden auch zur Schmerzlinderung bei traumatischen Hornhautabschürfungen eingesetzt. ⓘ
Diclofenac wird häufig zur Behandlung chronischer Schmerzen im Zusammenhang mit Krebs eingesetzt, insbesondere wenn eine Entzündung vorliegt. Die Verwendung von Diclofenac-Gel sollte 32 Gramm pro Tag nicht überschreiten. ⓘ
Arthrotec (Diclofenac und Misoprostol) 50 mg Tabletten
Sintofarm (Diclofenac) zur Verabreichung als Zäpfchen ⓘ
Kontraindikationen
- Überempfindlichkeit gegen Diclofenac
- Allergische Reaktionen in der Vorgeschichte (Bronchospasmus, Schock, Rhinitis, Urtikaria) nach Anwendung anderer NSAIDs wie Aspirin
- Schwangerschaft im dritten Trimester
- Aktive Magen- und/oder Zwölffingerdarmgeschwüre oder gastrointestinale Blutungen
- Entzündliche Darmerkrankungen wie Morbus Crohn oder Colitis ulcerosa
- Schwere kongestive Herzinsuffizienz (NYHA III/IV)
- Schmerzbehandlung im Rahmen einer koronaren Bypass-Operation (CABG)
- Schwere Leberinsuffizienz (Child-Pugh-Klasse C)
- Schwere chronische Nierenerkrankung (Kreatinin-Clearance <30 ml/min)
- Vorsicht bei Patienten mit vorbestehender hepatischer Porphyrie, da Diclofenac Anfälle auslösen kann
- Vorsicht bei Patienten mit schweren, aktiven Blutungen wie z. B. Hirnblutungen
- NSAIDs sollten bei Dengue-Fieber generell vermieden werden, da sie ein (oft schweres) Kapillarleck und ein anschließendes Herzversagen hervorrufen.
- Vorsicht bei Patienten mit Flüssigkeitsretention oder Herzinsuffizienz
- Kann zum Auftreten eines neuen Bluthochdrucks oder zur Verschlimmerung eines bereits bestehenden Bluthochdrucks führen
- Kann schwerwiegende Hautnebenwirkungen wie exfoliative Dermatitis, Stevens-Johnson-Syndrom (SJS) und toxische epidermale Nekrolyse (TEN) verursachen, die tödlich sein können ⓘ
Unerwünschte Wirkungen
Die Einnahme von Diclofenac wurde in einer Studie mit Coxib, Diclofenac, Ibuprofen und Naproxen mit einem signifikant erhöhten Gefäß- und Koronarrisiko in Verbindung gebracht. Es wurde auch über Komplikationen im oberen Magen-Darm-Bereich berichtet. Die Zahl der schwerwiegenden unerwünschten kardiovaskulären Ereignisse (MACE) wurde durch Diclofenac um etwa ein Drittel erhöht, was vor allem auf eine Zunahme schwerer koronarer Ereignisse zurückzuführen war. Im Vergleich zu Placebo traten bei 1000 Patienten, die ein Jahr lang Diclofenac erhielten, drei schwerwiegende vaskuläre Ereignisse mehr auf, von denen eines tödlich verlief. Die Zahl der vaskulären Todesfälle wurde durch Diclofenac signifikant erhöht. ⓘ
Im Oktober 2020 verlangte die US-Arzneimittelbehörde (FDA) eine Aktualisierung der Arzneimittelbeschreibung für alle nichtsteroidalen entzündungshemmenden Medikamente, um das Risiko von Nierenproblemen bei Ungeborenen zu beschreiben, die zu niedrigem Fruchtwasser führen. Sie empfehlen, NSAIDs bei Schwangeren ab der 20. Schwangerschaftswoche zu meiden. ⓘ
Herz
Im Jahr 2013 wurde in einer Studie festgestellt, dass Diclofenac die Zahl der schwerwiegenden vaskulären Ereignisse um etwa ein Drittel erhöht, was vor allem auf einen Anstieg der schwerwiegenden koronaren Ereignisse zurückzuführen ist. Im Vergleich zu Placebo traten bei 1000 Personen, die ein Jahr lang Diclofenac erhielten, drei schwerwiegende vaskuläre Ereignisse mehr auf, von denen eines tödlich verlief. Die Zahl der vaskulären Todesfälle wurde durch Diclofenac erhöht (1-65). ⓘ
Nachdem 2004 ein erhöhtes Risiko für Herzinfarkte unter dem selektiven COX-2-Hemmer Rofecoxib festgestellt worden war, konzentrierte sich die Aufmerksamkeit auf alle anderen Mitglieder der Gruppe der NSAIDs, einschließlich Diclofenac. Die Forschungsergebnisse sind uneinheitlich, wobei eine Metaanalyse von Arbeiten und Berichten bis April 2006 auf eine relativ erhöhte Rate von Herzerkrankungen von 1,63 im Vergleich zu Nichtanwendern hinweist. Professor Peter Weissberg, medizinischer Direktor der British Heart Foundation, sagte: "Das erhöhte Risiko ist jedoch gering, und viele Patienten mit chronischen, lähmenden Schmerzen sind vielleicht der Meinung, dass dieses geringe Risiko es wert ist, ihre Symptome zu lindern". Nur bei Aspirin wurde kein erhöhtes Risiko für Herzkrankheiten festgestellt; allerdings ist bekannt, dass dieses Medikament eine höhere Rate an Magengeschwüren aufweist als Diclofenac. In Großbritannien erklärte die Medicines and Healthcare products Regulatory Agency (MHRA) im Juni 2013, dass das Medikament nicht von Menschen mit schweren Herzerkrankungen eingenommen werden sollte - Menschen mit Herzinsuffizienz, Herzerkrankungen oder einem Schlaganfall wurde geraten, es ganz abzusetzen. Am 15. Januar 2015 gab die MHRA bekannt, dass Diclofenac aufgrund des Risikos kardiovaskulärer Nebenwirkungen als verschreibungspflichtiges Arzneimittel neu eingestuft wird. ⓘ
Eine daraufhin durchgeführte große Studie mit 74 838 dänischen Anwendern von NSAIDs oder Coxibs ergab kein zusätzliches kardiovaskuläres Risiko durch die Einnahme von Diclofenac. Eine sehr große Studie mit 1 028 437 dänischen Anwendern verschiedener NSAR oder Coxibs ergab, dass die Verwendung des nichtselektiven NSAR Diclofenac und des selektiven Cyclooxygenase-2-Hemmers Rofecoxib mit einem erhöhten Risiko für kardiovaskuläre Todesfälle verbunden war (Odds Ratio, 1,91; 95 % Konfidenzintervall, 1,62 bis 2,42; bzw. Odds Ratio, 1,66; 95 % Konfidenzintervall, 1,06 bis 2,59), wobei das Risiko dosisabhängig war. ⓘ
Diclofenac hat eine ähnliche COX-2-Selektivität wie Celecoxib. ⓘ
Gastrointestinale Beschwerden
- Gastrointestinale Beschwerden werden am häufigsten festgestellt. Das Auftreten von Geschwüren und/oder Blutungen erfordert einen sofortigen Abbruch der Behandlung mit Diclofenac. Die meisten Patienten erhalten zur Prophylaxe während der Langzeitbehandlung ein Magenschutzmittel (Misoprostol, Ranitidin 150 mg vor dem Schlafengehen oder Omeprazol 20 mg vor dem Schlafengehen). ⓘ
Leber
- Leberschäden treten nur selten auf und sind in der Regel reversibel. Eine Hepatitis kann selten ohne Warnsymptome auftreten und kann tödlich sein. Patienten mit Osteoarthritis entwickeln häufiger eine symptomatische Lebererkrankung als Patienten mit rheumatoider Arthritis. Die Leberfunktion sollte während einer Langzeitbehandlung regelmäßig überwacht werden. Bei kurzfristiger Behandlung von Schmerzen oder Fieber hat sich Diclofenac nicht als hepatotoxischer erwiesen als andere NSAIDs.
- Im Dezember 2009 haben Endo, Novartis und die US-amerikanische Arzneimittelbehörde FDA die Angehörigen der Gesundheitsberufe darüber informiert, dass bei der Behandlung mit allen Produkten, die Diclofenac-Natrium enthalten, neue Warnhinweise und Vorsichtsmaßnahmen in Bezug auf mögliche Erhöhungen der Leberfunktionstests hinzugefügt wurden.
- Fälle von arzneimittelbedingter Hepatotoxizität wurden im ersten Monat berichtet, können aber zu jedem Zeitpunkt der Behandlung mit Diclofenac auftreten. Im Rahmen der Postmarketing-Überwachung wurden Fälle von schweren Leberreaktionen, einschließlich Lebernekrose, Gelbsucht, fulminanter Hepatitis mit und ohne Gelbsucht und Leberversagen, gemeldet. Einige dieser gemeldeten Fälle endeten tödlich oder führten zu Lebertransplantationen.
- Ärzte sollten bei Patienten, die eine Langzeittherapie mit Diclofenac erhalten, regelmäßig die Transaminasen messen. Auf der Grundlage von Daten aus klinischen Studien und Erfahrungen nach der Markteinführung sollten die Transaminasen innerhalb von 4 bis 8 Wochen nach Beginn der Behandlung mit Diclofenac überwacht werden. ⓘ
Niere
- NSAIDs "sind mit unerwünschten Wirkungen auf die Nieren verbunden, die durch die Verringerung der Synthese von Prostaglandinen in den Nieren verursacht werden", und zwar bei empfindlichen Personen oder Tierspezies und möglicherweise bei langfristiger Anwendung bei nicht empfindlichen Personen, wenn die Resistenz gegen Nebenwirkungen mit dem Alter abnimmt. Diese Nebenwirkung kann jedoch nicht allein durch die Verwendung eines selektiven COX-2-Hemmers vermieden werden, da "beide Isoformen der COX, COX-1 und COX-2, in der Niere exprimiert werden... Folglich sollten bei der Verabreichung selektiver COX-2-Hemmer dieselben Vorsichtsmaßnahmen hinsichtlich des Nierenrisikos getroffen werden wie bei nicht-selektiven NSAIDs." Diclofenac scheint jedoch einen anderen Mechanismus der Nierentoxizität zu haben.
- Studien in Spanien haben gezeigt, dass Diclofenac bei Geiern akutes Nierenversagen hervorruft, wenn sie die Kadaver von Tieren fressen, die kurz zuvor damit behandelt worden waren. Bei arzneimittelempfindlichen Spezies und einzelnen Menschen wird zunächst angenommen, dass ihnen Gene fehlen, die spezifische Entgiftungsenzyme für Arzneimittel exprimieren. ⓘ
Psychische Gesundheit
- Es wurde über Nebenwirkungen auf die psychische Gesundheit berichtet. Diese Symptome sind zwar selten, treten aber in ausreichender Zahl auf, um als mögliche Nebenwirkungen berücksichtigt zu werden. Dazu gehören Depressionen, Angstzustände, Reizbarkeit, Albträume und psychotische Reaktionen. ⓘ
Mechanismus der Wirkung
Wie bei den meisten NSAR wird angenommen, dass der primäre Mechanismus, der für die entzündungshemmende, fiebersenkende und schmerzlindernde Wirkung verantwortlich ist, in der Hemmung der Prostaglandinsynthese durch COX-Hemmung besteht. Diclofenac hemmt COX-1 und COX-2 mit relativer Äquipotenz. ⓘ
Das Hauptziel der Hemmung der Prostaglandinsynthese scheint die vorübergehend exprimierte Prostaglandin-Endoperoxid-Synthase-2 (PGES-2) zu sein, die auch als Cycloxygenase-2 (COX-2) bekannt ist. ⓘ
Es scheint auch eine bakteriostatische Wirkung durch Hemmung der bakteriellen DNA-Synthese zu haben. ⓘ
Diclofenac hat eine relativ hohe Lipidlöslichkeit, was es zu einem der wenigen NSAIDs macht, die durch die Blut-Hirn-Schranke ins Gehirn gelangen können. Es wird angenommen, dass es seine Wirkung auch im Gehirn durch Hemmung von COX-2 entfaltet. Darüber hinaus kann es auch im Rückenmark wirken. ⓘ
Diclofenac ist möglicherweise auch in anderer Hinsicht ein einzigartiges Mitglied der NSAIDs. Einiges deutet darauf hin, dass es die Lipoxygenasewege hemmt und dadurch die Bildung von Leukotrienen (ebenfalls entzündungsfördernde Autoazoide) reduziert. Möglicherweise hemmt es auch die Phospholipase A2 als Teil seines Wirkmechanismus. Diese zusätzlichen Wirkungen können seine hohe Wirksamkeit erklären - es ist das stärkste NSAID auf breiter Basis. ⓘ
Es gibt deutliche Unterschiede zwischen den NSAIDs hinsichtlich ihrer selektiven Hemmung der beiden Subtypen der Cyclooxygenase, COX-1 und COX-2. Bei der Entwicklung von Arzneimitteln wurde häufig versucht, sich auf die selektive COX-2-Hemmung zu konzentrieren, um die gastrointestinalen Nebenwirkungen von NSAIDs wie Aspirin zu minimieren. In der Praxis hat die Verwendung einiger COX-2-Hemmer mit ihren unerwünschten Wirkungen zu einer großen Zahl von Klagen von Patientenfamilien wegen unrechtmäßigem Tod durch Herzinfarkt geführt, während andere deutlich COX-selektive NSAIDs, wie z. B. Diclofenac, von den meisten Bevölkerungsgruppen gut vertragen werden. ⓘ
Neben der COX-Hemmung wurden kürzlich eine Reihe weiterer molekularer Angriffspunkte von Diclofenac identifiziert, die möglicherweise zu seiner schmerzlindernden Wirkung beitragen. Dazu gehören:
- Blockierung spannungsabhängiger Natriumkanäle (nach der Aktivierung des Kanals hemmt Diclofenac seine Reaktivierung, auch bekannt als Phasenhemmung)
- Blockierung von säureempfindlichen Ionenkanälen (ASICs)
- Positive allosterische Modulation von KCNQ- und BK-Kaliumkanälen (Diclofenac öffnet diese Kanäle, was zu einer Hyperpolarisierung der Zellmembran führt) ⓘ
Die Wirkung einer Einzeldosis ist viel länger (6 bis 8 Stunden) als die sehr kurze Halbwertszeit des Medikaments von 1,2 bis 2 Stunden vermuten ließe. Dies könnte zum Teil darauf zurückzuführen sein, dass das Medikament über 11 Stunden in den Synovialflüssigkeiten verbleibt. ⓘ
Gesellschaft und Kultur
Geschichte
In den Vereinigten Staaten wurde 1%iges Diclofenac-Gel 2007 von der FDA zugelassen. Es wurde als verschreibungspflichtiges Arzneimittel zugelassen und zur Schmerzlinderung bei Osteoarthritis in Gelenken, die auf eine topische Behandlung ansprechen, eingesetzt; insbesondere wurde es für die Gelenke in Händen, Knien und Füßen verschrieben. Es hat sich nicht als wirksam bei Zerrungen, Verstauchungen, Prellungen oder Sportverletzungen erwiesen. Es war für die vorübergehende Linderung von Gelenkschmerzen bei der häufigsten Art von Arthritis, der Osteoarthritis, vorgesehen. Im Februar 2020 wurde das Gel zu einem rezeptfreien Arzneimittel, und die FDA erteilte der GlaxoSmithKline plc die Zulassung für das rezeptfreie Produkt. ⓘ
Formulierungen und Handelsnamen
Der Name "Diclofenac" leitet sich von seinem chemischen Namen ab: 2-(2,6-Dichloranilino) Phenylessigsäure. Diclofenac wurde erstmals von Alfred Sallmann und Rudolf Pfister synthetisiert und 1973 von Ciba-Geigy (heute Novartis) als Voltaren auf den Markt gebracht. 2015 wurde es dann von GlaxoSmithKline übernommen. ⓘ
Voltaren und Voltarol enthalten das Natriumsalz von Diclofenac. Im Vereinigten Königreich kann Voltarol entweder mit dem Natrium- oder dem Kaliumsalz geliefert werden, während Cataflam, das in einigen anderen Ländern verkauft wird, nur das Kaliumsalz enthält. Voltarol Emulgel enthält jedoch Diclofenac-Diethylammonium, bei dem eine Konzentration von 1,16 % einer Konzentration von 1 % des Natriumsalzes entspricht. Im Jahr 2016 war Voltarol mit einem Umsatz von 39,3 Millionen Pfund eines der umsatzstärksten rezeptfreien Markenarzneimittel, die in Großbritannien verkauft wurden. ⓘ
Am 14. Januar 2015 wurden die oralen Diclofenac-Präparate im Vereinigten Königreich als verschreibungspflichtige Arzneimittel neu eingestuft. Die topischen Präparate sind weiterhin rezeptfrei erhältlich. ⓘ
Diclofenac-Formulierungen sind weltweit unter vielen verschiedenen Handelsnamen erhältlich. ⓘ
Ökologische Auswirkungen
Die Verwendung von Diclofenac bei Tieren ist umstritten, da es giftig ist, wenn es von Aasfressern, die tote Tiere fressen, gefressen wird; das Medikament wurde in mehreren Ländern für die tierärztliche Verwendung verboten. ⓘ
Die Verwendung von Diclofenac bei Tieren hat Berichten zufolge zu einem starken Rückgang der Geierpopulation auf dem indischen Subkontinent geführt - um 95 % im Jahr 2003 und um 99,9 % im Jahr 2008. Als Ursache wird ein Nierenversagen vermutet; die Toxizität kann jedoch auch auf eine direkte Hemmung der Harnsäuresekretion bei Geiern zurückzuführen sein. Geier fressen die Kadaver von Tieren, denen tierärztliches Diclofenac verabreicht wurde, und werden durch die angesammelte Chemikalie vergiftet, da Geier nicht über ein spezielles Enzym zum Abbau von Diclofenac verfügen. Auf einer Sitzung des National Wildlife Board im März 2005 kündigte die indische Regierung an, dass sie die Verwendung von Diclofenac in der Tiermedizin schrittweise einstellen wolle. Meloxicam ist eine sicherere Alternative, um die Verwendung von Diclofenac zu ersetzen. Es ist teurer als Diclofenac, aber die Kosten sinken, da immer mehr Pharmaunternehmen mit der Herstellung beginnen. ⓘ
Steppenadler sind genauso anfällig für Diclofenac wie Geier und können ihm ebenfalls zum Opfer fallen. Diclofenac ist nachweislich auch für Süßwasserfische wie die Regenbogenforelle schädlich. Im Gegensatz dazu können Neuweltgeier wie der Truthahngeier mindestens die 100-fache Diclofenac-Menge vertragen, die für Gyps-Arten tödlich ist. ⓘ
"Der Verlust von mehreren zehn Millionen Geiern in den letzten zehn Jahren hatte auf dem gesamten indischen Subkontinent erhebliche ökologische Folgen, die eine potenzielle Gefahr für die menschliche Gesundheit darstellen. Vielerorts haben die Populationen verwilderter Hunde (Canis familiaris) stark zugenommen, da die Gyps-Geier als wichtigste Aasfresser von Wild- und Haushuftierkadavern verschwunden sind. Mit dem Anstieg der Hundezahlen geht ein erhöhtes Tollwutrisiko einher, dem fast 50.000 Menschen zum Opfer gefallen sind. Die indische Regierung führt dies als eine der Hauptfolgen des Aussterbens der Geier an. Die Übertragung von Krankheitserregern aus Kadavern von Geiern auf verwilderte Hunde und Ratten könnte zu einer Pandemie führen, die in einem überfüllten Land wie Indien Millionen von Todesopfern fordern würde, während das Verdauungssystem der Geier viele Arten solcher Erreger sicher vernichtet. Geier sind langlebig und brüten nur langsam. Sie beginnen erst im Alter von sechs Jahren zu brüten, und nur 50 % der Jungen überleben. Selbst wenn das staatliche Verbot vollständig umgesetzt wird, wird es mehrere Jahre dauern, bis sich die Geierpopulation wieder erholt. ⓘ
Der Verlust der Geier hat soziale Auswirkungen auf die indische zoroastrische Parsi-Gemeinschaft, die traditionell Geier für die Beseitigung menschlicher Leichen in den Türmen des Schweigens einsetzt, nun aber gezwungen ist, alternative Entsorgungsmethoden zu suchen. ⓘ
Trotz der Geierkrise ist Diclofenac in anderen Ländern, auch in vielen europäischen Ländern, weiterhin erhältlich. Es wurde 2013 in Spanien für die tierärztliche Verwendung zugelassen und ist weiterhin erhältlich, obwohl in Spanien rund 90 % der europäischen Geierpopulation leben und eine unabhängige Simulation gezeigt hat, dass das Medikament die Geierpopulation jährlich um 1-8 % reduzieren könnte. Die spanische Arzneimittelbehörde legte Simulationen vor, aus denen hervorging, dass die Zahl der Todesfälle recht gering sein würde. In einer im Jahr 2021 veröffentlichten Arbeit wurde der erste nachweisliche Tod eines Geiers durch Diclofenac in Spanien festgestellt, ein Mönchsgeier. ⓘ
70 Prozent des vom Menschen eingenommenen Diclofenacs werden vom Körper über den Urin unverändert wieder ausgeschieden. Da in Deutschland pro Jahr etwa 90 Tonnen des Wirkstoffes verbraucht werden, gelangen auf diesem Weg etwa 63 Tonnen Diclofenac über die Kläranlagen, wo Diclofenac nur zum Teil abgebaut wird, in die Oberflächengewässer und damit in den Wasserkreislauf. So wurden im Rahmen einer Studie von 2008 in europäischen Flüssen Diclofenac-Konzentrationen im ein- bis dreistelligen Nanogramm-pro-Liter-Bereich gemessen. ⓘ
2019 konnte Diclofenac in Österreich in sämtlichen 40 untersuchten Fließgewässern nachgewiesen werden (0,00042–1,1 μg/l). In Toxizitätsstudien wurden für bestimmte Fischarten schädigende Wirkung auf Leber und Nieren nachgewiesen. Bei Forellen z. B. führt bereits ein halbes Mikrogramm Diclofenac pro Liter Wasser zu Nierenschäden. ⓘ
Aufgrund dieser erhöhten Umweltrelevanz gehört Diclofenac zu den sogenannten „Chemicals of Emerging Concern“ (CECs), also Stoffen, die Mensch und Umwelt potenziell erheblich beeinträchtigen können, und wurde in die „Watch List“ prioritär zu überwachender Stoffe der EU aufgenommen. Die Predicted No Effect Concentration (PNEC) für Diclofenac liegt bei 0,05 µg/l. In Deutschland wurde 2016 die Diclofenac-Konzentration an 24 Messstellen in Oberflächengewässern analysiert. Dabei wurde die PNEC an 21 der 24 Messstellen überschritten (Jahresmittelwert). ⓘ
Aufgrund der umweltschädigenden Eigenschaften und des geringen Nutzens von auf der Haut aufzutragenden Diclofenac-Präparaten (Cremes, Gele) riet die schwedische Arzneimittelkommission 2019 von deren Verwendung ab. Nur wenig des Wirkstoffes werde überhaupt resorbiert, sondern der Großteil abgewaschen. ⓘ
Synthese
Alfred Sallmann und Rudolph Pfister synthetisierten in den 1960er-Jahren in der Schweizer J. R. Geigy AG verschiedene substituierte 2-(Phenylamino)phenylessigsäuren, darunter 2-{2-[(2,6-Dichlorphenyl)amino]phenyl}essigsäure. Die Verbindungen wurden als Wirkstoffe gegen Rheumatismus und Arthritis durch Patente geschützt. Anstatt der Decarboxylierung der N-(2,6-Dichlorphenyl)anthranilsäure wird auch eine Reduktion mit Lithiumalanat und Kettenverlängerung mittels Cyanid beschrieben. Die Synthese von Diclofenac wird heute nach einem wesentlich einfacheren Verfahren über 2,6-Dichlordiphenylamin (CAS-Nr. 15307-93-4) aus 2,6-Dichlorphenol über eine Smiles-Umlagerung mit anschließender Stollé-Reaktion mit Chloracetylchlorid durchgeführt (siehe Reaktionsschema). Neun Jahre später wurde dieses komplette Verfahren über einen Phenoxyessigester von einem indischen Unternehmen nochmals angemeldet. Teile des Verfahrenspatentes, die Smiles-Umlagerung, wurden von chinesischen Autoren vier Jahre nach der Erstanmeldung beansprucht. ⓘ

Anwendung
Wechselwirkungen
Die Anwendung anderer nichtsteroidaler Antirheumatika – wie Acetylsalicylsäure oder Ibuprofen – oder die Einnahme zusammen mit Glucocorticoiden erhöht das Risiko von Nebenwirkungen im Magen-Darm-Trakt. Wechselwirkungen gibt es auch mit Lithium, Phenytoin und Herzglykosiden, deren Serumspiegel durch Diclofenac erhöht werden. Da es sich bei diesen um Substanzen mit einer geringen therapeutischen Breite handelt, kann es zu Überdosierungen kommen. Diclofenac kann die Wirkung von entwässernden und blutdrucksenkenden Arzneimitteln abschwächen. ⓘ
Bisher konnten in klinischen Untersuchungen keine Wechselwirkungen zwischen blutgerinnungshemmenden Substanzen wie zum Beispiel Phenprocoumon und Diclofenac gefunden werden, dennoch wird empfohlen, bei gleichzeitiger Anwendung den Gerinnungsstatus engmaschig zu kontrollieren. ⓘ
Verwendung in der Tiermedizin
Die Anwendung bei Hunden und Katzen kann massive Magen-Darm-Schädigungen mit teilweise tödlichem Ausgang hervorrufen. Die durch Verabreichung dieses Medikamentes hervorgerufene Schädigung ist einer der häufigsten iatrogenen Notfälle bei Hunden. ⓘ
Die EU-Rückstandshöchstmengen-Verordnung für Lebensmittel tierischen Ursprungs erlaubt die Anwendung von Diclofenac bei Rindern und Schweinen, wobei für die gewonnenen Lebensmittel Rückstandshöchstmengen festgesetzt sind. ⓘ
Analytik
Für die zuverlässige qualitative und quantitative Bestimmung des Diclofenac in den unterschiedlichsten Untersuchungsmaterialien wie z. B. Wasser- und Abwasserproben oder Fischplasma werden heute die Kopplungsverfahren zwischen HPLC, Gaschromatographie und Massenspektrometrie nach geeigneter Probenvorbereitung eingesetzt. ⓘ
Verkaufsabgrenzung
In Deutschland sind Diclofenac-haltige Arzneimittel verschreibungspflichtig; ausgenommen sind Formulierungen mit einer Diclofenac-Konzentration bis 5 Prozent zur Anwendung auf der Haut und Pflaster zum äußeren Gebrauch ohne weiteren Zusatz arzneilich wirksamer Bestandteile in einer Wirkstoffmenge bis zu 140 mg je abgeteilter Arzneiform. Ferner können perorale Arzneiformen in Einzeldosen bis zu 25 mg je abgeteilter Form und einer Tagesdosis bis maximal 75 mg zur Fiebersenkung (für eine maximale Anwendungsdauer von drei Tagen) und zur Schmerzstillung (für eine maximale Anwendungsdauer von vier Tagen) ohne Rezept bezogen werden. ⓘ
In Österreich sind Diclofenac-haltige Arzneimittel verschreibungspflichtig, außer für die äußerliche Anwendung gegen Schmerzen und Schwellungen nach stumpfen Verletzungen, Muskelverspannungen und Hexenschuss. ⓘ
Handelspräparate
- Monopräparate
Das ursprüngliche Präparat des Unternehmens Geigy trägt den Namen Voltaren (D, A, CH). Weitere Medikamentennamen sind Dedolor (A), Deflamat (A), Deflamm (A), Diclac (D), Diclo (D), Difen-Stulln (CH), Dolpasse (A), Ecofenac (CH), Effigel (CH), Flam-X (CH), Flector (D, CH), Inflamac (CH), Itami (D), Olfen (D, CH), Pennsaid (A), Primofenac (CH), Relowa (CH), Sandoz Schmerzgel (D), Solacutan (D, A, CH; Generikum zu Solaraze), Solaraze (D, A, CH), Tonopan (CH), Tratul (A), Vifenac (CH), Voltadol (A), Voltfast (CH), zahlreiche Generika (D, A, CH)
- Kombinationspräparate
+ Omeprazol: Arthrocomb (A)
+ Misoprostol: Arthrotec/Arthotec (D, A, CH)
+ Codein: Combaren (D), Voltaren Plus (D)
+ Thiamin, Cyanocobalamin, Pyridoxin: Diclo-B (A), Diclovit (A)
+ Heparin: Flectoparin (CH)
+ Orphenadrin: Neodolpasse (A) ⓘ



