Saponine



R2 = verschiedene Alkylreste ⓘ
Saponine (lateinisch sapo ‚Seife‘) sind Glycoside von Steroiden, Steroidalkaloiden (stickstoffhaltige Steroide) oder Triterpenen. Man spricht daher auch von Steroidsaponinen, Steroidalkaloidsaponinen und Triterpensaponinen (wobei allerdings beachtet werden sollte, dass die Klassifizierung von „Steroidalkaloidsaponinen“ als Saponine umstritten ist und im Zweifelsfall die Terminologie „Steroidale Glykoalkaloide“ zu bevorzugen ist). Aufgrund der Vielzahl möglicher Kohlenhydratstrukturen und der großen strukturellen Variabilität der Aglycone weist diese Stoffgruppe eine entsprechend große Strukturvielfalt und damit eine große Variabilität in den biologischen Eigenschaften auf. ⓘ
Die Bezeichnung Saponinglykosid ist ein Pleonasmus und daher nicht korrekt. ⓘ
Saponine (lateinisch "sapon", Seife + "-in", eines von), auch Triterpenglykoside genannt, sind bitter schmeckende, in der Regel giftige pflanzliche organische Chemikalien, die beim Aufschütteln in Wasser eine schaumige Qualität aufweisen. Sie sind weit verbreitet, kommen aber insbesondere im Seifenkraut (Gattung Saponaria), einer blühenden Pflanze, und im Seifenrindenbaum (Quillaja saponaria) vor. Sie werden in Seifen, Arzneimitteln, Feuerlöschern, als Nahrungsergänzungsmittel, zur Synthese von Steroiden und in kohlensäurehaltigen Getränken (der Kopf auf einem Krug Root Beer) verwendet. Strukturell handelt es sich um Glykoside, d. h. Zucker, die an ein anderes organisches Molekül gebunden sind, in der Regel ein Steroid oder Triterpen, ein Steroidbaustein. Saponine sind sowohl wasser- als auch fettlöslich, was ihnen ihre nützlichen Seifeneigenschaften verleiht. Einige Beispiele für diese Chemikalien sind Glycyrrhizin, ein Lakritzaroma, und Quillaia (alt. quillaja), ein in Getränken verwendeter Rindenextrakt. ⓘ
Geschichte
Seifen als solches sind schon seit dem Altertum bekannt. Jedoch definierte erst Leopold Gmelin den Begriff „Saponine“. ⓘ
Johann Friedrich Zittmann stellte aus den Wurzeln von verschiedenen Smilax-Arten ein Decoct her, das 1795 von Johann Christian Anton Theden als „Decoctum Zittmanni“ bezeichnet wird und gegen Syphilis verwendet wird. ⓘ
Tennet begann 1736 die Senega-Wurzel als Expektorans zu verwenden. W. von Schulz konnte 1896 dann das enthaltene Saponin Senegin isolieren. Während der Weltkriege wurde die Droge sehr selten und teuer, sodass man sie durch Radix Saponariae albae oder Primelwurzeln und -blüten ersetzte, welche noch heute als Expektorans verwendet werden. ⓘ
Eigenschaften
Saponine werden so bezeichnet, da sie beim Schütteln mit Wasser oft einen seifenartigen Schaum ergeben. Demgemäß steht auch eine allgemeine Wirkungsweise dieser Verbindungsklasse im Vordergrund, die mit der Detergenzeigenschaft zusammenhängt. Saponine bilden im Allgemeinen stabile Schäume, zeigen häufig hämolytische Aktivität, beeinflussen die Membranpermeabilität, komplexieren Cholesterin, haben mitunter einen bitteren Geschmack (Ausnahmen: Glycyrrhizin, das den süßen Geschmack der Lakritze ausmacht sowie die sehr süßen Mogroside aus der chinesischen Pflanze Siraitia grosvenori) und sind piscizid (giftig für Fische). ⓘ
Vorkommen
Saponine sind in höheren Pflanzen weit verbreitet, besonders in nährstoffreichem Gewebe, wie Wurzeln, Knollen, Blättern, Blüten und Samen. Saponine wurden in über 90 Pflanzenfamilien beschrieben. In einer Untersuchung von 1730 zentralasiatischen Pflanzenarten wurden in 76 % der Familien Saponine gefunden. Man findet Saponine in Gemüsepflanzen, wie Sojabohnen, Kichererbsen, Erdnüssen, Mungobohnen, Saubohnen, Linsen, Erbsen, Quinoa, Spinat, Hafer, Auberginen, Spargel, Fenchel, Knoblauch, Zuckerrüben, Tomaten, grüne Paprika, Kartoffeln (Solanin), Zwiebeln, Cassava und Yams. Sie sind darüber hinaus Bestandteile von Tee, Ginseng oder Jiaogulan. Saponine sind Sekundäre Pflanzenstoffe. ⓘ

Der Saft aus den Rhizomen des Echten Seifenkrauts wurde schon früh als Waschmittel verwendet, daher auch der botanische Gattungsname Saponaria. In hoher Konzentration treten Saponine in Kastanien und in der Rinde des südamerikanischen Seifenrindenbaumes (Quillaja saponaria) auf, letzteres auch Panamarinde genannt. Aus ökologischen Gründen haben die indischen Waschnüsse, deren Waschwirkung auf die hohe Konzentration an Saponinen zurückgeht, in jüngster Zeit ein breiteres Interesse geweckt. Ferner findet man Saponine in marinen Kleinstlebewesen und Seewalzen (Holothurine). Verschiedene weitere Pflanzen enthalten Saponine, z. B. Alpenveilchen (Cyclamen spp.), Barringtonia asiatica, Bittersüßer Nachtschatten, Cestrum auriculatum, Efeu, Guajacum, Gypsophila struthium, Jiaogulan (Gynostemma pentaphyllum), Kornrade (Agrostemma githago), Lungenkraut, Luzerne, Polygala senega, Primeln, Quinoa, (Chenopodium quinoa), Seifenwurzel, Hundsnelke, Vogelmiere (Stellaria media), Waschnussbaum und Ginseng. ⓘ
Chemische Strukturen
Die strukturelle Klassifikation der Saponine erfolgt zunächst anhand der Aglycone, den sogenannten Sapogeninen, da der Saccharidteil selbst in ein und derselben natürlichen Quelle mitunter recht stark variiert und üblicherweise mehrere verschiedene Glykosylierungsmuster nebeneinander zu finden sind. Bei den Sapogeninen findet man hingegen meist eine sehr viel begrenztere Strukturvielfalt in einer Quelle. In beiden Fällen ist die Variabilität meist auf verwandte Stoffwechselwege und deren Zwischenschritte zurückzuführen, so dass regelmäßig eine ganze Reihe ähnlicher Verbindungen mit zum Teil ähnlichen, aber in ihrer biologischen Wirkung abgestuften Eigenschaften zu finden sind. ⓘ
Monodesmosidische Saponine haben eine Zuckerkette, bisdesmosidische Saponine zwei Zuckerketten, die an unterschiedlichen Positionen des Aglykons gebunden sind. ⓘ
- Steroidsapogenine mit C-27-Grundgerüst:
- Spirostane, bei denen die Seitenkette ein an den D-Ring anelliertes bicyclisches Spiroketal (E- und F-Ring) bildet (z. B. Digitogenin)
- Furostane, bei denen ein Teil der Seitenkette einen an den D-Ring anellierten Furanring (E-Ring) formt
- im Vergleich zum Cholestan umgelagerte C-27-Grundgerüste
- Steroidalkaloidsapogenine mit C-27-Grundgerüst und Stickstoffatom meist in der Seitenkette (auch hier findet man ähnliche Varianten, wie bei den Steroidsapogeninen) ⓘ

- Triterpensapogenine mit C-30-Grundgerüst u. a.:
- Cycloartane: Tetracyclisches Cholestan-Grundgerüst und einem zusätzlichen anellierten Cyclopropanring
- Dammarane, Tirucallane und Cucurbitane: drei anellierte Sechsringe (A–C) und ein an den C-Ring anellierter Fünfring (D)
- Holothurinogenine, die sich vom Holostan ((20S)-20-Hydroxy-5α-lanostan-18-säurelacton) bzw. Lanostan ableiten. Die Gruppe besitzt drei anellierte Sechsringe (A–C) und einen an den C-Ring anellierten, doppelten Fünfring (D,E), der äußere davon ist ein Lacton; dieser Ring trägt zusätzlich einen nicht anellierten Tetrahydrofuran-Ring. Die Glycoside bilden die Gruppe der Holothurine.
- Lupane (Stoffgruppe): vier anellierte Sechsringe (A–D) und ein an den D-Ring anellierter Fünfring (E)
- Oleanane (siehe Strukturformel des Ballonblumensaponins), Ursane und Taraxasterane: fünf anellierte Sechsringe (A–E), häufig ist die Methylgruppe C-28 bei diesen Saponinen zur Säure oxidiert, z. B. in Saponinen, die sich vom Aglykon Gypsogenin ableiten. ⓘ
Biologische Funktion
Saponine dienen den Pflanzen wahrscheinlich als Defensivstoffe, beispielsweise gegen Pilzbefall und Insektenfraß. Da Pflanzen kein aktives Immunsystem wie die Wirbeltiere haben, werden Schadorganismen oft chemisch bekämpft. Bei der Reifung von Nachtschattengewächsen wie der Tomate und der Kartoffel werden die giftigen Steroidalkaloidsaponine durch Denitrifikation (enzymatische Entfernung des Stickstoffs) in ungiftige Steroidsaponine umgewandelt. ⓘ
Biosynthese
Saponine entstammen dem Phytosterolanabolismus. Über den cytosolischen Mevalonatweg gebildetes DMAPP und IPP bildet dabei die Grundlage zur Bildung von 2,3-Oxidosqualen, das als letztes gemeinsames Vorläufermolekül den Scheidepunkt von Phytosterolen, Steroidsaponinen und Steroidalkaloidsaponinen auf der einen Seite und Triterpensaponinen auf der anderen Seite markiert. Sogenannte Oxidosqualencyclasen (auch: Triterpensynthasen) katalysieren Cyclisierungskaskaden von Oxidosqualen die in der Formierung von Cycloartenol im Falle ersterer oder verschiedener Triterpene wie bspw. Dammaran, Lupeol und β-Amyrin in der weiteren Biosynthese letzterer resultieren. An welchem Schritt sich Steroidsaponine bzw. Steroidalkaloidsaponine von der weiteren Phytosterolbiosynthese abspalten, ist nicht bekannt. ⓘ
Die Bildung des initialen Sapogeningrundgerüstes ist oftmals gefolgt von der Modifizierung einzelner Positionen. Zumeist handelt es sich dabei in erster Instanz um die Einführung von Hydroxy-, Keto- oder Carboxygruppen. Die Mehrzahl dieser Oxidierungen wird dabei vermutlich von „Cytochrom P450“-Enzymen katalysiert. Hydroxy- und Carboxygruppen können im Anschluss als Angriffspunkt für die Verknüpfung mit Seitengruppen unterschiedlichster chemischer Herkunft, wie bspw. kleineren aliphatischen und aromatischen Säuren ober eben auch Zuckerresten dienen. ⓘ
Die Glykosylierung des Aglycons, also die Verknüpfung mit Zuckerresten, ist in der Regel notwendig, um die biologische Aktivität von Saponinen zu gewährleisten. Typische Saponinzuckerseitenketten bestehen aus 2–5 Monosaccharideinheiten und sind mit der C3-Hydroxygruppe und/oder (sofern vorhanden) C28-Carboxygruppe des Sapogenins via Ether- bzw. Esterbindung verknüpft. Am häufigsten vorgefundene Zuckerreste in Saponinglykosylierungsmustern sind Glucosyl-, Galactosyl-, Glucuronyl-, Rhamnosyl-, Xylosyl- und Arabinosyl-Einheiten. Bisher identifizierte Enzyme die an der Synthese von Saponinzuckerseitenketten beteiligt sind, gehören alle zur Klasse der Familie 1 UDP-Glykosyltransferasen und katalysieren jeweils die Verknüpfung eines einzelnen Monosaccharidrestes mit dem Sapogenin oder der wachsenden Saponinzuckerseitenkette. ⓘ
Analyse
Die Analyse von Saponinen erfolgt üblicherweise per LC-MS, HPLC, Gaschromatografie, teilweise auch per Dünnschichtchromatographie. Ein Vorhandensein von Saponinen kann durch Aufschütteln geprüft werden, wobei sich ein Schaum bildet, der länger als 10 Minuten steht. Als Positivkontrolle dient dabei die Rinde von Entada phaseoloides. ⓘ
Anwendungen
Saponine sind wirksame Bestandteile des Adjuvans QS-21. Sie verstärken die zelluläre Immunantwort. In Kosmetikprodukten wird es in der Liste der Inhaltsstoffe als SAPONINS (INCI) angegeben. ⓘ
Verwendungen
Die Saponine sind eine Unterklasse der Terpenoide, der größten Klasse von Pflanzenextrakten. Die amphipathische Natur der Saponine verleiht ihnen Aktivität als Tenside mit der potenziellen Fähigkeit, mit Zellmembrankomponenten wie Cholesterin und Phospholipiden zu interagieren, was Saponine möglicherweise für die Entwicklung von Kosmetika und Medikamenten nützlich macht. Saponine wurden auch als Adjuvantien bei der Entwicklung von Impfstoffen verwendet, wie beispielsweise Quil A, ein Extrakt aus der Rinde von Quillaja saponaria. Dies macht sie für eine mögliche Verwendung in Untereinheiten-Impfstoffen und Impfstoffen gegen intrazelluläre Krankheitserreger interessant. Bei ihrer Verwendung als Adjuvantien für die Herstellung von Impfstoffen ist die mit der Sterolkomplexbildung verbundene Toxizität nach wie vor ein Problem. ⓘ
Saponine werden zwar als Nahrungsergänzungsmittel beworben und in der traditionellen Medizin verwendet, es gibt jedoch keine hochwertigen klinischen Beweise dafür, dass sie sich positiv auf die menschliche Gesundheit auswirken. Quillaja ist giftig, wenn es in großen Mengen konsumiert wird, was zu Leberschäden, Magenschmerzen, Durchfall und anderen unerwünschten Wirkungen führen kann. ⓘ
Die Saponine werden wegen ihrer Wirkung auf Ammoniakemissionen in der Tierfütterung verwendet. In den Vereinigten Staaten erforschen Forscher die Verwendung von aus Pflanzen gewonnenen Saponinen zur Bekämpfung invasiver Wurmarten, einschließlich des Springwurms. ⓘ
Saponine weisen ein antioxidatives Potenzial in den Mitochondrien des Gehirns auf. ⓘ
Biologische Funktionen
Saponine haben hypolipidämische Eigenschaften, da sie die Cholesterin- und Low-Density-Lipoproteinwerte senken und bei der Behandlung von Dyslipidämie hilfreich sein können. ⓘ
Saponine haben eine zytotoxische Wirkung auf Krebszellen durch Induktion der Apoptose. Sie haben auch chemotherapeutische Eigenschaften, da sie über Mechanismen verfügen, die die Proteinexpression im Zusammenhang mit dem Zellzyklus, dem Fortschreiten des Krebses und der Metastasierung kontrollieren. ⓘ
Über die antidiabetische Wirkung von Saponinen wurde ausführlich berichtet, wobei Saponine als antidiabetisches Prinzip von Heilpflanzen identifiziert wurden. Für die antidiabetischen Eigenschaften der Saponine wurden mehrere Mechanismen vorgeschlagen, darunter die Aktivierung des Peroxisom-Proliferator-aktivierten Rezeptors gamma (PPARγ), die Aktivierung des Glukosetransporters Typ 4 (Glut4), die Aktivierung der Adiponektin-Expression, die Aktivierung des PI3K/Akt-Wegs, die Erhöhung der Expression von Adipsin und die Aktivierung der AMP-aktivierten Proteinkinase (AMPK). ⓘ
Abkochung
Die wichtigste historische Verwendung dieser Pflanzen war das Auskochen zur Herstellung von Seife. Saponaria officinalis ist für dieses Verfahren am besten geeignet, aber auch andere verwandte Arten funktionieren. Die größte Saponinkonzentration tritt während der Blütezeit auf, wobei das meiste Saponin in den holzigen Stängeln und Wurzeln zu finden ist, aber auch die Blätter enthalten einiges. ⓘ
Quellen
Saponine werden seit jeher aus Pflanzen gewonnen, wurden aber auch aus Meeresorganismen wie der Seegurke isoliert. Ihren Namen haben sie von der Seifenkrautpflanze (Gattung Saponaria, Familie Caryophyllaceae), deren Wurzel früher als Seife verwendet wurde. Saponine finden sich auch in der botanischen Familie der Sapindaceae, einschließlich ihrer bestimmenden Gattung Sapindus (Seifenbeere oder Seifenkastanie) und der Rosskastanie, sowie in den eng verwandten Familien Aceraceae (Ahorngewächse) und Hippocastanaceae. Auch in Gynostemma pentaphyllum (Cucurbitaceae) in der Form der Gypenoside und in Ginseng oder Rotem Ginseng (Panax, Araliaceae) in der Form der Ginsenoside ist es stark vertreten. Saponine sind auch in den unreifen Früchten von Manilkara zapota (auch bekannt als Sapodillas) enthalten, die stark adstringierende Eigenschaften haben. Nerium oleander (Apocynaceae), auch bekannt als Weißer Oleander, ist eine Quelle des starken Herzgifts Oleandrin. Innerhalb dieser Familien kommt diese Klasse chemischer Verbindungen in verschiedenen Teilen der Pflanze vor: Blätter, Stängel, Wurzeln, Zwiebeln, Blüten und Früchte. Kommerzielle Formulierungen pflanzlicher Saponine, z. B. aus dem Seifenrindenbaum, Quillaja saponaria, und solche aus anderen Quellen sind durch kontrollierte Herstellungsverfahren verfügbar, wodurch sie als chemische und biomedizinische Reagenzien genutzt werden können. ⓘ
Rolle in der Pflanzenökologie und Auswirkungen auf die Nahrungssuche von Tieren
In Pflanzen können Saponine als Fraßschutzmittel und zum Schutz der Pflanze vor Mikroben und Pilzen dienen. Einige Pflanzensaponine (z. B. aus Hafer und Spinat) können die Nährstoffaufnahme verbessern und die Verdauung der Tiere unterstützen. Allerdings schmecken Saponine oft bitter und können daher die Schmackhaftigkeit von Pflanzen (z. B. in Viehfutter) verringern oder ihnen sogar eine lebensbedrohliche Toxizität für Tiere verleihen. Einige Saponine sind für Kaltblüter und Insekten in bestimmten Konzentrationen giftig. Weitere Forschungen sind erforderlich, um die Rolle dieser Naturstoffe in ihren Wirtsorganismen zu definieren, die bisher als "schlecht verstanden" bezeichnet wurde. ⓘ
Ethnobotanik
Die meisten Saponine, die sich leicht in Wasser auflösen, sind für Fische giftig. In der Ethnobotanik sind sie daher dafür bekannt, dass sie von den Ureinwohnern zur Gewinnung von aquatischen Nahrungsquellen verwendet werden. Seit prähistorischen Zeiten haben Kulturen auf der ganzen Welt fischabtötende Pflanzen, die in der Regel Saponine enthalten, für den Fischfang verwendet. ⓘ
Obwohl sie gesetzlich verboten sind, werden fischgiftige Pflanzen von indigenen Stämmen in Guyana immer noch häufig verwendet. ⓘ
Auf dem indischen Subkontinent verwendet das Volk der Gondi Giftpflanzenextrakte für den Fischfang. ⓘ
Viele indianische Stämme in Kalifornien verwendeten traditionell Seifenwurzel (Gattung Chlorogalum) und/oder die Wurzel verschiedener Yucca-Arten, die Saponin enthalten, als Fischgift. Sie pulverisierten die Wurzeln, mischten sie mit Wasser, um einen Schaum zu erzeugen, und leiteten die Seifenlauge dann in einen Fluss. Dadurch wurden die Fische getötet oder außer Gefecht gesetzt und konnten leicht von der Wasseroberfläche geholt werden. Zu den Stämmen, die diese Technik anwendeten, gehörten die Lassik, die Luiseño und die Mattole. ⓘ
Chemische Struktur
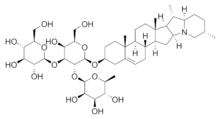
Die große Heterogenität der Strukturen, die dieser Verbindungsklasse zugrunde liegen, macht Verallgemeinerungen schwierig; sie sind eine Unterklasse der Terpenoide, sauerstoffhaltige Derivate von Terpenkohlenwasserstoffen. Terpene wiederum bestehen formal aus Isopren-Einheiten mit fünf Kohlenstoffatomen. (Die alternative Steroidbasis ist ein Terpen, dem einige Kohlenstoffatome fehlen.) Derivate werden gebildet, indem einige der Wasserstoffatome der Basisstruktur durch andere Gruppen ersetzt werden. Im Fall der meisten Saponine ist einer dieser Substituenten ein Zucker, so dass die Verbindung ein Glykosid des Basismoleküls ist. ⓘ
Genauer gesagt kann die lipophile Grundstruktur eines Saponins ein Triterpen, ein Steroid (wie Spirostanol oder Furostanol) oder ein steroidales Alkaloid (bei dem Stickstoffatome ein oder mehrere Kohlenstoffatome ersetzen) sein. Alternativ kann die Grundstruktur auch eine azyklische Kohlenstoffkette sein und nicht die für Steroide typische Ringstruktur. Eine oder zwei (selten drei) hydrophile Monosaccharideinheiten (Einfachzucker) binden sich über ihre Hydroxylgruppen (OH) an die Grundstruktur. In einigen Fällen sind andere Substituenten vorhanden, wie z. B. Kohlenstoffketten mit Hydroxyl- oder Carboxylgruppen. Solche Kettenstrukturen können 1-11 Kohlenstoffatome lang sein, sind aber meist 2-5 Kohlenstoffatome lang; die Kohlenstoffketten selbst können verzweigt oder unverzweigt sein. ⓘ
Die am häufigsten vorkommenden Zucker sind Monosaccharide wie Glukose und Galaktose, obwohl es in der Natur eine große Vielfalt an Zuckern gibt. Andere Moleküle wie organische Säuren können sich ebenfalls an die Base binden, indem sie über ihre Carboxylgruppen (COOH) Ester bilden. Besonders erwähnenswert sind Zuckersäuren wie Glucuronsäure und Galacturonsäure, die oxidierte Formen von Glucose und Galactose sind. ⓘ