Methylenblau
 | |
| Klinische Daten | |
|---|---|
| Handelsnamen | Urelene blue, Provayblue, Proveblue, andere |
| Andere Bezeichnungen | CI 52015, basisches Blau 9 |
| AHFS/Drugs.com | Monographie |
| Lizenz-Daten |
|
| Schwangerschaft Kategorie |
|
| Wege der Verabreichung | Durch den Mund, intravenös (IV) |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Eliminationshalbwertszeit | 5 bis 24 Stunden |
| Bezeichner | |
IUPAC-Bezeichnung
| |
| CAS-Nummer | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Chemische und physikalische Daten | |
| Formel | C16H18ClN3S |
| Molare Masse | 319,85 g-mol-1 |
| 3D-Modell (JSmol) | |
SMILES
| |
InChI
| |
| (Überprüfen) | |
Methylthioniniumchlorid, gemeinhin Methylenblau genannt, ist ein Salz, das als Farbstoff und als Medikament verwendet wird. Methylenblau ist ein Thiazin-Farbstoff. Als Medikament wird es hauptsächlich zur Behandlung von Methämoglobinämie eingesetzt, indem es das Eisen im Hämoglobin in Eisen umwandelt. Insbesondere wird es zur Behandlung von Methämoglobinwerten eingesetzt, die über 30 % liegen oder bei denen trotz Sauerstofftherapie Symptome auftreten. Früher wurde es bei Zyanidvergiftungen und Harnwegsinfektionen eingesetzt, aber diese Anwendung wird nicht mehr empfohlen. ⓘ
Methylenblau wird in der Regel durch Injektion in eine Vene verabreicht. Häufige Nebenwirkungen sind Kopfschmerzen, Erbrechen, Verwirrung, Kurzatmigkeit und hoher Blutdruck. Weitere Nebenwirkungen sind das Serotonin-Syndrom, der Zusammenbruch der roten Blutkörperchen und allergische Reaktionen. Bei der Einnahme färben sich Urin, Schweiß und Stuhl oft blau bis grün. Während die Einnahme während der Schwangerschaft das Baby schädigen kann, ist die Nichtanwendung bei Methämoglobinämie wahrscheinlich gefährlicher. ⓘ
Methylenblau wurde erstmals im Jahr 1876 von Heinrich Caro hergestellt. Es steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation. ⓘ
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Methylenblau | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C16H18ClN3S | ||||||||||||||||||
| Kurzbeschreibung |
dunkelgrüne, glänzende Kristalle | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code |
V03AB17 | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 319,86 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
ca. 190 °C (Zersetzung) | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
1180 mg·kg−1 (LD50, Ratte, oral) | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Methylenblau (Synonym: Methylthioniniumchlorid) ist ein Phenothiazin-Derivat. Der kationische Farbstoff wird in der Chemie, Medizin und Färbetechnik verwendet. ⓘ
Als reiner Farbstoff erscheint Methylenblau als dunkelgrünes Pulver, beziehungsweise als dunkelgrüne Kristalle. Handelsüblich ist es auch als Doppelsalz mit Zinkchlorid erhältlich, welches ein braunes Pulver ist. ⓘ
Medizinische Anwendungen
Methämoglobinämie
Methylenblau wird als Medikament zur Behandlung von Methämoglobinämie eingesetzt, die durch die Einnahme bestimmter Arzneimittel, Toxine oder Saubohnen entstehen kann. Normalerweise wird Methämoglobin durch die NADH- oder NADPH-abhängigen Methämoglobin-Reduktase-Enzyme wieder zu Hämoglobin reduziert. Wenn infolge von Toxinen große Mengen an Methämoglobin entstehen, sind die Methämoglobinreduktasen überfordert. Methylenblau wird, wenn es als Gegenmittel intravenös injiziert wird, zunächst selbst zu Leucomethylenblau reduziert, das dann die Häm-Gruppe von Methämoglobin zu Hämoglobin reduziert. Methylenblau kann die Halbwertszeit von Methämoglobin von Stunden auf Minuten verkürzen. In hohen Dosen führt Methylenblau jedoch zu einer Methämoglobinämie und kehrt diesen Weg um. ⓘ
Zyanidvergiftung
Da das Reduktionspotenzial von Methylenblau dem von Sauerstoff ähnelt und von den Komponenten der Elektronentransportkette reduziert werden kann, werden manchmal hohe Dosen von Methylenblau als Gegenmittel bei Kaliumcyanidvergiftungen eingesetzt. Diese Methode wurde erstmals 1933 von Dr. Matilda Moldenhauer Brooks in San Francisco erfolgreich getestet, obwohl sie bereits 1926 von Bo Sahlin von der Universität Lund demonstriert wurde. ⓘ
Farbstoff oder Färbung


Methylenblau wird bei der endoskopischen Polypektomie als Zusatz zu Kochsalzlösung oder Epinephrin verwendet und in die Submukosa um den zu entfernenden Polypen injiziert. Auf diese Weise kann die submuköse Gewebeebene nach der Entfernung des Polypen identifiziert werden, was nützlich ist, um festzustellen, ob mehr Gewebe entfernt werden muss oder ob ein hohes Perforationsrisiko besteht. Methylenblau wird auch als Farbstoff in der Chromoendoskopie verwendet und auf die Schleimhaut des Magen-Darm-Trakts gesprüht, um Dysplasien oder präkanzeröse Läsionen zu erkennen. Intravenös injiziertes Methylenblau wird leicht in den Urin abgegeben und kann daher zur Untersuchung der Harnwege auf Undichtigkeiten oder Fisteln verwendet werden. ⓘ
Bei chirurgischen Eingriffen wie der Sentinel-Lymphknotendissektion kann Methylenblau verwendet werden, um den Lymphabfluss des untersuchten Gewebes visuell zu verfolgen. In ähnlicher Weise wird Methylenblau bei orthopädischen Operationen dem Knochenzement zugesetzt, um eine einfache Unterscheidung zwischen nativem Knochen und Zement zu ermöglichen. Darüber hinaus beschleunigt Methylenblau die Aushärtung von Knochenzement, wodurch der Knochenzement schneller und effektiver appliziert werden kann. Methylenblau wird als Hilfsmittel zur Visualisierung/Orientierung in einer Reihe von Medizinprodukten verwendet, darunter eine chirurgische Versiegelungsfolie, TissuePatch. Bei Fisteln und Pilonidalsinus wird es zur Identifizierung des Trakts für die vollständige Exzision verwendet. Auch bei Magen-Darm-Operationen (z. B. Darmresektion oder Magenbypass) kann es zur Prüfung auf Undichtigkeiten verwendet werden. ⓘ
Wenn Methylenblau "polychromiert" wird (in Lösung oxidiert oder durch Pilzmetabolismus "gereift", wie ursprünglich in der Dissertation von Dr. D. L. Romanowsky in den 1890er Jahren festgestellt), wird es seriell demethyliert und bildet alle Tri-, Di-, Mono- und Nicht-Methyl-Zwischenprodukte, die Azure B, Azure A, Azure C bzw. Thionin sind. Dies ist die Grundlage für den basophilen Teil des Spektrums des Romanowski-Giemsa-Effekts. Wird nur synthetisches Azure B und Eosin Y verwendet, kann es als standardisierte Giemsa-Färbung dienen; ohne Methylenblau neigen die normalen neutrophilen Körnchen jedoch zur Überfärbung und sehen wie toxische Körnchen aus. Andererseits kann Methylenblau dazu beitragen, den neutrophilen Granula ein normales Aussehen zu verleihen und die Färbung von Nukleoli und polychromatophilen Erythrozyten (Retikulozyten) zu verbessern. ⓘ
Eine traditionelle Anwendung von Methylenblau ist die intravitale oder supravitale Färbung von Nervenfasern, ein Effekt, der erstmals 1887 von Paul Ehrlich beschrieben wurde. Eine verdünnte Lösung des Farbstoffs wird entweder in das Gewebe injiziert oder auf kleine, frisch entnommene Stücke aufgetragen. Die selektive Blaufärbung entwickelt sich an der Luft (Sauerstoff) und kann durch Eintauchen des gefärbten Präparats in eine wässrige Lösung von Ammoniummolybdat fixiert werden. Vitales Methylenblau wurde früher häufig für die Untersuchung der Innervation von Muskeln, Haut und inneren Organen verwendet. Der Mechanismus der selektiven Farbstoffaufnahme ist noch nicht vollständig geklärt; die Vitalfärbung von Nervenfasern in der Haut wird durch Ouabain verhindert, ein Medikament, das die Na/K-ATPase der Zellmembranen hemmt. ⓘ
Placebo
Methylenblau wurde als Placebo verwendet; Ärzte sagten ihren Patienten, sie sollten mit einer Verfärbung ihres Urins rechnen und dies als Zeichen für eine Verbesserung ihres Zustands ansehen. Genau diese Nebenwirkung macht es schwierig, Methylenblau in traditionellen placebokontrollierten klinischen Studien zu testen. ⓘ
Toxizität von Isobutylnitrit
Isobutylnitrit ist eine der Verbindungen, die als Poppers verwendet werden, eine inhalative Droge, die eine kurze Euphorie hervorruft. ⓘ
Isobutylnitrit kann bekanntermaßen eine Methämoglobinämie verursachen. Schwere Methämoglobinämie kann mit Methylenblau behandelt werden. ⓘ
Toxizität von Ifosfamid
Eine weitere Anwendung von Methylenblau ist die Behandlung der Neurotoxizität von Ifosfamid. Methylenblau wurde erstmals 1994 zur Behandlung und Prophylaxe der neuropsychiatrischen Toxizität von Ifosfamid eingesetzt. Ein toxischer Metabolit von Ifosfamid, Chloracetaldehyd (CAA), stört die mitochondriale Atmungskette, was zu einer Anhäufung von Nicotinamid-Adenin-Dinukleotid-Wasserstoff (NADH) führt. Methylenblau wirkt als alternativer Elektronenakzeptor und kehrt die NADH-Hemmung der hepatischen Gluconeogenese um, während es gleichzeitig die Umwandlung von Chlorethylamin in Chloracetaldehyd hemmt und mehrere Aminoxidase-Aktivitäten hemmt, wodurch die Bildung von CAA verhindert wird. Die Dosierung von Methylenblau zur Behandlung der Neurotoxizität von Ifosfamid variiert, je nachdem, ob es gleichzeitig als Adjuvans bei der Ifosfamid-Infusion oder zur Umkehrung psychiatrischer Symptome eingesetzt wird, die nach Abschluss einer Ifosfamid-Infusion auftreten. Berichten zufolge haben bis zu sechs Dosen Methylenblau pro Tag zu einer Verbesserung der Symptome innerhalb von 10 Minuten bis zu mehreren Tagen geführt. Als Alternative wurde vorgeschlagen, intravenöses Methylenblau alle sechs Stunden zur Prophylaxe während der Ifosfamid-Behandlung bei Patienten mit neuropsychiatrischer Toxizität von Ifosfamid in der Vorgeschichte zu verabreichen. Die prophylaktische Verabreichung von Methylenblau am Tag vor Beginn der Ifosfamid-Chemotherapie und dreimal täglich während der Ifosfamid-Chemotherapie wurde empfohlen, um das Auftreten von Ifosfamid-Neurotoxizität zu verringern. ⓘ
Schock
Es wurde auch bei septischem Schock und Anaphylaxie eingesetzt. ⓘ
Methylenblau erhöht durchweg den Blutdruck bei Menschen mit vasoplegischem Syndrom (redistributiver Schock), aber es konnte nicht nachgewiesen werden, dass es die Sauerstoffversorgung des Gewebes verbessert oder die Sterblichkeit verringert. ⓘ
Methylenblau wurde bei Kalziumkanalblocker-Toxizität als Rettungstherapie bei distributivem Schock eingesetzt, der nicht auf die Erstlinientherapie ansprach. Die Beweise für seine Verwendung in diesem Fall sind sehr dürftig und beschränken sich auf eine Handvoll Fallberichte. ⓘ
Nebeneffekte
| Herz-Kreislauf-System | Zentrales Nervensystem | Dermatologisch | Gastrointestinalbereich | Genitoharnwege | Hämatologie ⓘ |
|---|---|---|---|---|---|
| - Bluthochdruck - Präkordialer Schmerz |
- Schwindelgefühl - Geistige Verwirrung - Kopfschmerzen - Fieber |
- Verfärbung der Haut - Nekrose an der Injektionsstelle (SC) |
- Verfärbung des Stuhls - Übelkeit - Erbrechen - Unterleibsschmerzen |
- Verfärbung des Urins (Dosen über 80 µg) - Blasenreizung |
- Anämie |
Methylenblau ist ein Monoaminoxidase-Hemmer (MAOI) und kann bei intravenöser Verabreichung von Dosen über 5 mg/kg eine schwere Serotonin-Toxizität, das Serotonin-Syndrom, auslösen, wenn es mit selektiven Serotonin-Wiederaufnahme-Hemmern (SSRI) oder anderen Serotonin-Wiederaufnahme-Hemmern (z. B. Duloxetin, Sibutramin, Venlafaxin, Clomipramin, Imipramin) kombiniert wird. ⓘ
Es verursacht eine hämolytische Anämie bei Trägern des G6PD-Enzymmangels (Favismus). ⓘ
Chemie
Methylenblau ist ein formales Derivat von Phenothiazin. Es ist ein dunkelgrünes Pulver, das in Wasser eine blaue Lösung ergibt. Die hydratisierte Form enthält 3 Wassermoleküle pro Einheit Methylenblau. Methylenblau hat in Wasser (10 g/l) bei 25 °C (77 °F) einen pH-Wert von 6. ⓘ
Herstellung
Diese Verbindung wird durch Oxidation von Dimethyl-4-phenylendiamin in Gegenwart von Natriumthiosulfat hergestellt:
Lichtabsorptionseigenschaften
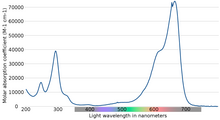
Das Absorptionsmaximum des Lichts liegt bei 670 nm. Die Besonderheiten der Absorption hängen von einer Reihe von Faktoren ab, darunter Protonierung, Adsorption an andere Materialien und Metachromasie - die Bildung von Dimeren und Aggregaten höherer Ordnung in Abhängigkeit von der Konzentration und anderen Wechselwirkungen:
| Spezies | Absorptionspeak | Extinktionskoeffizient (dm3/mol-cm) ⓘ |
|---|---|---|
| MB+ (Lösung) | 664 | 95000 |
| MBH2+ (Lösung) | 741 | 76000 |
| (MB+)2 (Lösung) | 605 | 132000 |
| (MB+)3 (Lösung) | 580 | 110000 |
| MB+ (adsorbiert an Ton) | 673 | 116000 |
| MBH2+ (adsorbiert an Ton) | 763 | 86000 |
| (MB+)2 (adsorbiert an Ton) | 596 | 80000 |
| (MB+)3 (adsorbiert an Ton) | 570 | 114000 |
Andere Verwendungen

Redox-Indikator
Methylenblau wird in der analytischen Chemie häufig als Redoxindikator verwendet. Lösungen dieser Substanz sind blau, wenn sie sich in einer oxidierenden Umgebung befinden, werden jedoch farblos, wenn sie einem Reduktionsmittel ausgesetzt sind. Die Redox-Eigenschaften lassen sich in einer klassischen Demonstration der chemischen Kinetik in der allgemeinen Chemie, dem "Blue Bottle"-Experiment, beobachten. In der Regel wird eine Lösung aus Glukose (Traubenzucker), Methylenblau und Natriumhydroxid hergestellt. Wenn die Flasche geschüttelt wird, oxidiert Sauerstoff Methylenblau, und die Lösung färbt sich blau. Der Traubenzucker reduziert das Methylenblau allmählich zu seiner farblosen, reduzierten Form. Wenn der gelöste Traubenzucker vollständig verbraucht ist, färbt sich die Lösung wieder blau. Das Redox-Mittelwertpotential E0' beträgt +0,01 V. ⓘ
Peroxid-Generator
Methylenblau ist ebenfalls ein Photosensibilisator, der Singulett-Sauerstoff erzeugt, wenn er sowohl Sauerstoff als auch Licht ausgesetzt wird. In diesem Zusammenhang wird es verwendet, um organische Peroxide durch eine Diels-Alder-Reaktion herzustellen, die mit normalem atmosphärischem Triplett-Sauerstoff verboten ist. ⓘ
Analyse von Sulfiden
Die Bildung von Methylenblau nach der Reaktion von Schwefelwasserstoff mit Dimethyl-p-phenylendiamin und Eisen(III) bei einem pH-Wert von 0,4 bis 0,7 wird zur Bestimmung der Sulfidkonzentration im Bereich von 0,020 bis 1,50 mg/L (20 ppb bis 1,5 ppm) durch photometrische Messungen verwendet. Der Test ist sehr empfindlich und die Blaufärbung, die sich bei Kontakt der Reagenzien mit gelöstem H2S entwickelt, ist 60 Minuten lang stabil. Gebrauchsfertige Kits wie der Spectroquant-Sulfid-Test erleichtern Routineanalysen. Der Methylenblau-Sulfid-Test ist eine praktische Methode, die häufig in der Bodenmikrobiologie eingesetzt wird, um die Stoffwechselaktivität von sulfatreduzierenden Bakterien (SRB) in Wasser schnell nachzuweisen. Es ist zu beachten, dass Methylenblau bei diesem Test ein Reaktionsprodukt und kein Reagenz ist. ⓘ
Die Zugabe eines starken Reduktionsmittels, wie z. B. Ascorbinsäure, zu einer sulfidhaltigen Lösung wird manchmal verwendet, um die Sulfidoxidation durch Luftsauerstoff zu verhindern. Dies ist zwar eine gute Vorsichtsmaßnahme für die Bestimmung von Sulfid mit einer ionenselektiven Elektrode, kann jedoch die Entwicklung der blauen Farbe behindern, wenn das frisch gebildete Methylenblau ebenfalls reduziert wird, wie oben im Abschnitt über Redoxindikatoren beschrieben. ⓘ
Prüfung von Wasser
Durch eine Farbreaktion in einer angesäuerten, wässrigen Methylenblau-Lösung mit Chloroform können anionische Tenside in einer Wasserprobe nachgewiesen werden. Ein solcher Test ist als MBAS-Test (Methylenblau-Aktivstoff-Test) bekannt. ⓘ
Der MBAS-Test kann jedoch nicht zwischen bestimmten Tensiden unterscheiden. Einige Beispiele für anionische Tenside sind Carboxylate, Phosphate, Sulfate und Sulfonate. ⓘ
Methylenblauwert von feinem Aggregat
Der Methylenblauwert gibt den Anteil an Tonmineralien in den Gesteinsproben an. Die Methylenblaulösung wird nacheinander zu den feinen Gesteinskörnungen gegeben, die in Wasser gerührt werden. Das Vorhandensein einer freien Farbstofflösung kann mit dem Färbetest auf einem Filterpapier überprüft werden. ⓘ
Biologische Färbung
In der Biologie wird Methylenblau als Farbstoff für eine Reihe verschiedener Färbeverfahren verwendet, z. B. für die Wright'sche Färbung und die Jenner'sche Färbung. Da es sich um ein temporäres Färbeverfahren handelt, kann Methylenblau auch zur Untersuchung von RNA oder DNA unter dem Mikroskop oder in einem Gel verwendet werden: So kann beispielsweise eine Methylenblau-Lösung zur Färbung von RNA auf Hybridisierungsmembranen beim Northern Blotting verwendet werden, um die Menge der vorhandenen Nukleinsäure zu überprüfen. Methylenblau ist zwar nicht so empfindlich wie Ethidiumbromid, ist aber weniger toxisch und lagert sich nicht in Nukleinsäureketten ein, so dass die Retention von Nukleinsäuren auf Hybridisierungsmembranen oder der Hybridisierungsprozess selbst nicht beeinträchtigt wird. ⓘ
Es kann auch als Indikator verwendet werden, um festzustellen, ob eukaryontische Zellen wie Hefe lebendig oder tot sind. Das Methylenblau wird in lebensfähigen Zellen reduziert, so dass sie ungefärbt bleiben. Tote Zellen sind jedoch nicht in der Lage, das oxidierte Methylenblau zu reduzieren, und die Zellen sind blau gefärbt. Methylenblau kann die Atmung der Hefe beeinträchtigen, da es Wasserstoffionen aufnimmt, die während des Prozesses entstehen. ⓘ
Aquakultur
Methylenblau wird in der Aquakultur und von Tropenfischliebhabern zur Behandlung von Pilzinfektionen eingesetzt. Es kann auch zur Behandlung von Fischen eingesetzt werden, die mit Ichthyophthirius infiziert sind, obwohl eine Kombination aus Malachitgrün und Formaldehyd weitaus wirksamer gegen den parasitären Protozoen Ichthyophthirius multifiliis ist. Es wird in der Regel verwendet, um neu abgelegte Fischeier vor einer Infektion durch Pilze oder Bakterien zu schützen. Dies ist nützlich, wenn der Hobbyist die Fischeier künstlich ausbrüten möchte. Methylenblau ist auch sehr wirksam, wenn es als Teil eines "medizinischen Fischbads" zur Behandlung von Ammoniak-, Nitrit- und Zyanidvergiftungen sowie zur topischen und internen Behandlung von verletzten oder kranken Fischen als "erste Reaktion" verwendet wird. ⓘ
Geschichte
Methylenblau wurde als "das erste vollsynthetische Medikament in der Medizin" bezeichnet. Methylenblau wurde erstmals 1876 von dem deutschen Chemiker Heinrich Caro hergestellt. ⓘ
Paul Guttmann und Paul Ehrlich leisteten 1891 Pionierarbeit bei der Behandlung von Malaria. In dieser Zeit vor dem Ersten Weltkrieg glaubten Forscher wie Ehrlich, dass Medikamente und Farbstoffe auf die gleiche Weise wirken, indem sie Krankheitserreger bevorzugt anfärben und ihnen möglicherweise schaden. Die Veränderung der Zellmembran von Krankheitserregern ist in der Tat die Art und Weise, wie verschiedene Medikamente wirken, so dass die Theorie teilweise richtig war, wenn auch bei weitem nicht vollständig. Methylenblau wurde auch im Zweiten Weltkrieg verwendet, wo es bei den Soldaten nicht gut ankam: "Selbst auf dem Klo sehen wir, wenn wir pinkeln, marineblau." Vor kurzem wurde die Verwendung des Mittels zur Bekämpfung von Malaria wiederbelebt. Matilda Brooks entdeckte 1933, dass es ein Gegenmittel gegen Kohlenmonoxid- und Zyanidvergiftungen ist. ⓘ
Der blaue Urin wurde verwendet, um zu überprüfen, ob psychiatrische Patienten ihre Medikamente einhalten. Dies führte dazu, dass man sich seit den 1890er Jahren bis heute für die antidepressive und andere psychotrope Wirkung der Droge interessiert. Es wurde zur Leitsubstanz in der Forschung, die zur Entdeckung von Chlorpromazin führte. ⓘ
Bezeichnungen
Der internationale Freiname (INN) von Methylenblau ist Methylthioniniumchlorid. ⓘ
Forschung
Malaria
Methylenblau wurde von Paul Ehrlich um 1891 als mögliches Mittel zur Behandlung von Malaria entdeckt. Während des Pazifikkriegs in den Tropen verschwand es als Malariamittel, da die amerikanischen und alliierten Soldaten seine beiden auffälligen, aber reversiblen Nebenwirkungen nicht mochten: Es färbt den Urin blau oder grün und die Sklera (das Weiße der Augen) blau. Das Interesse an seiner Verwendung als Malariamittel ist in letzter Zeit wieder erwacht, vor allem wegen seines niedrigen Preises. Derzeit laufen mehrere klinische Studien, in denen versucht wird, eine geeignete Wirkstoffkombination zu finden. Studien an Kindern in Afrika haben ergeben, dass es gegen Malaria wirksam ist, aber die Versuche, Methylenblau mit Chloroquin zu kombinieren, waren enttäuschend. ⓘ
Alzheimer-Krankheit
Eine klinische Phase-3-Studie mit LMTM (TauRx0237 oder LMT-X), einem Derivat von Methylenblau, zeigte bei Menschen mit leichter bis mittelschwerer Alzheimer-Krankheit keinen Nutzen in Bezug auf den kognitiven oder funktionellen Abbau. Das Fortschreiten der Krankheit war bei dem Medikament und dem Placebo praktisch identisch. ⓘ
Bipolare Störung
Methylenblau wurde als Zusatzmedikation bei der Behandlung von bipolaren Störungen untersucht. ⓘ
Infektionskrankheiten
Es wurde bei AIDS-bedingtem Kaposi-Sarkom, West-Nil-Virus und zur Inaktivierung von Staphylococcus aureus und HIV-1 untersucht. Die viruziden Eigenschaften von Phenothiazin-Farbstoffen und Licht sind seit über 70 Jahren bekannt. ⓘ
Herstellung
Methylenblau wird in mehreren Schritten aus N,N-Dimethyl-p-phenylendiamin unter Zusatz von Dichromat als Oxidationsmittel sowie der Addition von N,N-Dimethylanilin hergestellt. Abschließend muss es zum Indamin oxidiert werden, wobei sich Bindschedlers Grün bildet. Dieses wird in Gegenwart von Kupfersulfat mit Schwefelwasserstoff cyclisiert. ⓘ
Die Synthese von Methylenblau lässt sich in fünf Schritte unterteilen. Dabei wird N,N-Dimethylanilin vorgelegt und mit Salzsäure und Natriumnitrit versetzt. Dabei entsteht p-Nitroso-N,N-dimethylanilin. Durch Zugabe von Zinkchlorid wird die entstandene Nitrosogruppe zu einem Amin reduziert. Anschließend reagiert das Produkt der Reduktion p-Amino-N,N-dimethylanilin unter Zugabe von konzentrierter Schwefelsäure und Thioschwefelsäure zu der Thiosulfonsäure von p-Amino-N,N-dimethylanilin. Bei der erneuten Zugabe von konzentrierter Schwefelsäure und der Zugabe eines weiteren Äquivalents von N,N-Dimethylanilins entsteht die Thiosulfonsäure von Bindschedlers Grün. Dies geschieht in einer oxidativen Kupplungsreaktion. Aus der Thiosulfonsäure von Bindschedlers Grün entsteht durch Zugabe von Mangandioxid das gewünschte Produkt Methylenblau. ⓘ
Verwendung

Medizin
In der Heilkunde ist es ein wichtiges Antidot bei Nitrit- und Anilinvergiftungen, da es die Rück-Umwandlung von Methämoglobin zu funktionsfähigem Hämoglobin beschleunigt (s. Methämoglobinämie). Weiter wird es noch als Antiseptikum, zur Bekämpfung von Malaria, Antirheumatikum und zu Diagnosezwecken eingesetzt. In der Tiermedizin findet es, zusammen mit Malachitgrün, als Mittel gegen die bei Fischen auftretende Weißpünktchenkrankheit Verwendung. ⓘ
Weiterhin wird der vielseitige Farbstoff auf seine Eignung zur Behandlung von chronischen Schmerzen des unteren Rückens untersucht. Hierbei wird das Methylenblau zwischen die Wirbel direkt in die beschädigten Bandscheiben (lat. Discus intervertebralis) injiziert, was zu einer Zerstörung der Schmerzrezeptoren und somit zur Beseitigung bzw. Linderung des Schmerzes führt. Initiale Ergebnisse der im Rahmen einer Placebo-kontrollierten klinischen Studie durchgeführten Untersuchung waren ermutigend: Die Behandlungsmethode führte bei einem Großteil der Patienten zu einer nachhaltigen, für mindestens zwei Jahre anhaltenden Schmerzlinderung, wobei bei keinem der Patienten Komplikationen auftraten. Nachfolgende Studien lieferten allerdings teils widersprüchliche Ergebnisse. Die Behandlungsmethode ist nicht zugelassen. ⓘ
Methylenblau wirkt in bestimmten Konzentrationen neurotoxisch. Die Anwendung von Methylenblau kann zum Serotonin-Syndrom führen, wenn MAO-Hemmer wie z. B. Methylenblau und Antidepressiva der Gruppe Selektive Serotonin-Wiederaufnahmehemmer (SSRI), wie beispielsweise Fluoxetin, Fluvoxamin, Paroxetin, Sertralin und Citalopram kombiniert werden. ⓘ
Im Tierversuch zeigte sich an Mäusen nach oraler Verabreichung von M.-Trihydrat an 5 d/Woche über 106 Wochen per Schlundsonde in Dosierungen von 2,5 bis 25 mg/kg KG x d eine dosisabhängige Zunahme von Adenomen und Karzinomen des Dünndarms; bei der höchsten Dosis lag die kombinierte Inzidenz von Adenomen + Karzinomen mit 12 % signifikant über der historischer Kontrollen. [1] Weiterhin wurde ein leichter Anstieg der Inzidenz bösartiger Lymphome beobachtet, der jedoch bei den Männchen nur marginal über der Inzidenz historischer Kontrollen lag und bei den Weibchen keine klare Dosisabhängigkeit zeigte; der Zusammenhang mit der Exposition wurde vom NTP daher als „nicht eindeutig“ („equivocal“) bewertet. Der Bewertung der US-amerikanischen Arzneimittelbehörde FDA zufolge weisen die Ergebnisse dieser Studie hingegen nicht auf eine substanzbedingte Entstehung von Tumoren bei Mäusen hin. [2] Bei Ratten zeigte sich nach entsprechender Verabreichung an 5 d/Woche über 106 Wochen per Schlundsonde in Dosierungen von 5 bis 50 mg M.-Trihydrat/kg KG x d bei den Männchen ein Trend für eine dosisabhängige Zunahme von Inselzelladenomen und möglicherweise von Adenomen + Karzinomen der Bauchspeicheldrüse. Bei Weibchen wurden keine erhöhte Inzidenz von Tumoren festgestellt. Das NTP sieht in diesen Befunden „einige Anzeichen“ („some evidence“) für eine kanzerogene Wirkung von M. bei männlichen und keine derartige Evidenz bei weiblichen Ratten. Die FDA kam zu dem Schluss, dass M. bei männlichen Ratten Inselzelladenome oder -karzinome der Bauchspeicheldrüse verursacht. ⓘ
In der experimentellen Pharmakologie und auch schon in der klinischen Medizin wird Methylenblau als Enzymhemmer der löslichen Guanylylcyclase und damit beim katecholaminrefraktären septischen Schock eingesetzt. ⓘ
Methylenblau gilt auch als Hoffnungsträger für eine künftige Therapie der Frontotemporalen Demenz (FTLD), da es die Aggregation von Tau-Proteinen hemmt. ⓘ
Sonstige
In der Geologie dient die Methylenblau-Methode zur Bestimmung des Smektitgehalts in Tonmineralien. Es stellt damit ein wichtiges Verfahren zur Qualitätskontrolle in vielen Industriezweigen dar. ⓘ
In der Analytischen Chemie wird es in der Bestimmung von Aniontensiden nach der Longwell-Manience-Methode und bei der Epton-Titration verwendet. ⓘ
In der Abwasseranalytik wird eine Methylenblauprobe zur Bestimmung der Fäulnisfähigkeit herangezogen. Mit Hilfe der Methylenblauprobe kann der Nachweis geführt werden, ob bzw. in welchem Maße der Ablauf einer Kläranlage noch fäulnisfähige Stoffe enthält. Methylenblau ist ein Redoxindikator und entfärbt sich bei absolutem Luftabschluss in dem Maße, in dem anaerobe Verhältnisse (H2S-Bildung) überhandnehmen. Es wird die Zeit bis zur Entfärbung des der Probe zugesetzten Farbstoffes bestimmt. Man gibt 0,6 ml einer Methylenblaulösung (0,05 %ig) in eine 100 ml Schliffstopfenflasche, füllt randvoll mit Probe, setzt den Stopfen blasenfrei auf und bewahrt sie im Dunkeln bei 20 °C (Brutschrank) auf. Die Probe wird täglich beobachtet (am ersten Tag mehrmals) und stellt die Zeit bis zur Entfärbung fest; erfolgt diese bereits am ersten Tag (Angaben in Stunden) oder innerhalb vier Tagen (Angabe in Tagen), ist die Ablaufqualität unzulässig; tritt innerhalb von fünf Tagen keine Entfärbung ein, wird die Probe als "n. e." (nicht entfärbt) bezeichnet und der Test abgebrochen (s. DEV [1], H 22,"Prüfung auf Fäulnisfähigkeit" und ÖNORM M 6276). ⓘ
In der Biochemie wird Methylenblau als Redoxmediator eingesetzt. Das Halbwertspotential E0' beträgt +0,011 mV. ⓘ
Methylenblau-Kristalle ⓘ




