Sjögren-Syndrom
| Sjögren-Syndrom ⓘ | |
|---|---|
| Andere Namen | Sjögren-Syndrom, Sicca-Syndrom |
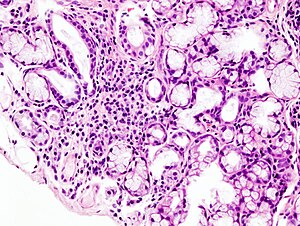 | |
| Mikroskopische Aufnahme einer fokalen lymphoiden Infiltration in der kleinen Speicheldrüse im Zusammenhang mit dem Sjögren-Syndrom. | |
| Aussprache |
|
| Symptome | Trockener Mund, trockene Augen, andere Bereiche der Trockenheit |
| Komplikationen | Lymphom |
| Übliches Auftreten | Mittleres Alter |
| Dauer | Langfristig |
| Ursachen | Autoimmunerkrankung (Ursache unbekannt) |
| Diagnostische Methode | Gewebebiopsie, Blutuntersuchungen |
| Differentialdiagnose | Medikamenten-Nebenwirkung, Angstzustände, Sarkoidose, Amyloidose |
| Behandlung | Künstliche Tränen, Medikamente zur Verringerung der Entzündung, Operation |
| Prognose | Normale Lebenserwartung |
| Häufigkeit | ~0.7% |
Das Sjögren-Syndrom (SjS, SS) ist eine langfristige Autoimmunerkrankung, die die feuchtigkeitsproduzierenden Drüsen (Tränendrüsen und Speicheldrüsen) des Körpers angreift und oft auch andere Organsysteme wie die Lunge, die Nieren und das Nervensystem schwer beeinträchtigt. Die Hauptsymptome sind Trockenheit (trockener Mund und trockene Augen), Schmerzen und Müdigkeit. Weitere Symptome können trockene Haut, Scheidentrockenheit, chronischer Husten, Taubheitsgefühl in Armen und Beinen, Müdigkeit, Muskel- und Gelenkschmerzen sowie Schilddrüsenprobleme sein. Die Betroffenen haben auch ein erhöhtes Risiko (15 %) für Lymphome. ⓘ
Die genaue Ursache ist unklar, man geht jedoch davon aus, dass eine Kombination aus genetischen Faktoren und einem umweltbedingten Auslöser, wie z. B. der Kontakt mit einem Virus oder Bakterium, eine Rolle spielt. Es kann unabhängig von anderen Gesundheitsproblemen (primäres Sjögren-Syndrom) oder als Folge einer anderen Bindegewebsstörung (sekundäres Sjögren-Syndrom) auftreten. Das Sjögren-Syndrom kann mit anderen Autoimmunkrankheiten wie rheumatoider Arthritis (RA), systemischem Lupus erythematosus (SLE) oder systemischer Sklerose einhergehen. Die daraus resultierende Entzündung führt zu einer fortschreitenden Schädigung der Drüsen. Die Diagnose erfolgt durch eine Biopsie der feuchtigkeitsproduzierenden Drüsen und einen Bluttest auf spezifische Antikörper. Bei der Biopsie finden sich typischerweise Lymphozyten in den Drüsen. ⓘ
Das Sjögren-Syndrom ist zwar eine der häufigsten Autoimmunerkrankungen, aber es gibt keine spezifischen und nicht-invasiven diagnostischen Tests, und die Behandlung zielt darauf ab, die Symptome der Betroffenen zu behandeln. Bei trockenen Augen können künstliche Tränen, entzündungshemmende Medikamente, Pünktchenpfropfen oder eine Operation zum Verschluss der Tränenkanäle versucht werden. Bei Mundtrockenheit können Kaugummi (vorzugsweise zuckerfrei), Wasser oder ein Speichelersatzmittel verwendet werden. Bei Gelenk- oder Muskelschmerzen kann Ibuprofen eingesetzt werden. Medikamente, die Trockenheit verursachen können, wie z. B. Antihistaminika, können ebenfalls abgesetzt werden. Der derzeit spezifischste diagnostische Test erfordert eine Lippenbiopsie. ⓘ
Die Krankheit wurde 1933 von Henrik Sjögren beschrieben, nach dem sie auch benannt ist; es gibt jedoch eine Reihe früherer Beschreibungen von Menschen mit diesen Symptomen. Zwischen 0,2 und 1,2 % der Bevölkerung sind betroffen, wobei die Hälfte die primäre Form und die andere Hälfte die sekundäre Form hat. Frauen sind etwa 10-mal so häufig betroffen wie Männer. Obwohl die Krankheit in der Regel im mittleren Alter beginnt, kann jeder betroffen sein. Die Lebenserwartung derjenigen, die keine anderen Autoimmunerkrankungen haben, ist unverändert. ⓘ
| Klassifikation nach ICD-10 ⓘ | |
|---|---|
| M35.0 | Sicca-Syndrom [Sjögren-Syndrom] |
| ICD-10 online (WHO-Version 2019) | |

Das Sjögren-Syndrom [ˈɧøːɡreːn] (auch Dacryo-Sialo-Adenopathia atrophicans genannt) ist eine chronisch verlaufende Autoimmunerkrankung aus dem rheumatischen Formenkreis und der Gruppe der Kollagenosen, bei der bestimmte Immunzellen exokrine Drüsen (besonders die Speicheldrüsen und Tränendrüsen) durch lymphozytäre Infiltration und übermäßige B-Zell-Aktivität angreifen und zu weiteren entzündlichen Veränderungen an inneren Organen und am zentralen Nervensystem führen können. Das Sjögren-Syndrom manifestiert sich in morphologischen Veränderungen der Tränen- und Speicheldrüsen. Die Leitsymptome trockene Augen und Mundtrockenheit (Xerostomie) werden auch als Sicca-Syndrom bezeichnet. Es wird unterschieden zwischen dem primären Sjögren-Syndrom (pSS) und dem sekundären Sjögren-Syndrom (sSS), welches in Begleitung anderer Autoimmunerkrankungen bzw. Kollagenosen auftreten kann, wie Lupus erythematodes, rheumatoider Arthritis oder systemischer Sklerose. Das anfängliche Auftreten einer Sicca-Symptomatik spricht für ein pSS. ⓘ
Die Erkrankung ist nach dem schwedischen Augenarzt Henrik Sjögren benannt, der sie 1933 in seiner Doktorarbeit erstmals beschrieb. ⓘ
Anzeichen und Symptome

Das charakteristische Symptom des Sjögren-Syndroms ist Mundtrockenheit und Keratokonjunktivitis sicca (trockene Augen). Auch Scheidentrockenheit, trockene Haut und trockene Nase können auftreten. Auch andere Organe des Körpers können betroffen sein, darunter die Nieren, die Blutgefäße, die Lunge, die Leber, die Bauchspeicheldrüse und das Gehirn. ⓘ
Die Trockenheit der Haut kann bei einigen Menschen mit SS auf eine lymphozytäre Infiltration der Hautdrüsen zurückzuführen sein. Die Symptome können sich schleichend entwickeln, wobei die Diagnose oft mehrere Jahre lang nicht in Betracht gezogen wird, weil die Sicca auf Medikamente, eine trockene Umgebung oder das Altern zurückgeführt oder als nicht so schwerwiegend angesehen wird, dass der für die Feststellung der zugrunde liegenden Autoimmunerkrankung erforderliche Untersuchungsaufwand gerechtfertigt ist. ⓘ
Das Sjögren-Syndrom kann lebenswichtige Organe schädigen, wobei die Symptome, wie bei anderen Autoimmunkrankheiten, abklingen oder sich verschlimmern können oder in Remission gehen. Manche Menschen leiden nur unter leichten Symptomen wie trockenen Augen und trockenem Mund, während andere Symptome einer schweren Erkrankung aufweisen. Viele Patienten können die Probleme symptomatisch behandeln. Andere leiden unter verschwommenem Sehen, ständigen Augenbeschwerden, wiederkehrenden Mundinfektionen, geschwollenen Ohrspeicheldrüsen, Dysphonie (Stimmstörungen einschließlich Heiserkeit) und Schwierigkeiten beim Schlucken und Essen. Lähmende Müdigkeit und Gelenkschmerzen können die Lebensqualität erheblich beeinträchtigen. Bei einigen Patienten kann es zu einer Nierenbeteiligung (autoimmune tubulointerstitielle Nephritis) kommen, die zu Proteinurie (überschüssiges Eiweiß im Urin), Konzentrationsstörungen im Urin und distaler renaler tubulärer Azidose führt. ⓘ
Eine hypokaliämische Lähmung aufgrund des primären Sjögren-Syndroms wurde in der Literatur selten beschrieben. ⓘ
Komplikationen
Zu den oben genannten Komplikationen gehört, dass Frauen mit Anti-Ro/SS-A- und Anti-La/SS-B-Antikörpern, die schwanger werden, eine erhöhte Rate an neonatalem Lupus erythematodes mit angeborenem Herzblock aufweisen, der einen Herzschrittmacher erfordert. Die Kryoglobulinämie Typ I ist eine bekannte Komplikation des Sjögren-Syndroms. ⓘ
Das Sjögren-Syndrom kann Organe wie die Leber, die Bauchspeicheldrüse, die Nieren, die Lunge und das zentrale Nervensystem befallen. ⓘ
Assoziierte Erkrankungen
Das Sjögren-Syndrom tritt in Verbindung mit einer Reihe anderer Erkrankungen auf, von denen viele Autoimmun- oder rheumatische Erkrankungen sind, z. B. Zöliakie, Fibromyalgie, SLE (Lupus), Autoimmunthyreoiditis, Multiple Sklerose und Spondyloarthropathie sowie verschiedene bösartige Erkrankungen, vor allem das Non-Hodgkin-Lymphom. ⓘ
Ursachen
Die Ursache des Sjögren-Syndroms ist nicht bekannt, aber wie bei vielen anderen Autoimmunkrankheiten kann es sich um eine Kombination aus genetischen, umweltbedingten und anderen Faktoren handeln. Etwa 20 Autoantikörper könnten daran beteiligt sein. ⓘ
Genetik
Die Beobachtung einer hohen Rate von Autoimmunerkrankungen in Familien mit einer Vorgeschichte des Sjögren-Syndroms wird mit einer genetischen Veranlagung für das Syndrom in Verbindung gebracht. Studien über die Polymorphismen der Genregionen der humanen Leukozytenantigene (HLA)-DR und HLA-DQ bei Sjögren-Patienten zeigen eine unterschiedliche Anfälligkeit für das Syndrom, die auf unterschiedliche Arten der daraus resultierenden Autoantikörperproduktion zurückzuführen ist. ⓘ
Hormone
Da das Sjögren-Syndrom sehr häufig bei Frauen auftritt, geht man davon aus, dass Sexualhormone, insbesondere Östrogen, die humorale und zellvermittelte Immunantwort beeinflussen und damit die Anfälligkeit für das Syndrom beeinflussen. Es wird allgemein angenommen, dass Androgene die Autoimmunität verhindern. Studien an Mäusen deuten darauf hin, dass Östrogenmangel die Präsentation von Autoantigenen stimuliert und so Sjögren-ähnliche Symptome hervorruft. ⓘ
Mikrochimärismus
Mikrochimärismus von fötalen Zellen (Lymphoidzellen des Nachwuchses im mütterlichen Kreislauf) kann bei Frauen, die zuvor schwanger waren, Autoimmunität auslösen. Die Entstehung eines Autoimmunpotenzials durch Mikrochimärismus kann zu einem Wechsel von einer stillen Form der Autoimmunität mit altersabhängiger Abnahme der Selbsttoleranz führen. ⓘ
Umwelt
Virale Proteine, verschlungene Moleküle oder abgebaute eigene Strukturen können durch molekulare Mimikry eine Autoimmunität auslösen und die Wahrscheinlichkeit der Entwicklung des Sjögren-Syndroms erhöhen. Das Epstein-Barr-Virus, Hepatitis C und das humane T-Zell-Leukämie-Virus-1 gehören zu den am besten untersuchten infektiösen Erregern des Sjögren-Syndroms. Bislang konnte kein direkter Zusammenhang zwischen diesen Erregern und der Entwicklung des Sjögren-Syndroms festgestellt werden. Geschädigte Selbststrukturen, die für die Apoptose vorgesehen sind, können fälschlicherweise dem Immunsystem ausgesetzt werden und so eine Autoimmunität in exokrinen Drüsen auslösen, die häufig zu Autoimmunreaktionen neigen. ⓘ
Pathogenese
Die pathogenetischen Mechanismen des Sjögren-Syndroms sind noch nicht vollständig geklärt, so dass die Pathophysiologie bei der Behandlung dieser autoimmunen Exokrinopathie nicht bekannt ist. Obwohl die zahlreichen Faktoren, die zum Fortschreiten dieser Krankheit beitragen, die Entdeckung des genauen Ursprungs und der Ursache erschweren, haben wichtige Fortschritte in den letzten zehn Jahren dazu beigetragen, dass eine Reihe von pathogenen Ereignissen vorgeschlagen wurde, die vor der Diagnose des Sjögren-Syndroms auftreten. ⓘ
Ursprünglich wurde das Sjögren-Syndrom als ein spezifischer, sich selbst erhaltender, durch das Immunsystem vermittelter Verlust von exokrinen Drüsen, insbesondere von azinären und duktalen Zellen, beschrieben. Dies erklärt zwar die offensichtlichen Symptome (z. B. das Fehlen von Speichel und Tränenflüssigkeit), nicht aber die weit verbreiteten systemischen Auswirkungen, die beim Fortschreiten der Krankheit auftreten. ⓘ
Es wird angenommen, dass sowohl Umwelt- als auch hormonelle Faktoren bei Vorhandensein eines anfälligen genetischen Hintergrunds die Infiltration von Lymphozyten, insbesondere CD4+ T-Zellen, B-Zellen und Plasmazellen, auslösen können, was zu Drüsenfunktionsstörungen in den Speichel- und Tränendrüsen führt. ⓘ
Das Sjögren-Syndrom geht mit erhöhten Konzentrationen von IL-1RA, einem Interleukin-1-Antagonisten, im Liquor (Liquor cerebrospinalis) einher. Dies lässt vermuten, dass die Krankheit mit einer erhöhten Aktivität des Interleukin-1-Systems beginnt, gefolgt von einer autoregulatorischen Hochregulierung von IL-1RA, um die erfolgreiche Bindung von Interleukin 1 an seine Rezeptoren zu verringern. Interleukin 1 ist wahrscheinlich der Marker für Müdigkeit, aber eine erhöhte IL-1RA-Konzentration wird im Liquor beobachtet und ist mit erhöhter Müdigkeit durch zytokininduziertes Krankheitsverhalten verbunden. Das Sjögren-Syndrom ist jedoch durch einen verminderten IL-1RA-Spiegel im Speichel gekennzeichnet, der für die Entzündung und Trockenheit im Mund verantwortlich sein könnte. Patienten mit sekundärem Sjögren-Syndrom weisen häufig auch Anzeichen und Symptome ihrer primären rheumatischen Erkrankungen auf, wie systemischer Lupus erythematodes, rheumatoide Arthritis oder systemische Sklerose. ⓘ
Genetische Veranlagung
Der genetische Locus, der am stärksten mit dem primären SS assoziiert ist, ist die Region des Haupthistokompatibilitätskomplexes/Humanleukozytenantigens (MHC/HLA), wie die vorläufigen Ergebnisse der ersten genomweiten Assoziationsstudie zeigen. Diese Studie umfasste Daten aus einer Entdeckungskohorte von 395 Patienten europäischer Abstammung mit primärem Sjögren-Syndrom und 1 975 gesunden Kontrollpersonen sowie aus einer Replikationsstudie, die 1 234 Fälle und 4 779 gesunde Kontrollpersonen umfasste. Es wurden auch Assoziationen mit Polymorphismen an sechs unabhängigen Loci festgestellt: IRF5, STAT4, BLK, IL12A, TNIP1 und CXCR5. Dies deutet auch auf eine Aktivierung des angeborenen Immunsystems hin, insbesondere durch das IFN-System, eine B-Zell-Aktivierung durch CXCR5-gesteuerte Rekrutierung zu lymphatischen Follikeln und B-Zell-Rezeptor (BCR)-Aktivierung unter Beteiligung von BLK sowie eine T-Zell-Aktivierung aufgrund der HLA-Anfälligkeit und der IL-12-IFN-γ-Achse. ⓘ
Patienten unterschiedlicher ethnischer Herkunft tragen unterschiedliche HLA-Empfindlichkeitsallele, von denen HLA-DR und HLA-DQ an der Pathogenese des Sjögren-Syndroms beteiligt sind. So weisen beispielsweise Patienten aus Nord- und Westeuropa sowie aus Nordamerika eine hohe Prävalenz der Gene B8, DRw52 und DR3 auf. HLA-Klasse-II-Allele werden eher mit dem Vorhandensein bestimmter Untergruppen von Autoantikörpern in Verbindung gebracht als mit der Krankheit selbst. Autoantikörper beziehen sich auf den Verlust der B-Zell-Toleranz, der zur Produktion von Antikörpern führt, die gegen verschiedene organspezifische und organnonspezifische Antigene gerichtet sind. Ein Zusammenhang zwischen HLA und SS besteht nur bei Patienten mit Anti-SSA/Ro oder Anti-SSB/La-Antikörpern. Eine Seropositivität für Anti-Ro und Anti-La wird mit einem höheren Schweregrad und einer längeren Krankheitsdauer in Verbindung gebracht, und die Entdeckung ihrer großen Menge in den Speicheldrüsen von Sjögren-Patienten deutet darauf hin, dass sie eine entscheidende Rolle bei der Pathogenese von SS spielen. ⓘ
Neben der Genetik spielen epigenetische Anomalien im Zusammenhang mit der DNA-Methylierung, der Histon-Acetylierung oder der mikroRNA-Expression wahrscheinlich eine Schlüsselrolle bei der Pathogenese von Autoimmunerkrankungen, einschließlich des Sjögren-Syndroms, obwohl die Forschung in diesem Bereich sehr begrenzt ist. ⓘ
Umweltbedingte Auslöser
Umweltfaktoren, wie z. B. virale Drüseninfektionen, könnten Epithelzellen dazu veranlassen, das HLA-unabhängige angeborene Immunsystem über Toll-like-Rezeptoren zu aktivieren. Obwohl eine Reihe infektiöser, exogener Erreger wie das Epstein-Barr-Virus (EBV), das humane T-lymphotrope Virus 1 und das Hepatitis-C-Virus in die Pathogenese des Sjögren-Syndroms einbezogen wurden, scheint ihr Zusammenhang mit dem Sjögren-Syndrom nur schwach ausgeprägt. Während EBV in den Speicheldrüsen normaler Menschen vorkommt, wurde eine hohe Inzidenz von EBV-Reaktivierung bei Sjögren-Patienten mit erhöhten EBV-DNA-Werten berichtet. Dies deutet auf eine virale Reaktivierung und die Unfähigkeit der lymphatischen Infiltrate hin, die EBV-Replikation beim Sjögren-Syndrom zu kontrollieren, was zur Auslösung oder Aufrechterhaltung einer Immunreaktion in den Zielorganen führt. Wie genau die Reaktivierung von EBV in den Läsionen von Patienten mit Sjögren-Syndrom ausgelöst wird und welche spezifischen molekularen Mechanismen an dem Prozess der viralen Reaktivierung beteiligt sind, muss jedoch noch geklärt werden. ⓘ
Entzündung
Epithelzellen in Läsionen des Sjögren-Syndroms sind aktiv an der Auslösung und Aufrechterhaltung des Entzündungsprozesses beteiligt. Es wird angenommen, dass Umwelt- und Hormonfaktoren in Verbindung mit einem entsprechenden genetischen Hintergrund das Sjögren-Syndrom auslösen, das die Epithelzellen dysreguliert und eine abnorme Ansiedlung und Aktivierung von dendritischen Zellen (DCs), T-Zellen und B-Zellen ermöglicht. Dendritische Zellen sind Antigen-präsentierende Zellen, die Antigenmaterial verarbeiten und es anderen T-Zellen präsentieren. Nach der Wanderung von Lymphozyten in die Drüsen als Reaktion auf Chemokine und spezifische Adhäsionsmoleküle interagieren T-Zellen mit Epithelzellen. Epithelzellen werden durch proinflammatorische Zytokine (IL-1β, IFN-γ und TNF), die von benachbarten T-Zellen produziert werden, weiter aktiviert. Die frühe Anhäufung plasmazytoider dendritischer Zellen in den Zielgeweben, die hohe Mengen an Typ-1-IFN produzieren, scheint wichtig zu sein, da diese Zellen die Immunreaktion durch abnormale Retention von Lymphozyten in den Geweben und deren anschließende Aktivierung weiter dysregulieren können. IFN-α stimuliert die Produktion des B-Zell-aktivierenden Faktors (BAFF) durch Epithelzellen, DCs und T-Zellen. BAFF stimuliert eine abnorme B-Zell-Reifung, die zur Entstehung selbstreaktiver B-Zellen führt, die lokal Autoantikörper produzieren, und zwar in einer Keimzentrums-ähnlichen Struktur (GC-like), die auch der Ort der Lymphomagenese ist (Ursprung des Lymphoms). ⓘ
Programmierter Zelltod
Es wird vermutet, dass eine Dysregulation der Apoptose (programmierter Zelltod) bei der Pathogenese einer Reihe von Autoimmunerkrankungen eine Rolle spielt, ihre Rolle beim Sjögren-Syndrom ist jedoch umstritten. Sowohl die Fas- als auch die Fas-Ligand-Proteine sind bei primären Sjögren-Patienten überexprimiert, während die Expression von BCL-1, von dem bekannt ist, dass es die Apoptose herunterreguliert, in azinären und duktalen Epithelzellen von Sjögren-Patienten im Vergleich zu Gesunden deutlich reduziert war. In-situ-Untersuchungen ergaben keine erhöhte Apoptose bei Drüsenepithelzellen, wohl aber eine verringerte Apoptose bei infiltrierenden mononukleären Zellen. Die verringerte Apoptose wurde auch mit der Anhäufung von autoreaktiven B-Zellen in den Drüsen in Verbindung gebracht. Der Zusammenhang zwischen den beim Sjögren-Syndrom exprimierten Autoantikörpern und der Apoptose wird noch erforscht. ⓘ
Hormonelle Faktoren
Geschlechtshormone scheinen die humorale und zellvermittelte Immunantwort zu beeinflussen, wobei Östrogen als einer der wichtigsten Faktoren für den geschlechtsimmunologischen Dimorphismus gilt. Östrogenmangel scheint eine Rolle bei der Entwicklung des Sjögren-Syndroms zu spielen. Es wurde die Hypothese aufgestellt, dass die Verabreichung von Androgenen an die Augenoberfläche eine wirksame Therapie für trockene Augen darstellen könnte. ⓘ
Diagnose

Die Diagnose des Sjögren-Syndroms (SS) wird durch die Vielfalt der Symptome erschwert, die ein Patient zeigen kann, und durch die Ähnlichkeit der Symptome des Sjögren-Syndroms mit denen anderer Erkrankungen. Außerdem wenden sich Patienten mit SS-Symptomen zur Behandlung an verschiedene Fachrichtungen, was die Diagnose erschweren kann. Da trockene Augen und ein trockener Mund sehr häufige Symptome sind und häufig bei Menschen über 40 Jahren auftreten, glauben die Betroffenen vielleicht, dass die Symptome altersbedingt sind, und ignorieren sie. Einige Medikamente können Symptome hervorrufen, die denen des Sjögren-Syndroms ähneln. Die Kombination mehrerer Tests, die in einer Reihe durchgeführt werden können, kann schließlich die Diagnose des Sjögren-Syndroms stellen. ⓘ
Mit Hilfe von Bluttests kann festgestellt werden, ob ein Patient hohe Werte von Antikörpern aufweist, die auf die Erkrankung hinweisen, wie z. B. antinukleäre Antikörper (ANA) und Rheumafaktor (da das Sjögren-Syndrom häufig sekundär zu rheumatoider Arthritis auftritt), die mit Autoimmunerkrankungen in Verbindung gebracht werden. Typische ANA-Muster beim SS sind SSA/Ro und SSB/La, wobei Anti-SSB/La weitaus spezifischer ist. Anti-SSA/Ro wird mit zahlreichen anderen Autoimmunerkrankungen in Verbindung gebracht, ist aber häufig beim SS vorhanden, während Anti-SSA- und Anti-SSB-Tests beim SS häufig nicht positiv sind. ⓘ
Der Rosenbengaltest verwendet eine Färbung, die den Zustand und die Funktion der Tränendrüsen misst. Bei diesem Test wird der ungiftige Farbstoff Bengalrosa auf die Augen aufgetragen. Die charakteristische Farbe des Farbstoffs hilft bei der Bestimmung des Zustands und der Funktion des Tränenfilms sowie der Verdunstungsrate der Tränen. Jede auffällige Farbveränderung kann auf SS hindeuten, aber zur Bestätigung der Erkrankung sind viele verwandte diagnostische Hilfsmittel erforderlich. ⓘ
Mit dem Schirmer-Test wird die Tränenproduktion gemessen: Ein Filterpapierstreifen wird fünf Minuten lang in das untere Augenlid gehalten und dann mit einem Lineal auf seine Nässe hin untersucht. Wenn weniger als 5 mm Flüssigkeit produziert wird, ist dies in der Regel ein Anzeichen für SS. Diese Messanalyse variiert von Person zu Person, abhängig von anderen Augenerkrankungen und den Medikamenten, die zum Zeitpunkt des Tests eingenommen werden. Eine Spaltlampenuntersuchung kann Trockenheit auf der Oberfläche des Auges aufzeigen. ⓘ
Die Symptome von Mundtrockenheit und Trockenheit in der Mundhöhle werden durch eine verminderte Speichelproduktion der Speicheldrüsen (Ohrspeicheldrüse, Unterkieferdrüse und Unterzungendrüse) verursacht. Um den Zustand der Speicheldrüsen und die Speichelproduktion zu überprüfen, wird ein Speichelflusstest durchgeführt, bei dem die Person aufgefordert wird, so viel wie möglich in einen Becher zu spucken, und die daraus resultierende Speichelprobe wird gesammelt und gewogen. Anhand der Ergebnisse dieses Tests kann festgestellt werden, ob die Speicheldrüsen ausreichend funktionieren. Wird nicht genügend Speichel produziert, könnte dies bedeuten, dass die Person an SS leidet. Ein alternativer Test ist die nicht stimulierte Sammlung des gesamten Speichelflusses, bei der die Person 15 Minuten lang jede Minute in ein Reagenzglas spuckt. Ein Ergebnis von weniger als 1,5 ml (0,053 imp fl oz; 0,051 US fl oz) wird als positives Ergebnis gewertet. ⓘ
| Grad | Lymphozyten ⓘ |
|---|---|
| 1 | Leichtes Infiltrat |
| 2 | Mäßiges Infiltrat oder weniger als ein Herd* |
| 3 | Ein Herd* |
| 4 | Mehr als ein Herd* |
| * Fokus = ein Aggregat von 50 Lymphozyten oder mehr. | |
Bei einer Lippen-/Speicheldrüsenbiopsie wird eine Gewebeprobe entnommen, die Lymphozyten um die Speicheldrüsen herum und Schäden an diesen Drüsen durch Entzündungen aufzeigen kann. Bei diesem Test wird eine Gewebeprobe aus der inneren Lippe/Speicheldrüse einer Person entnommen und unter einem Mikroskop untersucht. Bei solchen Biopsien ist das wichtigste Testergebnis für die Diagnose der oralen Komponente des Sjögren-Syndroms wahrscheinlich der Fokus-Score, d. h. die Anzahl der mononukleären Zellinfiltrate mit mindestens 50 Entzündungszellen in einem 4 mm2 großen Drüsenabschnitt. Die Chisholm-Mason-Grade werden auch häufig für Speicheldrüsenbiopsien verwendet (siehe Tabelle). ⓘ
Als zuverlässiger und genauer Test für das Sjögren-Syndrom steht ein radiologisches Verfahren in Form eines Sialogramms zur Verfügung. Dabei wird ein Kontrastmittel in den Ohrspeicheldrüsengang gespritzt, der von der Wange in den Mundvorhof gegenüber dem Hals des oberen zweiten Backenzahns mündet. Der Test dient dazu, eine eventuelle Verstopfung der Speicheldrüsengänge (d. h. des Ohrspeicheldrüsengangs) und die Menge des in den Mund fließenden Speichels festzustellen. ⓘ
Beim Sjögren-Syndrom kann die elektrochemische Messung der Hautleitfähigkeit die Diagnose der Sudomotorik unterstützen. ⓘ
Das Sjögren-Syndrom kann bei Personen mit einer früheren Strahlentherapie im Kopf- und Halsbereich, einem erworbenen Immundefizienzsyndrom, einem vorbestehenden Lymphom, einer Sarkoidose, einer Graft-versus-Host-Krankheit und der Einnahme von Anticholinergika ausgeschlossen werden. ⓘ

Das Sjögren-Syndrom kann – wie auch andere Kollagenosen – im Blut zum Abfall verschiedener Zellreihen sowie zu hohen Antinukleären-Antikörper-Werten (ANA) oder Rheumafaktor führen. Durch die Entzündung kommt es zum Anstieg der Blutkörperchensenkungsgeschwindigkeit (BSG) und des C-reaktiven Proteins (CRP). Als unspezifisches Zeichen kann es auch zu Leukopenie, Anämie und Thrombozytopenie kommen. Spezifisch sind aber ss-A- und ss-B-Autoantikörper bei bis zu 70 % der Patienten sowie manchmal Antikörper gegen Epithelzellen der Ausführungsgänge der Speicheldrüsen. Zur Diagnosesicherung kann eine Biopsie von der Lippeninnenseite entnommen werden. In dem Bioptat ist eine Drüsenentzündung mit Lymphozyteninfiltration zu sehen. ⓘ
Regelmäßige augenärztliche Kontrollen sind ratsam. Zu erwähnen ist der Schirmer-Test, bei dem mit einem Löschpapier die Produktion der Tränenflüssigkeit im Auge geprüft wird. Bei Sjögren-Syndrom bleibt das Löschpapier trocken. ⓘ
Vorbeugung
Aufgrund der Komplexität des Sjögren-Syndroms (SS) als Autoimmunerkrankung gibt es keine Präventionsmechanismen, aber eine Änderung des Lebensstils kann die Risikofaktoren für die Entwicklung von SS reduzieren oder den Schweregrad der Erkrankung bei Patienten, bei denen bereits eine Diagnose gestellt wurde, verringern. Die Ernährung steht in engem Zusammenhang mit den Entzündungen, die bei vielen Autoimmunkrankheiten, einschließlich SS, auftreten. Eine experimentelle Studie kam zu dem Schluss, dass SS-Patienten häufig eine hohe Empfindlichkeit gegenüber Gluten aufweisen, die in direktem Zusammenhang mit Entzündungen steht. Mäßige körperliche Betätigung ist bei SS-Patienten ebenfalls hilfreich, vor allem um die Auswirkungen der Lungenentzündung zu verringern. ⓘ
Behandlung
Eine kausale Behandlung des Sjögren-Syndroms ist nicht bekannt, eine Standardtherapie ist nicht gesichert. Die Prognose ist, insbesondere beim sekundären Sjögren-Syndrom, meist gut. Es werden Therapieansätze verwendet, die auch für andere Autoimmunerkrankungen Verwendung finden. Es können die Symptome gelindert werden: Sorgfältige Mundhygiene, ausreichend Flüssigkeitszufuhr, Gabe von künstlichem Speichel, Lichtschutz der Augen, Augentropfen („künstliche Tränenflüssigkeit“), bei Notwendigkeit Zahnimplantate. Eine mögliche Mykose der Mundschleimhaut wird mit Antimykotika behandelt. Medikamentös werden je nach Manifestation eingesetzt: Kortikosteroide (etwa Prednisolon bei Nieren- oder Lungenbeteiligung sowie systemischer Vaskulitis), NSAID, Hydroxychloroquin, Pirfenidon, Nintedanib, Antidepressiva, Rituximab, Plasmapherese. Von manchen Betroffenen wird zur Verstärkung des Speichelflusses das cholinerge Parasympathomimetikum Pilocarpin eingenommen. Seltene Komplikationen wie Lungen- oder Nierenentzündung können eine intensivmedizinische Behandlung erforderlich machen. ⓘ
Es ist weder eine Heilung noch eine spezifische Behandlung des Sjögren-Syndroms bekannt, die die Drüsensekretion dauerhaft wiederherstellt. Stattdessen ist die Behandlung im Allgemeinen symptomatisch und unterstützend. ⓘ
Augenpflege
Feuchtigkeitsersatztherapien wie künstliche Tränen können die Symptome von trockenen Augen lindern. Einige Patienten mit schwereren Problemen verwenden Schutzbrillen, um die lokale Luftfeuchtigkeit zu erhöhen, oder lassen sich Pünktchen einsetzen, um die Tränen länger auf der Augenoberfläche zu halten. ⓘ
Darüber hinaus ist Cyclosporin (Restasis) auf Rezept erhältlich, um chronisch trockene Augen zu behandeln, indem die Entzündung unterdrückt wird, die die Tränensekretion stört. Es gibt auch verschreibungspflichtige Medikamente, die den Speichelfluss anregen, z. B. Cevimelin (Evoxac) und Pilocarpin. Salagen, eine hergestellte Form von Pilocarpin, kann die Produktion von Tränen sowie von Speichel im Mund und im Darm anregen. Es wird aus der Jaborandi-Pflanze gewonnen. ⓘ
Trockenheit in der Scheide
Bei Frauen mit Sjögren-Syndrom wird häufig über Scheidentrockenheit, Vulvodynie und Dyspareunie (schmerzhafter Geschlechtsverkehr) berichtet; es werden persönliche Gleitmittel empfohlen, um Reizungen oder Schmerzen zu lindern, die durch Trockenheit im Vaginal- und Vulvabereich entstehen können. ⓘ
Muskel-Skelett-Erkrankungen
Nichtsteroidale Antirheumatika (NSAIDs) können zur Behandlung von Symptomen des Bewegungsapparats eingesetzt werden. Bei Personen mit schweren Komplikationen können Kortikosteroide oder Immunsuppressiva verschrieben werden, manchmal auch intravenöse Immunglobuline. Auch krankheitsmodifizierende Antirheumatika wie Methotrexat können hilfreich sein. Hydroxychloroquin (Plaquenil) ist eine weitere Option und gilt im Allgemeinen als sicherer als Methotrexat. Diese verschriebenen Medikamente haben jedoch eine Reihe von Nebenwirkungen wie Übelkeit, Appetitlosigkeit, Schwindel, Haarausfall, Magenschmerzen/-krämpfe, Kopfschmerzen, Lebertoxizität und ein erhöhtes Infektionsrisiko. Außerdem besteht bei Menschen, die Medikamente zur Unterdrückung des Immunsystems einnehmen, ein höheres Risiko, später an Krebs zu erkranken. ⓘ
Systemisch
Bei systemischen Symptomen wie Müdigkeit, Gelenkschmerzen, Myositis und Neuropathie werden häufig biologische Immunsuppressiva wie Rituximab und Belimumab eingesetzt, die über die B-Zell-Pathologie wirken und ein weniger toxisches Profil aufweisen als herkömmliche immunsuppressive Therapien. ⓘ
Zahnmedizinische Versorgung
Auch eine vorbeugende zahnärztliche Behandlung ist notwendig (und wird von den Patienten oft übersehen), da der mit der Xerostomie verbundene Speichelmangel ein ideales Umfeld für die Vermehrung von Bakterien schafft, die Karies verursachen. Zu den Behandlungen gehören die Anwendung von Fluorid zu Hause, um den Zahnschmelz zu stärken, und regelmäßige Zahnreinigungen durch eine Zahnhygienikerin. Bestehende Karies muss ebenfalls behandelt werden, da Karies, die in den Zahn hineinreicht, durch Zahnreinigung allein nicht wirksam behandelt werden kann und ein hohes Risiko besteht, dass sie sich auf das Zahnmark ausbreitet, was zum Verlust der Vitalität führt und eine Extraktion oder Wurzelbehandlung erforderlich macht. Dieses Behandlungsschema gilt für alle Xerostomie-Patienten, z. B. für Patienten, die sich einer Strahlentherapie im Kopf- und Halsbereich unterziehen, bei der die Speicheldrüsen häufig geschädigt werden; diese Drüsen sind für Strahlung empfindlicher als andere Körpergewebe. ⓘ
Prognose
Die veröffentlichten Studien über das Überleben von Patienten mit Sjögren-Syndrom sind in verschiedener Hinsicht begrenzt, was vielleicht auf die relativ kleinen Stichprobengrößen und die Tatsache zurückzuführen ist, dass das sekundäre Sjögren-Syndrom mit anderen Autoimmunerkrankungen einhergeht. Die Ergebnisse einer Reihe von Studien deuten darauf hin, dass das Sjögren-Syndrom im Vergleich zu anderen Autoimmunerkrankungen mit einer auffallend hohen Inzidenz des malignen Non-Hodgkin-Lymphoms, einer Krebserkrankung der weißen Blutkörperchen, verbunden ist. Etwa 5 % der Patienten mit SS entwickeln eine Form von bösartigem Lymphdrüsenkrebs. Bei Patienten mit schwerer SS ist die Wahrscheinlichkeit, ein Lymphom zu entwickeln, wesentlich höher als bei Patienten mit leichter oder mittelschwerer SS. Die häufigsten Lymphome sind extranodale Marginalzonen-B-Zell-Lymphome der Speicheldrüse (MALT-Lymphome in den Speicheldrüsen) und diffuse große B-Zell-Lymphome. ⓘ
Die Lymphomgenese bei Patienten mit primärem Sjögren-Syndrom wird als mehrstufiger Prozess betrachtet, wobei der erste Schritt die chronische Stimulation von autoimmunen B-Zellen ist, insbesondere von B-Zellen, die an den von der Krankheit betroffenen Stellen Rheumafaktor produzieren. Dadurch erhöht sich die Häufigkeit onkogener Mutationen, die dazu führen, dass eine Fehlfunktion an den Kontrollpunkten der autoimmunen B-Zell-Aktivierung in Malignität umschlägt. Eine Studie kommt zu dem Schluss, dass die kontinuierliche Stimulierung der autoimmunen B-Zellen zu subtilen Keimanomalien in Genen führt, die spezifische Auswirkungen auf die B-Zellen haben, was die Anfälligkeit für Lymphome begründet. ⓘ
Abgesehen von dieser deutlich höheren Inzidenz bösartiger NHL zeigen Sjögren-Patienten nur bescheidene oder klinisch unbedeutende Verschlechterungen spezifischer organbezogener Funktionen, was die nur geringfügig erhöhte Sterblichkeitsrate von Sjögren-Patienten im Vergleich zur übrigen Bevölkerung erklärt. ⓘ
Das Sjögren-Syndrom ist mit einer hohen Krankheitslast verbunden und führt nachweislich zu einer deutlichen Beeinträchtigung der Lebensqualität (LQ), wobei die Arbeitsfähigkeit durch eine erhöhte Erwerbsunfähigkeit erheblich beeinträchtigt wird. Die Beeinträchtigung der Lebensqualität ist ähnlich wie bei anderen chronischen Erkrankungen wie rheumatoider Arthritis, Lupus und Fibromyalgie. ⓘ
Epidemiologie
Das Sjögren-Syndrom (SS) ist die zweithäufigste rheumatische Autoimmunerkrankung nach der rheumatoiden Arthritis und dem systemischen Lupus erythematodes. Es gibt keine geografischen Unterschiede in der Häufigkeit des SS. Über das Sjögren-Syndrom wurde in allen Regionen der Welt berichtet, obwohl die regionalen Raten nicht gut untersucht wurden. Je nach den Kriterien für die Bestimmung der Prävalenz schätzen Studien die Prävalenz des SS auf 500.000 bis zwei Millionen Menschen in den Vereinigten Staaten. Breitere Studien über die Prävalenz von SS gehen weit auseinander, wobei einige Berichte von einer Prävalenz von bis zu 3 % der Bevölkerung ausgehen. Einige wenige Studien berichten, dass die Inzidenz des Syndroms zwischen drei und sechs pro 100.000 Menschen pro Jahr schwankt. ⓘ
Neun von 10 SS-Patienten sind Frauen. Neben der Prävalenz bei Frauen wurden ein Verwandter ersten Grades mit einer Autoimmunerkrankung und frühere Schwangerschaften als epidemiologische Risikofaktoren ermittelt. Trotz des geringeren Risikos für Männer stellt die primäre SS bei Männern tendenziell eine schwerere Form der Erkrankung dar. Die Rolle von Rasse und ethnischer Zugehörigkeit bei der Prävalenz der Krankheit ist unbekannt. ⓘ
Obwohl das Sjögren-Syndrom in allen Altersgruppen auftritt, liegt das Durchschnittsalter für den Ausbruch der Krankheit zwischen 40 und 60 Jahren, obwohl bis zur Hälfte aller Fälle nicht diagnostiziert oder nicht gemeldet werden. Die Prävalenz des SS nimmt im Allgemeinen mit dem Alter zu. ⓘ
Das Sjögren-Syndrom wird bei 30-50 % der Menschen mit rheumatoider Arthritis und bei 10-25 % mit systemischem Lupus erythematodes festgestellt. ⓘ
Vorgeschichte
Jan Mikulicz-Radecki (1850-1905) wird allgemein die Erstbeschreibung der SS zugeschrieben. Im Jahr 1892 beschrieb er einen 42-jährigen Mann mit einer Vergrößerung der Ohrspeicheldrüse und der Tränendrüse in Verbindung mit einem Rundzellinfiltrat und einer Azinusatrophie. Die Kriterien, die Mikulicz für die Diagnose aufstellte, führten jedoch häufig zu Fehldiagnosen des Mikulicz-Syndroms. Viele Erkrankungen wie Tuberkulose, Infektionen, Sarkoidose und Lymphome weisen ähnliche Symptome auf, wie sie dem Mikulicz-Syndrom zugeschrieben werden. Dennoch wird der Begriff "Mikulicz-Syndrom" gelegentlich noch verwendet, um das Auftreten von lymphozytären Infiltraten in Speicheldrüsenbiopsien zu beschreiben. ⓘ
1930 beobachtete Henrik Sjögren (1899-1986), Augenarzt im schwedischen Jönköping, einen Patienten mit geringer Sekretion aus den Tränen- und Speicheldrüsen. Sjögren führte den Begriff Keratokonjunktivitis sicca für das Symptom der trockenen Augen (Keratoconjunctivitis) ein. Im Jahr 1933 veröffentlichte er seine Doktorarbeit, in der er 19 Frauen beschrieb, von denen die meisten postmenopausal waren und an Arthritis litten, und die klinische und pathologische Manifestationen des Syndroms zeigten. Sjögren stellte klar, dass die Keratokonjunktivitis sicca, die auf Wassermangel zurückzuführen ist, nichts mit der Xerophthalmie zu tun hat, die auf Vitamin-A-Mangel beruht. Sjögrens Dissertation wurde nicht gut aufgenommen, da die Prüfungskommission einige klinische Aspekte kritisierte. ⓘ
Nach umfangreichen Untersuchungen und Datenerhebungen veröffentlichte Sjögren 1951 eine wichtige Arbeit, in der er 80 Patienten mit Keratokonjunktivitis sicca beschrieb, von denen 50 auch an Arthritis litten. Seine anschließenden Konferenzbesuche im Zusammenhang mit seiner Arbeit führten zu einem internationalen Interesse am Sjögren-Syndrom. Der Begriff Keratokonjunktivitis sicca" wurde von Sjögren selbst geprägt und wurde in der Literatur als Sjögren-Syndrom bezeichnet, obwohl er heute allgemeiner verwendet werden kann. ⓘ
Forschung

Die Forschung zu multifaktoriellen Autoimmunerkrankungen wie dem Sjögren-Syndrom konzentriert sich auf die Erweiterung des Wissens über die Erkrankung, die Verbesserung der Diagnoseinstrumente und die Suche nach Möglichkeiten zur Vorbeugung, Behandlung und Heilung der Erkrankung. Das Primary Sjögren's Syndrome Registry des Vereinigten Königreichs, eine vom Medical Research Council, UK, unterstützte Gewebe-Biobank für Forschungsproben, wurde 2010 eingerichtet. Es unterstützt klinische Studien und genetische Untersuchungen des Sjögren-Syndroms und steht Personen, die an Forschungsstudien teilnehmen möchten, sowie Forschern, die die Krankheit untersuchen, offen. ⓘ
Wie bei anderen Autoimmunkrankheiten wird die Anfälligkeit für das Sjögren-Syndrom stark durch das humane Leukozyten-Antigen beeinflusst. Die Allele DQA1*05:01, DQB1*02:01 und DRB1*03:01 wurden als Risikofaktoren identifiziert, während die Allele DQA1*02:01, DQA1*03:01 und DQB1*05:01 sich als Schutzfaktoren für die Krankheit erwiesen. Es wurde auch ein Zusammenhang zwischen den Allelen und der spezifischen Rasse festgestellt. HLA-DQ2 und HLA-B8 werden im Allgemeinen bei kaukasischen Patienten gefunden, während HLA-DR5 mit griechischen und israelischen Patienten in Verbindung gebracht wird. In Zukunft könnten mehrere genomweite Assoziationsuntersuchungen durchgeführt werden, um wichtige Risikovarianten zu ermitteln. ⓘ
Zu den Viren, die mit dem Sjögren-Syndrom in Verbindung gebracht werden, gehören das humane T-lymphotrope Virus Typ 1 (HTLV-1), das Epstein-Barr-Virus (EBV), das humane Immunschwächevirus (HIV), das Hepatitis-Delta-Virus (HDV) und das Hepatitis-C-Virus (HCV). ⓘ
Einige Untersuchungen haben gezeigt, dass ein Mangel an Vitamin A und Vitamin D mit der Krankheit in Verbindung steht. Es wurde festgestellt, dass ein Vitamin-D-Mangel mit neurologischen Manifestationen und dem Vorhandensein von Lymphomen bei den Patienten zusammenhängt, während der Vitamin-A-Spiegel in umgekehrtem Verhältnis zu den extraglandulären Manifestationen der Krankheit steht. ⓘ
Der Speichel ist ein potenzielles Diagnoseinstrument für das Sjögren-Syndrom, da sich die Speichelkomponente nach Ausbruch der Krankheit verändert. Mit der neuen Miniaturisierungstechnologie, dem so genannten "Lab on a Chip", kann die Diagnose einfacher gestellt werden. ⓘ
Was die Therapeutika betrifft, so wurden 2007 mehrere monoklonale Antikörper untersucht. Am vielversprechendsten schienen der Anti-CD20-Antikörper Rituximab und der Anti-CD22-Antikörper Epratuzumab zu sein, während die Anti-TNF-α- und IFN-α-Antikörper weniger wirksam schienen. ⓘ
Im Jahr 2014 gab die Sjögren-Syndrom-Stiftung das Fünfjahresziel bekannt, die durchschnittliche Zeit bis zur Diagnose der Krankheit zu halbieren. ⓘ
Bemerkenswerte Fälle
- Shannon Boxx (US-amerikanische olympische Fußballspielerin) hat sowohl das Sjögren-Syndrom als auch Lupus.
- Carrie Ann Inaba (Sängerin und Schauspielerin) ist die nationale Botschafterin und Sprecherin der Sjögren-Syndrom-Stiftung.
- Bei Venus Williams (Tennisweltmeisterin) wurde das Sjögren-Syndrom diagnostiziert, und sie sagte, sie habe jahrelang mit Müdigkeit zu kämpfen gehabt.
- Bei Stephen McPhail (Profifußballer für Irland, Leeds und Cardiff City) wurde im Alter von 29 Jahren ein Lymphom und das Sjögren-Syndrom diagnostiziert.
- Bei Halsey (Sängerin) wurden das Sjögren-Syndrom, das Ehlers-Danlos-Syndrom, das Mastzellen-Aktivierungssyndrom und das posturale orthostatische Tachykardiesyndrom diagnostiziert. ⓘ
Assoziation
Das Sjögren-Syndrom kann als eigenständige Erkrankung oder öfter noch als Begleiterscheinung anderer rheumatischer Erkrankungen auftreten: Rheumatoide Arthritis, Lupus erythematodes, Primär sklerosierende Cholangitis, Morbus Bechterew, Raynaud-Syndrom. ⓘ
Nicht selten ist das Sjögren-Syndrom mit einer Autoimmunthyreopathie vergesellschaftet, in 6 % der Fälle auch mit der Entwicklung eines malignen Lymphoms. Noch häufiger kann ein sogenanntes Pseudolymphom auftreten, das histologisch schwer von einem echten Lymphom unterschieden werden kann. ⓘ
Symptome
Allgemeine Symptome
Als Symptome finden sich starke Müdigkeit, Konzentrationsschwäche, Abgeschlagenheit, Depression, Gelenkentzündungen (Arthritis), zuweilen auch Haut-, Nasen- und Vaginaltrockenheit, entzündete Speicheldrüsen und ein Raynaud-Syndrom. Selten können andere Organe wie etwa Nieren, Blutgefäße, Lungen, Leber, Pankreas oder das Gehirn betroffen sein. Durch Exsudate kann es etwa auch zur Bildung von Pleuraergüssen kommen. Weiterhin können die Schleimdrüsen von Rachen, Kehlkopf, Luftröhre und Bronchien betroffen sein. ⓘ
Mund und Rachen
Mundtrockenheit (Xerostomie) wurde bei 94 bis zu 100 % der Sjögren-Patienten festgestellt. 80 % berichten von Problemen im Rachenraum. Späte Manifestationen sind Heiserkeit, Knotenbildung und Stimmbildungsstörungen. ⓘ
Die häufigsten Symptome der Mundschleimhaut bei primärem und sekundärem Sjögren-Syndrom sind:
- Mundwinkelentzündung (Cheilitis angularis)
- Lippenentzündung (Cheilitis)
- Verminderte Lippenfeuchtigkeit
- Unspezifische Ulzerationen, Aphthen und aphtenähnliche Zustände ⓘ
Myalgie, Fibromyalgie und Gelenkschmerzen
Gelenkschmerzen (Arthralgie), Morgensteifheit und Gelenkentzündungen (Arthritis) sind bei Sjögren-Patienten häufig anzutreffen. 40 bis 75 % der Sjögren-Patienten leiden unter Gelenkschmerzen ohne nachweisbare Gelenkentzündung. Bei 33 % der Patienten mit primärem Sjögren-Syndrom wurden Myalgien und bei 47 bis 55 % der Patienten Fibromyalgie festgestellt. ⓘ
Hautbeteiligung
Ein Austrocknen von Haut- und Schleimhautoberflächen sowie spröde, brüchige Haare, Finger- und Fußnägel sind typische Symptome beim Sjögren-Syndrom. Die Hauttrockenheit geht häufig mit Juckreiz einher. Es kann zu einer Ekzembildung auf den Augenlidern kommen, ggfs. mit Fremdkörperwahrnehmung. Es kann zu verschiedenen Formen der Entzündung des Unterhautfettgewebes (Pannikulitis) kommen wie z. B. Erythema nodosum sowie zu Amyloidose. Das Risiko für eine Bildung von Lymphomen ist 6,5- bis 40-fach erhöht. Das Sjögren-Syndrom kann mit subakut kutanem Lupus erythematodes, einer seltenen Form des Lupus erythematodes assoziiert sein. Weiterhin sind im Zusammenhang mit Sjögren-Syndrom Hautveränderungen, die mit rheumatoider Arthritis oder systemischer Sklerose (Bindegewebsverhärtungen) assoziiert sind, möglich. Außerdem kann das Sjögren-Syndrom mit Vaskulitis (Entzündungen von Blutgefäßen durch autoimmunologische Prozesse) einhergehen. ⓘ
Nase, Nasennebenhöhlen und Ohren
Die meisten Studien, die die Prävalenz der Beteiligung der Nase bzw. der Schleimdrüsen der Nase beim Sjögren-Syndrom untersuchen, sind reine Beobachtungsstudien mit unterschiedlichen Ergebnissen. Die häufigsten beobachteten Symptome sind Nasentrockenheit, Krustenbildung, Verstopfung der Nase, verstärkte Geruchswahrnehmung und Nasenbluten. Bekannt ist ein moderater Hörverlust bei hohen Frequenzen. ⓘ