Epstein-Barr-Virus
| Menschliches Gammaherpesvirus 4 ⓘ | |
|---|---|

| |
| Elektronenmikroskopische Aufnahme zweier Epstein-Barr-Virionen (Viruspartikel) mit runden Kapsiden, die locker von der Membranhülle umgeben sind | |
| Virus-Klassifizierung | |
| (ohne Rangfolge): | Virus |
| Bereich: | Duplodnaviria |
| Königreich: | Heunggongvirae |
| Phylum: | Peploviricota |
| Klasse: | Herviviricetes |
| Ordnung: | Herpesvirales |
| Familie: | Herpesviridae |
| Gattung: | Lymphocryptovirus |
| Spezies: | Menschliches Gammaherpesvirus 4
|
| Synonyme | |
| |
Das Epstein-Barr-Virus (EBV), offiziell Humanes Gammaherpesvirus 4 genannt, ist eines der neun bekannten humanen Herpesviren aus der Herpesfamilie und eines der häufigsten Viren beim Menschen. EBV ist ein doppelsträngiges DNA-Virus. ⓘ
Am bekanntesten ist es als Erreger der infektiösen Mononukleose ("Mono" oder "Drüsenfieber"). Es wird auch mit verschiedenen nicht-malignen, prämalignen und malignen Epstein-Barr-Virus-assoziierten lymphoproliferativen Erkrankungen in Verbindung gebracht, wie dem Burkitt-Lymphom, der hämophagozytischen Lymphohistiozytose und dem Hodgkin-Lymphom, nicht-lymphoiden malignen Erkrankungen wie Magenkrebs und Nasopharynxkarzinom sowie Erkrankungen, die mit dem Humanen Immundefizienz-Virus in Verbindung gebracht werden, wie haarige Leukoplakie und Lymphome des zentralen Nervensystems. Das Virus wird auch mit den Kinderkrankheiten Alice-im-Wunderland-Syndrom und akuter zerebellarer Ataxie in Verbindung gebracht, und es gibt Hinweise auf ein erhöhtes Risiko für die Entwicklung bestimmter Autoimmunerkrankungen, insbesondere Dermatomyositis, systemischer Lupus erythematodes, rheumatoide Arthritis und Sjögren-Syndrom. Man geht davon aus, dass etwa 200.000 Krebsfälle pro Jahr weltweit auf EBV zurückzuführen sind. Im Jahr 2022 wies eine große Studie (10 Millionen Menschen über 20 Jahre) darauf hin, dass EBV die Hauptursache für Multiple Sklerose ist, wobei eine kürzlich erfolgte EBV-Infektion das Risiko, an Multipler Sklerose zu erkranken, um das 32-Fache erhöht. ⓘ
Die Infektion mit EBV erfolgt durch die orale Übertragung von Speichel und Genitalsekreten. Die meisten Menschen infizieren sich mit EBV und erlangen eine adaptive Immunität. In den Vereinigten Staaten haben etwa die Hälfte aller fünfjährigen Kinder und etwa 90 % der Erwachsenen Hinweise auf eine frühere Infektion. Säuglinge werden für EBV empfänglich, sobald der mütterliche Antikörperschutz verschwindet. Viele Kinder infizieren sich mit EBV, und diese Infektionen verursachen in der Regel keine Symptome oder sind nicht von anderen leichten, kurzen Kinderkrankheiten zu unterscheiden. In den Vereinigten Staaten und anderen entwickelten Ländern werden viele Menschen in ihrer Kindheit nicht mit EBV infiziert. Wenn eine Infektion mit EBV im Jugendalter auftritt, verursacht sie in 35 bis 50 % der Fälle eine infektiöse Mononukleose. ⓘ
EBV infiziert B-Zellen des Immunsystems und Epithelzellen. Sobald die anfängliche lytische Infektion mit EBV unter Kontrolle gebracht ist, bleibt die EBV-Latenz in den Gedächtnis-B-Zellen der Person für den Rest ihres Lebens bestehen. ⓘ
Virologie

Struktur und Genom
Das Virus hat einen Durchmesser von etwa 122-180 nm und besteht aus einer Doppelhelix aus Desoxyribonukleinsäure (DNA), die etwa 172.000 Basenpaare enthält, die für 85 Gene kodieren. Die DNA ist von einem Protein-Nukleokapsid umgeben, das von einem Tegument aus Protein umgeben ist, das wiederum von einer Hülle umgeben ist, die sowohl Lipide als auch Oberflächenprojektionen von Glykoproteinen enthält, die für die Infektion der Wirtszelle wesentlich sind. Im Juli 2020 stellte ein Forscherteam das erste vollständige atomare Modell des Nukleokapsids des Virus vor. Dieses "erste vollständige atomare Modell [umfasst] das ikosaedrische Kapsid, den Kapsid-assoziierten Tegumentkomplex (CATC) und das dodekamere Portal - den Translokationsapparat des viralen Genoms". ⓘ
Tropismus
Der Begriff viraler Tropismus bezieht sich darauf, welche Zelltypen das EBV infiziert. EBV kann verschiedene Zelltypen infizieren, darunter B-Zellen und Epithelzellen. ⓘ
Die viralen dreiteiligen Glykoproteinkomplexe von gHgL gp42 vermitteln die B-Zellmembranfusion, während die zweiteiligen Komplexe von gHgL die Epithelzellmembranfusion vermitteln. EBV, die in B-Zellen gebildet werden, weisen eine geringe Anzahl von gHgLgp42-Komplexen auf, da diese dreiteiligen Komplexe mit Human-Leukozyten-Antigenklasse-II-Molekülen interagieren, die in B-Zellen im endoplasmatischen Retikulum vorhanden sind, und abgebaut werden. Im Gegensatz dazu sind EBV aus Epithelzellen reich an den dreiteiligen Komplexen, da diese Zellen normalerweise keine HLA-Klasse-II-Moleküle enthalten. Infolgedessen sind EBV aus B-Zellen für Epithelzellen infektiöser und EBV aus Epithelzellen für B-Zellen infektiöser. Viren, denen der gp42-Anteil fehlt, können sich zwar an menschliche B-Zellen binden, sind aber nicht in der Lage, diese zu infizieren. ⓘ
Replikationszyklus

Eintritt in die Zelle
EBV kann sowohl B-Zellen als auch Epithelzellen infizieren. Die Mechanismen für das Eindringen in diese beiden Zellen sind unterschiedlich. ⓘ
Um in B-Zellen einzudringen, bindet das virale Glykoprotein gp350 an den zellulären Rezeptor CD21 (auch bekannt als CR2). Anschließend interagiert das virale Glykoprotein gp42 mit zellulären MHC-Klasse-II-Molekülen. Dadurch wird die Fusion der Virushülle mit der Zellmembran ausgelöst, so dass EBV in die B-Zelle eindringen kann. Humanes CD35, auch bekannt als Komplementrezeptor 1 (CR1), ist ein zusätzlicher Bindungsfaktor für gp350/220 und kann einen Weg für den Eintritt von EBV in CD21-negative Zellen, einschließlich unreifer B-Zellen, darstellen. Bei einer EBV-Infektion wird die Expression von CD35 herunterreguliert. ⓘ
Um in Epithelzellen einzudringen, interagiert das virale Protein BMRF-2 mit zellulären β1-Integrinen. Anschließend interagiert das virale Protein gH/gL mit zellulären αvβ6/αvβ8-Integrinen. Dadurch wird die Fusion der Virushülle mit der Epithelzellmembran ausgelöst, wodurch EBV in die Epithelzelle eindringen kann. Im Gegensatz zum Eindringen in B-Zellen wird das Eindringen in Epithelzellen durch das virale Glykoprotein gp42 behindert. ⓘ
Sobald EBV in die Zelle eindringt, löst sich das virale Kapsid auf, und das virale Genom wird in den Zellkern transportiert. ⓘ
Lytische Replikation
Der lytische Zyklus oder die produktive Infektion führt zur Produktion von infektiösen Virionen. EBV kann sich sowohl in B-Zellen als auch in Epithelzellen lytisch vermehren. In B-Zellen findet die lytische Replikation normalerweise erst nach der Reaktivierung aus der Latenzzeit statt. In Epithelzellen folgt die lytische Replikation oft direkt auf den Eintritt des Virus. ⓘ
Damit eine lytische Replikation stattfinden kann, muss das virale Genom linear sein. Das latente EBV-Genom ist zirkulär, so dass es bei der lytischen Reaktivierung linearisiert werden muss. Während der lytischen Replikation ist die virale DNA-Polymerase für die Vervielfältigung des viralen Genoms verantwortlich. Dies steht im Gegensatz zur Latenz, bei der die DNA-Polymerase der Wirtszelle das virale Genom kopiert. ⓘ
Die lytischen Genprodukte werden in drei aufeinanderfolgenden Stadien produziert: sofort-früh, früh und spät. Unmittelbar-frühe lytische Genprodukte wirken als Transaktivatoren und verstärken die Expression der späteren lytischen Gene. Zu den unmittelbar frühen lytischen Genprodukten gehören BZLF1 (auch bekannt als Zta, EB1, assoziiert mit seinem Produktgen ZEBRA) und BRLF1 (assoziiert mit seinem Produktgen Rta). Frühe lytische Genprodukte haben viele weitere Funktionen, z. B. Replikation, Stoffwechsel und Blockierung der Antigenverarbeitung. Zu den frühen lytischen Genprodukten gehört BNLF2. Bei den späten lytischen Genprodukten schließlich handelt es sich in der Regel um Proteine mit strukturellen Funktionen, wie z. B. VCA, das das virale Kapsid bildet. Andere spätlytische Genprodukte, wie BCRF1, helfen dem EBV, sich dem Immunsystem zu entziehen. ⓘ
EGCG, ein Polyphenol aus grünem Tee, hat in einer Studie gezeigt, dass es die spontane lytische Infektion mit EBV auf DNA-, Gentranskriptions- und Proteinebene zeit- und dosisabhängig hemmt. Die Expression der lytischen EBV-Gene Zta, Rta und des frühen Antigenkomplexes EA-D (der durch Rta induziert wird), des hochstabilen Gens EBNA-1, das in allen Stadien der EBV-Infektion vorkommt, wird jedoch nicht beeinflusst. Spezifische Inhibitoren (für die Signalwege) deuten darauf hin, dass der Ras/MEK/MAPK-Signalweg über BZLF1 und der PI3-K-Signalweg über BRLF1 zur lytischen EBV-Infektion beiträgt, wobei letzterer die Fähigkeit eines BRLF1-Adenovirusvektors, die lytische Form der EBV-Infektion zu induzieren, vollständig aufhebt. Darüber hinaus wird die Aktivierung einiger Gene, nicht aber anderer, untersucht, um festzustellen, wie die Zerstörung latent infizierter B-Zellen durch das Immunsystem mit Hilfe von TPA oder Natriumbutyrat eingeleitet werden kann. ⓘ
Latenz
Im Gegensatz zur lytischen Replikation führt die Latenzzeit nicht zur Produktion von Virionen. Stattdessen befindet sich die zirkuläre DNA des EBV-Genoms als Episom im Zellkern und wird von der zellulären DNA-Polymerase kopiert. Im Latenzstadium wird nur ein Teil der EBV-Gene exprimiert. Das latente EBV exprimiert seine Gene in einem von drei Mustern, die als Latenzprogramme bekannt sind. EBV kann in B-Zellen und Epithelzellen latent persistieren, aber in den beiden Zelltypen sind unterschiedliche Latenzprogramme möglich. ⓘ
EBV kann eines von drei Latenzprogrammen aufweisen: Latenzzeit I, Latenzzeit II oder Latenzzeit III. Jedes Latenzprogramm führt zur Produktion eines begrenzten, unterschiedlichen Satzes viraler Proteine und viraler RNAs. ⓘ
| Ausgedrücktes Gen | EBNA-1 | EBNA-2 | EBNA-3A | EBNA-3B | EBNA-3C | EBNA-LP | LMP-1 | LMP-2A | LMP-2B | EBER ⓘ |
|---|---|---|---|---|---|---|---|---|---|---|
| Produkt | Protein | Protein | Protein | Protein | Protein | Protein | Protein | Protein | Protein | ncRNAs |
| Latenz I | + | – | – | – | – | – | – | – | – | + |
| Latenzzeit II | + | – | – | – | – | + | + | + | + | + |
| Latenzzeit III | + | + | + | + | + | + | + | + | + | + |
Außerdem wird ein Programm postuliert, bei dem die gesamte virale Proteinexpression ausgeschaltet ist (Latenz 0). ⓘ
Innerhalb von B-Zellen sind alle drei Latenzprogramme möglich. Die EBV-Latenz in B-Zellen verläuft in der Regel von Latenz III über Latenz II zu Latenz I. Jedes Latenzstadium beeinflusst das Verhalten der B-Zellen auf einzigartige Weise. Nach der Infektion einer ruhenden naiven B-Zelle tritt EBV in die Latenzphase III ein. Die in Latenz III produzierten Proteine und RNAs verwandeln die B-Zelle in eine proliferierende Blastenzelle (auch bekannt als B-Zell-Aktivierung). Später schränkt das Virus seine Genexpression ein und tritt in die Latenzphase II ein. Die begrenztere Anzahl von Proteinen und RNAs, die in Latenz II produziert werden, veranlassen die B-Zelle, sich in eine Gedächtnis-B-Zelle zu differenzieren. Schließlich schränkt EBV die Genexpression noch weiter ein und geht in die Latenz I über. Die Expression von EBNA-1 ermöglicht es dem EBV-Genom, sich zu replizieren, wenn sich die Gedächtnis-B-Zelle teilt. ⓘ
Innerhalb von Epithelzellen ist nur Latenz II möglich. ⓘ
Bei der Primärinfektion repliziert EBV in Epithelzellen des Oropharynx und etabliert Infektionen der Latenz III, II und I in B-Lymphozyten. Die latente EBV-Infektion von B-Lymphozyten ist für die Persistenz des Virus, die anschließende Replikation in Epithelzellen und die Freisetzung infektiöser Viren in den Speichel erforderlich. EBV-Latenz-III- und -II-Infektionen von B-Lymphozyten, Latenz-II-Infektionen von oralen Epithelzellen und Latenz-II-Infektionen von NK- oder T-Zellen können zu malignen Erkrankungen führen, die durch eine einheitliche EBV-Genompräsenz und Genexpression gekennzeichnet sind. ⓘ
Reaktivierung
Latentes EBV in B-Zellen kann reaktiviert werden und zur lytischen Replikation übergehen. Es ist bekannt, dass dies in vivo geschieht, aber was dies auslöst, ist nicht genau bekannt. In vitro kann latentes EBV in B-Zellen durch Stimulierung des B-Zell-Rezeptors reaktiviert werden, so dass die Reaktivierung in vivo wahrscheinlich stattfindet, wenn latent infizierte B-Zellen auf nicht verwandte Infektionen reagieren. ⓘ
Transformation von B-Lymphozyten
Wenn EBV B-Zellen in vitro infiziert, entstehen schließlich lymphoblastoide Zelllinien, die zu einem unbegrenzten Wachstum fähig sind. Die Wachstumstransformation dieser Zelllinien ist die Folge der viralen Proteinexpression. ⓘ
EBNA-2, EBNA-3C und LMP-1 sind essentiell für die Transformation, während EBNA-LP und die EBERs dies nicht sind. ⓘ
Es wird angenommen, dass das Virus nach einer natürlichen Infektion mit EBV einige oder alle Genexpressionsprogramme aus seinem Repertoire ausführt, um eine anhaltende Infektion zu etablieren. Da es anfangs keine Immunität des Wirts gibt, produziert der lytische Zyklus eine große Anzahl von Virionen, die andere (vermutlich) B-Lymphozyten des Wirts infizieren. ⓘ
Die latenten Programme reprogrammieren und subvertieren infizierte B-Lymphozyten, damit sie sich vermehren und infizierte Zellen an die Stellen bringen, an denen das Virus vermutlich persistiert. Wenn sich schließlich eine Wirtsimmunität entwickelt, bleibt das Virus bestehen, indem es die meisten (oder möglicherweise alle) seiner Gene abschaltet und nur gelegentlich reaktiviert wird, um neue Virionen zu produzieren. Schließlich wird ein Gleichgewicht zwischen gelegentlicher viraler Reaktivierung und der Überwachung durch das Wirtsimmunsystem hergestellt, das Zellen entfernt, die die virale Genexpression aktivieren. ⓘ
Der Ort, an dem das EBV persistiert, kann das Knochenmark sein. EBV-positive Patienten, deren eigenes Knochenmark durch das Knochenmark eines EBV-negativen Spenders ersetzt wurde, erweisen sich nach der Transplantation als EBV-negativ. ⓘ
Latente Antigene
Alle EBV-Kernproteine werden durch alternatives Spleißen eines Transkripts hergestellt, das entweder am Cp- oder am Wp-Promotor am linken Ende des Genoms beginnt (in der herkömmlichen Nomenklatur). Die Gene sind innerhalb des Genoms in der Reihenfolge EBNA-LP/EBNA-2/EBNA-3A/EBNA-3B/EBNA-3C/EBNA-1 angeordnet. ⓘ
Das Initiationscodon der EBNA-LP kodierenden Region wird durch einen alternativen Spleiß des Kernproteintranskripts erzeugt. Fehlt dieses Initiationscodon, wird EBNA-2/EBNA-3A/EBNA-3B/EBNA-3C/EBNA-1 exprimiert, je nachdem, welches dieser Gene alternativ in das Transkript gespleißt wird. ⓘ
Protein/Gene
| Protein/Gen/Antigen | Stadium | Beschreibung ⓘ |
|---|---|---|
| EBNA-1 | latent+lytisch | Das EBNA-1-Protein bindet an einen Replikationsursprung (oriP) innerhalb des viralen Genoms und vermittelt die Replikation und Aufteilung des Episoms während der Teilung der Wirtszelle. Es ist das einzige virale Protein, das während der Latenzzeit der Gruppe I exprimiert wird. |
| EBNA-2 | latent+lytisch | EBNA-2 ist der wichtigste virale Transaktivator. |
| EBNA-3 | latent+lytisch | Diese Gene binden auch das Wirts-RBP-Jκ-Protein. |
| LMP-1 | latent | LMP-1 ist ein sechsgliedriges Transmembranprotein, das auch für die EBV-vermittelte Wachstumstransformation wesentlich ist. |
| LMP-2 | latent | LMP-2A/LMP-2B sind Transmembranproteine, die die Tyrosinkinase-Signalübertragung blockieren. |
| EBER | latent | EBER-1/EBER-2 sind kleine nukleare RNAs, die an bestimmte Nukleoproteinpartikel binden und so die Bindung an PKR (dsRNA-abhängige Serin/Threonin-Proteinkinase) ermöglichen und deren Funktion hemmen. EBERs sind die bei weitem häufigsten EBV-Produkte, die in EBV-infizierten Zellen transkribiert werden. Sie werden häufig als Zielmoleküle für den Nachweis von EBV in histologischen Geweben verwendet. ER-Partikel induzieren auch die Produktion von IL-10, das das Wachstum fördert und zytotoxische T-Zellen hemmt. |
| v-snoRNA1 | latent | Die Epstein-Barr-Virus-snoRNA1 ist eine Box-CD-snoRNA, die vom Virus während der Latenzzeit gebildet wird. V-snoRNA1 kann als miRNA-ähnlicher Vorläufer fungieren, der zu RNA-Fragmenten mit einer Größe von 24 Nukleotiden verarbeitet wird, die auf die 3'UTR der viralen DNA-Polymerase-mRNA abzielen. |
| ebv-sisRNA | latent | Ebv-sisRNA-1 ist eine stabile intronische Sequenz-RNA, die während des Latenzprogramms III gebildet wird. Nach den EBERs ist sie die am dritthäufigsten vorkommende kleine RNA, die das Virus während dieses Programms produziert. |
| miRNAs | latent | EBV-microRNAs werden von zwei Transkripten kodiert, einem Satz im BART-Gen und einem Satz in der Nähe des BHRF1-Clusters. Die drei BHRF1 pri-miRNAS (die vier miRNAs erzeugen) werden während der Typ-III-Latenz exprimiert, während der große Cluster von BART miRNAs (bis zu 20 miRNAs) während der Typ-II-Latenz exprimiert wird. Die Funktionen dieser miRNAs sind derzeit noch unbekannt. |
| EBV-EA | lytisch | frühes Antigen |
| EBV-MA | lytisch | Membran-Antigen |
| EBV-VCA | lytisch | virales Kapsid-Antigen |
| EBV-AN | lytisch | alkalische Nuklease |
Übertragung
Hauptübertragungsweg des Virus ist eine Tröpfcheninfektion oder eine Kontaktinfektion (besonders Speichel) bzw. Schmierinfektion, seltener sind Übertragungen im Rahmen von Transplantationen oder Bluttransfusionen. Die Tatsache, dass EBV auch in Sekreten der Genitalien festgestellt werden konnte, macht auch den Übertragungsweg durch sexuelle Kontakte denkbar. ⓘ
Auf molekularer Ebene werden complement receptor type 1 (CR1) und complement receptor type 2 (CR2) als Adhäsionsfaktoren an der Zelloberfläche beschrieben. Für den Eintritt in Zellen benutzt das EBV Integrine oder HLA-II (HLA class II histocompatibility antigen). ⓘ
Nachweis
Die vom Epstein-Barr-Virus kodierten kleinen RNAs (EBERs) sind die bei weitem häufigsten EBV-Produkte, die in von EBV infizierten Zellen transkribiert werden. Sie werden häufig als Zielmoleküle für den Nachweis von EBV in histologischen Geweben verwendet. ⓘ
Rolle bei der Krankheit
- Siehe auch Infektiöse Mononukleose und die anderen in diesem Abschnitt aufgeführten Krankheiten ⓘ
EBV verursacht infektiöse Mononukleose. Bei Kindern, die mit EBV infiziert sind, treten nur wenige Symptome auf oder sie erscheinen asymptomatisch, aber wenn die Infektion bis zum Jugend- oder Erwachsenenalter hinausgezögert wird, kann sie Müdigkeit, Fieber, einen entzündeten Hals, geschwollene Lymphknoten im Nacken, eine vergrößerte Milz, eine geschwollene Leber oder einen Ausschlag verursachen. Auch das postinfektiöse chronische Müdigkeitssyndrom wurde mit einer EBV-Infektion in Verbindung gebracht. ⓘ
EBV wurde auch bei mehreren anderen Krankheiten nachgewiesen, darunter Burkitt-Lymphom, hämophagozytische Lymphohistiozytose, Hodgkin-Lymphom, Magenkrebs, Nasopharynxkarzinom, Multiple Sklerose und lymphomatoide Granulomatose. ⓘ
Es hat sich gezeigt, dass EBV-infizierte B-Zellen in den Hirnläsionen von Multiple-Sklerose-Patienten zu finden sind, und eine 2022 durchgeführte Studie mit Blutproben von 10 Millionen Soldaten zeigte, dass "Personen, die nicht mit dem Epstein-Barr-Virus infiziert waren, praktisch nie an Multipler Sklerose erkranken. Erst nach einer Infektion mit dem Epstein-Barr-Virus steigt das Risiko, an Multipler Sklerose zu erkranken, um mehr als das 30-fache", und dass von den vielen Infektionen nur das EBV einen so deutlichen Zusammenhang mit der Krankheit aufweist. ⓘ
Weitere Krankheiten, die mit EBV in Verbindung gebracht werden, sind das Gianotti-Crosti-Syndrom, Erythema multiforme, akute Genitalgeschwüre und orale haarige Leukoplakie. Die Virusinfektion steht auch im Zusammenhang mit einer Vielzahl nicht bösartiger lymphoproliferativer Erkrankungen wie schweren allergischen Überempfindlichkeitsreaktionen auf Mückenstiche, Epstein-Barr-Virus-positiven mukokutanen Ulzera und Hydroa vacciniforme sowie mit bösartigen lymphoproliferativen Erkrankungen wie dem Epstein-Barr-Virus-positiven Burkitt-Lymphom, dem Epstein-Barr-Virus-positiven Hodgkin-Lymphom und dem primären Ergusslymphom und trägt häufig zu deren Entstehung bei. ⓘ
Das Epstein-Barr-Virus wird mit Erkrankungen in Verbindung gebracht, die mit der Alpha-Synuclein-Aggregation zusammenhängen (z. B. Parkinson-Krankheit, Demenz mit Lewy-Körperchen und Atrophie des multiplen Systems). ⓘ
Geschichte
Das Epstein-Barr-Virus wurde nach Michael Anthony Epstein und Yvonne Barr benannt, die das Virus gemeinsam mit Bert Achong entdeckten. 1961 besuchte Epstein, Pathologe und Experte für Elektronenmikroskopie, einen Vortrag von Denis Parsons Burkitt, einem in Uganda praktizierenden Chirurgen, über "The Commonest Children's Cancer in Tropical Africa-A Hitherto Unrecognised Syndrome", in dem Burkitt die "endemische Variante" (pädiatrische Form) der Krankheit beschrieb, die seinen Namen trägt. 1963 wurde ein Exemplar aus Uganda zur Anzucht an das Middlesex Hospital gesandt. Die Viruspartikel wurden in den kultivierten Zellen identifiziert, und die Ergebnisse wurden 1964 von Epstein, Achong und Barr in The Lancet veröffentlicht. Die Zelllinien wurden an Werner und Gertrude Henle am Kinderkrankenhaus von Philadelphia gesandt, die serologische Marker entwickelten. Im Jahr 1967 erkrankte ein Techniker in ihrem Labor an Mononukleose, und sie konnten eine gelagerte Serumprobe vergleichen, die zeigte, dass sich Antikörper gegen das Virus entwickelten. 1968 entdeckten sie, dass EBV B-Zellen nach der Infektion direkt immortalisieren kann, was einige Formen von EBV-bedingten Infektionen nachahmt, und bestätigten die Verbindung zwischen dem Virus und infektiöser Mononukleose. ⓘ
Forschung
EBV ist ein relativ komplexes Virus, das noch nicht vollständig verstanden ist. Labors auf der ganzen Welt untersuchen das Virus weiterhin und entwickeln neue Methoden zur Behandlung der von ihm verursachten Krankheiten. Eine beliebte Methode, EBV in vitro zu untersuchen, ist die Verwendung bakterieller künstlicher Chromosomen. Das Epstein-Barr-Virus kann im Labor in ständiger Latenz gehalten und manipuliert werden (eine Eigenschaft, die es mit dem Kaposi-Sarkom-assoziierten Herpesvirus, einem anderen der acht menschlichen Herpesviren, teilt). Obwohl man davon ausgeht, dass viele Viren diese Eigenschaft während der Infektion ihrer natürlichen Wirte haben, gibt es kein einfach zu handhabendes System zur Untersuchung dieses Teils des viralen Lebenszyklus. Genomische Studien von EBV haben es ermöglicht, die lytische Reaktivierung und die Regulierung des latenten viralen Episoms zu untersuchen. ⓘ
Obwohl aktiv geforscht wird, gibt es noch keinen Impfstoff gegen das Epstein-Barr-Virus. Die Entwicklung eines wirksamen Impfstoffs könnte weltweit bis zu 200.000 Krebserkrankungen pro Jahr verhindern. Das Fehlen wirksamer Tiermodelle ist ein Hindernis für die Entwicklung von prophylaktischen und therapeutischen Impfstoffen gegen EBV. ⓘ
Wie andere humane Herpesviren könnte Epstein-Barr durch eine Behandlung mit dem Prodrug Valaciclovir ausgerottet werden, aber es bedarf weiterer Forschung, um festzustellen, ob eine Ausrottung tatsächlich möglich ist. Antivirale Mittel wirken durch Hemmung der viralen DNA-Replikation, aber es gibt nur wenige Hinweise darauf, dass sie gegen das Epstein-Barr-Virus wirksam sind. Außerdem sind sie teuer, bergen das Risiko einer Resistenz gegen antivirale Mittel und können (in 1 bis 10 % der Fälle) unangenehme Nebenwirkungen verursachen. ⓘ
Diagnostik
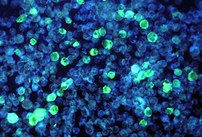
Allgemein findet man bei der Infektion mit dem Epstein-Barr-Virus fast immer einen erhöhten Anteil von Lymphozyten an den gesamten weißen Blutkörperchen (so genannte relative Lymphozytose). Die Gesamtzahl der weißen Blutkörperchen kann dabei verringert, normal oder erhöht sein. Wird ein Blutausstrich unter dem Mikroskop untersucht, sieht man atypische mononukleäre Zellen mit charakteristischen Veränderungen (so genannte Pfeiffer-Zellen – morphologisch gegen EBV gerichtete spezifische zytotoxische (CD8+) T-Lymphozyten, die einen runden oder gebuchteten Zellkern (selten gelappt) aufweisen), die manchmal bereits die Diagnose ermöglichen. Weiterhin sind die Leberwerte häufig erhöht. ⓘ
Die serologische Beurteilung des EBV-Status ist nicht immer einfach. Zum Nachweis der akuten Infektion werden mancherorts sogenannte Schnelltests angewendet, die jedoch je nach Lebensalter bis zu 20 % falsch positive und 30 % falsch negative Resultate liefern. Die Diagnostik (normaler immunkompetenter Patienten) sollte gestaffelt erfolgen, und die Konstellationen, die mancher Patient oder Arzt auf seinem Laborbericht findet, sind manchmal etwas schwierig zu deuten:
- Der Nachweis von IgG-Antikörpern gegen das nukleäre Antigen von EBV (EBNA-1-IgG) beweist das Vorhandensein des Virus. Ist der EBNA-1-IgG-Test eindeutig positiv, so ist jeder weitere Test zum Virusnachweis bei einer akuten Erkrankung (Mononukleose) unnötig. Eine Mononukleose nach frischer Infektion ist bei positivem EBNA-IgG-Nachweis ausgeschlossen, da diese Antikörper erst im Laufe von mehreren Wochen bis Monaten nach Auftreten der Symptome und beim Übergang in die Viruslatenz vom Immunsystem produziert werden. Bei etwa 95 % der Menschen mit zurückliegender EBV-Infektion sind EBNA-1-IgG-Antikörper nachweisbar.
- Ist das EBNA-1-IgG negativ, sollte das IgG gegen das virale Capsid-Antigen (VCA-IgG) getestet werden. Es ist ein Marker für aktuellen oder früheren Kontakt mit EBV und bleibt in der Regel lebenslang nachweisbar.
- Zum Nachweis einer akuten Infektion werden bei positivem VCA-IgG die IgM-Antikörper gegen das virale Capsid (VCA-IgM) getestet. Sind diese positiv, so spricht dies für eine frische bzw. kürzliche Infektion (beweist diese allerdings nicht!).
- Bei starker körperlicher Belastung (besonders bei Leistungssportlern) kann das VCA-IgM persistieren. Man spricht von einer verlängerten (prolongierten) Ausheilung, wenn das EBNA-1-IgG bereits positiv ist.
- In diagnostischen Problemfällen kann häufig durch einen Immunoblot und/oder eine Aviditätstestung eine akute von einer zurückliegenden Infektion unterschieden werden. Der Nachweis einer hohen Avidität der VCA-IgG-Antikörper beweist einen länger zurückliegenden Infektionszeitpunkt, eine deutliche VCA-p18-Bande im IgG-Immunoblot spricht ebenfalls dafür. Typische Befunde bei einer akuten Infektion sind: Fehlen von EBNA-1-IgG-Antikörpern, niedrige Avidität der VCA-IgG-Antikörper und Nachweis von IgG- und/oder IgM-Antikörper gegen EA (early antigen).
- Bei Immunschwäche (Immuninkompetenz) kann das Virus von der Ruhephase (Latenz) wieder in eine aktive Vermehrung übergehen (Reaktivierung). Hierbei kann das EBNA-1-IgG beispielsweise bei HIV-Patienten sekundär wieder negativ werden. Eine zuverlässige Einschätzung von EBV-Reaktivierungen bei Immunschwäche ist nur anhand der Bestimmung der Viruslast durch Polymerase-Kettenreaktion möglich.
- Der direkte Nachweis der Virus-DNA mittels Polymerase-Kettenreaktion ist bei Immungesunden meist nicht sinnvoll, da im Blut auch das latente Genom nachgewiesen werden kann und gleichzeitig symptomlose Träger das Virus konstant oder vorübergehend mit dem Speichel ausscheiden. Die oben genannten Reaktivierungen bereiten einem immungesunden Menschen in aller Regel keine Beschwerden, sie stellen lediglich ein labordiagnostisches Problem dar, da der Nachweis von VCA-IgG in hohen Konzentrationen und ggf. wieder auftretendes VCA-IgM zu Fehlinterpretationen führen kann. ⓘ
Eine Besonderheit des EBV ist es, dass durch die akute Infektion von B-Lymphozyten (v. a. B-Gedächtniszellen) mit EBV diese wieder IgM-Antikörper von schon lange ausgeheilten Infektionen oder Impfungen bilden können. Diese Patienten zeigen dann oft das gleichzeitige Vorhandensein von IgM gegen Röteln, Masern, Hepatitis A, CMV u. v. m. und imitieren somit serologisch eine akute Infektion mit diesen Erregern. Ein Patient mit mehr als einem positiven IgM ist daher stets EBV-verdächtig. ⓘ