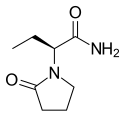
Levetiracetam
| |||
| Klinische Daten | |||
|---|---|---|---|
| Aussprache | /lɛvɪtɪˈræsɪtæm/ | ||
| Handelsnamen | Keppra, Elepsia, Spritam, andere | ||
| AHFS/Drugs.com | Monographie | ||
| MedlinePlus | a699059 | ||
| Lizenz-Daten |
| ||
| Schwangerschaft Kategorie |
| ||
| Wege der Verabreichung | Durch den Mund, intravenös | ||
| Wirkstoffklasse | Racetam-Antikonvulsivum | ||
| ATC-Code |
| ||
| Rechtlicher Status | |||
| Rechtlicher Status |
| ||
| Pharmakokinetische Daten | |||
| Bioverfügbarkeit | ~100% | ||
| Proteinbindung | <10% | ||
| Stoffwechsel | Enzymatische Hydrolyse der Acetamidgruppe | ||
| Eliminationshalbwertszeit | 6-8 Stunden | ||
| Ausscheidung | Urin | ||
| Bezeichner | |||
IUPAC-Bezeichnung
| |||
| CAS-Nummer | |||
| PubChem CID | |||
| IUPHAR/BPS | |||
| DrugBank | |||
| ChemSpider | |||
| UNII | |||
| KEGG | |||
| ChEBI | |||
| ChEMBL | |||
| Chemische und physikalische Daten | |||
| Formel | C8H14N2O2 | ||
| Molekulare Masse | 170.212 g-mol-1 | ||
| 3D-Modell (JSmol) | |||
SMILES
| |||
InChI
| |||
| | |||
Levetiracetam, das unter anderem unter dem Markennamen Keppra verkauft wird, ist ein Medikament zur Behandlung von Epilepsie. Es wird bei partiell auftretenden, myoklonischen oder tonisch-klonischen Anfällen eingesetzt und entweder durch den Mund in Form einer sofortigen oder verlängerten Wirkstofffreisetzung oder durch Injektion in eine Vene eingenommen. ⓘ
Zu den häufigen Nebenwirkungen von Levetiracetam gehören Schläfrigkeit, Schwindelgefühl, Müdigkeit und Aggressivität. Schwere Nebenwirkungen können Psychosen, Selbstmord und allergische Reaktionen wie das Stevens-Johnson-Syndrom oder Anaphylaxie sein. Es ist unklar, ob Levetiracetam während der Schwangerschaft und Stillzeit sicher angewendet werden kann. Levetiracetam ist das S-Enantiomer von Etiracetam. Sein Wirkmechanismus ist noch nicht geklärt. ⓘ
Levetiracetam wurde 1999 in den Vereinigten Staaten zur medizinischen Verwendung zugelassen und ist als Generikum erhältlich. Im Jahr 2019 war es mit mehr als 7 Millionen Verschreibungen das 97. am häufigsten verschriebene Medikament in den Vereinigten Staaten. ⓘ
| Strukturformel ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
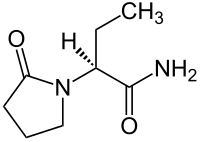
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Levetiracetam | ||||||||||||||||||
| Andere Namen |
(S)-2-(2-Oxopyrrolidin-1-yl)-butylamid | ||||||||||||||||||
| Summenformel | C8H14N2O2 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code |
N03AX14 | ||||||||||||||||||
| Wirkstoffklasse |
Antiepileptikum | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 170,21 g·mol−1 | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
1038 mg·kg−1 (LD50, Ratte, i.v.) | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Levetiracetam ist ein Ethyl-Derivat des Antidementivums (früherer Name: Nootropikum) Piracetam. Es ist ein Arzneistoff aus der Gruppe der Antiepileptika, welcher durch die belgische Firma UCB S.A. entwickelt und im Jahr 1985 patentiert wurde. Es ist weltweit unter dem Handelsnamen Keppra® erhältlich. Seit März 2011 wird es auch als Generikum angeboten. ⓘ
Es wird nicht in der Leber verstoffwechselt und kaum an Plasmaproteine gebunden. ⓘ
Medizinische Anwendungen
Fokale Epilepsie
Levetiracetam ist als Monotherapie bei neu diagnostizierter fokaler Epilepsie bei Erwachsenen wirksam. Als Zusatzmedikation reduziert es fokale Anfälle um 50 % oder mehr. ⓘ
Partiell-komplexe Epilepsie
Levetiracetam ist als Zusatztherapie bei partieller (fokaler) Epilepsie wirksam. ⓘ
Generalisierte Epilepsie
Levetiracetam ist wirksam zur Behandlung der generalisierten tonisch-klonischen Epilepsie. Es wurde in den Vereinigten Staaten als Zusatzbehandlung für myoklonische und tonisch-klonische Anfälle zugelassen. Levetiracetam wurde in der Europäischen Union als Monotherapie zur Behandlung von Epilepsie bei partiellen Anfällen oder als Zusatztherapie bei partiellen, myoklonischen und tonisch-klonischen Anfällen zugelassen. ⓘ
Levetiracetam wird manchmal auch zur Behandlung des Status epilepticus eingesetzt. ⓘ
Prävention von Krampfanfällen
Auf der Grundlage minderwertiger Belege ist Levetiracetam zur Vorbeugung früher Anfälle nach traumatischen Hirnverletzungen etwa so wirksam wie Phenytoin. Es kann zur Vorbeugung von Krampfanfällen im Zusammenhang mit Subarachnoidalblutungen wirksam sein. ⓘ
Andere
Levetiracetam hat sich weder bei der Behandlung von neuropathischen Schmerzen noch bei der Behandlung von essentiellem Zittern als nützlich erwiesen. Levetiracetam hat sich nicht als nützlich für die Behandlung von Autismus erwiesen, ist aber eine wirksame Behandlung für partielle, myoklonische oder tonisch-klonische Anfälle im Zusammenhang mit Autismus-Spektrum-Störungen. ⓘ
Besondere Gruppen
Studien an trächtigen weiblichen Ratten haben geringfügige fötale Skelettanomalien gezeigt, wenn die für den Menschen empfohlene Höchstdosis von Levetiracetam oral während der Schwangerschaft und Stillzeit verabreicht wurde. ⓘ
Es wurden Studien durchgeführt, um zu prüfen, ob bei älteren Menschen im Vergleich zu jüngeren Patienten vermehrt unerwünschte Wirkungen auftreten. Eine dieser Studien, die in der Fachzeitschrift Epilepsy Research veröffentlicht wurde, zeigte keinen signifikanten Anstieg der Häufigkeit von unerwünschten Symptomen bei jungen oder älteren Patienten mit Erkrankungen des zentralen Nervensystems (ZNS). ⓘ
Levetiracetam kann bei Kindern über vier Jahren mit Vorsicht angewendet werden. Es ist jedoch nicht geklärt, ob es Kindern unter vier Jahren sicher verabreicht werden kann. ⓘ
Unerwünschte Wirkungen
Zu den häufigsten unerwünschten Wirkungen der Behandlung mit Levetiracetam gehören Wirkungen auf das ZNS wie Schläfrigkeit, verminderte Leistungsfähigkeit, Kopfschmerzen, Schwindel, Stimmungsschwankungen und Koordinationsstörungen. Diese unerwünschten Wirkungen sind im ersten Monat der Therapie am stärksten ausgeprägt. Etwa 4 % der Patienten brachen die vor der Zulassung durchgeführten klinischen Studien aufgrund dieser Nebenwirkungen ab. ⓘ
Bei etwa 13 % der Patienten, die Levetiracetam einnehmen, treten unerwünschte neuropsychiatrische Symptome auf, die in der Regel leicht sind. Dazu gehören Unruhe, Feindseligkeit, Apathie, Angstzustände, emotionale Labilität und Depression. Schwerwiegende psychiatrische Nebenwirkungen, die durch Absetzen des Medikaments rückgängig gemacht werden können, treten bei etwa 1 % auf. Dazu gehören Halluzinationen, Selbstmordgedanken oder Psychosen. Diese traten meist innerhalb des ersten Monats der Therapie auf, können aber jederzeit während der Behandlung auftreten. ⓘ
Obwohl selten, wurde bei Patienten, die mit Levetiracetam behandelt wurden, über das Stevens-Johnson-Syndrom (SJS) und die toxische epidermale Nekrolyse (TEN) berichtet, die sich als schmerzhafter, sich ausbreitender Hautausschlag mit Rötung und Blasenbildung und/oder Schälen der Haut zeigt. Die Inzidenz von SJS nach Exposition gegenüber Antiepileptika wie Levetiracetam beträgt etwa 1 zu 3.000. ⓘ
Levetiracetam sollte nicht bei Personen angewendet werden, die in der Vergangenheit eine Überempfindlichkeit gegen Levetiracetam oder einen der inaktiven Bestandteile der Tablette oder der oralen Lösung gezeigt haben. Zu solchen Überempfindlichkeitsreaktionen gehören unter anderem ein unerklärlicher Hautausschlag mit Rötung oder Blasenbildung, Atembeschwerden und Engegefühl in der Brust oder den Atemwegen. ⓘ
In einer Studie war die Inzidenz einer verminderten Knochenmineraldichte bei Patienten, die Levetiracetam einnahmen, deutlich höher als bei anderen Epilepsiemedikamenten. ⓘ
Selbstmord
Levetiracetam kann zusammen mit anderen Antiepileptika das Risiko für suizidales Verhalten oder Suizidgedanken erhöhen. Menschen, die Levetiracetam einnehmen, sollten engmaschig auf Anzeichen einer sich verschlimmernden Depression, auf Selbstmordgedanken oder -tendenzen oder auf andere veränderte emotionale oder verhaltensbezogene Zustände überwacht werden. ⓘ
Niere und Leber
Eine Beeinträchtigung der Nierenfunktion vermindert die Ausscheidungsrate von Levetiracetam aus dem Körper. Bei Personen mit eingeschränkter Nierenfunktion kann eine Dosisanpassung erforderlich sein. Die Nierenfunktion kann anhand der Kreatinin-Clearance-Rate geschätzt werden. ⓘ
Eine Dosisanpassung von Levetiracetam ist bei Leberfunktionsstörungen nicht erforderlich. ⓘ
Wechselwirkungen mit anderen Arzneimitteln
Es wurden keine signifikanten pharmakokinetischen Wechselwirkungen zwischen Levetiracetam oder seinem Hauptmetaboliten und gleichzeitig eingenommenen Medikamenten beobachtet. Das pharmakokinetische Profil von Levetiracetam wird durch Phenytoin, Phenobarbital, Primidon, Carbamazepin, Valproinsäure, Lamotrigin, Gabapentin, Digoxin, Ethinylestradiol oder Warfarin nicht beeinflusst. ⓘ
Mechanismus der Wirkung
Der genaue Wirkmechanismus von Levetiracetam bei der Behandlung von Epilepsie ist unbekannt. Levetiracetam weist keine pharmakologischen Wirkungen auf, die denen der klassischen Antikonvulsiva ähneln. Es hemmt keine spannungsabhängigen Na+-Kanäle, beeinträchtigt nicht die GABA-erge Übertragung und bindet nicht an GABA-erge oder glutamaterge Rezeptoren. Das Medikament bindet jedoch an SV2A, ein synaptisches Vesikel-Glykoprotein, und hemmt präsynaptische Kalziumkanäle, wodurch die Freisetzung von Neurotransmittern verringert wird und es als Neuromodulator wirkt. Es wird angenommen, dass dies die Impulsleitung über die Synapsen behindert. ⓘ
Pharmakokinetik
Absorption
Die Resorption von Levetiracetam-Tabletten und oraler Lösung erfolgt schnell und im Wesentlichen vollständig. Die Bioverfügbarkeit von Levetiracetam liegt bei nahezu 100 Prozent, und der Einfluss der Nahrung auf die Absorption ist gering. ⓘ
Verteilung
Das Verteilungsvolumen von Levetiracetam entspricht dem des gesamten Körperwassers. Levetiracetam bindet in geringem Maße an Plasmaproteine (weniger als 10 %). ⓘ
Stoffwechsel
Levetiracetam unterliegt keinem umfassenden Metabolismus, und die gebildeten Metaboliten sind nicht aktiv und üben keine pharmakologische Wirkung aus. Der Metabolismus von Levetiracetam erfolgt nicht über Cytochrom-P450-Enzyme in der Leber, sondern über andere Stoffwechselwege wie Hydrolyse und Hydroxylierung. ⓘ
Ausscheidung
Bei Personen mit normaler Nierenfunktion wird Levetiracetam hauptsächlich über die Nieren ausgeschieden, wobei etwa 66 Prozent des ursprünglichen Wirkstoffs unverändert in den Urin gelangen. Die Plasmahalbwertszeit von Levetiracetam beträgt bei Erwachsenen etwa 6 bis 8 Stunden. ⓘ
Analoga
Brivaracetam, ein chemisches Analogon zu Levetiracetam, ist ein Racetam-Derivat mit ähnlichen Eigenschaften. ⓘ
Gesellschaft und Kultur
Levetiracetam ist als orale Formulierung mit normaler und verlängerter Wirkstofffreisetzung sowie als intravenöse Formulierung erhältlich. ⓘ
Die Tablette mit sofortiger Wirkstofffreisetzung ist in den Vereinigten Staaten seit 2008 und im Vereinigten Königreich seit 2011 als Generikum erhältlich. Das Patent für die Tablette mit verlängerter Wirkstofffreisetzung läuft im Jahr 2028 aus. ⓘ
Das Markenpräparat Keppra wird von UCB Pharmaceuticals Inc. hergestellt. ⓘ
Im Jahr 2015 wurde die 3D-gedruckte, oral zerfallende Tablettenform des Medikaments von Aprecia unter dem Handelsnamen Spritam von der FDA zugelassen. Es wird behauptet, dass das Medikament durch den 3D-Druck verbessert wurde, da die verwendete Formel nun über bessere Zerfallseigenschaften verfügt. ⓘ
Rechtlicher Status
Australien
Levetiracetam ist in Australien gemäß der Giftnorm (Februar 2020) eine Substanz der Liste 4. Eine Substanz der Liste 4 wird als "verschreibungspflichtige Medizin oder verschreibungspflichtiges Tierarzneimittel - Substanzen, deren Verwendung oder Abgabe durch oder auf Anordnung von Personen erfolgen sollte, die nach den Rechtsvorschriften des Bundesstaates oder des Territoriums zur Verschreibung berechtigt sind, und die von einem Apotheker auf Rezept erhältlich sein sollten" eingestuft. ⓘ
Japan
Nach japanischem Recht dürfen Levetiracetam und andere Racetams nicht ins Land gebracht werden, es sei denn, sie sind für den persönlichen Gebrauch eines Reisenden bestimmt, dem sie verschrieben worden sind. Reisende, die mehr als einen Monatsbedarf mitbringen wollen, müssen eine Einfuhrbescheinigung, ein so genanntes Yakkan Shoumei (薬監証明, yakkan shōmei), beantragen. ⓘ
Forschung
Levetiracetam wird bei psychiatrischen und neurologischen Erkrankungen wie dem Tourette-Syndrom und Angstzuständen untersucht. Die schwerwiegendsten unerwünschten Wirkungen sind jedoch verhaltensbezogen, und das Nutzen-Risiko-Verhältnis von Levetiracetam bei diesen Erkrankungen ist nicht gut bekannt. ⓘ
Levetiracetam wird derzeit als Medikament zur Verringerung der Hyperaktivität im Hippocampus bei der Alzheimer-Krankheit getestet. ⓘ
Außerdem wurde experimentell gezeigt, dass Levetiracetam die Levodopa-induzierte Dyskinesie, eine Art von Bewegungsstörung, oder die Dyskinesie, die mit der Einnahme von Levodopa, einem Medikament zur Behandlung der Parkinson-Krankheit, einhergeht, reduziert. ⓘ
Metabolismus
Die Substanz wird kaum in der Leber verstoffwechselt. Es gibt einen inaktiven Haupt-Metaboliten, der durch Hydrolyse im Gewebe gebildet wird. ⓘ
Durch den fehlenden Lebermetabolismus kann die Substanz mit allen anderen Antiepileptika kombiniert werden, ohne dass diese sich gegenseitig beeinflussen. ⓘ
Dosierung
Die empfohlene Dosis wird auf zwei Tagesdosen verteilt. Eine Steigerung ist alle zwei Wochen möglich. Bei Patienten mit verminderter Nierenleistung (insbesondere bei älteren Patienten) sollte die Dosis reduziert werden. ⓘ
Wirkung
Der Wirkungsmechanismus beruht auf der Bindung an das Vesikelprotein SV2A, was eine verminderte Freisetzung von Glutamat aus dem präsynaptischen Vesikel zur Folge hat. ⓘ
In-vitro-Studien zeigen, dass Levetiracetam die intraneuronalen Ca2+-Spiegel beeinflusst, indem der durch N-Typ-Kanäle vermittelte Ca2+-Strom partiell inhibiert sowie die Freisetzung von Ca2+ aus intraneuronalen Speichern vermindert wird. Weiterhin kehrt es partiell die Reduktion der GABA- und Glycin-gesteuerten Ströme um, die durch Zink und β-Carboline induziert wird. ⓘ
Nebenwirkungen
Der Wirkstoff Levetiracetam zeichnet sich durch gute Verträglichkeit aus. Durch plötzliches Absetzen des Medikamentes können, wie bei allen Antiepileptika, epileptische Anfälle provoziert werden. Deshalb muss es durch langsame Dosisreduktion ausgeschlichen werden. ⓘ
Nebenwirkungen, die sehr häufig (≥10 %) beobachtet wurden:
Nebenwirkungen, die häufig (1 bis ≤10 %) beobachtet wurden (Auszug): Abdominalschmerzen, Agitation, Anorexie, Ataxie, Benommenheit, Depression, Diarrhoe, Diplopie, Dyspepsie, Ekzem, emotionale Labilität / Stimmungsschwankungen, Erbrechen, Exanthem, Feindseligkeit / Aggression, Gewichtsverlust, Gewichtszunahme, Insomnie, Juckreiz, Konvulsion, Kopfschmerzen, Myalgie, nauseale Amnesie, Nervosität / Reizbarkeit, Persönlichkeitsstörung, Thrombozytopenie, Tremor, vermehrter Husten, Schwindel ⓘ