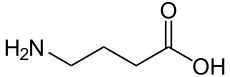
Γ-Aminobuttersäure
| |

| |
| Bezeichnungen | |
|---|---|
| Bevorzugter IUPAC-Name
4-Aminobuttersäure | |
| Andere Bezeichnungen
γ-Aminobuttersäure
4-Aminobuttersäure 3-Carboxypropylamin Piperidinsäure Piperidinsäure | |
| Bezeichner | |
3D-Modell (JSmol)
|
|
Beilstein-Referenz
|
906818 |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Arzneimittelbank | |
| EC-Nummer |
|
Gmelin Referenz
|
49775 |
IUPHAR/BPS
|
|
| KEGG | |
| MeSH | Gamma-Aminobuttersäure+Acid |
PubChem CID
|
|
| RTECS-Nummer |
|
| UNII | |
InChI
| |
SMILES
| |
| Eigenschaften | |
Chemische Formel
|
C4H9NO2 |
| Molare Masse | 103,120 g/mol |
| Erscheinungsbild | weißes mikrokristallines Pulver |
| Dichte | 1,11 g/ml |
| Schmelzpunkt | 203,7 °C (398,7 °F; 476,8 K) |
| Siedepunkt | 247,9 °C (478,2 °F; 521,0 K) |
Löslichkeit in Wasser
|
130 g/100 mL |
| log P | −3.17 |
| Acidität (pKa) |
|
| Gefahren | |
| Sicherheit und Gesundheitsschutz am Arbeitsplatz (OHS/OSH): | |
Hauptgefahren
|
Reizend, Gesundheitsschädlich |
| Tödliche Dosis oder Konzentration (LD, LC): | |
LD50 (mittlere Dosis)
|
12.680 mg/kg (Maus, oral) |
Wenn nicht anders angegeben, gelten die Daten für Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |
γ-Aminobuttersäure (Gamma-Aminobuttersäure) /ˈɡæmə əˈmiːnoʊbjuːˈtɪrɪk ˈæsɪd/, oder GABA /ˈɡæbə/, ist der wichtigste hemmende Neurotransmitter im zentralen Nervensystem von Säugetieren in der Reifephase. Seine Hauptaufgabe ist die Verringerung der neuronalen Erregbarkeit im gesamten Nervensystem. ⓘ
GABA wird in vielen Ländern als Nahrungsergänzungsmittel verkauft. Bisher ging man davon aus, dass exogenes GABA (d. h. als Nahrungsergänzungsmittel eingenommen) die Blut-Hirn-Schranke nicht überwindet; Daten aus neueren Forschungen zeigen jedoch, dass dieser Gedanke bis zum Abschluss weiterer Untersuchungen unklar ist. ⓘ
Die Carboxylatform von GABA ist γ-Aminobutyrat. ⓘ
Die γ-Aminobuttersäure (englisch gamma-Aminobutyric acid, abgekürzt GABA), seltener auch 4-Aminobuttersäure oder Piperidinsäure genannt, ist ein Amin der Buttersäure. Die Stellung der Aminogruppe am γ-Kohlenstoffatom bezüglich der Carboxygruppe unterscheidet sie von den proteinogenen α-Aminosäuren. ⓘ
Biologisch ist γ-Aminobuttersäure oder GABA bei vielen Lebewesen ein bedeutender endogener Botenstoff, der als biogenes Amin durch Decarboxylierung der Glutaminsäure gebildet wird, insbesondere von Nervenzellen. Im Gehirn erwachsener Säugetiere ist GABA so der hauptsächliche Neurotransmitter von inhibitorischen (hemmenden) Synapsen; während fetaler Reifungsphasen ist die Wirkung hingegen oft exzitatorisch (erregend). ⓘ
Funktion
Neurotransmitter
Es sind zwei allgemeine Klassen von GABA-Rezeptoren bekannt:
- GABAA, bei dem der Rezeptor Teil eines ligandengesteuerten Ionenkanalkomplexes ist
- Metabotrope GABAB-Rezeptoren, bei denen es sich um G-Protein-gekoppelte Rezeptoren handelt, die über Vermittler (G-Proteine) Ionenkanäle öffnen oder schließen ⓘ

Neuronen, die GABA als Output produzieren, werden als GABAerge Neuronen bezeichnet und haben bei erwachsenen Wirbeltieren hauptsächlich eine hemmende Wirkung auf Rezeptoren. Mittlere Stachelzellen sind ein typisches Beispiel für hemmende GABAerge Zellen des Zentralnervensystems. Im Gegensatz dazu wirkt GABA bei Insekten sowohl erregend als auch hemmend und vermittelt die Muskelaktivierung an Synapsen zwischen Nerven und Muskelzellen sowie die Stimulation bestimmter Drüsen. Bei Säugetieren sind einige GABAerge Neuronen, wie z. B. die Kronleuchterzellen, auch in der Lage, ihre glutamatergen Gegenspieler zu erregen. ⓘ
GABAA-Rezeptoren sind ligandenaktivierte Chloridkanäle: Wenn sie durch GABA aktiviert werden, ermöglichen sie den Fluss von Chloridionen durch die Zellmembran. Ob dieser Chloridfluss depolarisierend (macht die Spannung über der Zellmembran weniger negativ), rangierend (hat keinen Einfluss auf das Membranpotenzial der Zelle) oder hemmend/hyperpolarisierend (macht die Zellmembran negativer) ist, hängt von der Richtung des Chloridflusses ab. Wenn das Netto-Chlorid aus der Zelle herausfließt, wirkt GABA depolarisierend; wenn Chlorid in die Zelle hineinfließt, wirkt GABA hemmend oder hyperpolarisierend. Wenn der Netto-Chloridfluss gegen Null geht, wirkt GABA als Shunt. Die Shunting-Hemmung hat keine direkte Auswirkung auf das Membranpotenzial der Zelle; sie verringert jedoch die Wirkung eines zufälligen synaptischen Inputs, indem sie den elektrischen Widerstand der Zellmembran verringert. Die Shunt-Hemmung kann die erregende Wirkung von depolarisierendem GABA "außer Kraft setzen", was zu einer Gesamthemmung führt, auch wenn das Membranpotenzial weniger negativ wird. Es wurde vermutet, dass ein entwicklungsbedingter Wechsel in der molekularen Maschinerie, die die Chloridkonzentration in der Zelle steuert, die funktionelle Rolle von GABA zwischen dem neonatalen und dem erwachsenen Stadium verändert. Mit der Entwicklung des Gehirns bis zum Erwachsenenalter ändert sich die Rolle von GABA von erregend zu hemmend. ⓘ
Entwicklung des Gehirns
Während GABA im reifen Gehirn ein hemmender Transmitter ist, ging man davon aus, dass seine Wirkung im sich entwickelnden Gehirn hauptsächlich erregend ist. Es wurde berichtet, dass der Chloridgradient in unreifen Neuronen umgekehrt ist, wobei das Umkehrpotenzial höher ist als das Ruhemembranpotenzial der Zelle; die Aktivierung eines GABA-A-Rezeptors führt daher zu einem Abfluss von Cl--Ionen aus der Zelle (d. h. zu einem depolarisierenden Strom). Es wurde gezeigt, dass der unterschiedliche Chloridgradient in unreifen Neuronen in erster Linie auf die höhere Konzentration von NKCC1-Kotransportern im Vergleich zu KCC2-Kotransportern in unreifen Zellen zurückzuführen ist. GABAerge Interneuronen reifen im Hippocampus schneller heran, und die GABA-Maschinerie erscheint früher als die glutamaterge Übertragung. Daher gilt GABA in vielen Regionen des Gehirns als wichtigster exzitatorischer Neurotransmitter, bevor die glutamatergen Synapsen ausreifen. ⓘ
In den Entwicklungsstadien, die der Bildung synaptischer Kontakte vorausgehen, wird GABA von den Neuronen synthetisiert und wirkt sowohl als autokriner (auf dieselbe Zelle wirkender) als auch als parakriner (auf benachbarte Zellen wirkender) Signalvermittler. Die ganglionären Eminenzen tragen ebenfalls in hohem Maße zum Aufbau der GABA-ergen kortikalen Zellpopulation bei. ⓘ
GABA reguliert die Proliferation von neuralen Vorläuferzellen, die Migration und Differenzierung, die Verlängerung von Neuriten und die Bildung von Synapsen. ⓘ
GABA reguliert auch das Wachstum von embryonalen und neuralen Stammzellen. GABA kann die Entwicklung neuraler Vorläuferzellen über die Expression des neurotrophen Faktors des Gehirns (BDNF) beeinflussen. GABA aktiviert den GABAA-Rezeptor, wodurch der Zellzyklus in der S-Phase angehalten und das Wachstum begrenzt wird. ⓘ
Außerhalb des Nervensystems
Neben dem Nervensystem wird GABA auch in den insulinproduzierenden β-Zellen der Bauchspeicheldrüse in relativ hohen Mengen produziert. Die β-Zellen sezernieren GABA zusammen mit Insulin, und das GABA bindet an GABA-Rezeptoren auf den benachbarten α-Zellen der Inselzellen und hemmt diese an der Sekretion von Glukagon (was der Wirkung von Insulin entgegenwirken würde). ⓘ
GABA kann die Replikation und das Überleben von β-Zellen fördern und auch die Umwandlung von α-Zellen in β-Zellen begünstigen, was zu neuen Behandlungsmöglichkeiten für Diabetes führen könnte. ⓘ
Neben den GABA-ergen Mechanismen wurde GABA auch in anderen peripheren Geweben wie Darm, Magen, Eileiter, Gebärmutter, Eierstöcke, Hoden, Nieren, Harnblase, Lunge und Leber nachgewiesen, wenn auch in viel geringeren Mengen als in Neuronen oder β-Zellen. ⓘ
Versuche an Mäusen haben gezeigt, dass eine durch eine Fluoridvergiftung ausgelöste Schilddrüsenunterfunktion durch die Gabe von GABA gestoppt werden kann. Der Versuch ergab auch, dass sich die Schilddrüse ohne weitere Hilfe auf natürliche Weise erholte, nachdem das Fluorid durch das GABA vertrieben worden war. ⓘ
Immunzellen exprimieren Rezeptoren für GABA, und die Verabreichung von GABA kann entzündliche Immunreaktionen unterdrücken und "regulatorische" Immunreaktionen fördern, so dass die Verabreichung von GABA in mehreren Tiermodellen nachweislich Autoimmunkrankheiten hemmt. ⓘ
Im Jahr 2018 hat sich gezeigt, dass GABA die Sekretion einer größeren Anzahl von Zytokinen reguliert. Im Plasma von T1D-Patienten sind die Spiegel von 26 Zytokinen erhöht, von denen 16 durch GABA in Zelltests gehemmt werden. ⓘ
Im Jahr 2007 wurde ein erregendes GABA-erges System im Epithel der Atemwege beschrieben. Dieses System wird durch die Einwirkung von Allergenen aktiviert und könnte an den Mechanismen von Asthma beteiligt sein. GABAerge Systeme wurden auch in den Hoden und in der Augenlinse gefunden. ⓘ
Struktur und Konformation
GABA liegt meist als Zwitterion vor (d. h. mit deprotonierter Carboxylgruppe und protonierter Aminogruppe). Seine Konformation hängt von seiner Umgebung ab. In der Gasphase wird eine stark gefaltete Konformation aufgrund der elektrostatischen Anziehung zwischen den beiden funktionellen Gruppen stark begünstigt. Die Stabilisierung beträgt nach quantenchemischen Berechnungen etwa 50 kcal/mol. Im festen Zustand findet sich eine erweiterte Konformation mit einer trans-Konformation am Aminoende und einer gauche-Konformation am Carboxylende. Dies ist auf die Packungswechselwirkungen mit den benachbarten Molekülen zurückzuführen. In Lösung werden aufgrund von Solvatationseffekten fünf verschiedene Konformationen gefunden, von denen einige gefaltet und einige erweitert sind. Die Konformationsflexibilität von GABA ist wichtig für seine biologische Funktion, da es sich an verschiedene Rezeptoren mit unterschiedlichen Konformationen bindet. Viele GABA-Analoga, die pharmazeutisch verwendet werden, haben steifere Strukturen, um die Bindung besser kontrollieren zu können. ⓘ
Geschichte
Im Jahr 1883 wurde GABA erstmals synthetisiert und war zunächst nur als Stoffwechselprodukt von Pflanzen und Mikroben bekannt. ⓘ
Im Jahr 1950 wurde GABA als integraler Bestandteil des zentralen Nervensystems von Säugetieren entdeckt. ⓘ
Im Jahr 1959 wurde gezeigt, dass GABA an einer hemmenden Synapse an Krebsmuskelfasern wie eine Stimulation des hemmenden Nervs wirkt. Sowohl die Hemmung durch Nervenstimulation als auch durch appliziertes GABA wird durch Picrotoxin blockiert. ⓘ
Biosynthese

GABA wird hauptsächlich aus Glutamat über das Enzym Glutamat-Decarboxylase (GAD) mit Pyridoxalphosphat (der aktiven Form von Vitamin B6) als Cofaktor synthetisiert. Dieser Prozess wandelt Glutamat (den wichtigsten erregenden Neurotransmitter) in GABA (den wichtigsten hemmenden Neurotransmitter) um. ⓘ
GABA kann auch aus Putrescin durch Diaminoxidase und Aldehyddehydrogenase synthetisiert werden. ⓘ
Traditionell ging man davon aus, dass exogenes GABA die Blut-Hirn-Schranke nicht durchdringt; nach neueren Forschungsergebnissen ist dies jedoch unklar, da weitere Untersuchungen noch ausstehen. ⓘ
Stoffwechsel
GABA-Transaminase-Enzyme katalysieren die Umwandlung von 4-Aminobutansäure (GABA) und 2-Oxoglutarat (α-Ketoglutarat) in Bernsteinsemialdehyd und Glutamat. Bernsteinsäuresemialdehyd wird anschließend durch Bernsteinsäuresemialdehyd-Dehydrogenase zu Bernsteinsäure oxidiert und gelangt so als nutzbare Energiequelle in den Zitronensäurezyklus. ⓘ
Pharmakologie
Arzneimittel, die als allosterische Modulatoren von GABA-Rezeptoren wirken (so genannte GABA-Analoga oder GABAerge) oder die verfügbare GABA-Menge erhöhen, haben in der Regel entspannende, angstlösende und krampflösende Wirkungen (mit einer dem Lamotrigin vergleichbaren Wirksamkeit, wie Untersuchungen an Mäusen zeigen). Viele der unten aufgeführten Substanzen sind dafür bekannt, dass sie eine anterograde Amnesie und eine retrograde Amnesie verursachen. ⓘ
Im Allgemeinen überwindet GABA die Blut-Hirn-Schranke nicht, obwohl bestimmte Bereiche des Gehirns, die keine wirksame Blut-Hirn-Schranke haben, wie z. B. der periventrikuläre Nukleus, durch Medikamente wie systemisch injiziertes GABA erreicht werden können. Zumindest eine Studie deutet darauf hin, dass oral verabreichtes GABA die Menge des menschlichen Wachstumshormons (HGH) erhöht. GABA, das direkt in das Gehirn injiziert wird, hat Berichten zufolge sowohl stimulierende als auch hemmende Auswirkungen auf die Produktion von Wachstumshormonen, je nach der Physiologie der jeweiligen Person. ⓘ
GABA steigert bei Ratten den Abbau von Serotonin zu N-Acetylserotonin (der Vorstufe von Melatonin). Es wird daher vermutet, dass GABA an der Synthese von Melatonin beteiligt ist und somit regulierende Wirkungen auf den Schlaf und die Fortpflanzungsfunktionen ausüben könnte. ⓘ
Chemie
Obwohl GABA chemisch gesehen eine Aminosäure ist (da es sowohl eine primäre Amin- als auch eine Carbonsäurefunktion hat), wird es in der Fachwelt, in der Wissenschaft und in der Medizin selten als solche bezeichnet. Wenn der Begriff "Aminosäure" ohne einen Zusatz verwendet wird, bezieht er sich üblicherweise auf eine Alpha-Aminosäure. GABA ist keine Alpha-Aminosäure, das heißt, die Aminogruppe ist nicht an das Alpha-Kohlenstoffatom gebunden. Es ist auch nicht in Proteine eingebaut, wie viele andere Alpha-Aminosäuren. ⓘ
GABAerge Medikamente
Die Liganden der GABAA-Rezeptoren sind in der folgenden Tabelle aufgeführt ⓘ
| Aktivität am GABAA | Ligand ⓘ |
|---|---|
| Orthosterischer Agonist | Muscimol, GABA, Gaboxadol (THIP), Isoguvacin, Progabid, Piperidin-4-sulfonsäure (partieller Agonist) |
| Positiv-allosterische Modulatoren | Barbiturate, Benzodiazepine, neuroaktive Steroide, Niacin/Niacinamid, Nicht-Benzodiazepine (d. h. Z-Drogen, z. B. Zolpidem, Etomidat, Alkohol (Ethanol), Methaqualon, Propofol, Stiripentol und Narkosemittel (einschließlich flüchtige Narkosemittel) |
| Orthosterischer (kompetitiver) Antagonist | Bicucullin, Gabazin, Thujon, Flumazenil |
| Unkompetitiver Antagonist (z. B. Kanalblocker) | Cicutoxin |
| Negative allosterische Modulatoren | Furosemid, Önanthotoxin, Amentoflavon |
Zu den GABA-ergen Pro-Drogen gehört Chloralhydrat, das zu Trichlorethanol metabolisiert wird, das dann über den GABAA-Rezeptor wirkt. ⓘ
Die Pflanze Kava enthält GABAerge Verbindungen, darunter Kavain, Dihydrokavain, Methysticin, Dihydromethysticin und Yangonin. ⓘ
Andere GABA-erge Modulatoren sind:
- GABAB-Rezeptor-Liganden.
- GABA-Wiederaufnahmehemmer: Deramciclane, Hyperforin, Tiagabin.
- GABA-Transaminase-Hemmer: Gabaculin, Phenelzin, Valproat, Vigabatrin, Melisse (Melissa officinalis).
- GABA-Analoga: Pregabalin, Gabapentin, Picamilon, Progabid ⓘ
In Pflanzen
GABA kommt auch in Pflanzen vor. Es ist die am häufigsten vorkommende Aminosäure im Apoplast der Tomate. Es gibt auch Hinweise auf eine Rolle bei der Zellsignalisierung in Pflanzen. ⓘ
Rolle von GABA in der Bauchspeicheldrüse
GABA wirkt als inhibitorischer Transmitter in der Bauchspeicheldrüse, indem es in den Langerhans-Inseln die Glucagonsekretion der Alphazellen hemmt. Bakteriell im Darm von überfütterten, adipösen Mäusen produzierte GABA verbesserte die Insulinsekretion und verringerte die Akkumulation von Fettgewebe in der Darmwand. ⓘ
GABA-Modulatoren
Für die Grundlagenforschung werden als GABA-Antagonisten neben dem synthetischen Wirkstoff Gabazin die Pflanzengifte Picrotoxin der Scheinmyrte und Bicucullin der Herzblumen verwendet. Als GABA-Agonist ist Muscimol, eines der Gifte des Fliegenpilzes relevant. Als Agonist in der medizinischen Anwendung dient der Wirkstoff Baclofen. ⓘ