Siliciumdioxid
Eine Probe von Siliziumdioxid ⓘ
| ||
| Bezeichnungen | ||
|---|---|---|
| IUPAC-Bezeichnung
Siliziumdioxid
| ||
Andere Namen
| ||
| Bezeichner | ||
| ChEBI | ||
| ChemSpider | ||
| EC-Nummer |
| |
Gmelin-Referenz
|
200274 | |
| KEGG | ||
| MeSH | Silizium+Dioxid | |
PubChem CID
|
||
| RTECS-Nummer |
| |
| UNII | ||
InChI
| ||
| Eigenschaften | ||
Chemische Formel
|
SiO2 | |
| Molekulare Masse | 60,08 g/mol | |
| Erscheinungsbild | Durchsichtiger Feststoff (amorph) Weiß/Weißgelb (Pulver/Sand) | |
| Dichte | 2,648 (α-Quarz), 2,196 (amorph) g-cm-3 | |
| Schmelzpunkt | 1.713 °C (3.115 °F; 1.986 K) (amorph): 4,88 to | |
| Siedepunkt | 2.950 °C (5.340 °F; 3.220 K) | |
Magnetische Suszeptibilität (χ)
| ||
| Wärmeleitfähigkeit | 12 ( | c-Achse), 6,8 (⊥ c-Achse), 1,4 (am.) W/(m⋅K): 12.213 |
Brechungsindex (nD)
|
1,544 (o), 1,553 (e): 4.143 | |
| Gefährdungen | ||
| NFPA 704 (Feuerdiamant) | ||
| NIOSH (US-Grenzwerte für Gesundheitsgefährdung): | ||
PEL (Zulässig)
|
TWA 20 mppcf (80 mg/m3/%SiO2) (amorph) | |
REL (Empfohlen)
|
TWA 6 mg/m3 (amorph) Ca TWA 0,05 mg/m3 | |
IDLH (Unmittelbare Gefahr)
|
3000 mg/m3 (amorph) Ca [25 mg/m3 (Cristobalit, Tridymit); 50 mg/m3 (Quarz)] | |
| Verwandte Verbindungen | ||
Verwandte Dione
|
Kohlenstoffdioxid Germaniumdioxid Zinndioxid Bleidioxid | |
Verwandte Verbindungen
|
Siliziummonoxid Silizium-Sulfid | |
| Thermochemie | ||
Molare Standard
Entropie (S |
42 J-mol-1-K-1 | |
Std. Bildungsenthalpie
Bildung (ΔfH⦵298) | ||
Sofern nicht anders angegeben, gelten die Daten für Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| ||
Siliciumdioxid, auch Kieselsäure genannt, ist ein Oxid des Siliciums mit der chemischen Formel SiO2, das in der Natur vor allem als Quarz und in verschiedenen lebenden Organismen vorkommt. In vielen Teilen der Welt ist Kieselsäure der Hauptbestandteil von Sand. Kieselsäure ist eine der komplexesten und am häufigsten vorkommenden Materialfamilien, die aus mehreren Mineralien zusammengesetzt ist und auch als synthetisches Produkt vorkommt. Bemerkenswerte Beispiele sind Quarzglas, pyrogene Kieselsäure, Kieselgel, Opal und Aerogele. Es wird in Baumaterialien, in der Mikroelektronik (als elektrischer Isolator) und als Bestandteil in der Lebensmittel- und Pharmaindustrie verwendet. ⓘ
| Kristallstruktur ⓘ | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Grundlegendes Strukturelement der verschiedenen SiO2-Kristallstrukturen ist ein Tetraeder, bei dem ein Siliciumatom von vier Sauerstoffatomen umgeben ist. | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Siliciumdioxid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Verhältnisformel | SiO2 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 60,1 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
je nach Modifikation zwischen 2,19 und 2,66 g·cm−3 | ||||||||||||||||||
| Schmelzpunkt |
1713 °C | ||||||||||||||||||
| Siedepunkt |
> 2200 °C | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Brechungsindex |
1,458 (bei amorpher Dünnschicht λ = 589 nm) | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
| Durchbruchfeldstärke | 4–10 MV/cm (abhängig vom Herstellungsverfahren. z. B. bei nasser thermischer Oxidation 4–6 MV/cm bei trockener höher.) ⓘ |
Im deutschen Sprachraum wird, vorwiegend in der Kautschuk-Industrie, für Siliciumdioxid statt der korrekten Bezeichnung pyrogenes Siliciumdioxid oder gefälltes Siliciumdioxid die Bezeichnung Kieselsäure benutzt oder in letzter Zeit auch das aus dem Englischen übernommene Silica. Der Großteil der weltweiten Sandvorkommen besteht aus Siliciumdioxid (Quarz), denn dieses ist in der oberen kontinentalen Erdkruste nicht nur häufig, sondern aufgrund seiner Härte und seiner chemischen Widerständigkeit auch besonders verwitterungsbeständig. Siliciumdioxid ist der Hauptbestandteil aller Quarz-Gläser. ⓘ
Struktur
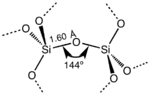


In den meisten Silikaten weist das Siliciumatom eine tetraedrische Koordination auf, wobei vier Sauerstoffatome ein zentrales Si-Atom umgeben (siehe 3-D-Einheitszelle). SiO2 bildet also 3-dimensionale Netzwerkfestkörper, in denen jedes Siliciumatom tetraedrisch an 4 Sauerstoffatome gebunden ist. Im Gegensatz dazu ist CO2 ein lineares Molekül. Die stark unterschiedlichen Strukturen der Kohlenstoff- und Siliciumdioxide sind eine Manifestation der Regel der Doppelbindung. ⓘ
SiO2 hat mehrere kristalline Formen, die jedoch fast immer die gleiche lokale Struktur um Si und O aufweisen. Bei α-Quarz beträgt die Si-O-Bindungslänge 161 pm, während sie bei α-Tridymit im Bereich von 154-171 pm liegt. Auch der Si-O-Si-Winkel schwankt zwischen einem niedrigen Wert von 140° in α-Tridymit und 180° in β-Tridymit. Bei α-Quarz beträgt der Si-O-Si-Winkel 144°. ⓘ
- Polymorphismus ⓘ
Alpha-Quarz ist die stabilste Form von festem SiO2 bei Raumtemperatur. Die Hochtemperaturminerale Cristobalit und Tridymit haben sowohl eine geringere Dichte als auch einen niedrigeren Brechungsindex als Quarz. Die Umwandlung von α-Quarz in Beta-Quarz findet bei 573 °C schlagartig statt. Da die Umwandlung mit einer beträchtlichen Volumenänderung einhergeht, kann sie leicht zum Bruch von Keramiken oder Gesteinen führen, die diese Temperaturgrenze überschreiten. Die Hochdruckminerale Seifertit, Stishovit und Coesit haben jedoch höhere Dichten und Brechungsindizes als Quarz. Stishovit weist eine rutilähnliche Struktur auf, bei der das Silicium in 6-facher Koordination vorliegt. Die Dichte von Stishovit beträgt 4,287 g/cm3, im Vergleich zu α-Quarz, der dichtesten der Niederdruckformen, mit einer Dichte von 2,648 g/cm3. Der Unterschied in der Dichte kann auf die Zunahme der Koordination zurückgeführt werden, da die sechs kürzesten Si-O-Bindungslängen in Stishovit (vier Si-O-Bindungslängen von 176 pm und zwei weitere von 181 pm) größer sind als die Si-O-Bindungslänge (161 pm) in α-Quarz. Die Änderung der Koordination erhöht die Ionizität der Si-O-Bindung. Noch wichtiger ist, dass jede Abweichung von diesen Standardparametern mikrostrukturelle Unterschiede oder Variationen darstellt, die eine Annäherung an einen amorphen, glasartigen oder glasartigen Festkörper bedeuten. ⓘ
Faujasit-Kieselsäure, ein weiteres Polymorph, wird durch Dealuminierung eines natriumarmen, ultrastabilen Y-Zeoliths mit kombinierter Säure- und Wärmebehandlung gewonnen. Das daraus resultierende Produkt enthält über 99 % Siliciumdioxid und hat eine hohe Kristallinität und spezifische Oberfläche (über 800 m2/g). Faujasit-Kieselsäure hat eine sehr hohe thermische und saure Stabilität. So behält es beispielsweise auch nach dem Sieden in konzentrierter Salzsäure einen hohen Grad an molekularer Ordnung oder Kristallinität über weite Strecken bei. ⓘ
- Geschmolzenes SiO2 ⓘ
Geschmolzenes Siliciumdioxid weist mehrere besondere physikalische Eigenschaften auf, die denen von flüssigem Wasser ähneln: negative Temperaturausdehnung, Dichtemaximum bei Temperaturen von ~5000 °C und ein Minimum der Wärmekapazität. Seine Dichte sinkt von 2,08 g/cm3 bei 1950 °C auf 2,03 g/cm3 bei 2200 °C. ⓘ
- Molekulares SiO2 ⓘ
Das molekulare SiO2 hat eine lineare Struktur wie CO2. Es wird durch die Verbindung von Siliciummonoxid (SiO) mit Sauerstoff in einer Argonmatrix hergestellt. Das dimere Siliciumdioxid (SiO2)2 wird durch Reaktion von O2 mit isoliertem dimeren Siliciummonoxid (Si2O2) in einer Matrix gewonnen. Im dimeren Siliciumdioxid sind zwei Sauerstoffatome zwischen den Siliciumatomen mit einem Si-O-Si-Winkel von 94° und einer Bindungslänge von 164,6 pm verankert; die Länge der endständigen Si-O-Bindung beträgt 150,2 pm. Die Si-O-Bindungslänge beträgt 148,3 pm, was mit der Länge von 161 pm in α-Quarz vergleichbar ist. Die Bindungsenergie wird auf 621,7 kJ/mol geschätzt. ⓘ
Natürliches Vorkommen
Geologie
SiO2 kommt in der Natur am häufigsten als Quarz vor, der mehr als 10 % der Masse der Erdkruste ausmacht. Quarz ist das einzige Polymorph der Kieselsäure, das an der Erdoberfläche stabil ist. Metastabile Vorkommen der Hochdruckformen Coesit und Stishovit wurden in der Nähe von Impaktstrukturen und in Verbindung mit Eklogiten gefunden, die während der Ultrahochdruckmetamorphose entstanden sind. Die Hochtemperaturformen von Tridymit und Cristobalit sind aus kieselsäurereichem Vulkangestein bekannt. In vielen Teilen der Welt ist Kieselsäure der Hauptbestandteil von Sand. ⓘ
Biologie
Obwohl Kieselsäure nur schwer löslich ist, kommt sie in vielen Pflanzen wie z. B. Reis vor. Pflanzenmaterial mit hohem Kieselsäuregehalt scheint für Weidetiere, von kauenden Insekten bis zu Huftieren, von Bedeutung zu sein. Kieselsäure beschleunigt die Zahnabnutzung, und ein hoher Kieselsäuregehalt in Pflanzen, die häufig von Pflanzenfressern gefressen werden, könnte sich als Abwehrmechanismus gegen Raubtiere entwickelt haben. ⓘ
Kieselsäure ist auch der Hauptbestandteil von Reishülsenasche, die z. B. in der Filtration und als zusätzliches zementartiges Material (SCM) in der Zement- und Betonherstellung verwendet wird. ⓘ
Die Verkieselung in und durch Zellen ist in der biologischen Welt seit weit über einer Milliarde Jahren üblich. In der modernen Welt kommt sie in Bakterien, Einzellern, Pflanzen und Tieren (Wirbellosen und Wirbeltieren) vor. Prominente Beispiele sind:
- Testate oder Frusteln (d. h. Schalen) von Kieselalgen, Radiolarien und testaten Amöben.
- Phytolithen aus Siliziumdioxid in den Zellen vieler Pflanzen, darunter Equisetaceae, praktisch alle Gräser und eine breite Palette von Zweikeimblättrigen.
- Die Spicula, die das Skelett vieler Schwämme bilden. ⓘ
Kristalline Minerale, die im physiologischen Milieu gebildet werden, weisen oft außergewöhnliche physikalische Eigenschaften auf (z. B. Festigkeit, Härte, Bruchzähigkeit) und neigen dazu, hierarchische Strukturen zu bilden, die eine mikrostrukturelle Ordnung über eine Reihe von Größenordnungen aufweisen. Die Minerale kristallisieren in einer Umgebung, die in Bezug auf Silizium untersättigt ist, und unter Bedingungen mit neutralem pH-Wert und niedriger Temperatur (0-40 °C). ⓘ
Es ist unklar, inwiefern Kieselsäure für die Ernährung von Tieren wichtig ist. Dieses Forschungsgebiet ist eine Herausforderung, da Kieselsäure allgegenwärtig ist und sich in den meisten Fällen nur in Spuren auflöst. Dennoch kommt sie im lebenden Körper durchaus vor, was die Herausforderung mit sich bringt, für Forschungszwecke kieselsäurefreie Kontrollen zu schaffen. Daher ist es schwierig, mit Sicherheit festzustellen, wann das vorhandene Siliziumdioxid eine positive Wirkung hat und wann es nur zufällig vorhanden oder sogar schädlich ist. Der derzeitige Konsens ist, dass Kieselsäure für das Wachstum, die Festigkeit und das Management vieler Bindegewebe wichtig zu sein scheint. Dies gilt nicht nur für hartes Bindegewebe wie Knochen und Zähne, sondern möglicherweise auch für die Biochemie der subzellulären enzymhaltigen Strukturen. ⓘ
Verwendungen
Strukturelle Verwendung
Etwa 95 % der kommerziellen Verwendung von Siliziumdioxid (Sand) erfolgt in der Bauindustrie, z. B. bei der Herstellung von Beton (Portlandzementbeton). ⓘ
Bestimmte Quarzsandvorkommen, die die gewünschte Korngröße und -form sowie den gewünschten Gehalt an Ton und anderen Mineralien aufweisen, waren für den Sandguss von Metallerzeugnissen wichtig. Der hohe Schmelzpunkt von Quarzsand ermöglicht seine Verwendung in solchen Anwendungen wie dem Eisenguss; beim modernen Sandguss werden manchmal andere Mineralien aus anderen Gründen verwendet. ⓘ
Kristalline Kieselsäure wird beim Hydraulic Fracturing von Formationen verwendet, die Tight Oil und Schiefergas enthalten. ⓘ
Vorläufer von Glas und Silizium
Siliziumdioxid ist der Hauptbestandteil bei der Herstellung der meisten Gläser. Wenn andere Mineralien mit Kieselsäure verschmolzen werden, senkt das Prinzip der Gefrierpunktserniedrigung den Schmelzpunkt der Mischung und erhöht die Fließfähigkeit. Die Glasübergangstemperatur von reinem SiO2 liegt bei etwa 1475 K. Wenn geschmolzenes Siliziumdioxid SiO2 schnell abgekühlt wird, kristallisiert es nicht, sondern erstarrt als Glas. Aus diesem Grund enthalten die meisten keramischen Glasuren Kieselsäure als Hauptbestandteil. ⓘ
Die strukturelle Geometrie von Silizium und Sauerstoff in Glas ähnelt der in Quarz und den meisten anderen kristallinen Formen von Silizium und Sauerstoff, wobei das Silizium von regelmäßigen Tetraedern aus Sauerstoffzentren umgeben ist. Der Unterschied zwischen Glas und kristallinen Formen ergibt sich aus der Konnektivität der tetraedrischen Einheiten: Obwohl es im glasartigen Netzwerk keine langreichweitige Periodizität gibt, bleibt die Ordnung auf Längenskalen weit über die SiO-Bindungslänge hinaus bestehen. Ein Beispiel für diese Ordnung ist die Vorliebe für die Bildung von Ringen aus 6-Tetraedern. ⓘ
Die meisten optischen Fasern für die Telekommunikation werden ebenfalls aus Siliziumdioxid hergestellt. Es ist ein Hauptrohstoff für viele Keramiken wie Steingut, Steinzeug und Porzellan. ⓘ
Siliziumdioxid wird zur Herstellung von elementarem Silizium verwendet. Das Verfahren umfasst eine karbothermische Reduktion in einem elektrischen Lichtbogenofen:
Pyrogene Kieselsäure
Pyrogene Kieselsäure, auch pyrogene Kieselsäure genannt, wird durch Verbrennen von SiCl4 in einer sauerstoffreichen Wasserstoffflamme hergestellt, wobei ein "Rauch" aus SiO2 entsteht. ⓘ
Sie kann auch durch Verdampfen von Quarzsand in einem elektrischen Lichtbogen bei 3000 °C hergestellt werden. Bei beiden Verfahren entstehen mikroskopisch kleine Tröpfchen amorphen Siliziumdioxids, die zu verzweigten, kettenförmigen, dreidimensionalen Sekundärpartikeln verschmelzen, die dann zu Tertiärpartikeln agglomerieren, einem weißen Pulver mit extrem niedriger Schüttdichte (0,03-,15 g/cm3) und damit hoher Oberfläche. Die Partikel wirken als thixotropes Verdickungsmittel oder als Antibackmittel und können so behandelt werden, dass sie entweder hydrophil oder hydrophob für Anwendungen in Wasser oder organischen Flüssigkeiten werden. ⓘ

Silicastaub ist ein ultrafeines Pulver, das als Nebenprodukt bei der Herstellung von Silicium und Ferrosiliciumlegierungen anfällt. Es besteht aus amorphen (nicht kristallinen) kugelförmigen Partikeln mit einem durchschnittlichen Partikeldurchmesser von 150 nm, ohne die Verzweigungen des pyrogenen Produkts. Es wird hauptsächlich als Puzzolanmaterial für Hochleistungsbeton verwendet. Nanopartikel aus pyrogener Kieselsäure können erfolgreich als Alterungsschutzmittel in Asphaltbindemitteln eingesetzt werden. ⓘ
Lebensmittel, kosmetische und pharmazeutische Anwendungen
Kieselsäure, entweder in kolloidaler, gefällter oder pyrogener Form, ist ein gängiger Zusatzstoff in der Lebensmittelproduktion. Sie wird vor allem als Fließ- oder Antibackmittel in pulverförmigen Lebensmitteln wie Gewürzen und milchfreiem Kaffeeweißer oder in Pulvern verwendet, die zu pharmazeutischen Tabletten geformt werden. In hygroskopischen Anwendungen kann es Wasser adsorbieren. Kolloidale Kieselsäure wird als Schönungsmittel für Wein, Bier und Saft verwendet und trägt die E-Nummer E551. ⓘ
In Kosmetika ist Kieselsäure wegen ihrer lichtstreuenden Eigenschaften und ihrer natürlichen Absorptionsfähigkeit nützlich. ⓘ
Kieselgur, ein Bergbauprodukt, wird seit Jahrhunderten in Lebensmitteln und Kosmetika verwendet. Sie besteht aus den Siliziumdioxidschalen mikroskopisch kleiner Kieselalgen; in einer weniger verarbeiteten Form wurde sie als "Zahnpulver" verkauft. Hergestelltes oder abgebautes hydratisiertes Siliziumdioxid wird als hartes Schleifmittel in Zahnpasta verwendet. ⓘ
Halbleiter
Siliciumdioxid wird in der Halbleitertechnologie häufig verwendet ⓘ
- für die Primärpassivierung (direkt auf der Halbleiteroberfläche),
- als ursprüngliches Gate-Dielektrikum in der MOS-Technologie. Heute, da die Skalierung (Dimension der Gate-Länge des MOS-Transistors) unter 10 nm fortgeschritten ist, wurde Siliziumdioxid durch andere dielektrische Materialien wie Hafniumoxid oder ähnliche Materialien mit einer höheren Dielektrizitätskonstante im Vergleich zu Siliziumdioxid ersetzt,
- als dielektrische Schicht zwischen metallischen (Verdrahtungs-)Schichten (manchmal bis zu 8-10) Verbindungselementen und
- als zweite Passivierungsschicht (zum Schutz der Halbleiterelemente und der Metallisierungsschichten), die heute in der Regel mit anderen Dielektrika wie Siliziumnitrid beschichtet ist. ⓘ
Da Siliziumdioxid ein natives Oxid von Silizium ist, ist es im Vergleich zu anderen Halbleitern wie Galliumarsenid oder Indiumphosphid weiter verbreitet. ⓘ
Siliziumdioxid könnte auf einer Silizium-Halbleiteroberfläche aufgewachsen werden. Siliziumoxidschichten könnten Siliziumoberflächen während Diffusionsprozessen schützen und zur Diffusionsmaskierung verwendet werden. ⓘ
Die Oberflächenpassivierung ist der Prozess, durch den eine Halbleiteroberfläche inertisiert wird und die Halbleitereigenschaften durch die Wechselwirkung mit Luft oder anderen Materialien, die mit der Oberfläche oder dem Rand des Kristalls in Kontakt kommen, nicht verändert werden. Durch die Bildung einer thermisch gewachsenen Siliziumdioxidschicht wird die Konzentration elektronischer Zustände an der Siliziumoberfläche stark reduziert. SiO2-Schichten bewahren die elektrischen Eigenschaften von p-n-Übergängen und verhindern, dass sich diese elektrischen Eigenschaften durch die gasförmige Umgebung verschlechtern. Siliziumoxidschichten können zur elektrischen Stabilisierung von Siliziumoberflächen verwendet werden. Die Oberflächenpassivierung ist eine wichtige Methode zur Herstellung von Halbleiterbauelementen, bei der ein Siliziumwafer mit einer isolierenden Schicht aus Siliziumoxid beschichtet wird, damit der Strom zuverlässig zum darunter liegenden leitenden Silizium durchdringen kann. Das Aufwachsen einer Siliziumdioxidschicht auf einem Siliziumwafer ermöglicht es, die Oberflächenzustände zu überwinden, die sonst verhindern, dass Elektrizität die Halbleiterschicht erreicht. ⓘ
Der Prozess der Passivierung der Siliziumoberfläche durch thermische Oxidation (Siliziumdioxid) ist für die Halbleiterindustrie von entscheidender Bedeutung. Es wird üblicherweise zur Herstellung von Metall-Oxid-Halbleiter-Feldeffekttransistoren (MOSFETs) und von Chips für integrierte Siliziumschaltungen (mit dem Planarverfahren) verwendet. ⓘ
Andere
Hydrophobes Siliziumdioxid wird als Entschäumerkomponente verwendet. ⓘ
In ihrer Eigenschaft als feuerfestes Material ist sie in Form von Fasern als Hochtemperatur-Wärmeschutzgewebe nützlich. ⓘ
Kieselsäure wird bei der Extraktion von DNA und RNA verwendet, da sie sich in Gegenwart von Chaotropen an die Nukleinsäuren binden kann. ⓘ
Silica-Aerogel wurde in der Raumsonde Stardust verwendet, um extraterrestrische Partikel zu sammeln. ⓘ
Reine Kieselsäure (Siliziumdioxid) kann, wenn sie als geschmolzener Quarz zu einem Glas ohne echten Schmelzpunkt abgekühlt wird, als Glasfaser für Glasfasern verwendet werden. ⓘ
Herstellung
Siliziumdioxid wird meist durch Bergbau gewonnen, einschließlich Sandabbau und Reinigung von Quarz. Quarz eignet sich für viele Zwecke, während eine chemische Verarbeitung erforderlich ist, um ein reineres oder anderweitig geeigneteres (z. B. reaktiveres oder feinkörnigeres) Produkt herzustellen. ⓘ
Gefällte Kieselsäure
Gefällte Kieselsäure oder amorphe Kieselsäure wird durch Ansäuern von Natriumsilikatlösungen hergestellt. Der gallertartige Niederschlag oder das Kieselgel wird zunächst gewaschen und dann dehydriert, um farblose mikroporöse Kieselsäure zu erhalten. Die idealisierte Gleichung mit einem Trisilikat und Schwefelsäure lautet:
Etwa eine Milliarde Kilogramm/Jahr (1999) Kieselsäure wurden auf diese Weise hergestellt, hauptsächlich für die Verwendung in Polymer-Verbundwerkstoffen - Reifen und Schuhsohlen. ⓘ
Auf Mikrochips
Dünne Schichten aus Siliziumdioxid wachsen spontan auf Siliziumscheiben durch thermische Oxidation, wobei eine sehr flache Schicht von etwa 1 nm oder 10 Å des so genannten nativen Oxids entsteht. Höhere Temperaturen und alternative Umgebungen werden verwendet, um gut kontrollierte Schichten aus Siliziumdioxid auf Silizium wachsen zu lassen, zum Beispiel bei Temperaturen zwischen 600 und 1200 °C, unter Verwendung der so genannten Trockenoxidation mit O2 ⓘ
oder Nassoxidation mit H2O. ⓘ
Die native Oxidschicht ist in der Mikroelektronik von Vorteil, wo sie als elektrischer Isolator mit hoher chemischer Stabilität wirkt. Sie kann das Silizium schützen, Ladung speichern, Strom blockieren und sogar als kontrollierter Pfad zur Begrenzung des Stromflusses dienen. ⓘ
Labor- oder Spezialverfahren
Aus siliziumorganischen Verbindungen
Viele Wege zur Herstellung von Siliciumdioxid beginnen mit einer siliciumorganischen Verbindung, z. B. HMDSO, TEOS. Die Synthese von Siliziumdioxid wird im Folgenden anhand von Tetraethylorthosilikat (TEOS) dargestellt. Durch einfaches Erhitzen von TEOS auf 680-730 °C entsteht das Oxid:
In ähnlicher Weise verbrennt TEOS bei etwa 400 °C:
TEOS wird durch den so genannten Sol-Gel-Prozess hydrolysiert. Der Verlauf der Reaktion und die Art des Produkts werden durch Katalysatoren beeinflusst, aber die idealisierte Gleichung gilt:
Andere Methoden
Da Siliziumdioxid sehr stabil ist, kann es mit vielen Methoden gewonnen werden. Die Verbrennung von Silan ist konzeptionell einfach, aber von geringem praktischem Wert und ergibt Siliciumdioxid. Diese Reaktion ist analog zur Verbrennung von Methan:
Die chemische Abscheidung von Siliciumdioxid aus der Gasphase auf der Kristalloberfläche von Silan wurde jedoch unter Verwendung von Stickstoff als Trägergas bei 200-500 °C eingesetzt. ⓘ
Chemische Reaktionen
Siliciumdioxid wird durch Reduktion mit Kohlenstoff in Silicium umgewandelt. ⓘ
Fluor reagiert mit Siliciumdioxid unter Bildung von SiF4 und O2, während die anderen Halogengase (Cl2, Br2, I2) im Wesentlichen nicht reaktiv sind. ⓘ
Die meisten Formen von Siliciumdioxid (mit Ausnahme von Stishovit, das nicht in nennenswertem Umfang reagiert) werden von Fluorwasserstoffsäure (HF) angegriffen, um Hexafluorkieselsäure zu bilden:
HF wird in der Halbleiterindustrie zur Entfernung oder Strukturierung von Siliziumdioxid verwendet. ⓘ
Unter normalen Bedingungen reagiert Silizium nicht mit den meisten Säuren, sondern wird von Flusssäure aufgelöst. ⓘ
Silizium wird von Basen wie wässrigem Natriumhydroxid angegriffen, wobei Silikate entstehen. ⓘ
Siliciumdioxid wirkt wie eine Lux-Flood-Säure und kann unter bestimmten Bedingungen mit Basen reagieren. Da es keinen Wasserstoff enthält, kann nicht hydratisierte Kieselsäure nicht direkt als Brønsted-Lowry-Säure wirken. Während Siliciumdioxid bei niedrigem oder neutralem pH-Wert nur schwer in Wasser löslich ist (typischerweise 2 × 10-4 M für Quarz bis 10-3 M für kryptokristallinen Chalcedon), reagieren starke Basen mit Glas und lösen es leicht auf. Daher müssen starke Basen in Kunststoffflaschen aufbewahrt werden, um ein Verklemmen des Flaschenverschlusses zu vermeiden, die Unversehrtheit des Gefäßes zu erhalten und eine unerwünschte Kontamination durch Silikatanionen zu verhindern. ⓘ
Siliciumdioxid löst sich in heißer konzentrierter Lauge oder in geschmolzenem Hydroxid, wie in dieser idealisierten Gleichung beschrieben:
Siliciumdioxid neutralisiert basische Metalloxide (z. B. Natriumoxid, Kaliumoxid, Blei(II)-oxid, Zinkoxid oder Mischungen von Oxiden, wobei sich Silikate und Gläser bilden, da die Si-O-Si-Bindungen im Siliciumdioxid nacheinander gebrochen werden). Die Reaktion von Natriumoxid und SiO2 kann beispielsweise Natriumorthosilicat, Natriumsilicat und Gläser hervorbringen, abhängig von den Anteilen der Reaktionspartner:
- . ⓘ
Beispiele für solche Gläser haben kommerzielle Bedeutung, z. B. Kalknatronglas, Borosilikatglas, Bleiglas. In diesen Gläsern wird die Kieselsäure als Netzbildner oder Gitterbildner bezeichnet. Die Reaktion wird auch in Hochöfen eingesetzt, um Sandverunreinigungen im Erz durch Neutralisation mit Calciumoxid zu entfernen, wobei Calciumsilicatschlacke entsteht. ⓘ

Siliciumdioxid reagiert in erhitztem Rückfluss unter Distickstoff mit Ethylenglykol und einer Alkalimetallbase zu hochreaktiven, pentakoordinierten Silikaten, die den Zugang zu einer Vielzahl neuer Siliciumverbindungen ermöglichen. Die Silikate sind im Wesentlichen in allen polaren Lösungsmitteln außer Methanol unlöslich. ⓘ
Siliciumdioxid reagiert bei hohen Temperaturen mit elementarem Silicium und bildet SiO:
Wasserlöslichkeit
Die Wasserlöslichkeit von Siliciumdioxid hängt stark von seiner kristallinen Form ab und ist bei Siliciumdioxid drei- bis viermal höher als bei Quarz; als Funktion der Temperatur erreicht sie bei 340 °C (644 °F) ihren Höhepunkt. Diese Eigenschaft wird für die Züchtung von Quarz-Einkristallen in einem hydrothermalen Verfahren genutzt, bei dem natürlicher Quarz in überhitztem Wasser in einem Druckbehälter gelöst wird, der nach oben hin kühler ist. Kristalle von 0,5-1 kg können 1-2 Monate lang gezüchtet werden. Diese Kristalle sind eine Quelle für sehr reines Quarz, das in elektronischen Anwendungen eingesetzt wird. Oberhalb der kritischen Temperatur von Wasser von 647,096 K (373,946 °C; 705,103 °F) und einem Druck von 22,064 Megapascal (3.200,1 psi) oder höher ist Wasser eine überkritische Flüssigkeit und die Löslichkeit ist wieder höher als bei niedrigeren Temperaturen. ⓘ
Gesundheitliche Auswirkungen

Oral aufgenommenes Siliziumdioxid ist im Wesentlichen ungiftig, mit einer LD50 von 5000 mg/kg (5 g/kg). Eine Studie aus dem Jahr 2008, in der Probanden 15 Jahre lang beobachtet wurden, ergab, dass ein höherer Gehalt an Kieselsäure im Wasser das Demenzrisiko zu senken scheint. Eine Erhöhung des Kieselsäuregehalts im Trinkwasser um 10 mg/Tag wurde mit einem um 11 % verringerten Demenzrisiko in Verbindung gebracht. ⓘ
Das Einatmen von fein verteiltem kristallinem Siliziumdioxidstaub kann zu Silikose, Bronchitis oder Lungenkrebs führen, da sich der Staub in der Lunge festsetzt und das Gewebe kontinuierlich reizt, was die Lungenkapazität verringert. Wenn feine Siliziumdioxidpartikel in ausreichender Menge eingeatmet werden (z. B. bei beruflicher Exposition), erhöht sich das Risiko für systemische Autoimmunerkrankungen wie Lupus und rheumatoide Arthritis im Vergleich zu den in der Allgemeinbevölkerung erwarteten Raten. ⓘ
Berufliche Gefährdung
Siliziumdioxid ist ein Berufsrisiko für Personen, die Sandstrahlen oder mit Produkten arbeiten, die pulverförmiges kristallines Siliziumdioxid enthalten. Amorphe Kieselsäure, wie z. B. pyrogene Kieselsäure, kann in einigen Fällen irreversible Lungenschäden verursachen, wird jedoch nicht mit der Entwicklung von Silikose in Verbindung gebracht. Kinder, Asthmatiker jeden Alters, Allergiker und ältere Menschen (die alle eine reduzierte Lungenkapazität haben) können in kürzerer Zeit betroffen sein. ⓘ
Kristallines Siliziumdioxid ist ein Berufsrisiko für diejenigen, die mit Steinarbeitsplatten arbeiten, da beim Schneiden und Verlegen der Arbeitsplatten große Mengen an Siliziumdioxid in der Luft entstehen. Kristallines Siliziumdioxid, das beim Hydraulic Fracturing verwendet wird, stellt ein Gesundheitsrisiko für die Arbeiter dar. ⓘ
Pathophysiologie
Im Körper lösen sich kristalline Kieselsäurepartikel über klinisch relevante Zeiträume nicht auf. Kieselsäurekristalle in der Lunge können das NLRP3-Inflammasom in Makrophagen und dendritischen Zellen aktivieren und dadurch die Produktion von Interleukin, einem stark entzündungsfördernden Zytokin im Immunsystem, auslösen. ⓘ
Verordnung
In den Verordnungen zur Beschränkung der Silikaexposition "im Hinblick auf die Silikosegefahr" ist festgelegt, dass sie sich nur auf kristallines und staubförmiges Silika beziehen. ⓘ
Im Jahr 2013 senkte die US-amerikanische Behörde für Arbeitssicherheit und Gesundheitsschutz den Grenzwert auf 50 µg/m3 Luft. Vor 2013 waren 100 µg/m3 und bei Bauarbeitern sogar 250 µg/m3 zulässig. Im Jahr 2013 verlangte die OSHA auch die "grüne Fertigstellung" von Fracking-Bohrlöchern, um die Exposition gegenüber kristallinem Siliziumdioxid zu verringern und den Grenzwert zu senken. ⓘ
Kristalline Formen
SiO2 kommt in vielen kristallinen Formen vor, mehr als fast alle anderen Materialien. Diese Formen werden als Polymorphe bezeichnet. ⓘ
| Form | Kristallsymmetrie Pearson-Symbol, Gruppen-Nr. |
ρ g/cm3 |
Anmerkungen | Struktur ⓘ |
|---|---|---|---|---|
| α-Quarz | rhomboedrisch (trigonal) hP9, P3121 Nr.152 |
2.648 | Helixketten machen einzelne Einkristalle optisch aktiv; α-Quarz wandelt sich bei 846 K in β-Quarz um | 
|
| β-Quarz | hexagonal hP18, P6222, Nr. 180 |
2.533 | Eng verwandt mit α-Quarz (mit einem Si-O-Si-Winkel von 155°) und optisch aktiv; β-Quarz wandelt sich bei 1140 K in β-Tridymit um | 
|
| α-Tridymit | orthorhombisch oS24, C2221, Nr.20 |
2.265 | Metastabile Form unter Normaldruck | 
|
| β-Tridymit | hexagonal hP12, P63/mmc, Nr. 194 |
Eng verwandt mit α-Tridymit; β-Tridymit wandelt sich bei 2010 K in β-Cristobalit um | 
| |
| α-Cristobalit | tetragonal tP12, P41212, Nr. 92 |
2.334 | Metastabile Form unter Normaldruck | 
|
| β-Cristobalit | kubisch cF104, Fd3m, Nr. 227 |
Eng verwandt mit α-Cristobalit; schmilzt bei 1978 K | 
| |
| Keatit | tetragonal tP36, P41212, Nr. 92 |
3.011 | Si5O10, Si4O8, Si8O16-Ringe; synthetisiert aus glasartiger Kieselsäure und Alkali bei 600-900 K und 40-400 MPa | 
|
| Moganit | monoklin mS46, C2/c, Nr.15 |
Si4O8- und Si6O12-Ringe | 
| |
| Coesit | monoklin mS48, C2/c, Nr. 15 |
2.911 | Si4O8- und Si8O16-Ringe; 900 K und 3-3,5 GPa | 
|
| Stishovit | tetragonal tP6, P42/mnm, Nr.136 |
4.287 | Eines der dichtesten (zusammen mit Seifertit) Polymorphe der Kieselsäure; rutilähnlich mit 6-fach koordiniertem Si; 7,5-8,5 GPa | 
|
| Seifertit | orthorhombisch oP, Pbcn |
4.294 | Eines der dichtesten (zusammen mit Stishovit) Polymorphe von Siliciumdioxid; entsteht bei Drücken über 40 GPa. | 
|
| Melanophlogit | kubisch (cP*, P4232, Nr.208) oder tetragonal (P42/nbc) | 2.04 | Si5O10-, Si6O12-Ringe; Mineral, das immer mit Kohlenwasserstoffen in Zwischenräumen vorkommt - ein Clathrasil (Kieselsäureclathrat) | 
|
| faserig W-Kieselsäure |
orthorhombisch oI12, Ibam, Nr.72 |
1.97 | wie SiS2, bestehend aus kantenteilenden Ketten, schmilzt bei ~1700 K | 
|
| 2D-Kieselsäure | hexagonal | Blattartige Doppelschichtstruktur | 
|
Sicherheit
Das Einatmen von fein verteiltem kristallinem Siliziumdioxid kann zu schweren Entzündungen des Lungengewebes, Silikose, Bronchitis, Lungenkrebs und systemischen Autoimmunkrankheiten wie Lupus und rheumatoider Arthritis führen. Das Einatmen von amorphem Siliziumdioxid in hohen Dosen führt zu einer nicht dauerhaften kurzfristigen Entzündung, bei der alle Auswirkungen abheilen. ⓘ
Andere Namen
Diese erweiterte Liste zählt Synonyme für Siliziumdioxid auf; alle diese Werte stammen aus einer einzigen Quelle; die Werte in der Quelle wurden großgeschrieben dargestellt.
- CAS 112945-52-5
- Acitcel
- Aerosil
- Amorpher Kieselsäurestaub
- Aquafil
- CAB-O-GRIP II
- CAB-O-SIL
- CAB-O-SPERSE
- Katalog
- Kolloidales Siliziumdioxid
- Kolloidales Siliziumdioxid
- Dicalite
- DRI-DIE Insektizid 67
- FLO-GARD
- Fossiles Mehl
- Pyrogene Kieselsäure
- Pyrogenes Siliziumdioxid
- HI-SEL
- LO-VEL
- Ludox
- Nalcoag
- Nyacol
- Santocel
- Kieselsäure
- Kieselsäure-Aerogel
- Kieselsäure, amorphe
- Kieselsäureanhydrid
- Kieselsäure
- Synthetische amorphe Kieselsäure
- Vulkasil ⓘ
Mineralogie und Vorkommen

Amorphes SiO2
Nichtkristallines (amorphes) SiO2 kommt in der Natur als wesentlicher Bestandteil in folgenden Substanzen vor, die in ihrer Zusammensetzung sehr inhomogen und uneinheitlich sind:
- biogen: Skelette von Radiolarien, Diatomeen und Schwämmen aus Opal, diagenetisch zu Gestein verfestigt, zum Beispiel zu Kieselschiefer
- Geyserit: amorphe Sinterprodukte heißer Quellen
- Tachylit: vulkanisches Glas basaltischer Zusammensetzung, das neben SiO2 größere Gehalte an FeO, MgO, CaO und Al2O3 enthält
- Obsidian: vulkanisches Glas granitischer Zusammensetzung
- Tektit: Gesteinsgläser, entstanden durch Schmelzen von Gestein infolge von Meteoriteneinschlägen
- Lechatelierit: reines natürliches SiO2-Glas, wie es z. B. in Tektiten vorkommt oder bei Blitzeinschlägen in Quarzsande entsteht (Fulgurit)
- Opal
- SiO2-Schmelze: bei Temperaturen oberhalb von 1727 °C (bei 1 bar) ⓘ
Kristallines SiO2
Im Gegensatz zum amorphen SiO2 haben die kristallinen Formen nur eine sehr geringe Toleranz gegenüber Verunreinigungen. Sie unterscheiden sich nur in ihrer Struktur.
- Mogánit (Chalcedon)
- α-Quarz (Tiefquarz): Bildungsbedingungen: Temperatur T < 573 °C, Druck p < 20 kbar
- β-Quarz (Hochquarz): 573 °C < T < 867 °C, p < 30 kbar
- Tridymit: 867 °C < T <1470 °C, p < 5 kbar
- Cristobalit: 1470 °C < T < 1727 °C
- Coesit: 20 kbar < p < 75 kbar
- Stishovit: 75 kbar < p < ? kbar ⓘ
Siliciumdioxid bildet als Teil von Silicaten wie z. B. Feldspat, Tonmineralen oder in freier Form als Quarz den Hauptbestandteil der Erdkruste und somit auch die häufigste Siliciumverbindung. ⓘ
Kieselsäureanhydrid
In der Natur kommen Stützgerüste aus Kieselsäureanhydrid in pflanzlichen und tierischen Lebewesen vor, etwa bei den im Meer weit verbreiteten Kieselalgen (Diatomeen) und Strahlentierchen (Radiolarien) und Glasschwämmen (Hexactinellida) sowie beim Schachtelhalm. Die Kieselsäureanhydrid-Skelette abgestorbener Kieselalgen und Strahlentierchen sinken auf den Meeresgrund, reichern sich dort an und bilden Ablagerungen aus Kieselgur (Diatomeenerde) bzw. Radiolarienschlamm. Ablagerungen aus dem Miozän enthalten 70–90 % SiO2, 3–12 % Wasser und Spuren von Metalloxiden. ⓘ
Technische Herstellung
Synthetisches SiO2, das meist amorph vorliegt, wird großtechnisch in unterschiedlichen Prozessen in großen Mengen erzeugt. Als Sammelbegriff wird neudeutsch auch „Silica“ verwendet. ⓘ
Die großtechnische Herstellung von synthetischem SiO2 erfolgt hauptsächlich über Fällungsprozesse, ausgehend von Wasserglas, das durch Aufschließen von Quarzsand mit Natriumcarbonat oder Kaliumcarbonat erhältlich ist. So erzeugtes SiO2 nennt man je nach Prozessbedingungen gefälltes Siliciumdioxid (historisch: Fällungskieselsäuren), Kieselsolen oder Kieselgele. Eine weitere wichtige Herstellungsvariante ist die Erzeugung von so genanntem pyrogenem SiO2 in einer Knallgasflamme, ausgehend von flüssigen Chlorsilanen wie Siliciumtetrachlorid (SiCl4). ⓘ
Pyrogenes Siliciumdioxid
Pyrogenes Siliciumdioxid ist amorphes SiO2-Pulver von 5–50 nm Durchmesser und mit einer spezifischen Oberfläche von 50 bis 600 m2/g. Der Name verweist auf das häufig angewandte Herstellungsverfahren durch Flammenhydrolyse: der bei der Verbrennung von Knallgas entstehende Wasserdampf zersetzt Silane zu SiO2, eine andere Methode nutzt SiCl4 als Si-Quelle. In wartungsfreien Blei-Säure-Akkumulatoren wird pyrogenes Siliciumdioxid als Ausgangsstoff für den Gelelektrolyten verwendet, worin der Massenanteil an SiO2 aber nur wenige Prozente ausmacht. ⓘ
Technische Anwendung
Synthetisches SiO2 spielt im Alltag meist unbemerkt eine große Rolle. In Farben und Lacken, Kunst- und Klebstoffen ist es ebenso wichtig wie in modernen Fertigungsprozessen in der Halbleitertechnik oder als Pigment in Inkjetpapier-Beschichtungen. Als ungiftige Substanz ist es in pharmazeutischen Artikeln genauso vertreten wie in kosmetischen Produkten, wird in Lebensmittelprozessen (z. B. Bierklärung) und als Putzhilfe in Zahnpasta verwendet. Auch findet Siliciumdioxid Anwendung in der biologischen Landwirtschaft: es wird dort in Form eines feinen Pulvers zur Vorbeugung gegen Kornkäferbefall mit Getreide vermischt. Mengenmäßig zu den Hauptanwendungen zählen der Einsatz als Füllstoff für Kunststoffe und Dichtmassen, insbesondere in Gummiartikeln. Autoreifen profitieren von der Verstärkung durch ein spezielles SiO2-System. ⓘ
Die mengenmäßig größte Bedeutung kommt Siliciumdioxid in Form von Glas zu. Meistens wird es mit Stoffen wie Aluminiumoxid, Bortrioxid, Calcium- und Natriumoxid vermischt, um die Schmelztemperatur zu senken, die Verarbeitung zu erleichtern oder die Eigenschaften des Endprodukts zu verbessern. Reines Siliciumdioxid ist schwer schmelzbares Quarzglas, das besonders temperatur- und temperaturwechselbeständig ist. ⓘ
Quarzglas wird in der Optik in Form von Linsen, Prismen etc. verwendet. Im chemischen Labor wird Quarzglas als Geräteglas eingesetzt, sobald besonders hohe UV-Durchlässigkeit oder Temperaturfestigkeit gefordert wird. Einen glühenden Quarztiegel kann man in kaltes Wasser tauchen, ohne dass er springt. Dennoch wird im Labor üblicherweise das ebenfalls temperaturwechselbeständige Borosilicatglas verwendet, da es billiger in der Herstellung und Verarbeitung ist. ⓘ
Ein weiteres Anwendungsgebiet von Siliciumdioxid ist die Betonherstellung. So ist dieser Stoff Hauptbestandteil von Microsilica, einem Zusatzstoff bei der Produktion von Hochleistungsbeton und Ultrahochleistungsbetonen (C100…). Der Silicastaub reagiert mit dem Calciumhydroxid (Ca(OH)2), das bei der Zementhydratation freigesetzt wird, und formt so genannte Calciumsilicathydrat-Phasen. Weiter führen die Partikel in der Größenordnung von 0,1 µm zu einer mechanischen Erhöhung der Festigkeit, indem der Kapillarporenanteil im Zementstein verringert wird. ⓘ
Auch wird SiO2 in der Lebensmittelindustrie als Lebensmittelzusatzstoff (E 551) eingesetzt. So findet man es beispielsweise in Form von Kieselsäure als Rieselhilfe für Speisesalz, in Gewürzen und Gewürzmischungen. Wegen Bedenken in Bezug auf die enthaltenen Nanopartikel hat Bio Suisse die Zulassung von E 551 ab Anfang 2019 beendet. ⓘ
In der pharmazeutischen Technologie wird feindisperses Siliciumdioxid als pharmazeutischer Hilfsstoff bei der Herstellung von Tabletten verwendet. ⓘ
Eine weitere Verwendungsmöglichkeit für Siliciumdioxid findet sich in der Pyrotechnik. Dort wird es unter anderem für die Herstellung von Brandgelen verwendet. ⓘ
Siliciumdioxid in der Halbleitertechnik
Siliciumdioxid ist ein wichtiges Material in der Halbleiter- und Mikrosystemtechnik. Hauptsächlich wird es als Isolations- und Passivierungsmaterial eingesetzt, beispielsweise als Gate-Dielektrikum der eingesetzten Transistoren oder als Zwischenmetalldielektrikum in der Verdrahtungsebene von integrierten Schaltkreisen. Diese Schichten werden beispielsweise durch thermische Oxidation von Silicium oder durch chemische Gasphasenabscheidung hergestellt und sind meist amorph. Da die elektrischen Eigenschaften für aktuelle mikroelektronische Produkte nicht mehr ausreichend sind, wird Siliciumdioxid seit Mitte der 2000er Jahre nach und nach von sogenannten Low-k- und High-k-Dielektrika verdrängt. Ein weiterer Anwendungsbereich von Siliciumdioxid (sowohl Quarz als auch spezielle Gläser) ist die Fotolithografie, wo es als Trägermaterial für Masken eingesetzt wird. ⓘ
Dünne Schichten aus Siliciumoxid können durch verschiedene Beschichtungsverfahren hergestellt werden. Die einfachste Art der Herstellung von Siliciumoxidschichten auf kristallinem Silicium ist die Oxidation des Siliciums durch Sauerstoff (siehe Thermische Oxidation von Silicium). Dieser Prozess findet in Rohröfen, im industriellen Bereich heutzutage meist Vertikalöfen, statt.
Die trockene Oxidation findet bei Temperaturen von 850–1200 °C statt und verläuft relativ langsam, aber mit sehr guter Gleichmäßigkeit. Bei der nassen Oxidation wird die Abscheidung des Oxids stark beschleunigt. Die Feuchtigkeit wird entweder direkt in Form von Wasserdampf oder über einen Knallgasbrenner eingebracht, d. h. Wasserstoff und Sauerstoff werden unmittelbar vor Einbringung in den Ofen zur Reaktion gebracht, wobei sich das gewünschte Wasser in sehr großer Reinheit bildet. ⓘ
Soll Siliciumoxid auf einem anderen Substrat als Silicium gebildet werden, ist die thermische Oxidation nicht mehr nutzbar und es müssen andere Verfahren verwendet werden. Hauptsächlich werden hier Verfahren der chemischen Gasphasenabscheidung (CVD) eingesetzt, bei denen beide Elemente durch eine Reaktion von Gasen, die Silicium enthalten, wie Silan oder Tetraethylorthosilicat (TEOS, auch Tetraethoxysilan), gebildet werden. ⓘ
Die Oxidabscheideverfahren, die auf der Reaktion von Silan basieren, finden meist bei reduziertem Druck (engl. low preassure cvd, LPCVD) statt. Es gibt mehrere gängige Methoden. Im LTO-Verfahren (engl. low temperature oxid) wird bei ca. 430 °C verdünntes Silan direkt mit Sauerstoff umgesetzt:
Bei höheren Temperaturen (900 °C) lässt sich SiO2 im sogenannten HTO-Verfahren (engl. high temperature oxid), aber auch aus einer Kombination von Dichlorsilan und Lachgas bilden:
In der Halbleitertechnik sind weiterhin sogenannte TEOS-Verfahren wichtig – dabei wird Tetraethylorthosilicat (TEOS) thermisch zersetzt:
Die so hergestellten SiO2-Schichten haben in der Regel bessere Eigenschaften und können mit höherer Schichtkonformität abgeschieden werden, der Herstellungsprozess ist jedoch etwas teurer als beispielsweise beim HTO-Verfahren. ⓘ
Toxikologie
Die Auswirkungen von Siliciumdioxid auf die menschliche Gesundheit und die Umwelt werden unter REACH seit dem Jahr 2012 im Rahmen der Stoffbewertung von den Niederlanden geprüft. Die Bewertung ist noch nicht abgeschlossen. Insbesondere bestehen begründete Bedenken, sofern die Stoffe eingeatmet werden, sowie bei oberflächenbehandeltem Siliciumdioxid im Allgemeinen. Daher fordert die Behörde weitere Daten der Hersteller. Mehrere Hersteller legten Widerspruch ein. ⓘ
Amorphes synthetisches Siliciumdioxid mit einer Primärteilchengröße < 25 nm wurde zum 1. November 2015 als Insektizid-Wirkstoff zugelassen. ⓘ








