Pneumothorax
| Pneumothorax ⓘ | |
|---|---|
| Andere Bezeichnungen | Kollabierte Lunge |
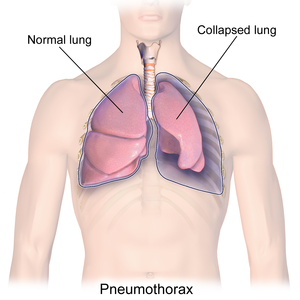 | |
| Illustration einer kollabierten Lunge oder eines Pneumothorax | |
| Fachgebiet | Pulmonologie, Thoraxchirurgie |
| Symptome | Schmerzen in der Brust, Kurzatmigkeit, Müdigkeit |
| Übliches Auftreten | Plötzlich |
| Ursachen | Unbekannt, Trauma |
| Risikofaktoren | COPD, Tuberkulose, Rauchen |
| Diagnostische Methode | Röntgen des Brustkorbs, Ultraschall, CT-Scan |
| Differentialdiagnose | Lungenbläschen, Hämothorax |
| Vorbeugung | Raucherentwöhnung |
| Behandlung | konservativ, Nadelaspiration, Thoraxdrainage, Pleurodese |
| Häufigkeit | 20 pro 100.000 pro Jahr |
Ein Pneumothorax ist eine anormale Luftansammlung im Pleuraraum zwischen der Lunge und der Brustwand. Zu den typischen Symptomen gehören plötzlich auftretende, stechende, einseitige Brustschmerzen und Kurzatmigkeit. In einer Minderheit der Fälle bildet sich durch einen Bereich geschädigten Gewebes ein Einwegventil, und die Luftmenge im Raum zwischen Brustwand und Lunge nimmt zu; dies wird als Spannungspneumothorax bezeichnet. Dies kann zu einem sich ständig verschlimmernden Sauerstoffmangel und niedrigem Blutdruck führen. Dies führt zu einer Art Schock, dem sogenannten obstruktiven Schock, der tödlich sein kann, wenn er nicht behoben wird. Sehr selten können auch beide Lungenflügel von einem Pneumothorax betroffen sein. Dieser wird oft als "kollabierte Lunge" bezeichnet, obwohl sich dieser Begriff auch auf eine Atelektase beziehen kann. ⓘ
Ein primärer Spontanpneumothorax tritt ohne offensichtliche Ursache und ohne eine signifikante Lungenerkrankung auf. Ein sekundärer Spontanpneumothorax tritt bei einer bestehenden Lungenerkrankung auf. Rauchen erhöht das Risiko eines primären Spontanpneumothorax, während die Hauptursachen für einen sekundären Pneumothorax COPD, Asthma und Tuberkulose sind. Ein traumatischer Pneumothorax kann durch ein physisches Trauma des Brustkorbs (einschließlich einer Explosionsverletzung) oder durch eine Komplikation bei einem medizinischen Eingriff entstehen. ⓘ
Die Diagnose eines Pneumothorax allein durch eine körperliche Untersuchung kann schwierig sein (insbesondere bei kleineren Pneumothoraces). Eine Röntgenaufnahme des Brustkorbs, eine Computertomografie (CT) oder eine Ultraschalluntersuchung werden in der Regel zur Bestätigung des Vorliegens eines Pneumothorax eingesetzt. Andere Erkrankungen, die zu ähnlichen Symptomen führen können, sind Hämothorax (Blutansammlung im Pleuraraum), Lungenembolie und Herzinfarkt. Eine große Bulla kann auf einem Röntgenbild der Brust ähnlich aussehen. ⓘ
Ein kleiner Spontanpneumothorax bildet sich in der Regel ohne Behandlung zurück und muss nur überwacht werden. Dieser Ansatz ist am besten für Menschen geeignet, die keine zugrunde liegende Lungenerkrankung haben. Bei einem größeren Pneumothorax oder bei Kurzatmigkeit kann die Luft mit einer Spritze oder einem an ein Einwegventilsystem angeschlossenen Brustschlauch entfernt werden. Gelegentlich kann ein chirurgischer Eingriff erforderlich sein, wenn die Schlauchdrainage erfolglos bleibt oder als vorbeugende Maßnahme, wenn es zu wiederholten Anfällen gekommen ist. Zu den chirurgischen Behandlungen gehören in der Regel die Pleurodese (Verklebung der Pleuraschichten) oder die Pleurektomie (chirurgische Entfernung der Pleuramembranen). Jährlich treten etwa 17-23 Fälle von Pneumothorax pro 100 000 Menschen auf. Sie treten bei Männern häufiger auf als bei Frauen. ⓘ
| Klassifikation nach ICD-10 | |
|---|---|
| J93.0 | Spontaner Spannungspneumothorax |
| J93.1 | Sonstiger Spontanpneumothorax |
| J93.2 | Iatrogener Pneumothorax |
| J93.8 | Sonstiger Pneumothorax |
| S27.0 | Pneumothorax, traumatisch |
| ICD-10 online (WHO-Version 2019) | |
Der Pneumothorax (von altgriechisch πνεῦμα pneuma, deutsch ‚Luft‘, und θώραξ thōrax, deutsch ‚Brustkorb‘; das von Sauerbruch mit „Luftbrust“ übersetzte Wort „Pneumothorax“ wurde von dem britischen Chirurgen William Hewson im 18. Jahrhundert eingeführt. Im Medizinerjargon wird er auch Pneu genannt.) ist ein meist akut auftretendes, je nach Ausprägung lebensbedrohliches Krankheitsbild, bei dem Luft in den Pleuraspalt (Pleuraraum) zwischen den beiden Pleurablättern gelangt und damit die Ausdehnung eines Lungenflügels oder beider Lungenflügel behindert, sodass diese für die Atmung nicht oder nur noch eingeschränkt zur Verfügung stehen. ⓘ
Ein Pneumothorax kann nur bei Säugetieren (außer bei Rüsseltieren) entstehen, da nur sie einen Pleuraspalt besitzen. ⓘ
Die Ausprägung reicht von minimalen Luftmengen im Pleuraraum, die vom Patienten kaum bemerkt werden, über einen Lungenkollaps bis hin zum Spannungspneumothorax, bei dem die Funktion beider Lungenflügel und auch die Herz-Kreislauf-Funktion drastisch eingeschränkt sein können. Bei einem Spannungspneumothorax muss von einer akuten Lebensgefahr ausgegangen werden. ⓘ
Anzeichen und Symptome
Ein primärer Spontanpneumothorax (PSP) tritt in der Regel bei jungen Erwachsenen ohne zugrunde liegende Lungenprobleme auf und verursacht in der Regel nur geringe Symptome. Schmerzen in der Brust und manchmal leichte Atemnot sind in der Regel die vorherrschenden Anzeichen. Menschen, die von einem PSP betroffen sind, sind sich der potenziellen Gefahr oft nicht bewusst und warten möglicherweise mehrere Tage, bevor sie einen Arzt aufsuchen. PSPs treten häufiger bei Veränderungen des Luftdrucks auf, was bis zu einem gewissen Grad erklärt, warum Pneumothorax-Episoden gehäuft auftreten können. Es ist selten, dass ein PSP einen Spannungspneumothorax verursacht. ⓘ
Sekundäre Spontanpneumothoraces (SSP) treten definitionsgemäß bei Personen mit einer signifikanten zugrunde liegenden Lungenerkrankung auf. Die Symptome bei SSPs sind in der Regel schwerwiegender als bei PSPs, da die nicht betroffenen Lungen im Allgemeinen nicht in der Lage sind, den Funktionsverlust in den betroffenen Lungen zu ersetzen. Eine Hypoxämie (verminderter Sauerstoffgehalt im Blut) ist in der Regel vorhanden und kann sich als Zyanose (Blaufärbung der Lippen und der Haut) bemerkbar machen. Gelegentlich tritt Hyperkapnie (Anhäufung von Kohlendioxid im Blut) auf, die zu Verwirrung und - in sehr schweren Fällen - zum Koma führen kann. Das plötzliche Auftreten von Atemnot bei Personen mit chronisch obstruktiver Lungenerkrankung (COPD), Mukoviszidose oder anderen schweren Lungenerkrankungen sollte daher Anlass für Untersuchungen sein, um die Möglichkeit eines Pneumothorax zu ermitteln. ⓘ
Ein traumatischer Pneumothorax tritt am häufigsten auf, wenn die Brustwand durchstochen wird, z. B. wenn durch eine Stich- oder Schusswunde Luft in den Pleuraraum eindringt, oder weil eine andere mechanische Verletzung der Lunge die Integrität der betroffenen Strukturen beeinträchtigt. Traumatische Pneumothoraces treten in bis zur Hälfte aller Fälle von Thoraxtrauma auf, wobei nur Rippenbrüche in dieser Gruppe häufiger sind. Der Pneumothorax kann in der Hälfte dieser Fälle okkult (nicht ohne weiteres erkennbar) sein, sich aber vergrößern, insbesondere wenn eine mechanische Beatmung erforderlich ist. Sie treten auch bei Personen auf, die bereits aus anderen Gründen mechanisch beatmet werden. ⓘ
Bei der körperlichen Untersuchung können die Atemgeräusche (die mit einem Stethoskop abgehört werden) auf der betroffenen Seite vermindert sein, was teilweise darauf zurückzuführen ist, dass die Luft im Pleuraraum die Schallübertragung dämpft. Die Messung der Weiterleitung von Stimmvibrationen an die Oberfläche des Brustkorbs kann beeinträchtigt sein. Die Perkussion des Brustkorbs kann als hyperresonant (wie eine dröhnende Trommel) wahrgenommen werden, und sowohl die stimmliche Resonanz als auch der taktile Fremitus können merklich vermindert sein. Wichtig ist, dass das Volumen des Pneumothorax nicht unbedingt mit der Intensität der vom Opfer empfundenen Symptome korreliert, und dass körperliche Anzeichen möglicherweise nicht erkennbar sind, wenn der Pneumothorax relativ klein ist. ⓘ
Spannungspneumothorax
Ein Spannungspneumothorax liegt im Allgemeinen vor, wenn ein Pneumothorax (primär spontan, sekundär spontan oder traumatisch) zu einer erheblichen Beeinträchtigung der Atmung und/oder des Blutkreislaufs führt. Dies führt zu einer Art von Kreislaufschock, dem so genannten obstruktiven Schock. Ein Spannungspneumothorax tritt in der Regel in klinischen Situationen wie Beatmung, Wiederbelebung, Trauma oder bei Menschen mit Lungenerkrankungen auf. Es handelt sich um einen medizinischen Notfall, der unter Umständen eine sofortige Behandlung ohne weitere Untersuchungen erfordert (siehe Abschnitt Behandlung). ⓘ
Die häufigsten Befunde bei einem Spannungspneumothorax sind Schmerzen in der Brust und Atemnot, oft mit erhöhter Herzfrequenz (Tachykardie) und schneller Atmung (Tachypnoe) im Anfangsstadium. Weitere Befunde können leisere Atemgeräusche auf einer Seite des Brustkorbs, niedrige Sauerstoffwerte und Blutdruckwerte sowie eine Verlagerung der Luftröhre von der betroffenen Seite weg sein. In seltenen Fällen kann es zu Zyanose (bläuliche Verfärbung der Haut aufgrund des niedrigen Sauerstoffgehalts), verändertem Bewusstsein, einem hyperresonanten Perkussionsgeräusch bei der Untersuchung der betroffenen Seite mit verminderter Ausdehnung und verminderter Bewegung, Schmerzen im Epigastrium (Oberbauch), Verschiebung des Apex-Schlags (Herzimpuls) und Resonanzgeräuschen beim Klopfen des Brustbeins kommen. ⓘ
Ein Spannungspneumothorax kann auch bei Personen auftreten, die mechanisch beatmet werden. In diesem Fall kann er schwer zu erkennen sein, da die Person in der Regel sediert wird; er wird oft durch eine plötzliche Verschlechterung des Zustands bemerkt. Neuere Studien haben gezeigt, dass die Entwicklung von Spannungszuständen nicht immer so schnell erfolgt, wie bisher angenommen. Das Abweichen der Luftröhre nach einer Seite und das Vorhandensein eines erhöhten Jugularvenendrucks (geblähte Halsvenen) sind als klinische Anzeichen nicht zuverlässig. ⓘ
Ursache
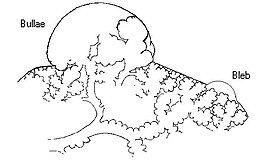
Primärer Spontanpneumothorax
Spontanpneumothoraces werden in zwei Arten unterteilt: primär, d. h. ohne bekannte Lungenerkrankung, und sekundär, d. h. bei Personen mit einer zugrunde liegenden Lungenerkrankung. Die Ursache des primären Spontanpneumothorax ist nicht bekannt, aber zu den bekannten Risikofaktoren gehören männliches Geschlecht, Rauchen und ein Pneumothorax in der Familie. Das Rauchen von Cannabis oder Tabak erhöht das Risiko. Die verschiedenen vermuteten Ursachen werden im Folgenden erörtert. ⓘ
Sekundärer Spontanpneumothorax
Ein sekundärer Spontanpneumothorax tritt bei einer Vielzahl von Lungenerkrankungen auf. Die häufigste ist die chronisch obstruktive Lungenerkrankung (COPD), die etwa 70 % der Fälle ausmacht. Bekannte Lungenerkrankungen, die das Risiko für einen Pneumothorax deutlich erhöhen können, sind ⓘ
| Typ | Ursachen ⓘ |
|---|---|
| Erkrankungen der Atemwege | COPD (insbesondere wenn ein bullöses Emphysem vorliegt), akutes schweres Asthma, Mukoviszidose |
| Infektionen der Lunge | Pneumocystis-Pneumonie (PCP), Tuberkulose, nekrotisierende Lungenentzündung |
| Interstitielle Lungenerkrankung | Sarkoidose, idiopathische Lungenfibrose, Histiozytose X, Lymphangioleiomyomatose (LAM) |
| Erkrankungen des Bindegewebes | Rheumatoide Arthritis, Spondylitis ankylosans, Polymyositis und Dermatomyositis, systemische Sklerose, Marfan-Syndrom und Ehlers-Danlos-Syndrom |
| Krebs | Lungenkrebs, Sarkome mit Beteiligung der Lunge |
| Sonstiges | Katamnestischer Pneumothorax (in Verbindung mit dem Menstruationszyklus und im Zusammenhang mit Endometriose in der Brust) |
Bei Kindern sind weitere Ursachen Masern, Echinokokkose, das Einatmen eines Fremdkörpers und bestimmte angeborene Fehlbildungen (angeborene Fehlbildung der Atemwege und angeborenes Lungenemphysem). ⓘ
11,5 % der Menschen mit einem Spontanpneumothorax haben ein Familienmitglied, das bereits einen Pneumothorax erlitten hat. Die Erbkrankheiten Marfan-Syndrom, Homocystinurie, Ehlers-Danlos-Syndrome, Alpha-1-Antitrypsin-Mangel (der zu Emphysemen führt) und das Birt-Hogg-Dubé-Syndrom wurden alle mit einem familiären Pneumothorax in Verbindung gebracht. Im Allgemeinen verursachen diese Erkrankungen auch andere Anzeichen und Symptome, und der Pneumothorax ist in der Regel nicht der Hauptbefund. Das Birt-Hogg-Dubé-Syndrom wird durch Mutationen im FLCN-Gen (auf Chromosom 17p11.2) verursacht, das für ein Protein namens Folliculin kodiert. FLCN-Mutationen und Lungenläsionen wurden auch bei familiären Fällen von Pneumothorax festgestellt, bei denen andere Merkmale des Birt-Hogg-Dubé-Syndroms fehlten. Zusätzlich zu den genetischen Assoziationen ist auch der HLA-Haplotyp A2B40 eine genetische Prädisposition für PSP. ⓘ
Traumatische
Ein traumatischer Pneumothorax kann entweder durch ein stumpfes Trauma oder durch eine penetrierende Verletzung der Brustwand entstehen. Der häufigste Mechanismus ist das Eindringen scharfer knöcherner Punkte bei einer neuen Rippenfraktur, die das Lungengewebe schädigen. Ein traumatischer Pneumothorax kann auch bei Personen beobachtet werden, die Explosionen ausgesetzt waren, auch wenn keine offensichtliche Verletzung des Brustkorbs vorliegt. ⓘ
Sie können als "offen" oder "geschlossen" klassifiziert werden. Bei einem offenen Pneumothorax gibt es einen Durchgang von der äußeren Umgebung in den Pleuraraum durch die Brustwand. Wenn durch diesen Durchgang Luft in den Pleuraraum gesaugt wird, spricht man von einer "saugenden Brustwunde". Ein geschlossener Pneumothorax liegt vor, wenn die Brustwand intakt bleibt. ⓘ
Medizinische Eingriffe, wie das Einführen eines zentralen Venenkatheters in eine der Brustvenen oder die Entnahme von Biopsieproben aus dem Lungengewebe, können zu einem Pneumothorax führen. Die Verabreichung einer Überdruckbeatmung, sei es eine mechanische oder eine nichtinvasive Beatmung, kann zu einem Barotrauma (druckbedingte Verletzung) führen, das einen Pneumothorax verursacht. ⓘ
Taucher, die mit einem Unterwassergerät atmen, werden mit Atemgas bei Umgebungsdruck versorgt, was dazu führt, dass ihre Lungen Gas mit einem höheren Druck als dem Atmosphärendruck enthalten. Taucher, die mit Pressluft atmen (z. B. beim Gerätetauchen), können einen Pneumothorax als Folge eines Barotraumas entwickeln, wenn sie nur 1 Meter aufsteigen, während sie bei voll aufgeblasener Lunge den Atem anhalten. Ein zusätzliches Problem in diesen Fällen besteht darin, dass Personen mit anderen Merkmalen der Dekompressionskrankheit in der Regel in einer Tauchkammer mit hyperbarer Therapie behandelt werden; dies kann dazu führen, dass sich ein kleiner Pneumothorax schnell vergrößert und Spannungszustände verursacht. ⓘ
Neugeborene Säuglinge
Neugeborene im Alter von 3-9 Tagen mit niedrigem Geburtsgewicht haben ein höheres Risiko für einen Pneumothorax. ⓘ
Mechanismus

Die Brusthöhle ist der Raum im Inneren des Brustkorbs, in dem sich die Lunge, das Herz und zahlreiche große Blutgefäße befinden. Auf jeder Seite der Brusthöhle bedeckt eine Pleuramembran die Oberfläche der Lunge (viszerale Pleura) und kleidet auch die Innenseite der Brustwand aus (parietale Pleura). Normalerweise sind die beiden Schichten durch eine kleine Menge an schmierender seröser Flüssigkeit getrennt. Die Lunge ist in der Höhle vollständig aufgeblasen, da der Druck in den Atemwegen (intrapulmonaler Druck) höher ist als der Druck im Pleuraraum (intrapleuraler Druck). Trotz des niedrigen Drucks im Pleuraraum dringt keine Luft in diesen ein, da es keine natürlichen Verbindungen zu einem luftführenden Gang gibt und der Druck der Gase im Blutkreislauf zu niedrig ist, um sie in den Pleuraraum zu drücken. Ein Pneumothorax kann daher nur entstehen, wenn Luft eindringen kann, sei es durch eine Beschädigung der Brustwand oder der Lunge selbst, oder gelegentlich auch, weil Mikroorganismen im Pleuraraum Gas produzieren. Sobald Luft in die Pleurahöhle eindringt, erhöht sich der intrapleurale Druck, was dazu führt, dass die Differenz zwischen dem intrapulmonalen Druck und dem intrapleuralen Druck (definiert als transpulmonaler Druck) gleich Null ist, was dazu führt, dass sich die Lunge im Gegensatz zu einem normalen transpulmonalen Druck von ~4 mm Hg entleert. ⓘ
Brustwanddefekte treten in der Regel bei Verletzungen der Brustwand auf, z. B. bei Stich- oder Schussverletzungen ("offener Pneumothorax"). Bei sekundären Spontanpneumothoraces werden Schwachstellen im Lungengewebe durch eine Vielzahl von Krankheitsprozessen verursacht, insbesondere durch das Aufplatzen von Bullae (große luftgefüllte Läsionen) bei schweren Emphysemen. Bereiche mit Nekrose (Absterben von Gewebe) können Pneumothorax-Episoden auslösen, obwohl der genaue Mechanismus unklar ist. Beim primären Spontanpneumothorax (PSP) ging man lange Zeit davon aus, dass er durch "Blebs" (kleine luftgefüllte Läsionen direkt unter der Pleuraoberfläche) verursacht wird, die aufgrund mechanischer Faktoren häufiger bei Personen auftreten, die klassischerweise ein erhöhtes Pneumothoraxrisiko haben (große Männer). Bei PSP finden sich Blebs in 77 % der Fälle, gegenüber 6 % in der Allgemeinbevölkerung ohne PSP-Anamnese. Da diese gesunden Personen nicht alle später einen Pneumothorax entwickeln, reicht die Hypothese möglicherweise nicht aus, um alle Episoden zu erklären; außerdem kann der Pneumothorax auch nach einer chirurgischen Behandlung der Blasen wieder auftreten. Es wurde daher vorgeschlagen, dass PSP auch durch Bruchstellen (Porosität) in der Pleuraschicht verursacht werden kann, die zu Rupturen neigen. Rauchen kann zusätzlich zu einer Entzündung und Obstruktion der kleinen Atemwege führen, was das deutlich erhöhte Risiko von PSP bei Rauchern erklärt. Sobald keine Luft mehr in die Pleurahöhle eindringt, wird sie allmählich resorbiert. ⓘ
Ein Spannungspneumothorax entsteht, wenn die Öffnung, durch die Luft in den Pleuraraum gelangt, wie ein Einwegventil funktioniert, so dass mit jedem Atemzug mehr Luft eintritt, aber keine entweicht. Der Körper kompensiert dies durch eine Erhöhung der Atemfrequenz und des Tidalvolumens (Größe der einzelnen Atemzüge), was das Problem verschlimmert. Wird das Problem nicht behoben, kommt es schließlich zu Hypoxie (verminderter Sauerstoffgehalt) und Atemstillstand. ⓘ
Diagnose
Die Symptome eines Pneumothorax können vage und nicht eindeutig sein, vor allem bei Patienten mit einem kleinen PSP; in der Regel ist eine Bestätigung durch medizinische Bildgebung erforderlich. Im Gegensatz dazu ist ein Spannungspneumothorax ein medizinischer Notfall und kann vor der Bildgebung behandelt werden, insbesondere wenn eine schwere Hypoxie, ein sehr niedriger Blutdruck oder eine Bewusstseinsstörung vorliegt. Bei einem Spannungspneumothorax sind manchmal Röntgenaufnahmen erforderlich, wenn Zweifel an der anatomischen Lage des Pneumothorax bestehen. ⓘ
Röntgenaufnahme des Brustkorbs
Eine Röntgenaufnahme des Brustkorbs, bei der die Röntgenstrahlen idealerweise von hinten (posteroanterior oder "PA") und bei maximaler Inspiration (Anhalten des Atems) projiziert werden, ist die am besten geeignete erste Untersuchung. Es wird nicht davon ausgegangen, dass die routinemäßige Anfertigung von Aufnahmen während der Ausatmung irgendwelche Vorteile bringt. Dennoch können sie bei der Entdeckung eines Pneumothorax nützlich sein, wenn der klinische Verdacht groß ist, das Röntgenbild bei der Einatmung jedoch normal erscheint. Wenn die PA-Röntgenaufnahme keinen Pneumothorax zeigt, aber ein starker Verdacht auf einen solchen besteht, können auch seitliche Röntgenaufnahmen (mit seitlich einfallenden Strahlen) durchgeführt werden, was jedoch keine Routine ist. ⓘ
Röntgenaufnahme des Brustkorbs mit den Merkmalen eines Pneumothorax auf der linken Seite der Person (rechts im Bild) ⓘ
Es ist nicht ungewöhnlich, dass sich das Mediastinum (die Struktur zwischen den Lungen, die das Herz, die großen Blutgefäße und die großen Atemwege enthält) aufgrund der Druckunterschiede von der betroffenen Lunge wegbewegt. Dies ist nicht gleichbedeutend mit einem Spannungspneumothorax, der hauptsächlich durch die Konstellation von Symptomen, Hypoxie und Schock bestimmt wird. ⓘ
Die Größe des Pneumothorax (d. h. das Luftvolumen im Pleuraraum) kann durch Messung des Abstands zwischen der Brustwand und der Lunge mit angemessener Genauigkeit bestimmt werden. Dies ist für die Behandlung von Bedeutung, da kleinere Pneumothoraces anders behandelt werden können. Ein Luftrand von 2 cm bedeutet, dass der Pneumothorax etwa 50 % des Hemithorax einnimmt. In den britischen Leitlinien wird traditionell angegeben, dass die Messung auf Höhe des Hilums (wo Blutgefäße und Atemwege in die Lunge eintreten) erfolgen sollte, wobei 2 cm als Grenzwert gelten, während in den amerikanischen Leitlinien angegeben wird, dass die Messung am Apex (oben) der Lunge erfolgen sollte, wobei 3 cm den Unterschied zwischen einem "kleinen" und einem "großen" Pneumothorax ausmachen. Bei der letztgenannten Methode kann die Größe eines Pneumothorax überschätzt werden, wenn er sich hauptsächlich am Apex befindet, was häufig der Fall ist. Die verschiedenen Methoden korrelieren nur schlecht miteinander, sind aber die besten leicht verfügbaren Methoden zur Schätzung der Größe eines Pneumothorax. Die CT-Untersuchung (siehe unten) kann eine genauere Bestimmung der Größe des Pneumothorax ermöglichen, ihre routinemäßige Anwendung in diesem Bereich wird jedoch nicht empfohlen. ⓘ
Nicht alle Pneumothoraces sind gleichförmig; manche bilden nur eine Lufttasche an einer bestimmten Stelle im Brustkorb. Auf dem Röntgenbild des Brustkorbs können kleine Flüssigkeitsmengen zu sehen sein (Hydropneumothorax), bei denen es sich um Blut handeln kann (Hämopneumothorax). In einigen Fällen kann die einzige signifikante Anomalie das "tiefe Sulcus-Zeichen" sein, bei dem der normalerweise kleine Raum zwischen der Brustwand und dem Zwerchfell aufgrund der abnormalen Anwesenheit von Flüssigkeit vergrößert erscheint. ⓘ
Am wichtigsten ist es, bei unklarer Atemnot überhaupt an einen Pneumothorax zu denken.
- Bei der Inspektion kann ein „Nachschleppen“ (eingeschränkte Atemexkursionen) der erkrankten Seite erkennbar sein.
- Die Zwischenrippenräume sind verbreitert, verstrichen, eventuell auch vorgewölbt.
- Beim Abhören der Lunge mittels Stethoskop ist das Atemgeräusch abgeschwächt oder aufgehoben.
- Die Bronchophonie ist ebenfalls abgeschwächt. Auch der Stimmfremitus ist abgeschwächt oder aufgehoben.
- Bei der Perkussion (Abklopfen des Brustkorbes) fällt ein lauter, hohler (tympanitischer) Klopfschall, ein sogenannter Schachtelton auf. Die Perkussion sollte allerdings immer im Seitenvergleich geschehen (in diesem Fall mit der anderen Thoraxhälfte).
- Im Thorax-Röntgenbild (Röntgenaufnahme der Lunge) ist ein bedeutsamer Pneumothorax sicher erkennbar.
- Die Diagnose durch Ultraschall ist eine neuere Methode, schnell, zuverlässig und für einen kleinen Pneumothorax (Mantelpneumothorax) sensibler als die Röntgenaufnahme. Beim Pneumothorax zeigt der M-Mode das Barcode-Zeichen, wohingegen beim Normalbefund das Seashore-Zeichen zu sehen ist. ⓘ
- Sicher ist auch die aufwändigere Computertomographie (CT), die weitere Begleitverletzungen oder -erkrankungen erkennen lässt. ⓘ
Computertomographie

Eine CT-Untersuchung ist für die Diagnose eines Pneumothorax nicht erforderlich, kann aber in bestimmten Situationen nützlich sein. Bei einigen Lungenkrankheiten, insbesondere bei Emphysemen, kann es vorkommen, dass anormale Lungenbereiche wie Bullae (große luftgefüllte Säcke) auf dem Röntgenbild das gleiche Aussehen wie ein Pneumothorax haben, und es ist möglicherweise nicht sicher, eine Behandlung durchzuführen, bevor die Unterscheidung getroffen und die genaue Lage und Größe des Pneumothorax bestimmt wurde. Bei Traumata, bei denen eine aufrechte Aufnahme möglicherweise nicht möglich ist, kann die Röntgenaufnahme des Brustkorbs bis zu einem Drittel der Pneumothoraxe übersehen, während die CT sehr empfindlich bleibt. ⓘ
Ein weiterer Einsatzbereich der CT ist die Erkennung von zugrunde liegenden Lungenläsionen. Bei einem vermuteten primären Pneumothorax kann es helfen, Blasen oder zystische Läsionen zu erkennen (in Erwartung einer Behandlung, siehe unten), und bei einem sekundären Pneumothorax kann es helfen, die meisten der oben genannten Ursachen zu identifizieren. ⓘ
Ultraschall
Ultraschall wird häufig bei der Beurteilung von Personen eingesetzt, die ein physisches Trauma erlitten haben, z. B. im Rahmen des FAST-Protokolls. Ultraschall kann bei der Erkennung eines Pneumothorax nach einem stumpfen Trauma des Brustkorbs empfindlicher sein als Röntgenaufnahmen des Brustkorbs. Die Ultraschalluntersuchung kann auch in anderen Notfallsituationen eine schnelle Diagnose liefern und eine Quantifizierung der Größe des Pneumothorax ermöglichen. Die Ultraschalluntersuchung des Brustkorbs zeigt einige besondere Merkmale, die zur Bestätigung oder zum Ausschluss der Diagnose herangezogen werden können. ⓘ
Ultraschalluntersuchung eines Pneumothorax
Ultraschalluntersuchung, die einen falschen Lungenpunkt und keinen Pneumothorax zeigt ⓘ
Behandlung
Die Behandlung eines Pneumothorax hängt von einer Reihe von Faktoren ab und kann von der Entlassung mit frühzeitiger Nachsorge bis zur sofortigen Dekompression mit einer Nadel oder dem Einsetzen einer Thoraxdrainage reichen. Die Behandlung richtet sich nach dem Schweregrad der Symptome und den Anzeichen einer akuten Erkrankung, dem Vorliegen einer zugrundeliegenden Lungenerkrankung, der geschätzten Größe des Pneumothorax auf dem Röntgenbild und - in einigen Fällen - nach den persönlichen Vorlieben der betroffenen Person. ⓘ
Bei einem traumatischen Pneumothorax wird in der Regel eine Thoraxdrainage gelegt. Ist eine maschinelle Beatmung erforderlich, ist das Risiko eines Spannungspneumothorax stark erhöht und das Einlegen einer Thoraxdrainage zwingend erforderlich. Jede offene Brustwunde sollte luftdicht verschlossen werden, da sie ein hohes Risiko für einen Spannungspneumothorax birgt. Idealerweise sollte ein Verband mit der Bezeichnung "Asherman-Versiegelung" verwendet werden, da er wirksamer zu sein scheint als ein herkömmlicher "dreiseitiger" Verband. Die Asherman-Dichtung ist eine speziell entwickelte Vorrichtung, die an der Brustwand haftet und durch einen ventilähnlichen Mechanismus das Entweichen von Luft, nicht aber das Eindringen in den Brustkorb ermöglicht. ⓘ
Ein Spannungspneumothorax wird in der Regel mit einer dringenden Nadeldekompression behandelt. Dies kann vor dem Transport ins Krankenhaus erforderlich sein und kann von einem Notfallsanitäter oder einer anderen ausgebildeten Fachkraft durchgeführt werden. Die Nadel oder Kanüle wird an Ort und Stelle belassen, bis eine Thoraxdrainage gelegt werden kann. Intensivpflegeteams können den Brustkorb anschneiden, um einen größeren Kanal zu schaffen, wie es beim Legen einer Thoraxdrainage der Fall ist, ohne jedoch eine Thoraxdrainage einzuführen. Dies wird als einfache Thorakostomie bezeichnet. Wenn ein Spannungspneumothorax zu einem Herzstillstand führt, wird im Rahmen der Wiederbelebung eine Nadeldekompression oder eine einfache Thorakostomie durchgeführt, da dadurch die Herzleistung wiederhergestellt werden kann. ⓘ
Ein geringer Pneumothorax, beispielsweise ein Mantelpneumothorax, kann unerkannt bleiben und braucht oft keine Therapie, da der Körper mit der Zeit die eingedrungene Luft selbst beseitigt. Ein mögliches Sauerstoffdefizit kann durch Sauerstoffinsufflation behoben werden. Therapie der Wahl, falls ein offener Pneumothorax nicht sofort zu einem geschlossenen gemacht werden konnte, bei einem ausgedehnteren Pneumothorax ist ein Schlauch, über den die eingedrungene Luft wieder abgesaugt wird (Thoraxdrainage). Diese Drainage wird meist unterhalb der Mitte des Schlüsselbeins (medioklavikulär) im zweiten oder dritten Zwischenrippenraum mit Stichrichtung nach oben-seitlich (kraniolateral) eingebracht (Monaldi-Drainage). Der Drain kann mit einem Ventil, dem sogenannten Heimlichventil, offengelassen werden oder an Unterdruck angeschlossen werden, um eine allmähliche Wiederentfaltung der Lunge zu erreichen. ⓘ
Ist der Pneumothorax traumatisch entstanden und liegen weitere Verletzungen vor, beispielsweise Rippenfrakturen, Hämatothorax (Blut im Pleuraspalt), dann muss eine Bülau-Drainage angelegt werden, das heißt in der mittleren bis hinteren Axillarlinie auf Höhe der unteren Schulterblattspitze (5. bis 6. Intercostalraum), um auch Flüssigkeiten (Blut, Erguss) ableiten zu können. ⓘ
Konservative Maßnahmen
Kleine Spontanpneumothoraces müssen nicht immer behandelt werden, da es unwahrscheinlich ist, dass sie zu einem Atemstillstand oder einem Spannungspneumothorax führen, und sie sich im Allgemeinen spontan zurückbilden. Dieser Ansatz ist am besten geeignet, wenn die geschätzte Größe des Pneumothorax gering ist (definiert als <50 % des Volumens des Hemithorax), keine Atemnot besteht und keine zugrunde liegende Lungenerkrankung vorliegt. Es kann angemessen sein, einen größeren PSP konservativ zu behandeln, wenn die Symptome begrenzt sind. Eine Einweisung in ein Krankenhaus ist oft nicht erforderlich, solange klare Anweisungen gegeben werden, bei einer Verschlechterung der Symptome wieder ins Krankenhaus zu kommen. Weitere Untersuchungen können ambulant durchgeführt werden, wobei Röntgenaufnahmen wiederholt werden, um eine Besserung zu bestätigen, und Ratschläge zur Verhinderung eines erneuten Auftretens erteilt werden (siehe unten). Die geschätzten Resorptionsraten liegen zwischen 1,25 % und 2,2 % des Hohlraumvolumens pro Tag. Dies würde bedeuten, dass sich selbst ein vollständiger Pneumothorax innerhalb von etwa 6 Wochen spontan zurückbilden würde. Es gibt jedoch keine qualitativ hochwertigen Belege für einen Vergleich zwischen konservativer und nichtkonservativer Behandlung. ⓘ
Ein sekundärer Pneumothorax wird nur dann konservativ behandelt, wenn er sehr klein ist (1 cm oder weniger Luftrand) und nur wenige Symptome vorhanden sind. In der Regel wird eine Einweisung ins Krankenhaus empfohlen. Die Verabreichung von Sauerstoff mit hoher Flussrate kann die Resorption um das Vierfache beschleunigen. ⓘ
Aspiration
Bei einem großen PSP (>50 %) oder bei einem PSP, das mit Atemnot einhergeht, wird in einigen Leitlinien empfohlen, dass eine Verkleinerung durch Aspiration ebenso wirksam ist wie das Einlegen einer Thoraxdrainage. Dabei wird ein Lokalanästhetikum verabreicht und eine Nadel eingeführt, die mit einem Dreiwegehahn verbunden ist; bis zu 2,5 Liter Luft (bei Erwachsenen) werden abgesaugt. Wenn sich die Größe des Pneumothorax auf dem anschließenden Röntgenbild deutlich verringert hat, kann die weitere Behandlung konservativ erfolgen. Dieser Ansatz hat sich in über 50 % der Fälle als wirksam erwiesen. Im Vergleich zur Schlauchdrainage verringert die Aspiration bei PSP die Zahl der Patienten, die ins Krankenhaus eingewiesen werden müssen, ohne dass sich das Risiko von Komplikationen erhöht. ⓘ
Eine Aspiration kann auch bei einem mittelgroßen Sekundärpneumothorax (Luftrand 1-2 cm) ohne Atemnot in Betracht gezogen werden, mit dem Unterschied, dass auch nach einem erfolgreichen Eingriff eine ständige Beobachtung im Krankenhaus erforderlich ist. Nach den amerikanischen Berufsrichtlinien sollten alle großen Pneumothoraces - auch solche, die auf PSP zurückzuführen sind - mit einer Thoraxdrainage behandelt werden. Mittelgroße iatrogene traumatische Pneumothoraces (aufgrund medizinischer Verfahren) können zunächst mit einer Aspiration behandelt werden. ⓘ
Thoraxdrainage

Eine Thoraxdrainage (oder Interkostaldrainage) ist die definitivste Erstbehandlung eines Pneumothorax. Diese werden in der Regel in einem Bereich unter der Achselhöhle, dem so genannten "sicheren Dreieck", eingelegt, wo eine Schädigung der inneren Organe vermieden werden kann; dieser Bereich wird durch eine horizontale Linie in Höhe der Brustwarze und zweier Brustwandmuskeln (Latissimus dorsi und Pectoralis major) abgegrenzt. Es wird ein Lokalanästhetikum verabreicht. Es können zwei Arten von Schläuchen verwendet werden. Bei Spontanpneumothorax können Röhrchen mit kleinem Durchmesser (kleiner als 14 F, 4,7 mm Durchmesser) nach der Seldinger-Technik eingeführt werden; größere Röhrchen sind nicht von Vorteil. Bei traumatischem Pneumothorax werden größere Schläuche (28 F, 9,3 mm) verwendet. Wenn Brustschläuche aufgrund eines stumpfen oder penetrierenden Traumas gelegt werden, verringern Antibiotika das Risiko infektiöser Komplikationen. ⓘ
Thoraxdrainagen sind bei PSPs, die nicht auf die Nadelaspiration ansprechen, bei großen SSPs (>50 %) und bei Spannungspneumothorax erforderlich. Sie werden an ein Einweg-Ventilsystem angeschlossen, durch das Luft entweichen, aber nicht wieder in den Brustkorb gelangen kann. Dies kann eine Flasche mit Wasser sein, die wie eine Wasserdichtung funktioniert, oder ein Heimlich-Ventil. Normalerweise werden sie nicht an einen Unterdruckkreislauf angeschlossen, da dies zu einer raschen Wiederausdehnung der Lunge und dem Risiko eines Lungenödems ("Re-Expansions-Lungenödem") führen würde. Der Schlauch wird so lange belassen, bis über einen bestimmten Zeitraum keine Luft mehr aus dem Schlauch austritt und Röntgenaufnahmen die erneute Ausdehnung der Lunge bestätigen. ⓘ
Wenn nach 2-4 Tagen immer noch ein Luftaustritt zu erkennen ist, gibt es verschiedene Möglichkeiten. Insbesondere bei PSP kann eine Unterdruckabsaugung (bei niedrigem Druck von -10 bis -20 cmH2O) mit hoher Flussrate versucht werden; es wird angenommen, dass dies die Heilung des Lecks beschleunigen kann. Gelingt dies nicht, kann eine Operation erforderlich sein, vor allem bei SSP. ⓘ
Thoraxdrainagen werden in erster Linie eingesetzt, wenn bei AIDS-Patienten ein Pneumothorax auftritt, der in der Regel auf eine zugrunde liegende Pneumocystis-Pneumonie (PCP) zurückzuführen ist, da diese Erkrankung mit einem anhaltenden Luftaustritt verbunden ist. Ein bilateraler Pneumothorax (beidseitiger Pneumothorax) ist bei Menschen mit Pneumocystis-Pneumonie relativ häufig, und häufig ist eine Operation erforderlich. ⓘ
Es ist möglich, eine Person mit einer Thoraxdrainage ambulant zu behandeln, indem ein Heimlich-Ventil verwendet wird, obwohl die Qualität der Untersuchungen zum Nachweis der Gleichwertigkeit mit einem Krankenhausaufenthalt begrenzt ist. ⓘ
Pleurodese und Operation
Die Pleurodese ist ein Verfahren, bei dem der Pleuraraum dauerhaft beseitigt und die Lunge an der Brustwand befestigt wird. Es gibt keine Langzeitstudie (20 Jahre oder länger) über die Folgen dieses Verfahrens. Kurzfristig gute Ergebnisse werden mit einer Thorakotomie (chirurgische Öffnung des Brustkorbs) mit Identifizierung jeglicher Quelle von Luftlecks und Klammerung von Blasen erzielt, gefolgt von einer Pleurektomie (Ablösung der Pleuraschicht) der äußeren Pleuraschicht und einer Pleuraabschabung (Abschabung der Pleura) der inneren Schicht. Während des Heilungsprozesses haftet die Lunge an der Brustwand, wodurch der Pleuraraum effektiv verödet wird. Die Rezidivrate liegt bei etwa 1 %. Schmerzen nach der Thorakotomie sind relativ häufig. ⓘ
Ein weniger invasiver Ansatz ist die Thorakoskopie, in der Regel in Form eines Verfahrens namens videoassistierte thorakoskopische Chirurgie (VATS). Die Ergebnisse der VATS-basierten Pleuraresektion sind kurzfristig etwas schlechter als die der Thorakotomie, führen aber zu kleineren Narben in der Haut. Im Vergleich zur offenen Thorakotomie bietet die VATS eine kürzere Verweildauer im Krankenhaus, einen geringeren Bedarf an postoperativer Schmerzbehandlung und ein geringeres Risiko von Lungenproblemen nach der Operation. Mit der VATS kann auch eine chemische Pleurodese durchgeführt werden. Dabei wird Talkum insuffliert, das eine Entzündungsreaktion auslöst, die ein Anhaften der Lunge an der Brustwand bewirkt. ⓘ
Wenn bereits eine Thoraxdrainage vorhanden ist, können verschiedene Wirkstoffe wie Talk, Tetrazyklin, Minozyklin oder Doxyzyklin durch die Drainage verabreicht werden, um eine chemische Pleurodese zu erreichen. Die Ergebnisse der chemischen Pleurodese sind in der Regel schlechter als bei chirurgischen Eingriffen, doch hat sich gezeigt, dass die Talk-Pleurodese bei jüngeren Menschen kaum negative Langzeitfolgen hat. ⓘ
Nachsorge
Wenn ein Pneumothorax bei einem Raucher auftritt, ist dies eine gute Gelegenheit, auf das deutlich erhöhte Risiko eines erneuten Auftretens bei Rauchern und die vielen Vorteile der Raucherentwöhnung hinzuweisen. Es kann ratsam sein, nach einem Spontanpneumothorax bis zu einer Woche der Arbeit fernzubleiben. Bei Personen, die normalerweise schwere körperliche Arbeit verrichten, können mehrere Wochen erforderlich sein. Personen, die sich einer Pleurodese unterzogen haben, müssen möglicherweise zwei bis drei Wochen von der Arbeit freigestellt werden, um sich zu erholen. ⓘ
Von Flugreisen wird bis zu sieben Tage nach der vollständigen Abheilung eines Pneumothorax abgeraten, sofern kein Rückfall auftritt. Tauchen gilt nach einem Pneumothorax als unsicher, es sei denn, es wurde ein präventives Verfahren durchgeführt. Professionelle Richtlinien empfehlen, dass eine Pleurektomie an beiden Lungenflügeln durchgeführt wird und dass sich die Lungenfunktionstests und die CT-Untersuchung normalisieren, bevor das Tauchen wieder aufgenommen wird. Auch Flugzeugpiloten müssen möglicherweise für eine Operation untersucht werden. ⓘ
Neugeborenenzeit
Für Neugeborene mit Pneumothorax wurden verschiedene Behandlungsstrategien vorgeschlagen, darunter sorgfältige Beobachtung, Thorakozentese (Nadelaspiration) oder Einsetzen einer Thoraxdrainage. Die Nadelaspiration kann die Notwendigkeit einer Thoraxdrainage verringern, allerdings sind die Wirksamkeit und Sicherheit beider invasiver Verfahren noch nicht vollständig untersucht worden. ⓘ
Vorbeugung
Nach einem Pneumothorax kann ein präventiver Eingriff (Thorakotomie oder Thorakoskopie mit Pleurodese) empfohlen werden, um ein erneutes Auftreten zu verhindern. Die Erkenntnisse über die wirksamste Behandlung sind in einigen Bereichen noch widersprüchlich, und es gibt Unterschiede zwischen den in Europa und in den USA verfügbaren Behandlungen. Nicht bei allen Pneumothorax-Episoden sind solche Eingriffe erforderlich; die Entscheidung hängt weitgehend von der Einschätzung des Risikos eines erneuten Auftretens ab. Diese Verfahren werden häufig nach dem Auftreten eines zweiten Pneumothorax empfohlen. Ein chirurgischer Eingriff kann in Betracht gezogen werden, wenn ein Pneumothorax auf beiden Seiten aufgetreten ist ("bilateral"), wenn beide Seiten betroffen sind oder wenn ein Pneumothorax mit einer Schwangerschaft einherging. ⓘ
Epidemiologie
Es wird angenommen, dass die jährliche altersbereinigte Inzidenzrate (AAIR) der PSP bei Männern drei- bis sechsmal so hoch ist wie bei Frauen. Fishman nennt eine AAIR von 7,4 bzw. 1,2 Fällen pro 100.000 Personenjahre bei Männern und Frauen. Eine deutlich überdurchschnittliche Körpergröße wird ebenfalls mit einem erhöhten PSP-Risiko in Verbindung gebracht - bei Menschen, die mindestens 1,93 Meter groß sind, liegt der AAIR-Wert bei etwa 200 Fällen pro 100.000 Personenjahre. Auch eine schlanke Statur scheint das Risiko einer PSP zu erhöhen. ⓘ
Das Risiko, einen ersten Spontanpneumothorax zu erleiden, ist bei männlichen und weiblichen Rauchern im Vergleich zu Nichtrauchern desselben Geschlechts um den Faktor 22 bzw. 9 erhöht. Personen, die intensiver rauchen, haben ein höheres Risiko, wobei der Effekt "größer als linear" ist; Männer, die 10 Zigaretten pro Tag rauchen, haben ein etwa 20-fach erhöhtes Risiko gegenüber vergleichbaren Nichtrauchern, während Raucher, die 20 Zigaretten pro Tag konsumieren, ein schätzungsweise 100-fach erhöhtes Risiko aufweisen. ⓘ
Bei sekundärem Spontanpneumothorax liegt das geschätzte jährliche AAIR bei 6,3 bzw. 2,0 Fällen pro 100 000 Personenjahre für Männer bzw. Frauen, wobei das Risiko eines erneuten Auftretens vom Vorhandensein und der Schwere einer zugrunde liegenden Lungenerkrankung abhängt. Nach einem zweiten Anfall ist die Wahrscheinlichkeit für weitere Anfälle hoch. Die Inzidenz bei Kindern ist nicht gut untersucht, wird aber auf 5 bis 10 Fälle pro 100 000 Personenjahre geschätzt. ⓘ
Der Tod durch einen Pneumothorax ist sehr selten (außer bei Spannungspneumothorax). Britische Statistiken zeigen eine jährliche Sterblichkeitsrate von 1,26 bzw. 0,62 Todesfällen pro Million Personenjahre bei Männern und Frauen. Ein deutlich erhöhtes Sterberisiko ist bei älteren Patienten und bei Patienten mit sekundären Pneumothoraces zu beobachten. ⓘ
Geschichte
Eine frühe Beschreibung des traumatischen Pneumothorax infolge von Rippenfrakturen findet sich in der Kaiserlichen Chirurgie des türkischen Chirurgen Şerafeddin Sabuncuoğlu (1385-1468), der auch eine einfache Aspirationsmethode empfiehlt. ⓘ
Der Pneumothorax wurde 1803 von Jean Marc Gaspard Itard, einem Schüler von René Laennec, beschrieben, der 1819 eine ausführliche Beschreibung des Krankheitsbildes lieferte. Itard und Laennec erkannten zwar an, dass einige Fälle nicht auf eine Tuberkulose (damals die häufigste Ursache) zurückzuführen waren, doch der Begriff des Spontanpneumothorax ohne Tuberkulose (primärer Pneumothorax) wurde 1932 von dem dänischen Arzt Hans Kjærgaard wieder eingeführt. Im Jahr 1941 führten die Chirurgen Tyson und Crandall die Pleuraabtragung zur Behandlung des Pneumothorax ein. ⓘ
Vor dem Aufkommen von Medikamenten gegen Tuberkulose wurden Pneumothoraces bei Tuberkulosepatienten absichtlich vom medizinischen Personal verursacht, um einen Lappen oder die gesamte Lunge um eine kavitierende Läsion herum zum Kollabieren zu bringen. Dies wurde als "Ruhigstellung der Lunge" bezeichnet. Es wurde 1888 von dem italienischen Chirurgen Carlo Forlanini eingeführt und Anfang des 20. Jahrhunderts von dem amerikanischen Chirurgen John Benjamin Murphy bekannt gemacht (nachdem er dasselbe Verfahren unabhängig davon entdeckt hatte). Murphy nutzte die (damals) neu entdeckte Röntgentechnik, um Pneumothoraces in der richtigen Größe zu erzeugen. ⓘ
Etymologie
Das Wort Pneumothorax stammt aus dem Griechischen und bedeutet Luft und Thorax bedeutet Brustkorb. Der Plural lautet Pneumothoraces. ⓘ
Andere Tiere
Bei nichtmenschlichen Tieren kann sowohl ein Spontan- als auch ein traumatischer Pneumothorax auftreten. Der Spontanpneumothorax wird wie beim Menschen als primärer oder sekundärer Pneumothorax klassifiziert, während beim traumatischen Pneumothorax zwischen offenem und geschlossenem Pneumothorax (mit oder ohne Verletzung der Brustwand) unterschieden wird. Der Tierarzt erkennt die Diagnose unter Umständen daran, dass das Tier Schwierigkeiten beim Einatmen oder eine flache Atmung aufweist. Pneumothoraces können durch Lungenläsionen (z. B. Bullae) oder durch ein Trauma der Brustwand entstehen. Bei Pferden kann ein traumatischer Pneumothorax beide Hemithoraces betreffen, da das Mediastinum unvollständig ist und eine direkte Verbindung zwischen den beiden Brusthälften besteht. Ein Spannungspneumothorax - dessen Vorhandensein aufgrund einer sich rasch verschlechternden Herzfunktion, fehlender Lungengeräusche im gesamten Thorax und eines tonnenförmigen Brustkorbs vermutet werden kann - wird mit einem Einschnitt in den Brustkorb des Tieres behandelt, um den Druck zu entlasten, und anschließend wird eine Thoraxdrainage eingelegt. Bei Spontanpneumothorax ist die Verwendung der CT zur Diagnose bei Hunden und Kunekune-Schweinen beschrieben worden. ⓘ
Ursachen

Aufgrund der Entstehung werden zwei Formen des Pneumothorax unterschieden. ⓘ
Der Spontanpneumothorax tritt bei jedem dritten Patienten ohne erkennbare Ursache auf. Er betrifft oft junge, schlanke Männer im Alter zwischen ca. 15 und 35 Jahren. Betroffen sind häufig Raucher nach einem mehr oder weniger heftigen Hustenstoß und Träger eines bullösen Lungenemphysems, angeboren durch einen α1-Antitrypsin-Mangel oder erworben durch eine chronisch-obstruktive Lungenerkrankung. Ursachen für den gelegentlich auftretenden Spontanpneumothorax bei Neugeborenen sind nicht bekannt. ⓘ
Ein Zusammenhang mit dem erstmaligen Auftreten mit folgenden Faktoren ist nicht nachgewiesen:
- körperliche Aktivität oder Sport
- Fliegen oder Aufenthalt in großen Höhen (z. B. Bergsteigen)
- Klima & Wetter
- Psychischer Stress ⓘ
Der traumatische Pneumothorax entsteht immer durch eine direkte oder indirekte Verletzung des Brustkorbs und seiner Organe. Folgende Mechanismen sind typisch:
- Verletzung der Lunge durch nach innen spießende Rippenbrüche
- Stich- und Schussverletzungen mit Eröffnung der Brusthöhle oder Verletzung der Lunge
- hochgradige Quetschung des Brustkorbs (Einklemmen, Überrollen) verursacht eine Schädigung und Schwächung des Lungengewebes
- starke Bässe können Körpergewebe zum Vibrieren bringen und zu Rissen im Lungengewebe führen
- Barotrauma: extreme, plötzliche Druckveränderung der Lunge beim Fliegen und Tauchen oder iatrogen im Rahmen einer Überdruckbeatmung
- iatrogene (= durch ärztliche Maßnahme bedingte) Verletzung der Lunge oder der Brustwand, beispielsweise durch ohne endotracheale Intubation bzw. Überdruckbeatmung durchgeführte Operationen mit Eröffnung des Brustkorbs, Fehlpunktion der Vena subclavia oder bei Regionalanästhesien wie der infraklavikulären Plexusblockade sowie in 0,6 bis 6 % aller Punktionen eines Pleuraergusses. ⓘ
Früher wurde, nach einer 1882 von Carlo Forlanini eingeführten Methode, ein intrapleuraler Pneumothorax auch als Therapieverfahren vor allem bei der Lungentuberkulose künstlich angelegt (therapeutischer Pneumothorax, künstlicher Pneumothorax, artifizieller Pneumothorax). Dieses, durch John Benjamin Murphy sowie Ludolph Brauer international bekannt gemachte Verfahren wurde zunächst oft ergänzt durch Thorakokaustik (so publiziert 1913 von Hans Christian Jacobaeus), später durch die Thorakoplastik ersetzt und nach Entwicklung effektiver Antibiotika wieder ganz verlassen. ⓘ
Wegen der, wohl schon Epaminondas im 4. Jahrhundert v. Chr. bekannten, Gefahr eines Pneumothorax als lebensbedrohliche Komplikation wurden bis zum Ende des 19. Jahrhunderts im Allgemeinen keine Operationen am offenen Brustkorb durchgeführt. Sicherer wurde die chirurgische Versorgung von Brustkorbverletzungen erst mit Einführung der ursprünglich zur Entfernung von Eiteransammlungen innerhalb des Brustfells gedachten Heberdrainage durch den Internisten Gotthard Bülau. ⓘ
Symptome
Die individuellen Beschwerden des Kranken sind sehr unterschiedlich: Sie reichen von geringem Hustenreiz bis zum existentiellen Erstickungsgefühl. Schnelle Atmung (Tachypnoe) trotz körperlicher Ruhe ist ein erstes Symptom, oft verbunden mit Ziehen in den Lungenspitzen beim tiefen Einatmen. Hinzu kommen oft Druckgefühl oder Schmerzen (zum Teil in Intervallen auftretend) im Brustkorbbereich, die auf Arme, Kopf oder Rücken ausstrahlen können. Bei ausgeprägter Luftnot zeigt sich eine bläulich graue Hautfarbe, die auf einen Sauerstoffmangel im Blut schließen lässt (Zyanose). Manchmal ist ein Hautemphysem zu tasten: Bei leichtem Druck auf die Haut fühlt man ein Knistern oder ein Knirschen, als wenn man Schnee zusammendrücken würde. Beim Hydropneumothorax findet sich zudem ein Exsudat im Pleuraraum. Beim traumatisch bedingten Pneumothorax kann zudem gelegentlich ein Hautemphysem ertastet werden. ⓘ
Spannungspneumothorax

Besonders schwerwiegend ist ein Spannungspneumothorax, bei dem durch Verletzung der Lunge oder Brustwand ein Lippenventil entsteht, das mit jedem Atemzug weitere Luft in den Pleuraspalt zieht, ohne diese bei der Ausatmung entweichen zu lassen. Dadurch steigt der Druck in der betroffenen Brusthöhle an, komprimiert den Lungenflügel, schränkt damit die Atmung weiter ein, verschiebt das Mittelfell zur Gegenseite und behindert durch Verziehung und Kompression der Hohlvene den Blutrückfluss zum Herzen, sodass ein kritischer Blutdruckabfall bis hin zum Herz-Kreislauf-Stillstand resultieren kann. Man findet
- alle Symptome des „einfachen“ Pneumothorax, weiter zunehmende Atemnot und weiteren Kreislaufabfall, wobei
- die Atembewegung des Brustkorbs asymmetrisch ist, der Brustkorb auf der betroffenen Seite hochsteht und sich bei Ausatmung kaum senkt,
- pralle Halsvenen und gesteigerter peripherer Venendruck (venöse Einflussstauung) auf einen gesteigerten Druck im Brustraum hinweisen.
- Erholt sich ein Patient mit schwerer Atemnot nach Intubation und Beatmung nicht, ist immer an einen Spannungspneumothorax zu denken.
- Der Spannungspneumothorax ist eine wichtige Differentialdiagnose des unklaren Kreislaufschocks.
- Im Röntgenbild ist von einem Spannungspneumothorax auszugehen, wenn das Mediastinum zur gesunden Seite hin verschoben ist. ⓘ
Flugreisefähigkeit
Flugreisen nach behandeltem Pneumothorax, thoraxchirurgischen Eingriffen oder Punktionen sollten frühestens nach drei Wochen unternommen werden. Danach sind Komplikationen während der Flugreise zwar möglich, aber sehr selten. ⓘ





