Stress-Kardiomyopathie
| Takotsubo-Kardiomyopathie ⓘ | |
|---|---|
| Andere Bezeichnungen | Transientes apikales Ballooning-Syndrom, apikale Ballooning-Kardiomyopathie, stressinduzierte Kardiomyopathie, Syndrom des gebrochenen Herzens |
 | |
| Schematische Darstellung der Takotsubo-Kardiomyopathie (A) im Vergleich zu einem normalen Herzen (B) | |
| Fachgebiet | Kardiologie |
Die Takotsubo-Kardiomyopathie oder das Takotsubo-Syndrom (TTS), auch als Stress-Kardiomyopathie bezeichnet, ist eine Form der nicht-ischämischen Kardiomyopathie, bei der es zu einer plötzlichen vorübergehenden Schwächung des muskulären Teils des Herzens kommt. Sie tritt in der Regel nach einem erheblichen körperlichen oder seelischen Stressfaktor auf; wird sie durch letzteren verursacht, wird sie auch als Syndrom des gebrochenen Herzens bezeichnet. Beispiele für körperliche Stressoren, die ein TTS auslösen können, sind Sepsis, Schock und Phäochromozytom, und zu den emotionalen Stressoren gehören Trauerfälle, Scheidungen oder der Verlust des Arbeitsplatzes. Aus Übersichten geht hervor, dass von den Patienten, bei denen ein TTS diagnostiziert wurde, etwa 70-80 % in letzter Zeit einen größeren Stressfaktor erlebt haben, darunter 41-50 % mit einem körperlichen Stressfaktor und 26-30 % mit einem emotionalen Stressfaktor. TTS kann auch bei Patienten auftreten, die keine größeren Stressfaktoren erlebt haben. ⓘ
Die Pathophysiologie ist noch nicht ganz geklärt, aber man geht davon aus, dass ein plötzlicher massiver Anstieg von Katecholaminen wie Adrenalin und Noradrenalin aufgrund von extremem Stress oder eines Tumors, der diese Stoffe absondert, eine zentrale Rolle spielt. Überschüssige Katecholamine haben, wenn sie direkt von Nerven freigesetzt werden, die die Herzmuskelzellen stimulieren, eine toxische Wirkung und können zu einer verminderten Herzmuskelfunktion oder "Betäubung" führen. Außerdem führt dieser Adrenalinschub zu einer Verengung der Arterien, wodurch der Blutdruck steigt und das Herz stärker belastet wird, und kann zu einer Verkrampfung der Koronararterien führen, die den Herzmuskel mit Blut versorgen. Dadurch werden die Arterien daran gehindert, den Herzmuskel ausreichend mit Blut und Sauerstoff zu versorgen. Zusammen können diese Ereignisse zu einer Herzinsuffizienz führen und die Blutausstoßleistung des Herzens mit jedem Druck verringern. ⓘ
Die Takotsubo-Kardiomyopathie kommt weltweit vor. Man geht davon aus, dass diese Erkrankung für 2 % aller Fälle von akutem Koronarsyndrom in Krankenhäusern verantwortlich ist. Obwohl das TTS im Allgemeinen als eine selbstlimitierende Erkrankung angesehen wurde, die sich im Laufe von Tagen bis Wochen spontan zurückbildet, zeigen aktuelle Beobachtungen, dass "eine Untergruppe von TTS-Patienten Symptome aufweisen kann, die auf Komplikationen zurückzuführen sind, z. B. Herzversagen, Lungenödem, Schlaganfall, kardiogener Schock oder Herzstillstand". Dies bedeutet nicht, dass die Schock-/Todesraten des TTS mit denen des akuten Koronarsyndroms (ACS) vergleichbar sind, sondern dass bei Patienten mit akuten Komplikationen auch ein TTS auftreten kann. Diese Fälle von Schock und Tod wurden mit dem Auftreten von TTS in Verbindung gebracht, das sekundär zu einem einschneidenden physischen Stressor wie Blutung, Hirnverletzung, Sepsis, Lungenembolie oder schwerer COPD auftrat. ⓘ
Es tritt häufiger bei postmenopausalen Frauen auf. Der Name "Takotsubo" leitet sich von dem japanischen Wort takotsubo "Krakenfalle" ab, weil die linke Herzkammer bei dieser Erkrankung eine Form annimmt, die einer Krakenfalle ähnelt. ⓘ
Eine Studie, die im Oktober 2021 im Journal of the American Heart Association veröffentlicht wurde, ergab, dass die Takotsubo-Kardiomyopathie zwischen 2006 und 2017 sowohl bei Frauen als auch bei Männern jährlich zunahm, wobei der stärkste Anstieg bei Frauen ab 50 Jahren zu verzeichnen war. ⓘ
| Klassifikation nach ICD-10 ⓘ | |
|---|---|
| I42 | Kardiomyopathie |
| I42.88 | Sonstige Kardiomyopathien |
| ICD-10 online (WHO-Version 2019) | |

Eine neuere Fall-Kontroll-Studie „zeigt, dass die Patienten in den Jahren vor der kardialen Krise in der Positronen-Emissions-Tomographie (PET) eine vermehrte Aktivität in den Corpora amygdaloideum haben, den Angst- und Stresszentren des Gehirns.“ ⓘ
Die Prognose ist bei den meisten Patienten günstig, nach einigen Wochen ist die Herzfunktion bei der Mehrzahl von ihnen normalisiert. Im Akutstadium allerdings sind ernste und auch lebensbedrohliche Komplikationen häufig. ⓘ
Anzeichen und Symptome
Die Takotsubo-Kardiomyopathie äußert sich typischerweise durch Brustschmerzen mit oder ohne Kurzatmigkeit und damit verbundene EKG-Veränderungen, die einen Vorderwandinfarkt vortäuschen. Bei der Untersuchung des Patienten wird häufig eine Ausstülpung der linken Herzspitze mit einer hyperkontraktilen Basis des linken Ventrikels festgestellt. Es ist die charakteristische Ausbuchtung der Herzspitze bei erhaltener Funktion der Basis, die dem Syndrom in Japan, wo es erstmals beschrieben wurde, den Namen Takotsubo "Krakenfalle" einbrachte. ⓘ
Stress ist der Hauptfaktor bei der Takotsubo-Kardiomyopathie, wobei mehr als 85 % der Fälle durch ein körperlich oder emotional belastendes Ereignis ausgelöst werden, das dem Beginn der Symptome vorausgeht. Beispiele für emotionale Stressoren sind Trauer über den Tod eines geliebten Menschen, Angst vor öffentlichen Auftritten, Streit mit dem Ehepartner, Meinungsverschiedenheiten in der Beziehung, Verrat und finanzielle Probleme. Akutes Asthma, Operationen, Chemotherapie und Schlaganfall sind Beispiele für körperliche Stressfaktoren. In einigen wenigen Fällen kann der Stress durch ein freudiges Ereignis ausgelöst werden, z. B. eine Hochzeit, der Gewinn eines Jackpots, ein sportlicher Triumph oder ein Geburtstag. ⓘ
Risikofaktoren
Auslöser für Stress
Obwohl es dokumentierte Fälle von TTS ohne einen auslösenden Stressor gibt, ist allgemein anerkannt, dass dem TTS ein stressiges Ereignis vorausgeht. In Fallserien, in denen große Gruppen von Patienten untersucht wurden, wird berichtet, dass einige Patienten nach einer emotionalen Belastung eine Takotsubo-Kardiomyopathie entwickeln. Bei einigen Patienten geht ein klinischer Stressor voraus (z. B. eine Hirnverletzung, ein Asthmaanfall oder die Verschlimmerung einer chronischen Krankheit), und Untersuchungen haben ergeben, dass diese Art von Stress sogar häufiger auftreten kann als emotional belastende Auslöser. Etwa ein Drittel der Patienten hat kein vorangegangenes belastendes Ereignis. Eine große Fallserie aus Europa aus dem Jahr 2009 ergab, dass die Takotsubo-Kardiomyopathie in der Wintersaison etwas häufiger auftritt. Dies könnte mit zwei möglichen/vermuteten pathophysiologischen Ursachen zusammenhängen: koronare Spasmen der Mikrogefäße, die bei kaltem Wetter häufiger auftreten, und virale Infektionen - wie das Parvovirus B19 -, die im Winter häufiger auftreten. ⓘ
Geschlecht
Frauen, insbesondere Frauen nach der Menopause, haben das größte Risiko, an TTS zu erkranken. Dies hat einige Forscher dazu veranlasst, über die mögliche schützende Wirkung von Östrogen bei der Verhinderung von TTS zu theoretisieren. ⓘ
Genetische Risikofaktoren
Derzeit wird untersucht, ob bestimmte genetische Merkmale, die mit Katecholaminrezeptoren auf Herzmuskelzellen zusammenhängen, bei der Entstehung von TTS eine Rolle spielen. Es gibt nur wenige Belege dafür, dass TTS direkt mit einer bestimmten genetischen Ausprägung oder Mutation zusammenhängt, jedoch gibt es derzeit eine weit verbreitete Hypothese, die die Idee unterstützt, dass die Interaktion zwischen Umweltfaktoren und dem Zusammenspiel der genetischen Veranlagung zu einer Anfälligkeit für mikrovaskuläre Veränderungen führt, die zum TTS-Krankheitsprozess beitragen. ⓘ
Hormonelle Dysregulation
Bestimmte endokrine Erkrankungen, darunter das Phäochromozytom und die Thyreotoxikose, wurden als potenzielle Risikofaktoren für TTS identifiziert. Die Beziehung zwischen Schilddrüsenfunktion und Stresskardiomyopathie ist durch einen dualen Phänotyp gekennzeichnet, bei dem sowohl eine drohende primäre Hyperthyreose als auch ein hoher Sollwert der Schilddrüsenhomöostase (der für eine allostatische Belastung vom Typ 2 steht) gemeinsame Phänomene sind. Eine multizentrische Beobachtungsstudie ergab, dass eine normale Schilddrüsenfunktion bei TTS eher die Ausnahme als die Regel ist. Insbesondere die Hyperthyreose ist bei der Takotsubo-Kardiomyopathie weit verbreitet und scheint eine schlechte Prognose in Bezug auf Komplikationen und Mortalität vorauszusagen. ⓘ
Pathophysiologie
Die Ursache der Takotsubo-Kardiomyopathie ist nicht vollständig geklärt, aber es wurden mehrere Mechanismen vorgeschlagen. Es ist gut dokumentiert, dass bei der überwiegenden Mehrheit der TTS-Fälle ein erhöhter Katecholaminspiegel festgestellt wurde. Es gibt Theorien, die einen Zusammenhang zwischen der Aktivierung von stressbedingten Biochemikalien im Gehirn und den Auswirkungen dieser Chemikalien auf Bereiche des Herzens vermuten lassen. Genauer gesagt wurde eine Stimulierung der Nebennieren durch das sympathische Nervensystem in Fällen festgestellt, die von körperlichen Ereignissen wie einem ischämischen Schlaganfall bis hin zu emotionalen Ereignissen wie Depressionen oder dem Verlust eines geliebten Menschen reichen. Wie diese erhöhten Katecholaminspiegel im Körper wirken und die bei TTS beobachteten Veränderungen hervorrufen, ist nicht eindeutig geklärt. Die Forschung stützt die weit verbreitete Auffassung, dass mikrovaskuläre Dysfunktion und koronarer Vasospasmus, die durch einen raschen Einstrom von Katecholaminen in die Herzmuskelzellen verursacht werden, zu einer apikalen Betäubung und transienten Kardiomyopathie führen. ⓘ
- Mikrovaskuläre Dysfunktion/Transienter Vasospasmus: Einige der ursprünglichen Takotsubo-Forscher vermuteten, dass mehrere gleichzeitige Spasmen der Koronararterien einen ausreichenden Blutflussverlust verursachen könnten, um eine vorübergehende Betäubung des Herzmuskels zu bewirken. Andere Forscher haben gezeigt, dass Vasospasmen viel seltener auftreten als ursprünglich angenommen. Es wurde festgestellt, dass Vasospasmen, selbst wenn sie in mehreren Arterien auftreten, nicht mit den Bereichen des Herzmuskels korrelieren, die sich nicht zusammenziehen. Es wird jedoch immer noch angenommen, dass Koronararterien-Vasospasmen zum TTS-Krankheitsprozess beitragen. Die Theorie des Vasospasmus lässt sich nicht ohne Weiteres von der Theorie der mikrovaskulären Dysfunktion trennen, und in der Tat könnte eine mikrovaskuläre Dysfunktion die Vasospastik erklären. Eine Beeinträchtigung der mikrovaskulären Funktion ist bei der überwiegenden Mehrheit, wenn nicht sogar bei allen Patienten mit TTS zu beobachten und stellt derzeit eine der am meisten unterstützten Theorien dar. Die meisten Funktionsstörungen sind auf Anomalien in den Endothelauskleidungen der Blutgefäße zurückzuführen, die das Herz versorgen. Beim TTS sind diese hochempfindlichen Innenauskleidungen der Gefäße in ihrer Funktion eingeschränkt, was zu einer Dysregulation des Gefäßtonus führt und die Betroffenen zu einer Vasokonstriktion veranlasst. Wenn die verstärkte vasokonstriktorische Wirkung von Katecholaminen hinzukommt, führt dies zu einer akuten Herzischämie.
- Katecholamin-induzierte Myozytenschädigung: Es wurde vermutet, dass die Reaktion auf Katecholamine (wie Epinephrin und Norepinephrin, die als Reaktion auf Stress freigesetzt werden) zu einer Dysfunktion des Herzmuskels führt, die zur Takotsubo-Kardiomyopathie beiträgt. Die Auswirkungen dieser Toxizität können bei Menschen mit einer Veranlagung zu Angst- oder Panikstörungen stärker sein. Die Ausschüttung von Katecholaminen (Epinephrin, Norepinephrin) über das zirkulierende Blut und durch direkte Ausschüttung aus den Herznerven wird durch die Stimulation der Stresskontrollzentren des Gehirns verstärkt. Während eines emotional oder physisch belastenden Ereignisses schalten die Gehirnzentren die sympathischen Nervenbahnen ein und erhöhen die Herzmuskelaktivität. Eine übermäßige Stimulation durch Katecholamine hat eine toxische Wirkung auf die Herzmuskelzellen, die zu einer Nekrose der kontraktilen Einheiten der Zellen führt, wie sie auch bei einem akuten Myokardinfarkt zu beobachten ist. Die durch die Stimulierung der Katecholamine hervorgerufene erhöhte Arbeitsbelastung des Herzmuskels steigert den Bedarf an mehr Blut und Sauerstoff für diese Muskeln, um die Funktion aufrechtzuerhalten. Wenn diese Anforderungen nicht erfüllt werden können, wird das Herz mit Blut und Sauerstoff unterversorgt und beginnt zu sterben. Zu den zytotoxischen Folgen der Katecholamintoxizität gehört auch die molekulare Umwandlung des Herzmuskels, die zu einer apikalen Betäubung führt.
- Mittelventrikuläre Obstruktion, apikale Betäubung: Es wurde vermutet, dass eine Verdickung der mittleren Kammerwand mit Abflussbehinderung für die Pathophysiologie von Bedeutung ist. Diese Betäubung wird weitgehend als Schutzwirkung angesehen, die durch die Überflutung der Herzmuskelzellen mit Katecholaminen hervorgerufen wird. Eine Überstimulation der Katecholaminrezeptoren führt zu physiologischen Veränderungen des Rezeptors, die sich umgekehrt auf die Zellfunktion des Herzens auswirken. Diese als "cellular-trafficking" bezeichnete Eigenschaft der Herzmuskelzelle ist eigentlich eine molekulare Umwandlung der Zelle, die zu einer Herabregulierung der katecholaminergen Empfindlichkeit führt. Das bedeutet, dass in Gegenwart von überschüssigem Adrenalin eine normale Herzkontraktion gehemmt wird, um den Energiebedarf zu senken, Hyperaktivität zu verhindern und die Integrität der Zelle zu erhalten. Die Konzentration dieser Art von Rezeptoren im Herzen unterstreicht diesen Gedanken noch. Höhere Konzentrationen des Rezeptors, der die Betäubung des Herzens bewirkt, finden sich näher an der Spitze der Herzkammer. Dadurch entsteht der klassische Ballon-Effekt der Herzkammer. ⓘ
Wahrscheinlich sind mehrere Faktoren im Spiel, zu denen auch ein gewisses Maß an Vasospasmus und ein Versagen des Mikrogefäßsystems gehören könnten. Diese Faktoren können sich überlagern und eine komplexe Folgeerscheinung hervorrufen, die zu Ischämie und einer Kontraktionsstörung des linken Ventrikels führt. So ist beispielsweise Östrogen, das Frauen einen Schutz bietet, indem es die Durchblutung des Herzmuskels verbessert, ein biochemischer Weg, der in den TTS-Krankheitsprozess involviert ist. Sobald dieser Schutzmechanismus durch die verringerte Östrogenproduktion nach der Menopause reduziert wird, kommt es vermutlich zu einer Zunahme der endothelialen Dysfunktion, die eine Person für eine Gefäßverengung und kardiale Ischämie prädisponiert. Ein auslösendes Stressereignis löst die Freisetzung von Katecholaminen in den Blutkreislauf aus, die eine erhöhte Herzmuskelaktivität und einen erhöhten Stoffwechsel bewirken. Dies führt zu einer weiteren Dysfunktion der mikrovaskulären Endothelien des Herzens durch oxidativen Stress, Veränderung von ionenvermittelten Kanälen und Elektrolytstörungen, die letztlich die Permeabilität der Herzmuskelmembranen und die Dysfunktion verändern. In Verbindung mit einer direkten Toxizität für den Herzmuskel ist dieses Crescendo von Faktoren für die Ballonbildung und die Herzinsuffizienz verantwortlich, die typischerweise bei TTS auftreten. ⓘ
Ein Fall aus dem Jahr 2019 betraf eine 60-jährige Frau, die sich mit einer Takotsubo-Kardiomyopathie vorstellte, die auf den übermäßigen Verzehr von Wasabi zurückzuführen war, den sie fälschlicherweise für Avocado hielt. ⓘ
Entstehung und Entwicklung der Erkrankung (Pathogenese) sind nicht vollständig geklärt. Bei vielen Patienten mit einer Stress-Kardiomyopathie sind deutlich erhöhte Blutspiegel der körpereigenen Katecholamine festgestellt worden. Adrenalin, Noradrenalin, Metanephrine (Metanephrin und Normetanephrin) und Vanillinmandelsäure sind in höheren Konzentrationen gefunden worden als bei schweren Herzinfarkten. Die hohe Konzentration dieser auch als Stresshormone bezeichneten Substanzen wird als Ursache der Stress-Kardiomyopathie diskutiert, was durch mehrere Einzelfallbeobachtungen von Tako-Tsubo-ähnlichen Ereignissen bei Patienten mit Phäochromozytom, einem katecholaminproduzierenden Tumor der Nebenniere, gestützt wird. 2004 wurde erstmals über zwei Schwestern mit apical ballooning berichtet, was eine genetische Veranlagung vermuten lässt. Anlässlich des Nachweises einer Infektion mit dem Cytomegalievirus bei einem Patienten mit Tako-Tsubo-Syndrom wurde 2006 auch über eine mögliche Verursachung durch Viren diskutiert. ⓘ
Hinsichtlich der Pathophysiologie wird vermutet, dass die stark erhöhte Katecholaminkonzentration die Aktivität des Herzmuskels dahingehend verändert, dass es zu einer Verkrampfung der Wandungen von Herzkranzgefäßen oder zu einer Überladung mit Calcium kommt. Ursache der erhöhten Katecholaminspiegel könnte nach bisherigen Erkenntnissen eine Überaktivität des autonomen Nervensystems sein, das durch die plötzliche Stresssituation zu viele Stresshormone produziert. Ein relativer Mangel an Östrogenen nach der Menopause trägt möglicherweise zur verstärkten Aktivierung des Sympathikus bei. Die für andere Durchblutungsstörungen des Herzens ungewöhnliche Betroffenheit besonders der spitzennahen Muskelregionen könnte auf eine unterschiedliche Dichte von Beta-Adrenozeptoren zurückzuführen sein, die zumindest bei Hunden nachgewiesen ist. Auch eine Thyreotoxikose kann eine Takotsubo-Kardiomyopathie auslösen, und eine multizentrische Beobachtungsstudie hat kürzlich nachgewiesen, dass eine normale Schilddrüsenfunktion bei von einer Stress-Kardiomyopathie Betroffenen eher die Ausnahme als die Regel darstellt. Schilddrüsenhormone könnten dabei über eine Hochregulation von Betarezeptoren die Empfindlichkeit des Myokards für Katecholamine erhöhen. ⓘ
Diagnose
Mehrere angesehene medizinische Forschungsinstitute haben klinische Kriterien für die Diagnose von TTS aufgestellt. Einer der ersten Leitfäden wurde erstmals 2004 und erneut 2008 von der Mayo Clinic veröffentlicht. Weitere Forschungseinrichtungen, die Diagnosekriterien vorschlagen, sind die Japanese Takotsubo Cardiomyopathy Study Group, die Universität Göteborg, die Johns Hopkins University, das Takotsubo Italian Network und die Heart Failure Associates TTS Taskforce der European Society of Cardiology. Alle Forschungseinrichtungen sind sich über mindestens zwei Hauptkriterien einig, die für eine genaue Diagnose des TTS erforderlich sind: 1) eine vorübergehende linksventrikuläre Wandbewegungsanomalie und 2) das Fehlen einer Erkrankung, die diese Wandbewegungsanomalie offensichtlich erklärt (Koronararterienläsion, Hypoperfusion, Myokarditis, Toxizität usw.). Weitere allgemein anerkannte Kriterien, die für die Diagnose erforderlich sind, sind charakteristische EKG-Veränderungen und ein leichter bis mäßiger Anstieg des kardialen Troponins. ⓘ
Das transiente apikale Ballonsyndrom oder die Takotsubo-Kardiomyopathie tritt bei 1,7-2,2 % der Patienten auf, die ein akutes Koronarsyndrom haben. Während die ursprünglichen Fallstudien über Personen in Japan berichteten, wurde die Takotsubo-Kardiomyopathie erst in jüngerer Zeit in den Vereinigten Staaten und Westeuropa festgestellt. Es ist wahrscheinlich, dass das Syndrom zuvor nicht diagnostiziert wurde, bevor es in der japanischen Literatur ausführlich beschrieben wurde. Die Untersuchung von Personen mit Takotsubo-Kardiomyopathie umfasst in der Regel ein Koronarangiogramm, um einen Verschluss der linken vorderen absteigenden Arterie auszuschließen, wobei keine signifikanten Blockaden festgestellt werden, die die linksventrikuläre Dysfunktion verursachen würden. Sofern der Betroffene die Erstvorstellung überlebt, verbessert sich die linksventrikuläre Funktion innerhalb von zwei Monaten. ⓘ
Die Diagnose der Takotsubo-Kardiomyopathie kann bei der Vorstellung schwierig sein. Die EKG-Befunde werden oft mit denen verwechselt, die bei einem akuten Vorderwandinfarkt auftreten. Die Takotsubo-Kardiomyopathie ahmt klassischerweise einen Myokardinfarkt mit ST-Strecken-Hebung nach und ist gekennzeichnet durch das akute Auftreten vorübergehender ventrikulärer apikaler Wandbewegungsstörungen (Ballooning), begleitet von Brustschmerzen, Kurzatmigkeit, ST-Strecken-Hebung, T-Wellen-Inversion oder QT-Intervall-Verlängerung im EKG. Die Herzenzyme sind in der Regel negativ und im schlimmsten Fall mäßig, und eine Herzkatheteruntersuchung zeigt in der Regel keine signifikante Koronararterienerkrankung. ⓘ
Die Diagnose wird anhand der pathognomonischen Wandbewegungsanomalien gestellt, bei denen die Basis des linken Ventrikels normal kontrahiert oder hyperkinetisch ist, während der Rest des linken Ventrikels akinetisch oder dyskinetisch ist. Dies geht einher mit dem Fehlen einer signifikanten koronaren Herzerkrankung, die die Wandbewegungsanomalien erklären würde. Obwohl die apikale Ballonierung klassischerweise als angiografische Manifestation des Takotsubo-Syndroms beschrieben wurde, hat sich gezeigt, dass die linksventrikuläre Dysfunktion bei diesem Syndrom nicht nur die klassische apikale Ballonierung umfasst, sondern auch verschiedene angiografische Morphologien wie die mittelventrikuläre Ballonierung und, selten, die lokale Ballonierung anderer Segmente. ⓘ
Die Ballonierungsmuster wurden von Shimizu et al. als Takotsubo-Typ für apikale Akinesie und basale Hyperkinesie, als reverser Takotsubo-Typ für basale Akinesie und apikale Hyperkinesie, als mittelventrikulärer Typ für mittelventrikuläre Ballonierung in Verbindung mit basaler und apikaler Hyperkinesie und als lokalisierter Typ für jede andere segmentale linksventrikuläre Ballonierung mit klinischen Merkmalen einer Takotsubo-ähnlichen linksventrikulären Dysfunktion klassifiziert. ⓘ
Kurz gesagt, die Hauptkriterien für die Diagnose der Takotsubo-Kardiomyopathie sind: Der Patient muss einen Stressor erlebt haben, bevor die Symptome auftraten; die EKG-Werte des Patienten müssen Anomalien gegenüber einem normalen Herzen aufweisen; der Patient darf keine Anzeichen einer Koronarblockade oder anderer üblicher Ursachen für Herzbeschwerden aufweisen; die Werte der Herzenzyme im Herzen müssen erhöht oder unregelmäßig sein; und der Patient muss innerhalb kurzer Zeit eine vollständige Kontraktion wiedererlangen und normal funktionieren. ⓘ
Echokardiogramm, das die Auswirkungen der Krankheit zeigt ⓘ
Behandlung
Die Behandlung der Takotsubo-Kardiomyopathie ist im Allgemeinen unterstützend, da es sich um eine vorübergehende Störung handelt. Die Behandlung hängt davon ab, ob bei den Patienten eine Herzinsuffizienz oder eine akute Hypotonie und ein Schock auftreten. Bei vielen Betroffenen normalisiert sich die linksventrikuläre Funktion innerhalb von zwei Monaten. Auch Aspirin und andere Herzmedikamente scheinen bei der Behandlung dieser Krankheit zu helfen, selbst in extremen Fällen. Nach der Diagnose und dem Ausschluss eines Myokardinfarkts (Herzinfarkts) kann die Aspirin-Kur abgesetzt werden, und die Behandlung besteht nun in der Unterstützung des Patienten. Derzeit gibt es kein international anerkanntes Protokoll für die Behandlung dieser Erkrankung. ⓘ
Während medizinische Behandlungen wichtig sind, um die akuten Symptome der Takotsubo-Kardiomyopathie zu behandeln, umfasst die weitere Behandlung auch Änderungen der Lebensweise. Es ist wichtig, dass der Betroffene körperlich gesund bleibt und gleichzeitig Methoden zur Stressbewältigung und zur Bewältigung künftiger schwieriger Situationen erlernt und beibehält. ⓘ
Obwohl die Symptome der Takotsubo-Kardiomyopathie in der Regel von selbst abklingen und sich die Erkrankung innerhalb weniger Wochen vollständig zurückbildet, können einige ernste kurz- und langfristige Komplikationen auftreten, die behandelt werden müssen. Zu diesen Komplikationen gehören am häufigsten Herzinsuffizienz und sehr niedriger Blutdruck, seltener Blutgerinnsel in der Spitze der linken Herzkammer, Herzrhythmusstörungen und Risse in der Herzwand. ⓘ
Herzinsuffizienz
Bei Patienten mit akuter Herzinsuffizienz gelten ACE-Hemmer, Angiotensin-Rezeptorblocker und Betablocker als Hauptpfeiler der Behandlung der Herzinsuffizienz. Der Einsatz von Betablockern speziell bei Takotsubo-Kardiomyopathie ist jedoch umstritten, da sie möglicherweise keinen Nutzen bringen. ⓘ
Niedriger Blutdruck
Bei Menschen mit kardiogenem Schock richtet sich die medizinische Behandlung danach, ob eine Obstruktion des linksventrikulären Ausflusstrakts (LVOT) vorliegt. Daher ist eine frühzeitige Echokardiografie erforderlich, um die richtige Behandlung festzulegen. Bei Patienten mit einer Obstruktion des linken Ventrikelausflusses (LVOT) sollten keine inotropen Wirkstoffe eingesetzt werden, sondern sie sollten wie Patienten mit hypertropher Kardiomyopathie behandelt werden (z. B. mit Phenylephrin und Flüssigkeitszufuhr). In Fällen, in denen der LVOT nicht blockiert ist, kann eine inotrope Therapie (z. B. Dobutamin und Dopamin) eingesetzt werden, wobei jedoch zu bedenken ist, dass Takotsubo durch einen Überschuss an Katecholaminen verursacht wird. ⓘ
Darüber hinaus hat sich die mechanische Kreislaufunterstützung (MCS) mit einer intraaortalen Ballonpumpe (IABP) als unterstützende Behandlung bewährt. ⓘ
Prognose
Trotz des schwerwiegenden Ausgangszustands bei einigen Patienten überleben die meisten Patienten das erste akute Ereignis mit einer sehr geringen Sterblichkeits- oder Komplikationsrate im Krankenhaus. Sobald sich ein Patient von der akuten Phase des Syndroms erholt hat, kann er mit einem günstigen Ausgang rechnen, und die Langzeitprognose ist bei den meisten Patienten ausgezeichnet. Selbst wenn die ventrikuläre systolische Funktion bei der Vorstellung stark beeinträchtigt ist, verbessert sie sich in der Regel innerhalb der ersten Tage und normalisiert sich innerhalb der ersten Monate. Obwohl selten, wurde über ein Wiederauftreten des Syndroms berichtet, das offenbar mit der Art des Auslösers zusammenhängt. Die Stresskardiomyopathie ist heute eine anerkannte Ursache für akute Herzinsuffizienz, tödliche Herzrhythmusstörungen und Rupturen der Herzwand. ⓘ
Epidemiologie
Verlässliche epidemiologische Daten fehlen, das Wissen über die Stress-Kardiomyopathie stützt sich auf Einzelfallschilderungen und die Beschreibung von „Kleinstserien“ mit wenigen Patienten. Bis Mitte 2006 sind weltweit erst etwa 700 Patienten mit einer Tako-Tsubo-Kardiomyopathie beschrieben worden, davon etwa 400 in Japan und jeweils etwa 150 in Europa und Nordamerika. Seit 2004 wurde auch über Patienten in Australien und Südamerika berichtet, so dass von einer weltweiten und bislang unterschätzten Verbreitung ausgegangen wird. ⓘ
Anhand jeweils geringer Patientenzahlen ist bislang festgestellt worden, dass in Japan 1,2 bis 2,2 %, in den USA etwa 2,2 % und in Deutschland 2,3 bis 2,6 % aller Patienten mit einem akuten Koronarsyndrom an einer Stress-Kardiomyopathie litten, unter den weiblichen Patienten betrug dieser Anteil immerhin etwa 7,5 %. Mehr als 90 % der beschriebenen Patienten waren Frauen, das mittlere Alter lag bei 62–75 Jahren. ⓘ
Auch extrem scharfe Speisen können eine Tako-Tsubo-Kardiomyopathie auslösen. ⓘ
Geschichte

Rees et al. schrieben 1967, dass der Tod eines nahen Verwandten das Risiko, innerhalb eines Jahres zu sterben, um das Siebenfache erhöht. ⓘ
Engel schrieb 1971 über den plötzlichen und schnellen Tod bei psychischem Stress und zählte acht Ursachenkategorien auf: (1) bei den Auswirkungen des Zusammenbruchs oder des Todes einer nahestehenden Person; (2) bei akuter Trauer; (3) bei drohendem Verlust einer nahestehenden Person; (4) während der Trauer oder an einem Jahrestag; (5) bei Verlust von Status oder Selbstwertgefühl; (6) bei persönlicher Gefahr oder drohender Verletzung; (7) nach Überwindung der Gefahr; (8) bei Wiedersehen, Triumph oder Happy End. Er schlug vor, dass diese Ereignisse neurovegetative Reaktionen auslösen, an denen sowohl das Flucht-Kampf- als auch das Erhaltungs-Rückzug-System beteiligt sind, was zu tödlichen kardialen Ereignissen führen kann, insbesondere bei Personen mit vorbestehenden Herz-Kreislauf-Erkrankungen. ⓘ
Obwohl die erste wissenschaftliche Beschreibung der Takotsubo-Kardiomyopathie erst in den 1990er Jahren erfolgte, schrieben Cebelin und Hirsch 1980 über die Stress-Kardiomyopathie beim Menschen. Die beiden untersuchten tödliche Angriffe, die sich in den letzten 30 Jahren in Cuyahoga County, Ohio, ereignet hatten, und zwar speziell diejenigen mit Autopsien, die keine inneren Verletzungen aufwiesen, aber an körperlichen Angriffen gestorben waren. Sie fanden heraus, dass 11 von 15 eine myofibrilläre Degeneration aufwiesen, ähnlich wie bei Stressstudien an Tieren. Schließlich kamen sie zu dem Schluss, dass ihre Daten "die Theorie der Katecholamin-Vermittlung dieser myokardialen Veränderungen beim Menschen und des tödlichen Potenzials von Stress durch seine Wirkung auf das Herz" stützen. ⓘ
Der erste untersuchte Fall von Takotsubo-Kardiomyopathie wurde 1991 in Japan von Sato et al. beschrieben. In den folgenden zehn Jahren traten in Japan weitere Fälle des Syndroms auf, obwohl es in der westlichen Medizin noch nicht anerkannt war. Das Syndrom trat schließlich 1997 auf, als Pavin et al. über zwei Fälle von "reversibler LV-Dysfunktion, die durch akuten emotionalen Stress ausgelöst wurde", schrieben. Die westliche Welt hatte zu diesem Zeitpunkt noch nichts davon gehört, da es unglaublich selten war und oft falsch diagnostiziert wurde. Die Japaner berichteten dem Westen schließlich 2001 über das Syndrom unter dem Namen "transient LV apical ballooning", obwohl zu diesem Zeitpunkt im Westen bereits zahlreiche Fälle bekannt waren. Ein internationales Publikum erreichte das Syndrom über die Medien im Jahr 2005, als das New England Journal of Medicine über das Syndrom schrieb. ⓘ
Das Krankheitsbild wurde 1991 erstmals beschrieben, Namensgeber war eine japanische Tintenfischfalle in Form eines Kruges mit kurzem Hals (Tako-Tsubo, s. Abbildung). Die daran erinnernde eigentümliche Form der linken Herzkammer (linker Ventrikel) am Ende der Systole wurde von den Erstautoren als Folge einer Durchblutungsstörung des Herzmuskels angesehen, verursacht durch die krampfartige Verengung mehrerer Herzkranzgefäße (Koronarspasmen). ⓘ
In der im März 2006 aktualisierten Definition und Klassifikation der Kardiomyopathien der US-amerikanischen American Heart Association (AHA) ist die „Stress (‚Tako-Tsubo‘) Cardiomyopathy“ neben der Myokarditis als erworbene primäre Kardiomyopathie klassifiziert. ⓘ
In der Popkultur
Der Name und der Titelsong des 2021 erschienenen Albums Tako Tsubo der französischen Band L'Impératrice beziehen sich auf den starken emotionalen Stress, der dieses Syndrom auslösen kann. ⓘ
Krankheitsbild
Akutphase
Die Symptome der Stress-Kardiomyopathie gleichen denen eines Herzinfarktes. Charakteristisch sind plötzlich beginnende heftige Brustschmerzen (Angina Pectoris) und Luftnot (Dyspnoe). Im Akutstadium ist eine Unterscheidung zum Herzinfarkt ohne Herzkatheteruntersuchung nicht möglich, so dass das Ereignis zunächst als akutes Koronarsyndrom bezeichnet und behandelt wird. ⓘ
Fast allen Patienten ist gemeinsam, dass die Symptome kurz nach einem emotional belastenden Ereignis wie beispielsweise dem Tod einer nahestehenden Person, der Trennung vom Partner, einem Unfall, einem Überfall, einer Naturkatastrophe, einem heftigen Streit, dem Verlust der materiellen Existenz oder der Diagnose einer schweren Erkrankung einsetzen, durchaus aber auch nach erfreulichen Überraschungen wie der Nachricht von einem größeren Lottogewinn. Entgegen ersten und auch heute noch verbreitet geäußerten Vermutungen ist die Tako-Tsubo-Kardiomyopathie nicht ungefährlich. Besonders in den ersten Stunden ist die Gefahr von ernsthaften Komplikationen hoch. Angaben über deren Häufigkeit schwanken zwischen 18,9 % und bis zu 46 %. Ein kardiogener Schock tritt bei etwa 15 %, eine ernste Herzrhythmusstörung (ventrikuläre Tachykardie oder Kammerflimmern) bei etwa 9 % der Patienten auf. ⓘ
Verlauf und Prognose
Die Veränderungen am Herzmuskel bilden sich in der Regel innerhalb von Wochen vollständig zurück, auch das EKG normalisiert sich meist. In einer 2005 publizierten Übersicht aller bis dato veröffentlichten Fälle wird eine Mortalität von 3,2 % angegeben. Nach überstandener Akutphase scheint das Risiko für ein erneutes Auftreten (Rezidiv) des Syndroms gering zu sein. ⓘ

Diagnostik
Als diagnostische Kriterien für die Stress-Kardiomyopathie gelten:
- eine vorübergehende Bewegungsstörung der linken Herzkammer, die nicht dem Versorgungsgebiet eines Herzkranzgefäßes entspricht,
- der Ausschluss von höhergradigen Verengungen der Herzkranzgefäße,
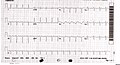
- neu aufgetretene EKG-Veränderungen ähnlich denen eines Herzinfarktes und
- der zeitliche Zusammenhang mit einer vorausgegangenen Stresssituation. ⓘ
Die körperliche Untersuchung kann normale Befunde ergeben oder Zeichen der Herzinsuffizienz wie einen dritten Herzton oder Rasselgeräusche über der Lunge aufdecken. ⓘ
Differentialdiagnostisch gilt es, die Stress-Kardiomyopathie abzugrenzen einerseits von einem akuten Koronarsyndrom auf der Basis einer koronaren Herzkrankheit und andererseits von einem Phäochromozytom oder auch drittens von einer hypertroph-obstruktiven Kardiomyopathie. ⓘ
Bildgebende Verfahren


A Stress-Kardiomyopathie
B Normalperson ⓘ
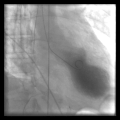
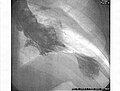
Die Röntgenaufnahme der Thoraxorgane ist unauffällig oder zeigt eine sogenannte Lungenstauung („Wasser in der Lunge“) als Folge der Herzinsuffizienz. Bei der Echokardiografie ist die für das Tako-Tsubo-Syndrom typische Bewegungsstörung (Kontraktionsstörung) der linken Herzkammer oft nachweisbar, das apical ballooning. Diese auch bei der Laevokardiografie im Rahmen einer Herzkatheteruntersuchung nachweisbare Kontraktionsstörung des linken Ventrikels macht sich als oft eindrucksvolle Unbeweglichkeit (Akinesie) oder gar als paradoxe Beweglichkeit (Dyskinesie) der Herzspitze bemerkbar, die Ähnlichkeit mit einem Aneurysma aufweisen kann. ⓘ
Im Unterschied zum Herzinfarkt ist allerdings bei der Koronarangiografie keine Verstopfung der Herzkranzgefäße nachweisbar. Erst dieser Befund der Herzkatheteruntersuchung erlaubt die zuverlässige Abgrenzung zum Herzinfarkt. ⓘ
Aussagekräftige Befunde liefert auch die Magnetresonanztomografie (MRT), die sowohl die Bewegungsstörung des Herzmuskels in guter Qualität als auch nach Gadoliniumgabe das Fehlen einer Vernarbung erkennen lässt. ⓘ
Therapie
Mangels entsprechender Therapiestudien gibt es keine durch objektive Daten abgesicherte Standardtherapie der Stress-Kardiomyopathie. Auf Grund der hohen Komplikationsrate im Akutstadium wird eine Monitorüberwachung auf der Intensivstation vorgenommen. Da die hohen Katecholaminspiegel als Ursache angesehen werden, wird zu einer möglichst weitgehenden Zurückhaltung bei der Zufuhr weiterer Katecholamine geraten. Für Patienten im Schock wird eine vorsichtige Volumenzufuhr empfohlen, gegebenenfalls auch die frühzeitige Anwendung der intraaortalen Ballonpumpe (IABP). Analog zur Therapie der Phäochromozytom-Krise können Alphablocker und bei hämodynamisch stabilen Patienten Betablocker sinnvoll sein. ⓘ