Akromegalie
| Akromegalie ⓘ | |
|---|---|
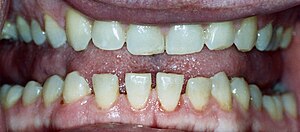 | |
| Unterkiefer mit klassischer Zahnspreizung aufgrund von Akromegalie. | |
| Aussprache |
|
| Fachgebiet | Endokrinologie |
| Symptome | Vergrößerung von Händen, Füßen, Stirn, Kiefer und Nase, Verdickung der Haut, Vertiefung der Stimme |
| Komplikationen | Typ-2-Diabetes, Schlafapnoe, Bluthochdruck, hoher Cholesterinspiegel, Herzprobleme, insbesondere Vergrößerung des Herzens (Kardiomyopathie), Osteoarthritis, Rückenmarkskompression oder -brüche, erhöhtes Risiko für Krebstumore, Krebsvorstufen (Polypen) in der Darmschleimhaut. |
| Übliches Auftreten | Mittleres Alter |
| Ursachen | Überschüssiges Wachstumshormon |
| Diagnostische Methode | Bluttests, medizinische Bildgebung |
| Differentialdiagnose | Pachydermoperiostose |
| Behandlung | Operation, Medikamente, Strahlentherapie |
| Medikation | Somatostatin-Analogon, GH-Rezeptor-Antagonist |
| Prognose | Normalerweise normal (mit Behandlung), 10 Jahre kürzere Lebenserwartung (ohne Behandlung) |
| Häufigkeit | 3 pro 50.000 Menschen |
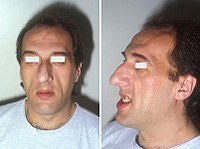
Akromegalie ist eine Erkrankung, die durch einen Überschuss an Wachstumshormonen (GH) entsteht, nachdem sich die Wachstumsfugen geschlossen haben. Das erste Symptom ist in der Regel eine Vergrößerung der Hände und Füße. Es kann auch zu einer Vergrößerung von Stirn, Kiefer und Nase kommen. Weitere Symptome können Gelenkschmerzen, dickere Haut, eine tiefere Stimme, Kopfschmerzen und Sehstörungen sein. Zu den Komplikationen der Krankheit können Typ-2-Diabetes, Schlafapnoe und Bluthochdruck gehören. ⓘ
Akromegalie wird in der Regel dadurch verursacht, dass die Hirnanhangsdrüse einen Überschuss an Wachstumshormonen produziert. In mehr als 95 % der Fälle ist die übermäßige Produktion auf einen gutartigen Tumor, ein so genanntes Hypophysenadenom, zurückzuführen. Die Erkrankung wird nicht von den Eltern vererbt. Selten ist die Akromegalie auf einen Tumor in einem anderen Teil des Körpers zurückzuführen. Die Diagnose wird durch Messung des Wachstumshormons nach Einnahme einer Glukoselösung oder durch Messung des insulinähnlichen Wachstumsfaktors I im Blut gestellt. Nach der Diagnose wird eine medizinische Bildgebung der Hypophyse durchgeführt, um festzustellen, ob ein Adenom vorhanden ist. Wird in der Kindheit ein Überschuss an Wachstumshormonen produziert, spricht man nicht von Akromegalie, sondern von Gigantismus, der durch übermäßige Körpergröße gekennzeichnet ist. ⓘ
Zu den Behandlungsmöglichkeiten gehören die operative Entfernung des Tumors, Medikamente und Strahlentherapie. Eine Operation ist in der Regel die bevorzugte Behandlung; je kleiner der Tumor ist, desto wahrscheinlicher ist es, dass er durch eine Operation geheilt werden kann. Ist eine Operation kontraindiziert oder nicht heilbar, können Somatostatin-Analoga oder GH-Rezeptor-Antagonisten eingesetzt werden. Eine Strahlentherapie kann eingesetzt werden, wenn weder eine Operation noch Medikamente vollständig wirksam sind. Ohne Behandlung verringert sich die Lebenserwartung um 10 Jahre, mit Behandlung bleibt sie gleich. ⓘ
Akromegalie betrifft etwa 3 von 50.000 Menschen. Am häufigsten wird sie im mittleren Lebensalter diagnostiziert. Männer und Frauen sind gleich häufig betroffen. Sie wurde erstmals 1772 von Nicolas Saucerotte in der medizinischen Literatur beschrieben. Der Begriff leitet sich aus dem griechischen ἄκρον (akron) für "Extremität" und μέγα (mega) für "groß" ab. ⓘ
| Klassifikation nach ICD-10 ⓘ | |
|---|---|
| E22.0 | Akromegalie und hypophysärer Hochwuchs |
| ICD-10 online (WHO-Version 2019) | |
Als Akromegalie (aus altgriechisch ἄκρος akros, ‚äußerst‘, + μέγας megas, ‚groß‘) wird eine ausgeprägte chronische, durch einen Überschuss an Wachstumshormon (Somatotropin) verursachte Vergrößerung von Akren (distale Teile (periphere Enden) der Extremitäten und vorspringende Teile des Körpers) bezeichnet. Dazu zählen z. B. Hände, Füße, Kinn, Ohren, Nase und die äußeren Genitalien.
Ihren Namen erhielt die Krankheit 1886 von dem französischen Neurologen Pierre Marie, weswegen sie manchmal auch (Pierre-)Marie-Syndrom genannt wird. Ein weiteres, gelegentlich gebrauchtes Synonym ist Pachyakrie (altgr. παχύς pachýs, ‚dick‘). ⓘ
Die Inzidenz (Neuerkrankungsrate) liegt im Jahr bei etwa drei bis vier Menschen pro eine Million Einwohner, die Prävalenz (Krankheitshäufigkeit) in Deutschland bei ungefähr 3.000 bis 6.000 Menschen. ⓘ
Anzeichen und Symptome
Zu den Merkmalen, die sich aus einem hohen GH-Spiegel oder einem expandierenden Tumor ergeben können, gehören:
- Kopfschmerzen - oft stark und lang anhaltend
- Weichteilschwellungen, die zu einer sichtbaren Vergrößerung von Händen, Füßen, Nase, Lippen und Ohren sowie zu einer allgemeinen Verdickung der Haut führen
- Weichteilschwellung der inneren Organe, insbesondere des Herzens mit der damit verbundenen Schwächung seiner Muskulatur und der Nieren, sowie der Stimmbänder, was zu einer charakteristischen dicken, tiefen Stimme und einer Verlangsamung der Sprache führt
- Generalisierte Ausdehnung des Schädels an der Fontanelle
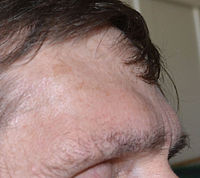
- Ausgeprägte Vorwölbung der Augenbrauen, oft mit einer Vergrößerung des Auges (frontale Vorwölbung)
- Ausgeprägter Unterkieferprotrusion (Prognathismus) mit einhergehender Makroglossie (Vergrößerung der Zunge) und Zahnspreizung
- Hypertrichose, Hyperpigmentierung und Hyperhidrose können bei diesen Menschen auftreten.
- Hautanhängsel
- Karpaltunnelsyndrom ⓘ
Komplikationen
- Probleme mit Knochen und Gelenken, einschließlich Osteoarthritis, Nervenkompressionssyndrom aufgrund von Knochenüberwucherungen und Karpaltunnelsyndrom
- Bluthochdruck
- Diabetes mellitus
- Kardiomyopathie, die zu Herzversagen führen kann
- Kolorektaler Krebs
- Schlaf-Apnoe
- Schilddrüsenknötchen und Schilddrüsenkrebs
- Hypogonadismus
- Kompression des Chiasma opticum durch das Wachstum eines Hypophysenadenoms, was zu Sehproblemen führt ⓘ
Ursachen
Die Akromegalie ist eine endokrinologische Erkrankung, die durch eine Überproduktion des Wachstumshormons Somatropin hervorgerufen wird. In 95 Prozent der Fälle liegt der Krankheit ein wachstumshormon-produzierendes Adenom (gutartiger Tumor) in der Adenohypophyse (Vorderlappen der Hirnanhangdrüse) zugrunde, nur selten ein maligner (bösartiger) Tumor. ⓘ
Sehr selten tritt eine Akromegalie im Rahmen von erblichen Krankheiten auf, z. B. bei der Lipodystrophie Typ Berardinelli. ⓘ
Die Anwendung von Somatropin bei Menschen ohne vorliegenden Mangel führt zu Akromegalie mit schwersten Nebenwirkungen, die oft irreversibel sind. ⓘ
Hypophysenadenom
Etwa 98 % der Fälle von Akromegalie sind auf eine Überproduktion von Wachstumshormonen durch einen gutartigen Tumor der Hirnanhangsdrüse, ein so genanntes Adenom, zurückzuführen. Diese Tumore produzieren übermäßig viel Wachstumshormon und komprimieren das umliegende Hirngewebe, wenn sie größer werden. In einigen Fällen können sie auch die Sehnerven zusammendrücken. Die Ausdehnung des Tumors kann zu Kopfschmerzen und Sehstörungen führen. Darüber hinaus kann die Kompression des umgebenden normalen Hypophysengewebes die Produktion anderer Hormone verändern, was bei Frauen zu Veränderungen der Menstruation und des Brustausflusses und bei Männern zu Impotenz aufgrund einer verminderten Testosteronproduktion führt. ⓘ
Die Geschwindigkeit der GH-Produktion und die Aggressivität des Tumors variieren stark. Einige Adenome wachsen langsam und die Symptome eines GH-Überschusses werden oft erst nach vielen Jahren bemerkt. Andere Adenome wachsen schnell und dringen in die umliegenden Hirnregionen oder in die Nebenhöhlen ein, die sich in der Nähe der Hypophyse befinden. Im Allgemeinen neigen jüngere Menschen dazu, aggressivere Tumore zu haben. ⓘ
Die meisten Hypophysentumoren entstehen spontan und werden nicht genetisch vererbt. Viele Hypophysentumoren entstehen durch eine genetische Veränderung in einer einzelnen Hypophysenzelle, die zu einer vermehrten Zellteilung und Tumorbildung führt. Diese genetische Veränderung, oder Mutation, ist nicht bei der Geburt vorhanden, sondern wird im Laufe des Lebens erworben. Die Mutation tritt in einem Gen auf, das die Übertragung chemischer Signale innerhalb der Hypophysenzellen regelt; sie schaltet das Signal, das die Zelle zur Teilung und zur Ausschüttung von Wachstumshormonen anregt, dauerhaft ein. Die Vorgänge innerhalb der Zelle, die das gestörte Wachstum der Hypophysenzellen und die Überproduktion von GH verursachen, sind derzeit Gegenstand intensiver Forschung. ⓘ
Hypophysenadenome und diffuse somatomammotrophe Hyperplasie können aus somatischen Mutationen resultieren, die GNAS aktivieren, was erworben oder mit dem McCune-Albright-Syndrom assoziiert sein kann. ⓘ
Andere Tumore
Bei einigen wenigen Menschen wird die Akromegalie nicht durch Hypophysentumore, sondern durch Tumore der Bauchspeicheldrüse, der Lunge und der Nebennieren verursacht. Diese Tumore führen ebenfalls zu einem Überschuss an GH, entweder weil sie selbst GH produzieren oder, was häufiger der Fall ist, weil sie GHRH (Wachstumshormon-freisetzendes Hormon) produzieren, das Hormon, das die Hypophyse zur GH-Produktion anregt. Bei diesen Menschen kann das überschüssige GHRH im Blut gemessen werden, was beweist, dass die Ursache der Akromegalie nicht auf einen Hypophysendefekt zurückzuführen ist. Wenn diese nicht-hypophysären Tumore operativ entfernt werden, sinkt der GH-Spiegel und die Symptome der Akromegalie verbessern sich. ⓘ
Bei Menschen mit GHRH-produzierenden, nicht-hypophysären Tumoren kann die Hypophyse dennoch vergrößert sein und fälschlicherweise für einen Tumor gehalten werden. Daher ist es wichtig, dass Ärzte alle "Hypophysentumore", die bei Menschen mit Akromegalie entfernt werden, sorgfältig untersuchen, um nicht die Möglichkeit zu übersehen, dass ein Tumor an anderer Stelle im Körper die Erkrankung verursacht. ⓘ
Diagnose

Wenn der Verdacht auf Akromegalie besteht, können medizinische Laboruntersuchungen, gefolgt von einer medizinischen Bildgebung, wenn die Labortests positiv sind, das Vorliegen dieser Erkrankung bestätigen oder ausschließen. ⓘ
IGF1 ist der empfindlichste Labortest für die Diagnose der Akromegalie, und ein GH-Suppressionstest nach einer oralen Glukosebelastung, der ein sehr spezifischer Labortest ist, bestätigt die Diagnose nach einem positiven Screeningtest für IGF1. Ein einziger GH-Wert ist angesichts der Pulsatilität des GH (die Blutspiegel schwanken selbst bei gesunden Personen stark) nicht sinnvoll.
GH-Werte, die 2 Stunden nach einem 75- oder 100-Gramm-Glukosetoleranztest gemessen werden, sind für die Diagnose hilfreich: GH-Spiegel werden bei normalen Menschen unter 1 μg/L unterdrückt, und Werte, die über diesem Grenzwert liegen, bestätigen die Akromegalie. ⓘ
Andere Hypophysenhormone müssen bestimmt werden, um die sekretorischen Wirkungen des Tumors sowie die Massenwirkung des Tumors auf die normale Hypophyse zu erfassen. Dazu gehören das schilddrüsenstimulierende Hormon (TSH), gonadotrope Hormone (FSH, LH), adrenokortikotropes Hormon und Prolaktin. ⓘ
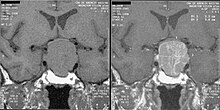
Eine MRT des Gehirns mit Schwerpunkt auf der Sella turcica nach Gadolinium-Gabe ermöglicht eine klare Abgrenzung der Hypophyse und des Hypothalamus sowie die Lokalisierung des Tumors. Eine Reihe von anderen Überwuchssyndromen kann zu ähnlichen Problemen führen. ⓘ
Die Akromegalie verläuft schleichend, was die Diagnose erschwert. Häufig werden ihre Symptome zunächst fehlgedeutet. Es wird selten ein Verdacht auf Akromegalie geäußert. So kommt es, dass die Diagnose im Mittel erst neun bis zehn Jahre nach dem Beginn der Symptome gestellt wird. ⓘ
Neben dem typischen klinischen Bild der Erkrankung mit fast immer vergrößerten Händen und Füßen ist die Bestimmung der Hormonaktivität entscheidend. ⓘ
Sobald der Verdacht auf eine Akromegalie besteht, sollte zuerst IGF-1 (insulin-like growth factor-I) bestimmt werden. Dieses Hormon eignet sich am besten sowohl als Suchtest als auch zur Beurteilung des Erfolgs nach einer Behandlung, da eine Akromegalie bei normalen Werten extrem selten vorliegt. ⓘ
Die Bestimmung des Wachstumshormons (auch: GH = Growth Hormone = Somatotropin = Somatotropes Hormon = STH) selbst ist möglich, aber wesentlich weniger empfindlich und daher von geringer Bedeutung. Seit über 40 Jahren ist deshalb die empfindlichere Messung des Wachstumshormons nach einer Provokation mit Traubenzucker (STH-Suppressionstest beim oralen Glukosetoleranztest OGTT) in Gebrauch. Keine praktische Bedeutung hat die Bestimmung des Growth-hormone releasing factors (GHRF). ⓘ
Selten tritt die Akromegalie als Teil eines genetischen Syndroms auf. Dazu gehören die multiple endokrine Neoplasie Typ 1 (MEN 1), das McCune-Albright-Syndrom, die familiäre Akromegalie und der Carney-Komplex. Zur weiteren Diagnostik (Tumornachweis) dienen zusätzlich CT und MRT. ⓘ
Differentialdiagnose
Pseudoakromegalie ist ein Zustand mit den üblichen akromegaloiden Merkmalen, jedoch ohne Anstieg von Wachstumshormon und IGF-1. Sie ist häufig mit einer Insulinresistenz verbunden. Es wurde über Fälle berichtet, die durch Minoxidil in einer ungewöhnlich hohen Dosis verursacht wurden. Sie kann auch durch einen selektiven Postrezeptordefekt der Insulinsignalisierung verursacht werden, der zu einer Beeinträchtigung der metabolischen, aber Erhaltung der mitogenen Signalisierung führt. ⓘ
Behandlung
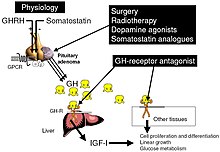
Ziel der Behandlung ist es, die GH-Produktion auf ein normales Niveau zu senken und damit die Anzeichen und Symptome der Akromegalie rückgängig zu machen oder zu lindern, den Druck, den der wachsende Hypophysentumor auf die umliegenden Hirnareale ausübt, zu verringern und die normale Hypophysenfunktion zu erhalten. Zu den derzeitigen Behandlungsmöglichkeiten gehören die chirurgische Entfernung des Tumors, die medikamentöse Therapie und die Strahlentherapie der Hypophyse. ⓘ
Medikamente
Somatostatin-Analoga
Die wichtigste derzeitige medikamentöse Behandlung der Akromegalie besteht in der Anwendung von Somatostatin-Analoga - Octreotid (Sandostatin) oder Lanreotid (Somatuline). Diese Somatostatin-Analoga sind synthetische Formen eines Hormons im Gehirn, Somatostatin, das die GH-Produktion stoppt. Die langwirksamen Formen dieser Medikamente müssen für eine wirksame Behandlung alle 2 bis 4 Wochen injiziert werden. Die meisten Menschen mit Akromegalie sprechen auf diese Medikamente an. Bei vielen Menschen mit Akromegalie sinkt der GH-Spiegel innerhalb einer Stunde und die Kopfschmerzen bessern sich innerhalb von Minuten nach der Injektion. Octreotid und Lanreotid sind für die Langzeitbehandlung wirksam. Octreotid und Lanreotid wurden auch erfolgreich zur Behandlung von Menschen mit Akromegalie eingesetzt, die durch nicht-hypophysäre Tumoren verursacht wurde. ⓘ
Somatostatinanaloga werden manchmal auch zur Verkleinerung großer Tumore vor einer Operation eingesetzt. ⓘ
Da Octreotid die Funktion des Magen-Darm-Trakts und der Bauchspeicheldrüse hemmt, führt die Langzeitanwendung bei einem Drittel der Patienten zu Verdauungsproblemen wie lockerem Stuhlgang, Übelkeit und Blähungen. Darüber hinaus entwickeln etwa 25 Prozent der Menschen mit Akromegalie Gallensteine, die in der Regel symptomlos sind. In einigen Fällen kann die Behandlung mit Octreotid zu Diabetes führen, da Somatostatin und seine Analoga die Freisetzung von Insulin hemmen können. Bei einem aggressiven Adenom, das nicht operiert werden kann, kann eine Resistenz gegen Octreotid vorliegen; in diesem Fall kann ein SSA der zweiten Generation, Pasireotid, zur Tumorkontrolle eingesetzt werden. In diesem Fall kann ein SSA der zweiten Generation, Pasireotid, zur Tumorkontrolle eingesetzt werden. Allerdings sollten die Insulin- und Glukosespiegel sorgfältig überwacht werden, da Pasireotid durch die Verringerung der Insulinsekretion mit Hyperglykämie in Verbindung gebracht wurde. ⓘ
Dopamin-Agonisten
Bei Patienten, die nicht auf Somatostatin-Analoga ansprechen oder bei denen diese aus anderen Gründen kontraindiziert sind, ist eine Behandlung mit einem der Dopamin-Agonisten Bromocriptin oder Cabergolin möglich. Da sie als Tabletten und nicht als Injektionen verabreicht werden, sind sie wesentlich kostengünstiger. Diese Medikamente können auch als Ergänzung zu einer Therapie mit Somatostatinanaloga eingesetzt werden. Am wirksamsten sind sie bei Patienten, deren Hypophysentumore Prolaktin ausscheiden. Zu den Nebenwirkungen dieser Dopaminagonisten gehören Magen-Darm-Beschwerden, Übelkeit, Erbrechen, Schwindelgefühl beim Stehen und verstopfte Nase. Diese Nebenwirkungen können verringert oder beseitigt werden, wenn die Medikation mit einer sehr niedrigen Dosis vor dem Schlafengehen begonnen, mit Nahrung eingenommen und allmählich auf die volle therapeutische Dosis erhöht wird. Bromocriptin senkt die GH- und IGF-1-Spiegel und verringert die Tumorgröße bei weniger als der Hälfte der Patienten mit Akromegalie. Einige Betroffene berichten über eine Besserung ihrer Symptome, obwohl ihre GH- und IGF-1-Spiegel weiterhin erhöht sind. ⓘ
Wachstumshormon-Rezeptor-Antagonisten
Die neueste Entwicklung in der medizinischen Behandlung der Akromegalie ist der Einsatz von Wachstumshormonrezeptor-Antagonisten. Das einzige verfügbare Mitglied dieser Familie ist Pegvisomant (Somavert). Durch die Blockierung der Wirkung der körpereigenen Wachstumshormonmoleküle ist dieser Wirkstoff in der Lage, die Krankheitsaktivität der Akromegalie bei praktisch allen Patienten mit Akromegalie zu kontrollieren. Pegvisomant muss durch tägliche Injektionen subkutan verabreicht werden. Kombinationen aus langwirksamen Somatostatinanaloga und wöchentlichen Injektionen von Pegvisomant scheinen ebenso wirksam zu sein wie tägliche Injektionen von Pegvisomant. ⓘ
Chirurgie
Die chirurgische Entfernung des Hypophysentumors ist in der Regel wirksam, um den Wachstumshormonspiegel zu senken. Es stehen zwei chirurgische Verfahren zur Verfügung. Das erste ist die endonasale transsphenoidale Chirurgie, bei der der Chirurg die Hypophyse durch einen Einschnitt in der Nasenhöhlenwand erreicht. Die Wand wird mit mikrochirurgischen Instrumenten durch die Nasenlöcher erreicht. Die zweite Methode ist die transsphenoidale Chirurgie, bei der ein Einschnitt in das Zahnfleisch unterhalb der Oberlippe vorgenommen wird. Durch weitere Schnitte wird die Nasenscheidewand durchtrennt, um in die Nasenhöhle zu gelangen, wo sich die Hypophyse befindet. Die endonasale transsphenoidale Chirurgie ist ein weniger invasives Verfahren mit einer kürzeren Erholungszeit als die ältere Methode der transsphenoidalen Chirurgie, und die Wahrscheinlichkeit, den gesamten Tumor zu entfernen, ist größer bei geringeren Nebenwirkungen. Daher ist die endonasale transsphenoidale Chirurgie die häufigere chirurgische Wahl. ⓘ
Diese Verfahren entlasten normalerweise die umliegenden Hirnregionen und führen zu einer Senkung des GH-Spiegels. Am erfolgreichsten ist die Operation bei Personen, deren GH-Spiegel im Blut vor der Operation unter 40 ng/ml liegt und deren Hypophysentumor nicht größer als 10 mm im Durchmesser ist. Der Erfolg hängt von den Fähigkeiten und der Erfahrung des Chirurgen ab. Die Erfolgsquote hängt auch davon ab, welcher GH-Spiegel als Heilung definiert wird. Das beste Maß für den chirurgischen Erfolg ist die Normalisierung der GH- und IGF-1-Werte. Im Idealfall sollte der GH-Wert nach einer oralen Glukosebelastung unter 2 ng/ml liegen. Eine Untersuchung der GH-Werte von 1.360 Personen weltweit unmittelbar nach der Operation ergab, dass 60 % zufällige GH-Werte unter 5 ng/ml aufwiesen. Zu den Komplikationen der Operation können Liquorverluste, Meningitis oder eine Schädigung des umgebenden normalen Hypophysengewebes gehören, so dass eine lebenslange Hypophysenhormonsubstitution erforderlich ist. ⓘ
Selbst wenn die Operation erfolgreich verläuft und sich die Hormonwerte wieder normalisieren, müssen die Betroffenen über Jahre hinweg sorgfältig auf ein mögliches Wiederauftreten überwacht werden. Häufiger kommt es vor, dass sich die Hormonwerte zwar verbessern, aber nicht vollständig normalisieren. Diese Menschen benötigen dann möglicherweise eine zusätzliche Behandlung, in der Regel mit Medikamenten. ⓘ
Strahlentherapie
Die Strahlentherapie wird sowohl als alleinige Behandlung als auch in Kombination mit einer Operation oder Medikamenten eingesetzt. Sie ist in der Regel Menschen vorbehalten, bei denen nach der Operation ein Tumor verbleibt. Diese Menschen erhalten häufig auch Medikamente zur Senkung des GH-Spiegels. Die Strahlentherapie wird in geteilten Dosen über vier bis sechs Wochen verabreicht. Diese Behandlung senkt den GH-Spiegel über 2 bis 5 Jahre um etwa 50 Prozent. Bei Personen, die länger als 5 Jahre beobachtet werden, ist eine weitere deutliche Verbesserung festzustellen. Die Strahlentherapie führt mit der Zeit zu einem allmählichen Verlust der Produktion anderer Hypophysenhormone. Der Verlust des Sehvermögens und Hirnschäden, über die berichtet wurde, sind sehr seltene Komplikationen der Strahlenbehandlung. ⓘ
Auswahl der Behandlung
Die anfängliche Behandlung sollte je nach den Merkmalen der Person, wie Alter und Tumorgröße, individuell gewählt werden. Wenn der Tumor noch nicht in das umliegende Hirngewebe eingedrungen ist, ist die Entfernung des Hypophysenadenoms durch einen erfahrenen Neurochirurgen in der Regel die erste Wahl. Nach der Operation muss der Betroffene langfristig auf steigende GH-Spiegel überwacht werden. ⓘ
Wenn sich der Hormonspiegel durch die Operation nicht normalisiert oder ein Rückfall auftritt, wird der Arzt in der Regel eine zusätzliche medikamentöse Therapie einleiten. Die erste Wahl ist derzeit in der Regel Octreotid oder Lanreotid; Bromocriptin und Cabergolin sind jedoch billiger und einfacher zu verabreichen. Bei all diesen Medikamenten ist eine Langzeittherapie erforderlich, da ihr Absetzen zu einem Anstieg des GH-Spiegels und einer erneuten Vergrößerung des Tumors führen kann. ⓘ
Eine Strahlentherapie wird in der Regel bei Personen eingesetzt, deren Tumor durch eine Operation nicht vollständig entfernt werden kann, bei Personen, die aufgrund anderer gesundheitlicher Probleme nicht für eine Operation in Frage kommen, und bei Personen, die nicht ausreichend auf eine Operation und Medikamente ansprechen. ⓘ
Prognose
Die Lebenserwartung von Menschen mit Akromegalie hängt davon ab, wie früh die Krankheit erkannt wird. Die Lebenserwartung nach erfolgreicher Behandlung einer frühen Erkrankung entspricht derjenigen der Allgemeinbevölkerung. Die Akromegalie kann oft schon jahrelang vor der Diagnose bestehen, was zu schlechteren Ergebnissen führt, und es wird angenommen, dass die Ergebnisse umso besser sind, je besser das Wachstumshormon kontrolliert wird. Nach einer erfolgreichen chirurgischen Behandlung verschwinden in der Regel die Kopfschmerzen und die visuellen Symptome. Eine Ausnahme ist die Schlafapnoe, die in etwa 70 % der Fälle auftritt, sich aber bei erfolgreicher Behandlung des Wachstumshormonspiegels in der Regel nicht auflöst. Bluthochdruck ist zwar in 40 % der Fälle eine Komplikation, spricht aber in der Regel gut auf die regelmäßige Einnahme von Blutdruckmedikamenten an. Diabetes, der bei Akromegalie auftritt, wird mit den üblichen Medikamenten behandelt, aber eine erfolgreiche Senkung des Wachstumshormonspiegels lindert oft die Symptome des Diabetes. Hypogonadismus ohne Zerstörung der Keimdrüsen ist mit einer Behandlung reversibel. Akromegalie ist mit einem leicht erhöhten Krebsrisiko verbunden. ⓘ
Die Lebenserwartung von Menschen mit Akromegalie ist deutlich eingeschränkt, und die Sterblichkeit im Vergleich zum Durchschnittskollektiv um das Zwei- bis Vierfache erhöht. Dies liegt einerseits an den direkten Manifestationen der Erkrankung, andererseits aber an den Folgeerscheinungen wie begleitendem Bluthochdruck und Zuckerkrankheit, die zu einer erhöhten Rate an Herzkreislauferkrankungen führen. Ob eine verstärkte Bereitschaft zur Entstehung von Krebserkrankungen, namentlich Darmkrebs, besteht, gilt derzeit als umstritten. ⓘ
Bemerkenswerte Menschen
Berühmte Persönlichkeiten mit Akromegalie sind unter anderem:
- Daniel Cajanus (1704-1749), "der finnische Goliath". Sein Porträt in natürlicher Größe und sein Oberschenkelknochen sind noch erhalten. Seine Körpergröße wurde auf 247 cm geschätzt.
- Mary Ann Bevan (1874-1933), eine Engländerin, die, nachdem sie an Akromegalie erkrankt war, als "die hässlichste Frau der Welt" durch die Gegend zog.
- André the Giant (geboren als André Roussimoff, 1946-1993), französischer Profi-Wrestler und Schauspieler
- Salvatore Baccaro (1932-1984), italienischer Charakterdarsteller. Aktiv in B-Movies, Komödien und Horrorfilmen wegen seiner eigenwilligen Gesichtszüge und spontanen Sympathie
- Paul Benedict (1938-2008), amerikanischer Schauspieler. Am bekanntesten für seine Darstellung von Harry Bentley, dem englischen Nachbarn der Jeffersons
- Big Show (geboren als Paul Wight; 1972), amerikanischer Profi-Wrestler und Schauspieler, dem 1991 ein Hypophysentumor entfernt wurde.
- Eddie Carmel, geboren als Oded Ha-Carmeili (1936-1972), in Israel geborener Entertainer mit Gigantismus und Akromegalie, im Volksmund bekannt als "Der jüdische Riese".
- Ted Cassidy (1932-1979), amerikanischer Schauspieler. Am bekanntesten für seine Darstellung des Lurch in der Fernsehsitcom The Addams Family
- Rondo Hatton (1894-1946), amerikanischer Journalist und Schauspieler. Ein Hollywood-Liebling in den B-Movie-Horrorfilmen der 1930er und 1940er Jahre. Hattons Entstellung, die auf Akromegalie zurückzuführen ist, entwickelte sich im Laufe der Zeit, beginnend während seines Dienstes im Ersten Weltkrieg.
- Sultan Kösen, der größte Mann der Welt
- Maximinus Thrax, römischer Kaiser (um 173, regierte 235-238). Beschreibungen und Darstellungen deuten auf Akromegalie hin, aber es wurden noch keine Überreste seines Körpers gefunden.
- The Great Khali (geboren als Dalip Singh Rana), indischer Profi-Wrestler, ist vor allem durch seine Zeit bei der WWE bekannt. Im Jahr 2012 wurde ihm im Alter von 39 Jahren ein Hypophysentumor entfernt.
- Maurice Tillet (1903-1954), russischstämmiger französischer Profi-Wrestler, besser bekannt unter seinem Ringnamen "French Angel".
- Richard Kiel (1939-2014), Schauspieler, "Jaws" aus zwei James-Bond-Filmen und Mr. Larson in Happy Gilmore
- Pío Pico, der letzte mexikanische Gouverneur von Kalifornien (1801-1894), wies mindestens zwischen 1847 und 1858 Akromegalie ohne Gigantismus auf. Einige Zeit nach 1858 verschwanden die Anzeichen des Wachstumshormone produzierenden Tumors zusammen mit allen sekundären Auswirkungen, die der Tumor bei ihm verursacht hatte. In seinen 90er Jahren sah er normal aus. Seine bemerkenswerte Genesung ist wahrscheinlich ein Beispiel für einen spontanen selektiven Hypophysentumor-Apoplex.
- Earl Nightingale (12. März 1921 - 25. März 1989) war ein amerikanischer Radiosprecher und Autor, der sich hauptsächlich mit den Themen menschliche Charakterentwicklung, Motivation und sinnvolle Existenz beschäftigte. In den frühen 1950er Jahren war er die Stimme von Sky King, dem Helden einer Radioabenteuerserie, und von 1950 bis 1956 war er Moderator des WGN-Radioprogramms. Nightingale war der Autor von The Strangest Secret, das der Wirtschaftswissenschaftler Terry Savage als "eines der größten Motivationsbücher aller Zeiten" bezeichnet hat. Nightingales Tochter Pamela erwähnte in einem Podcast über ihren Vater, der im Juni 2022 ausgestrahlt wurde, dass ihr Vater Akromegalie hatte.
- Tony Robbins, Motivationsredner
- Carel Struycken, niederländischer Schauspieler, 2,13 m, bekannt für seine Rolle des Lurch in der Addams-Family-Filmtrilogie, des Riesen in Twin Peaks, des stummen Dieners von Lwaxana Troi, Mr. Homn, in Star Trek: The Next Generation, und des Mondscheinmannes in Geralds Spiel, basierend auf dem Buch von Stephen King.
- Peter Mayhew (1944-2019), britisch-amerikanischer Schauspieler, bei dem im Alter von acht Jahren Gigantismus diagnostiziert wurde. Am bekanntesten ist er für seine Rolle als Chewbacca in der Star-Wars-Filmreihe.
- Irwin Keyes, amerikanischer Schauspieler. Am bekanntesten für seine Rolle als Hugo Mojoloweski, Georges gelegentlicher Leibwächter in der Serie The Jeffersons
- Morteza Mehrzad, iranischer Paralympionike und Medaillengewinner. Mitglied der iranischen Sitzvolleyballmannschaft. Torschützenkönig im Goldmedaillenspiel 2016
- Neil McCarthy, britischer Schauspieler. Bekannt durch Rollen in Zulu, Time Bandits und vielen britischen Fernsehserien
- Nikolai Valuev, russischer Politiker und ehemaliger Profiboxer
- Antônio "Bigfoot" Silva, brasilianischer Kickboxer und Mixed Martial Arts-Kämpfer.
- (Leonel) Edmundo Rivero, argentinischer Tango-Sänger, Komponist und Impresario
Es wurde behauptet, dass Lorenzo de' Medici (1449-92) an Akromegalie gelitten haben könnte. Historische Dokumente und Porträts sowie eine spätere Analyse seines Skeletts stützen diese Spekulation. Bei dem Pianisten und Komponisten Sergej Rachmaninow, der für seine sehr großen Hände bekannt ist, wurde zu Lebzeiten nie eine Akromegalie diagnostiziert, aber ein medizinischer Artikel aus dem Jahr 2006 legt nahe, dass er sie gehabt haben könnte. ⓘ
Die Bogdanoff-Zwillinge wiesen einige Anzeichen von Akromegalie auf, und ihr ständiges Leugnen, dass sie sich einer plastischen Operation unterzogen hatten, die ihr Gesicht stark veränderte, veranlasste einige, diese Krankheit in Betracht zu ziehen. Die Akromegalie wurde jedoch vor ihrem Tod nicht nachgewiesen. ⓘ
Symptome
Die Symptomatik der Akromegalie wird davon geprägt, ob die Erkrankung in der Zeit vor oder nach dem Schluss der Epiphysenfugen eintritt, d. h. vor oder nach der Pubertät: Vor Abschluss des Längenwachstums kommt es zum sogenannten Gigantismus oder hypophysären Riesenwuchs. Die normalen Körperproportionen bleiben weitgehend erhalten, d. h. der Mensch wächst dann auch weiterhin in die Länge. ⓘ
Nach Verschluss der Epiphysenfugen ist ein Wachstum nur noch an den knöchernen Akren, Weichteilen wie dem Kehlkopf und inneren Organen möglich. Die Organe vergrößern sich insgesamt, Viszeromegalie genannt. Ein Beispiel hierfür stellt der Kropf dar. Die Haut gewinnt an Dicke, und der Haarwuchs wird angeregt. Unkoordinierter Überschuss der Gelenkknorpel prädisponiert zu degenerativen Gelenkerkrankungen. Die Körperproportionen wirken durch dieses Wachstum insgesamt unharmonisch und vergröbert. ⓘ
Weitere Symptome entstehen durch eine Zuckerkrankheit oder zumindest verminderte Glukosetoleranz. Als belastend mag sich das allmähliche Nachlassen der Fähigkeit zu einem aktiven Sexualleben erweisen, hervorgerufen durch eine Erektionsschwäche, abgemildert durch ein gleichzeitiges Desinteresse daran. Bei Frauen kommt es selten zu einer sekundären Amenorrhoe, also einem Ausbleiben der Regelblutung, bei gleichzeitig scheinbar unmotivierter eigener Milchproduktion, sogenanntes Galaktorrhö-Amenorrhö-Syndrom. 30 % der Patienten messen dauerhaft einen erhöhten Blutdruck. ⓘ
Die Patienten klagen häufig über Kopfschmerzen und allgemeine Abgeschlagenheit sowie Knochenschmerzen. Eine vermehrte Neigung zum Schwitzen ist nicht selten. Taubheitsgefühl oder Kribbeln in den Händen weisen auf ein Karpaltunnelsyndrom hin. Bei bis zu 64 % der Patienten mit Akromegalie findet man eine beidseitige Manifestation, die in der Regel nach Behandlung der Akromegalie verschwindet. ⓘ
Mehr als 90 % der Patienten haben ein Schlaf-Apnoe-Syndrom mit Schnarchen, nächtlichen Atemstillständen, kaum erholsamem Nachtschlaf und infolgedessen Tagesmüdigkeit und Konzentrationsstörungen. Den Betroffenen fällt die langsame Umgestaltung ihrer Physiognomie selten selbst auf, aufschlussreich kann aber der Vergleich mit alten Fotografien sein; ein anderer Hinweis ist eine Zunahme der Hut- oder Schuhgrößen im Erwachsenenalter. ⓘ
Kieferorthopädische Konsultationen wegen einer zunehmenden Fehlstellung des Gebisses (etwa durch einen im Vergleich zum Oberkiefer vergrößerten Unterkiefer, Progenie) sind nicht selten. ⓘ
Kommt es durch das Wachstum des Hypophysentumors infolge lokaler Druckwirkungen zu Gesichtsfeldausfällen oder anderen Hirnnervenausfällen, ist erkennbar das Stadium ernsthafter Komplikationen erreicht. ⓘ
Therapie
Die Therapie der Wahl besteht in der chirurgischen Entfernung des Tumors der Hirnanhangdrüse bzw. eines Teils der Hypophyse. Für die Operation stehen ein transsphenoidaler (durch die Nase und Teile der Nasennebenhöhlen) und ein transkranieller Zugang (durch die Schädeldecke) zur Verfügung. Die operative Therapie wird nur an Zentren für Neurochirurgie angeboten, bei der transspenoidalen Resektion sind unterschiedliche Verfahren der optischen Führung möglich. ⓘ
Nach unvollständiger Resektion des hormonproduzierenden Tumors wird eine zusätzliche medikamentöse Behandlung erforderlich. Mehrere Wirkstoffgruppen stehen für die medikamentöse Behandlung zur Verfügung: die Dopaminagonisten Cabergolin (Cabaseril®) und Bromocriptin (Pravidel®), die Somatostatinanaloga Octreotid (Sandostatin®), Lanreotid (Somatuline Autogel®) und Pasireotid (Signifor®) sowie der Wachstumshormonantagonist Pegvisomant (Somavert®). Gegebenenfalls kann bei einem großen Tumor eine medikamentöse Therapie vor einer chirurgischen Entfernung angewendet werden. Das Ziel einer Vorbehandlung mit den genannten Medikamenten ist, den Tumor zu verkleinern und den Allgemeinzustand der Patienten zu verbessern. ⓘ
Nach operativer Beseitigung des hormonproduzierenden Gewebes ist eine regelmäßige Kontrolle des Hormonstatus im Labor sinnvoll, um ggf. weiterhin aktives Gewebe an seiner endokrinen Aktivität identifizieren zu können. ⓘ
Die allein medikamentöse Behandlung sollte nur einer kleinen Gruppe von Patienten vorbehalten bleiben. ⓘ
Bei großen nichtoperierbaren Hormontumoren oder zur Behandlung von Resttumoren nach Operation werden auch unterschiedliche Methoden der Bestrahlungstherapie (insbesondere mit Röntgenstrahlen) mit Erfolg eingesetzt. ⓘ