Penicilline
 Penicillin-Kernstruktur, wobei "R" die variable Gruppe ist | |
| Klinische Daten | |
|---|---|
| AHFS/Drugs.com | Micromedex Ausführliche Verbraucherinformationen |
| Wege der Verabreichung | Intravenös, intramuskulär, durch den Mund |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Pharmakokinetische Daten | |
| Stoffwechsel | Leber |
| Eliminationshalbwertszeit | Zwischen 0,5 und 56 Stunden |
| Ausscheidung | Nieren |
Penicilline (P, PCN oder PEN) sind eine Gruppe von Antibiotika, die ursprünglich aus Penicillium-Schimmelpilzen, vor allem P. chrysogenum und P. rubens, gewonnen werden. Die meisten Penicilline, die in der Klinik verwendet werden, werden von P. chrysogenum durch Tiefenfermentation synthetisiert und anschließend gereinigt. Es wurde eine Reihe natürlicher Penicilline entdeckt, aber nur zwei gereinigte Verbindungen werden klinisch verwendet: Penicillin G (intramuskuläre oder intravenöse Anwendung) und Penicillin V (Verabreichung durch den Mund). Penicilline gehörten zu den ersten Medikamenten, die gegen viele bakterielle Infektionen, die durch Staphylokokken und Streptokokken verursacht werden, wirksam waren. Sie gehören zu den β-Laktam-Antibiotika. Sie werden auch heute noch häufig gegen verschiedene bakterielle Infektionen eingesetzt, obwohl viele Bakterienarten nach ausgiebiger Anwendung Resistenzen entwickelt haben. ⓘ
Etwa 10 % der Menschen geben an, allergisch auf Penicillin zu reagieren; bis zu 90 % dieser Gruppe sind jedoch möglicherweise gar nicht allergisch. Schwere Allergien treten nur bei etwa 0,03 % auf. Die Forschung unterstreicht, wie wichtig es ist, dass sowohl Ärzte als auch Patienten über festgestellte Penicillinallergien sprechen. Diejenigen, die auf Penicillin allergisch reagieren, erhalten am häufigsten Cephalosporin C (ein anderes β-Lactam-Antibiotikum), da es nur 10 % Kreuzallergien zwischen Penicillinen und Cephalosporinen gibt. ⓘ
Penicillin wurde 1928 vom schottischen Wissenschaftler Alexander Fleming als Rohextrakt von P. rubens entdeckt. Flemings Schüler Cecil George Paine war der erste, der 1930 Penicillin erfolgreich zur Behandlung einer Augeninfektion (Ophthalmia neonatorum) einsetzte. Die gereinigte Verbindung (Penicillin F) wurde 1940 von einem Forschungsteam unter der Leitung von Howard Florey und Ernst Boris Chain an der Universität Oxford isoliert. Fleming verwendete das gereinigte Penicillin erstmals 1942 zur Behandlung von Streptokokken-Meningitis. Für diese Entdeckung erhielt Fleming 1945 gemeinsam mit Florey und Chain den Nobelpreis für Physiologie oder Medizin. ⓘ
Mehrere halbsynthetische Penicilline sind gegen ein breiteres Spektrum von Bakterien wirksam: Dazu gehören die Antistaphylokokken-Penicilline, die Aminopenicilline und die Antipseudomonaden-Penicilline. ⓘ
Die Penicilline oder Penizilline (Singular Penicillin, von lateinisch penicillium, ‚Pinselschimmel‘) sind eine Gruppe von antibiotisch wirksamen Substanzen, die sich strukturell von der 6-Aminopenicillansäure ableiten. Neben natürlich vorkommenden Penicillinen, die als sekundäre Stoffwechselprodukte von verschiedenen Penicillium-, Aspergillus-, Trichophyton- und Streptomyces-Arten gebildet werden, zählt man dazu auch biosynthetisch und teilsynthetisch hergestellte Penicilline. Das zuerst entdeckte natürlich vorkommende Penicillin wurde aus der Pinselschimmelart Penicillium notatum isoliert. ⓘ
Penicilline gehören zur Gruppe der β-Lactam-Antibiotika. Die Summenformel lautet R-C9H11N2O4S, wobei „R“ für eine variable Seitenkette steht. ⓘ
Nomenklatur
Der Begriff "Penicillin" ist definiert als ein natürliches Produkt des Schimmelpilzes Penicillium mit antimikrobieller Wirkung. Er wurde von Alexander Fleming am 7. März 1929 geprägt, als er die antibakterielle Eigenschaft von Penicillium rubens entdeckte. Fleming erklärte in seinem 1929 im British Journal of Experimental Pathology erschienenen Aufsatz, dass "um die Wiederholung des eher umständlichen Ausdrucks 'Schimmelpilzbrühefiltrat' zu vermeiden, der Name 'Penicillin' verwendet wird". Der Name bezieht sich also auf den wissenschaftlichen Namen des Schimmelpilzes, wie er von Fleming in seiner Nobelvorlesung im Jahr 1945 beschrieben wurde:
"Ich bin oft gefragt worden, warum ich den Namen 'Penicillin' erfunden habe. Ich bin einfach der Orthodoxie gefolgt und habe ein Wort geprägt, das erklärt, dass die Substanz Penicillin von einer Pflanze der Gattung Penicillium stammt, so wie vor vielen Jahren das Wort "Digitalin" für eine Substanz erfunden wurde, die von der Pflanze Digitalis stammt.
Im modernen Sprachgebrauch wird der Begriff Penicillin im weiteren Sinne für jedes antimikrobielle β-Lactam verwendet, das einen mit dem β-Lactamkern verschmolzenen Thiazolidinring enthält und ein Naturprodukt sein kann oder nicht. Wie die meisten Naturprodukte liegt Penicillin in Penicillium-Schimmelpilzen als eine Mischung aktiver Bestandteile vor (Gentamicin ist ein weiteres Beispiel für ein Naturprodukt, das eine undefinierte Mischung aktiver Komponenten ist). Die wichtigsten aktiven Bestandteile von Penicillium sind in der folgenden Tabelle aufgeführt:
| Chemische Bezeichnung | Britische Nomenklatur | US-Nomenklatur | Potenz im Verhältnis zu Penicillin G ⓘ |
|---|---|---|---|
| 2-Pentenylpenicillin | Penizillin I | Penicillin F | 70–82% |
| Benzylpenicillin | Penizillin II | Penicillin G | 100% |
| p-Hydroxybenzylpenicillin | Penizillin III | Penicillin X | 130–140% |
| n-Heptylpenicillin | Penizillin IV | Penicillin K | 110–120% |
Weitere weniger aktive Bestandteile von Penicillium sind Penicillin O, Penicillin U1 und Penicillin U6. Andere benannte Bestandteile von natürlichem Penicillium, wie Penicillin A, erwiesen sich später als nicht antibiotisch wirksam und sind chemisch nicht mit den antibiotischen Penicillinen verwandt. ⓘ
Die genaue Zusammensetzung des extrahierten Penicillins hängt von der Art des verwendeten Penicillium-Schimmels und vom Nährmedium ab, das für die Kultur des Schimmels verwendet wird. Flemings ursprünglicher Stamm von Penicillium rubens produziert vor allem das nach Fleming benannte Penicillin F. Penicillin F ist jedoch instabil, schwer zu isolieren und wird vom Schimmelpilz nur in geringen Mengen produziert. ⓘ
Der wichtigste handelsübliche Stamm von Penicillium chrysogenum (der Peoria-Stamm) produziert Penicillin G als Hauptkomponente, wenn Maisquellwasser als Kulturmedium verwendet wird. Wenn dem Nährmedium Phenoxyethanol oder Phenoxyessigsäure zugesetzt wird, produziert der Schimmelpilz stattdessen Penicillin V als Hauptpenicillin. ⓘ
6-Aminopenicillansäure (6-APA) ist eine von Penicillin G abgeleitete Verbindung. 6-APA enthält den Beta-Lactam-Kern von Penicillin G, wobei jedoch die Seitenketten entfernt wurden; 6-APA ist ein nützliches Vorprodukt für die Herstellung anderer Penicilline. Es gibt viele halbsynthetische Penicilline, die von 6-APA abgeleitet sind, und diese lassen sich in drei Gruppen einteilen: Antistaphylococcen-Penicilline, Breitspektrum-Penicilline und antipseudomonale Penicilline. Die halbsynthetischen Penicilline werden alle als Penicilline bezeichnet, da sie sich letztlich alle von Penicillin G ableiten. ⓘ
Penicillin-Einheiten
- Eine Einheit Penicillin G-Natrium ist definiert als 0,600 Mikrogramm. Daher entsprechen 2 Millionen Einheiten (2 Megaeinheiten) Penicillin G 1,2 g.
- Eine Einheit Penicillin V Kalium ist definiert als 0,625 Mikrogramm. Daher entsprechen 400.000 Einheiten Penicillin V 250 mg. ⓘ
Die Verwendung von Einheiten für die Verschreibung von Penicillin ist ein historischer Zufall und außerhalb der USA weitgehend überholt. Da das ursprüngliche Penicillin eine undefinierte Mischung von Wirkstoffen war (ein amorphes gelbes Pulver), schwankte die Potenz jeder Charge von Penicillin von Charge zu Charge. Es war daher nicht möglich, 1 g Penicillin zu verschreiben, da sich die Aktivität von 1 g Penicillin einer Charge von der Aktivität einer anderen Charge unterschied. Nach der Herstellung musste jede Charge Penicillin mit einer bekannten Penicillineinheit standardisiert werden: Jedes Glasfläschchen wurde dann mit der erforderlichen Anzahl von Einheiten gefüllt. In den 1940er Jahren war ein Fläschchen mit 5.000 Oxford-Einheiten Standard, konnte aber je nach Charge zwischen 15 mg und 20 mg Penicillin enthalten. Später wurde ein Fläschchen mit 1.000.000 internationalen Einheiten zum Standard, das 2,5 g bis 3 g natürliches Penicillin (eine Mischung aus Penicillin I, II, III und IV und natürlichen Verunreinigungen) enthalten konnte. Mit dem Aufkommen reiner Penicillin-G-Präparate (ein weißes, kristallines Pulver) gibt es kaum noch einen Grund, Penicillin in Einheiten zu verschreiben. ⓘ
Für die "Einheit" von Penicillin gab es bisher drei Definitionen, und jede Definition wurde so gewählt, dass sie der vorhergehenden ungefähr gleichwertig war.
- Oxford- oder Florey-Einheit (1941). Ursprünglich war dies definiert als die Mindestmenge an Penicillin, die in 50 ml Fleischextrakt gelöst ist und das Wachstum eines Standardstammes von Staphylococcus aureus (dem Oxford-Staphylococcus) hemmt. Als Referenzstandard diente eine große Charge unreinen Penicillins, die in Oxford aufbewahrt wurde. Der Test wurde später von Floreys Gruppe zu einem besser reproduzierbaren "Bechertest" modifiziert: Bei diesem Test wurde eine Penicillinlösung als eine Einheit/ml Penicillin enthaltend definiert, wenn 339 Mikroliter der Lösung in einem "Becher" auf einer Platte mit festem Agar eine 24 Millimeter große Hemmzone für das Wachstum von Oxford-Staphylococcus erzeugten.
- Erste internationale Norm (1944). Eine einzige 8-Gramm-Charge reinen kristallinen Penicillin-G-Natriums wurde im National Institute for Medical Research in Mill Hill in London gelagert (die internationale Norm). Eine Penicillineinheit wurde mit 0,6 Mikrogramm des internationalen Standards definiert. Es wurde auch ein unreiner "Arbeitsstandard" definiert, der in viel größeren Mengen auf der ganzen Welt verteilt wurde: Eine Einheit des Arbeitsstandards entsprach 2,7 Mikrogramm (die Menge pro Einheit war aufgrund der Verunreinigungen viel größer). Gleichzeitig wurde der Bechertest verfeinert, bei dem statt eines Zonendurchmessers von 24 mm die Zonengröße gegen eine Referenzkurve aufgetragen wurde, um eine Aussage über die Potenz zu treffen.
- Zweiter internationaler Standard (1953). Es wurde eine einzige Charge von 30 Gramm reinem kristallinem Penicillin G-Natrium gewonnen, die ebenfalls in Mill Hill gelagert wurde. Eine Penicillineinheit wurde als 0,5988 Mikrogramm des Zweiten Internationalen Standards definiert. ⓘ
Es gibt eine ältere Einheit für Penicillin V, die nicht mit der aktuellen Penicillin V-Einheit übereinstimmt. Der Grund dafür ist, dass die US-amerikanische FDA fälschlicherweise davon ausging, dass die Potenz von Penicillin V die gleiche ist wie die von Penicillin G. Tatsächlich ist Penicillin V weniger stark als Penicillin G, und die aktuelle Penicillin V-Einheit spiegelt diese Tatsache wider.
- Erste internationale Einheit von Penicillin V (1959). Eine Einheit Penicillin V wurde als 0,590 Mikrogramm eines in Mill Hill in London aufbewahrten Referenzstandards definiert. Diese Einheit ist inzwischen überholt. ⓘ
Ein ähnlicher Standard wurde auch für Penicillin K festgelegt. ⓘ
Arten
Natürliche Penicilline
Penicillin G (Benzylpenicillin) wurde erstmals aus einem in der Natur vorkommenden Penicillium-Pilz hergestellt. Der heute für die Herstellung von Penicillin G verwendete Pilzstamm wurde durch gentechnische Eingriffe geschaffen, um die Ausbeute im Herstellungsprozess zu verbessern. Keines der anderen natürlichen Penicilline (F, K, N, X, O, U1 oder U6) wird derzeit klinisch eingesetzt. ⓘ
Halbsynthetisches Penicillin
Penicillin V (Phenoxymethylpenicillin) wird hergestellt, indem die Vorstufe Phenoxyessigsäure dem Medium zugesetzt wird, in dem ein genetisch veränderter Stamm des Penicillium-Pilzes kultiviert wird. ⓘ
Aus 6-APA hergestellte Antibiotika
Es gibt drei große Gruppen von anderen halbsynthetischen Antibiotika, die mit den Penicillinen verwandt sind. Sie werden durch Anhängen verschiedener Seitenketten an die aus Penicillin G isolierte Vorstufe 6-APA synthetisiert. Es handelt sich dabei um Antistaphylococcus-Antibiotika, Breitband-Antibiotika und antipseudomonische Antibiotika. ⓘ
Antistaphylococcus-Antibiotika
- Cloxacillin, Dicloxacillin, Flucloxacillin, Methicillin, Oxacillin
Durch Abschirmung des Betalactamringes mit Isoxazolylstrukturen gegenüber der von manchen Erregern gebildeten Penicillinase sind solche Penicilline auch wirksam gegen penicillinasebildende Staphylokokken („Staphylokokken-Penicillin“). Im Vergleich zu Penicillin G ist ihre Wirkstärke deutlich geringer und gegenüber gramnegativen Erregern sind Isoxazolylpenicilline gänzlich wirkungslos. ⓘ
- Cloxacillin (durch den Mund oder durch Injektion)
- Dicloxacillin (durch den Mund oder durch Injektion)
- Flucloxacillin (durch den Mund oder durch Injektion)
- Methicillin (nur Injektion)
- Nafcillin (nur Injektion)
- Oxacillin (durch den Mund oder durch Injektion)
Antistaphylococcal-Antibiotika werden so genannt, weil sie gegen den Abbau durch Staphylokokken-Penicillinase resistent sind. Sie werden daher auch als penicillinase-resistent bezeichnet. ⓘ
Breitspektrum-Antibiotika
Diese Gruppe von Antibiotika wird als Breitspektrum-Antibiotika bezeichnet, weil sie gegen ein breites Spektrum gramnegativer Bakterien wie Escherichia coli und Salmonella typhi wirksam sind, für die Penicillin nicht geeignet ist. Allerdings sind Resistenzen bei diesen Organismen inzwischen weit verbreitet.
- Ampicillin
- Amoxicillin ⓘ
Es gibt viele Vorstufen von Ampicillin. Dabei handelt es sich um inaktive Verbindungen, die im Darm abgebaut werden, um Ampicillin freizusetzen. Keine dieser Vorstufen von Ampicillin wird derzeit verwendet:
- Pivampicillin (Pivaloyloxymethylester von Ampicillin)
- Bacampicillin
- Metampicillin (Formaldehyd-Ester von Ampicillin)
- Talampicillin
- Hetacillin (Ampicillin, konjugiert mit Aceton) ⓘ
Epicillin ist ein Aminopenicillin, das nie in großem Umfang klinisch eingesetzt wurde. ⓘ
Antipseudomonische Antibiotika
Die gramnegative Art Pseudomonas aeruginosa ist von Natur aus gegen viele Antibiotikaklassen resistent. In den 1960er und 1970er Jahren wurden zahlreiche Anstrengungen unternommen, um Antibiotika zu entwickeln, die gegen Pseudomonas-Arten wirksam sind. Innerhalb dieser Gruppe gibt es zwei chemische Klassen: Carboxypenicilline und Ureidopenicilline. Alle werden durch Injektion verabreicht, keines kann durch den Mund eingenommen werden. ⓘ
Carboxypenicilline
- Carbenicillin
- Ticarcillin
- Temocillin ⓘ
Ureidopenicilline
- Mezlocillin
- Piperacillin
- Azlocillin ⓘ
β-Laktamase-Hemmer
- Clavulansäure
- Sulbactam
- Tazobactam ⓘ
Medizinische Verwendung
Der Begriff "Penicillin" kann sich, wenn er allein verwendet wird, auf eine der beiden chemischen Verbindungen Penicillin G oder Penicillin V beziehen. ⓘ
| Gebräuchlicher Name | Chemische Bezeichnung | Methode von Verabreichung ⓘ |
|---|---|---|
| Penicillin V | Phenoxymethylpenicillin | oral |
| Penicillin G | Benzylpenicillin | intravenös intramuskulär |
Penicillin G
Penicillin G wird durch die Magensäure zerstört und kann daher nicht über den Mund eingenommen werden, aber es können Dosen von bis zu 2,4 g verabreicht werden (viel höher als Penicillin V). Es wird als intravenöse oder intramuskuläre Injektion verabreicht. Es kann als unlösliches Salz formuliert werden, und es gibt zwei solche Formulierungen, die derzeit verwendet werden: Procain-Penicillin und Benzathin-Benzylpenicillin, die nur bei der Behandlung von Syphilis eingesetzt werden. Wenn eine hohe Konzentration im Blut aufrechterhalten werden soll, muss Penicillin G in relativ kurzen Abständen verabreicht werden, da es über die Niere recht schnell aus dem Blutkreislauf ausgeschieden wird. ⓘ
Penicillin G ist für die Behandlung von Septikämie, Empyem, Lungenentzündung, Perikarditis, Endokarditis und Meningitis zugelassen, die durch empfindliche Stämme von Staphylokokken und Streptokokken verursacht werden. Es ist auch zur Behandlung von Milzbrand, Aktinomykose, Erkrankungen des Halses und des Gesichts, des Brustkorbs und der Bauchhöhle, Clostridieninfektionen, Botulismus, Gasgangrän (mit begleitendem Débridement und/oder chirurgischen Eingriffen je nach Indikation), Tetanus (als Zusatztherapie zu humanem Tetanus-Immunglobulin) zugelassen, Diphtherie (als Zusatztherapie zu Antitoxin und zur Vorbeugung des Trägerstatus), Erysipelothrix-Endokarditis, Fusospirochetose (schwere Infektionen des Oropharynx, der unteren Atemwege und des Genitalbereichs), Listerien-Infektionen, Meningitis, Endokarditis, Pasteurella-Infektionen einschließlich Bakteriämie und Meningitis, Haverhill-Fieber; Rattenbiss-Fieber und disseminierte Gonokokken-Infektionen, Meningokokken-Meningitis und/oder Septikämie, verursacht durch Penicillin-empfängliche Organismen, sowie Syphilis. ⓘ
Penicillin V
Penicillin V kann durch den Mund eingenommen werden, da es relativ resistent gegen Magensäure ist. Höhere Dosen als 500 mg sind wegen der schlechten Resorption nicht voll wirksam. Es wird bei denselben bakteriellen Infektionen eingesetzt wie Penicillin G und ist die am häufigsten verwendete Form von Penicillin. Es wird jedoch nicht bei Krankheiten wie Endokarditis eingesetzt, bei denen hohe Blutspiegel von Penicillin erforderlich sind. ⓘ
Bakterielle Anfälligkeit
Da Penicillin-Resistenzen inzwischen so weit verbreitet sind, werden heute bevorzugt andere Antibiotika zur Behandlung eingesetzt. So war Penicillin früher das Mittel der ersten Wahl bei Infektionen mit Neisseria gonorrhoeae und Neisseria meningitidis, wird aber nicht mehr für die Behandlung dieser Infektionen empfohlen. ⓘ
| Bakterium | Empfindlich (S) | Mittelmäßig (I) | Resistent (R) ⓘ |
|---|---|---|---|
| Staphylococcus aureus | ≤0,12 mcg/ml | - | ≥0,25 mcg/ml |
| Streptokokkus pneumoniae Meningitis | ≤0,06 mcg/ml | - | ≥0,12 mcg/ml |
| Streptokokkus pneumoniae (nicht Meningitis) | ≤2 mcg/ml | ≥8 mcg/ml | |
| Streptokokkus Viridans-Gruppe | 0,12 mcg/ml | 0,25-2 mcg/ml | 4 mcg/ml |
| Listeria monocytogenes | ≤2 mcg/ml | - | - |
| Bacillus anthracis | ≤0,12 mcg/ml | - | ≥0,25 mcg/ml |
Unerwünschte Wirkungen
Zu den häufigen (≥ 1 % der Patienten) unerwünschten Arzneimittelwirkungen im Zusammenhang mit der Anwendung von Penicillinen gehören Durchfall, Überempfindlichkeit, Übelkeit, Hautausschlag, Neurotoxizität, Urtikaria und Superinfektion (einschließlich Candidiasis). Zu den seltenen unerwünschten Wirkungen (0,1-1 % der Menschen) gehören Fieber, Erbrechen, Erythem, Dermatitis, Angioödem, Krampfanfälle (insbesondere bei Menschen mit Epilepsie) und pseudomembranöse Kolitis. Penicillin kann bei einigen Personen auch die Serumkrankheit oder eine serumkrankheitsähnliche Reaktion auslösen. Die Serumkrankheit ist eine Überempfindlichkeitsreaktion vom Typ III, die ein bis drei Wochen nach der Einnahme von Arzneimitteln, einschließlich Penicillin, auftritt. Es handelt sich nicht um eine echte Arzneimittelallergie, da Allergien Überempfindlichkeitsreaktionen vom Typ I sind, aber eine wiederholte Exposition gegenüber dem schädigenden Wirkstoff kann zu einer anaphylaktischen Reaktion führen. Die Allergie tritt bei 1-10 % der Menschen auf und äußert sich durch einen Hautausschlag nach der Exposition. Eine IgE-vermittelte Anaphylaxie tritt bei etwa 0,01 % der Patienten auf. ⓘ
Schmerzen und Entzündungen an der Injektionsstelle sind auch bei parenteral verabreichtem Benzathin-Benzylpenicillin, Benzylpenicillin und, in geringerem Maße, Procain-Benzylpenicillin häufig. Dieser Zustand ist als Livedoid-Dermatitis oder Nicolau-Syndrom bekannt. ⓘ
Struktur
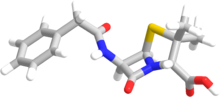
Der Begriff "Penam" wird verwendet, um das gemeinsame Kerngerüst eines Mitglieds der Penicilline zu beschreiben. Dieser Kern hat die Molekularformel R-C9H11N2O4S, wobei R die variable Seitenkette ist, die die Penicilline voneinander unterscheidet. Der Penam-Kern hat eine molare Masse von 243 g/mol, wobei größere Penicilline eine molare Masse von fast 450 haben - Cloxacillin hat beispielsweise eine molare Masse von 436 g/mol. 6-APA (C8H12N2O3S) bildet die Grundstruktur der Penicilline. Es besteht aus einem geschlossenen Dipeptid, das durch die Kondensation von L-Cystein und D-Valin gebildet wird. Dies führt zur Bildung von β-Lactam- und Thiazolidinringen. ⓘ
Das wichtigste Strukturmerkmal der Penicilline ist der viergliedrige β-Lactamring; diese Struktureinheit ist für die antibakterielle Wirkung des Penicillins wesentlich. Der β-Lactamring selbst ist mit einem fünfgliedrigen Thiazolidinring verschmolzen. Die Verschmelzung dieser beiden Ringe bewirkt, dass der β-Lactamring reaktiver ist als monozyklische β-Lactame, da die beiden verschmolzenen Ringe die β-Lactam-Amidbindung verzerren und somit die Resonanzstabilisierung aufheben, die normalerweise in diesen chemischen Bindungen zu finden ist. Eine Acyl-Seitenkette, die an den β-Lactamring gebunden ist. ⓘ
Eine Vielzahl von β-Lactam-Antibiotika wurde durch chemische Modifikation der 6-APA-Struktur während der Synthese hergestellt, insbesondere durch chemische Substitutionen in der Acyl-Seitenkette. Das erste chemisch veränderte Penicillin, Methicillin, hatte zum Beispiel Substitutionen durch Methoxygruppen an den Positionen 2' und 6' des 6-APA-Benzolrings von Penicillin G. Dieser Unterschied macht Methicillin resistent gegen die Aktivität von β-Lactamase, einem Enzym, durch das viele Bakterien von Natur aus unempfindlich gegen Penicilline sind. ⓘ
Pharmakologie

Eintritt in die Bakterien
Penicillin kann bei Gram-positiven Arten leicht in die Bakterienzelle eindringen. Das liegt daran, dass grampositive Bakterien keine äußere Zellmembran haben und einfach von einer dicken Zellwand umgeben sind. Die Penicillinmoleküle sind klein genug, um durch die Zwischenräume der Glykoproteine in der Zellwand zu gelangen. Aus diesem Grund sind Gram-positive Bakterien sehr empfindlich gegenüber Penicillin (wie die Entdeckung des Penicillins im Jahr 1928 erstmals zeigte). ⓘ
Penicillin oder jedes andere Molekül dringt in gramnegative Bakterien auf andere Weise ein. Diese Bakterien haben dünnere Zellwände, aber die äußere Oberfläche ist mit einer zusätzlichen Zellmembran, der so genannten äußeren Membran, überzogen. Die äußere Membran besteht aus einer Lipidschicht (Lipopolysaccharidkette), die den Durchgang wasserlöslicher (hydrophiler) Moleküle wie Penicillin blockiert. Dies ist der Grund für die relative Resistenz gegenüber Antibiotika im Vergleich zu Gram-positiven Arten. Penicillin kann jedoch immer noch in Gram-negative Arten eindringen, indem es durch wässrige Kanäle diffundiert, die Porine (Proteine der äußeren Membran) genannt werden, die zwischen den Fettmolekülen verteilt sind und Nährstoffe und Antibiotika in die Bakterien transportieren können. Die Porine sind groß genug, um die Diffusion der meisten Penicilline zu ermöglichen, aber die Diffusionsgeschwindigkeit durch sie wird durch die spezifische Größe der Arzneimittelmoleküle bestimmt. Penicillin G beispielsweise ist groß und dringt nur langsam durch die Porine ein, während kleineres Ampicillin und Amoxicillin viel schneller diffundieren. Im Gegensatz dazu kann das große Vancomycin die Porine nicht passieren und ist daher für gramnegative Bakterien unwirksam. Die Größe und Anzahl der Porine ist bei den verschiedenen Bakterien unterschiedlich. Infolge dieser beiden Faktoren - Größe des Penicillins und Porin - können gramnegative Bakterien unempfindlich sein oder einen unterschiedlichen Grad an Empfindlichkeit gegenüber einem bestimmten Penicillin aufweisen. ⓘ
Mechanismus der Wirkung


Die chemische Struktur von Penicillin wird durch einen sehr präzisen, pH-abhängigen Wirkmechanismus ausgelöst, der durch eine einzigartige räumliche Anordnung von Molekülkomponenten beeinflusst wird, die durch Protonierung aktiviert werden können. Es kann durch Körperflüssigkeiten wandern und Enzyme, die für die Zellwandsynthese in gram-positiven Bakterien verantwortlich sind, anvisieren und inaktivieren, während es gleichzeitig die umgebenden Nicht-Ziele vermeidet. Penicillin kann sich in seiner anionischen Form vor der spontanen Hydrolyse im Körper schützen und gleichzeitig sein Potenzial als starker Acylierer bewahren, der erst bei Annäherung an das Zielenzym Transpeptidase aktiviert und im aktiven Zentrum protoniert wird. Diese gezielte Protonierung neutralisiert den Carbonsäurerest, wodurch die N-C(=O)-Bindung des β-Lactamrings geschwächt wird, was zu einer Selbstaktivierung führt. Spezifische strukturelle Anforderungen sind gleichzusetzen mit der Konstruktion der perfekten Mausefalle für den Fang der gewünschten Beute. ⓘ
Penicillin tötet Bakterien ab, indem es den Abschluss der Synthese von Peptidoglykanen, dem Strukturbestandteil der bakteriellen Zellwand, hemmt. Es hemmt speziell die Aktivität von Enzymen, die für die Vernetzung von Peptidoglykanen während des letzten Schritts der Zellwandbiosynthese erforderlich sind. Dies geschieht durch Bindung an Penicillin-bindende Proteine mit dem β-Lactamring, einer Struktur, die auf Penicillinmolekülen zu finden ist. Dadurch wird die Zellwand durch weniger Querverbindungen geschwächt und Wasser strömt unkontrolliert in die Zelle, weil sie den korrekten osmotischen Gradienten nicht aufrechterhalten kann. Dies führt zur Zelllyse und zum Tod. ⓘ
Bakterien bauen ihre Peptidoglykan-Zellwände ständig um, indem sie während ihres Wachstums und ihrer Teilung gleichzeitig Teile der Zellwand aufbauen und abbauen. In den letzten Stadien der Peptidoglykanbiosynthese wird das Uridindiphosphat-N-Acetylmuraminsäure-Pentapeptid (UDP-MurNAc) gebildet, bei dem die vierte und fünfte Aminosäure beide D-Alanyl-D-Alanin sind. Die Übertragung von D-Alanin erfolgt (katalysiert) durch das Enzym DD-Transpeptidase (Penicillin-bindende Proteine sind ein solcher Typ). Die strukturelle Integrität der bakteriellen Zellwand hängt von der Vernetzung von UDP-MurNAc und N-Acetylglucosamin ab. Penicillin und andere β-Lactam-Antibiotika wirken aufgrund von Konformationsähnlichkeiten als Analogon von D-Alanin-D-Alanin (dem Dipeptid) in UDP-MurNAc. Die DD-Transpeptidase bindet dann den viergliedrigen β-Lactamring von Penicillin anstelle von UDP-MurNAc. Infolgedessen wird die DD-Transpeptidase inaktiviert, die Bildung von Querverbindungen zwischen UDP-MurNAc und N-Acetylglucosamin wird blockiert, so dass ein Ungleichgewicht zwischen Zellwandproduktion und -abbau entsteht, wodurch die Zelle schnell abstirbt. ⓘ
Die Enzyme, die die Peptidoglykan-Vernetzungen hydrolysieren, funktionieren weiter, während die Enzyme, die solche Vernetzungen bilden, nicht funktionieren. Dadurch wird die Zellwand des Bakteriums geschwächt, und der osmotische Druck wird zunehmend unkompensiert, was schließlich zum Zelltod (Zytolyse) führt. Darüber hinaus löst die Anhäufung von Peptidoglykanvorläufern die Aktivierung von bakteriellen Zellwandhydrolasen und Autolysinen aus, die die Peptidoglykane der Zellwand weiter verdauen. Die geringe Größe der Penicilline erhöht ihre Wirksamkeit, da sie die gesamte Tiefe der Zellwand durchdringen können. Dies steht im Gegensatz zu den Glykopeptid-Antibiotika Vancomycin und Teicoplanin, die beide viel größer sind als die Penicilline. ⓘ
Gram-positive Bakterien werden als Protoplasten bezeichnet, wenn sie ihre Zellwände verlieren. Gramnegative Bakterien verlieren ihre Zellwände nicht vollständig und werden nach der Behandlung mit Penicillin als Sphäroplasten bezeichnet. ⓘ
Penicillin zeigt eine synergistische Wirkung mit Aminoglykosiden, da die Hemmung der Peptidoglykansynthese es den Aminoglykosiden ermöglicht, leichter in die bakterielle Zellwand einzudringen, wodurch sie die bakterielle Proteinsynthese innerhalb der Zelle stören können. Dies führt zu einer niedrigeren MBC für anfällige Organismen. ⓘ
Penicilline blockieren wie andere β-Laktam-Antibiotika nicht nur die Teilung von Bakterien, einschließlich Cyanobakterien, sondern auch die Teilung von Cyanellen, den photosynthetischen Organellen der Glaukophyten, und die Teilung der Chloroplasten von Bryophyten. Auf die Plastiden der hoch entwickelten Gefäßpflanzen haben sie dagegen keinen Einfluss. Dies spricht für die endosymbiotische Theorie der Evolution der Plastidenteilung bei Landpflanzen. ⓘ
Einige Bakterien produzieren Enzyme, die den β-Lactamring aufspalten, so genannte β-Lactamasen, die die Bakterien resistent gegen Penicillin machen. Daher werden einige Penicilline für den Einsatz gegen antibiotikaresistente Bakterien oder bei immungeschwächten Patienten modifiziert oder mit anderen Medikamenten verabreicht. Die Verwendung von Clavulansäure oder Tazobactam, β-Lactamase-Hemmern, zusammen mit Penicillin verleiht dem Penicillin Aktivität gegen β-Lactamase produzierende Bakterien. β-Lactamase-Hemmer binden irreversibel an β-Lactamase und verhindern, dass diese die Beta-Lactam-Ringe des Antibiotikamoleküls spaltet. Alternativ dazu ist Flucloxacillin ein modifiziertes Penicillin, das aufgrund einer Acyl-Seitenkette, die den Beta-Lactam-Ring vor β-Lactamase schützt, gegen β-Lactamase-produzierende Bakterien wirksam ist. ⓘ
Pharmakokinetik
Penicillin hat eine geringe Proteinbindung im Plasma. Die Bioverfügbarkeit von Penicillin hängt vom Typ ab: Penicillin G hat eine geringe Bioverfügbarkeit von unter 30 %, während Penicillin V eine höhere Bioverfügbarkeit von 60 bis 70 % aufweist. ⓘ
Penicillin hat eine kurze Halbwertszeit und wird über die Nieren ausgeschieden. Das bedeutet, dass es mindestens viermal täglich verabreicht werden muss, um ausreichende Penicillinspiegel im Blut aufrechtzuerhalten. In frühen Handbüchern über die Anwendung von Penicillin wurde daher empfohlen, Penicillin alle drei Stunden zu injizieren, und die Dosierung von Penicillin wurde mit dem Versuch verglichen, eine Badewanne mit herausgezogenem Stöpsel zu füllen. Dies ist heute nicht mehr erforderlich, da viel größere Penicillindosen billig und leicht erhältlich sind; einige Behörden empfehlen jedoch aus diesem Grund die Verwendung von Penicillin-Dauerinfusionen. ⓘ
Nebenwirkungen
Wie bei allen Antibiotika kann es auch gegen Penizillinen zu einer Resistenzbildung kommen. Weit geringer als bisher angenommen ist die Häufigkeit einer Allergie gegen eine Penizillintherapie (). Allergische Reaktionen können dabei von leichter Hautrötung bis zum anaphylaktischen Schock reichen. ⓘ
Durch Penicilline können nützliche Bakterien wie die der Darmflora abgetötet werden, insbesondere durch Breitbandpenicilline, die auch gegen gramnegative Bakterien wirken. Im ungünstigsten Fall können sich so schädliche Mikroorganismen im Darm ausbreiten und zu einer antibiotikaassoziierten Kolitis führen. ⓘ
Eine weitere seltene (mit einer Wahrscheinlichkeit von etwa drei Promille) unerwünschte Wirkung ist die Auslösung epileptischer Anfälle. ⓘ
Resistenz
Als Alexander Fleming 1928 das rohe Penicillin entdeckte, machte er die wichtige Beobachtung, dass viele Bakterien nicht auf Penicillin reagierten. Dieses Phänomen wurde von Ernst Chain und Edward Abraham erkannt, als sie versuchten, das Penicillin genau zu bestimmen. Im Jahr 1940 entdeckten sie, dass unempfindliche Bakterien wie Escherichia coli spezifische Enzyme produzieren, die Penicillinmoleküle abbauen können und sie damit resistent gegen das Antibiotikum machen. Sie nannten das Enzym Penicillinase. Penicillinase wird jetzt als Mitglied der Enzyme, die β-Laktamasen genannt werden, klassifiziert. Diese β-Laktamasen kommen natürlich auch in vielen anderen Bakterien vor, und viele Bakterien produzieren sie bei ständiger Einwirkung von Antibiotika. Bei den meisten Bakterien kann die Resistenz durch drei verschiedene Mechanismen entstehen: verringerte Permeabilität der Bakterien, verringerte Bindungsaffinität der Penicillin-bindenden Proteine (PBPs) oder Zerstörung des Antibiotikums durch die Expression von β-Laktamase. Mit Hilfe eines dieser Mechanismen entwickeln Bakterien häufig eine Resistenz gegen verschiedene Antibiotika, ein Phänomen, das als Multiresistenz bezeichnet wird. ⓘ
Der eigentliche Prozess des Resistenzmechanismus kann sehr komplex sein. Im Falle einer verminderten Permeabilität bei Bakterien sind die Mechanismen zwischen grampositiven und gramnegativen Bakterien unterschiedlich. Bei Gram-positiven Bakterien ist die Blockade von Penicillin auf Veränderungen in der Zellwand zurückzuführen. So ist die Resistenz gegen Vancomycin bei S. aureus auf eine zusätzliche Peptidoglykansynthese zurückzuführen, die die Zellwand wesentlich dicker macht und das Eindringen von Penicillin verhindert. Die Resistenz bei gramnegativen Bakterien ist auf Mutationsvariationen in der Struktur und Anzahl der Porine zurückzuführen. Bei Bakterien wie Pseudomonas aeruginosa ist die Zahl der Porine reduziert, während bei Bakterien wie Enterobacter species, Escherichia coli und Klebsiella pneumoniae veränderte Porine wie unspezifische Porine (z. B. OmpC- und OmpF-Gruppen) vorhanden sind, die kein Penicillin transportieren können. ⓘ
Die Resistenz aufgrund von PBP-Veränderungen ist sehr unterschiedlich. Ein häufiger Fall ist Streptococcus pneumoniae, wo das Gen für PBP mutiert ist und die mutierten PBPs eine geringere Bindungsaffinität für Penicilline aufweisen. In S. pneumoniae gibt es sechs mutierte PBPs, von denen PBP1a, PBP2b, PBP2x und manchmal PBP2a für die verminderte Bindungsaffinität verantwortlich sind. S. aureus kann ein verstecktes Gen aktivieren, das ein anderes PBP, PBD2, produziert, das eine geringe Bindungsaffinität für Penicilline hat. Es gibt einen anderen Stamm von S. aureus, den methicillinresistenten S. aureus (MRSA), der nicht nur gegen Penicillin und andere β-Lactame, sondern auch gegen die meisten Antibiotika resistent ist. Der Bakterienstamm entwickelte sich nach der Einführung von Methicillin im Jahr 1959. Bei MRSA führen Mutationen in den Genen (mec-System) für PBP zur Bildung einer Proteinvariante namens PBP2a (auch PBP2' genannt), während vier normale PBPs entstehen. PBP2a hat eine geringe Bindungsaffinität für Penicillin und besitzt auch keine Glykosyltransferase-Aktivität, die für die vollständige Peptidoglykan-Synthese erforderlich ist (die von den vier normalen PBPs durchgeführt wird). Bei Helicobacter cinaedi gibt es mehrere Mutationen in verschiedenen Genen, die zu PBP-Varianten führen. ⓘ
Die enzymatische Zerstörung durch β-Laktamasen ist der wichtigste Mechanismus der Penicillinresistenz und wird als "die größte Bedrohung für die Verwendung [von Penicillinen]" bezeichnet. Es war der erste entdeckte Mechanismus der Penicillinresistenz. Bei den Experimenten zur Reinigung und biologischen Aktivität von Penicillin im Jahr 1940 wurde festgestellt, dass E. coli unempfindlich war. Der Grund dafür wurde in der Produktion eines Enzyms Penicillinase (also der ersten bekannten β-Lactamase) in E. coli entdeckt, das Penicillin leicht abbaut. Es gibt über 2.000 Arten von β-Lactamasen, von denen jede eine einzigartige Aminosäuresequenz und damit enzymatische Aktivität hat. Sie alle sind in der Lage, β-Lactamringe zu hydrolysieren, aber ihre genauen Zielorte sind unterschiedlich. Sie werden von grampositiven Bakterien in großen Mengen auf der Bakterienoberfläche sezerniert, von gramnegativen Arten dagegen weniger. Daher können bei einer bakteriellen Mischinfektion die grampositiven Bakterien die ansonsten für Penicillin empfänglichen gramnegativen Zellen schützen. ⓘ
Bei P. aeruginosa gibt es ungewöhnliche Mechanismen, bei denen es zu einer Biofilm-vermittelten Resistenz und zur Bildung von multitoleranten Persisterzellen kommen kann. ⓘ
Geschichte
Entdeckung

Seit dem späten 19. Jahrhundert gab es Berichte über die antibakteriellen Eigenschaften des Penicillium-Schimmels, aber die Wissenschaftler waren nicht in der Lage zu erkennen, welcher Prozess die Wirkung hervorrief. Der schottische Arzt Alexander Fleming vom St. Mary's Hospital in London (heute Teil des Imperial College) war der erste, der nachweisen konnte, dass Penicillium rubens antibakterielle Eigenschaften besitzt. Am 3. September 1928 beobachtete er, dass eine Pilzkontamination einer Bakterienkultur (Staphylococcus aureus) die Bakterien abzutöten schien. Diese Beobachtung bestätigte er am 28. September 1928 in einem neuen Versuch. Er veröffentlichte sein Experiment 1929 und nannte die antibakterielle Substanz (den Pilzextrakt) Penicillin. ⓘ
C. J. La Touche identifizierte den Pilz als Penicillium rubrum (später von Charles Thom als P. notatum und P. chrysogenum neu klassifiziert, aber später als P. rubens korrigiert). Fleming zeigte sich anfangs optimistisch, dass Penicillin ein nützliches Antiseptikum sein würde, da es im Vergleich zu anderen damaligen Antiseptika eine hohe Wirksamkeit und eine geringe Toxizität aufwies, und wies auf seinen Laborwert bei der Isolierung von Bacillus influenzae (heute Haemophilus influenzae genannt) hin. ⓘ
Fleming konnte niemanden davon überzeugen, dass seine Entdeckung wichtig war. Das lag vor allem daran, dass Penicillin so schwierig zu isolieren war, dass seine Entwicklung als Medikament unmöglich schien. Es wird spekuliert, dass, wenn es Fleming besser gelungen wäre, andere Wissenschaftler für seine Arbeit zu interessieren, Penicillin möglicherweise schon Jahre früher entwickelt worden wäre. ⓘ
Die Bedeutung seiner Arbeit wurde dadurch gewürdigt, dass das Alexander-Fleming-Labormuseum in London am 19. November 1999 zum Internationalen Historischen Chemiedenkmal ernannt wurde. ⓘ
Medizinische Anwendung

1930 behandelte Cecil George Paine, Pathologe an der Royal Infirmary in Sheffield, am 25. November 1930 erfolgreich die Ophthalmia neonatorum, eine Gonokokkeninfektion bei Säuglingen, mit Penicillin (Pilzextrakt). ⓘ
1940 erzielten der australische Wissenschaftler Howard Florey (später Baron Florey) und ein Forscherteam (Ernst Chain, Edward Abraham, Arthur Duncan Gardner, Norman Heatley, Margaret Jennings, Jean Orr-Ewing und Arthur Gordon Sanders) an der Sir William Dunn School of Pathology der Universität Oxford Fortschritte bei der Herstellung von konzentriertem Penicillin aus Pilzkulturbrühe, das sowohl in vitro als auch in vivo bakterientötend wirkte. Im Jahr 1941 behandelten sie einen Polizisten, Albert Alexander, mit einer schweren Gesichtsinfektion; sein Zustand verbesserte sich, aber dann gingen die Penicillinvorräte zur Neige und er starb. In der Folge wurden mehrere andere Patienten erfolgreich behandelt. Im Dezember 1942 waren die Überlebenden des Cocoanut Grove-Brandes in Boston die ersten Brandopfer, die erfolgreich mit Penicillin behandelt wurden. ⓘ
Der erste erfolgreiche Einsatz von reinem Penicillin war die Behandlung von Harry Lambert mit einer tödlichen Infektion des Nervensystems (Streptokokkenmeningitis) im Jahr 1942 durch Fleming. Zu diesem Zeitpunkt konnte das Team in Oxford nur eine kleine Menge herstellen. Florey gab die einzige verfügbare Probe bereitwillig an Fleming ab. Bei Lambert trat bereits am nächsten Tag der Behandlung eine Besserung ein, und innerhalb einer Woche war er vollständig geheilt. Fleming veröffentlichte seine klinische Studie 1943 in The Lancet. Nach diesem medizinischen Durchbruch setzte das britische Kriegskabinett am 5. April 1943 den Penicillin-Ausschuss ein, der Projekte für die Massenproduktion in Angriff nahm. ⓘ
Die Massenproduktion
Als die medizinische Anwendung feststand, stellte das Team in Oxford fest, dass es unmöglich war, in ihrem Labor brauchbare Mengen herzustellen. Da es ihnen nicht gelang, die britische Regierung zu überzeugen, reisten Florey und Heatley im Juni 1941 mit ihren Schimmelpilzproben in die USA, um die US-Regierung für eine Massenproduktion zu interessieren. Sie wandten sich an das USDA Northern Regional Research Laboratory (NRRL, heute National Center for Agricultural Utilization Research) in Peoria, Illinois, wo Einrichtungen für großtechnische Fermentationen eingerichtet wurden. Die Massenkultur des Schimmels und die Suche nach besseren Schimmelpilzen folgten sofort. ⓘ
Am 14. März 1942 wurde der erste Patient wegen einer Streptokokken-Sepsis mit dem in den USA hergestellten Penicillin der Firma Merck & Co. behandelt. Die Hälfte des gesamten damals produzierten Vorrats wurde für diese eine Patientin, Anne Miller, verwendet. Im Juni 1942 war gerade noch genug US-Penicillin für die Behandlung von zehn Patienten verfügbar. Im Juli 1943 erstellte das War Production Board einen Plan für die Massenverteilung von Penicillinvorräten an die in Europa kämpfenden alliierten Truppen. Dank der Ergebnisse der Fermentationsforschung an Maisbrei am NRRL konnten die Vereinigten Staaten rechtzeitig vor der Invasion in der Normandie im Frühjahr 1944 2,3 Millionen Dosen herstellen. Nach einer weltweiten Suche im Jahr 1943 wurde auf einem Markt in Peoria, Illinois, eine verschimmelte Melone gefunden, die den besten Schimmelpilzstamm für die Herstellung nach dem Mais-Steillaugen-Verfahren enthielt. Der Pfizer-Wissenschaftler Jasper H. Kane schlug vor, für die Herstellung großer Mengen von Penicillin in pharmazeutischer Qualität ein Fermentationsverfahren in tiefen Tanks anzuwenden. Die Entwicklung einer Fermentationsanlage in tiefen Tanks durch die Chemieingenieurin Margaret Hutchinson Rousseau ermöglichte die Produktion in großem Maßstab. Als unmittelbare Folge des Krieges und des War Production Board wurden bis Juni 1945 über 646 Milliarden Einheiten pro Jahr hergestellt. ⓘ
G. Raymond Rettew leistete einen bedeutenden Beitrag zu den amerikanischen Kriegsanstrengungen, indem er seine Kenntnisse über Pilzbrut mit der Funktionsweise des Sharples Cream Separators kombinierte, um Penicillin in kommerziellen Mengen herzustellen. Bis 1943 wurde in Rettews Labor der größte Teil des weltweiten Penicillins hergestellt. Während des Zweiten Weltkriegs trug Penicillin wesentlich dazu bei, die Zahl der durch infizierte Wunden verursachten Todesfälle und Amputationen bei den alliierten Streitkräften zu verringern und rettete schätzungsweise 12 % bis 15 % der Menschenleben. Die Verfügbarkeit des Medikaments war jedoch stark eingeschränkt, da es schwierig war, große Mengen Penicillin herzustellen, und da das Medikament schnell über die Nieren ausgeschieden wurde, was eine häufige Dosierung erforderlich machte. Verfahren zur Massenproduktion von Penicillin wurden 1945 von Andrew Jackson Moyer patentiert. Florey hatte das Penicillin nicht patentieren lassen, da er von Sir Henry Dale darauf hingewiesen wurde, dass dies unethisch wäre. ⓘ
Penicillin wird aktiv ausgeschieden, und etwa 80 % einer Penicillin-Dosis werden innerhalb von drei bis vier Stunden nach der Verabreichung aus dem Körper ausgeschieden. In der Tat war das Medikament in der frühen Penicillin-Ära so knapp und hoch geschätzt, dass es üblich wurde, den Urin der behandelten Patienten zu sammeln, um das darin enthaltene Penicillin zu isolieren und wieder zu verwenden. Da dies keine zufriedenstellende Lösung war, suchten die Forscher nach einer Möglichkeit, die Penicillinausscheidung zu verlangsamen. Sie hofften, ein Molekül zu finden, das mit dem Penicillin um den für die Ausscheidung verantwortlichen Transporter für organische Säuren konkurrieren könnte, so dass der Transporter das konkurrierende Molekül bevorzugt ausscheiden und das Penicillin zurückhalten würde. Das Urikosurikum Probenecid erwies sich als geeignet. Bei gleichzeitiger Verabreichung von Probenecid und Penicillin hemmt Probenecid konkurrierend die Ausscheidung von Penicillin, wodurch sich die Penicillinkonzentration erhöht und die Wirkung des Penicillins verlängert wird. Mit dem Aufkommen von Massenproduktionstechniken und halbsynthetischen Penicillinen wurden die Versorgungsprobleme schließlich gelöst, so dass die Verwendung von Probenecid zurückging. Bei bestimmten Infektionen, die besonders hohe Penicillinkonzentrationen erfordern, ist Probenecid jedoch immer noch nützlich. ⓘ
Nach dem Zweiten Weltkrieg war Australien das erste Land, das das Medikament für den zivilen Gebrauch zur Verfügung stellte. In den USA wurde Penicillin am 15. März 1945 für die Allgemeinheit zugänglich gemacht. ⓘ
Fleming, Florey und Chain erhielten 1945 gemeinsam den Nobelpreis für Physiologie oder Medizin für die Entwicklung von Penicillin. ⓘ
Dorothy Hodgkin bestimmt die chemische Struktur von Penicillin. ⓘ
Nachdem 1940 und 1941 der „Oxforder Kreis“ um E. B. Chain und H. W. Florey ein Verfahren zur Produktion und Isolierung von Penicillin in „Lancet“ veröffentlicht hatte, wurden ab 1942 die ersten industriellen Produktionen gestartet, allen voran durch Glaxo und ICI in England, MSD Sharp & Dohme (MSD), Pfizer & Co. und Squibb & Sons in den USA sowie Schott Jena (vorangetrieben durch Hans Knöll) in Deutschland. ⓘ
Im Jahre 1943 stellten Pharmafirmen in den USA knapp 1,5 Tonnen reines Penicillin her, 1945 konnte die Produktion bereits auf über 400 Tonnen gesteigert werden. ⓘ
Ab 1942 wurde auch bei den Farbwerken Hoechst an Penicillin geforscht (die Produktion in kleinerem Maßstab begann dort im Frühjahr 1945). Die Forscher mussten sich dabei auf die knappen Veröffentlichungen Flemings stützen. Hoechst hatte auch nicht den ergiebigen Chrysogenum-Stamm zur Verfügung. Eine Probe dieses Stamms schickte erst 1950 der US-Konzern MSD im Rahmen einer Zusammenarbeit nach Westdeutschland. ⓘ
Parallel dazu forschte Robert Thren bei Madaus im sächsischen Radebeul an der Penicillinherstellung, aus der in Zusammenarbeit mit dem Chemiker Alfred Kuhn die ostdeutsche Produktion im Arzneimittelwerk Dresden hervorging. Als Stammhaus des Pharmazeutischen Kombinats GERMED wurde der Ostblock beliefert. ⓘ
Im Jahre 1945 war die in den USA produzierte Penicillinmenge 20-mal größer als die in Europa produzierte Menge. Gewöhnlicher Mais, in Wasser eingeweicht, von den Amerikanern corn steep liquor genannt (Maisquellwasser), erwies sich als ideales Nährmedium für den Pilz. Dabei wurde (1944 bei Pfizer) das zunächst angewandte Oberflächenverfahren (Emerskultur) durch das Submersverfahren (Flüssigkultur im Rührkesselreaktor) abgelöst, mit dem höhere Produktivitäten erreicht wurden. Im Oktober 1944 wurden die ersten Injektionspräparate hergestellt. 1943 boten 22 Firmen Penicillin an. Es blieb zunächst hauptsächlich verwundeten Soldaten vorbehalten, denn die Produktionsmenge reichte noch nicht aus, um auch alle zivilen Patienten damit zu behandeln. Seit 1944 waren die USA jedoch in der Lage, ihren gesamten zivilen und militärischen Bedarf an Penicillin zu decken. Hingegen war in Europa nach dem Zweiten Weltkrieg die Nachfrage groß und die Penicillinproduktion reichte hier nicht für alle Patienten. Es entwickelten sich Schmuggel und Schwarzhandel mit Penicillin, was auch Thema des Films Der dritte Mann ist. ⓘ
In den Jahrzehnten nach dem Zweiten Weltkrieg entwickelte sich die Nederlandsche Gist-en Spiritusfabrik (NG & SF), später Gist Brocades, heute DSM, zum weltgrößten Penicillinhersteller. Heute produziert die DSM Penicilline im Rahmen von Joint Ventures in der Volksrepublik China, während die Sandoz GmbH in Kundl (Österreich) heute den größten Produktionsstandort für Penicilline in der westlichen Welt betreibt. ⓘ
Strukturbestimmung und Totalsynthese

Die chemische Struktur des Penicillins wurde erstmals 1942 von Edward Abraham vorgeschlagen und 1945 von Dorothy Crowfoot Hodgkin, die ebenfalls in Oxford arbeitete, durch Röntgenkristallographie bestätigt. Für diese und andere Strukturbestimmungen erhielt sie 1964 den Nobelpreis für Chemie. ⓘ
Der Chemiker John C. Sheehan am Massachusetts Institute of Technology (MIT) stellte 1957 die erste chemische Synthese von Penicillin fertig. Sheehan hatte 1948 mit seinen Studien zur Penicillinsynthese begonnen und im Laufe dieser Untersuchungen neue Methoden zur Synthese von Peptiden sowie neue Schutzgruppen entwickelt, die die Reaktivität bestimmter funktioneller Gruppen maskieren. Obwohl die von Sheehan entwickelte Ausgangssynthese nicht für die Massenproduktion von Penicillinen geeignet war, war eine der Zwischenverbindungen in Sheehans Synthese die 6-Aminopenicillansäure (6-APA), der Kern des Penicillins. ⓘ
6-APA wurde 1957 von Forschern der Beecham Research Laboratories (später Beecham Group) in Surrey entdeckt (1959 veröffentlicht). Durch das Anhängen verschiedener Gruppen an den 6-APA-"Kern" des Penicillins konnten neue Formen von Penicillinen geschaffen werden, die vielseitiger sind und eine bessere Wirkung haben. ⓘ
Die Entwicklungen von Penicillin
Das enge Spektrum der behandelbaren Krankheiten oder "Wirkungsspektrum" der Penicilline sowie die geringe Aktivität des oral wirksamen Phenoxymethylpenicillins führten zur Suche nach Penicillinderivaten, die ein breiteres Spektrum von Infektionen behandeln können. Die Isolierung von 6-APA, dem Kern von Penicillin, ermöglichte die Herstellung halbsynthetischer Penicilline mit verschiedenen Verbesserungen gegenüber Benzylpenicillin (Bioverfügbarkeit, Spektrum, Stabilität, Verträglichkeit). ⓘ
Die erste große Entwicklung war 1961 das Ampicillin. Es bot ein breiteres Wirkungsspektrum als eines der ursprünglichen Penicilline. Die weitere Entwicklung führte zu β-Lactamase-resistenten Penicillinen, darunter Flucloxacillin, Dicloxacillin und Methicillin. Diese Penicilline zeichneten sich durch ihre Aktivität gegen β-Lactamase produzierende Bakterienspezies aus, waren jedoch unwirksam gegen die später aufgetretenen Methicillin-resistenten Staphylococcus aureus (MRSA)-Stämme. ⓘ
Eine weitere Entwicklung in der Reihe der echten Penicilline waren die antipseudomonischen Penicilline wie Carbenicillin, Ticarcillin und Piperacillin, die wegen ihrer Wirkung gegen gramnegative Bakterien nützlich sind. Die Nützlichkeit des β-Lactamrings war jedoch so groß, dass verwandte Antibiotika, darunter die Mecilliname, die Carbapeneme und vor allem die Cephalosporine, ihn noch immer im Zentrum ihrer Struktur haben. ⓘ
Herstellung

Penicillin ist ein Sekundärmetabolit bestimmter Penicillium-Arten und wird produziert, wenn das Wachstum des Pilzes durch Stress gehemmt wird. Während des aktiven Wachstums wird es nicht produziert. Die Produktion wird auch durch Rückkopplungen im Syntheseweg von Penicillin begrenzt. ⓘ
- α-Ketoglutarat + AcCoA → Homocitrat → L-α-Aminoadipinsäure → L-Lysin + β-Lactam ⓘ
Das Nebenprodukt L-Lysin hemmt die Produktion von Homocitrat, so dass die Anwesenheit von exogenem Lysin bei der Penicillinproduktion vermieden werden sollte. ⓘ
Die Penicillium-Zellen werden in einer so genannten Fed-Batch-Kultur gezüchtet, bei der die Zellen ständig Stress ausgesetzt sind, der für die Induktion der Penicillinproduktion erforderlich ist. Auch die verfügbaren Kohlenstoffquellen sind wichtig: Glukose hemmt die Penicillinproduktion, Laktose hingegen nicht. Der pH-Wert und der Gehalt an Stickstoff, Lysin, Phosphat und Sauerstoff in den Chargen müssen ebenfalls sorgfältig kontrolliert werden. ⓘ
Die biotechnologische Methode der gerichteten Evolution wurde angewandt, um durch Mutation eine große Zahl von Penicillium-Stämmen zu erzeugen. Zu diesen Techniken gehören die fehleranfällige PCR, das DNA-Shuffling, ITCHY und die PCR mit Strangüberlappung. ⓘ
Semisynthetische Penicilline werden ausgehend von dem Penicillinkern 6-APA hergestellt. ⓘ
Biosynthese

Die Biosynthese von Penicillin G (Benzylpenicillin) besteht aus drei wichtigen Schritten.
- Der erste Schritt ist die Kondensation von drei Aminosäuren - L-α-Aminoadipinsäure, L-Cystein und L-Valin - zu einem Tripeptid. Vor der Kondensation zum Tripeptid muss die Aminosäure L-Valin epimerisiert werden, um zu D-Valin zu werden. Das kondensierte Tripeptid wird als δ-(L-α-Aminoadipyl)-L-Cystein-D-valin (ACV) bezeichnet. Die Kondensationsreaktion und die Epimerisierung werden beide durch das Enzym δ-(L-α-Aminoadipyl)-L-Cystein-D-Valin-Synthetase (ACVS) katalysiert, eine nichtribosomale Peptidsynthetase oder NRPS.
- Der zweite Schritt in der Biosynthese von Penicillin G ist die oxidative Umwandlung von linearem ACV in das bicyclische Zwischenprodukt Isopenicillin N durch die Isopenicillin-N-Synthase (IPNS), die durch das Gen pcbC kodiert wird. Isopenicillin N ist ein sehr schwaches Zwischenprodukt, da es keine starke antibiotische Aktivität aufweist.
- Der letzte Schritt ist eine Transamidierung durch Isopenicillin N N-Acyltransferase, bei der die α-Aminoadipyl-Seitenkette von Isopenicillin N entfernt und gegen eine Phenylacetyl-Seitenkette ausgetauscht wird. Diese Reaktion wird durch das Gen penDE kodiert, das für den Prozess der Penicillin-Gewinnung einzigartig ist. ⓘ
Einteilung
Bio- und partialsynthetische Penicilline
Das oral wirksame Penicillin V (Phenoxymethylpenicillin) entsteht ebenfalls fermentativ, aber nicht spontan, sondern durch Zusatz eines synthetischen Präkursors, der Phenoxyessigsäure („Biosynthese“). ⓘ
Partialsynthetische Weiterentwicklungen der natürlichen Penicilline entstehen durch Umsetzung von 6-Aminopenicillinsäure mit Carbonsäurehalogeniden. Sie zeichnen sich gegenüber dem Penicillin G durch bestimmte Vorteile aus wie Säure- und Penicillinasestabilität oder ein erweitertes Wirkspektrum. ⓘ
Säurestabile (oral wirksame) Penicilline ohne bzw. mit geringer Penicillinasestabilität
- Phenoxymethylpenicillin (Penicillin V), Propicillin, Pheneticillin
Durch eine verminderte Nucleophilie des Carbonylsauerstoffs ist der Angriff von Hydronium-Ionen erschwert, wodurch die Umwandlung zur unwirksamen Penillsäure gehemmt wird. Säurestabile Penicilline werden also durch Magensäure nicht zerstört und können daher oral verabreicht werden. Sie haben das gleiche Wirkspektrum wie Penicillin G. ⓘ
Breitspektrumpenicilline
- Aminopenicilline: Amoxicillin, Ampicillin, Bacampicillin, Pivampicillin, Sultamicillin
- Carboxypenicilline: Carbenicillin, Ticarcillin
- Ureidopenicilline (Acylaminopenicilline): Azlocillin, Piperacillin, Mezlocillin ⓘ
Durch die Einführung polarer Substituenten vermögen solche hydrophilen Penicilline die Zellwände von gramnegativen Erregern zu passieren, wodurch ihr Wirkspektrum erweitert wird. Die Breitspektrumpenicilline sind teilweise säure- und penicillinaseempfindlich, teilweise ist auch die Wirksamkeit gegenüber einigen grampositiven Bakterien vermindert. ⓘ
Kein Acylierungsprodukt der 6-Aminopenicillansäure ist das Pivmecillinam, es besitzt jedoch das bicyclische Lactam-Grundgerüst der Penicilline. ⓘ




