Tocopherol
| Strukturformel ⓘ | |||||||||
|---|---|---|---|---|---|---|---|---|---|

| |||||||||
| (RRR)-Isomer von Tocopherol (α-Tocopherol) | |||||||||
| Allgemeines | |||||||||
| Trivialname | Vitamin E | ||||||||
| Andere Namen |
| ||||||||
| Summenformel | C29H50O2 | ||||||||
| CAS-Nummer |
| ||||||||
| PubChem | 14985 | ||||||||
| ATC-Code |
A11HA03 | ||||||||
| DrugBank | DB00163 | ||||||||
| Kurzbeschreibung | gelbe bis braune Flüssigkeit | ||||||||
| Vorkommen | Getreide, Nüsse, Samen, Pflanzenöle, Milch, Eier | ||||||||
| Physiologie | |||||||||
| Funktion | Antioxidans | ||||||||
| Täglicher Bedarf | 10 mg | ||||||||
| Folgen bei Mangel | Unfruchtbarkeit, unspezifische Symptome wie: trockene, faltige Haut, Müdigkeit, verminderte Wundheilung | ||||||||
| Überdosis | >300 mg/Tag | ||||||||
| Eigenschaften | |||||||||
| Molare Masse | 430,71 g/mol | ||||||||
| Aggregatzustand | flüssig | ||||||||
| Dichte | 0,95 g·cm−3 | ||||||||
| Schmelzpunkt |
2,5–3,5 °C | ||||||||
| Siedepunkt |
| ||||||||
| Löslichkeit | fettlöslich, <1 mg/l in Wasser | ||||||||
| Sicherheitshinweise | |||||||||
| |||||||||
| Toxikologische Daten |
| ||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||
Tocopherole ist ein Sammelbegriff für verschiedene fettlösliche Substanzen, die einen modifizierten Chromanring mit einer gesättigten Seitenkette haben. Hiervon weisen die (RRR)-Stereoisomere eine biologische, antioxidative Aktivität auf und werden dann zu Vitamin E zugeordnet. Häufig wird der Begriff Vitamin E allein für (RRR)-α-Tocopherol, die am besten erforschte Form von Vitamin E, verwendet. Ferner gibt es noch MDT (marine derived tocopherols). ⓘ
Der Name leitet sich vom altgriechischen Wörtern τόκος tókos „Geburt, Nachkommen“ und φέρειν phérein „tragen, bringen“ ab, da man einen Einfluss auf die Reproduktionsfähigkeit von Ratten als erstes entdeckte. Die Endsilbe „ol“ weist auf den chemischen Charakter eines Alkohols hin. ⓘ
(RRR)-Tocopherole sind Bestandteile aller Membranen tierischer Zellen, werden jedoch nur von photosynthetisch aktiven Organismen wie Pflanzen und Cyanobakterien gebildet. ⓘ
α-Tocopherol ist die wichtigste Quelle, die in Nahrungsergänzungsmitteln und in der europäischen Ernährung zu finden ist, wo Oliven- und Sonnenblumenöl die wichtigsten Nahrungsquellen sind, während γ-Tocopherol in der amerikanischen Ernährung aufgrund des höheren Verzehrs von Soja- und Maisöl die häufigste Form ist. ⓘ
Formen
Vitamin E gibt es in acht verschiedenen Formen, vier Tocopherole und vier Tocotrienole. Alle haben einen Chromanring mit einer Hydroxylgruppe, die ein Wasserstoffatom spenden kann, um freie Radikale zu reduzieren, und eine hydrophobe Seitenkette, die das Eindringen in biologische Membranen ermöglicht. Sowohl die Tocopherole als auch die Tocotrienole kommen in α- (alpha), β- (beta), γ- (gamma) und δ- (delta) Formen vor, die durch die Anzahl und Position der Methylgruppen am Chromanolring bestimmt werden. ⓘ
| Form | Struktur ⓘ |
|---|---|
| α-Tocopherol | 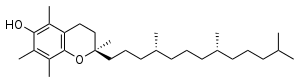
|
| β-Tocopherol | 
|
| γ-Tocopherol | 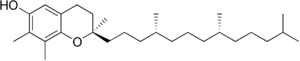
|
| δ-Tocopherol | 
|
Die Tocotrienole haben die gleiche Methylstruktur am Ring und die gleiche griechische Buchstaben-Methyl-Notation, unterscheiden sich aber von den analogen Tocopherolen durch das Vorhandensein von drei Doppelbindungen in der hydrophoben Seitenkette. Durch die Ungesättigtheit der Schwänze haben die Tocotrienole nur ein einziges stereoisomeres Kohlenstoffatom (und damit zwei mögliche Isomere pro Strukturformel, von denen eines natürlich vorkommt), während die Tocopherole drei Zentren haben (und acht mögliche Stereoisomere pro Strukturformel, von denen wiederum nur eines natürlich vorkommt). ⓘ
Jede Form hat eine andere biologische Aktivität. Im Allgemeinen fehlt den unnatürlichen l-Isomeren der Tocotrienole fast die gesamte Vitaminaktivität, und die Hälfte der 8 möglichen Isomere der Tocopherole (diejenigen mit 2S-Chiralität an der Ringschwanzverbindung) haben ebenfalls keine Vitaminaktivität. Bei den Stereoisomeren, die ihre Aktivität beibehalten, erhöht eine zunehmende Methylierung, insbesondere eine vollständige Methylierung zur Alpha-Form, die Vitaminaktivität. Bei Tocopherolen ist dies auf die Vorliebe des Tocopherol-Bindungsproteins für die α-Tocopherolform des Vitamins zurückzuführen. ⓘ
Als Lebensmittelzusatzstoff wird Tocopherol mit diesen E-Nummern gekennzeichnet: E306 (Tocopherol), E307 (α-Tocopherol), E308 (γ-Tocopherol) und E309 (δ-Tocopherol). Alle diese Stoffe sind in den USA, der EU, Australien und Neuseeland als Antioxidantien zugelassen. ⓘ
α-Tocopherol
α-Tocopherol ist die Form von Vitamin E, die vom Menschen bevorzugt absorbiert und akkumuliert wird. Die Messung der "Vitamin E"-Aktivität in internationalen Einheiten (IE) basierte auf der Verbesserung der Fruchtbarkeit durch die Verhinderung von Fehlgeburten bei trächtigen Ratten im Vergleich zu α-Tocopherol. ⓘ
Obwohl die monomethylierte Form ddd-γ-Tocopherol die in Ölen am weitesten verbreitete Form von Vitamin E ist, gibt es Hinweise darauf, dass Ratten diese Form zum bevorzugten α-Tocopherol methylieren können, da mehrere Generationen von Ratten die α-Tocopherol-Gewebespiegel beibehielten, selbst wenn diese Generationen ihr Leben lang nur mit γ-Tocopherol gefüttert wurden. ⓘ
α-Tocopherol hat drei Stereozentren und ist somit ein chirales Molekül. Die acht Stereoisomere von α-Tocopherol unterscheiden sich durch die Anordnung der Gruppen um diese Stereozentren. In der folgenden Abbildung von RRR-α-Tocopherol liegen alle drei Stereozentren in der R-Form vor. Würde man jedoch die Mitte der drei Stereozentren verändern (so dass der Wasserstoff nun nach unten und die Methylgruppe nach oben zeigt), würde dies die Struktur von RSR-α-Tocopherol ergeben. Diese Stereoisomere können auch nach einer alternativen älteren Nomenklatur benannt werden, bei der die Stereozentren entweder in der d- oder l-Form vorliegen. ⓘ

1 IE Tocopherol ist definiert als ⅔ Milligramm RRR-α-Tocopherol (früher d-α-Tocopherol oder manchmal ddd-α-Tocopherol genannt). 1 IE ist auch definiert als 1 Milligramm einer gleichwertigen Mischung der acht Stereoisomere, d. h. einer racemischen Mischung, die als All-rac-α-Tocopherylacetat bezeichnet wird. Diese Mischung von Stereoisomeren wird häufig als dl-α-Tocopherylacetat bezeichnet, obwohl es sich genauer gesagt um dl,dl,dl-α-Tocopherylacetat handelt.) Allerdings wird 1 IE dieses racemischen Gemischs heute nicht mehr als äquivalent zu 1 IE natürlichem (RRR) α-Tocopherol angesehen, und das Institute of Medicine und das USDA rechnen jetzt die IE des racemischen Gemischs in Milligramm äquivalentes RRR um, wobei 1 IE racemisches Gemisch = 0,45 "Milligramm α-Tocopherol". ⓘ
Tocotrienole
Tocotrienole sind zwar weniger bekannt, gehören aber ebenfalls zur Vitamin-E-Familie. Tocotrienole haben vier natürliche 2'-d-Isomere (sie haben ein stereoisomeres Kohlenstoffatom nur an der 2'-Ringschwanzposition). Die vier Tocotrienole (in der Reihenfolge der abnehmenden Methylierung: d-α-, d-β-, d-γ- und d-δ-Tocotrienol) haben Strukturen, die denen der vier Tocopherole entsprechen, jedoch mit einer ungesättigten Bindung in jeder der drei Isopreneinheiten, die den Kohlenwasserstoffschwanz bilden, während die Tocopherole einen gesättigten Phytylschwanz haben (der Phytylschwanz der Tocopherole bietet die Möglichkeit für zwei weitere stereoisomere Stellen in diesen Molekülen, die Tocotrienole nicht haben). Tocotrienol war Gegenstand weniger klinischer Studien und wurde weniger erforscht als Tocopherol. Allerdings wächst das Interesse an den gesundheitlichen Auswirkungen dieser Verbindungen. ⓘ
Funktion und Verzehrempfehlungen

Mechanismus der Wirkung
Tocopherole sind Radikalfänger, die ein H-Atom abgeben, um freie Radikale abzuschrecken. Mit 323 kJ/mol ist die O-H-Bindung in Tocopherolen etwa 10 % schwächer als in den meisten anderen Phenolen. Diese schwache Bindung ermöglicht es dem Vitamin, dem Peroxylradikal und anderen freien Radikalen ein Wasserstoffatom zu spenden und so deren schädliche Wirkung zu minimieren. Das so entstandene Tocopherylradikal ist relativ reaktionslos, wird aber durch eine Redoxreaktion mit einem Wasserstoffspender wie Vitamin C wieder zu Tocopherol. Da Tocopherole fettlöslich sind, werden sie in die Zellmembranen eingebaut, die dadurch vor oxidativen Schäden geschützt sind. ⓘ
Ernährungstechnische Überlegungen
Die empfohlene Tagesdosis (Recommended Dietary Allowance, RDA) der USA für Erwachsene beträgt 15 mg/Tag. Die RDA basiert auf der α-Tocopherolform, da diese die aktivste Form ist, die ursprünglich getestet wurde. Vitamin-E-Ergänzungen werden am besten absorbiert, wenn sie mit den Mahlzeiten eingenommen werden. Das U.S. Institute of Medicine hat eine obere tolerierbare Aufnahmemenge (UL) für Vitamin E von 1.000 mg (1.500 IU) pro Tag festgelegt. Die Europäische Behörde für Lebensmittelsicherheit setzt den UL auf 300 mg α-Tocopherol-Äquivalente/Tag fest. ⓘ
α-Tocopherol-Äquivalente
Für diätetische Zwecke wird die Vitamin-E-Aktivität der Vitamin-E-Isomere als α-Tocopherol-Äquivalente (a-TE) ausgedrückt. Ein a-TE ist definiert als die biologische Aktivität von 1 mg (natürlichem) d-α-Tocopherol im Resorptions-Gestations-Test. Nach den Auflistungen der FAO und anderer sollte β-Tocopherol mit 0,5, γ-Tocopherol mit 0,1 und α-Tocotrienol mit 0,3 multipliziert werden. Die IU werden in aTE umgerechnet, indem sie mit 0,67 multipliziert werden. Diese Faktoren korrelieren nicht mit der antioxidativen Aktivität der Vitamin-E-Isomere, wobei die Tocotrienole in vivo sogar eine viel höhere Aktivität aufweisen. ⓘ
Quellen
Das US-Landwirtschaftsministerium (USDA), Agricultural Research Services, unterhält eine Datenbank zur Lebensmittelzusammensetzung. Die letzte größere Überarbeitung war Release 28, September 2015. Im Allgemeinen sind die Lebensmittelquellen mit den höchsten Konzentrationen an Vitamin E pflanzliche Öle, gefolgt von Nüssen und Samen. Berücksichtigt man jedoch die typischen Portionsgrößen, so gehören für viele Menschen in den Vereinigten Staaten angereicherte Frühstücksflocken zu den wichtigsten Vitamin-E-Quellen. ⓘ
Mangel
Vitamin-E-Mangel ist selten und wird in fast allen Fällen durch eine Grunderkrankung und nicht durch eine Vitamin-E-arme Ernährung verursacht. Vitamin-E-Mangel verursacht neurologische Probleme aufgrund einer schlechten Nervenleitung. Dazu gehören neuromuskuläre Probleme wie die spinozerebelläre Ataxie und Myopathien. Ein Mangel kann auch zu Anämie führen, die auf eine oxidative Schädigung der roten Blutkörperchen zurückzuführen ist. ⓘ
Ergänzungen
Die im Handel erhältlichen Vitamin-E-Ergänzungen lassen sich in verschiedene Kategorien einteilen:
- Vollsynthetisches Vitamin E, "dl-α-Tocopherol", die preiswerteste, am häufigsten verkaufte Ergänzungsform, in der Regel als Acetat-Ester
- Halbsynthetische Vitamin-E-Ester "natürlicher Herkunft", die in Tabletten und Mehrfachvitaminen verwendet werden; dabei handelt es sich um stark fraktioniertes d-α-Tocopherol oder seine Ester, die häufig durch synthetische Methylierung von aus Pflanzenölen gewonnenen Gamma- und Beta-d,d,d-Tocopherolvitameren hergestellt werden.
- Weniger fraktionierte "natürliche gemischte Tocopherole" und Nahrungsergänzungsmittel mit hohem d-γ-Tocopherol-Anteil ⓘ
Synthetisches vollracemisches
Synthetisches Vitamin E, das aus Erdölprodukten gewonnen wird, wird als vollracemisches α-Tocopherylacetat mit einer Mischung aus acht Stereoisomeren hergestellt. In dieser Mischung liegt ein α-Tocopherolmolekül von acht Molekülen in Form von RRR-α-Tocopherol vor (12,5 % der Gesamtmenge). ⓘ
Das 8-isomere All-Rac-Vitamin E wird auf den Etiketten immer einfach als dl-Tocopherol oder dl-Tocopherylacetat bezeichnet, obwohl es (wenn es vollständig ausgeschrieben ist) dl,dl,dl-Tocopherol heißt. Die derzeit größten Hersteller dieses Typs sind DSM und BASF. ⓘ
Natürliches α-Tocopherol ist die RRR-α- (oder ddd-α-) Form. Die synthetische dl,dl,dl-α ("dl-α") Form ist nicht so aktiv wie die natürliche ddd-α ("d-α") Tocopherolform. Dies ist hauptsächlich auf die geringere Vitaminaktivität der vier möglichen Stereoisomere zurückzuführen, die durch das l- oder S-Enantiomer am ersten Stereozentrum (eine S- oder l-Konfiguration zwischen dem Chromanolring und dem Schwanz, d. h. die Stereoisomere SRR, SRS, SSR und SSS) vertreten werden. Die drei unnatürlichen "2R"-Stereoisomere mit natürlicher R-Konfiguration an diesem 2'-Stereocenter, aber S an einem der anderen Zentren im Schwanz (d. h. RSR, RRS, RSS), scheinen eine beträchtliche RRR-Vitaminaktivität beizubehalten, da sie vom alpha-Tocopherol-Transportprotein erkannt werden und somit im Plasma verbleiben, während die anderen vier Stereoisomere (SRR, SRS, SSR und SSS) dies nicht tun. Somit hätte das synthetische all-rac-α-Tocopherol theoretisch etwa die Hälfte der Vitaminaktivität von RRR-α-Tocopherol im Menschen. Experimentell beträgt das Aktivitätsverhältnis der 8-isomeren racemischen Mischung zum natürlichen Vitamin im Schwangerschaftsmodell der Ratte 1 zu 1,36 (was auf ein gemessenes Aktivitätsverhältnis von 1/1,36 = 74 % des natürlichen Vitamins für die 8-isomere racemische Mischung schließen lässt). ⓘ
Obwohl es klar ist, dass Stereoisomermischungen nicht so aktiv sind wie die natürliche Form des RRR-α-Tocopherols in den oben genannten Verhältnissen, sind spezifische Informationen über etwaige Nebenwirkungen der sieben synthetischen Vitamin-E-Stereoisomere nicht ohne weiteres verfügbar. ⓘ
Ester
Die Hersteller wandeln auch die Phenolform der Vitamine (mit einer freien Hydroxylgruppe) häufig in Ester um, wobei Essig- oder Bernsteinsäure verwendet wird. Diese Tocopherylester sind stabiler und lassen sich leicht in Vitaminpräparaten verwenden. α-Tocopherylester werden im Darm entestert und dann als freies Tocopherol resorbiert. Tocopheryl-Nicotinat, Tocopheryl-Linolat und Tocopheryl-Palmitat-Ester werden auch in Kosmetika und einigen Arzneimitteln verwendet. ⓘ
Gemischte Tocopherole
| Lebensmittel | Gehalt mg/100 g ⓘ |
|---|---|
| Weizenkeimöl | 215,4 |
| Sonnenblumenöl | 55,8 |
| Erdnussöl | 17,2 |
| Olivenöl | 12,0 |
| Weizenkleie | 2,4 |
| Mais | 2,0 |
| Haferflocken | 1,5 |
| Spargel | 2,0 |
| Tomate | 0,9 |
| Möhre | 0,6 |
| Blumenkohl | 0,1 |
| Mandel | 25,0 |
| Haselnuss | 25,0 |
| Walnuss | 6,2 |
Tocopherol kommen sowohl in tierischen als auch pflanzlichen Nahrungsmitteln vor, wobei die Gehalte bei letzteren wesentlich höher sind. Besonders hohe Gehalte an Vitamin E weisen pflanzliche Öle auf, in der Regel überwiegt der Anteil von α-Tocopherol. Dagegen dominiert in Sojaöl γ-Tocopherol. Je mehr ungesättigte Fettsäuren in den Ölen enthalten ist, desto mehr Vitamin E kommt darin vor. ⓘ
Gemüse enthält im Vergleich zu den Ölen wenig Vitamin E, allgemein kommt in grünen Pflanzenteilen abhängig von der Menge an Chloroplasten viel α-Tocopherol vor. Daneben findet man es auch in anderen, „gelben“ Pflanzenteilen wie Wurzeln oder Früchten, dort korreliert es mit dem Gehalt an Chromoplasten (überwiegend als γ-Tocopherol). ⓘ
Vitamin E wird nur in Pflanzen aufgebaut, die Biosynthese startet aus Homogentisinsäure sowie Phytylpyrophosphat größtenteils in den Plastiden. ⓘ
In Palmöl wurde auch α-Tocomonoenol nachgewiesen, während manche marinen Organismen das sogenannte marine Tocopherol (marine derived tocopherol, MDT) enthalten. ⓘ
"Gemischte Tocopherole" enthalten in den USA mindestens 20 % (w/w) andere natürliche R,R,R-Tocopherole, d. h. R,R,R-α-Tocopherolgehalt plus mindestens 25 % R,R,R-β-, R,R,R-γ-, R,R,R-δ-Tocopherole. ⓘ
Verwendet
Beobachtungsstudien, bei denen die Nahrungsaufnahme und/oder die Serumkonzentration gemessen wird, und experimentelle Studien, bei denen es sich idealerweise um randomisierte klinische Studien (RCTs) handelt, sind zwei Möglichkeiten, die Auswirkungen oder das Fehlen von Auswirkungen einer vorgeschlagenen Maßnahme auf die menschliche Gesundheit zu untersuchen. Man kann davon ausgehen, dass die Ergebnisse von Beobachtungsstudien und experimentellen Studien übereinstimmen. Wenn es keine Übereinstimmung gibt, müssen andere Faktoren als das Design in Betracht gezogen werden. In Beobachtungsstudien zu Vitamin E kann eine umgekehrte Korrelation zwischen der Nahrungsaufnahme und dem Krankheitsrisiko oder der Serumkonzentration und dem Krankheitsrisiko als suggestiv angesehen werden, aber alle Schlussfolgerungen sollten auch auf randomisierten klinischen Studien von ausreichender Größe und Dauer beruhen, um klinisch signifikante Ergebnisse zu messen. Ein Problem bei Korrelationen besteht darin, dass andere Nährstoffe und Nicht-Nährstoff-Verbindungen (z. B. Polyphenole) in derselben Ernährung, die einen höheren Vitamin-E-Gehalt aufweist, möglicherweise höher sind. Ein weiteres Problem für die Relevanz von RCTs, das weiter unten beschrieben wird, besteht darin, dass in Beobachtungsstudien zwar das Krankheitsrisiko zwischen einer niedrigen und einer hohen Aufnahme von natürlich vorkommendem Vitamin E aus der Nahrung verglichen wird (weltweit liegt die mittlere Nahrungsaufnahme von Erwachsenen bei 6. 2 mg/Tag für d-α-Tocopherol; 10,2 mg/Tag, wenn alle Tocopherol- und Tocotrienol-Isomere einbezogen werden), wurden in den prospektiven RCTs häufig 400 IE/Tag synthetisches dl-α-Tocopherol als Testprodukt verwendet, was 268 mg α-Tocopheroläquivalenten entspricht. ⓘ
Zur Pharmakoepidemiologie des α-Tocopherols liegen umfangreiche Daten aus den Nationalen Untersuchungs-Surveys der Deutschen Herz-Kreislauf-Präventionsstudie (DHP) und aus dem Bundes-Gesundheitssurvey für die Bevölkerung vor. Durch die regelmäßige Anwendung α-tocopherolhaltiger Präparate kommt es danach zu einer dosisabhängigen und statistisch signifikanten Verringerung des β- und des γ-Tocopherols im Serum. Gesundheitliche Aspekte einer möglichen erhöhten Blutungsneigung unter Komedikation mit Acetylsalicylsäurepräparaten werden in der Literatur diskutiert. Auch zu Tocopheroloxidationsprodukten, wie z. B. dem Tocopherolchinon liegen Untersuchungsergebnisse aus Survey-Daten vor. ⓘ
Auch aus der Berliner Studie an Vegetariern liegen Daten zum Gehalt an Tocopherolen im Serum der Studienteilnehmer vor. Trotz höherer Aufnahme an Tocopherolen waren die Tocopherolgehalte im Serum der Vegetarier niedriger als bei den Vergleichspersonen. ⓘ
In einer großangelegten Studie an 35533 Männern wurde untersucht, ob Vitamin E gegen Prostatakrebs schützt. Verwendet wurden 400 IE/d all rac-α-tocopheryl acetate (synthetisch hergestelltes dl-α-Tocopherylacetat). Im Ergebnis trat Prostatakrebs zu 17 Prozent häufiger im Vergleich zur Kontrollgruppe auf. Dagegen wurde bei mehreren in vitro-Studien mit den gamma-Isomeren (gTP bzw. gTE) eine apoptotische Wirkung auf Prostatakrebszellen beobachtet. Zu ähnlich positiven Ergebnissen hinsichtlich der Schutzwirkung der Tocopherole kommt eine Multizentrische Studie mit mehr als 2000 Studienteilnehmern unter Berücksichtigung ernährungsepidemiologischer Daten zur Tocopherolaufnahme mit der Nahrung. ⓘ
Beliebtheit von Nahrungsergänzungsmitteln im Laufe der Zeit
In den USA könnte die Beliebtheit von Vitamin E als Nahrungsergänzungsmittel um das Jahr 2000 ihren Höhepunkt erreicht haben. Im Rahmen der Nurses' Health Study (NHS) und der Health Professionals Follow-up Study (HPFS) wurde die Einnahme von Nahrungsergänzungsmitteln durch Personen über 40 Jahre in den Jahren 1986-2006 verfolgt. Bei Frauen lag die Prävalenz 1986 bei 16,1 %, 1998 bei 46,2 % und 2002 bei 44,3 %, war aber 2006 auf 19,8 % zurückgegangen. Bei den Männern lag die Prävalenz in denselben Jahren bei 18,9 %, 52,0 %, 49,4 % und 24,5 %. Die Autoren stellten die Theorie auf, dass die rückläufige Verwendung in diesen gesundheitsbewussten Bevölkerungsgruppen auf die Veröffentlichung von Studien zurückzuführen sein könnte, die entweder keinen Nutzen oder negative Folgen von Vitamin-E-Ergänzungen zeigten. Es gibt noch weitere Belege für die rückläufige Verwendung von Vitamin E. Bei den US-Streitkräften wurden die Verschreibungen von Vitamin E für aktive, reservierte und pensionierte Soldaten und deren Angehörige über die Jahre 2007-2011 verfolgt. Die Verschreibungen von Vitamin E gingen um 53 % zurück, während Vitamin C konstant blieb und Vitamin D um 454 % zunahm. In einem Bericht über die Verkaufszahlen von Vitamin E in den USA wurde ein Rückgang um 50 % zwischen 2000 und 2006 dokumentiert, der zu einem großen Teil auf eine viel beachtete Meta-Analyse zurückgeführt wurde, die zu dem Schluss gekommen war, dass hochdosiertes Vitamin E die Gesamtsterblichkeit erhöht. ⓘ
Altersbedingte Makuladegeneration
In einem 2017 veröffentlichten Cochrane-Review über antioxidative Vitamin- und Mineralstoffpräparate zur Verlangsamung des Fortschreitens der altersbedingten Makuladegeneration (AMD) wurde nur eine klinische Vitamin-E-Studie identifiziert. Diese Studie verglich 500 IE/Tag α-Tocopherol mit Placebo über einen Zeitraum von vier Jahren und zeigte keine Wirkung auf das Fortschreiten der AMD bei Menschen, bei denen die Krankheit bereits diagnostiziert wurde. In einer weiteren Cochrane-Studie aus demselben Jahr und von denselben Autoren wurde die Literatur über die Vorbeugung der Entwicklung von AMD durch α-Tocopherol untersucht. Bei dieser Überprüfung wurden vier Studien mit einer Dauer von 4 bis 10 Jahren identifiziert, und es wurde keine Veränderung des Risikos für die Entwicklung von AMD festgestellt. Eine große klinische Studie, bekannt als AREDS, verglich β-Carotin (15 mg), Vitamin C (500 mg) und α-Tocopherol (400 IE) mit Placebo über einen Zeitraum von bis zu zehn Jahren und kam zu dem Schluss, dass die Kombination von Antioxidantien das Fortschreiten der AMD deutlich verlangsamt. Da es in der Studie jedoch keine Gruppe gab, die nur Vitamin E erhielt, konnten keine Rückschlüsse auf den Beitrag des Vitamins zur Wirkung gezogen werden. ⓘ
Komplementär- und Alternativmedizin
Befürworter der Megavitamintherapie und der orthomolekularen Medizin befürworten natürliche Tocopherole. In der Zwischenzeit konzentrierten sich die klinischen Studien weitgehend auf die Verwendung von synthetischem, rein racemischem d-α-Tocopherylacetat oder synthetischem dl-α-Tocopherylacetat. ⓘ
Theorie der Antioxidantien
Tocopherol wird eine antioxidative Wirkung zugeschrieben. Bei Personen mit chronischem oxidativem Stress, der auf einen erhöhten Serumcholesterinspiegel zurückzuführen ist, wurde eine Studie mit unterschiedlichen Dosierungen durchgeführt. Die F2-Isoprostan-Konzentration im Plasma wurde als Biomarker für die durch freie Radikale vermittelte Lipidperoxidation ausgewählt. Nur die beiden höchsten Dosen - 1600 und 3200 IE/Tag - führten zu einer signifikanten Senkung von F2-Isoprostan. ⓘ
Alzheimer-Krankheit
Die Alzheimer-Krankheit (AD) und die vaskuläre Demenz sind häufige Ursachen für den altersbedingten Rückgang der Gehirnfunktionen. Alzheimer ist eine chronische neurodegenerative Erkrankung, die sich mit der Zeit verschlimmert. Der Krankheitsprozess ist mit Plaques und Knäueln im Gehirn verbunden. Vaskuläre Demenz kann durch ischämische oder hämorrhagische Infarkte verursacht werden, die mehrere Hirnregionen betreffen, darunter das Gebiet der vorderen Hirnarterie, die Scheitellappen oder den Gyrus cingulatus. Es können beide Arten von Demenz vorliegen. Es wird vermutet, dass der Vitamin-E-Status (und der anderer antioxidativer Nährstoffe) einen möglichen Einfluss auf das Risiko der Alzheimer-Krankheit und der vaskulären Demenz hat. In einer Übersicht über Studien zur Nahrungsaufnahme wurde berichtet, dass ein höherer Verzehr von Vitamin E aus Lebensmitteln das Risiko, an Alzheimer zu erkranken, um 24 % senkt. Eine zweite Übersichtsarbeit untersuchte den Serum-Vitamin-E-Spiegel und berichtete über einen niedrigeren Serum-Vitamin-E-Spiegel bei Alzheimer-Patienten im Vergleich zu gesunden, altersgleichen Personen. In einer Konsenserklärung der British Association for Psychopharmacology aus dem Jahr 2017 heißt es, dass Vitamin E bis zum Vorliegen weiterer Informationen nicht zur Behandlung oder Prävention der Alzheimer-Krankheit empfohlen werden kann. ⓘ
Krebs
Die Auswertung von Beobachtungsstudien ergab, dass eine Ernährung mit einem höheren Vitamin-E-Gehalt mit einem geringeren relativen Risiko für Nieren-, Blasen- und Lungenkrebs verbunden ist. Bei Vergleichen zwischen der Gruppe mit dem niedrigsten und der Gruppe mit dem höchsten Vitamin-E-Konsum aus der Nahrung lag die durchschnittliche Verringerung des relativen Risikos im Bereich von 16-19 %. Für alle diese Übersichten merkten die Autoren an, dass die Ergebnisse durch prospektive Studien bestätigt werden müssten. Die Ergebnisse der randomisierten klinischen Studien (RCTs), in denen α-Tocopherol als Nahrungsergänzungsmittel verabreicht wurde, unterschieden sich von den Ergebnissen der Überprüfungen der Nahrungsaufnahme. Eine RCT mit 400 IU/Tag α-Tocopherol verringerte das Risiko für Blasenkrebs nicht. Bei männlichen Tabakrauchern hatten 50 mg/Tag keinen Einfluss auf die Entwicklung von Lungenkrebs. Eine Überprüfung von RCTs für Darmkrebs ergab keine statistisch signifikante Verringerung des Risikos. Bei männlichen Tabakrauchern verringerten 50 mg/Tag das Prostatakrebsrisiko um 32 %, aber in einer anderen Studie, die mehrheitlich von Nichtrauchern durchgeführt wurde, erhöhten 400 IU/Tag das Risiko um 17 %. Bei Frauen, die über einen Zeitraum von durchschnittlich 10,1 Jahren abwechselnd entweder ein Placebo oder 600 IE Vitamin E aus natürlichen Quellen zu sich nahmen, gab es keine signifikanten Unterschiede in Bezug auf Brust-, Lungen- oder Darmkrebs. ⓘ
Die U.S. Food and Drug Administration (FDA) hat 1993 ein Verfahren zur Überprüfung und Genehmigung von gesundheitsbezogenen Angaben für Lebensmittel und Nahrungsergänzungsmittel eingeführt. Eine 2012 herausgegebene qualifizierte gesundheitsbezogene Angabe erlaubt es, auf dem Etikett von Produkten zu behaupten, dass Vitamin E das Risiko von Nieren-, Blasen- und Darmkrebs verringern kann, mit der Auflage, dass das Etikett einen obligatorischen qualifizierenden Satz enthalten muss: "Die FDA ist zu dem Schluss gekommen, dass es nur sehr wenige wissenschaftliche Beweise für diese Behauptung gibt." Die Europäische Behörde für Lebensmittelsicherheit (EFSA) prüft vorgeschlagene gesundheitsbezogene Angaben für die Länder der Europäischen Union. Bis März 2018 hat die EFSA keine Angaben zu Vitamin E und Krebsprävention bewertet. ⓘ
Cataracts
In einer Meta-Analyse aus dem Jahr 2015 wurde berichtet, dass in Studien, in denen Tocopherol im Serum nachgewiesen wurde, eine höhere Serumkonzentration mit einer 23-prozentigen Verringerung des relativen Risikos für altersbedingten Katarakt (ARC) verbunden war, wobei der Effekt auf Unterschiede beim nuklearen Katarakt und nicht beim kortikalen oder posterioren subkapsulären Katarakt - den drei Hauptklassifikationen des altersbedingten Katarakts - zurückzuführen war. In diesem Artikel und in einer zweiten Metaanalyse, in der über klinische Studien zur Supplementierung mit α-Tocopherol berichtet wurde, wurde jedoch keine statistisch signifikante Veränderung des Risikos für ARC im Vergleich zu Placebo festgestellt. ⓘ
Herz-Kreislauf-Erkrankungen
Die Forschung über die Auswirkungen von Vitamin E auf Herz-Kreislauf-Erkrankungen hat widersprüchliche Ergebnisse erbracht. Es wurde ein umgekehrter Zusammenhang zwischen koronarer Herzkrankheit und dem Verzehr von Lebensmitteln mit hohem Vitamin-E-Gehalt sowie einer höheren Serumkonzentration von α-Tocopherol festgestellt. In einer der größten Beobachtungsstudien wurden fast 90.000 gesunde Krankenschwestern acht Jahre lang beobachtet. Verglichen mit dem untersten Fünftel der Personen, die über ihren Vitamin-E-Konsum (aus Lebensmitteln und Nahrungsergänzungsmitteln) berichteten, hatten die Personen im obersten Fünftel ein um 34 % geringeres Risiko für eine schwere Koronarerkrankung. Eine Ernährung mit einem höheren Vitamin-E-Gehalt könnte auch einen höheren Gehalt an anderen, noch nicht identifizierten Bestandteilen aufweisen, die die Herzgesundheit fördern, oder die Menschen, die sich für eine solche Ernährung entscheiden, treffen möglicherweise andere gesunde Lebensstilentscheidungen. Es gibt einige Belege aus randomisierten klinischen Studien (RCTs). Eine Metaanalyse über die Auswirkungen einer α-Tocopherol-Supplementierung in RCTs auf Aspekte der kardiovaskulären Gesundheit ergab, dass das relative Risiko eines Herzinfarkts um 18 % gesenkt wurde, wenn die Nahrung ohne andere antioxidative Nährstoffe eingenommen wurde. Die Ergebnisse waren nicht für alle in die Meta-Analyse einbezogenen Einzelstudien konsistent. So zeigte die Physicians' Health Study II nach acht Jahren mit 400 IE jeden zweiten Tag keinen Nutzen für Herzinfarkt, Schlaganfall, koronare Sterblichkeit oder Gesamtmortalität. Die Auswirkungen einer Vitamin-E-Supplementierung auf das Auftreten von Schlaganfällen wurden 2011 zusammengefasst. Es ergab sich kein signifikanter Nutzen von Vitamin E im Vergleich zu Placebo für das Schlaganfallrisiko oder für die Untergruppenanalyse für ischämische Schlaganfälle, hämorrhagische Schlaganfälle, tödliche Schlaganfälle oder nicht-tödliche Schlaganfälle. ⓘ
Im Jahr 2001 lehnte die US-Arzneimittelbehörde Food and Drug Administration vorgeschlagene gesundheitsbezogene Angaben zu Vitamin E und kardiovaskulärer Gesundheit ab. Die U.S. National Institutes of Health überprüften ebenfalls die Literatur und kamen zu dem Schluss, dass es keine ausreichenden Beweise dafür gibt, dass die routinemäßige Einnahme von Vitamin-E-Präparaten Herz-Kreislauf-Erkrankungen vorbeugt oder deren Morbidität und Mortalität verringert. Im Jahr 2010 überprüfte die Europäische Behörde für Lebensmittelsicherheit die Behauptungen, dass ein kausaler Zusammenhang zwischen der Aufnahme von Vitamin E über die Nahrung und der Aufrechterhaltung einer normalen Herzfunktion oder eines normalen Blutkreislaufs nachgewiesen wurde, und wies sie zurück. ⓘ
Schwangerschaft
Antioxidative Vitamine als Nahrungsergänzungsmittel wurden als vorteilhaft für die Einnahme in der Schwangerschaft vorgeschlagen. Was die Kombination von Vitamin E und Vitamin C als Nahrungsergänzung für Schwangere betrifft, so kam ein Cochrane-Review von 21 klinischen Studien zu dem Schluss, dass die Daten die Wirksamkeit einer Vitamin-E-Supplementierung - in der Mehrzahl der Studien α-Tocopherol in einer Dosierung von 400 IE/Tag plus Vitamin C in einer Dosierung von 1000 mg/Tag - im Hinblick auf die Verringerung des Risikos einer Totgeburt, des Todes von Neugeborenen, einer Frühgeburt, einer Präeklampsie oder anderer mütterlicher oder kindlicher Folgen nicht belegen, und zwar weder bei gesunden Frauen noch bei Frauen, die als Risikogruppe für Schwangerschaftskomplikationen gelten. Bei der Überprüfung wurden nur drei kleine Studien gefunden, in denen Vitamin E ohne gleichzeitige Gabe von Vitamin C supplementiert wurde. ⓘ
Topische Anwendung
Obwohl Vitamin E als topisches Medikament weit verbreitet ist und eine verbesserte Wundheilung und eine Verringerung des Narbengewebes angepriesen wird, sind Überprüfungen wiederholt zu dem Schluss gekommen, dass es keine ausreichenden Beweise für diese Behauptungen gibt. ⓘ
Nebeneffekte
Das U.S. Food and Nutrition Board hat eine tolerierbare Höchstmenge (UL) von 1.000 mg (1.500 IU) pro Tag festgelegt, die aus Tiermodellen abgeleitet wurde, die Blutungen bei hohen Dosen zeigten. Die Europäische Behörde für Lebensmittelsicherheit prüfte dieselbe Sicherheitsfrage und legte eine UL von 300 mg/Tag fest. Eine Meta-Analyse langfristiger klinischer Studien ergab einen nicht signifikanten Anstieg der Gesamtmortalität um 2 %, wenn nur α-Tocopherol eingenommen wurde. Eine andere Meta-Analyse ergab einen nicht signifikanten Anstieg der Gesamtmortalität um 1 %, wenn α-Tocopherol die einzige Nahrungsergänzung war. Eine Untergruppenanalyse ergab keinen Unterschied zwischen natürlichem (aus Pflanzen gewonnenem) und synthetischem α-Tocopherol, und auch nicht, ob die eingenommene Menge weniger oder mehr als 400 IE/Tag betrug. Es gibt Berichte über Vitamin-E-induzierte allergische Kontaktdermatitis durch die Verwendung von Vitamin-E-Derivaten wie Tocopheryllinoleat und Tocopherolacetat in Hautpflegeprodukten. Die Inzidenz ist trotz der weit verbreiteten Verwendung gering. ⓘ
Wechselwirkungen mit Arzneimitteln
Die Mengen an α-Tocopherol, anderen Tocopherolen und Tocotrienolen, die Bestandteile von Vitamin E in der Nahrung sind, scheinen keine Wechselwirkungen mit Arzneimitteln zu verursachen, wenn sie mit der Nahrung aufgenommen werden. Die Einnahme von α-Tocopherol als Nahrungsergänzungsmittel in Mengen von mehr als 300 mg/Tag kann zu Wechselwirkungen mit Aspirin, Warfarin, Tamoxifen und Cyclosporin A führen, die die Funktion verändern. Bei Aspirin und Warfarin können hohe Mengen an Vitamin E die blutgerinnungshemmende Wirkung verstärken. In einer kleinen Studie wurde nachgewiesen, dass Vitamin E in einer Dosierung von 400 mg/Tag die Blutkonzentration des Brustkrebsmedikaments Tamoxifen senkt. In mehreren klinischen Studien senkte Vitamin E die Blutkonzentration des Immunsuppressivums Cyclosporin A. Das U.S. National Institutes of Health, Office of Dietary Supplements, gibt zu bedenken, dass die gleichzeitige Verabreichung von Vitamin E die Mechanismen der Strahlen- und einiger Chemotherapien gegen Krebs beeinträchtigen könnte, und rät daher von der Verwendung bei diesen Patientengruppen ab. In den zitierten Quellen wird über Fälle berichtet, in denen die Nebenwirkungen der Behandlungen verringert wurden, aber auch über ein schlechteres Überleben der Krebspatienten, was die Möglichkeit eines Schutzes des Tumors vor den durch die Behandlungen beabsichtigten oxidativen Schäden aufwirft. ⓘ
Synthese
Natürlich vorkommendes d-α-Tocopherol kann aus Samenölen extrahiert und gereinigt werden, oder γ-Tocopherol kann extrahiert, gereinigt und methyliert werden, um d-alpha-Tocopherol zu erzeugen. Im Gegensatz zum aus Pflanzen gewonnenen α-Tocopherol, das auch als d-α-Tocopherol bezeichnet wird, entsteht bei der industriellen Synthese dl-α-Tocopherol. "Es wird aus einem Gemisch von Toluol und 2,3,5-Trimethyl-Hydrochinon synthetisiert, das mit Isophytol zu all-rac-α-Tocopherol reagiert, wobei Eisen in Gegenwart von Chlorwasserstoffgas als Katalysator verwendet wird. Das erhaltene Reaktionsgemisch wird filtriert und mit wässriger Natronlauge extrahiert. Toluol wird durch Eindampfen entfernt, und der Rückstand (alles rac-α-Tocopherol) wird durch Vakuumdestillation gereinigt." Die Spezifikation für den Inhaltsstoff ist >97% rein. Dieses synthetische dl-α-Tocopherol hat etwa 50 % der Wirksamkeit von d-α-Tocopherol. Die Hersteller von Nahrungsergänzungsmitteln und angereicherten Lebensmitteln für Menschen und Nutztiere wandeln die Phenolform des Vitamins entweder mit Essigsäure oder mit Bernsteinsäure in einen Ester um, da die Ester chemisch stabiler sind und eine längere Haltbarkeit bieten. Die Esterformen werden im Darm entestert und als freies α-Tocopherol absorbiert. ⓘ
Geschichte
Vitamin E wurde als „Fruchtbarkeits-Vitamin“ entdeckt und als „Fortpflanzungsvitamin“ sowie als „Antisterilitätsvitamin“ beschrieben. Herbert M. Evans und Katherine S. Bishop wiesen 1922 als erste auf einen bis dahin unbekannten fettlöslichen Faktor hin, der für die Reproduktion von Ratten notwendig war. In den Folgejahren wurde dieser Faktor in Form von α-Tocopherol vor allem aus Weizenkeimöl, Hafer und Mais isoliert, als Vitamin erkannt und aufgrund der bereits bekannten Vitamine A, B, C und D nun Vitamin „E“ genannt. Die antioxidative Wirkung wurde durch Harold S. Olcott und Oliver H. Emerson (Gladys Anderson Emersons Ehemann) 1937 beschrieben. 1938 wurde die Struktur von Vitamin E (hier α-Tocopherol) von Erhard Fernholz aufgeklärt, zudem kam es im gleichen Jahr zur ersten chemischen Synthese durch Paul Karrer. ⓘ
1968 wurde Vitamin E als essentieller Nährstoff durch das Food and Nutrition Board anerkannt. ⓘ
Beschreibung
Plastochromanol
Plastochromanole sind eine Gruppe von Molekülen die von Pflanzen gegen die Lipidperoxidation produziert werden und die mögliche prooxidative Aktivität von α-Tocopherol verhindern können. Bei γ-Tocotrienol handelt es sich um Plastochromanol-3. Plastochromanole kommen beispielsweise in Leinöl, Leindotteröl, Sacha Inchi und Arabidopsis vor. ⓘ
Aufgabe/Funktion im Körper

Eine seiner wichtigsten Funktionen ist die eines lipidlöslichen Antioxidans, das in der Lage ist, mehrfach ungesättigte Fettsäuren in Membranlipiden, Lipoproteinen und Depotfett vor einer Zerstörung durch Oxidation (Lipidperoxidation) zu schützen. Freie Radikale würden die Doppelbindungen der Fettsäuren der Zell- und Organellmembranen angreifen. Tocopherol wirkt als Radikalfänger, indem es selbst zu einem reaktionsträgen, da mesomeriestabilisierten Radikal wird. Das Tocopherol-Radikal wird dann unter Bildung eines Ascorbatradikals reduziert. Das Ascorbatradikal wird mit Hilfe von Glutathion (GSH) regeneriert. Dabei werden zwei Monomere (GSH) zu einem Dimer (GSSG) oxidiert. ⓘ
Vitamin E hat Funktionen in der Steuerung der Keimdrüsen und wird daher auch als Antisterilitätsvitamin bezeichnet. ⓘ
Der menschliche Körper kann am besten (RRR)-α-Tocopherol speichern und transportieren. Der Grund hierfür: Das in der Leber befindliche α-Tocopherol-Transfer-Protein (α-TTP), welches für den Transport des Vitamin E via VLDL in den Blutkreislauf verantwortlich ist, hat die höchste Affinität zum natürlichen α-Tocopherol. Durch die Speicherkapazität kann eine einmalige Gabe für längere Zeit wirken. Das im Wesentlichen in Sojaprodukten vorkommende γ-Tocopherol zeigt eine geringere Aktivität. Neuerdings wird aber diskutiert, ob diesem eine besondere Rolle zugeschrieben werden muss. In humanem LDL, einem Lipoprotein, sind α-Tocopherol und in geringer Konzentration auch γ-Tocopherol vorhanden. ⓘ
Die biologische Aktivität unterscheidet sich unter den Vitameren. Bezogen auf α-Tocopherol (100 %) weist β-Tocopherol 50 %, γ-Tocopherol 10 %, δ-Tocopherol 3 %, α-Tocotrienol 30 % und β-Tocotrienol 5 % der Aktivität auf. ⓘ
Besondere Eigenschaften von α-Tocopherol
α-Tocopherol, das am meisten verwendete und auch synthetisch hergestellte Isomer von Vitamin E hat einige positive und weniger positive Eigenschaften im Vergleich zu anderen Tocochromanolen:
- Es wird vom Transportprotein TTP in Säugetieren bevorzugt transportiert und in der Leber gespeichert.
- Es kann sogar pro-oxidativ wirken, also die Haltbarkeit von Lipiden (Speiseölen) verschlechtern. Diese pro-oxidative Wirkung wird von Plastochromanolen verhindert.
- Während sehr geringe Mengen die Cholesterinproduktion leicht drosseln, bewirken größere Mengen (im Tierversuch bei Meerschweinchen ab 5 mg/d) eine deutliche Steigerung des Plasma-Cholesterins.
- Die cholesterinsenkende Eigenschaft von Tocotrienolen wird durch alpha-Tocopherol stark reduziert. ⓘ
Bedarf
Der Mindestbedarf an Vitamin E beträgt 4 mg/d, zuzüglich etwa 0,4 mg pro Gramm Zufuhr an mehrfach ungesättigten Fettsäuren. Um die von verschiedenen Autoren als protektiv angesehenen Plasmaspiegel zu erreichen, ist eine Zufuhr von 20 bis 35 mg/d erforderlich. Aufgrund der geringen Toxizität werden teilweise Dosierungen von 268 mg/d empfohlen. Der Plasmaspiegel sollte oberhalb von 30 µmol/l liegen (bei einem Cholesterinwert von 220 mg/dl). ⓘ
Mangelerscheinungen beim Menschen (Hypovitaminosen) sind heutzutage in Europa sehr selten, da Tocopherol sehr gut in der Leber und im Fettgewebe gespeichert werden kann. Nachgewiesene Mangelerscheinungen treten meist nur im Zusammenhang mit Krankheiten wie z. B. einer exokrinen Pankreasinsuffizienz oder einer Verminderung des Gallenflusses auf, bei denen gleichzeitig die Aufnahme von Fetten gestört ist. ⓘ
Genauso wie die fettlöslichen Vitamine Vitamin A, Vitamin D und Vitamin K werden (RRR)-α-Tocopherol und die (2R)-Stereoisomere [(RSR)-, (RRS)- und (RSS)-α-Tocopherol] im Fettgewebe bzw. Blutplasma des Körpers angereichert. Die synthetisch hergestellten (2S)-Stereoisomere [(SRR)-, (SSR)-, (SRS)- und (SSS)-α-Tocopherol] werden hingegen nicht im Blutplasma gespeichert. ⓘ
Das BfR hat auf Basis der sogenannten akzeptablen täglichen Aufnahmemenge (Acceptable Daily Intake, ADI) bei 0,15–2 mg/kg Körpergewicht neue Grenzen für eine akzeptable Tagesaufnahmemenge festgelegt. Bei einem Referenzkörpergewicht für Erwachsene von 70 kg entspricht diese 105–140 mg Vitamin E. Jugendliche der Altersgruppe der 15- bis 17-Jährigen haben ein Referenzgewicht von 61,3 kg, wodurch die tägliche Aufnahme von 92–123 mg Vitamin E als akzeptabel bewertet wird. ⓘ
Das BfR schlägt für Nahrungsergänzungsmittel eine Höchstmenge von 30 mg pro Tag vor, warnt aber davor, dass bei Männern ab 55 Jahren bei einer unkontrollierten Supplementierung das Risiko für Prostatakrebs erhöht werden kann. ⓘ
Verwendung
Tocopherole finden in der Lebensmittelindustrie als Antioxidationsmittel Verwendung. Sie sind in der EU als Lebensmittelzusatzstoffe der Nummern E 306 (Tocopherol-haltige Extrakte), E 307 (Alpha-), E 308 (Gamma-) und E 309 (Delta-Tocopherol) für alle für Zusatzstoffe zugelassenen Nahrungsmittel, zum Teil (in Form von tocopherolhaltigen Extrakten natürlichen Ursprungs) auch für „Bio“-Lebensmittel (E 306), zugelassen. ⓘ
Neben Lebensmitteln wird Vitamin E auch Kosmetika (Sonnenschutzmitteln) und Anstrichmitteln zugesetzt sowie in künstlichen Gelenken zur höheren Beständigkeit gegen die Oxidation des verwendeten Kunststoffs. Bei Kondomen soll eine Vitamin-E-Beschichtung u. a. die Reißfestigkeit erhöhen. ⓘ
Auch im Adjuvans AS03 in COVID-19-Impfstoffen findet DL-α-Tocopherol Verwendung. ⓘ
Mit Sebacinsäure und Polyethylenglycol verestert erhält man das nichtionische Tensid Polyoxyethanyl-α-tocopherylsebacat (PTS), das als Hilfsmittel bei der Phasentransferkatalyse eingesetzt werden kann. ⓘ
Analytik
Die heute fast ausschließlich eingesetzten Methoden zur zuverlässigen qualitativen und quantitativen Bestimmung der einzelnen Tocopherole sind die HPLC, die Gaschromatographie und die Kopplungsverfahren der HPLC-MS und der GC/MS. Beide Verfahren werden sowohl in der lebensmittelchemischen Analytik als auch bei pharmazeutischen und physiologischen Fragestellungen verwandt. Das Massenspektrum des Tocopherols findet sich auch in der Spektrenbibliothek des NIST. In Abhängigkeit von den zu untersuchenden Matrices empfehlen sich adäquate Probenvorbereitungsverfahren wie z. B. Extraktionsmethoden, auch unter Einsatz von Festphasenextraktionssäulen oder anderen Extraktionshilfsmitteln wie z. B. dem aus Diatomeenerde hergestellten Extrelut. Die früher häufig eingesetzten photometrischen Verfahren finden fast keine Verwendung mehr, da sie in der Regel keine Unterscheidung der einzelnen Tocopherole zulassen. Stereoisomere racemischen alpha-Tocopherols lassen sich sowohl durch HPLC als auch durch Gaschromatographie trennen. ⓘ
