Polioimpfstoff
 | |
| Beschreibung des Impfstoffs | |
|---|---|
| Ziel | Poliomyelitis |
| Typ des Impfstoffs | IPV: inaktiviert OPV: abgeschwächt |
| Klinische Daten | |
| Handelsnamen | Ipol, Poliovax, andere |
| AHFS/Drugs.com | Monographie |
| MedlinePlus | a601177 |
| Lizenz-Daten |
|
| Schwangerschaft Kategorie |
|
| Wege der Verabreichung | IPV: parenteral OPV: oral |
| ATC-Code |
|
| Rechtlicher Status | |
| Rechtlicher Status |
|
| Kennzeichnungsmittel | |
| CAS-Nummer | |
| DrugBank | |
| ChemSpider |
|
| | |
Polioimpfstoffe sind Impfstoffe, die zur Vorbeugung von Poliomyelitis (Kinderlähmung) eingesetzt werden. Es werden zwei Arten verwendet: ein inaktiviertes Poliovirus, das durch Injektion verabreicht wird (IPV), und ein abgeschwächtes Poliovirus, das durch den Mund verabreicht wird (OPV). Die Weltgesundheitsorganisation (WHO) empfiehlt, dass alle Kinder vollständig gegen Polio geimpft werden. Die beiden Impfstoffe haben die Kinderlähmung in den meisten Teilen der Welt ausgerottet und die Zahl der jährlich gemeldeten Fälle von schätzungsweise 350.000 im Jahr 1988 auf 33 im Jahr 2018 gesenkt. ⓘ
Die inaktivierten Polioimpfstoffe sind sehr sicher. An der Injektionsstelle können leichte Rötungen oder Schmerzen auftreten. Orale Polioimpfstoffe verursachen etwa drei Fälle von impfstoffassoziierter paralytischer Poliomyelitis pro Million verabreichter Dosen. Demgegenüber stehen 5.000 Fälle pro Million Menschen, die nach einer Polio-Infektion gelähmt sind. Beide Arten von Impfstoffen sind im Allgemeinen sicher, wenn sie während der Schwangerschaft und bei HIV/AIDS-Kranken verabreicht werden, die ansonsten gesund sind. Das Auftreten des zirkulierenden impfstoffabgeleiteten Poliovirus (cVDPV), einer Form des Impfvirus, die wieder Poliomyelitis auslöst, hat jedoch zur Entwicklung des neuartigen oralen Polioimpfstoffs Typ 2 (nOPV2) geführt, der den Impfstoff sicherer machen und damit weitere Ausbrüche von cVDPV2 verhindern soll. ⓘ
Die erste erfolgreiche Demonstration eines Polio-Impfstoffs wurde 1950 von Hilary Koprowski mit einem abgeschwächten Lebendvirus durchgeführt, das die Menschen tranken. Der Impfstoff wurde in den Vereinigten Staaten nicht zugelassen, wurde aber in anderen Ländern erfolgreich eingesetzt. Der Erfolg eines von Jonas Salk entwickelten inaktivierten (abgetöteten) Polio-Impfstoffs wurde 1955 bekannt gegeben. Ein weiterer attenuierter oraler Polio-Lebendimpfstoff wurde von Albert Sabin entwickelt und kam 1961 auf den Markt. ⓘ
Der Polioimpfstoff steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation. ⓘ
Zur Grundimmunisierung von Kindern und Jugendlichen wird in Deutschland seit 1998 nur noch der inaktivierte Polioimpfstoff eingesetzt. Die Weltgesundheitsorganisation (WHO) hat mit einigen anderen Organisationen das Ziel, im Rahmen der 1988 beschlossenen Global Polio Eradication Initiative (GPEI) das Poliovirus vor allem durch Impfungen mit OPV und abschließender Umstellung auf IPV weltweit auszurotten. ⓘ
Medizinische Anwendungen

Die Unterbrechung der Übertragung des Virus von Mensch zu Mensch durch die Impfung ist für die weltweite Ausrottung der Kinderlähmung von großer Bedeutung, da es bei Personen mit normaler Immunfunktion keinen langfristigen Überträgerstatus für Polioviren gibt, Polioviren in der Natur kein Reservoir für Nichtprimaten haben und ein Überleben des Virus in der Umwelt über einen längeren Zeitraum unwahrscheinlich erscheint. Es gibt zwei Arten von Impfstoffen: inaktivierter Polioimpfstoff (IPV) und oraler Polioimpfstoff (OPV). ⓘ
Zur Herstellung der IPV werden vermehrungsfähige Viren verwendet. Dementsprechend hoch sind die Sicherheitsanforderungen an die Impfstoffhersteller. Die WHO empfiehlt für die Zeit nach der Ausrottung des Wildvirus für IPV-Herstellungseinrichtungen die Biologische Schutzstufe 3/Polio. Eine mögliche Lösung für dieses Problem könnte die Verwendung von attenuierten Viren zur Herstellung des inaktivierten Polioimpfstoffs sein. ⓘ
Inaktiviert
Bei Verwendung des IPV (Injektion) entwickeln 90 % oder mehr der Personen nach zwei Dosen des inaktivierten Polioimpfstoffs (IPV) schützende Antikörper gegen alle drei Serotypen des Poliovirus, und mindestens 99 % sind nach drei Dosen immun gegen das Poliovirus. Die Dauer der durch IPV hervorgerufenen Immunität ist nicht mit Sicherheit bekannt, obwohl man davon ausgeht, dass eine vollständige Impfserie über viele Jahre hinweg Schutz bietet. Die IPV hat in den 1990er Jahren in vielen Industrieländern den Schluckimpfstoff ersetzt, vor allem wegen des (geringen) Risikos, dass der Schluckimpfstoff das Polio-Virus enthält. ⓘ
Abgeschwächte
Schluckimpfstoffe waren einfacher zu verabreichen als IPV, da keine sterilen Spritzen benötigt wurden und sie sich daher besser für Massenimpfkampagnen eigneten. OPV bietet auch eine länger anhaltende Immunität als der Salk-Impfstoff, da er sowohl eine humorale als auch eine zellvermittelte Immunität vermittelt. ⓘ
Eine Dosis OPV bewirkt bei etwa 50 % der Geimpften eine Immunität gegen alle drei Serotypen des Poliovirus. Drei Dosen des abgeschwächten Lebendimpfstoffs OPV erzeugen bei mehr als 95 % der Empfänger schützende Antikörper gegen alle drei Poliovirustypen. OPV erzeugt eine ausgezeichnete Immunität im Darm, dem primären Eintrittsort des Polio-Wildvirus, was dazu beiträgt, eine Infektion mit dem Wildvirus in Gebieten, in denen das Virus endemisch ist, zu verhindern. Das im Impfstoff verwendete Lebendvirus wird nur selten über den Stuhl ausgeschieden und kann nur selten auf andere Personen innerhalb einer Gemeinschaft übertragen werden. Das Lebendvirus stellt außerdem strenge Anforderungen an Transport und Lagerung, was in einigen heißen oder abgelegenen Gebieten ein Problem darstellt. Wie bei anderen Lebendvirusimpfstoffen ist die durch OPV ausgelöste Immunität wahrscheinlich lebenslang. ⓘ
Mit dem trivalenten OPV (gegen die Wildtypen 1, 2 und 3) konnte die Polioinfektion weltweit nahezu ausgerottet werden. Unter der Leitung der Globalen Initiative zur Ausrottung der Kinderlähmung haben 155 Länder zwischen dem 17. April und dem 1. Mai 2016 auf die Verwendung des bivalenten Impfstoffs (gegen die Wildtypen 1 und 3) umgestellt. Die bivalente OPV ist wirksamer gegen die Typen 1 und 3, deckt aber nicht den Typ 2 ab. Die Vereinigten Staaten empfehlen ab 2017 weiterhin die Verwendung einer trivalenten Version, allerdings einer vollständig inaktivierten Version. Die Umstellung auf den bivalenten Impfstoff und die damit verbundene fehlende Immunität gegen Stämme des Typs 2 führten neben anderen Faktoren zu Ausbrüchen des zirkulierenden, aus dem Impfstoff abgeleiteten Poliovirus Typ 2 (cVDPV2), die von zwei Fällen im Jahr 2016 auf 1037 Fälle im Jahr 2020 anstiegen. Als Reaktion darauf wurde ein neuartiger oraler Polioimpfstoff Typ 2 (nOPV2) entwickelt, der eine sicherere Form der Impfung gegen Typ-2-Stämme mit geringerem Risiko eines Rückfalls in die infektiöse Kinderlähmung bieten soll. ⓘ
Zeitplan

In Ländern, in denen Polio endemisch ist oder in denen ein hohes Risiko für importierte Fälle besteht, empfiehlt die WHO die OPV-Impfung bei der Geburt, gefolgt von einer Primärserie von drei OPV-Dosen und mindestens einer IPV-Dosis ab einem Alter von sechs Wochen, wobei zwischen den OPV-Dosen mindestens vier Wochen liegen sollten. In Ländern mit einem Durchimpfungsgrad von mehr als 90 % und einem geringen Risiko der Einschleppung empfiehlt die WHO eine oder zwei IPV-Dosen ab dem zweiten Lebensmonat, gefolgt von mindestens zwei OPV-Dosen, wobei die Dosen je nach Expositionsrisiko im Abstand von 4 bis 8 Wochen verabreicht werden sollten. In Ländern mit dem höchsten Durchimpfungsgrad und dem geringsten Risiko der Einschleppung und Übertragung empfiehlt die WHO eine Primärserie von drei IPV-Injektionen mit einer Auffrischungsdosis nach einem Abstand von sechs Monaten oder mehr, wenn die erste Dosis vor dem zweiten Lebensmonat verabreicht wurde. ⓘ
Nebeneffekte
Die inaktivierten Polioimpfstoffe sind sehr sicher. An der Injektionsstelle können leichte Rötungen oder Schmerzen auftreten. Der orale Polioimpfstoff führt bei etwa drei von einer Million Dosen zu einer impfstoffassoziierten paralytischen Poliomyelitis. Die Verabreichung an Schwangere und HIV/AIDS-Infizierte, die ansonsten gesund sind, ist im Allgemeinen unbedenklich. ⓘ
Allergische Reaktion auf den Impfstoff
Inaktivierter Polio-Impfstoff kann bei einigen wenigen Personen eine allergische Reaktion hervorrufen, da der Impfstoff Spuren von Antibiotika, Streptomycin, Polymyxin B und Neomycin enthält. Der Impfstoff sollte nicht an Personen verabreicht werden, die allergisch auf diese Arzneimittel reagieren. Zu den Anzeichen und Symptomen einer allergischen Reaktion, die in der Regel innerhalb von Minuten oder wenigen Stunden nach der Injektion des Impfstoffs auftreten, gehören Atembeschwerden, Schwäche, Heiserkeit oder Keuchen, Schwankungen des Herzschlags, Hautausschlag und Schwindelgefühl. ⓘ
Durch Impfung verursachte Polio
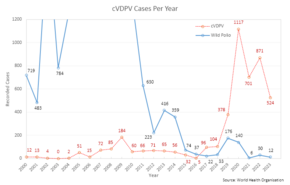
Eine potenzielle, negative Auswirkung der OPV ist ihre bekannte Fähigkeit, sich zu einer Form zu rekombinieren, die neurologische Infektionen und Lähmungen verursacht. Diese genetische Umkehrung des Erregers in eine virulente Form dauert eine beträchtliche Zeit (mindestens 12 Monate) und betrifft nicht die Person, die ursprünglich geimpft wurde. Das aus dem Impfstoff stammende abgeschwächte Virus wird normalerweise von geimpften Personen für einen begrenzten Zeitraum ausgeschieden. In Gebieten mit schlechter Hygiene und geringer Durchimpfungsrate kann daher die spontane Umwandlung des aus dem Impfstoff stammenden Virus in eine virulente Form und seine Verbreitung in der Umwelt dazu führen, dass sich ungeimpfte Personen infizieren. Klinische Erkrankungen, einschließlich Lähmungen, die durch geimpfte Polioviren (VDPV) verursacht werden, sind nicht von denen zu unterscheiden, die durch Polio-Wildviren verursacht werden. Ausbrüche der impfstoffassoziierten paralytischen Poliomyelitis (VAPP), die durch ein zirkulierendes impfstoffabgeleitetes Poliovirus (cVDPV) verursacht wird, wurden gemeldet und treten in der Regel in Gebieten mit geringer OPV-Abdeckung auf, vermutlich weil das OPV selbst gegen den entsprechenden Ausbruchsstamm schützt. Da sich die Zahl der Polio-Wildviren auf einem Rekordtief befindet, wurden 2017 erstmals mehr Fälle von cVDPV als von Polio-Wildviren gemeldet - ein Trend, der sich voraussichtlich fortsetzen wird. ⓘ
Um dem entgegenzuwirken, beschloss die WHO 2016, vom dreiwertigen Polioimpfstoff auf den zweiwertigen Polioimpfstoff umzustellen. Dieser Impfstoff enthält das Polio-Virus vom Typ 2 nicht mehr, da es 1999 ausgerottet wurde. ⓘ
Bedenken wegen Kontamination
1960 wurde festgestellt, dass die Nierenzellen von Rhesusaffen, die zur Herstellung der Polioimpfstoffe verwendet wurden, mit dem ebenfalls 1960 entdeckten Simian-Virus-40 (SV40) infiziert waren, einem natürlich vorkommenden Virus, das Affen infiziert. Im Jahr 1961 wurde festgestellt, dass SV40 bei Nagetieren Tumore verursacht. In jüngerer Zeit wurde das Virus bei bestimmten Krebsarten beim Menschen gefunden, z. B. bei Hirn- und Knochentumoren, Pleura- und Peritonealmesotheliom und einigen Arten von Non-Hodgkin-Lymphomen. Es wurde jedoch nicht nachgewiesen, dass SV40 diese Krebsarten verursacht. ⓘ
SV40 wurde in Beständen der injizierten Form der IPV gefunden, die zwischen 1955 und 1963 verwendet wurde. In der OPV-Form ist es nicht enthalten. Mehr als 98 Millionen Amerikaner erhielten zwischen 1955 und 1963 eine oder mehrere Dosen Polioimpfstoff, wobei ein Teil des Impfstoffs mit SV40 kontaminiert war; schätzungsweise 10-30 Millionen Amerikaner könnten eine mit SV40 kontaminierte Impfstoffdosis erhalten haben. Spätere Analysen ergaben, dass Impfstoffe, die von den Ländern des ehemaligen Sowjetblocks bis 1980 hergestellt und in der UdSSR, China, Japan und mehreren afrikanischen Ländern verwendet wurden, kontaminiert gewesen sein könnten, was bedeutet, dass Hunderte von Millionen weiterer Menschen mit SV40 in Kontakt gekommen sein könnten. ⓘ
Im Jahr 1998 führte das National Cancer Institute eine große Studie durch, bei der Informationen über Krebsfälle aus der SEER-Datenbank des Instituts verwendet wurden. Die veröffentlichten Ergebnisse der Studie ergaben keine erhöhte Krebshäufigkeit bei Personen, die möglicherweise einen SV40-haltigen Impfstoff erhalten hatten. In einer weiteren großen Studie in Schweden wurden die Krebsraten von 700 000 Personen untersucht, die noch 1957 einen potenziell kontaminierten Polioimpfstoff erhalten hatten; auch diese Studie ergab keine erhöhte Krebshäufigkeit bei Personen, die SV40-haltige Polioimpfstoffe erhalten hatten, und solchen, die dies nicht taten. Die Frage, ob SV40 beim Menschen Krebs verursacht, bleibt jedoch umstritten, und die Entwicklung verbesserter Tests zum Nachweis von SV40 in menschlichem Gewebe wird erforderlich sein, um die Kontroverse zu lösen. ⓘ

Während des Wettlaufs um die Entwicklung eines oralen Polio-Impfstoffs wurden mehrere groß angelegte Versuche am Menschen durchgeführt. Bis 1958 hatten die National Institutes of Health festgestellt, dass die mit den Sabin-Stämmen hergestellten OPV am sichersten waren. Zwischen 1957 und 1960 setzte Hilary Koprowski jedoch die Verabreichung seines Impfstoffs in der ganzen Welt fort. In Afrika wurden die Impfstoffe etwa einer Million Menschen in den belgischen Gebieten (der heutigen Demokratischen Republik Kongo, Ruanda und Burundi) verabreicht. Die Ergebnisse dieser Versuche am Menschen waren umstritten, und in den 1990er Jahren kamen unbegründete Anschuldigungen auf, der Impfstoff habe die Voraussetzungen für die Übertragung des Affen-Immunschwäche-Virus von Schimpansen auf Menschen geschaffen und damit HIV/AIDS verursacht. Diese Hypothesen konnten jedoch eindeutig widerlegt werden. Bis 2004 waren die Fälle von Poliomyelitis in Afrika auf einige wenige isolierte Regionen im westlichen Teil des Kontinents und sporadische Fälle in anderen Regionen zurückgegangen. In jüngster Zeit hat sich auf lokaler Ebene Widerstand gegen die Impfkampagnen entwickelt, der auf einen Mangel an angemessenen Informationen zurückzuführen ist und häufig mit der Befürchtung zusammenhängt, der Impfstoff könne zu Sterilität führen. Seitdem ist die Krankheit in Nigeria und in mehreren anderen afrikanischen Ländern wieder aufgetreten, ohne dass die erforderlichen Informationen zur Verfügung standen, was nach Ansicht von Epidemiologen darauf zurückzuführen ist, dass sich bestimmte Bevölkerungsgruppen weigerten, ihre Kinder gegen Polio impfen zu lassen. ⓘ
Herstellung
Inaktiviert
Der Salk-Impfstoff, IPV, basiert auf drei wilden, virulenten Referenzstämmen, Mahoney (Polio-Virus Typ 1), MEF-1 (Polio-Virus Typ 2) und Saukett (Polio-Virus Typ 3), die in einer Art Gewebekultur aus Affennieren (Vero-Zelllinie) gezüchtet und anschließend mit Formalin inaktiviert werden. Der injizierte Salk-Impfstoff verleiht eine IgG-vermittelte Immunität in der Blutbahn, die verhindert, dass die Polio-Infektion zu einer Virämie fortschreitet, und die Motoneuronen schützt, wodurch das Risiko einer bulbären Polio und eines Post-Polio-Syndroms ausgeschlossen wird. ⓘ
In den Vereinigten Staaten wird der Impfstoff zusammen mit den Impfstoffen gegen Tetanus, Diphtherie und azelluläre Keuchhusten (DTaP) und einer pädiatrischen Dosis des Hepatitis-B-Impfstoffs verabreicht. Im Vereinigten Königreich wird IPV mit den Impfstoffen gegen Tetanus, Diphtherie, Pertussis und Haemophilus influenzae Typ b kombiniert. ⓘ
Abgeschwächte


OPV ist ein abgeschwächter Impfstoff, der durch die Passage des Virus durch nicht-menschliche Zellen bei subphysiologischer Temperatur hergestellt wird, wodurch spontane Mutationen im viralen Genom entstehen. Orale Polioimpfstoffe wurden von mehreren Gruppen entwickelt, von denen eine von Albert Sabin geleitet wurde. Andere Gruppen unter der Leitung von Hilary Koprowski und H.R. Cox entwickelten ihre eigenen abgeschwächten Impfstämme. Im Jahr 1958 richteten die National Institutes of Health einen Sonderausschuss für Polio-Lebendimpfstoffe ein. Die verschiedenen Impfstoffe wurden sorgfältig auf ihre Fähigkeit geprüft, eine Immunität gegen Polio zu erzeugen und gleichzeitig eine geringe Inzidenz der Neuropathogenität bei Affen zu gewährleisten. Groß angelegte klinische Versuche, die Ende der 1950er bis Anfang der 1960er Jahre in der Sowjetunion von Michail Tschumakow und seinen Kollegen durchgeführt wurden, zeigten die Sicherheit und hohe Wirksamkeit des Impfstoffs. Auf der Grundlage dieser Ergebnisse wurden die Sabin-Stämme für die weltweite Verbreitung ausgewählt. Siebenundfünfzig Nukleotid-Substitutionen unterscheiden den abgeschwächten Sabin-1-Stamm von seinem virulenten Elternteil (dem Mahoney-Serotyp), zwei Nukleotid-Substitutionen schwächen den Sabin-2-Stamm ab, und 10 Substitutionen sind an der Abschwächung des Sabin-3-Stammes beteiligt. Der wichtigste Abschwächungsfaktor, der allen drei Sabin-Impfstoffen gemeinsam ist, ist eine Mutation an der internen Ribosomen-Eintrittsstelle des Virus, die die Struktur der Stammschleife verändert und die Fähigkeit des Poliovirus zur Übersetzung seiner RNA-Vorlage in der Wirtszelle verringert. Das abgeschwächte Poliovirus im Sabin-Impfstoff repliziert sich sehr effizient im Darm, dem Hauptinfektions- und Replikationsort, ist aber nicht in der Lage, sich effizient im Gewebe des Nervensystems zu replizieren. 1961 wurde der monovalente orale Poliovirus-Impfstoff (MOPV) der Typen 1 und 2 und 1962 der MOPV des Typs 3 zugelassen. Im Jahr 1963 wurde trivalenter OPV (TOPV) zugelassen, der in den Vereinigten Staaten und den meisten anderen Ländern der Welt zum Impfstoff der Wahl wurde und den inaktivierten Polioimpfstoff weitgehend ersetzte. Eine zweite Welle von Massenimpfungen führte zu einem weiteren dramatischen Rückgang der Zahl der Poliofälle. Zwischen 1962 und 1965 wurden rund 100 Millionen Amerikaner (etwa 56 % der damaligen Bevölkerung) mit dem Sabin-Impfstoff geimpft. Das Ergebnis war ein erheblicher Rückgang der Zahl der Poliomyelitis-Fälle, sogar im Vergleich zu den stark gesunkenen Zahlen nach der Einführung des Salk-Impfstoffs. ⓘ
OPV wird in der Regel in Fläschchen mit 10-20 Impfstoffdosen geliefert. Eine Einzeldosis Polio-Schluckimpfstoff (in der Regel zwei Tropfen) enthält 1 000 000 infektiöse Einheiten des Sabin-1-Stammes (wirksam gegen PV1), 100 000 infektiöse Einheiten des Sabin-2-Stammes und 600 000 infektiöse Einheiten des Sabin-3-Stammes. Der Impfstoff enthält geringe Spuren von Antibiotika - Neomycin und Streptomycin -, aber keine Konservierungsstoffe. ⓘ
Geschichte
Im allgemeinen Sinne funktioniert die Impfung durch die Aktivierung des Immunsystems mit einem "Immunogen". Die Stimulierung der Immunreaktion durch einen infektiösen Erreger wird als Immunisierung bezeichnet. Die Entwicklung einer Immunität gegen Polio blockiert wirksam die Übertragung des Polio-Wildvirus von Mensch zu Mensch und schützt so sowohl den einzelnen Geimpften als auch die Allgemeinheit. ⓘ
Die Entwicklung von zwei Polio-Impfstoffen führte zu den ersten modernen Massenimpfungen. Die letzten Fälle von paralytischer Poliomyelitis, die durch eine endemische Übertragung des Wildvirus in den Vereinigten Staaten verursacht wurden, traten 1979 bei einem Ausbruch unter den Amischen in mehreren Staaten des Mittleren Westens auf. ⓘ
1930s
In den 1930er Jahren wurde das Poliovirus als besonders furchteinflößend empfunden, da nur wenig darüber bekannt war, wie die Krankheit übertragen wurde oder wie sie verhindert werden konnte. Da das Virus vor allem wohlhabende Kinder befiel, war es trotz seiner relativ geringen Sterblichkeit und Morbidität ein bevorzugtes Ziel für die Entwicklung von Impfstoffen. Trotzdem hatte die Gemeinschaft der Forscher auf diesem Gebiet bis dahin weitgehend ein informelles Moratorium für die Entwicklung von Impfstoffen eingehalten, da sie als zu großes Risiko mit zu geringen Erfolgsaussichten angesehen wurde. ⓘ
Dies änderte sich in den frühen 1930er Jahren, als amerikanische Gruppen die Herausforderung annahmen: Maurice Brodie leitete ein Team des öffentlichen Gesundheitslabors der Stadt New York und Dr. John A. Kolmer arbeitete mit dem Research Institute of Cutaneous Medicine in Philadelphia zusammen. Die Rivalität zwischen diesen beiden Forschern führte zu einer rassistischen Mentalität, die sich in Verbindung mit der mangelnden Kontrolle medizinischer Studien in der Methodik und den Ergebnissen dieser frühen Impfstoffentwicklungen niederschlug. ⓘ
Kolmers Lebendimpfstoff
Kolmer begann sein Impfstoffentwicklungsprojekt im Jahr 1932 und konzentrierte sich letztlich auf die Herstellung eines Impfstoffs mit abgeschwächten oder lebenden Viren. Inspiriert durch den Erfolg von Impfstoffen gegen Tollwut und Gelbfieber, hoffte er, das Poliovirus mit einem ähnlichen Verfahren denaturieren zu können. Um seinen Polio-Impfstoff zu attenuieren, ließ er das Virus wiederholt durch Affen laufen. Mit Produktionsmethoden, die später als "haarsträubend dilettantisch, das therapeutische Äquivalent von Badewannen-Gin" beschrieben wurden, zermahlte Kolmer die Rückenmarkshäute seiner infizierten Affen und tauchte sie in eine Salzlösung. Anschließend filterte er die Lösung durch ein Sieb, behandelte sie mit Ricinolat und kühlte das Produkt 14 Tage lang, um schließlich etwas herzustellen, das später als "wahres Hexengebräu" kritisiert wurde. ⓘ
Wie damals üblich, führte Kolmer zunächst einen relativ kleinen Tierversuch mit 42 Affen durch, bevor er 1934 zum Selbstversuch überging. Er testete seinen Impfstoff an sich selbst, seinen beiden Kindern und seiner Assistentin. Er verabreichte seinen Impfstoff nur noch 23 weiteren Kindern, bevor er ihn für sicher erklärte und ihn an Ärzte und Gesundheitsämter für einen größeren Wirksamkeitstest verschickte. Im April 1935 konnte er berichten, dass er den Impfstoff an 100 Kindern getestet hatte, ohne dass es zu Beeinträchtigungen gekommen war. Kolmers erste offizielle Präsentation der Ergebnisse erfolgte erst im November 1935, als er die Ergebnisse von 446 Kindern und Erwachsenen vorstellte, die er mit seinem attenuierten Impfstoff geimpft hatte. Er berichtete auch, dass das Research Institute of Cutaneous Medicine und die Merrell Company of Cincinnati (der Hersteller, der das Patent für sein Ricinoleating-Verfahren besaß) zusammen 12.000 Dosen des Impfstoffs an etwa 700 Ärzte in den Vereinigten Staaten und Kanada verteilt hatten. Kolmer beschrieb weder eine Überwachung dieses experimentellen Impfprogramms noch gab er diesen Ärzten Anweisungen zur Verabreichung des Impfstoffs oder zur Meldung von Nebenwirkungen. Kolmer widmete den Großteil seiner Veröffentlichungen danach der Erklärung dessen, was er für die Ursache der mehr als 10 gemeldeten Fälle von paralytischer Polio nach der Impfung hielt, in vielen Fällen in Städten, in denen es keinen Polioausbruch gegeben hatte. Sechs dieser Fälle waren tödlich verlaufen. Kolmer hatte keine Kontrollgruppe, behauptete aber, dass viel mehr Kinder erkrankt wären. ⓘ
Der inaktivierte Impfstoff von Brodie
Fast zur gleichen Zeit wie Kolmers Projekt hatte sich Maurice Brodie dem Immunologen Dr. William H. Park im Gesundheitsamt der Stadt New York angeschlossen, wo sie gemeinsam am Poliovirus arbeiteten. Mit Hilfe von Zuschüssen der President's Birthday Ball Commission (einem Vorläufer des späteren March of Dimes) konnte Brodie die Entwicklung eines inaktivierten oder "abgetöteten" Impfstoffs vorantreiben. Auch Brodie begann mit der Zerkleinerung des Rückenmarks infektiöser Affen und der anschließenden Behandlung mit verschiedenen Bakteriziden, wobei sich eine Formaldehydlösung als am wirksamsten erwies. Am 1. Juni 1934 konnte Brodie seinen ersten wissenschaftlichen Artikel veröffentlichen, in dem er beschrieb, wie er bei drei Affen mit inaktivierten Polio-Viren erfolgreich eine Immunität herbeiführte. Nach weiteren Untersuchungen an 26 Affen kam Brodie schließlich zu dem Schluss, dass die Verabreichung von Lebendvirus-Impfstoffen eher zu einer humoralen Immunität führte, während die Verabreichung von Impfstoffen mit abgetöteten Viren eher zu einer Gewebeimmunität führte. ⓘ
Bald darauf führte Brodie nach einem ähnlichen Protokoll wie Kolmer Selbstversuche an sich selbst und seinen Mitarbeitern im Labor des New Yorker Gesundheitsamtes durch. Über Brodies Fortschritte wurde in der Presse eifrig berichtet, da die Öffentlichkeit auf einen erfolgreichen Impfstoff hoffte. In diesen Berichten wurden die 12 Kinder in einem New Yorker Asyl nicht erwähnt, die frühen Sicherheitstests unterzogen wurden. Da bei keinem der Probanden gesundheitliche Probleme auftraten, erklärte Dr. Park, der von Zeitgenossen als jemand beschrieben wurde, der "nie Gras über die Sache wachsen lässt", den Impfstoff für sicher. Als eine schwere Polio-Epidemie in Kern County, Kalifornien, ausbrach, wurde dieses Gebiet sehr kurzfristig zum ersten Testgebiet für den neuen Impfstoff. Zwischen November 1934 und Mai 1935 wurden in Kern County über 1.500 Dosen des Impfstoffs verabreicht. Die ersten Ergebnisse waren zwar sehr vielversprechend, aber die unzureichende Personalausstattung und die mangelhafte Gestaltung des Protokolls führten dazu, dass Brodie bei der Veröffentlichung der kalifornischen Ergebnisse im August 1935 kritisiert wurde. Mit Hilfe von Privatärzten führte Brodie auch eine umfassendere Feldstudie durch, an der 9.000 Kinder, die geimpft wurden, und 4.500 alters- und ortsgleiche Kontrollkinder, die keinen Impfstoff erhielten, teilnahmen. Auch hier waren die Ergebnisse vielversprechend. Von den geimpften Kindern erkrankten nur wenige später an Polio. Die meisten von ihnen waren bereits vor der Impfung dem Virus ausgesetzt gewesen, und keiner von ihnen hatte die vollständige Serie der untersuchten Impfdosen erhalten. Darüber hinaus bot eine Polio-Epidemie in Raleigh, North Carolina, dem U.S. Public Health Service die Gelegenheit, mit Mitteln der Birthday Ball Commission einen stark strukturierten Versuch mit dem Brodie-Impfstoff durchzuführen. ⓘ
Akademischer Empfang
Noch während die Arbeiten liefen, begannen die Bakteriologen Bedenken hinsichtlich der Sicherheit und Wirksamkeit der neuen Poliovirus-Impfstoffe zu äußern. Zu dieser Zeit gab es nur sehr wenig Aufsicht über medizinische Studien, und die ethische Behandlung von Studienteilnehmern hing weitgehend vom moralischen Druck gleichgesinnter akademischer Wissenschaftler ab. Brodies inaktivierte Impfstoffe wurden von vielen kritisch beäugt, die der Meinung waren, dass Impfstoffe mit abgetöteten Viren nicht wirksam sein könnten. Zwar konnten Forscher die von ihm in Tierversuchen erzeugte Gewebeimmunität replizieren, doch herrschte die Meinung vor, dass eine humorale Immunität für einen wirksamen Impfstoff unerlässlich sei. Kolmer stellte den Ansatz der abgetöteten Viren in Fachzeitschriften direkt in Frage. Kolmers Studien gaben jedoch noch mehr Anlass zur Besorgnis, da sich die Berichte über Lähmungen bei Kindern nach der Impfung mit seinem Lebendvirusimpfstoff häuften, wobei die Lähmung in vielen Fällen am Arm und nicht am Fuß begann. Sowohl Kolmer als auch Brodie wurden aufgefordert, ihre Forschungsergebnisse auf der Jahrestagung der American Public Health Association in Milwaukee WI im Oktober 1935 vorzustellen. Außerdem wurde Dr. Thomas M. Rivers, ein prominenter Kritiker der Impfstoffentwicklung, gebeten, jedes der vorgestellten Papiere zu diskutieren. Dies führte dazu, dass die APHA ein Symposium über Poliomyelitis organisierte, das auf der Jahrestagung der südlichen Abteilung im folgenden Monat abgehalten werden sollte. Während der Diskussion auf dieser Tagung stellte sich Dr. James Leake vom U.S. Public Health Service hin, um sofort klinische Beweise dafür vorzulegen, dass der Kolmer-Impfstoff mehrere Todesfälle verursacht hatte, und beschuldigte Kolmer dann angeblich, ein Mörder zu sein. Wie sich Rivers in seiner mündlichen Erzählung erinnerte, "brach die Hölle los, und es schien, als ob jeder versuchte, gleichzeitig zu sprechen....Jimmy Leake benutzte die schärfste Sprache, die ich je auf einer wissenschaftlichen Tagung gehört habe." Als Reaktion auf die Angriffe von allen Seiten soll Brodie aufgestanden sein und gesagt haben: "Es sieht so aus, als ob laut Dr. Rivers mein Impfstoff nichts taugt, und laut Dr. Leake ist der von Dr. Kolmer gefährlich." Kolmer entgegnete lediglich: "Meine Herren, dieses eine Mal wünschte ich, der Boden würde sich öffnen und mich verschlucken." Letztlich erwies sich Kolmers Lebendimpfstoff zweifellos als gefährlich und wurde bereits im September 1935 vor der Tagung in Milwaukee zurückgezogen. Während der Konsens des Symposiums die Wirksamkeit des Brodie-Impfstoffs weitgehend in Frage stellte, wurde seine Sicherheit nicht in Frage gestellt, und es wurde eine viel größere, gut kontrollierte Studie empfohlen. Als jedoch drei Kinder nach einer Dosis des Impfstoffs an Kinderlähmung erkrankten, forderten die Direktoren der Warm Springs Foundation in Georgia (die als Hauptgeldgeber für das Projekt fungierten) im Dezember 1935 die Rücknahme des Impfstoffs. Nach der Rücknahme des Projekts wurde das zuvor beobachtete Moratorium für die Entwicklung eines Impfstoffs gegen Poliomyelitis beim Menschen wieder aufgenommen, und es sollte fast 20 Jahre lang kein weiterer Versuch unternommen werden. ⓘ
Obwohl Brodie wohl die größten Fortschritte bei der Entwicklung eines Impfstoffs gegen das Poliovirus gemacht hatte, erlitt er aufgrund seines Status als weniger bekannter Forscher die schwerwiegendsten Auswirkungen auf seine Karriere. Heutige Forscher sind sich darüber im Klaren, dass Brodie zwar einen wirksamen Polio-Impfstoff entwickelt hat, dass aber die damaligen wissenschaftlichen und technischen Grundlagen nicht ausreichten, um diesen Durchbruch zu verstehen und zu nutzen. Brodies Arbeit mit formalininaktivierten Viren sollte später die Grundlage für den Salk-Impfstoff bilden, aber er erlebte diesen Erfolg nicht mehr. Brodie wurde innerhalb von drei Monaten nach der Veröffentlichung des Symposiums entlassen. Er konnte zwar eine andere Stelle im Labor finden, starb aber nur drei Jahre später im Alter von 36 Jahren an einem Herzinfarkt. Im Gegensatz dazu konnte Park, von dem man in der Gemeinde annahm, dass er zu diesem Zeitpunkt bereits das Rentenalter erreicht hatte, vor seinem Tod im Jahr 1939 mit allen Ehren in den Ruhestand treten. Kolmer, der bereits ein etablierter und angesehener Forscher war, kehrte als Professor für Medizin an die Temple University zurück. Kolmer hatte eine sehr produktive Karriere, wurde mehrfach ausgezeichnet und veröffentlichte bis zu seiner Pensionierung im Jahr 1957 unzählige Arbeiten, Artikel und Lehrbücher. ⓘ
1948
Ein Durchbruch gelang 1948, als eine Forschergruppe unter der Leitung von John Enders am Kinderkrankenhaus in Boston das Poliovirus erfolgreich im Labor in menschlichem Gewebe züchtete. Diese Gruppe hatte kurz zuvor erfolgreich Mumps in Zellkulturen gezüchtet. Im März 1948 versuchte Thomas H. Weller, das Varizellenvirus in embryonalem Lungengewebe zu züchten. Er hatte die geplante Anzahl von Röhrchen beimpft, als er bemerkte, dass einige Röhrchen unbenutzt waren. Er entnahm eine mit dem Poliovirus infizierte Probe von Mäusegehirn und fügte sie den verbleibenden Reagenzgläsern hinzu, in der Annahme, dass das Virus wachsen könnte. Die Varizellenkulturen wuchsen nicht, aber die Polio-Kulturen waren erfolgreich. Diese Entwicklung erleichterte die Impfstoffforschung erheblich und ermöglichte schließlich die Entwicklung von Impfstoffen gegen Polio. Enders und seine Kollegen, Thomas H. Weller und Frederick C. Robbins, wurden 1954 für ihre Bemühungen mit dem Nobelpreis für Physiologie oder Medizin ausgezeichnet. Weitere wichtige Fortschritte, die zur Entwicklung von Polio-Impfstoffen führten, waren: die Identifizierung von drei Poliovirus-Serotypen (Poliovirus Typ 1 - PV1 oder Mahoney; PV2, Lansing; und PV3, Leon); die Feststellung, dass das Virus vor der Lähmung im Blut vorhanden sein muss; und der Nachweis, dass die Verabreichung von Antikörpern in Form von Gammaglobulin vor paralytischer Polio schützt. ⓘ
1950–1955

In den frühen 1950er Jahren lag die Zahl der Poliofälle in den USA bei über 25.000 pro Jahr. 1952 und 1953 kam es in den USA zu einem Ausbruch von 58.000 bzw. 35.000 Poliofällen, nachdem die Zahl der Poliofälle zuvor bei etwa 20.000 pro Jahr gelegen hatte; die Zahl der Todesfälle lag in diesen Jahren bei 3.200 und 1.400. Inmitten dieser Polio-Epidemie in den USA investierten kommerzielle Interessengruppen, darunter die Lederle Laboratories in New York unter der Leitung von H. R. Cox, Millionen von Dollar in die Entwicklung und Vermarktung eines Polio-Impfstoffs. Bei Lederle arbeitete auch der in Polen geborene Virologe und Immunologe Hilary Koprowski vom Wistar Institute in Philadelphia, der 1950 den ersten erfolgreichen Polio-Impfstoff testete. Sein Impfstoff, ein attenuierter Lebendvirus, der oral verabreicht wurde, befand sich jedoch noch im Forschungsstadium und sollte erst fünf Jahre nach dem Polio-Impfstoff von Jonas Salk (ein injizierbarer Impfstoff mit toten Viren) auf den Markt kommen. Koprowskis abgeschwächter Impfstoff wurde durch aufeinanderfolgende Passagen durch die Gehirne von Schweizer Albinomäusen hergestellt. Nach der siebten Passage konnten die Impfstämme kein Nervengewebe mehr infizieren oder Lähmungen verursachen. Nach ein bis drei weiteren Passagen an Ratten wurde der Impfstoff als sicher für den menschlichen Gebrauch eingestuft. Am 27. Februar 1950 wurde der abgeschwächte Lebendimpfstoff von Koprowski zum ersten Mal an einem achtjährigen Jungen getestet, der in Letchworth Village, einer Einrichtung für körperlich und geistig Behinderte in New York, lebte. Nachdem das Kind keine Nebenwirkungen zeigte, weitete Koprowski sein Experiment auf 19 weitere Kinder aus. ⓘ
Jonas Salk


Der erste wirksame Polio-Impfstoff wurde 1952 von Jonas Salk und einem Team an der Universität Pittsburgh entwickelt, zu dem Julius Youngner, Byron Bennett, L. James Lewis und Lorraine Friedman gehörten, und musste anschließend jahrelang getestet werden. Am 26. März 1953 berichtete Salk im CBS-Radio über einen erfolgreichen Test an einer kleinen Gruppe von Erwachsenen und Kindern; zwei Tage später wurden die Ergebnisse im JAMA veröffentlicht. Leone N. Farrell erfand eine wichtige Labortechnik, die die Massenproduktion des Impfstoffs durch ein von ihr geleitetes Team in Toronto ermöglichte. Ab dem 23. Februar 1954 wurde der Impfstoff in der Arsenal Elementary School und dem Watson Home for Children in Pittsburgh, Pennsylvania, getestet. ⓘ
Der Impfstoff von Salk wurde dann in einem Test, dem so genannten Francis Field Trial, unter der Leitung von Thomas Francis verwendet, dem damals größten medizinischen Experiment der Geschichte. Der Test begann mit etwa 4.000 Kindern an der Franklin Sherman Elementary School in McLean, Virginia, und umfasste schließlich 1,8 Millionen Kinder in 44 Staaten von Maine bis Kalifornien. Am Ende der Studie hatten etwa 440.000 Kinder eine oder mehrere Injektionen des Impfstoffs erhalten, etwa 210.000 Kinder erhielten ein Placebo, das aus harmlosen Nährböden bestand, und 1,2 Millionen Kinder wurden nicht geimpft und dienten als Kontrollgruppe, die dann beobachtet wurde, um festzustellen, ob sie an Polio erkrankten. ⓘ
Die Ergebnisse des Feldversuchs wurden am 12. April 1955 bekannt gegeben (dem zehnten Jahrestag des Todes von Präsident Franklin D. Roosevelt, dessen Lähmungskrankheit nach allgemeiner Auffassung durch Polio verursacht worden war). Der Salk-Impfstoff war zu 60-70 % wirksam gegen PV1 (Poliovirus Typ 1), zu über 90 % wirksam gegen PV2 und PV3 und zu 94 % wirksam gegen die Entwicklung der bulbären Polio. Bald nach der Zulassung des Impfstoffs von Salk im Jahr 1955 wurden Impfkampagnen für Kinder gestartet. In den USA ging die Zahl der jährlichen Poliofälle nach einer vom March of Dimes geförderten Massenimpfkampagne von 35.000 im Jahr 1953 auf 5.600 im Jahr 1957 zurück. Bis 1961 wurden in den Vereinigten Staaten nur noch 161 Fälle registriert. ⓘ
Eine Woche vor der Bekanntgabe der Ergebnisse des Francis-Feldversuchs im April 1955 hatte Pierre Lépine vom Institut Pasteur in Paris ebenfalls einen wirksamen Polio-Impfstoff angekündigt. ⓘ
Zwischenfälle bei der Sicherheit
Im April 1955, kurz nach Beginn der Massenimpfung gegen Polio in den USA, gingen beim Surgeon General Berichte über Patienten ein, die etwa eine Woche nach der Impfung mit dem Polio-Impfstoff Salk des Pharmaunternehmens Cutter an Lähmungen erkrankten, die sich auf die Gliedmaße beschränkten, in die der Impfstoff injiziert worden war. Mit dem Cutter-Impfstoff waren 200.000 Kinder im Westen und Mittleren Westen der USA geimpft worden. Spätere Untersuchungen ergaben, dass der Cutter-Impfstoff 40.000 Polio-Fälle verursacht hatte, an denen 10 Kinder starben. Daraufhin nahm der Surgeon General alle von Cutter Laboratories hergestellten Polioimpfstoffe vom Markt, allerdings erst, nachdem 250 Fälle von Lähmungserscheinungen aufgetreten waren. Auch der Polio-Impfstoff von Wyeth hatte Berichten zufolge zu Lähmungen und zum Tod mehrerer Kinder geführt. Bald stellte sich heraus, dass einige Chargen des von Cutter und Wyeth hergestellten Salk-Polio-Impfstoffs nicht ordnungsgemäß inaktiviert worden waren, so dass in mehr als 100 000 Impfstoffdosen lebende Polioviren enthalten waren. Im Mai 1955 richteten die National Institutes of Health und die Public Health Services ein Technical Committee on Poliomyelitis Vaccine ein, das alle Polioimpfstoffchargen testen und überprüfen und den Public Health Service bei der Entscheidung beraten sollte, welche Chargen für den öffentlichen Gebrauch freigegeben werden sollten. Diese Vorfälle schwächten das Vertrauen der Öffentlichkeit in den Polioimpfstoff und führten zu einem Rückgang der Impfraten. ⓘ
1961

Zur gleichen Zeit, als Salk seinen Impfstoff testete, arbeiteten sowohl Albert Sabin als auch Hilary Koprowski weiter an der Entwicklung eines Impfstoffs mit Lebendviren. Bei einem Treffen in Stockholm im November 1955, bei dem es um Polioimpfstoffe ging, stellte Sabin die Ergebnisse einer Gruppe von 80 Freiwilligen vor, während Koprowski einen Bericht über die Ergebnisse einer Studie mit 150 Personen verlas. Sowohl Sabin als auch Koprowski gelang es schließlich, Impfstoffe zu entwickeln. Aufgrund des Engagements für den Salk-Impfstoff in Amerika führten Sabin und Koprowski ihre Versuche außerhalb der Vereinigten Staaten durch, Sabin in Mexiko und der Sowjetunion, Koprowski im Kongo und in Polen. 1957 entwickelte Sabin einen dreiwertigen Impfstoff, der abgeschwächte Stämme aller drei Poliovirustypen enthielt. Im Jahr 1959 erhielten zehn Millionen Kinder in der Sowjetunion den Schluckimpfstoff von Sabin. Für diese Arbeit wurde Sabin mit der Medaille des Ordens der Völkerfreundschaft ausgezeichnet, der höchsten zivilen Auszeichnung der Sowjetunion. Sabins Schluckimpfstoff mit Lebendviren kam 1961 auf den Markt. ⓘ
Als der Schluckimpfstoff von Sabin allgemein verfügbar wurde, verdrängte er den gespritzten Impfstoff von Salk, der in der Öffentlichkeit durch den Cutter-Zwischenfall von 1955 in Verruf geraten war, bei dem unsachgemäß zubereitete Salk-Impfstoffe eines Unternehmens zum Tod oder zu Lähmungen mehrerer Kinder führten. ⓘ
1987
Der inaktivierte Polioimpfstoff wird intramuskulär injiziert. Heute wird der Impfstoff häufig als Bestandteil eines Kombinationsimpfstoffes, beispielsweise eines hexavalenten Impfstoffs, eingesetzt. Er kann auch bei Patienten mit einem Immundefekt angewendet werden, da kein infektiöses Virus enthalten ist. Einerseits sind Säuglinge von Müttern, die ihre Polio-Antikörper über die Plazenta auf das Ungeborene übertragen haben (Nestschutz), dadurch zunächst vor Polio geschützt, andererseits führt die Impfung bei ihnen in dieser Zeit nur unzureichend zur Bildung eigener Antikörper. ⓘ
Nach Empfehlung der STIKO (und einigen anderen europäischen Ländern) wird die Grundimmunisierung durch ein „2+1-Schema“ realisiert (Impfung im 2. und 4. Monat, abschließend im 11. Monat), falls die einzelnen Impfungen zu den empfohlenen Zeitpunkten durchgeführt und das Impfschema rechtzeitig abgeschlossen wird. Bei Frühgeborenen wird eine zusätzliche Impfstoffdosis im Alter von 3 Monaten empfohlen (sogenanntes „3+1-Schema“). Bei der Impfung handelt es sich in der Regel um Kombinationsimpfstoffe (z. B. mit azellulärer Pertussis- und Diphtheriekomponente). Sofern kein Kombinationsimpfstoff verwendet wird, werden je nach Impfstoff zwei bzw. drei Impfungen im 1. und 2. Lebensjahr durchgeführt. ⓘ
Im Alter von 9–17 Jahren wird eine Auffrischimpfung mit einem IPV-haltigen Impfstoff empfohlen. Eine mit OPV begonnene Grundimmunisierung wird mit IPV komplettiert. ⓘ
Im November 1987 wurde in den Vereinigten Staaten ein IPV-Impfstoff mit erhöhter Potenz zugelassen, der dort derzeit der Impfstoff der Wahl ist. Die erste Dosis des Polioimpfstoffs wird kurz nach der Geburt verabreicht, in der Regel im Alter von 1 bis 2 Monaten, und eine zweite Dosis wird im Alter von 4 Monaten verabreicht. Der Zeitpunkt der dritten Dosis hängt von der Formulierung des Impfstoffs ab, sollte aber zwischen dem 6. und 18. Lebensmonat verabreicht werden. Eine Auffrischungsimpfung wird im Alter von 4 bis 6 Jahren verabreicht, insgesamt also vier Dosen bei oder vor der Einschulung. In einigen Ländern wird eine fünfte Impfung im Jugendalter verabreicht. Eine routinemäßige Impfung von Erwachsenen (ab 18 Jahren) ist in den Industrieländern weder notwendig noch empfehlenswert, da die meisten Erwachsenen bereits immun sind und in ihren Heimatländern nur ein sehr geringes Risiko besteht, dem Polio-Wildvirus ausgesetzt zu sein. Im Jahr 2002 wurde in den Vereinigten Staaten ein pentavalenter (Fünfkomponenten-) Kombinationsimpfstoff (Pediarix), der IPV enthält, zur Verwendung zugelassen. ⓘ
1988
Die von der Weltgesundheitsorganisation (WHO), UNICEF und der Rotary Foundation geleiteten weltweiten Bemühungen zur Ausrottung der Kinderlähmung begannen 1988 und stützten sich weitgehend auf den von Albert Sabin und Michail Tschumakow entwickelten oralen Polio-Impfstoff (Sabin-Chumakow-Impfstoff). ⓘ
Nach 1990
Polio wurde in Amerika bis 1994 eliminiert. Im Jahr 2000 wurde die Krankheit in 36 westpazifischen Ländern, darunter China und Australien, offiziell ausgerottet. Europa wurde im Jahr 2002 für poliofrei erklärt. Seit Januar 2011 wurden in Indien keine Krankheitsfälle mehr gemeldet, so dass das Land im Februar 2012 von der WHO-Liste der polio-endemischen Länder gestrichen wurde. Im März 2014 wurde Indien zu einem poliofreien Land erklärt. ⓘ
Obwohl die Übertragung des Poliovirus in weiten Teilen der Welt unterbrochen wurde, besteht weiterhin die Gefahr der Einschleppung von Polio-Wildviren in zuvor poliofreie Regionen. Wenn Polioviren eingeschleppt werden, kann es zu Ausbrüchen von Poliomyelitis kommen, insbesondere in Gebieten mit geringer Durchimpfungsrate und schlechten sanitären Verhältnissen. Aus diesem Grund muss eine hohe Durchimpfungsrate aufrechterhalten werden. Im November 2013 meldete die WHO einen Polioausbruch in Syrien. Daraufhin gab die armenische Regierung einen Aufruf heraus, in dem sie syrische Armenier unter 15 Jahren aufforderte, sich gegen Polio impfen zu lassen. Im Jahr 2014 hatte sich das Poliovirus in zehn Ländern ausgebreitet, vor allem in Afrika, Asien und im Nahen Osten, wobei Pakistan, Syrien und Kamerun Ausreisenden zu Impfungen rieten. ⓘ
In Pakistan, Afghanistan und Nigeria - den drei Ländern, in denen 2017 noch Polio-Fälle aufgetreten sind - wehren sich einige Menschen gegen Polio-Impfprogramme. Fast alle religiösen und politischen Führer der Muslime haben den Impfstoff befürwortet, aber eine Minderheit glaubt, dass die Impfstoffe heimlich zur Sterilisierung von Muslimen eingesetzt werden. Die Tatsache, dass die CIA 2011 ein gefälschtes Impfprogramm organisierte, um bei der Suche nach Osama Bin Laden zu helfen, ist ein zusätzlicher Grund für das Misstrauen. Im Jahr 2015 kündigte die WHO ein Abkommen mit den Taliban an, um sie zu ermutigen, den Impfstoff in den von ihnen kontrollierten Gebieten zu verteilen. Die pakistanischen Taliban waren jedoch nicht bereit, dies zu unterstützen. Am 11. September 2016 erschossen zwei nicht identifizierte Bewaffnete, die mit der pakistanischen Talibanorganisation Jamaat-ul-Ahrar in Verbindung stehen, Zakaullah Khan, einen Arzt, der in Pakistan Polioimpfstoffe verabreichte. Der Anführer der Jamaat-ul-Ahrar bekannte sich zu den Schüssen und erklärte, dass die Gruppe diese Art von Anschlägen fortsetzen werde. Dieser Widerstand gegen und diese Skepsis gegenüber Impfungen hat den Prozess der Ausrottung der Kinderlähmung in den beiden verbleibenden endemischen Ländern verlangsamt. ⓘ
Reiseanforderungen

Reisende, die in bestimmte Länder ein- oder ausreisen wollen, müssen gegen Polio geimpft sein, in der Regel höchstens 12 Monate und mindestens 4 Wochen vor dem Grenzübertritt, und bei den Grenzkontrollen einen Impfpass/eine Impfbescheinigung vorlegen können. Die meisten Anforderungen gelten nur für Reisen in oder aus sogenannten "polioendemischen", "poliobetroffenen", "polioexportierenden", "polioübertragenden" oder "Hochrisikoländern". Ab August 2020 sind Afghanistan und Pakistan die einzigen polio-endemischen Länder der Welt (in denen die wilde Kinderlähmung noch nicht ausgerottet ist). Für mehrere Länder gelten zusätzliche Anforderungen für eine vorsorgliche Polioimpfung bei Reisen, z. B. in und aus "wichtigen Risikoländern", zu denen ab Dezember 2020 China, Indonesien, Mosambik, Myanmar und Papua-Neuguinea gehören. ⓘ
| Polio-Impfvorschriften für internationale Reisen ⓘ | |
|---|---|
| Land | Einzelheiten |
| Reisende aus polioendemischen Ländern (Pakistan) benötigen bei der Einreise einen Carte-Jaune-Nachweis der Polioimpfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). Einwohner und ALLE Reisenden, die sich länger als 4 Wochen in Afghanistan aufhalten, benötigen bei der Abreise aus Afghanistan einen Nachweis über die Polioimpfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus Afghanistan und Pakistan benötigen bei ihrer Ankunft einen Nachweis über eine OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). In Belize ansässige Personen, die in Länder mit bestätigten Poliofällen reisen, benötigen ebenfalls einen Nachweis über die Impfung. | |
| Reisende aus Ländern, die Polio exportieren, benötigen bei der Einreise einen Carte Jaune Nachweis über eine OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus Afghanistan, Angola, Benin, Kamerun, der Zentralafrikanischen Republik, China, Kongo-Kinshasa, Äthiopien, Ghana, Indonesien, Kenia, Mosambik, Myanmar, Niger, Nigeria, Pakistan, Papua-Neuguinea, den Philippinen und Somalia benötigen bei ihrer Ankunft einen Carte-Jaune-Nachweis über eine OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus Risikoländern benötigen bei der Einreise einen Carte Jaune-Nachweis über eine OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). Reisenden ohne Nachweis wird bei der Ankunft eine OPV-Impfung angeboten. | |
| Reisende aus Afghanistan, Kongo-Kinshasa, Äthiopien, Kenia, Nigeria, Pakistan, Somalia und Syrien benötigen bei der Ankunft einen Carte Jaune Nachweis über eine OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus Afghanistan, Pakistan und Nigeria benötigen bei der Einreise einen Carte Jaune-Nachweis über die OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). Reisende ohne Nachweis werden bei der Ankunft geimpft. | |
| Reisende ab 15 Jahren aus Afghanistan und Pakistan benötigen bei der Ankunft einen Carte Jaune Nachweis über eine OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde); Kinder unter 15 Jahren müssen vor der Reise drei Dosen Polio-Impfstoff erhalten haben. Reisende ohne Nachweis werden bei der Ankunft geimpft. Reisende, die aus dem Irak nach Afghanistan und Pakistan ausreisen, müssen bei der Ausreise ebenfalls einen Impfnachweis vorlegen. | |
| Reisende aus Afghanistan und Pakistan benötigen bei der Einreise einen Carte-Jaune-Nachweis über die OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus und in poliogefährdete Länder benötigen bei der Einreise einen Carte Jaune Nachweis über die OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus Afghanistan und Pakistan benötigen bei der Einreise einen Carte-Jaune-Nachweis über die OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus und in Länder, die Polio exportieren, sowie Hajj- und Umrah-Pilger benötigen bei ihrer Ankunft einen Carte Jaune-Nachweis über die OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus von der Kinderlähmung betroffenen Ländern benötigen bei der Einreise eine Carte Jaune zum Nachweis der OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus Afghanistan, Kenia, Nigeria, Pakistan und Papua-Neuguinea benötigen bei der Einreise einen Carte Jaune-Nachweis über die OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus Ländern, die Polio exportieren, benötigen bei der Einreise einen Carte Jaune Nachweis über eine OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus ALLEN Ländern, die einen Aufenthalt von mehr als 4 Wochen in Pakistan planen, benötigen bei der Ankunft einen Carte Jaune Nachweis über die OPV-Impfung. Einheimische und ALLE Reisenden, die sich länger als 4 Wochen in Pakistan aufhalten, benötigen bei der Ausreise aus Pakistan einen Nachweis über die OPV-Impfung. | |
| Reisende aus oder in Hochrisikoländer benötigen bei der Ankunft bzw. vor der Abreise einen Carte Jaune Nachweis über die Polioimpfung. Aufgrund eines anhaltenden lokalen VDPV2-Ausbruchs empfiehlt die Regierung allen anderen Reisenden, eine Polio-Impfung oder eine Auffrischungsimpfung zu erwägen, je nach ihrer Situation. | |
| Reisende aus Ländern, die Polio exportieren (von Katar als Afghanistan, Nigeria, Pakistan und die Philippinen bezeichnet), benötigen bei der Ankunft einen Carte Jaune Nachweis über eine OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus den von der WHO als polio-endemisch eingestuften Ländern (Afghanistan und Pakistan) benötigen bei der Einreise eine Carte Jaune zum Nachweis einer OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus Ländern mit aktiver Übertragung (einschließlich des Polio-Wildvirus oder des Polio-Impfstoffs) und aus Risikoländern sowie alle Reisenden aus Afghanistan, Kongo-Kinshasa, Mosambik, Myanmar, Niger, Nigeria, Pakistan, Papua-Neuguinea, Somalia, Syrien und Jemen benötigen bei der Ankunft einen Carte-Jaune-Nachweis über eine OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). Unabhängig vom Impfstatus erhalten alle Reisenden aus Afghanistan, Myanmar, Nigeria, Pakistan, Papua-Neuguinea, Somalia, Syrien und Jemen bei ihrer Ankunft eine Dosis der oralen Polio-Impfung. | |
| Reisende aus Ländern, in denen die Kinderlähmung ausgebrochen ist, benötigen bei der Ankunft einen Carte Jaune Nachweis über eine OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). | |
| Reisende aus Kamerun, Äquatorialguinea und Pakistan benötigen bei der Einreise einen Carte Jaune Nachweis über eine OPV- oder IPV-Impfung (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde). ALLE in Syrien ansässigen Personen, die aus Syrien in ein anderes Land ausreisen, benötigen ebenfalls einen Nachweis über die Impfung. | |
| Langzeitbesucher, die in Länder reisen, in denen das Polio-Wildvirus oder zirkulierende, durch Impfung übertragene Polioviren vorkommen, müssen mit der Carte Jaune einen Nachweis über eine Impfung mit mindestens einer Dosis bivalentem OPV oder IPV (die zwischen 4 Wochen und 12 Monaten vor der Abreise erhalten wurde) vorlegen. Personen, die zu einer dringenden internationalen Reise verpflichtet sind, müssen vor ihrer Abreise mit einer Einzeldosis Polioimpfstoff geimpft werden. Auch in der Ukraine selbst besteht das Risiko einer Übertragung des Poliovirus, und Reisenden in die Ukraine wird empfohlen, ihre Polioimpfung vor der Einreise auf den neuesten Stand zu bringen. | |
Gesellschaft und Kultur
Kosten
Die Global Alliance for Vaccines and Immunization liefert den inaktivierten Impfstoff an Entwicklungsländer für nur 0,75 € (ca. 0,86 US$) pro Dosis in 10-Dosen-Fläschchen (2015). ⓘ
Missverständnisse
In Pakistan herrscht der Irrglaube, der Polio-Impfstoff enthalte haramistische Bestandteile und könne bei männlichen Kindern Impotenz und Unfruchtbarkeit hervorrufen, was einige Eltern dazu veranlasst, ihre Kinder nicht impfen zu lassen. Dieser Glaube ist vor allem in der Provinz Khyber Pakhtunkhwa und in der Region FATA verbreitet. Es kam auch zu Angriffen auf Polio-Impfteams, was die internationalen Bemühungen um die Ausrottung der Kinderlähmung in Pakistan und weltweit behindert hat. ⓘ
Populäre Kultur
Der Popsong A Spoonful of Sugar (Helps the Medicine Go Down) aus dem Jahr 1964 bezieht sich auf den Schluckimpfstoff, der in einem Zuckerwürfel verabreicht wird. ⓘ
Inaktivierter Polioimpfstoff (Salk, IPV)
Der inaktivierte Polioimpfstoff nach Salk, ein Totimpfstoff, ist der derzeit in Europa routinemäßig eingesetzte Impfstoff. ⓘ
Herstellung

Virulente Polioviren der Typen 1, 2 oder 3 werden durch Zellkultur in Vero-Zellen, einer etablierten Zelllinie aus Nierenzellen der grünen Meerkatze, alternativ auch in humanen diploiden Zellen, vermehrt. Aus dem Kulturmedium wird durch Filtration, Ultrafiltration und Chromatografie eine gereinigte Virussuspension erzeugt. Die sorgfältige Abtrennung von Zellbestandteilen ist eine Voraussetzung für die vollständige Virusinaktivierung. Diese erfolgt durch mehrtägige Behandlung mit Formaldehyd; durch chemische Reaktion des Formaldehyds mit Virusbestandteilen geht die Vermehrungsfähigkeit der Viren verloren. Nachdem keine infektiösen Viren mehr nachweisbar sind, wird das restliche Formaldehyd entfernt. Die Prüfung auf nicht inaktivierte Viren erfolgt in einem Zellkultur-Test, der Nachweis des Antigen-Gehalts wird mit einem ELISA-Test durchgeführt, oft auch ergänzt durch Tierversuche mit Ratten, die nach einer Testimpfung schützende Antikörper entwickeln müssen. ⓘ
Der fertige Impfstoff, monovalent oder eine der Kombinationen aus inaktivierten Polioviren der Typen 1, 2 und/oder 3, enthält oft noch Spuren von Antibiotika wie Neomycin oder Streptomycin. ⓘ
Kontraindikationen
Der Impfstoff soll nicht angewendet werden, wenn eine bekannte schwere Allergie gegen einen der Bestandteile vorliegt. Auch während einer akuten, schwerwiegenden und fieberhaften Erkrankung sollte nicht geimpft werden. ⓘ
Oraler Polioimpfstoff (Sabin, OPV)
Anwendung und Wirkung

Der orale Polioimpfstoff wird als Schluckimpfung angewendet; dabei wird der Impfstoff oft auf ein Stück Würfelzucker gegeben, das dann geschluckt wird. Die Impfung führt nach regelrechter Anwendung unter günstigen Randbedingungen bei nahezu 100 % der Geimpften zu einer stillen Feiung, indem nach einer Infektion des Magen-Darm-Traktes ohne Krankheitssymptome zuverlässig vor den Lähmungen schützende Antikörpern nicht nur im Blut, sondern in Form von IgA auch in den Schleimhäuten des Darmes erzeugt werden. Da das Impfvirus nach der Impfung teilweise ausgeschieden wird, können durch das Impfvirus auch Kontaktpersonen infiziert werden, die auf diese Weise ebenfalls einen Impfschutz gewinnen („passive“ Immunisierung). Der orale Polioimpfstoff kann somit eine Herdenimmunität erzeugen. Das erklärt, dass die tatsächliche Wirksamkeit (efficiency) der OPV-Kampagnen gerade in Entwicklungsländern höher war als auf Grund dort manchmal ungünstiger Randbedingungen erwartet. Aus diesem Grund wird in Ländern, in denen das Poliovirus noch auftritt, trotz der bekannten Einschränkungen und Risiken durch VAPP und VDPV zumindest zu Beginn von Impfkampagnen noch der Lebendimpfstoff verwendet. Es kommt hinzu, dass der orale Impfstoff kostengünstig herzustellen und einfach anzuwenden ist. ⓘ
In Deutschland und vielen anderen Polio-freien Ländern wird der orale Polioimpfstoff wegen seiner Risiken durch VAPP und VDPV nicht mehr regelmäßig angewandt; vorgesehen ist sein Einsatz nur noch als Riegelimpfung im Fall von Polio-Ausbrüchen nach Einschleppung aus dem Ausland. Auch weltweit wird die Verwendung des Lebendimpfstoffs mittelfristig eingestellt werden, nachdem das Ziel erreicht ist, das Wildvirus auszurotten. ⓘ
Einfluss ungünstiger Randbedingungen
Die tatsächliche Wirksamkeit (efficiency) der OPV wird vor allem verringert durch:
- mütterliche Leihantikörper bei Neugeborenen (nachteilig auch bei IPV),
- geringe intestinale Immun-Kompetenz bei mangelernährten Kindern,
- Durchfall und Darminfektionen,
- eingeschränkte Qualität des Impfstoffes (Kühlkette) ⓘ
Durch solche ungünstigen Bedingungen kann die tatsächliche Wirksamkeit von OPV-Kampagnen deutlich absinken, so wurden in Ghana nach dreifacher OPV nur bei etwa 60 % der Geimpften neutralisierende Antikörper gegen alle 3 Poliovirus-Typen nachgewiesen. ⓘ
