Nitroglycerin

| |
| |
| |
| Bezeichnungen | |
|---|---|
| Bevorzugte IUPAC-Bezeichnung
Propan-1,2,3-triyltrinitrat | |
| Andere Bezeichnungen
*1,2,3-Tris(nitrooxy)propan
| |
| Kennzeichnungsmittel | |
3D-Modell (JSmol)
|
|
Beilstein-Referenz
|
1802063 |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Arzneimittelbank | |
| EC-Nummer |
|
Gmelin Referenz
|
165859 |
IUPHAR/BPS
|
|
| KEGG | |
| MeSH | Nitroglyzerin |
PubChem CID
|
|
| UNII | |
| UN-Nummer | 0143, 0144, 1204, 3064, 3319 |
InChI
| |
SMILES
| |
| Eigenschaften | |
Chemische Formel
|
C3H5N3O9 |
| Molekulare Masse | 227,085 g-mol-1 |
| Erscheinungsbild | Farblose Flüssigkeit |
| Dichte | 1,6 g⋅cm-3 (bei 15 °C) |
| Schmelzpunkt | 14 °C (57 °F; 287 K) |
| Siedepunkt | 50 °C (122 °F; 323 K) Explosionsfähigkeit |
Löslichkeit in Wasser
|
Geringfügig |
| Löslichkeit | Aceton, Ether, Benzol, Alkohol |
| log P | 2.154 |
| Struktur | |
Koordinationsgeometrie
|
|
Molekulare Form
|
|
| Explosive Daten | |
| Schockempfindlichkeit | Hoch |
| Reibungsempfindlichkeit | Hoch |
| Detonationsgeschwindigkeit | 7700 m⋅s-1 |
| RE-Faktor | 1.50 |
| Thermochemie | |
Std. Bildungsenthalpie
Bildung (ΔfH⦵298) |
-370 kJ⋅mol-1 |
Std. Bildungsenthalpie
Verbrennung (ΔcH⦵298) |
-1,529 MJ⋅mol-1 |
| Pharmakologie | |
ATC-Code
|
C01DA02 (WHO) C05AE01 (WHO) |
Wege der
Verabreichung |
Intravenös, durch den Mund, unter die Zunge, äußerlich |
| Pharmakokinetik: | |
Bioverfügbarkeit
|
<1% |
| Leber | |
Biologische Halbwertszeit
|
3 Minuten |
| Rechtlicher Status |
|
| Gefahren | |
| Sicherheit und Gesundheitsschutz am Arbeitsplatz (OHS/OSH): | |
Hauptgefahren
|
Explosiv, giftig |
| GHS-Kennzeichnung: | |
Piktogramme
|
   
|
Signalwort
|
Gefahr |
Gefahrenhinweise
|
H202, H205, H241, H301, H311, H331, H370 |
Sicherheitshinweise
|
P210, P243, P250, P260, P264, P270, P271, P280, P302+P352, P410 |
| NFPA 704 (Feuerdiamant) | |
| NIOSH (US-Grenzwerte für die Gesundheit): | |
PEL (Zulässig)
|
C 0,2 ppm (2 mg/m3) [Haut] |
Sofern nicht anders angegeben, gelten die Daten für Materialien in ihrem Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |
Nitroglycerin (NG), (alternative Schreibweise Nitroglycerin), auch bekannt als Trinitroglycerin (TNG), Nitro, Glyceryltrinitrat (GTN), Nobel Oil oder 1,2,3-Trinitroxypropan, ist eine dichte, farblose, ölige, explosive Flüssigkeit, die am häufigsten durch Nitrierung von Glycerin mit weiß rauchender Salpetersäure unter geeigneten Bedingungen für die Bildung des Salpetersäureesters hergestellt wird. Chemisch gesehen handelt es sich bei der Substanz um eine organische Nitratverbindung und nicht um eine Nitroverbindung, aber die traditionelle Bezeichnung wird beibehalten. Nitroglycerin wurde 1847 von Ascanio Sobrero erfunden und wird seitdem als aktiver Bestandteil bei der Herstellung von Sprengstoffen, namentlich Dynamit, verwendet und findet als solcher in der Bau-, Abbruch- und Bergbauindustrie Verwendung. Seit den 1880er Jahren wird es vom Militär als Wirkstoff und Geliermittel für Nitrocellulose in einigen Festtreibstoffen wie Kordit und Ballistit verwendet. Es ist ein Hauptbestandteil von rauchlosen Treibladungen auf doppelter Basis, die von Wiederladern verwendet werden. In Kombination mit Nitrocellulose werden Hunderte von Pulverkombinationen von Wiederladern für Gewehre, Pistolen und Flinten verwendet. ⓘ
Nitroglycerin wird seit über 130 Jahren in der Medizin als starker Vasodilatator (Gefäßerweiterung) zur Behandlung von Herzerkrankungen wie Angina pectoris und chronischer Herzinsuffizienz eingesetzt. Obwohl früher bekannt war, dass diese positiven Wirkungen darauf zurückzuführen sind, dass Nitroglycerin in Stickstoffmonoxid, einen starken Venenerweiterer, umgewandelt wird, wurde das Enzym für diese Umwandlung erst im Jahr 2002 als mitochondriale Aldehyddehydrogenase (ALDH2) entdeckt. Nitroglycerin ist in Form von sublingualen Tabletten, Sprays, Salben und Pflastern erhältlich. ⓘ
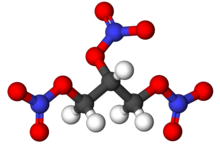
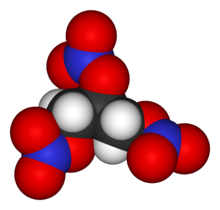
| Strukturformel ⓘ | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Nitroglycerin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C3H5N3O9 | |||||||||||||||
| Kurzbeschreibung |
gelbliche, ölige Flüssigkeit | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code | ||||||||||||||||
| Wirkstoffklasse |
Vasodilatator | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 227,09 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
1,59 g·cm−3 (20 °C) | |||||||||||||||
| Schmelzpunkt |
| |||||||||||||||
| Siedepunkt |
160 °C (20 hPa) | |||||||||||||||
| Dampfdruck |
0,5 Pa (30 °C) | |||||||||||||||
| Löslichkeit |
schlecht in Wasser | |||||||||||||||
| Brechungsindex |
1,4786 (12 °C) | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
| |||||||||||||||
| Toxikologische Daten |
| |||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−370,9 kJ/mol | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Nitroglycerin (auch Nitroglyzerin), Glycerintrinitrat oder Glyceroltrinitrat, auch Trisalpetersäureglycerinester ist ein Sprengstoff. Daneben wird es auch als Arzneistoff mit gefäßerweiternder Wirkung eingesetzt. Der Stoff fällt in den Geltungsbereich des Sprengstoffgesetzes und wird in der Anlage II in die Stoffgruppe A eingeteilt. ⓘ
Geschichte
Nitroglycerin war der erste praktisch hergestellte Sprengstoff, der stärker war als Schwarzpulver. Es wurde erstmals 1847 von dem italienischen Chemiker Ascanio Sobrero synthetisiert, der unter Théophile-Jules Pelouze an der Universität von Turin arbeitete. Sobrero nannte seine Entdeckung zunächst Pyroglycerin und warnte eindringlich vor seiner Verwendung als Sprengstoff. ⓘ
Nitroglycerin wurde später von Alfred Nobel als kommerziell nutzbarer Sprengstoff übernommen, der mit sichereren Methoden zur Handhabung der gefährlichen Verbindung experimentierte, nachdem sein jüngerer Bruder Emil Oskar Nobel und mehrere Fabrikarbeiter bei einer Explosion in der Rüstungsfabrik der Nobels 1864 in Heleneborg, Schweden, ums Leben gekommen waren. ⓘ

Ein Jahr später gründete Nobel in Deutschland die Alfred Nobel und Company und baute eine isolierte Fabrik in den Krümmelhügeln von Geesthacht bei Hamburg. Dieses Unternehmen exportierte eine flüssige Kombination aus Nitroglyzerin und Schießpulver, das so genannte "Sprengöl", das jedoch äußerst instabil und schwierig zu handhaben war, wie zahlreiche Katastrophen bewiesen. Die Gebäude der Fabrik in Krümmel wurden zweimal zerstört. ⓘ
Im April 1866 wurden drei Kisten Nitroglyzerin für die Central Pacific Railroad nach Kalifornien verschifft, die damit als Sprengstoff experimentieren wollte, um den Bau des 506 m langen Gipfeltunnels durch die Sierra Nevada Mountains zu beschleunigen. Eine der Kisten explodierte und zerstörte ein Büro der Firma Wells Fargo in San Francisco, wobei 15 Menschen ums Leben kamen. Dies führte zu einem vollständigen Verbot des Transports von flüssigem Nitroglyzerin in Kalifornien. Die Herstellung von Nitroglyzerin vor Ort war daher für die verbleibenden Bohr- und Sprengarbeiten in hartem Gestein erforderlich, die für die Fertigstellung der ersten transkontinentalen Eisenbahn in Nordamerika notwendig waren. ⓘ
Im Juni 1869 explodierten zwei mit Nitroglyzerin beladene Ein-Tonnen-Waggons, die damals unter dem Namen "Powder-Oil" bekannt waren, auf der Straße bei dem nordwalisischen Dorf Cwm-y-glo. Die Explosion forderte sechs Menschenleben, viele Verletzte und verursachte große Schäden im Dorf. Von den beiden Pferden wurde keine Spur gefunden. Die Regierung des Vereinigten Königreichs war angesichts des entstandenen Schadens und der möglichen Folgen in einer Stadt (die beiden Tonnen waren Teil einer größeren Ladung, die aus Deutschland über Liverpool kam) so alarmiert, dass sie bald darauf das Nitroglyzerin-Gesetz von 1869 verabschiedete. Flüssiges Nitroglyzerin wurde auch andernorts weitgehend verboten, und diese gesetzlichen Beschränkungen führten dazu, dass Alfred Nobel und sein Unternehmen 1867 Dynamit entwickelten. Dieses wurde durch Mischen von Nitroglyzerin mit Kieselgur hergestellt, die in den Krümmelbergen gefunden wurde. Ähnliche Mischungen wie "Dualin" (1867), "Lithofracteur" (1869) und "Gelignit" (1875) wurden durch Mischen von Nitroglycerin mit anderen inerten Absorptionsmitteln hergestellt, und viele Kombinationen wurden von anderen Unternehmen ausprobiert, um Nobels streng gehütete Patente für Dynamit zu umgehen. ⓘ
Dynamitmischungen, die Nitrocellulose enthalten, die die Viskosität der Mischung erhöht, sind allgemein als "Gelatine" bekannt. ⓘ
Nach der Entdeckung, dass Amylnitrit zur Linderung von Brustschmerzen beiträgt, experimentierte der Arzt William Murrell mit der Verwendung von Nitroglycerin zur Linderung von Angina pectoris und zur Senkung des Blutdrucks. Er begann 1878 damit, seine Patienten mit kleinen verdünnten Dosen von Nitroglyzerin zu behandeln, und diese Behandlung wurde bald weit verbreitet, nachdem Murrell seine Ergebnisse 1879 in der Zeitschrift The Lancet veröffentlicht hatte. Wenige Monate vor seinem Tod im Jahr 1896 wurde Alfred Nobel Nitroglycerin für dieses Herzleiden verschrieben, und er schrieb an einen Freund: "Ist es nicht eine Ironie des Schicksals, dass man mir Nitro-Glycerin verschrieben hat, das ich innerlich einnehmen soll! Sie nennen es Trinitrin, um den Apotheker und die Öffentlichkeit nicht zu erschrecken." Aus demselben Grund verwendet die Medizin auch den Namen "Glyceryltrinitrat". ⓘ
Produktionsmengen in Kriegszeiten
Während des Ersten und Zweiten Weltkriegs wurden große Mengen Nitroglycerin für die Verwendung als militärisches Treibmittel und für militärtechnische Arbeiten hergestellt. Während des Ersten Weltkriegs produzierte die HM Factory in Gretna, die größte Treibladungsfabrik im Vereinigten Königreich, etwa 800 Tonnen Kordit RDB pro Woche. Für diese Menge wurden mindestens 336 Tonnen Nitroglycerin pro Woche benötigt (vorausgesetzt, es gab keine Produktionsausfälle). Die Royal Navy verfügte über eine eigene Fabrik in der Royal Navy Cordite Factory, Holton Heath, in Dorset, England. Auch in Kanada wurde während des Ersten Weltkriegs eine große Korditfabrik gebaut. Die Korditfabrik der Canadian Explosives Limited in Nobel, Ontario, war für die Produktion von 680 Tonnen Kordit pro Monat ausgelegt, wofür etwa 286 Tonnen Nitroglyzerin pro Monat benötigt wurden. ⓘ
Instabilität und Desensibilisierung
In unverdünnter Form ist Nitroglyzerin ein Kontaktsprengstoff, der bei Erschütterung explodiert. Wenn es bei der Herstellung nicht angemessen gereinigt wurde, kann es im Laufe der Zeit zu noch instabileren Formen zerfallen. Dies macht den Transport und die Verwendung von Nitroglycerin äußerst gefährlich. In unverdünnter Form ist es einer der stärksten Sprengstoffe der Welt, vergleichbar mit den in jüngerer Zeit entwickelten RDX und PETN. ⓘ
Schon früh wurde festgestellt, dass flüssiges Nitroglycerin durch Einfrieren bei einer Temperatur von weniger als 7 bis 13 °C (45 bis 55 °F), je nach Reinheit, "desensibilisiert" werden kann. Seine Schockempfindlichkeit im gefrorenen Zustand ist nicht vorhersehbar: "In diesem Zustand ist es unempfindlicher gegen den Schock einer Fulminatkapsel oder einer Gewehrkugel, aber andererseits scheint es beim Zerbrechen, Zerkleinern, Stampfen usw. eher zu explodieren". Gefrorenes Nitroglyzerin ist viel weniger energiereich als flüssiges und muss daher vor der Verwendung aufgetaut werden. Das Auftauen kann extrem sensibilisierend sein, insbesondere wenn Verunreinigungen vorhanden sind oder die Erwärmung zu schnell erfolgt. Ethylenglykoldinitrat oder ein anderes Polynitrat kann zugesetzt werden, um die Schmelztemperatur zu senken und damit das Auftauen von gefrorenem Sprengstoff zu vermeiden. ⓘ
Nitroglycerin kann chemisch so weit "desensibilisiert" werden, dass es als ebenso "sicher" wie moderne Sprengstoffe angesehen werden kann, z. B. durch Zusatz von Ethanol, Aceton oder Dinitrotoluol. Das Nitroglycerin muss unter Umständen aus der Desensibilisierungschemikalie extrahiert werden, um seine Wirksamkeit vor der Verwendung wiederherzustellen, zum Beispiel durch Zugabe von Wasser, um das als Desensibilisierungsmittel verwendete Ethanol zu entfernen. ⓘ
Detonation
Nitroglycerin und alle Verdünnungsmittel können durchaus verpuffen (brennen). Die Sprengkraft von Nitroglycerin beruht auf der Detonation: Die Energie der anfänglichen Zersetzung verursacht eine starke Druckwelle, die den umgebenden Brennstoff zur Explosion bringt. Dabei handelt es sich um eine sich selbst erhaltende Schockwelle, die sich mit der 30-fachen Schallgeschwindigkeit durch das explosive Medium ausbreitet, da sich der Treibstoff durch den Druck fast augenblicklich in ein weißglühendes Gas zersetzt. Bei der Detonation von Nitroglyzerin entstehen Gase, die bei normaler Raumtemperatur und normalem Druck mehr als das 1.200-fache des ursprünglichen Volumens einnehmen würden. Durch die freigesetzte Wärme steigt die Temperatur auf etwa 5.000 °C (9.000 °F). Dies ist etwas völlig anderes als eine Verpuffung, die allein vom verfügbaren Brennstoff abhängt, unabhängig von Druck und Stoß. Die Zersetzung führt im Vergleich zu anderen Sprengstoffen zu einem viel höheren Verhältnis von Energie zu freigesetzten Gasmolen, was ihn zu einem der heißesten detonierenden Sprengstoffe macht. ⓘ
Herstellung
Nitroglycerin kann durch säurekatalysierte Nitrierung von Glycerin hergestellt werden. ⓘ

Bei der industriellen Herstellung wird Glycerin häufig mit einer nahezu 1:1-Mischung aus konzentrierter Schwefelsäure und konzentrierter Salpetersäure umgesetzt. Dies kann durch Mischen von weiß rauchender Salpetersäure - einer recht teuren reinen Salpetersäure, bei der die Stickoxide entfernt wurden, im Gegensatz zur rot rauchenden Salpetersäure, die Stickoxide enthält - und konzentrierter Schwefelsäure erfolgen. Häufiger wird diese Mischung durch die billigere Methode des Mischens von rauchender Schwefelsäure, auch bekannt als Oleum - Schwefelsäure mit überschüssigem Schwefeltrioxid - und azeotroper Salpetersäure (bestehend aus etwa 70 % Salpetersäure, der Rest ist Wasser) erreicht. ⓘ
Die Schwefelsäure erzeugt protonierte Salpetersäurespezies, die von den nucleophilen Sauerstoffatomen des Glycerins angegriffen werden. Die Nitrogruppe wird somit als Ester C-O-NO2 angehängt und es entsteht Wasser. Dies unterscheidet sich von einer elektrophilen aromatischen Substitutionsreaktion, bei der Nitronium-Ionen das Elektrophil sind. ⓘ
Die Zugabe von Glycerin führt zu einer exothermen Reaktion (d. h. es wird Wärme erzeugt), wie sie bei Nitrationen mit gemischten Säuren üblich ist. Wird das Gemisch zu heiß, kommt es zu einer "Runaway"-Reaktion, einem Zustand beschleunigter Nitrierung, der mit der zerstörerischen Oxidation organischer Materialien durch die heiße Salpetersäure und der Freisetzung giftigen Stickstoffdioxids einhergeht und ein hohes Explosionsrisiko birgt. Daher wird die Glycerinmischung langsam in das Reaktionsgefäß gegeben, das die gemischte Säure enthält (nicht Säure zu Glycerin). Der Nitrator wird mit kaltem Wasser oder einem anderen Kühlmittelgemisch gekühlt und während der gesamten Glycerinzufuhr auf einer Temperatur von etwa 22 °C gehalten, die heiß genug ist, um eine schnelle Veresterung zu ermöglichen, aber auch kalt genug, um ein Durchgehen der Reaktion zu vermeiden. Der Nitrierbehälter, der häufig aus Eisen oder Blei besteht und in der Regel mit Druckluft gerührt wird, hat an seinem Boden eine Notklappe, die über einem großen Becken mit sehr kaltem Wasser hängt und in die das gesamte Reaktionsgemisch (die so genannte Charge) gekippt werden kann, um eine Explosion zu verhindern, ein Vorgang, der als Ertrinken bezeichnet wird. Wenn die Temperatur der Ladung etwa 30 °C (86 °F) übersteigt (der tatsächliche Wert variiert von Land zu Land) oder braune Dämpfe in der Entlüftungsöffnung des Nitrators zu sehen sind, wird sie sofort ertränkt. ⓘ
Man unterscheidet diskontinuierliche und kontinuierliche Herstellungsverfahren. Bei diskontinuierlichen Verfahren wird eine bestimmte Menge Nitriersäure vorgelegt und bei starker Kühlung kleine Mengen Glycerin zugegeben. Aufgrund der Wärmeentwicklung und einer autokatalytischen Zersetzung bei Temperaturen über 30 °C bergen diese Methoden jedoch häufig unkalkulierbare Risiken. Das Auftreten von Nitroglycerindämpfen kann wegen der blutdrucksenkenden Wirkung (s. o.) zum Bewusstseinsverlust führen, was dadurch die Kontrolle über die Temperaturen bei der Herstellung unmöglich und damit eine unkontrollierte Zersetzung wahrscheinlich werden lässt. ⓘ
Um die Glycerintrinitratmengen in den einzelnen Verarbeitungsstufen so gering wie möglich zu halten und die Produktivität zu erhöhen, wurden daher kontinuierliche Herstellungsverfahren entwickelt. Im einfachsten Fall werden Nitriersäure und Glycerin kontinuierlich in ein gekühltes Rohrsystem gegeben und mischen sich dort aufgrund der laminaren Strömungsverhältnisse. Die modernsten Verfahren benutzen Injektorpumpen, bei denen die durchfließende Nitriersäure einen Unterdruck erzeugt, mit dem das Glycerin angesaugt und in dem Säurestrahl verwirbelt wird. Die Reaktionstemperatur liegt bei etwa 70 °C. ⓘ
Allgemein erfordert die Synthese von Glycerintrinitrat besondere Sorgfalt und Kenntnisse im Umgang mit Gefahrstoffen, es darf daher nur in professionellen Laboratorien oder technischen Produktionsanlagen hergestellt werden. Neben den offensichtlichen, selbst wohl den meisten Laien bekannten Gefahren einer ungewollten Detonation sind auch die toxikologischen Eigenschaften, sowohl des Endstoffes Glycerinnitrat (welcher u. A. durch Aufnahme über die Lunge schnell zu einem massiven Blutdruckabfall und somit im schlimmsten Fall zum Kreislaufkollaps und Tod führen kann), als auch weitere Gefahrenquellen – wie die Nitriersäure und deren hoch toxische 'nitrose Gase' (Stickstoffdioxide) keinesfalls zu unterschätzen. Da Glycerinnitrat auch transdermal (über die Haut) absorbiert werden kann und schon in relativ geringen Dosen letal wirkt, ist neben einer Atemschutzmaske auch speziell-imprägnierte Arbeitskleidung zum Schutz der Extremitäten erforderlich. ⓘ
Verwendung als Sprengstoff und Treibmittel
Nitroglycerin wird hauptsächlich in Sprengstoffen wie Dynamit und in Treibmitteln verwendet. ⓘ
Nitroglycerin ist eine ölige Flüssigkeit, die unter Einwirkung von Hitze, Schock oder Flammen explodieren kann. ⓘ
Alfred Nobel entwickelte die Verwendung von Nitroglyzerin als Sprengstoff, indem er Nitroglyzerin mit inerten Absorptionsmitteln, insbesondere Kieselgur, mischte. Er nannte diesen Sprengstoff Dynamit und ließ ihn 1867 patentieren. Es wurde gebrauchsfertig in Form von Stäbchen geliefert, die einzeln in gefettetes, wasserfestes Papier eingewickelt waren. Dynamit und ähnliche Sprengstoffe fanden breite Anwendung im Bauwesen, z. B. beim Bohren von Straßen- und Eisenbahntunneln, im Bergbau, bei der Beseitigung von Baumstümpfen auf landwirtschaftlichen Flächen, im Steinbruch und bei Abbrucharbeiten. Auch Militäringenieure haben Dynamit für Bau- und Abbrucharbeiten verwendet. ⓘ
Nitroglycerin wurde auch als Bestandteil von militärischen Treibladungen für Feuerwaffen verwendet. ⓘ
Nitroglycerin wurde in Verbindung mit Hydraulic Fracturing verwendet, einem Verfahren zur Gewinnung von Öl und Gas aus Schieferformationen. Bei dieser Technik wird Nitroglycerin in natürlichen oder hydraulisch erzeugten Rissen verdrängt und gezündet oder Nitroglycerin in hydraulisch erzeugten Rissen verdrängt und gezündet, gefolgt von Schüssen aus dem Bohrloch mit pelletiertem TNT. ⓘ
Nitroglyzerin hat gegenüber einigen anderen Sprengstoffen den Vorteil, dass es bei der Detonation praktisch keinen sichtbaren Rauch erzeugt. Daher ist es ein nützlicher Bestandteil bei der Herstellung verschiedener Arten von rauchfreiem Pulver. ⓘ
Seine Empfindlichkeit hat den Nutzen von Nitroglycerin als militärischer Sprengstoff eingeschränkt, und weniger empfindliche Sprengstoffe wie TNT, RDX und HMX haben es in der Munition weitgehend ersetzt. In der Militärtechnik ist es nach wie vor von Bedeutung, und Kampfingenieure verwenden nach wie vor Dynamit. ⓘ
Alfred Nobel entwickelte dann Ballistit, indem er Nitroglycerin und Schießbaumwolle kombinierte. Er ließ es im Jahr 1887 patentieren. Ballistit wurde von einer Reihe europäischer Regierungen als militärisches Treibmittel eingeführt. Italien war das erste Land, das es einführte. Die britische Regierung und die Regierungen der Commonwealth-Staaten übernahmen stattdessen Kordit, das 1889 von Sir Frederick Abel und Sir James Dewar im Vereinigten Königreich entwickelt worden war. Das ursprüngliche Kordit Mk I bestand zu 58 % aus Nitroglyzerin, zu 37 % aus Schießbaumwolle und zu 5,0 % aus Petroleumgelee. Ballistit und Kordit wurden beide in Form von "Schnüren" hergestellt. ⓘ
Rauchlose Pulver wurden ursprünglich unter Verwendung von Nitrocellulose als einzigem Sprengstoffbestandteil entwickelt. Daher wurden sie als einbasige Treibladungspulver bezeichnet. Es wurde auch eine Reihe von rauchlosen Pulvern entwickelt, die sowohl Nitrocellulose als auch Nitroglycerin enthalten, die so genannten zweibasigen Treibladungspulver. Ursprünglich wurden rauchlose Pulver nur für militärische Zwecke geliefert, aber schon bald wurden sie auch für den zivilen Gebrauch entwickelt und schnell für den Sport übernommen. Einige sind als Sportpulver bekannt. Dreistofftreibladungen enthalten Nitrocellulose, Nitroglycerin und Nitroguanidin, sind aber hauptsächlich für extrem hochkalibrige Munition, wie sie in Panzerkanonen und Marineartillerie verwendet wird, reserviert. Sprenggelatine, auch als Gelignit bekannt, wurde 1875 von Nobel erfunden, wobei Nitroglycerin, Holzschliff und Natrium- oder Kaliumnitrat verwendet wurden. Dies war ein früher, kostengünstiger und flexibler Sprengstoff. ⓘ
Medizinische Verwendung
Nitroglycerin gehört zu einer Gruppe von Arzneimitteln, die als Nitrate bezeichnet werden und zu denen viele andere Nitrate wie Isosorbiddinitrat (Isordil) und Isosorbidmononitrat (Imdur, Ismo, Monoket) gehören. Alle diese Wirkstoffe entfalten ihre Wirkung, indem sie im Körper durch die mitochondriale Aldehyddehydrogenase (ALDH2) in Stickstoffoxid umgewandelt werden, und Stickstoffoxid ist ein starker natürlicher Vasodilatator. ⓘ
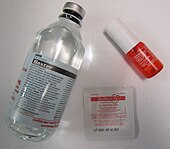
In der Medizin wird Nitroglycerin wahrscheinlich am häufigsten bei Angina pectoris, einem schmerzhaften Symptom einer ischämischen Herzerkrankung, die durch unzureichende Blut- und Sauerstoffzufuhr zum Herzen verursacht wird, und als starkes blutdrucksenkendes Mittel verschrieben. Nitroglycerin korrigiert das Ungleichgewicht zwischen der Zufuhr von Sauerstoff und Blut zum Herzen und dem Energiebedarf des Herzens. Auf dem Markt gibt es eine Vielzahl von Formulierungen in unterschiedlichen Dosierungen. In niedrigen Dosen erweitert Nitroglycerin die Venen stärker als die Arterien und verringert so die Vorlast (das Blutvolumen im Herzen nach der Füllung); man geht davon aus, dass dies sein primärer Wirkmechanismus ist. Durch die Verringerung der Vorlast muss das Herz weniger Blut pumpen, wodurch der Sauerstoffbedarf sinkt, da das Herz nicht so hart arbeiten muss. Außerdem wird durch die geringere Vorlast der ventrikuläre transmurale Druck (Druck, der auf die Herzwände ausgeübt wird) reduziert, wodurch die Kompression der Herzarterien verringert wird und mehr Blut durch das Herz fließen kann. In höheren Dosen erweitert es auch die Arterien, wodurch die Nachlast (der Druck, gegen den das Herz pumpen muss) verringert wird. Ein verbessertes Verhältnis zwischen dem Sauerstoffbedarf des Herzmuskels und der Sauerstoffversorgung führt zu folgenden therapeutischen Wirkungen bei Angina pectoris: Nachlassen der Brustschmerzen, Senkung des Blutdrucks, Erhöhung der Herzfrequenz und orthostatische Hypotonie. Patienten, die bei bestimmten körperlichen Aktivitäten unter Angina pectoris leiden, können die Symptome häufig durch die Einnahme von Nitroglycerin 5 bis 10 Minuten vor der Aktivität verhindern. Eine Überdosierung kann zu einer Methämoglobinämie führen. ⓘ
Nitroglycerin ist in Form von Tabletten, Salben, Lösungen für die intravenöse Anwendung, transdermalen Pflastern oder Sprays erhältlich, die sublingual verabreicht werden. Einige Formen von Nitroglycerin wirken im Körper wesentlich länger als andere. Nitroglycerin sowie der Wirkungseintritt und die Wirkungsdauer sind bei jeder Form unterschiedlich. Die sublinguale oder als Tablette verabreichte Form von Nitroglycerin hat einen Wirkungseintritt von zwei Minuten und eine Wirkungsdauer von fünfundzwanzig Minuten. Die orale Formulierung von Nitroglycerin hat einen fünfunddreißigminütigen Wirkungseintritt und eine Wirkungsdauer von 4-8 Stunden. Das transdermale Pflaster hat einen Wirkungseintritt von dreißig Minuten und eine Wirkungsdauer von zehn bis zwölf Stunden. Es hat sich gezeigt, dass eine kontinuierliche Nitratbelastung dazu führt, dass der Körper nicht mehr normal auf dieses Medikament reagiert. Experten empfehlen, die Pflaster nachts zu entfernen, damit der Körper einige Stunden Zeit hat, wieder auf die Nitrate zu reagieren. Nitroglycerin-Präparate mit kürzerer Wirkdauer können mehrmals täglich angewendet werden, wobei das Risiko einer Toleranzentwicklung geringer ist. Nitroglycerin wurde erstmals 1878 von William Murrell zur Behandlung von Angina-Pectoris-Anfällen eingesetzt; die Entdeckung wurde noch im selben Jahr veröffentlicht. ⓘ
Es kommt in der Notfallmedizin weiterhin auch bei Linksherzinsuffizienzen und kardial bedingten Lungenödemen zur Anwendung. Weitere Anwendungsgebiete sind die hypertensive Krise (Nitroglycerin, bei Erwachsenen mit 25–300 µg/min intravenös verabreicht, senkt sowohl den Blutdruck als auch den Gefäßwiderstand) und spastische Harnleiter- und Gallenkoliken. Zu beachten ist allerdings, dass es zu lebensgefährlichen Komplikationen kommen kann, wenn das Medikament Sildenafil (Viagra) bis zu 72 Stunden vor der Einnahme des Präparats genommen wurde. ⓘ
Häufige Anwendung findet Nitroglycerin ebenfalls als Wirkstoff in 'Nitrosalben' (z. B. Rectogesic), welche bei Analfissuren auf erkranktes Gewebe aufgetragen werden und mit der u. A. durchblutungsfördernden Wirkung für eine Entkrampfung des Muskeltonus sorgen. ⓘ
Industrielle Exposition
Eine seltene Exposition gegenüber hohen Dosen von Nitroglycerin kann schwere Kopfschmerzen verursachen, die als "NG-Kopf" oder "Knallkopf" bekannt sind. Diese Kopfschmerzen können so stark sein, dass manche Menschen handlungsunfähig werden; nach längerer Exposition entwickeln Menschen jedoch eine Toleranz gegenüber Nitroglycerin und werden davon abhängig. Obwohl selten, kann der Entzug tödlich sein. Zu den Entzugssymptomen gehören Brustschmerzen und andere Herzprobleme. Diese Symptome können durch eine erneute Exposition gegenüber Nitroglycerin oder anderen geeigneten organischen Nitraten gelindert werden. ⓘ
Bei Arbeitnehmern in Nitroglycerin (NTG)-Herstellungsbetrieben führen die Entzugserscheinungen bei regelmäßiger Nitroglycerin-Exposition am Arbeitsplatz manchmal zu "Sonntags-Herzanfällen", was zur Entwicklung einer Toleranz gegenüber den venenerweiternden Wirkungen führt. Im Laufe des Wochenendes verlieren die Arbeitnehmer die Toleranz, und wenn sie am Montag erneut exponiert werden, führt die drastische Gefäßerweiterung zu einer schnellen Herzfrequenz, Schwindel und Kopfschmerzen. Dies wird als "Montagskrankheit" bezeichnet. ⓘ
Menschen können Nitroglycerin am Arbeitsplatz ausgesetzt sein, indem sie es einatmen, über die Haut aufnehmen, verschlucken oder mit den Augen in Kontakt kommen. Die Occupational Safety and Health Administration hat den gesetzlichen Grenzwert (zulässiger Expositionsgrenzwert) für die Nitroglycerin-Exposition am Arbeitsplatz auf 0,2 ppm (2 mg/m3) Hautexposition an einem 8-Stunden-Arbeitstag festgelegt. Das National Institute for Occupational Safety and Health hat einen empfohlenen Grenzwert von 0,1 mg/m3 für die Exposition der Haut an einem 8-Stunden-Arbeitstag festgelegt. Bei einer Konzentration von 75 mg/m3 ist Nitroglycerin unmittelbar lebens- und gesundheitsgefährlich. ⓘ
Name
Die geläufige Bezeichnung Nitroglycerin ist gemäß IUPAC-Nomenklatur irreführend, da das Präfix Nitro- auf eine Kohlenstoff-gebundene NO2-Gruppe hinweist. Im Glycerintrinitrat jedoch ist der Alkylrest über je ein überbrückendes Sauerstoffatom an je ein Stickstoffatom gebunden, weswegen es sich um einen Trisalpetersäureester handelt. ⓘ
Noch exakter als Glycerintrinitrat wäre demnach die Bezeichnung Glycerintris(nitrat), wobei das Präfix tris darauf hinweist, dass es sich beim Säurerest nicht um ein Kondensat aus drei Molekülen HNO3 handelt, sondern dreimal mit je einem Molekül verestert wurde. Da die Bezeichnung Glycerin lediglich der Trivialname des dreiwertigen Alkohols Propan-1,2,3-triol ist, ist für dessen Salpetersäureester (also das so genannte Nitroglyzerin) die Bezeichnung Propantrioltrinitrat ebenfalls korrekt. ⓘ
Eigenschaften
Glycerintrinitrat ist bei Standardbedingungen eine farblose, geruchlose und schlecht wasserlösliche Flüssigkeit. Es hat einen süßlichen Geschmack, und schon die Einnahme einer geringen Menge Glycerintrinitrat (10 mg bzw. 0,15 mg/kg Körpergewicht) führt zu Kopfschmerzen. Der Schmelzpunkt liegt je nach Polymorph bei 2,8 °C oder 13,5 °C. ⓘ
Glycerintrinitrat explodiert bereits bei einem Fallhammerversuch mit einem 2-kg-Fallhammer aus einem Zentimeter Höhe. ⓘ
- Art: Sekundärsprengstoff
- Explosionswärme: 6,264 kJ·g−1
- Detonationsgeschwindigkeit: 6700–8500 m/s (7600 m/s (Dichte: 1,599 g/cm³))
- Bleiblockausbauchung: 52 cm³/g
- Schlagempfindlichkeit: 0,2 J
- Reibempfindlichkeit: bis 350 N Stiftbelastung keine Reaktion
- Grenzdurchmesser Stahlhülsentest: 24 mm ⓘ
Bei der Explosion oder beim Zerfall von Glycerintrinitrat entstehen aus chemischer Sicht in einer intramolekularen Redoxreaktion – mit den Nitrogruppen als Oxidationsmitteln und den C-Atomen als Reduktionsmitteln – die Reaktionsprodukte Kohlendioxid, Wasser, Stickstoff und Stickstoffmonoxid:

Die vollständige Umwandlung des flüssigen Sprengstoffes in extrem kurzer Zeit in Produkte, die bei hoher Temperatur gasförmig sind, führt zu einer massiven Volumenausdehnung, das heißt zu hoher Sprengkraft. ⓘ
Verwendung
Sprengstoff
Glycerintrinitrat wird als Sprengstoff verwendet. Wegen der starken Stoß- und Erschütterungsempfindlichkeit ist die Handhabung allerdings eher schwierig. Alfred Nobel gelang es 1867, Glycerintrinitrat in Kieselgur einzulagern. Das entstehende Dynamit war einfacher zu benutzen. Da aber dessen Anteil von 25 Prozent inaktiven Kieselgurs die Sprengkraft reduzierte, stellte ebenfalls Nobel 1875 Sprenggelatine her, eine ideal zerfallende Mischung aus Nitroglycerin und Schießbaumwolle (Zellulosenitrat, Ballistit bzw. Cordit). Später wurde Glycerintrinitrat als Sprengstoffbestandteil wegen seines Gefrierpunkts bei 13,5 °C (stabile, rhombische Modifikation) bzw. 2,8 °C (labile, trikline Form) teilweise durch Nitroglycol (Ethylenglycoldinitrat oder EGDN) ersetzt, das erst bei −22 °C gefriert. Nitroglycol ist allerdings recht flüchtig und daher in warmen Ländern mit nur wenig prozentualem Anteil an Sprengöl im Gesamtsprengstoff nicht zu empfehlen. Glycerintrinitrat ist dagegen heute noch ein wichtiger Bestandteil vieler Treibladungspulver. In geringen Mengen zugesetzt erhöht es die Sprengkraft von Ammonsalpetersprengstoffen. ⓘ
Nebenwirkungen
Zu den Nebenwirkungen des Mittels zählen eine Erhöhung des intrakraniellen Drucks, eine mögliche Reflextachykardie sowie Kopfschmerzen, Erröten und ein Hitzegefühl. ⓘ
Handelsnamen
- Monopräparate
Corangin Nitrospray (D), Deponit (D, A, CH), Glytrin (A), MinitranTM (CH), Minitrans (D), Nitrangin (D), Nitro (D, A), Nitroderm (D, A, CH), Nitro-Dur (A, CH), Nitronal (CH), Nitrolingual (D, A), Perlinganit (D, A, CH), Trinitrin (CH), Trinitrosan (D), Rectogesic (Salbe), diverse Generika (CH). ⓘ

